------♡ 서로 배려하는 물화생지 ♡------ (지우지 마세용)
1. 답변 달아주신 분께 감사의 댓글은 필수!
2. 모두 볼 수 있도록 비밀댓글은 금지!
3. 답변을 받은 후 질문글 삭제하지 않기!
4. 질문 전에 검색해보기! 질문은 구체적으로!
------♡ 서로 배려하는 물화생지 ♡------ (지우지 마세용)
학교에서 화학1을 가르치고 있는 교사입니다. 화학에 관심이 많은 학생의 질문을 받았는데 물리학 부분과 겹치는 것 같아 여기에도 올려봅니다.
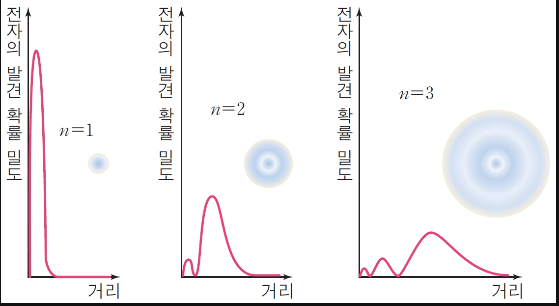
1. n=2, n=3의 경우 핵 근처에서도 전자 발견확률이 있는데 그럼 예를들어 3s까지 전자가 채워진 원자의 경우 3s의 전자나 2s의 전자가 1s의 전자보다 원자핵에 가까울 수도 있는 건가요?
2. 전자발견확률이 최대인 지점이 보어의 전자껍질과 일치하나요? 1s의 경우 보어반지름이라고 해서 k전자껍질의 위치인건 알겠는데 2s, 3s도 L, M 전자껍질인건지 궁금합니다.
같은 맥락입니다.
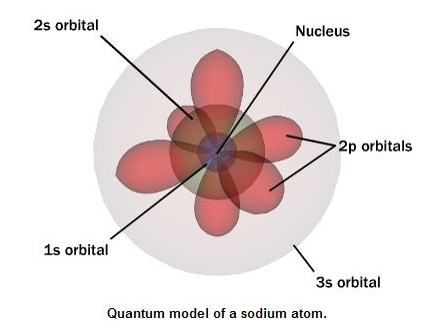
3. 그림에서처럼 3차원 공간에서 오비탈들이 서로 중첩되는 게 맞나요?
4. 전자는 정상파인거라고 하던데 그럼 파동이 중첩되거나 상쇄되는 부분이 있는데 파동이 중첩되는 부분은 확률이 증가하고 상쇄되는 부분이 마디가 되는건가요?
5. 파동함수라고 하는 것이 전자의 움직임의 모든 경우의 수를 고려하여 확률로 나타낸 것이라 이해해되 되나요?
물리에 대해서는 잘 몰라서 양자부분이 어렵네요. 원자 내 전자의 운동에 대해 설명해주시면 고맙겠습니다.^^
다음검색
댓글
댓글 리스트-
답댓글 작성자으헉으헉 작성시간 18.10.28 2. n=1인 경우는 맞으나, n=2,3인 경우는 다릅니다. 보어의 전자껍질은 수소원자에서 바닥상태의 전자가 지니는 궤도만 현대의 양자물리와 일치하는 것으로 알고 있습니다. 그러기에 보어의 원자모형은 고전 물리와 현대 양자물리 사이에 있는 모형이라고 생각하시면 되겠네요. 실제 현대 양자물리학에 의하면 수소원자 2s의 경우 전자발견확률이 최대인 지점은 L껍질의 반지름보다 대략 5/4배 정도 큽니다.
-
답댓글 작성자으헉으헉 작성시간 18.10.28 으헉으헉 3. 그림에서 그려진 오비탈은 수소 원자의 오비탈 같은데요. 오비탈이 중첩되는 게 맞습니다. 수소꼴 원자의 경우 전자가 어차피 1개 밖에 없기에, 각 영역의 오비탈들이 겹쳐도 전자의 초기에너지만 주어지면 궤도운동에 지장이 없습니다. 다만 다전자 원자의 경우 오비탈들이 제시된 그림과 상당히 다를 것으로 예상되며, 이유는 중첩되는 영역에서는 전자들간의 반발로 인해 궤도 운동에 영향을 줄 것 같습니다.
-
답댓글 작성자으헉으헉 작성시간 18.10.29 으헉으헉 4.[수정부분] 네 맞습니다. 드브로이의 물질파 얘기하시는 것 같은데, 드브로이의 물질파의 진폭값이 현대 물리의 파동함수입니다. 물질파 내의 배 지점에서는 전자발견확률이 높고, 마디 부분에서는 0이 됩니다.
-
답댓글 작성자으헉으헉 작성시간 18.10.28 으헉으헉 5. 네 맞습니다. 그러기에 어떠한 원자에 속해 있는 전자냐 또는, 원자 내부에 전자가 몇개 있는냐에 따라 제각각 파동함수 모양이 달라지게 됩니다.
-
답댓글 작성자으헉으헉 작성시간 18.10.28 으헉으헉 혹시 고수님들, 제가 생각한 내용 중에 잘못된 부분이 있다면 지적 부탁드립니다(__)