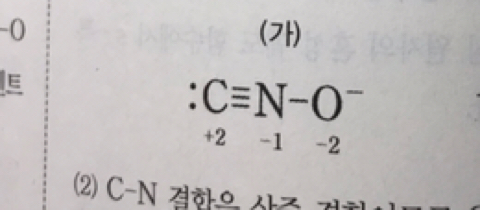------♡ 서로 배려하는 물화생지 ♡------ (지우지 마세용)
1. 답변 달아주신 분께 감사의 댓글은 필수!
2. 모두 볼 수 있도록 비밀댓글은 금지!
3. 답변을 받은 후 질문글 삭제하지 않기!
4. 질문 전에 검색해보기! 질문은 구체적으로!
------♡ 서로 배려하는 물화생지 ♡------ (지우지 마세용)
왜 질소의 산화수가 -1 일까요?
저는 탄소한테서 전자 뺏어오고 -3
산소로 인해 하나 잃으니 +1해서 총 -2라고 생각했거든요~
답이 -1 인데 도통 뭐가 잘못 된지 모르겠네요! ㅠ
다음검색
댓글
댓글 리스트-
작성자화학 합격! 작성시간 19.02.01 형식전하는 전기음성도 고려 없이 공유전자쌍을 공평하게 서로 50%씩 가져가고,
산화수는 전기음성도 큰 원자가 공유전자쌍을 100% 가져가는걸로 계산해요
위에서는 탄소보다는 질소가 전기음성도 크기때문에 공유전자쌍 3개에서 6개의 전자를 가져오고, 질소보다는 산소가 전기음성도 크기때문에 공유전자쌍 1개에서 전자2개 모두 산소가 가져가요
따라서 질소 원자가전자 5개 - 전기음성도 차이에 따라 가진 전자6개 = -1 -
답댓글 작성자마지막을후회없이 작성자 본인 여부 작성자 작성시간 19.02.02 선생님 답 감사합니다! 궁금한게 맨 아래 문장에서 질소 원자가전자 5개에서 전기음성도 차이에 따라 전자를 빼줘야 하나요?
사실 저는 산화수 규칙하고 제가 글에 쓴 저렇게 밖에 생각해 본 적이 없어서요~ 원래 산화수를 구할 때도 형식전하 구할때처럼 원자가전자 수 따져줘야 하는게 정석인가요??? -
답댓글 작성자화학 합격! 작성시간 19.02.05 마지막을후회없이 넵! 산화수 규칙이 전기음성도차이로 100프로 가져가는걸 가정하고 주로 쓰는걸 정리한거라 똑같아요
예를들어 수소가 +1인건
수소 전기음성도가 2.1 이고 보통 결합하는 원자가 2.1이상이기때문에
수소 원자가전자1개 - 전기음성도차이에 따른 전자0개(결합 1개) = +1
산소를 보면 산소의 전기음성도 3.5 플루오린 제외하고 전부 3.5아래기때문에 항상 전자를 다 뺏어옴
산소 원자가전자 6개 - 전기음성도차이에 따른 전자 8개(결합2개) = -2