------♡ 서로 배려하는 물화생지 ♡------ (지우지 마세용)
1. 답변 달아주신 분께 감사의 댓글은 필수!
2. 모두 볼 수 있도록 비밀댓글은 금지!
3. 답변을 받은 후 질문글 삭제하지 않기!
4. 질문 전에 검색해보기! 질문은 구체적으로!
------♡ 서로 배려하는 물화생지 ♡------ (지우지 마세용)
미즐러 연습 문제에 있는것인데요....
해설을 봐도 이해가 안되서 질문 올립니다....
(요즘 질문 자주 올리는데....너그럽게 양해해주시길~^^)
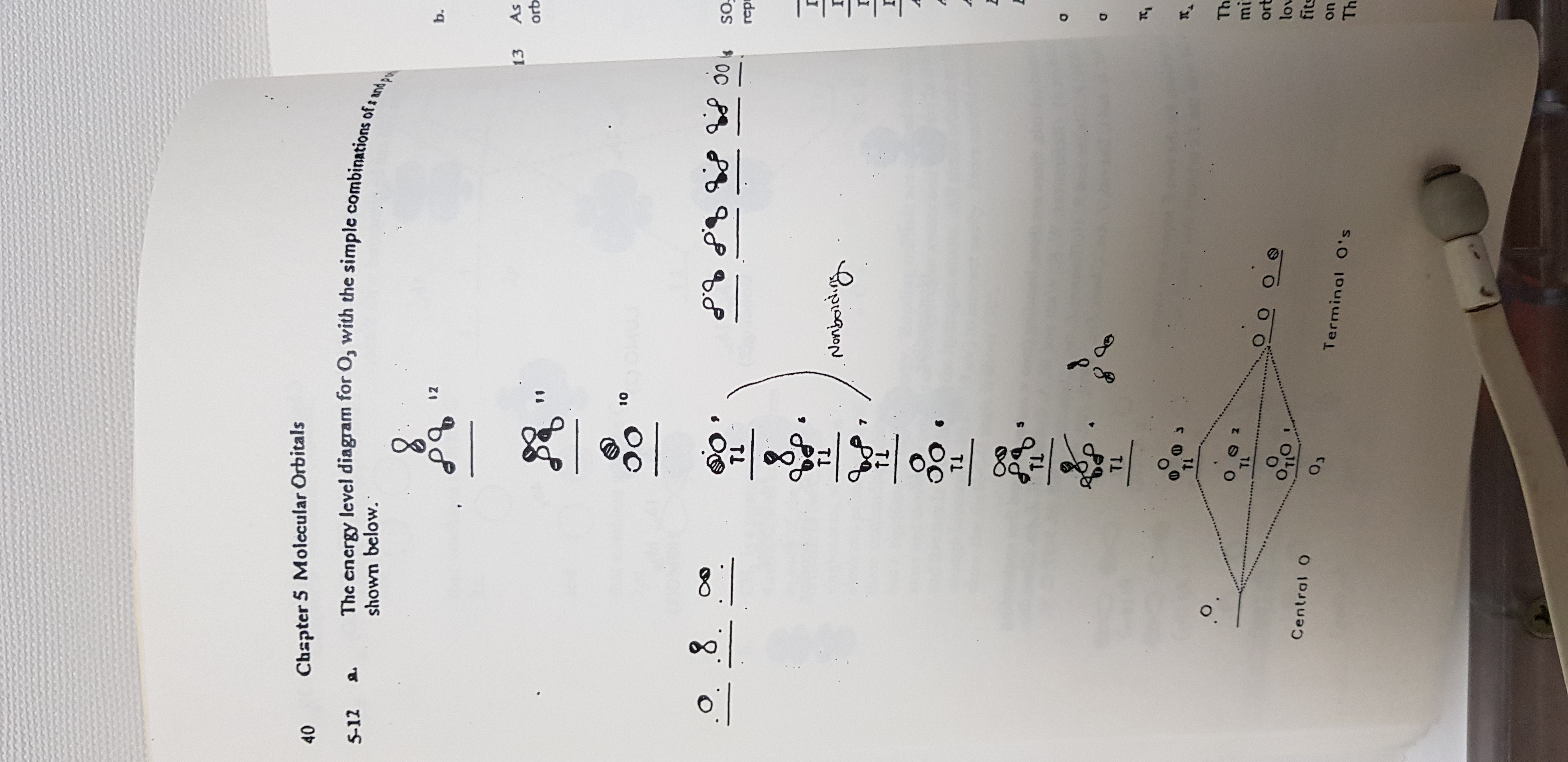
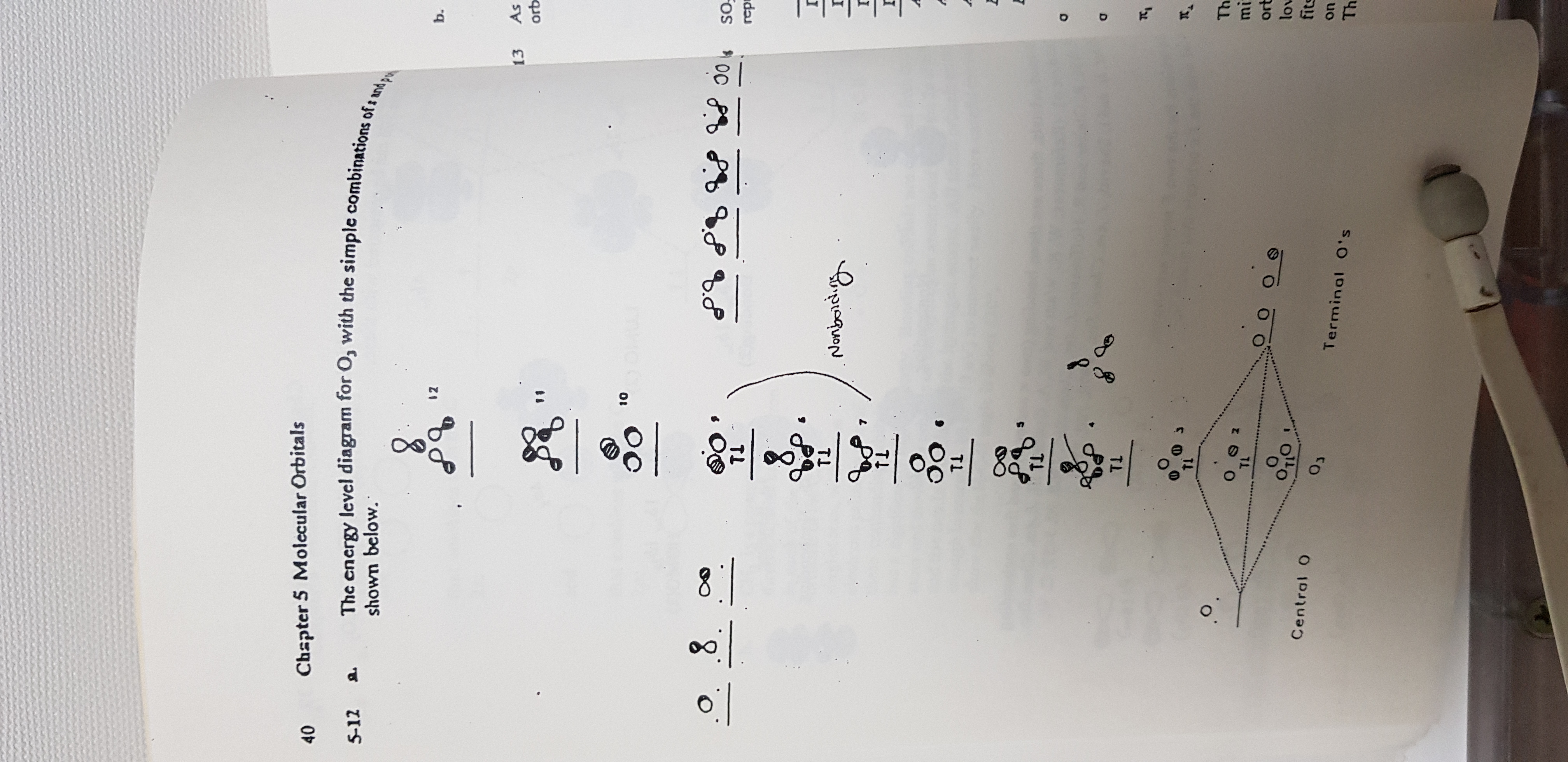
O3의 분자 궤도 함수 에너지 도표를 그려라
a) s와 p 궤도의 혼합이 없을때
사진을 참고 하면....
분자 궤도 함수에서
센트럴 O 터미널 O's 이렇게 나오는 것이
O3가되기 위해 O O2 이것을 이야기 하고 있는것 같구요
O의 원자가 전자가 6이니 18개의 전자가 채워져야 해서
1 부터 9까지 2개의 전자를 채워서 나타낸것 같습니다(여기 까진 맞게 이해 한것 이겠죠?)
그럼
1번은 s오비탈 함수 세개에 전자 2개를 채웠다는 것일까요?
2번은 nonboning 이니깐 s오비탈 2개( 그럼 색 칠해진것은 센트럴 O, 안칠해진것은 터미널 O)?
3번은 s오비탈 함수 세개 이고 전자는 2개 채웠다(터미널O의 2개) 왜 그럼 터미널 O의 2개가 되죠?
4-9번은 p오비탈이 되는거죠?
그럼 센트럴 O라고 되어 있는 부분에 3칸에 오비탈이 차례대로 px py pz 라고 생각 하면 될까요?
그럼 4번은 py오비탈이 3개(p오비탈은 방이 3칸이라고 생각 하면 되니깐?) 거기에 전자가 두개 들어 갔다?
근데 왜 py 오비탈만 3개지?
그런식으로 접근 하면 9번은 px오비탈이 2개만 있어요?
1개를 누락해서 잘못 나타낸 것 일까요?
이 문제에 지금 거의 2시간 가까이 머리를 싸매이고 있습니다....
혹시, 명쾌하게 알려주실분 있으시다면 도움 주시면 감사 하겠습니다.
함께 힘내 보아요~~~~^^
댓글
댓글 리스트-
답댓글 작성자종구아빠 작성시간 21.04.27 Q: 3번은 s오비탈 함수 세개 이고 전자는 2개 채웠다(터미널O의 2개) 왜 그럼 터미널 O의 2개가 되죠?
A: 제가 선생님의 질문을 잘 이해하지 못했는데,,, 그냥 3번에 대해서 차근차근 설명하자면,,, 터미널 산소들의 s오비탈 2개가 군 궤도함수 2개를 이루는 거고, 이 2개의 군 궤도함수가 센트럴 산소의 s오비탈과 상호작용해서 총 3개의 분자 오비탈을 만드는 거예요(군 궤도함수 2개 + 센트럴 산소의 s오비탈 1개 = 총 3개의 오비탈이 관여했으므로 생성되는 MO도 3개). 그 중에 한 개가 1번, 다른 한 개가 2번(이건 위에서 말씀 드린대로 사실상 겹침이 없는 nonbonding MO), 나머지 한 개가 3번이에요. MO도 오비탈 한 개로 치기 때문에 파울리 베타원리를 적용해서 전자 2개만 배치되는 거예요. -
답댓글 작성자종구아빠 작성시간 21.04.27 Q: 4-9번은 p오비탈이 되는거죠?
A: 네 맞아요. 4~9번은 군 궤도함수도 p오비탈로 이루어진 거고, 센트럴 원자도 p오비탈이 참여한거예요.
Q: 그럼 센트럴 O라고 되어 있는 부분에 3칸에 오비탈이 차례대로 px py pz 라고 생각 하면 될까요?
A: 제가 이 문제를 못찾아서,,, 문제에서 그림으로 축을 제시해줬는지는 모르겠는데, 축은 각자 설정하기 나름이라,, 더군다가 해답지에도 각 MO마다 기약표현이 표시 안되어 있어서, 어떤 오비탈이 px고 py고 pz인지 확답을 할 수 없어요. 근데 보통 C2v는 주축을 z축으로 잡고요, 만약 x축을 종이를 뚫고 나오는 수직방향 축으로 둔다면, 그림 순서대로 px, pz, py예요. -
답댓글 작성자종구아빠 작성시간 21.04.27 Q: 그럼 4번은 py오비탈이 3개(p오비탈은 방이 3칸이라고 생각 하면 되니깐?) 거기에 전자가 두개 들어 갔다? 근데 왜 py 오비탈만 3개지?
A: 음,, 제가 이해한 바로는, 선생님은 p오비탈 세 개로 구성된 분자오비탈은, 구성된 오비탈이 세 개니깐 방이 세 칸이라서 전자가 6개 채워지는 거로 생각하시는 거 같은데,,,, 원자 오비탈이 몇 개가 됐든, 그것들끼리 상호작용해서 새로 생성된 분자오비탈은, 그냥 오비탈 1개로 보는거예요. 그래서 지금 O3는 1번부터 12번까지 총 12개의 분자 오비탈이 만들어진거고, 그래서 이 분자는 방이 12개 인 거예요
Q: 그런식으로 접근 하면 9번은 px오비탈이 2개만 있어요? 1개를 누락해서 잘못 나타낸 것 일까요?
A: 이것도 2번과 마찬가지로 센트럴 산소의 p오비탈이 어떤 위상을 갖든, 한쪽하고는 보강, 다른 한쪽하고는 상쇄가 일어나서 실질적인 유효겹침이 없어, 센트럴 원자의 오비탈은 점으로 표시해서 생략하고, 터미널 산소들의 오비탈(군 궤도함수)만 표시한거고, 이것도사실상 nonbonding MO와 같습니다. -
작성자종구아빠 작성시간 21.04.27 제가 너무 늦게 답을 단건 아닌가 싶네요ㅎㅎ 저도 이부분 많이 부족해서 최대한 아는대로 말씀드린건데, 다른 의견 있으시거나 의문있으신 부분 말씀해주세요!
-
답댓글 작성자좋은쌤이될꺼야 작성자 본인 여부 작성자 작성시간 21.05.25 이제서야 댓글 봤네요...감사하구요..종구아빠님이 남기신 글 토대로 한번더 이해해보도록 공부해보고 추가 질문 있으면 드릴께요~
감사합니다^^