------♡ 서로 배려하는 물화생지 ♡------ (지우지 마세용)
1. 답변 달아주신 분께 감사의 댓글은 필수!
2. 모두 볼 수 있도록 비밀댓글은 금지!
3. 답변을 받은 후 질문글 삭제하지 않기!
4. 질문 전에 검색해보기! 질문은 구체적으로!
------♡ 서로 배려하는 물화생지 ♡------ (지우지 마세용)
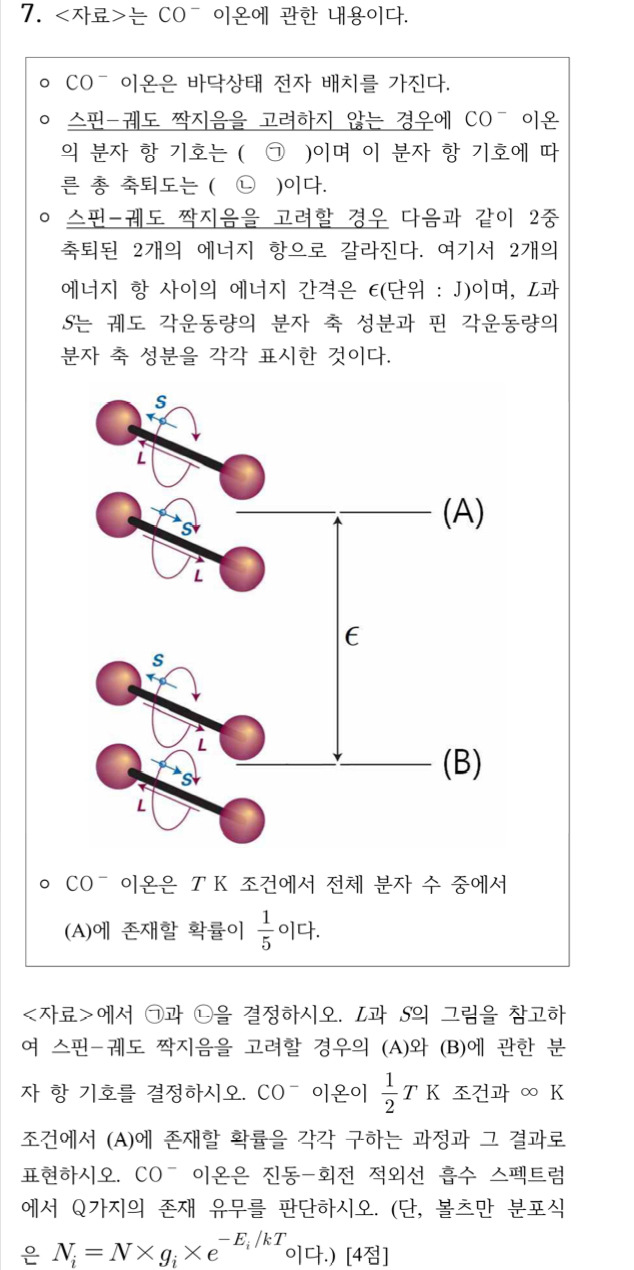
질문1. 이 문제에서 ㄴ 총 축퇴도 구할 때 왜 (2S+1)(2L+1)이 아닌가요...? 2(2S+1)로 구하는 이유가 궁금합니다
2. 스핀-궤도 짝지음에서 1/2보다 3/2가 에너지 더 높은 이유가 무엇일까요...?ㅠㅠ 어디까지 채워져야 전자가 반 이상 채워진건지 모르겠습니다...!
알려주시면 정말 감사하겠습니다 :)
다음검색
댓글
댓글 리스트-
작성자aswha123 작성시간 24.10.19 1. 원자 항기호에서의 축퇴도와 분자 항기호에서의 축퇴도는 다르게 계산됩니다. 가령 파이 오비탈에 1개의 전자가 있게 되면 분자 항기호는 2pi 가 되는데 실제로 그려보시면 나오겠지만 축퇴도는 4가 됩니다. 계산 시 (2S+1)X2 해주시면 됩니다.
2. 이부분은 원자항기호와 마찬가지로 전자가 오비탈에 반보다 적게 점유되어 있기 때문에 J값(정확히는 오메가 값)이 작은게 가장 안정한 항기호가 됩니다 -
답댓글 작성자24최합가즈아 작성시간 24.10.20 선생님 ! 질문이 있는데 CO-라 12개 오비탈 중 7개 전자로 반이상 점유되어 있어 J값이 큰게 안정한거 아닌가요? 왜 반보다 적게 점유 되었는지를 모르겠습니다ㅠ
-
답댓글 작성자aswha123 작성시간 24.10.20 전체 오비탈이 아니라 파이 오비탈만 보시면 됩니다! 파이오비탈에는 전자가 1개 점유되어있으니 반 이하가 점유되어있습니다!
-
답댓글 작성자화학합격하자 작성자 본인 여부 작성자 작성시간 24.10.20 아하!! 원자항기호와 다르게 생각해야하는군요! 감사합니다 선생님 :)
-
답댓글 작성자24최합가즈아 작성시간 24.10.20 aswha123 우와 이부분은 처음 알았네요 감사합니다 선생님~~