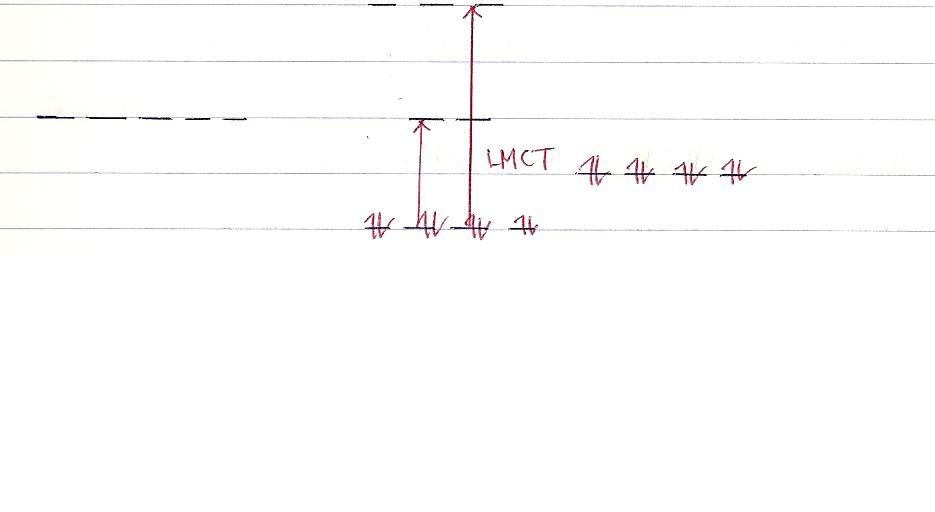
MnO4- 는 자주색을 띄고 MnO4 2-는 녹색을 띄는데
그 이유를 설명할때 LMCT로 설명하더군요.
MnO4- 는 자주색을 띄고 MnO4 2-는 녹색을 띄므로 그 보색인 MnO4- 는 노란색을 흡수하고 MnO4 2-는 붉은 색을 흡수하므로
MnO4- 이 더 단파를 흡수 즉 에너지 차이가 더 커야한다로 해석되는데
근데 책에는 LMCT로 설명하더군요.
LMCT로 설명하면 금속의 전하가 클수록 에너지 준위가 낮은 것이 에너지 gap차이가 작아지지않나요?
MnO4- 는 Mn이 7+ 전하이고 MnO4 2-는 6+이니까 전하가 큰 MnO4- 가 더 에너지 준위가 낮아서 리간드로부터의 에너지 준위가 더 적다 라고 반대로 해석되요.
제가 뭘 잘못 이해하고 있나요?
도와주세요~
다음검색
댓글
댓글 리스트-
작성자날아라펭귄 작성시간 10.07.12 어? 맞는데요? 전하가 클수록 리간드로부터 받는 궤도함수 에너지가 더 낮아지니까...(더 아래로...) 에너지 갭 차이가 큰거 아닌가요?? LMCT는 리간드로부터 온 전자가 채워진(위 그림에서 8개 전자가 채워진) 에너지 준위에서 금속의 빈 궤도함수로의 전이를 말하니까.. 아. 설마 금속의 전하가 클수록 금속의 에너지준위가 전체적으로 낮아진다는 것으로 이해하신건 아닌지??? 금속의 에너지 준위가 전체적으로 낮아지는게 아니라.. 안정한건 안정하고, 불안정한건 더 불안정해지는.. 즉 t2g와 eg의 간격이 벌어지게 되는거 같은데..
음..-_-; 급자신감 상실이네요;; 맞나;; 무기 고수님들의 조언 필요합니다;;; -
작성자할수있어! 작성자 본인 여부 작성자 작성시간 10.07.12 d-d 간의 차이로 색을 보는게 아니라 전하 이동 으로 인한 색이 더 크게 영향을 미치는 걸로 알고있어서 t2g와 eg의 간격으로 인한 색을 결정하는건 아니라고 알고있습니다.
그리고 저또한 전하가 커져서 t2g와 eg의 간격이 벌어져 eg가 낮아지니까 리간드에서 금속의 eg로 전이 되는걸 생각하여 그러면 리간드로부터 금속의 eg로의 에너지 갭이 작아진다고 생각하였습니다. 근데 가만히 보니까 t2g로의 전이는 증가하는데 이럴때는 어떤걸로 비교해야하는건지 모르겠습니다.
LMCT는 모두 리간드에서 금속의 t2g와 eg로 전이 될때 어떤걸로 에너지갭을비교해야하는걸까요?