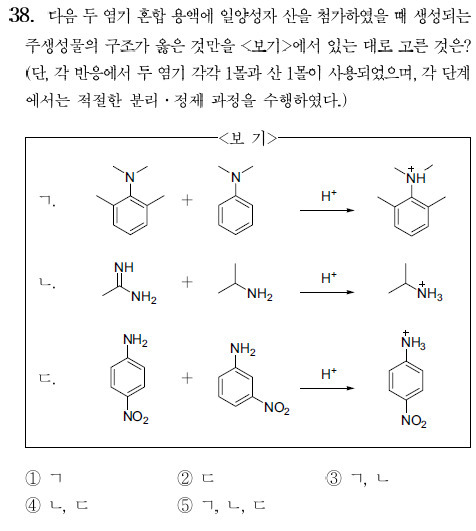
어떤 반응물의 염기도가 더 큰 것인지 묻는 문제인데요. 전자쌍을 잘 줄수록 염기도가 큰 것이라고 생각하였습니다. 근데 ㄴ의 경우 이민은 공명안정화가 일어나 아민에 비해 염기도가 작다고 생각하였는데 답은 이민의 염기도가 더 큰 것으로 되어있더라구요. 어떻게 이해하는게 좋을까요? 답변 부탁드려요..^^
다음검색
댓글
댓글 리스트-
답댓글 작성자카프카 작성시간 13.11.02 짝산이더안정하면 염기도가높은거구 전자쌍주는능력도 크겠죠..다같은말이라 구분하긴좀그러네요ㅜㅜ
왼쪽염기 공명구조그려보면 탄소가 플러스되고 질소가 마이너스가되네요ㅎㅎ(이민질소 음이온되고 아민질소 양이온되는 공명구조는 고려안함)
질소가 음전하띠니 전자를더잘준다고 봐도될듯해요 -
답댓글 작성자카프카 작성시간 13.11.02 지금보니 왼쪽염기가 공명안정화되서 염기도가 작아진다하셨는데..그렇게되려면 공명구조에서 질소가 양전하띨때만 해당이되겠죠
이경우는 오히려 공명에의해 질소가 음전하띠니 염기도가 증가하네요^^ -
답댓글 작성자알로릉 작성자 본인 여부 작성자 작성시간 13.11.04 친절한 답변 정말 감사해요^^ 음전하를 띠니 염기도가 증가하겠군요! 그런데 왼쪽염기 공명구조에서 탄소가 플러스되고 질소가 마이너스가 된다는게 어떤 구조인지 잘 모르겠어요ㅜ 이민질소가 음이온이되고 아민질소는 양이온이 되는것이 맞는 것 아닌가요?
-
답댓글 작성자알로릉 작성자 본인 여부 작성자 작성시간 13.11.04 정말정말 감사합니다^^ 완전 이해되었어요!!^^