1. 답변 달아주신 분께 감사의 댓글은 필수!
2. 모두 볼 수 있도록 비밀댓글은 지양!
3. 답변을 받은 후 질문글 삭제하지 않기!
------♡ 서로 배려하는 물화생지 ♡------
내부에너지와 엔탈피의 개념을 어떻게 구분해야 하는지 헛갈리네요..
정의가 이러하긴 한데..
H=U+PV
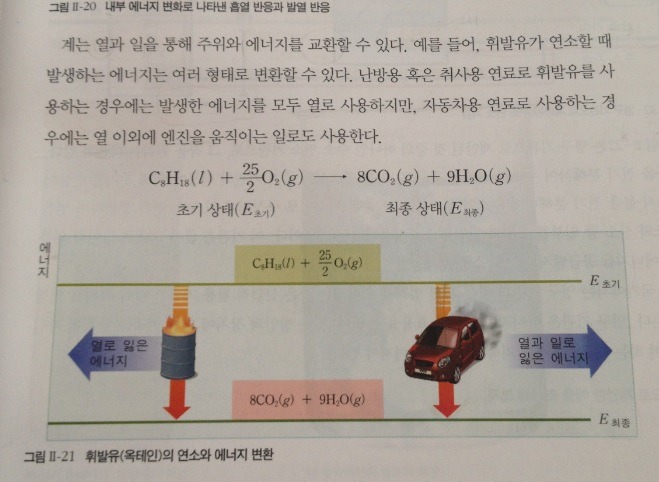
여기 그림에서 에너지 도표가 의미하는 물리량 값이
왼쪽 연소반응은 정부피 조건이라고 생각하면 (델타엔탈피=델타내부에너지)라고 생각해도 될 것 같은데
오른쪽 자동차 연료로 사용하는 반응은 부피 팽창에 의한 일을 고려해서 에너지 도표의 값에
내부에너지를 쓸 수 없고 엔탈피를 써야할 것 같은데..
에너지 보존법칙의 내용에서 에너지 전환이라는 관점을 강조하기 위해 쓴건지..
제가 뭘 잘못알고 있는건지 ㅠㅠ 너무 답답합니다.
다음검색