안녕하세요 1500제 <09.화학결합> 예제 9.4.14
질문드립니다
c번의 결합각이 134도 인 것을 잘 모르겠습니다
( d번처럼 ) 중심원자에 붙어 있는 주변원자가 3개일 경우 120도 인데
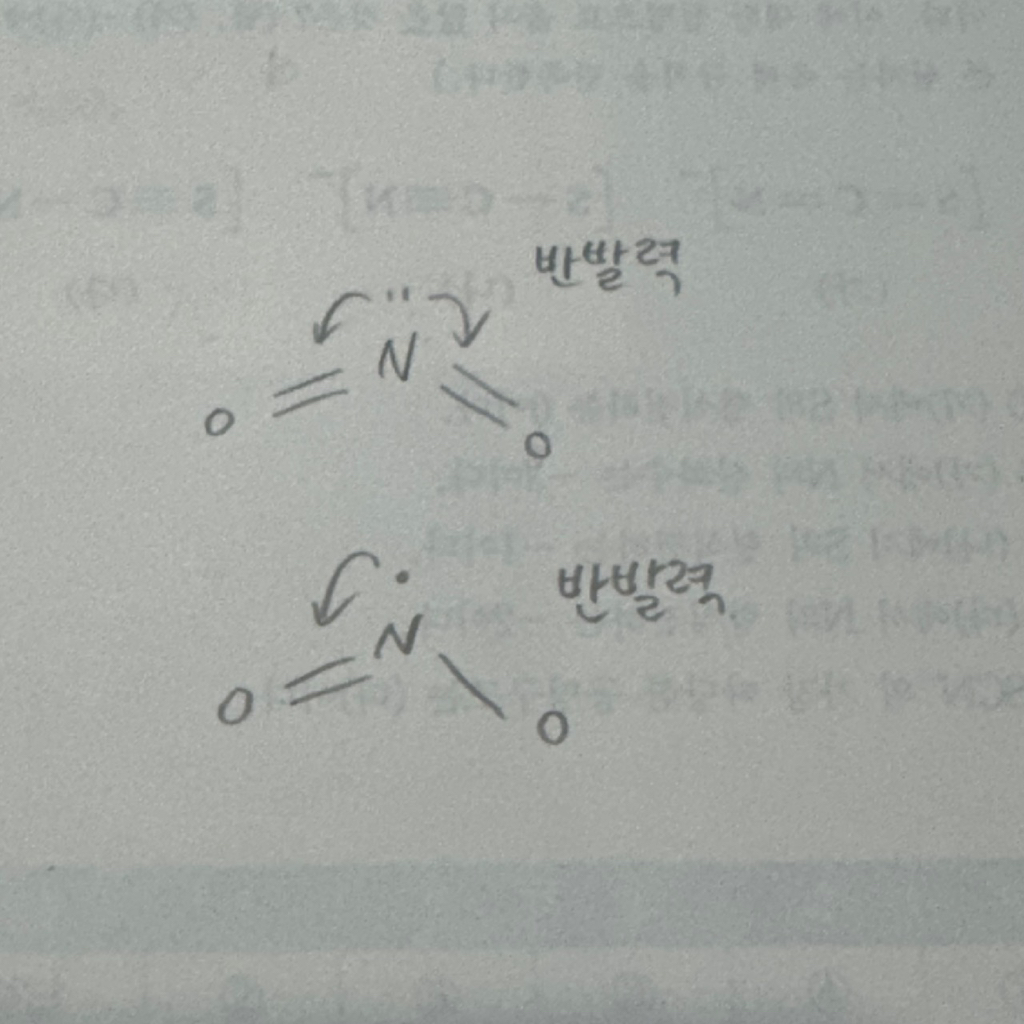
( b번처럼 ) 중심원자에 주변원자 2개에 비공유 전자가 1쌍이 있는 경우
주변 원자와의 반발력으로 인해 각도가 줄어드는 것까지 이해했는데 따라서 120도⬇️⬇️ 로 표현하자면
라디칼처럼 비공유 전자가 1개 있는 경우는
반발력이 바로 위 케이스 보다는 작으므로
120도⬇️ 라고 저는 느껴져요 ㅠㅠ
잘 모르겠어요 가르쳐주세요 !! 감사합니당 !!

양식을 지키지 않으면 예고없이 강등될 수 있습니다.
<제목양식>
강의교재 질문: 해당과정, 단원, 문제번호 명시 (적중 2000제 17-34번)
편입기출문제 질문 : 학교, 연도, 문제번호를 명시(중앙대 2022년도 12번)
<질문글 양식>
1. 질문이 2개 이상일 때 각각의 질문마다 번호를 붙여주세요.
2. 한번에 한 문제에 대해서만 질문 해주세요.
3. 문제의 그림이나 사진을 첨부하시면 답변을 빨리 받으실 수 있습니다.
4. 한번에 정확히 질문해주세요. 답변에 대한 추가댓글 질문 X
5. '이렇게 풀면 왜 답이 안나오나요?' 유형의 질문 X
다음검색
댓글
댓글 리스트-
작성자박인규 작성시간 26.04.09 답변하기 전에 일단 루이스구조가 너무 엉망으로 그려졌습니다. 옥텟규칙을 만족하도록 새로 그려야합니다. NO2-와 NO2를 비교할 때, NO2-는 비공유전자쌍 1개가 두개의 결합각을 밀고, NO2는 홀전자가 두개의 결합각을 밉니다. 비공유전자쌍의 반발력이 홀전자의 반발력보다 크므로 결합각은 NO2-에서가 더 작습니다. 기본적으로 전자구역이 3개면 결합각은 120도 근처입니다. NO2에서는 홀전자의 반발력이 작기때문에 120도보다 오히려 커졌습니다.