태학원생 물리이야기 20강)
우리 주변 사물은 "분자 (molecule; 몰레큘)"로 이루어져 있습니다.
예컨대, 물 (water)은 "물 분자"로 이루어져 있습니다.
분자를 더 잘게 쪼개면 "원자 (atom; 아톰)"가 나옵니다.
원자는, 그냥 잘게 쪼개면 나오는 덩어리일 뿐이고, 기존에 우리가 알고 있던 성질 ("물"이라는 물질의 성질 등)을 가지고 있지는 않습니다. 그냥 부스러기일 뿐입니다.
원자는 "원자핵 (nucleus; 뉴클레어스)"과 "전자 (electron; 일렉트론)"로 이루어져 있습니다.
(출처: Pinterest.)
물론, 위의 그림은 전자를 점입자로 가정한, 고전역학적 그림일 뿐입니다.
실제로는 전자는 파동함수 ψ(x,y,z)의 형태로 표현되므로, 아래와 같을 것입니다.
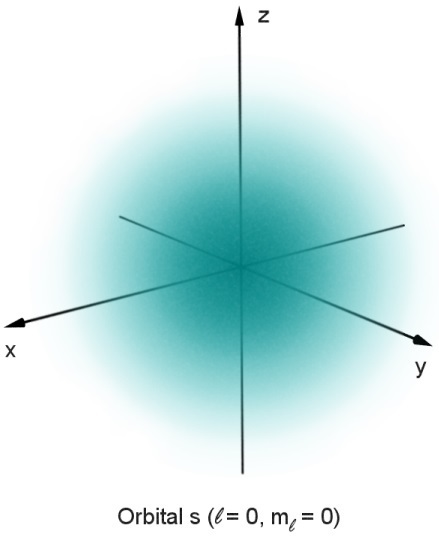
(출처: Wikimedia.)
오늘 우리는, 원자핵 주변의 전자의 움직임을 양자역학적으로 분석해 볼 것입니다.
방법은 간단합니다. 일단 슈뢰딩거 방정식을 적겠습니다.
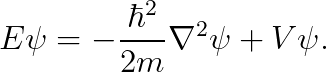
여기에 적절한 위치 에너지를 넣기만 하면 됩니다.
원자핵 주변의 전자는 "쿨롱 힘"을 받으므로, 아래와 같이 쿨롱 힘에 의한 위치 에너지를 넣어 주면 됩니다.
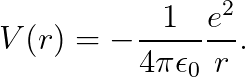
(편의상, 전자의 전하량을 (-e)라 두고, 원자핵의 전하량을 "e"라고 두었습니다. 실제로 원자핵의 전하량은 이것보다 크지만, 가장 작은 원자인 "수소 원자"의 경우에는 위와 같은 전하량을 가집니다.)
위 식에 나타난 위치 에너지를 그래프로 그리면, 다음과 같습니다.
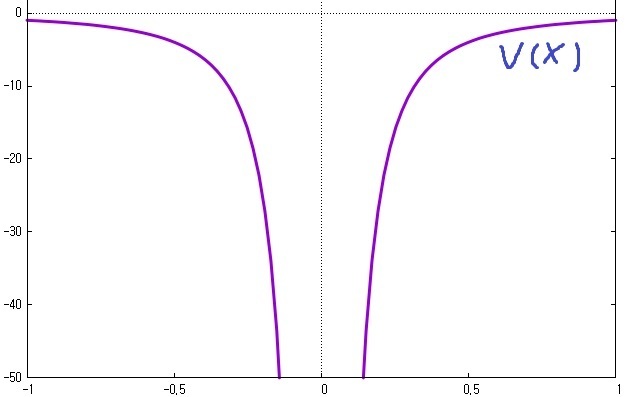
즉, "0"보다 작은 값을 가지는군요.
우리가 관심을 가지는 경우는 "bound state"이므로 (scattering state는 "대학원 양자역학" 게시판에서 합니다),
역학적 에너지 E는 "0"보다 작아야 합니다.
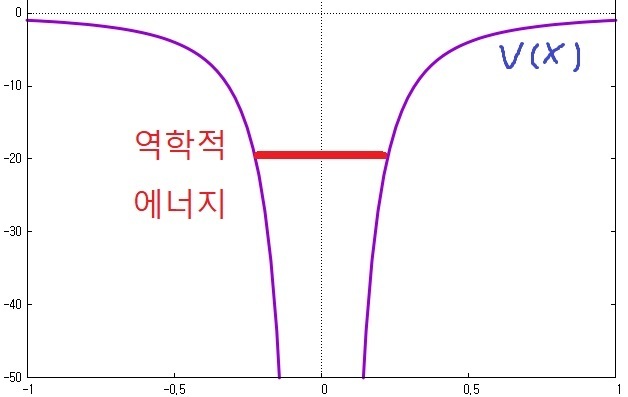
따라서, 역학적 에너지를 (-E)로 기술하여 다음을 얻습니다.
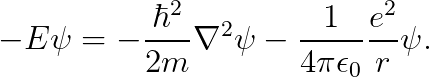
또한, 라플라시안 연산자는 아래와 같이 기술됨을 지난 "18강"에서 배웠습니다.
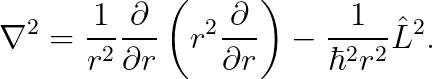
따라서, 슈뢰딩거 방정식은 다음과 같습니다.
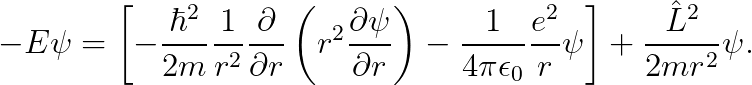
지난 시간에 보았듯이, 에너지 고유상태 ψ(r,θ,φ)를 아래와 같이 변수분리할 수 있습니다.
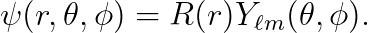
대입하여 다음을 얻습니다.
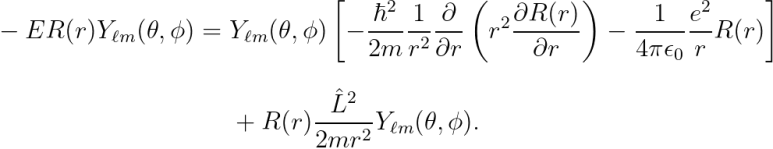
양 변을 "ψ"로 나눕니다.
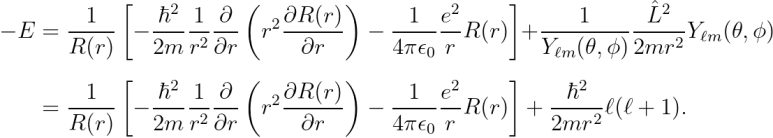
이로써, 변수는 "r" 하나만 남게 됩니다.
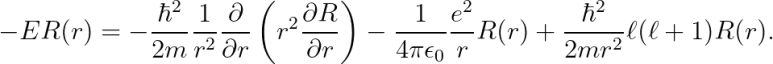
여기서, 우변의 미분 기호를 아래와 같이 전개할 수 있습니다.
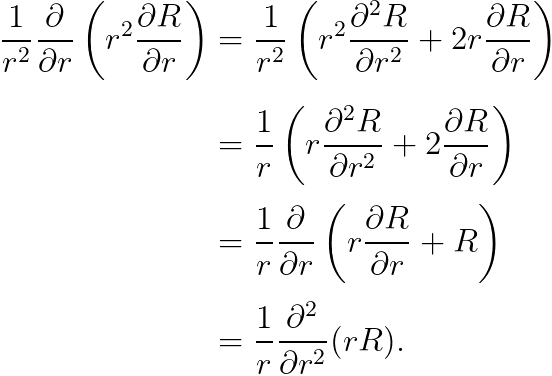
대입하여 다음을 얻습니다.
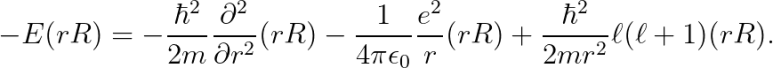
아래와 같이 치환합니다.
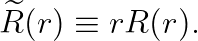
정리하여 다음을 얻습니다.
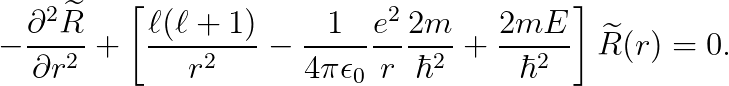
위의 미분 방정식을 풀 수 있을까요...? 글쎄요, 상당히 어려워 보이는군요.
일단, 위의 미분 방정식을 약간 변형해 보겠습니다.
"r값"이 매우 크다고 해 볼까요?
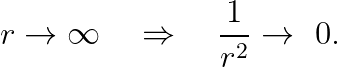
즉, r이 매우 큰 상황에서는, 위의 슈뢰딩거 방정식이 아래와 같이 근사될 수 있습니다.
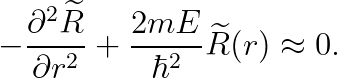
위의 미분 방정식은, 쉽게 풀 수가 있겠군요!
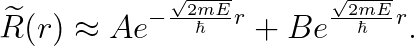
(위 식의 A, B는 적분상수입니다.) "r=∞"에서 발산하면 안 되므로, B=0이어야 합니다:
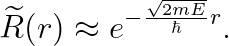
(상수 A는 나중에 규격화를 하기로 하고, 생략하겠습니다.)
다음으로, "r값"이 매우 작다고 해 봅시다.
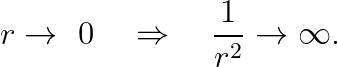
즉, r이 매우 작은 상황에서는 아래와 같이 근사할 수 있겠습니다.
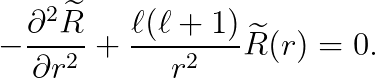
위 식의 첫 번째 항은 "두 번 미분한 값"이고, 두 번째 항은 "r^2으로 나눈 값"입니다.
이로부터 유추할 수 있는 것은, R(r)이 아래와 같은 형태라는 것입니다.
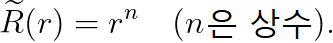
이를 대입하여 다음을 얻습니다.
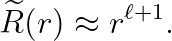
물론, 지금까지의 과정은 "r값"이 매우 크거나 매우 작은 경우에 대한 "근사값"에 불과합니다.
일반적인 경우에 대해서는, 슈뢰딩거 방정식의 해를 아래와 같이 쓸 수 있습니다.
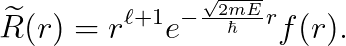
슈뢰딩거 방정식을 풀기 위해, 이를 미분합니다.
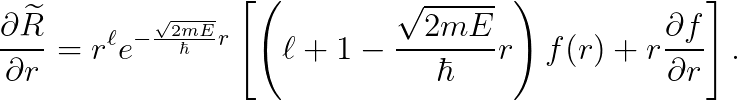
한 번 더 미분합니다.
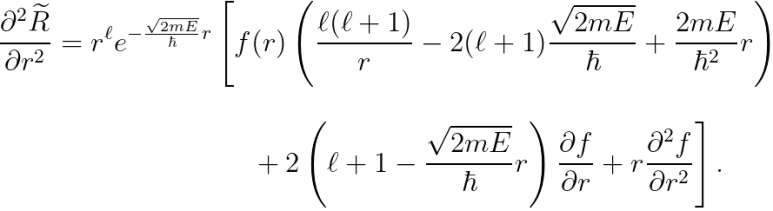
이제, 슈뢰딩거 방정식에 대입하여 다음을 얻습니다.
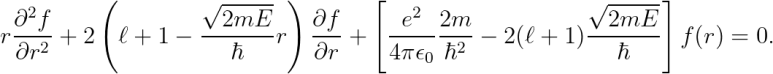
결론적으로, 위 식에서 "f(r)"만 구하면 끝나는 상황이군요.
그러나... 위 식의 해는 하나만 있는 게 아닙니다.
쉬운 이해를 위해서, "16강"에서 배웠던 "무한퍼텐셜 우물"을 기억해 봅시다.
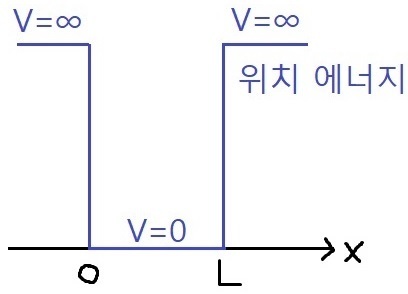
(위 그림: 예전에 배웠던 "무한퍼텐셜 우물".)
위의 상황에서 파동함수를 구하려면, 슈뢰딩거 방정식을 풀어야 했습니다.
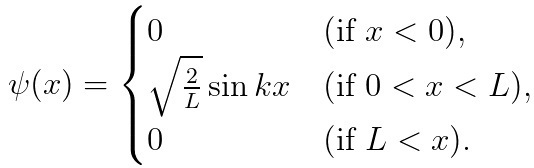
이때, 위 식의 "상수 k"는 여러 개의 값을 가질 수 있었습니다!
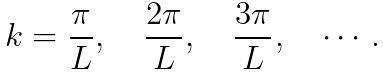
즉, 주어진 슈뢰딩거 방정식의 해는 "여러 개" 존재합니다.
자, 우리가 다루었던 방정식으로 돌아가 봅시다.
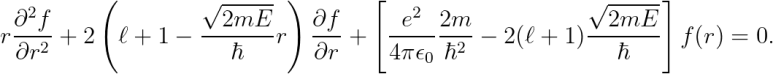
원래대로라면 f(r)을 급수 형태로 전개하여 위의 방정식을 풀어야 하지만,
우리는 이를 생략하고, 간단한 방법으로 접근해 볼 것입니다.
"보어의 원자 모형"에 의하면, 수소 원자 내부의 전자는 아래와 같은 역학적 에너지를 가집니다.
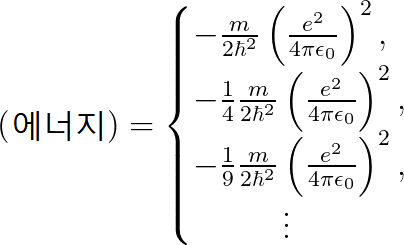
우리는 역학적 에너지를 (-E)라고 하였으므로, 마이너스 기호를 없애고 아래와 같이 표기하겠습니다.
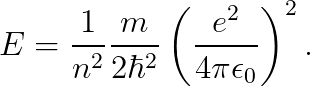
위의 에너지 E를 대입하여 다음을 얻습니다.
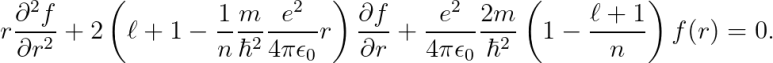
위 식으로부터, 우리는 아래의 조건을 강요할 것입니다.
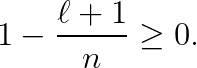
이유를 설명해 드리겠습니다. 만일 위의 값이 음수라면, 우리는 아래와 같은 방정식을 풀어야 합니다.
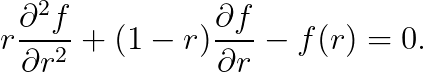
(편의상 상수는 모두 1로 두었습니다.) 아래와 같이 정리합시다.
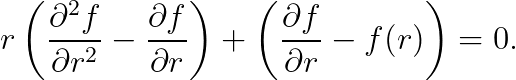
즉, 아래의 방정식을 풀면 됩니다.
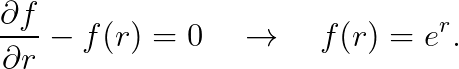
이를 원래의 파동함수 R(r)에 대입하면, "r → ∞"에서 발산하는 결과가 나오게 됩니다.
우리가 구하고자 하는 파동함수는 bound state이므로, 발산해서는 안 됩니다. 따라서,
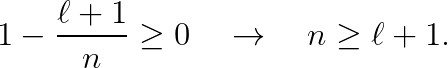
때늦은 설명입니다만, 위 식의 "n"을 "주 양자수 (principal quantum number; 프린시펄 퀀텀 넘버)"라고 부르며
"ℓ"을 "각운동량 양자수 (angular monentum quantum number; 앵귤러 모멘텀 퀀텀 넘버)"라고 부릅니다.
또한, "ℓ=0"인 경우에 대한 파동함수를 "s-오비탈 (s-orbital)"이라고 부릅니다.
주 양자수 n은 입자의 에너지를 결정하며, 각운동량 양자수 ℓ은 입자의 각운동량을 결정합니다.
오늘 우리가 구해 볼 파동함수는 "ground state"인데요, 즉 에너지가 가장 낮은 상태이니 n=1을 대입하면 될 것입니다.
이때, 위에서 배운 공식 "n ≥ ℓ+1"에 의해, 주어진 파동함수는 s-오비탈 (ℓ=0)이어야 합니다.
참고로, "n=1인 s-오비탈"을 일컬어 "1s 오비탈"이라고 부릅니다.
자, 주어진 값을 대입해 봅시다:

결과는 다음과 같습니다.
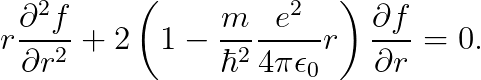
위의 미분 방정식은, 매우 쉽습니다:
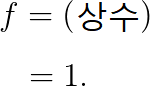
(나중에 규격화할 것이므로, f=1로 두었습니다.) 따라서,
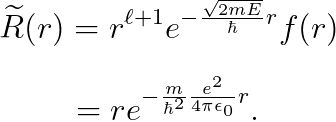
이로써, "r"에 대한 파동함수 R(r)을 구했습니다.
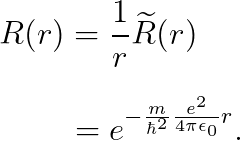
거의 다 끝났습니다.
전자의 파동함수 ψ(r,θ,φ)는 아래와 같이 기술되었습니다.
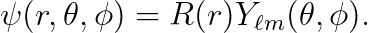
이때, 구면조화함수의 "m값" (질량 m이 아닙니다!)은 다음을 만족합니다 (증명은 "24강) 구면조화함수" 참조).
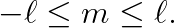
따라서, "ℓ=0"이면 "m=0"이어야 합니다:
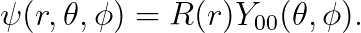
이때, "ℓ=0, m=0"인 구면조화함수는 다음과 같이 주어집니다 (증명은 "24강) 구면조화함수" 참조).
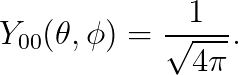
즉, 파동함수는 다음과 같습니다.
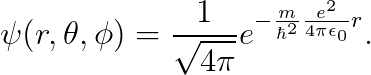
수식이 조금 복잡하니, 아래와 같이 치환하겠습니다.
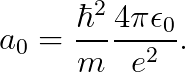
규격화하면 다음을 얻습니다.
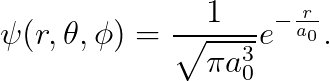
이로써, 1s 오비탈에 해당하는 파동함수를 구했습니다. 그래프는 아래와 같습니다.
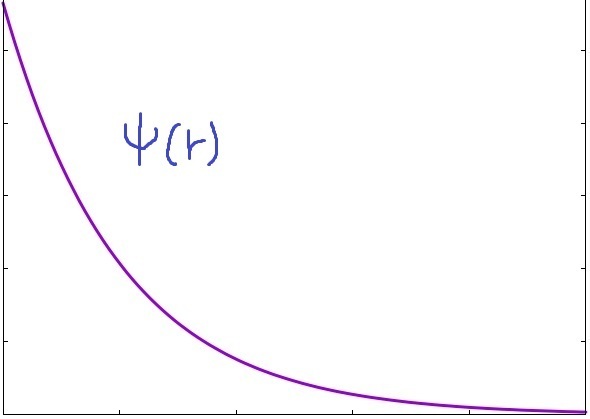
마지막으로 우리가 구할 값은, 바로 "수소 원자의 반지름"입니다.
수소 원자의 반지름이란, "전자가 존재할 확률이 가장 높은 곳"을 말합니다.
우선, 아래와 같이 파동함수를 전체 공간에서 적분하면 "1"이 나옵니다.
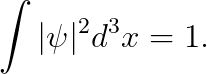
이는 "전체 확률"이 1이라는 뜻인데요, 우리는 (r,θ,φ) 좌표 중에서 "r값"만 볼 것이므로,
아래와 같이 "r값"을 제외한 값을 적분합니다.
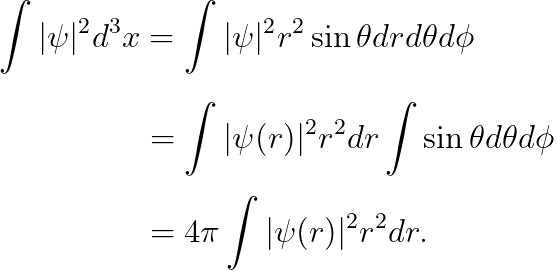
따라서, 우리는 아래의 값에 주목하겠습니다.
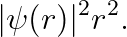
그래프는 다음과 같습니다.
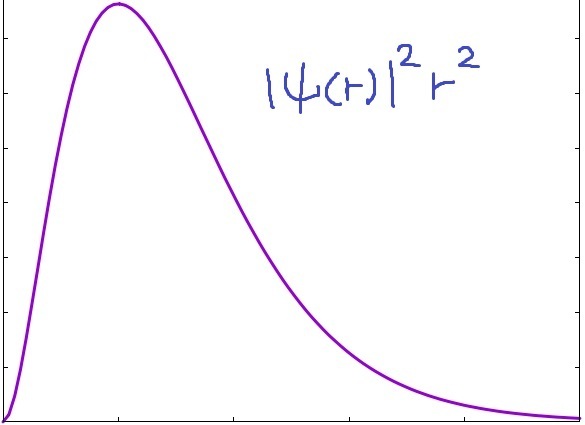
위 그래프가 최대값을 가지는 조건 (즉, 미분값이 "0"인 지점)은 다음과 같습니다.
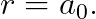
따라서, 위의 값이 수소 원자의 반지름이라고 할 수 있겠습니다.
(위 식의 "a_0"를 일컬어, "보어 반지름 (Bohr radius; 보어 래이디어스)"이라고 부릅니다.)