
방정식
가스의 양은 압력, 부피 및 온도에 의해 결정됩니다. 방정식의 현대적 형태는 이들을 단순히 두 가지 주요 형태로 관련시킵니다. 상태 방정식에 사용되는 온도는 절대 온도입니다 : 적절한 SI 단위는 켈빈입니다.
가장 자주 도입되는 양식은 다음과 같습니다.

SI 단위에서 p는 파스칼, V는 입방 미터, n은 몰, T는 켈빈 단위로 측정됩니다
(켈빈 눈금은 이동 된 섭씨 눈금으로 0.00K = -273.15 ° C, 가능한 최저 온도). R은 값 8.314 J/(mol· K) = 1.989 ≈ 2 cal / (mol· K) 또는 0.0821 L⋅atm/(mol⋅K).
얼마나 많은 가스가 존재하는지는 가스의 화학적 양 대신 질량을 주어 지정할 수 있습니다.
따라서, 이상 기체 법칙의 대안적인 형태가 유용할 수 있다. 화학량 n (몰)은 가스의 총 질량 (m) (킬로그램)을 몰 질량 M (몰 당 킬로그램)으로 나눈 값과 같습니다.

이러한 형태의 이상 기체 법칙은 고려되는 기체의 양과 무관하게 압력, 밀도 및 온도를 고유한 공식으로 연결하기 때문에 매우 유용합니다. 대안적으로, 법칙은 특정 부피 v, 밀도의 역수로 쓰여질 수 있습니다.

특히 엔지니어링 및 기상 응용 분야에서 특정 가스 상수를 기호 R로 나타내는 것이 일반적입니다.
통계 역학

복합 가스 법칙

가스와 관련된 에너지
이상 기체의 운동 이론의 가정에 따르면, 이상 기체의 분자 또는 원자 사이에는 분자간 인력이 없다고 생각할 수 있습니다.
즉, 위치 에너지는 0입니다. 따라서 기체가 소유하는 모든 에너지는 기체의 분자 또는 원자의 운동 에너지입니다.

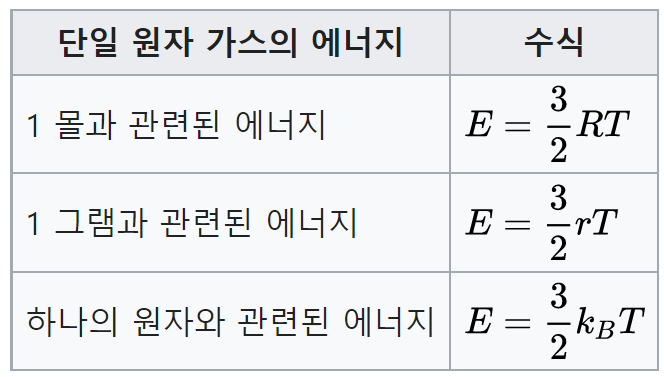
이것은 3 자유도를 갖는 단일 원자 가스의 n 몰의 운동 에너지에 해당합니다. x, y, z. 아래 표는 다양한 양의 단일 원자 가스에 대해이 관계를 제공합니다.
실제 기체의 이상적인 거동으로부터의 편차
여기에 주어진 상태 방정식 (PV = nRT)은 이상 기체에만 적용되거나 이상 기체처럼 충분히 행동하는 실제 기체에 대한 근사치로 적용됩니다. 실제로 상태 방정식에는 여러 가지 형태가 있습니다. 이상 기체 법칙은 분자 크기와 분자간 인력을 모두 무시하기 때문에 고온 및 저압에서 단원자 기체에 가장 정확합니다. 분자 크기의 무시는 인접한 분자 사이의 평균 거리가 분자 크기보다 훨씬 커지기 때문에 더 낮은 밀도, 즉 더 낮은 압력에서 더 큰 부피에 대해 덜 중요해집니다. 분자간 인력의 상대적 중요성은 열 운동 에너지가 증가함에 따라, 즉 온도가 증가함에 따라 감소합니다. van der Waals 방정식과 같은보다 상세한 상태 방정식은 분자 크기와 분자간 힘으로 인한 이상과의 편차를 설명합니다.
이상기체 법칙으로부터 파생 원리
이상 기체 법칙의 유도로 이어진 경험적 법칙은 기체의 2 가지 상태 변수 만 변경하고 다른 모든 변수를 일정하게 유지하는 실험을 통해 발견되었습니다.
이러한 종류의 설정으로 발견 될 수있는 모든 가능한 가스 법칙은 다음과 같습니다.

기체 운동 이론
이상 기체 법칙은 또한 기체의 운동 이론을 사용하는 첫 번째 원리에서 파생될 수 있는데, 여기서 몇 가지 단순화된 가정이 이루어지며, 그 중 가장 중요한 것은 기체의 분자 또는 원자가 점 질량이고 질량은 있지만 상당한 부피는 없으며 선형 운동량과 운동 에너지가 모두 보존되는 용기의 측면과 서로 탄성 충돌만 겪는다는 것입니다.
기체 운동 이론의 기본 가정은 다음을 의미합니다.

통계 역학
입자의 시간 평균 운동 에너지는 다음과 같습니다.

d차원 시스템의 경우, 이상 기체 압력은 다음과 같다
