인간혼= 자유전자= 불사혼
사멸혼 : 속박된 전자 - 쌍소멸
속박된 전자와 자유전자
속박된 전자는 빛이되어 사멸한다.쌍소멸
인간혼( 자유전자)가 불사혼인 근거는?
π^2=9.8696044011> 37,324,800(자유전자)
√(371=19.2613602843=3,732,480
1,658,880×225=373,248,000
518,400×72=37,324,800
-----------------------------------------------------------
1,658,880÷373,248=4.4444444444
4.4444444445×373,248=1,658,880.000020736
5,184,000÷3,732,480=1.3888888889
1.3888888889×3,732,480=5,184,000.000041472
37,324,800÷518,400=72
518,400×72=37,324,800
14,696,640÷1,658,880=8.859375
8×8×5×9×3×7×5×1,536=464,486,400=8×58,060,800
14,696,640÷373,248=39.375
3×9×3×7×5×3×7×3×2×4×8=11,430,720=9×1,270,080
14,696,640÷5,184=2,835
2×8×3×5×5×1×8×4=3840
자유전자의 물리학적 환생
자유전자는 8가지로 윤회를 거듭한다.
물리학에서 자유 전자는 다음을 가리킬 수 있습니다.
- electron as free electron
- Solvated electron
- Charge carrier, as carriers of electric charge
- Valence electron, as an outer shell electron that is associated with an atom
- Valence and conduction bands, as a conduction band electron relative to the electronic band structure of a solid
- Fermi gas, as a particle of a non-interacting electron gas
- Free electron model, as a particle in the Drude-Sommerfeld model of metals
- Free-electron laser, as a particle in the electron beam
- 자유 입자로서의 전자
- 용매화된 전자
- 전하 운반체, 전하 운반체로서
- 원자와 관련된 외피 전자로서의 원자가 전자
- 원자가 및 전도대, 고체의 전자 띠 구조에 상대적인 전도대 전자로서
- 페르미 가스, 상호 작용하지 않는 전자 가스의 입자
- 금속의 Drude-Sommerfeld 모델의 입자로서의 자유 전자 모델
- 전자빔의 입자로서의 자유 전자 레이저
용매화된 전자 solvated electron - Wikipedia
From Wikipedia, the free encyclopedia Free electron in a solution, often liquid ammonia A solvated electron is a free electron in a solution, in which it behaves like an anion.[1] An electron's being solvated in a solution means it is bound by the solution
en.wikipedia.org
같이 보기
자유전자쌍
화학에서 고독한 쌍은 공유 결합에서 다른 원자와 공유되지 않는 원자가 전자 쌍을 말하며[1] 때로는 공유되지 않은 쌍 또는 비결합 쌍이라고도 합니다. 고독한 쌍은 원자의 가장 바깥쪽 전자 껍질에서 발견됩니다. Lewis 구조체를 사용하여 식별할 수 있습니다. 따라서 두 개의 전자가 쌍을 이루지만 화학 결합에 사용되지 않는 경우 전자 쌍은 단독 쌍으로 간주됩니다. 따라서 고독한 쌍의 전자 수와 결합의 전자 수는 원자 주위의 원자가 전자의 수와 같습니다.
고독한 쌍은 분자의 모양을 설명하는 원자가 껍질 전자쌍 반발 이론(VSEPR 이론)에서 사용되는 개념입니다. 그들은 또한 루이스 산과 염기의 화학에서 언급됩니다. 그러나 화학자들은 결합하지 않는 모든 전자 쌍을 고독한 쌍으로 간주하지 않습니다. 예를 들어, 비결합 쌍이 분자 기하학에 영향을 미치지 않고 입체화학적으로 비활성이라고 하는 전이 금속이 있습니다. 분자 궤도 이론 (완전히 비 편소화 된 표준 궤도 또는 어떤 형태로 국소화 됨)에서 궤도와 루이스 구조의 구성 요소 사이의 대응이 종종 간단하지 않기 때문에 고독한 쌍의 개념은 덜 뚜렷합니다. 그럼에도 불구하고, 점유된 비결합 궤도(또는 대부분 결합하지 않는 특성의 궤도)는 종종 고독한 쌍으로 식별됩니다.
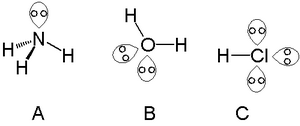
암모니아(A), 물(B) 및 염화수소(C)의 고독한 쌍
암모니아의 질소와 같은 질소 그룹의 원자와 함께 단일 고독한 쌍을 찾을 수 있습니다. 두 개의 고독한 쌍은 물 속의 산소와 같은 칼코겐 그룹의 원자와 함께 발견 될 수 있습니다. 할로겐은 염화수소와 같이 3 개의 고독한 쌍을 운반 할 수 있습니다.
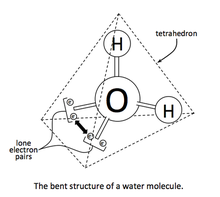
VSEPR 이론에서 물의 산소 원자에 있는 전자 쌍은 4개의 꼭짓점 중 2개에 고독한 쌍을 가진 사면체의 꼭짓점을 형성합니다. H-O-H 결합 각도는 104.5°로 사면체각에 대해 예측된 109°보다 작으며 이는 고독한 쌍 간의 반발력 상호 작용으로 설명할 수 있습니다. [2][3][4]
고독한 쌍의 존재에 대한 다양한 계산 기준이 제안되었습니다. 전자 밀도 ρ(r) 자체는 일반적으로 이와 관련하여 유용한 지침을 제공하지 않지만 전자 밀도의 라플라시안은 나타내며 고독한 쌍의 위치에 대한 한 가지 기준은 L(r) = –∇2ρ(r)이 국소 최대값입니다. 정전기 전위 V(r)의 최소값은 또 다른 제안된 기준입니다. 또 다른 하나는 전자 국소화 함수(ELF)를 고려합니다. [5]
각도 변화
쌍은 종종 높은 전하 밀도로 음의 극성 특성을 나타내며 전자의 결합 쌍에 비해 평균적으로 원자핵에 더 가깝습니다. 고독한 쌍의 존재는 높은 전하로 인해 결합 쌍의 전자 사이의 결합 각도를 감소시켜 전자 사이에 큰 반발력을 유발합니다. 그들은 또한 데이트 결합의 형성에 관여합니다. 예를 들어, 히드로늄 (H3O +) 이온의 생성은 산이 물에 용해 될 때 발생하며 산소 원자가 수소 이온에 고독한 쌍을 기증하기 때문입니다.
이것은 두 개의 더 일반적인 분자에서 볼 때 더 명확하게 볼 수 있습니다. 예를 들어, 고독한 쌍이 없는 이산화탄소(CO2)에서 산소 원자는 탄소 원자의 반대쪽에 있는 반면(선형 분자 기하학), 두 개의 고독한 쌍이 있는 물(H2O)에서는 수소 원자 사이의 각도가 104.5°(구부러진 분자 기하학)입니다. 이것은 수소 원자에 대한 모든 전자의 힘이 평형을 이룰 때까지 수소 원자를 더 멀리 밀어내는 산소 원자의 두 고독한 쌍의 반발력에 의해 발생합니다. 이것은 VSEPR 이론의 그림입니다.
쌍극자 모멘트
고독한 쌍은 분자의 쌍극자 모멘트에 기여할 수 있습니다. NH3의 쌍극자 모멘트는 1.42D입니다. 질소(3.04)의 전기 음성도가 수소(2.2)의 전기 음성도보다 크기 때문에 N-H 결합은 질소 원자의 순 음전하와 수소 원자의 순 양전하가 더 작은 극성입니다. 또한 고독한 쌍과 관련된 쌍극자가 있으며 이는 암모니아의 쌍극자 모멘트에 대한 극성 공유 N-H 결합에 의한 기여를 강화합니다. NH3 와 달리 NF3 는 0.234 D의 쌍극자 모멘트가 훨씬 낮습니다. 불소는 질소보다 전기 음성도가 높고 N-F 결합의 극성은 암모니아의 N-H 결합의 극성과 반대이므로 고독한 쌍으로 인한 쌍극자가 N-F 결합 쌍극자와 반대되어 분자 쌍극자 모멘트가 발생합니다.
입체성 고독한 쌍
고독한 쌍은 원자에 부착 된 세 개의 다른 그룹이 모두 다를 때 분자의 카이랄성 존재에 기여할 수 있습니다. 이 효과는 특정 아민, 포스핀, [7] 술포늄 및 옥소늄 이온, 설폭사이드, 심지어 카르바니온에서도 볼 수 있습니다.
입체 중심이 아민인 거울상 이성질체의 분해능은 입체 중심에서 질소 역전을 위한 에너지 장벽이 낮기 때문에 일반적으로 배제되며, 이는 2개의 입체 이성질체가 실온에서 빠르게 상호 변환되도록 합니다. 결과적으로, 이러한 키랄 아민은 아민 그룹이 순환 구조(예: Tröger의 염기)로 제한되지 않는 한 분해될 수 없습니다.
특이한 고독한 쌍
입체화학적으로 활성화된 고독한 쌍은 또한 2가 납 및 주석 이온에 대해 ns2 의 공식적인 전자 구성으로 인해 예상됩니다. 고체 상태에서는 PbO와 SnO 모두에 의해 채택된 정방형 암석 구조에서 관찰되는 왜곡된 금속 배위가 발생합니다. 이러한 중금속 ns2 고독한 쌍의 형성은 이전에 금속 s 및 p 상태의 원자 내 혼성화에 기인했습니다 [8] 최근에는 강한 음이온 의존성을 갖는 것으로 나타났습니다. [9] 음이온의 전자 상태에 대한 이러한 의존성은 PbS 및 SnTe와 같은 일부 2가 납 및 주석 물질이 고독한 쌍의 입체 화학적 증거를 나타내지 않고 대칭 암염 결정 구조를 채택하는 이유를 설명할 수 있습니다. [10][11]
분자 시스템에서 고독한 쌍은 금속 이온 주위의 리간드 조정에 왜곡을 일으킬 수도 있습니다. 납의 고독한 쌍 효과는 질산납(II)의 초분자 복합체에서 관찰할 수 있으며, 2007년 한 연구에서는 고독한 쌍을 납 중독과 연관시켰습니다. [12] 납 이온은 포르포빌리노겐 합성 효소라고도 하는 ALAD 효소의 아연 양이온과 같은 여러 주요 효소의 천연 금속 이온을 대체할 수 있으며 산소 운반 분자 헤모글로빈의 핵심 구성 요소인 헴의 합성에 중요합니다. 이러한 헴 합성의 억제는 납 중독 ( "토성"또는 "배관"이라고도 함)의 분자 기초 인 것으로 보입니다. [13][14][15]
계산 실험은 배위 수가 칼슘 결합 단백질의 치환시 변하지 않더라도 납의 도입으로 리간드가 그러한 새로운 고독한 쌍을 수용하기 위해 스스로를 구성하는 방식을 왜곡한다는 것을 보여줍니다. 이 고독한 쌍 효과는 위에서 언급한 포르포빌리노겐 합성효소와 같은 아연 결합 단백질에 대해 극적이 되는데, 이는 천연 기질이 더 이상 결합할 수 없기 때문입니다.
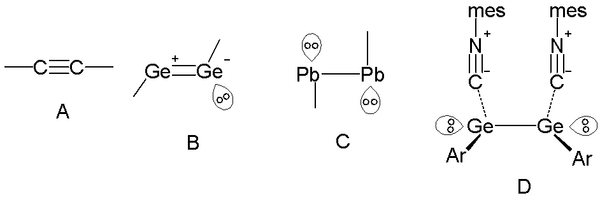
14족 원소(탄소기)에서 고독한 쌍은 단일 결합(결합 순서 1) 길이를 줄이거나 늘림으로써 나타날 수 있으며,[16] 삼중 결합의 유효 순서에서도 나타날 수 있습니다. [17][18] 친숙한 알카인은 탄소-탄소 삼중 결합(결합 순서 3)과 180° 결합 각도의 선형 형상을 가지고 있습니다(참조 [19]의 그림 A). 그러나 그룹(실리콘, 게르마늄 및 주석)에서 더 아래로 내려가면 공식적인 삼중 결합은 하나의 단독 쌍(그림 B[19])과 트랜스 벤트 형상을 갖는 유효 결합 차수 2를 갖습니다. 납에서 유효 결합 순서는 각 납 원자에 대해 두 개의 고독한 쌍을 가진 단일 결합으로 훨씬 더 감소합니다(그림 C[19]). 유기게르마늄 화합물(참고문헌의 반응식 1)에서, 유효 결합 차수는 또한 1이며, 게르마늄의 빈 4p 오비탈과의 상호작용을 기반으로 산성 이소니트릴(또는 이소시아나이드) C-N 그룹의 복합체가 있습니다. [19][20]
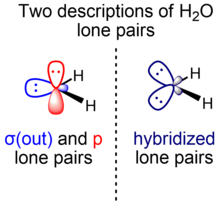
짝을 이루지 않은 전자
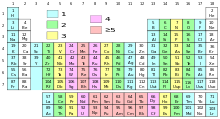
화학에서 짝을 이루지 않은 전자는 전자 쌍의 일부가 아닌 원자의 궤도를 단독으로 차지하는 전자입니다. 원자의 각 원자 궤도(세 개의 양자 수 n, l 및 m으로 지정됨)는 반대 스핀을 가진 두 개의 전자(전자쌍)를 포함할 수 있는 용량을 가지고 있습니다. 전자 쌍의 형성은 화학 결합의 형태 또는 고독한 쌍으로 에너지적으로 유리한 경우가 많기 때문에 짝을 이루지 않은 전자를 운반하는 개체는 일반적으로 반응성이 높기 때문에 화학에서 짝을 이루지 않은 전자는 상대적으로 드뭅니다. 유기 화학에서는 일반적으로 라디칼이라고 불리는 실체에 대한 반응 중에 잠깐 만 발생합니다. 그러나 반응 경로를 설명하는 데 중요한 역할을 합니다.
라디칼은 s- 및 p- 블록 화학에서 흔하지 않은데, 이는 짝을 이루지 않은 전자가 원자가 p 궤도 또는 sp, sp2 또는 sp3 하이브리드 궤도를 차지하기 때문입니다. 이 오비탈은 방향성이 강하기 때문에 겹쳐져 강한 공유 결합을 형성하여 라디칼의 이합체화를 선호합니다. 이합체화로 인해 결합이 약해지거나 짝을 이루지 않은 전자가 비국소화에 의해 안정화되는 경우 라디칼은 안정적일 수 있습니다. 대조적으로, d- 및 f- 블록 화학의 라디칼은 매우 일반적입니다. 짝을 이루지 않은 전자가 상주하는 방향성이 낮고 확산이 심한 d 및 f 오비탈은 덜 효과적으로 겹치고 더 약한 결합을 형성하므로 일반적으로 이합체화가 바람직하지 않습니다. 이러한 d 및 f 오비탈은 또한 비교적 작은 방사형 확장을 가지므로 이량체를 형성하기 위해 겹치는 것을 선호하지 않습니다. [1]
짝을 이루지 않은 전자를 가진 상대적으로 더 안정적인 실체가 존재하는데, 예를 들어 산화질소 분자가 전자를 가지고 있습니다. Hund의 법칙에 따르면 짝을 이루지 않은 전자의 스핀은 평행하게 정렬되어 이러한 분자에 상자성 특성을 부여합니다.
짝을 이루지 않은 전자의 가장 안정적인 예는 란탄족과 악티늄족의 원자와 이온에서 발견됩니다. 이러한 개체의 불완전한 f-shell은 해당 개체가 있는 환경과 매우 강력하게 상호 작용하지 않으며 이로 인해 쌍을 이루지 못합니다. 짝을 이루지 않은 전자가 가장 많은 이온은 7개의 짝을 이루지 않은 전자가 있는 Gd3+ 및 Cm3+입니다.
짝을 이루지 않은 전자는 자기 쌍극자 모멘트를 갖는 반면, 전자 쌍은 두 전자가 반대 스핀을 가지므로 자기 쌍극자 필드가 반대 방향에 있고 상쇄되기 때문에 쌍극자 모멘트가 없습니다. 따라서 짝을 이루지 않은 전자를 가진 원자는 자기 쌍극자 역할을 하고 자기장과 상호 작용합니다. 짝을 이루지 않은 전자를 가진 원소만이 상자성, 강자성 및 반강자성을 나타냅니다.
자유전자의 집단성= 플라즈마
플라즈마(plasma)-첨단기술의 원천인 제4의 물질 참조
플라즈마는 외래어다. 어떤 현상을 지칭하는 말로 막연히 알고 있다. 플라즈마란 세포의 원형질이나 혈장과 같이 말랑말랑한 상태로서, 고체.액체.기체에 이어 제4의 물질상태로 불린다.
플라즈마는 제4의 물질 상태라고 알려져 있는 물질의 형태이다. 강력한 전기장 혹은 열원으로 가열되어 기체상태를 뛰어넘어 전자, 중성입자, 이온 등 입자들로 나누어진 상태. 이때는 전하 분리도가 상당히 높으면서도 전체적으로 음과 양의 전하수가 같아서 중성을 띠게 된다. 전자가 열을 받아 원자에게서 자유로워지면 끝이기 때문에 당연히 어떤 원소든 플라즈마화 될 수 있으며, 전자의 탈출로 인해 전하를 띠기 때문에 전자기장으로 가두거나 특정 방향으로 가속시킬 수도 있다. 이를 실제로 특정 방향으로 가속하는 방법으로 이용한 것이 우주선 등에 쓰이는 이온 엔진이고 열을 가진 플라즈마를 전자기장으로 가두는 것이 토카막장치이다.
플라즈마(plasma)는 물리학이나 화학 분야에서 디바이 차폐(Debye sheath)를 만족하는 이온화된 기체를 말한다. 고체, 액체, 기체에 이어 4번째 상태로 원자핵과 자유전자가 따로따로 떠돌아다니는 상태이다. 자유 전하로 인해 플라즈마는 높은 전기 전도도를 가지며, 전자기장에 대한 매우 큰 반응성을 갖는다. 우주에 존재하는 물질의 99%가 플라스마로 이루어져 있다. 물리적으로, 플라즈마는 전기 전도도를 가지는 전하를 띤 입자들의 집합체로, 외부 전자기장에 집합적으로 반응한다. 플라즈마는 일반적으로 중성 기체와 같은 집합체 또는 이온 빔의 형태를 취하지만, 티끌을 포함하기도 하며, 이러한 플라즈마를 티끌 플라즈마(dusty plasma)라 한다.
=============================================
자유전자(free electron)는 원자로부터 해방되어 자유롭게 돌아다닐 수 있는 전자이다. 따라서 균일한 전기장이나 자기장 이외에 외부로부터 힘을 받는 일 없이 자유로이 움직인다. 원자 1개 속에는 원자번호와 같은 수의 전자가 있는데 대부분은 원자핵과의 전기적 작용에 의해 원자 안에 묶여 있다. 원자가 모여서 금속이 되면 원자 사이의 상호작용에 의해 각 원자의 가장 바깥쪽에 있는 전자가 해방되어 금속 안을 돌아다니는 자유전자가 된다.
금속이 전기나 열을 전하기 쉬운 것은 자유전자가 전하나 열운동의 에너지를 운반하기 때문이다. 반도체에서는 불순물 원자의 둘레에 느슨하게 묶여 있는 전자가 열운동에 의해 해방되어 자유전자가 된다. 열전자관이나 브라운관 등의 전자관은 음극에서 방출된 자유전자의 운동을 제어해 이용하는 것이다.또 대기 상층의 전리층에는 자유전자가 자연으로 존재해 전파반사의 원인이 된다.
물질 속의 자유전자라는 개념은 20세기초에 독일의 P.K.L.드루데와 H.A.로렌츠에 의해 금속의 원자가전자(原子價電子)가 자유전자의 기제로서 존재한다고 가정하면 금속의 전기전도·열전도 및 광학적 성질 등을 대략 섣명할 수 있다는 데서 형성되었다. 이것을 고전 자유전자모형이라고 하는데, 금속의 전기전도도(電氣傳導度)와 열전도도의 비는 같은 온도에서는 금속의 종류에 상관없이 같은 값을 가진다는 비데만-프란츠의 법칙을 설명할 수 있다. 그러나 고전적인 모형으로는 금속의 비열이나 상자성 대자율(常磁性帶磁率) 등에 대해서는 실험과 모순되고, 전자가 왜 격자간격(格子間隔)의 수백배의 거리를 마치 진공속에 있는 것과 같이 자유로이 운동할 수 있는냐 하는 점도 설명할 수 없다.
원자·분자 등의 내부에 속박되어 자유로이 운동할 수 없는 전자는 속박전자(구속전자)라고한다.
현재는 양자역학에 의거한 밴드이론에 의해 금속의 자유전자모형의 기초설정이 이루어지고 있다.
자유전자는 도체 물질에 대한 모형에서 상호작용이 없이 자유롭게 움직일 수 있다고 가정한 전자들이다. 금속 원자들이 금속결합을 하며 고체를 이룰 때 각 원자에서 떨어져 나온 원자가전자를 자유전자로 근사할 수 있다.
고전적인 드루드 모형(Drude model)에서 원자가전자는 원자로부터 완전히 떨어져 나와 자유롭게 움직이는 전자 기체를 형성한다. 이 기체는 이상기체로 취급될 수 있다. 즉, 전자와 전자 사이의 상호작용은 완전히 무시된다. 이온이 된 원자에 의한 전기장은 스크린 효과에 의해 미약하다고 가정한다.
드루드 모형은 옴의 법칙을 설명하는데 유용하다. 외부의 전기장이 없는 경우, 전자들은 열적 효과에 의해 무작위로 움직인다.
금속결합에 의한 자유전자
원자모형은 양파껍질처럼 서로 떨어진 껍질들이 있고 한 껍질내의 전자들은 같은 에너지를 갖는다고 설명한다. 그런데 각 껍질 내에 들어갈 수 있는 전자의 수는 정해져 있어 안쪽으로부터 2, 8, 8. 18. 18, 32 등이 된다. 원자핵에서 멀어질수록 전자의 에너지는 높고 원자핵의 인력은 작아진다.
금속결합이란 금속의 양이온과 자유전자 사이에 정전기적 인력(쿨롱의 힘)에 의해 이루어진 결합이다. 금속결합에서 원자내 전자들이 위치하는 껍질들이 다른 원자들의 껍질과 겹쳐 전자들이 위치하는 띠를 형성하게 된다. 원자가 전자들은 가전자대(valence band)에 위치하게 된다. 금속 내에서 자유로이 움직일 수 있는 에너지띠를 전도대(conduction band)라고 한다. 이 전도대에 있는 전자들을 여러 원자핵들이 공유하게 되어 개별적인 원자핵의 인력으로부터 자유롭게 된다. 가전자대에는 원자 안쪽의 궤도들이 서로 겹치면서 만들어진 것으로 연속적인 에너지를 가지는 전자들이 모(母)원자 주위에 구속된 채로 다른 곳으로 이동을 할 수가 없는 곳이다. 이에 반해, 전도대는 원자 바깥쪽의 궤도들이 겹치면서 만들어진 것으로 연속적인 에너지를 가진 전자들이 이 원자 주변에서 저 원자 주변으로 자유롭게 이동할 수 있는 곳으로, 이 전도대에 올라와 있는 전자를 자유전자라고 한다.
도체란, 가전자대와 전도대의 에너지 격차가 아주 작거나 서로 겹쳐 있어서 평상시에도 전도대에 다수의 전자가 존재하는 물질을 말하며, 부도체란 이 에너지 격차가 너무 커서 가전자대의 전자가 전도대로 오르지 못하는 물질이다. 금속결합은 원자가 전자가 1~2개여서 안정된 전자배열이 되기에 전자를 내버리는 쪽이 수월한 원자들이 서로 가전자대에 가깝거나 겹치게 전도대를 형성하여 전자를 서로 공유하므로 자유전자가 생긴다. 자유전자수가 많을수록 금속의 결합력은 커지게 된다. 이렇게 생긴 금속 내 자유전자는 다른 입자와의 상호작용으로 에너지를 얻어 금속을 빠져 나가게 될 때까지 금속 내에서 자유로이 움직이게 된다.
전리층에서 자유전자
전리층은 고도 약 60km~400km에 이르는 구간에 있다. 대양에서 복사된 자외선, 대전된 미립자 등과 우주에서 입사되는 우주선이 질소나 산소원자와 충돌하고 이 충돌에 의한 에너지로 전자가 방출되면서 양이온이 된다. 이러한 전리작용에 의해 자유전자와 양이온이 형성된다. 이 전리층에 의해 지상으로부터의 전파가 반사되기도 한다.
자유전자와 열전도와 관계
보통의 물질의 경우 열에너지는 순전히 분자들끼리 진동하면서 전해진다. 예를 들어 알갱이들이 서로 뭉쳐 있는 상태라고 한다면, 그 가운데 하나가 떨리면 그 떨림이 옆 알갱이에 전파되고, 그 전파된 알갱이는 또 전파하는 식으로 진동이 전체로 퍼지게 된다. 하지만 금속은 자유전자가 어디든 이동할 수 있는 구조여서 열에 대한 효과적인 전파자의 역할을 한다. 금속은 열전도율이 좋게 된다.
자유전자모형 이론
아놀드 섬머펠트(Arnold Sommerfeld)에 의해 개발된 이론이다. 고체물리학에서 이 이론은 고전 드루드 모형(classical drude model)과 양자역학적 페르미-디락 통계를 통합하여 만들었다. 이 이론으로써 전기 전도성, 열 전도성, 열용량에 관한 온도 의존성, 전자의 상태밀도, 결합에너지 범위 등을 설명한다.
격자 구조 내부의 원자가 전자(valence electron)들은 페르미-디랙 통계를 따르는데, 이 전자들 간의 상호작용과 원자핵의 퍼텐셜을 무시하는 것이 자유전자 모델이다. 결국 고체 내의 전자가 페르미 기체로 근사하는 모델. 금속을 설명할 때 많이 사용된다.
대학교 때 양자역학 시간에 수소원자의 전자궤도에 대해 배우다보면 알겠지만, 원자핵이 두개 이상, 즉 수소 분자 모델만 되어도 전자-전자, 원자핵-전자, 원자핵-원자핵 등 상호작용에 대해 고려하다보니 설명이 그리 만만치 않다는 것을 느낄 것이다. 그렇다보니 분자를 넘어서는 금속 결정 같은 거대한 구조에서는 고려해야 할 상호작용의 개수가 정말 무시무시하게 많아 도저히 정확히 풀어낼 수 없다. 그래서 '우리 그냥 심플하게 상호작용 같은 거 고민하지말고, 원자핵이나 다른 전자와 상호작용하지 않는 자유전자들로 기술하자!'라는 아이디어가 바로 자유전자 모델이다.
이 모델에서는 각 격자점에 고정된 원자핵이 존재하고 원자핵 주변에 자유 기체와 비슷한, 상호작용하지 않는 전자들이 자유롭게 퍼져있는 상황을 가정한다. 자유 전자들이 물체의 전도율이나 열용량을 결정하게 된다.
허나 이러한 기술은 전제조건에서 설명한 것처럼, 원자핵과 전자간의 상호작용의 크기가 작아야 잘 맞아 들어간다. 이러한 가정에 잘 맞는 게 바로 금속, 특히 알칼리 금속 계열의 금속 원소들이 가정한 모델과 가장 잘 맞았기 때문에, 주로 금속의 물성을 설명하는데 쓰인다.
자유 입자의 열용량은 32𝑘𝐵23kB에 자유입자의 개수를 곱한 값이다. 헌데, 실제로 전자가 열용량에 영향을 미치는 정도는 위 값보다 압도적으로 작다는 것이 문제였다. 이렇게 되면 자유 전자 모델로는 전혀 열용량을 설명할 수 없다는 문제가 생기게 된다!
이는 당시에 전자 궤도와 파울리 배타 원리와 같은 페르미온의 특성이 알려져있지 않다보니 생긴 일이었다. 이러한 문제는 양자역학과 통계역학의 발전을 통해 해결되는데, 전자는 페르미 - 디랙 분포를 따른다는 결과를 얻게 된 것이다. 이를 통해 원자 내부에 있는 전자들이 '전부' 에너지를 받아 들뜨는 것이 아니라 페르미 준위에서 특정 에너지의 범위 안에 있는 일부 전자들만이 자유전자가 된다는 사실을 알게 된 것이다.
이러한 수정을 통해 열전도율이나 홀 효과, 비저항값 등을 더욱 자세하게 설명할 수 있게 되었다.
========================================

트랜지스터(Transistor, Tr)의 기능 중 메모리 반도체에서는 스위칭 기능이 매우 중요합니다. MOSFET Tr의 스위칭 기능은 드레인 전류로 ON/OFF를 결정하는데, 드레인 전류는 소스 단자를 떠난 전자들이 채널(Channel)을 거쳐 드레인 단자로 건너가면서 흐르게 됩니다. 반도체의 주기능 중 하나는 이러한 역할을 수행하는 자유전자를 생성하고 운반하는 것인데요. 이번 장에서는 Tr 단자를 형성하기 위해 불순물을 주입한 후(농도 변화) 잉여전자와 자유전자를 생성하는 과정과 그에 따라 전자가 존재하는 확률에 대해 알아보겠습니다.
자유전자의 생성
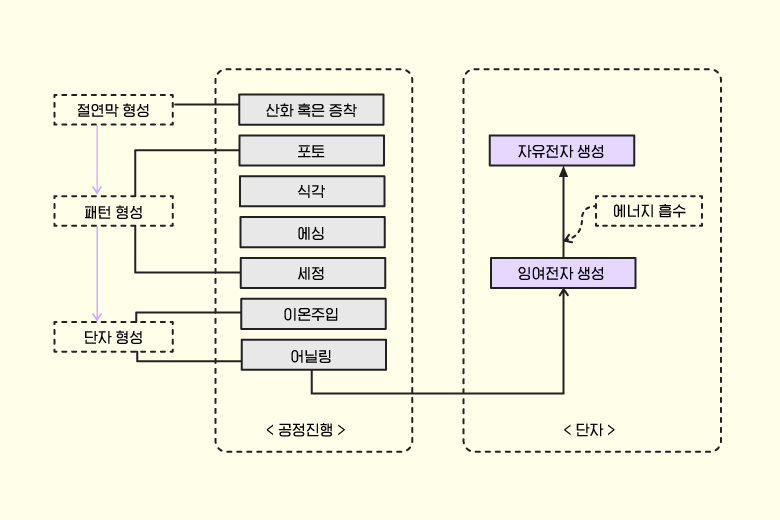
▲ 자유전자의 생성 과정
반도체에서 필요한 자유전자는 실리콘(Substrate)에 불순물 원자의 이온을 주입한 후, 온도를 약 800℃~1,000℃까지 올려 담금질하는 어닐링(Annealing)을 거쳐 형성된 소스 단자에서 생성됩니다. 소스 단자는 3족 혹은 5족의 원소(도펀트)가 4족인 실리콘과 공유결합한 후 공유결합에 참여하지 못한 잉여전자 혹은 정공들을 만들어냅니다. 이 잉여전자를 떼어내는 데는 공유결합에 참여한 전자들을 떼어내는 에너지보다 1/20 정도로 약한 에너지를 투입해도 가능하지요. 자유전자를 취득하는 데 있어 이같은 이점은 반도체 산업을 흥하게 한 요인 중 하나가 되기도 했지요. 전자뿐 아니라 정공 역시 조건만 약간 상이할 뿐 생성과정은 전자와 유사합니다. ▶<이온-임플란테이션 방식> 편 / <어닐링: 웨이퍼를 담금질하다> 편 참고
캐리어의 존재와 페르미-디락분포 확률함수의 의미
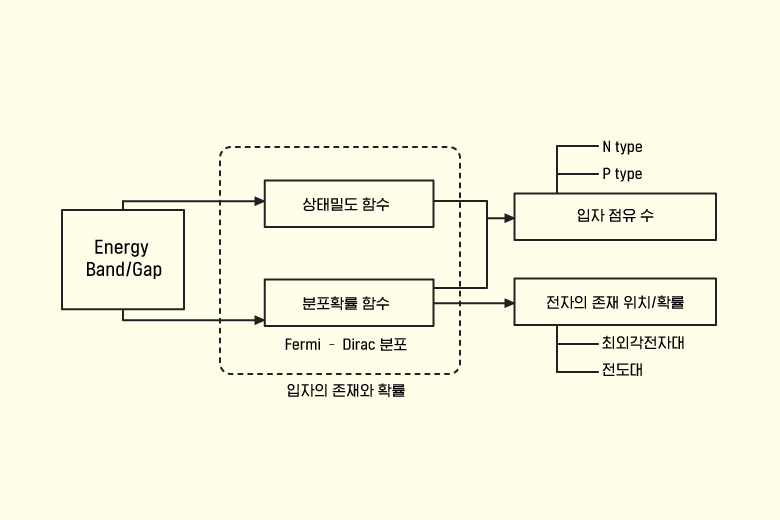
▲ 페르미-디락분포 확률함수의 역할
반도체 내 전자는 반도체를 구성하는 원자 내 궤도(오비탈)를 돌거나 혹은 원자와 원자 사이를 자유롭게 떠다니는 (자유전자) 2가지 경우로 존재합니다. 페르미-디락분포 확률함수는 캐리어(Carrier, 전자 혹은 정공)가 원자 내(최외각 껍질)에 머무는 확률을 지표로 나타낼 수 있는 함수인데요. 이를 통해 n형 반도체 및 p형 반도체 내에서 각각 Major 캐리어, Minor 캐리어를 확률값으로 나타내어 캐리어의 존재 여부를 확인할 수 있습니다.
페르미-디락분포 함수의 확률값이 높다는 것은 캐리어가 원자 내 최외각 껍질에 많이 머문다는 것이고, 확률값이 낮다는 것은 전자가 원자의 굴레로부터 탈출하여 자유전자로 많이 전이되었다는 의미입니다. 또한, 온도 변수와 농도 변수는 전자의 행동과 위치에 큰 영향을 끼치게 되는데요. 특히 이온 주입 시 도핑가스를 웨이퍼 표면에 얼마나 노출시켰느냐로 잉여전자(원자 내 포획된 전자)와 자유전자(원자로부터 탈출한 전자)를 확률적으로 예측할 수 있습니다. 단, 이는 어닐링(RTA)에 의해 도펀트들이 모두 실리콘과 공유결합에 성공했다는 전제가 성립되어야 가능합니다.
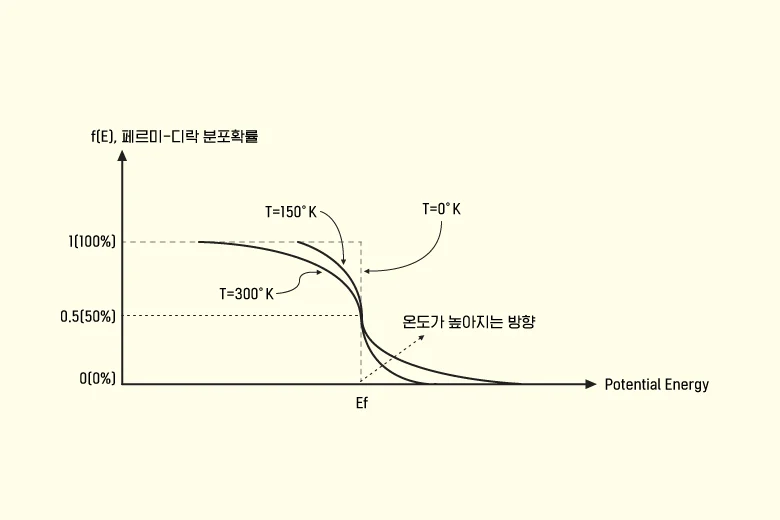
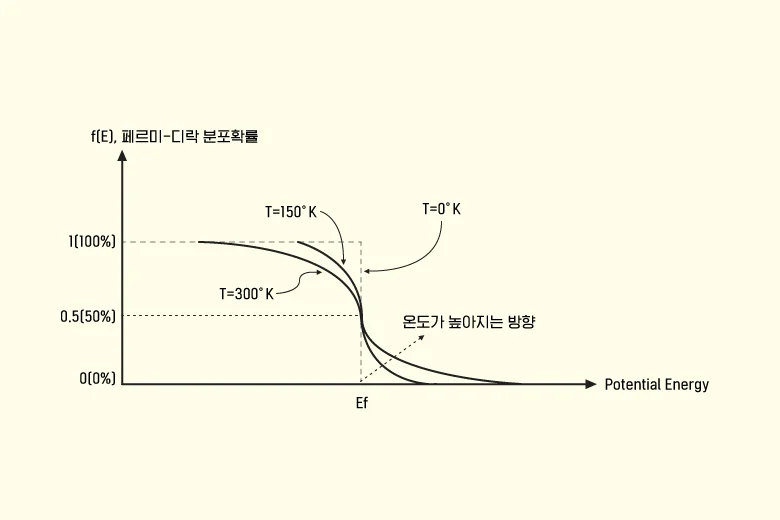
전자의 포텐셜 에너지 @ 페르미-디락분포 확률함수의 독립변수
Previous
Next
- 1
- 2
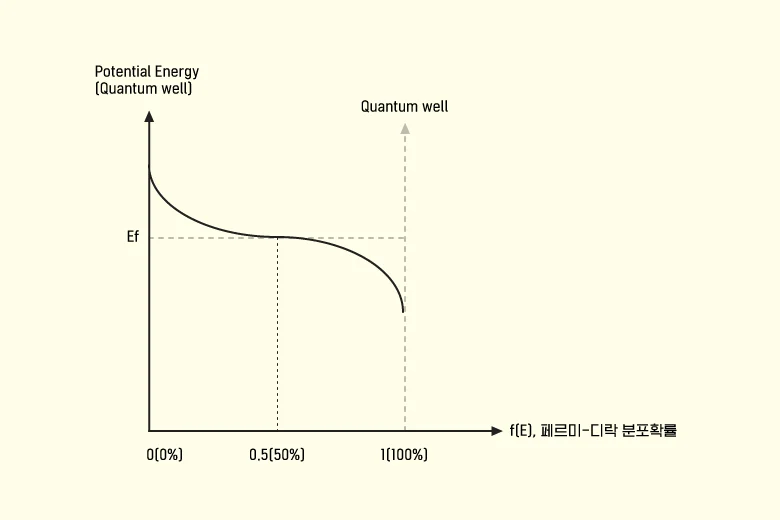
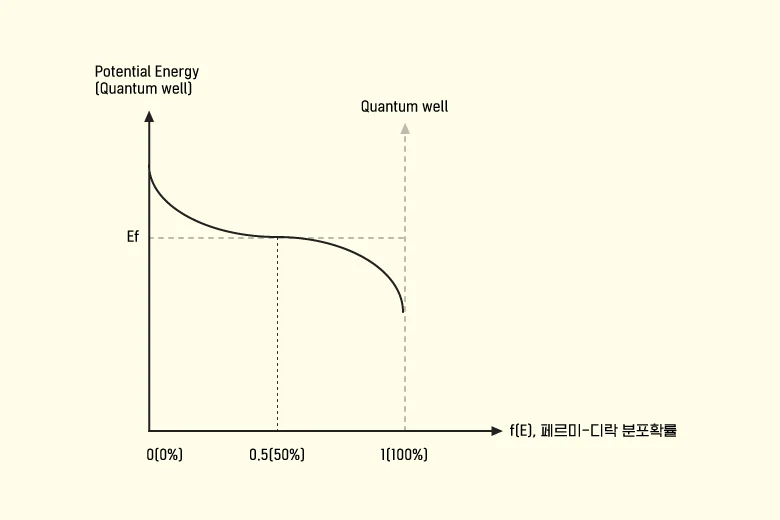
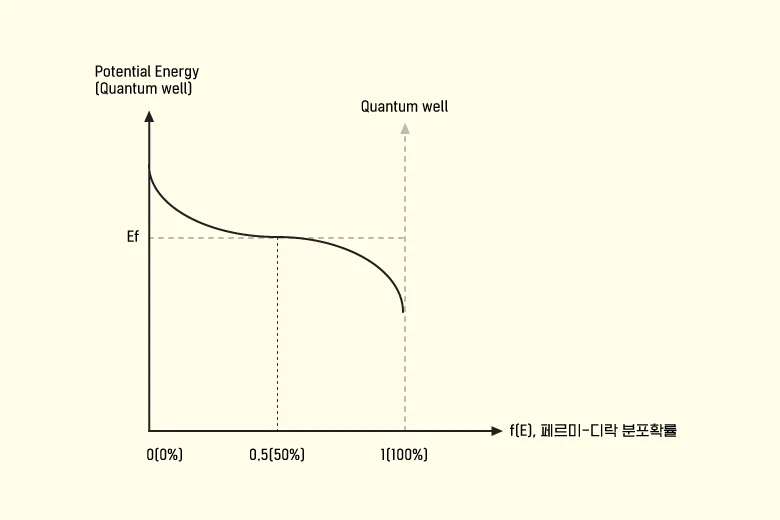
▲ 페르미-디락분포 함수 @2개 그래프는 x축(potential energy)과 y축(확률)값을 서로 교환한 그래프
반도체에서 페르미-디락 함수를 응용할 때 주어지는 조건인 독립변수는 캐리어(전자 혹은 정공을 의미하지만, 이하는 전자로 통칭)의 포텐셜 에너지(Potential Energy)입니다. MOSFET의 소스 단자와 채널, 혹은 드레인 단자 내 전자들이 어디(원자 내 혹은 밖)에 얼마나 있는지를 알아내기 위해 페르미-디락분포를 적용할 때, 전자가 가진 포텐셜 에너지를 독립변수로 페르미-디락분포에 대입하여 위치를 확률적으로 추정합니다(단, 정확한 전자 개수는 상태밀도함수를 함께 적용하여 계산해야 함). 여기서 전자의 위치를 통해 전자가 몇 퍼센트의 확률로 원자 내 최외각 껍질에 존재하는지 혹은 몇 퍼센트의 확률로 최외각 껍질에서 탈출했는지를 알아낼 수 있습니다.
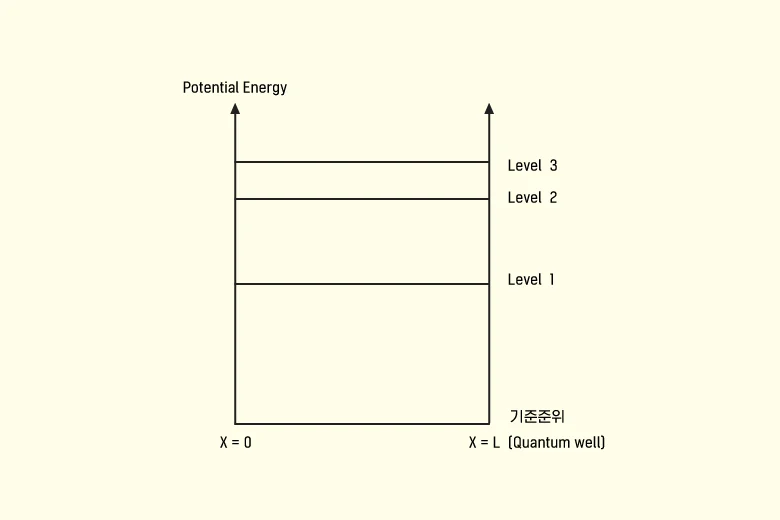
양자우물과 포텐셜 에너지
Previous
Next
- 1
- 2
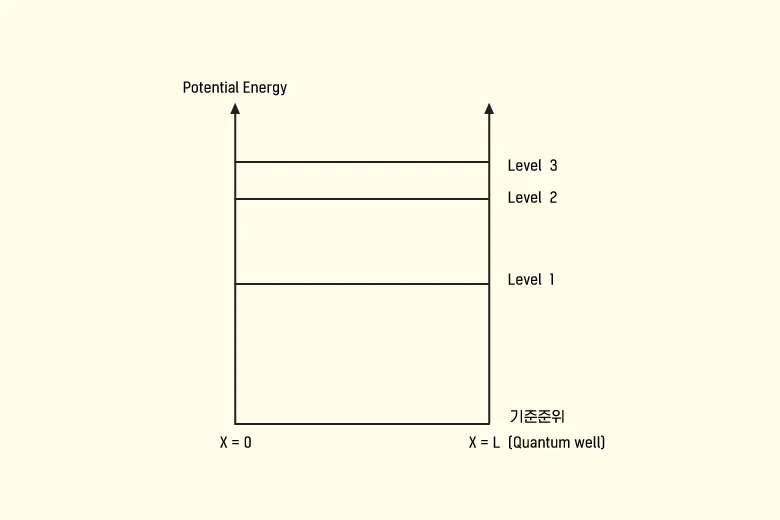
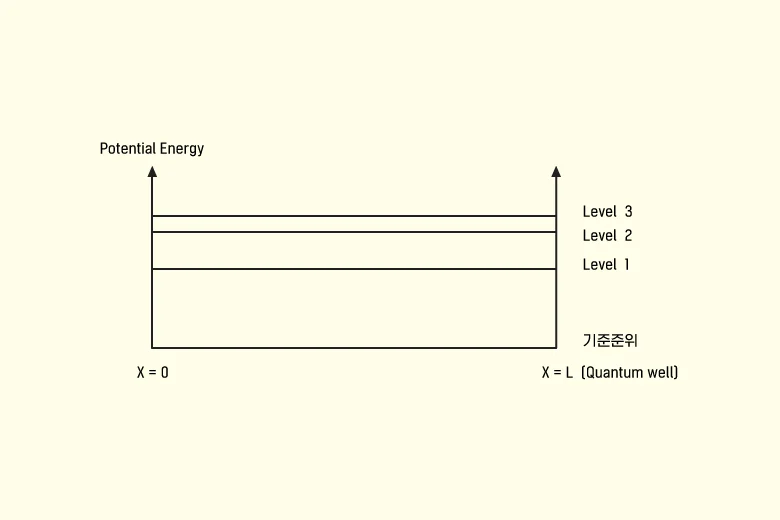
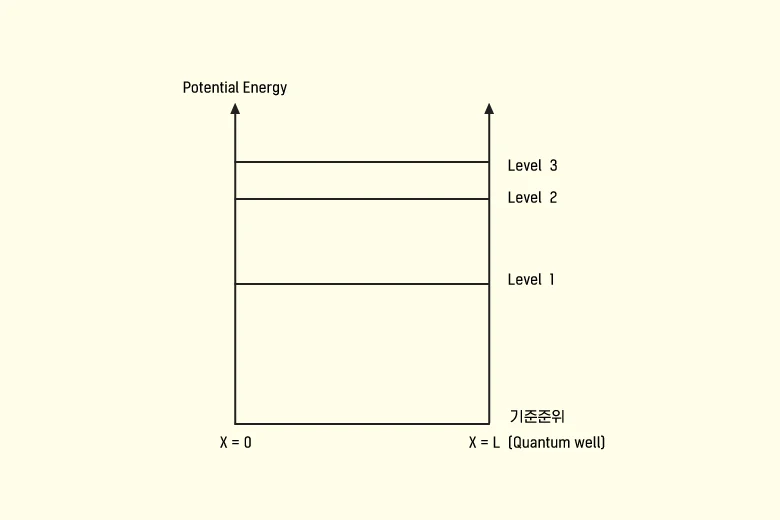
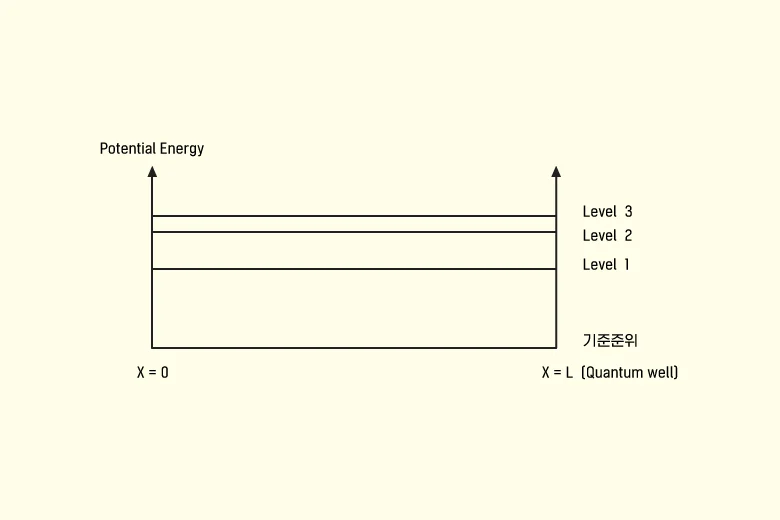
▲ 양자우물과 포텐셜 에너지 @ 입자 사이의 거리변수에 따른 영향
밀집대형을 이룬 결정성 실리콘 격자구조에 있어서는, 전자의 포텐셜 에너지는 양자우물의 에너지와 동일하다고 볼 수 있습니다. 다시 말해 원자와 원자 간 거리가 가까워지면 원자를 구성하면서 궤도를 돌고 있는 전자들의 포텐셜 에너지가 높아진다는 것이지요(슈뢰딩거 파동방정식: 전자의 양자화 개념을 베이스로 볼 때 양자우물의 길이가 좁아지면 양자우물에서의 입자에너지 준위level가 높아짐). 따라서 이온 주입 시 도즈량을 조절하여 불순물 농도에 변화를 주는 방식으로도 전자(입자)의 포텐셜 에너지값을 조절할 수 있습니다. 이렇게 얻은 전자의 포텐셜 에너지값을 페르미-디락분포 함수에 독립변수로 대입하여, 전자가 도펀트 원자 내 최외각 껍질에 존재할 확률을 알아낼 수 있습니다.
에너지 갭의 실체적 차이
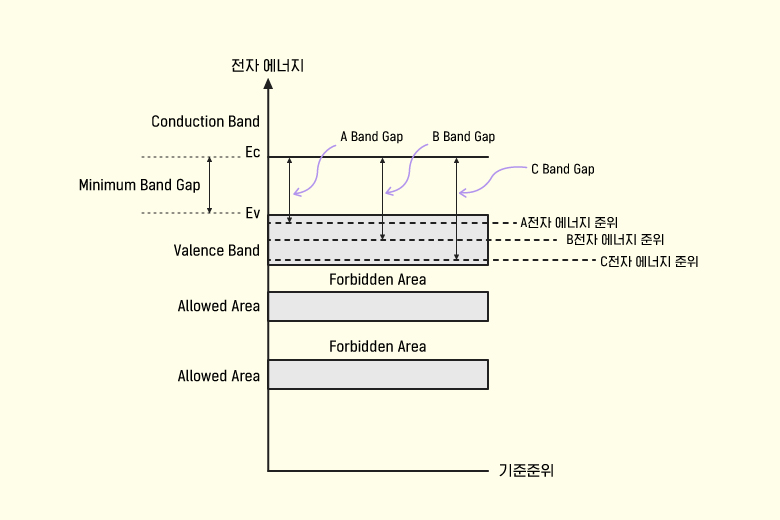
▲ 에너지 갭의 실체적 차이
원자의 에너지 준위 Level이 고체 내에서는 원자 간 거리가 가까워지면서, 에너지밴드(대표적으로는 Valence band) 및 에너지 갭(밴드갭, 최외각 껍질의 전자를 원자로부터 탈출시키는데 소요되는 최소에너지)의 개념으로 발전했습니다. ▶<반도체 전자와 에너지> 편 참고 에너지 밴드의 각 준위값들은 각 원자들의 최외각전자들이 보유하고 있는 에너지 준위값과 1:1로 대응되지요. 즉 여러 원자들이 모여 밴드를 형성(파울리의 배타원리에 의거)함으로써 각 원자 내 최외각전자들의 에너지 준위값은 제각각 달라집니다. 따라서 실리콘의 에너지 갭이 1.12eV(최소치)이지만 에너지 준위는 실체적 전자들의 포텐셜 에너지를 나타내므로, 각 원자들의 실제 에너지 갭 값들은 매우 미세하게 상이(1.12eV보다 높은 쪽으로)하다고 볼 수 있습니다. 이러한 에너지 갭 차이는 드레인 전류를 구성하는 최소한의 전자 개수를 예측하는 데 어려움을 줍니다. 다른 모든 공정변수가 이상적이라 할지라도 결국은 이상적이지 않은 상황(에너지 갭이 동일하지 않은 상황)이 발생할 수밖에 없다는 의미이지요.
전자 위치와 에너지
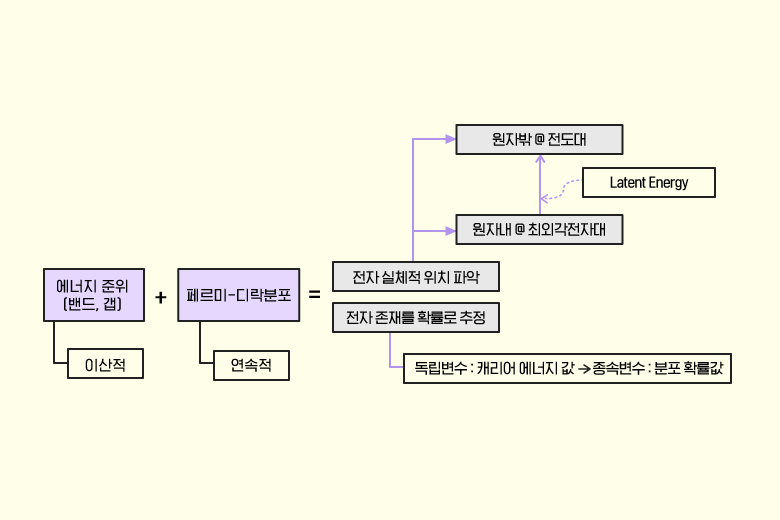
▲ 전자 위치와 Latent 에너지
#. Latent 에너지
반도체를 설계하거나 제품을 개발하는 입장에서는, 웨이퍼가 Fab out이 된 후 MOSFET 소자가 제대로 동작하느냐가 최대의 관심사입니다. 태아가 태어나서 숨을 쉬지 않으면 큰일이듯이 말입니다. 디바이스 동작의 주인공은 드레인 전류고, 드레인 전류의 핵심은 자유전자(정공)의 확보입니다. 자유전자는 최외각 껍질에 존재하던 전자가 일정량의 잠복 에너지(Latent 에너지)를 얻어야만 원자의 최외각 궤도를 이탈할 수 있습니다. Latent 에너지가 진성반도체인 경우는 에너지 갭인 셈이지요. 그런데 에너지 갭은 실리콘 결정격자가 형성되면서 고정되지만, Latent 에너지는 전자의 포텐셜 에너지(불순물 주입이 완료된 후 고정)에 따라서 가변적입니다(Latent 에너지=에너지 갭–불순물 주입으로 추가로 상승된 포텐셜 에너지). 포텐셜 에너지는 소스 단자 형성 시 도핑하는 불순물 농도가 높아지면 함께 상승합니다. 따라서 3족 혹은 5족의 불순물 도핑 농도를 높이면, 전도대까지 도달하는 경우 Latent 에너지를 줄일 수 있어 더욱 쉽게 자유전자를 획득할 수 있습니다. 또한, 도핑 농도를 높이면 페르미-디락분포 확률함수 전체가 상승합니다.
#. 에너지 개념에 대한 오해
전자의 존재와 이동은 미시세계의 물리적 현상이기에 고전물리학 개념으로 파악하기에는 어려움이 따릅니다. 에너지 개념은 이러한 반도체 전자를 이해하기 위해 도입되었지만, 전자의 물리적 현상을 에너지 개념(특히 페르미 에너지 레벨)으로만 해석하려다 보면 오해가 발생하기도 합니다. 물리적 현상과 에너지 개념을 함께 고려하면서, 반도체 내에서 전자의 존재와 이동을 이해해야 합니다.
먼저 전자의 물리적 위치는 원자 내(원자핵에 속박) 혹은 원자 밖(속박에서 해제), 2가지 경우로만 존재합니다. 전자/정공이 전도대 혹은 최외각전자대로 근접했다가 에너지 획득으로 jump하여 전도대(전자)/최외각전자대(정공) 속으로 들어가는 것이 아니라, 최외각 껍질에서 타원운동을 하던 전자가 Latent 에너지를 공급받아 물리적으로 원자 속박에서 탈출하는 형태이지요. Latent 에너지를 공급받는 동안에는 전자는 최외각궤도에 그대로 위치해 있습니다. 정공인 경우는, 옆에서 공유결합을 하고 있던 전자가 Latent 에너지를 공급받아 바로 이웃한 정공으로 뛰어 들면서 원래 있었던 자리에 정공을 만들어 놓는 형국이지요.
#. 에너지 금지대에 대한 오해
또한 궤도와 궤도 사이에 전자가 침범할 수 없는 물리적인 금지대가 있는 것은 아닙니다. 전자는 물리적으로 원자 내에 확률적으로 넓게 펴져 존재하며, 심지어 상위궤도를 도는 전자가 하위궤도를 도는 전자와 위치가 공간적으로 중첩(전기적 배타성으로 충돌되지는 않음)되기도 하지요. 하지만 전자들을 물리적으로 추적할 수 없어 이를 에너지로 환산하여 나타낸 것이 에너지 준위 혹은 밴드입니다. Ev는 최외각궤도 상에서 최외각전자가 어떤 위치에 있던 최대로 보유할 수 있는 포텐셜 에너지 값을 나타낸 것이지요. 또, 전자가 보유한 에너지 Level(에너지값)을 계산해 보았더니, 전자가 보유할 수 없는 에너지 영역(Ev보다 더 높은 에너지 영역)이 있어 이를 에너지 금지대(에너지 갭)라고 정의했습니다. 그러나 에너지 금지대는 Intrinsic 실리콘(혹은 저마늄) 상태일 때의 에너지 갭이고, 불순물이 첨가되면 전자의 포텐셜 에너지 Level이 Ev보다 상승하게 됩니다.
오늘은 원자 내 전자의 미시적인 세계에 대해 에너지를 매개체로 해석해보았습니다. 전자와 에너지의 관계를 설정하였고, 잉여전자와 자유전자의 차이점 및 에너지 밴드와 에너지 갭에 대하여도 알아보았습니다. 반도체 과학은 현재의 모순을 찾아내고 이를 해결하는 과정에서 계속 발전해나가야 합니다. 다음 장에서는 전자가 고체인 반도체 내에서 곧바로 드레인 전류로 투입 가능한 상태인지 예측할 수 있도록, 페르미-디락분포 함수를 이용하여 Intrinsic 및 Extrinsic, 절대온도 0도[K] 및 상온인 경우 등에 대해 확률적으로 알아보도록 하겠습니다.
================================
반도체 역할
'반도체'
너무도 익숙하고, 중요하다는 말을 워낙 많이 들어서 그런가보다.. 하고는 있지만 왜 중요한지는 잘 모르겠는 그 이름.
삼성전자, 하이닉스 주식에 투자는 하고 있지만, 아직 아리송한 그 녀석.
오늘은 대한민국 산업의 주춧돌이자 경제의 기반, 반도체가 무엇인지를 알아보고 왜 필요한지에 대해 설명해 드리겠습니다.
반도체는 도체(전기가 통하는 물질_철, 은, 구리 등)와 부도체(유리, 나무, 고무 등)의 중간 성질을 가진 물질로 그래서 이름도 반만 도체, '반도체'입니다. 즉, 전기가 통할 수도.. 통하지 않을 수도 있는 있는 물질의 집단을 말하죠. 대표적인 물질은 실리콘(Si, 규소)으로 IT 연구단지로 유명한 미국의 실리콘 밸리도 반도체의 주 재료인 실리콘(규소)와 산타클라라 인근의 계곡(Valley)를 합쳐서 만든 이름입니다.
이런 반도체가 전자기기에서 널리 쓰이는 이유는 중요한 특징이 있기 때문인데요.
그냥 있을때는 전기가 흐르지 않지만(부도체), 인위적으로 특정 불순물을 주입하면 전기가 흐르게 됩니다(도체). 또한 주입하는 불순물의 양을 조절하면 반도체의 전기전도도(전기가 통하는 정도)도 바꿀 수 있는데요. 이를 통해 실리콘 웨이퍼*가 전기회로의 기능을 갖추게 되는 것입니다.
*반도체를 만드는 토대가 되는 얇은 판으로 그 위에 트랜지스터와 다이오드 등의 미소 회로나 집적회로(IC)를 만들 수 있다
반도체는 크게 두 가지 기능을 합니다.
첫 번째는 전기신호의 처리입니다. 전기 신호의 처리 방식에는 정류, 증폭, 변환의 세 가지가 있습니다.
| 정류(Rectification) | 한 방향으로 흐르는 전류를 만드는 작용 한쪽에 낮은 저항을, 다른 쪽에 높은 저항을 둬 전류가 한쪽으로 흐르게 만드는 과정을 정류라고 한다. 가정용 및 산업용 전기는 거의 모든 경유 교류(양방향으로 전기가 흐르는 것)의 형태로 공급된다. 허나 많은 전자기기에는 그 내부에 직류가 필요하기 때문에 교류를 직류로 바꿔주는 정류회로(다이오드)가 탑재되어 있다. |
| 증폭 (Amplification) | 전기신호가 이동 중 약해지는 것을 강한 신호로 세기를 높여주는 작용 얻는 신호 대비 높은 출력 신호를 얻는 것으로 전압, 전력, 전류 값이 증가하는 것을 의미하며, 증폭을 가능하게 하는 반도체를 '트랜지스터'라 한다. |
| 변환 (Conversion) | 전기신호를 빛 또는 소리로 바꿔주는 작용 전기신호가 빛으로 전환되는 반도체가 'LED'이다. |

두 번째로는 데이터를 처리합니다. 데이터 처리 방식에는 전환, 저장/기억, 연산/제어의 세 가지가 있습니다.
| 전환 | 정보의 값을 아날로그에서 디지털 등으로 바꿔주는 작용 아날로그 정보. 즉, 숫자 '327'이, 문자 '엄마'가, 내가 노래방에서 부른 노래가, 친구가 찍은 사진은 모두 디지털 정보인 숫자 0,1로 표현이 가능하다. |
| 저장, 기억 | 정보를 프로그램화해서 저장하는 작용 이러한 정보를 저장하는 용도로 사용되는 반도체를 '메모리 반도체'라고 하며, 우리가 잘 아는 컴퓨터의 램(RAM)이 이에 속한다. 우리나라의 삼성전자와 하이닉스가 세계적인 경쟁력을 보유하고 있다. |
| 연산, 제어 | 기계나 설비가 정해진 순서에 따라 동작하도록 제어하는 작용 수치 정보를 계산하고 작동 순서를 프로그램화 해서 자동으로 제어해주는 반도체를 '논리반도체', '마이크로 프로세서' 혹은 '시스템 반도체'라고 한다. 컴퓨터의 CPU에 해당하는 반도체로 인텔, AMD 등이 글로벌 표준이다. |
반도체는 이처럼 많은 역할을 합니다. 실제로 전자기기를 구동하기 위한 대부분의 일을 반도체가 하고 있다고 해도 과언이 아니죠.
이처럼 반도체 기술이 발전하고 컴퓨터, 스마트폰 등 대부분의 IT 제품에 반도체가 쓰이면서 인류 문명은 크게 발전했습니다. 특히 메모리 반도체는 우리나라의 수출 1위 품목으로 사실상 대한민국 경제를 떠받쳐 주고 있다고 해도 과언이 아니죠.

앞으로도 세계 반도체산업은 4차 산업혁명으로 대표되는 사물인터넷(Iot)와 자율주행자동차, 인공지능(AI) 기술 등에 의해 더욱 성장해 나갈 것으로 예상됩니다. 하지만 우리나라 반도체 산업은 소자와 공정 부문에서는 강점이 있으나, 장비와 소재 부분에서는 미국, 일본 등 선도 국가와 큰 기술 격차를 보이고 있습니다. 일본이 반도체를 만드는데 필요한 불화수소나 불화폴리이미드 등의 수출을 규제했던 이유도 소재 부분에서 우리 기술이 부족하기 때문입니다. 실제로 우리나라 반도체 산업은 이런 수출규제와 중국의 반도체 굴기, 미국 반도체 기업의 메모리 소자에 대한 개발투자 등 외적 요인에 의해 큰 위기를 함께 겪고 있습니다.
우리나라 반도체 산업이 중국 등 후발주자의 추격을 따돌리고 경쟁 우위를 유지하기 위해서는 지속적인 기술 개발과 투자가 필요합니다. 또 반도체 공정 난이도 증가에 따라 그 중요성이 점점 커지고 있는 장비와 소재에 대한 해외 의존도를 낮춰야 합니다. 이를 위해서는 국내 반도체 대기업과 장비-소재 기업 간의 협력을 통한 동반성장이 무엇보다 중요합니다. 모쪼록 메모리 반도체 분야의 현재의 위기를 넘어, 앞으로는 시스템 반도체 쪽에서도 대한민국 기술의 이름이 세계에 널리 퍼지기를 기원합니다.
---------------------------------------------------
반도체가 뭘까?
- 철에는 전기가 통한다(도체). 플라스틱에는 전기가 통하지 않는다(부도체)
- 반도체는 도체와 부도체의 성격을 모두 가지고 있어 어떨 땐 전기가 통하고 어떨 때는 통하지 않음
- 순수 반도체는 전기가 거의 통하지 않지만, 어떤 인공적인 조작을 가하면 도체처럼 전기가 흐르기도 함
- 즉, 빛이나 열을 가하거나 특정 불순물을 주입하게 되면 반도체에 도체처럼 전기가 흐르게 됨.
반도체의 원리
일반적으로 반도체에 쓰이는 원소는 다음의 두 가지임.
1. 주기율표 4족에 있는 원소(Elemental) 반도체
- 실리콘(Si) 혹은 게르마늄(Ge) 등 한 가지 원소로 구성된 반도체
- 실리콘은 집적회로 IC(Integrated Circuits)에 가장 많이 사용되는 반도체로, 모래에서 얻음
- 실리콘 반도체의 경우 반도체 물질에 불순물을 주입하여 전기전도도를 조절함
2. 주기율표 3족, 5족 원소의 결합으로 이루어지는 화합물(Compound) 반도체
반도체가 만들어지는 실리콘 단결정
- 단결정: 시료의 어느 부분을 보아도 결정(Crystal) 축의 방향이 같은 것
- 다결정: 많은 단결정들이 여러 방향으로 모여 있는 것
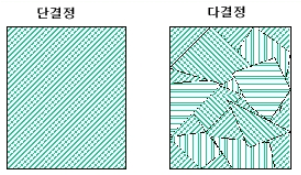
실리콘 단결정에 불순물을 주입하면 외인성 반도체가 만들어진다
- 실리콘 단결정은 실리콘 원자가 규칙적으로 늘어서 있는 상태를 의미
- 한 개의 실리콘 원자는 최외각에 4개의 전자를 가지기 때문에 이웃하는 원자끼리 굳게 결합해 결정을 이룸
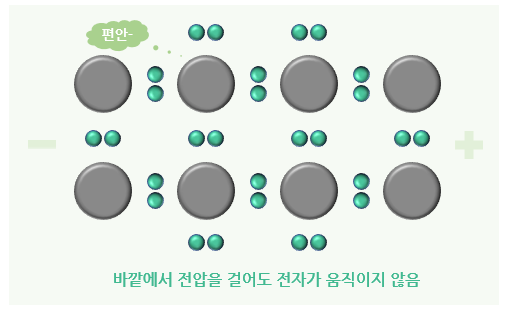
<실리콘 원자들의 공유결합 상태>
- 이런 순수한 실리콘에서는 최외각전자가 8개가 채워진 상태로, 원자핵에 결합되어 있는 전자가 움직일 수 없음
- 따라서 실리콘 외부에서 전압을 걸어도 전류가 흐르지 않음 (이를 진성(Intrinsic) 반도체라고 부름)
- 이러한 진성반도체는 부도체와 다를 바 없는 상태지만, 특정 불순물을 주입해주면 전류가 흐르게 됨.
- 인(P), 붕소(B) 등의 물질은 실리콘 웨이퍼가 전자회로의 기능을 같게 해 줌
- 불순물에 있는 전자나 정공이 전류가 흐르는 매개체 역할을 하여 원하는 방법으로 성질을 변화시키는 것
- 이렇게 불순물로 자신의 전기전도도를 조절하는 반도체를 외인성(Extinsic) 반도체(=불순물 반도체)라고 부름
WHY?
: 8개의 전자가 모여 평화로웠던 세상에 3개 혹은 5개의 전자를 가지는 불순물을 넣어 전자가 움직일 수 있는 길을 열어주는 것
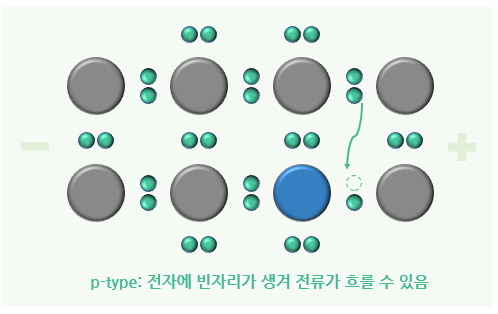
- p-type 실리콘: 3족 원소를 소량 넣어주게 되면 전자가 비려있는 상태, 즉 정공(Hole)이 생김. 이 상태에서 전압을 걸어주면 전류가 흐름
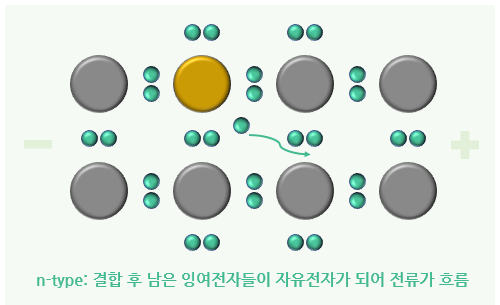
- n-type 실리콘: 5족 원소를 소량 넣어주면 원자가 남는 상태, 즉 잉여 전자가 생김. 이때 전압을 걸면 잉여 전자가 자유전자가 되어 전류가 흐름

흥미진진반도체가 만들어지는 과정
반도체를 만드는 8대 공정이라는 것이 있다고 한다

1. 웨이퍼 공정
- 모래에서 추출한 실리콘을 고온의 열로 녹여 고순도의 실리콘 용액을 만들고 굳히며 잉곳을 만듦
- 얇은 웨이퍼를 만들기 위해 다이아몬드 톱을 이용해 잉곳을 균일한 두께로 절단함
- 거친 표면을 매끄럽게 갈아내고 표면을 평평하게 만드는 화학적 기계적 연마 공정(CMP)을 거침
- 마지막으로 세척과 검사를 통해 웨이퍼를 확인함
(참고) 잉곳: 고온에서 녹인 실리콘으로 만든 실리콘 기둥
이 단계까지 만들어진 웨이퍼는 전기가 통하지 않는 부도체 상태임!
2. 산화 공정
- 이어지는 공정에서 생길 수 있는 오염물질/ 산화물질 등으로부터 웨이퍼를 보호하는 산화막을 씌움
- 건식 산화: 산소만 이용, 산화막 성장 속도가 느리기 때문에 얇은 막을 만들 때 사용
- 습식 산화: 산소+수증기 이용, 산화막 성장 속도가 빠르고 두꺼운 막을 형성함
3. 포토 공정
- 웨이퍼 위에 반도체 회로를 그려 넣는 공정으로, 감광액 도포 - 노광 - 세부공정 단계로 진행
- 필름을 인화지에 새기는 방법과 같은 원리로, 필름 역할을 하는 마스크(Mask)를 인화지 역할을 하는 웨이퍼에 얹어 현상하는 과정이라고 이해하면 쉬움
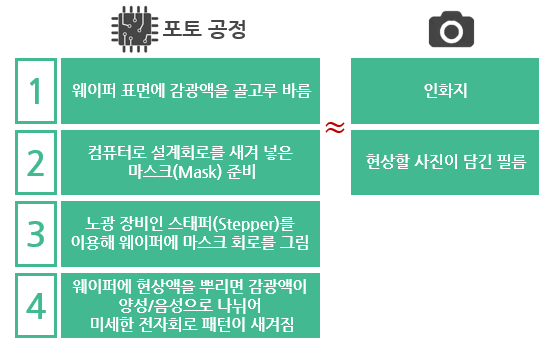
- 여기서 노광이란, 빛을 선택적으로 조사하는 과정을 말함
- 웨이퍼 위에 마스크를 놓고 빛을 쪼이면 회로 패턴을 통과한 빛으로 인해 웨이퍼에 패턴이 옮겨짐
- 이 웨이퍼에 현상액을 뿌리면 감광액이 빛을 받은 부분이 제거된 부분과 빛을 받은 부분으로 나뉘며 전자회로 패턴이 새겨지는 것
4. 식각 공정
- 포토공정에서 형성된 감광액 부분을 남겨두고 나머지 부분을 제거해 회로를 형성하는 과정
- 건식 식각: 가스 이용. 정확성이 좋아 작은 패터닝 가능. 단 고비용, 과정이 어렵고 한 장씩 공정을 해야 함
- 습식 식각: 화학액 이용. 저비용, 그러나 정확도가 떨어짐
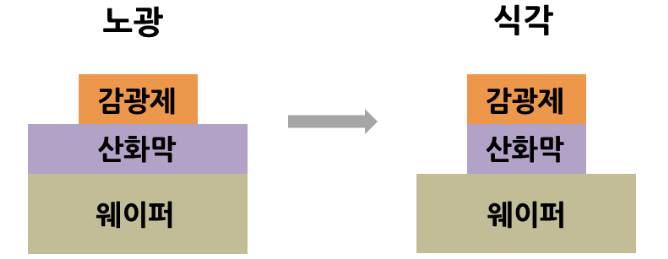
<Source: SK careers journal>
최근에는 건식 식각이 확대되고 있는 추세라고 함.
5. 박막 공정
웨이퍼에 불순물을 확산하고 박막을 형성해 웨이퍼가 반도체의 성질을 가질 수 있도록 하는 단계 (드디어!!)
- 증착: 웨이퍼 위에 분자 혹은 원자 단위의 물질을 입혀 전기적 특성을 가지게 하는 공정
- 화학적 기상 증착(CVD, Chemical Vapor Deposition)과 물리적 기상 증착(PVD) 방법이 있음
- 반도체에서는 CVD를 주로 사용
- CVD에서는 금속막을 씌우면 전기가 잘 흘러 소통을 원활하게 하고 절연막을 씌우면 회로와 회로를 분리해주는 역할을 하게 됨. 여기에 웨이퍼 내부에 이온 불순물을 집어넣는 확산 공정을 통해 부도체였던 웨이퍼를 위에서 배운 외인성 반도체로 만드는 것.
- 박막: 기계 가공으로는 실현 불가능한 두께인 1 마이크로미터 이하의 얇은 막으로, 회로를 구분하고 보호해줌
- 반도체 칩은 여러 개의 회로를 쌓아 만드는데, 각 층의 회로를 구분하고 보호하기 위해 박막을 씌워줌
6. 금속 배선 공정
- 전기가 잘 통하는 금속을 골라 신호가 전달되는 금속선을 연결해줌
- 외부에서 얻어지는 전기적 에너지를 받아 소자들끼리 신호가 섞이지 않고 전달되도록 선을 연결함

<Source: LG display Blog>
7. EDS
- 전기적 특성 검사를 통해 각각의 칩들이 원하는 품질 수준에 도달하는지 테스트하는 과정
- 총 다섯 단계로 진행됨
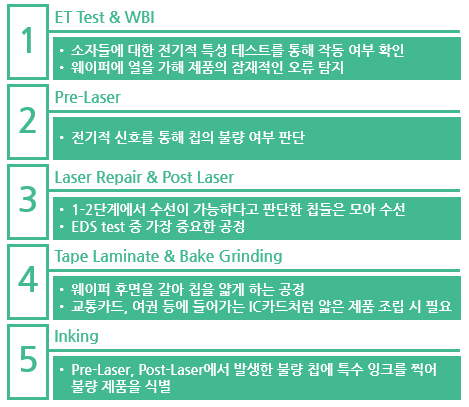
8. 패키징
- 제품이 출하되기 전 거치는 마지막 테스트로 다섯 단계로 진행됨

========================================