01. 녹는점과 끓는점
1. 물질의 특성
(1)물질의 특성: 다른 물질과 구별되는 그 물질만이 가지는 고유한 성질이다.
①물질을 구별하는 데 이용된다.
②물질의 양에 관계없이 일정하다.
(2)물질의 특성이 될 수 없는 것: 같은 물질이라도 조건에 따라 다른값이 나올 수 있는 경우에는 물질의 특성이 될 수 없다.
(3)겉보기 성질: 사람의 감각 기관이나 간단한 도구를 이용하여 구별할 수 있는 물질의 성질이다.
|
겉보기성질 |
조사방법 |
예 |
|
색 |
흰 종이를 뒤에 대고 색을 관찰한다. |
금(노란색),황산구리(푸른색) |
|
맛 |
물에 녹여서 거름종이에 묻혀 혀끝에 살짝 대어 본다. |
설탕(단맛),소금(짠맛),식초(신맛),소다(쓴맛) |
|
냄새 |
손으로 바람을 일으켜 시약의 증기가 코쪽으로 오게하여 간접적으로 맡는다/ |
식초(신 냄새),암모니아(자극성 냄새) |
|
굳기 |
기준 물질을 정한 후 긁어보고 기준 물질과 비교한다. |
석고(무름),금강석(단단함) |
|
촉감 |
손으로 비벼본다. |
밀가루(부드러움),소금(거침) |
|
결정 모양 |
돋보기나 현미경을 이용하여 관찰한다. |
염화나트륨(정육면체),석영(육각기둥) |
2. 녹는점과 어는점
(1)녹는점: 고체가 녹아서 액체로 상태 변화할 때의 온도이다.
①고체의 가열 곡선에서 온도가 일정하게 유지되는 부분의 온도이다.
②녹는점에서는 가해진 열이 모두 고체를 액체르 상태변화시키는 데 쓰이기 때문에 온도가 높아지지 않고 일정하게 유지된다.
(2)어는점: 액체가 얼어서 고체로 상태 변화할 때의 온도이다.
①액체의 냉각곡선에서 온도가 일정하게 유지되는 부분의 온도이다.
②어는점에서는 액체가 고체로 어는 동안 열을 방출하기 때문에 온도가 낮아지지 않고 일정하게 유지된다.
(3)녹는점과 어는점의 특징
①녹는점과 어는점에서는 고체와 액체 상태의 물질이 함께 존재한다.
②순수한 물질은 녹는점과 어는점이 같다.
③논ㄱ는점과 어는점은 물질의 종류에 따라 다르므로 물질의 특성이 된다.
④녹는점과 어는점은 물질의 양이나 가열하는 불꽃의 세기에 관계없이 일정하다.
-질량이 많아지면 녹는점(어는점)에 도달하는 데 걸리는 시간이 길어진다.
-불꽃의 세기가 세지면 녹는점(어는점)에 도달하는데 걸리는 시간이 짧아진다.
(4)녹는점과 어는점의 이용
①쉽게 녹으면 안 되는 경우: 녹는점이 높아야 한다.
②쉽게 녹일수 있어야 하는 경우: 녹는점이 낮아야 한다.
3. 끓는점
(1)끓는점: 액체가 끓어서 기체로 상태 변화할 때의 온도이다.
①액체의 가열 곡선에서 온도가 일정하게 유지되는 부분의 온도이다.
②끓는점에서는 가해진 열이 모두 액체를 기체로 상태 변화시키는데 쓰기이 때문에 온도가 높아지지 않고 일정하게 유지된다.
(2)끓는점의 특징
①끓는점에서는 액체와 기체상태의 물질이 함께 존재한다.
②끓는점은 물질의 종류에 따라 다르므로 물질의 특성이 된다.
③끓는점은 물질의 양이나 가열하는 불꽃의 세기에 관계없이 일정하다.
(3)압력과 끓는점
①외부 압력이 높아지면 끓는점이 높아진다.
②외부 압력이 낮아지면 끓는점이 낮아진다.
4. 온도와 물질의 상태
(1)물질은 온도에 따라 고체, 액체, 기체 중의 어느 한 가지 상태로 존대한다.
(2)물질이 상온에서 존재하는 상태는 물질의 녹는점과 끓는점에 따라 다르다.
①녹는점보다 낮은 온도에서는 고체 상태로 존재한다.
②녹는점과 끓는점 사이의 온도에서는 액체 상태로 존재한다.
③끓는점보다 높은 온도에서는 기체 상태로 존재한다.
02. 밀도
1. 부피
(1)부피: 물질이 차지하는 공간의 크기를 말한다
(2)부피의 단위: ㎖,ℓ,㎤,㎥ 등
(3)부피의 측정
①고체의 부피 측정
-모양이 규칙적인 고체의 부피: 자로 길이를 측정하여 계산한다
-모양이 불규칙한 고체의 부피: 액체와 눈금 실린더를 이용한다
②액체의 부피 측정: 눈금 실린더, 피펫 등으로 측정
③기체의 부피 측정: 물을 가득 채운 눈금 실린더를 물이 담긴 수조에 거꾸로 세우고 기체를 넣어 밀려나오는 물의 부피를 측정한다
2. 질량
(1)질량: 상태나 모양에 관계없이 일정한 물질의 고유한 양
①표준 질량인 분동과 비교하여 질량을 측정한다.
②측정 장소가 달라지더라도 질량은 변하지 않는다
③질량 측정 도구: 윗접시 저울, 양팔 저울 등
④질량의 단위: ㎎,g,㎏ 등
(2)윗접시 저울을 사용한 질량 측정
①물체의 질량을 측정할때
-평평한 곳에 윗접시 저울을 놓고 영점 조절 나사를 돌려 수평을 맞춘다
-왼쪽 접시에 측정할 물체를 올려놓는다
-오른쪽 접시에 무거운 분동부터 핀셋을 사용하여 올려놓는다
-저울이 수평이 되었을때 오른쪽 접시에 있는 분동의 질량이 물체의 질량이다
②일정한 양의 약품을 잴 때
-평평한 곳에 윗접시 저울을 놓고 질량이 같은 약포지를 양쪽 접시 위에 올려놓는다
-영점 조절 나사를 돌려 수평을 맞춘다
-왼쪽 접시에 필요한 만큼의 질량에 해당하는 분동을 올려놓는다
-오른쪽 접시에 저울이 수평이 될 때까지 약수저로 약품을 조금씩 올려놓는다
3. 밀도
(1)밀도: 어떤 물질을 단위 분피에 대한 질량이다
밀도= 질량/부피 (단위: g/㎤㎏/㎥g/㎖)
①밀도는 물질의 종류에 따라 고유한 값을 가지므로 물질의 특성이다
②밀도가 큰 물질은 아래에 가라앉고, 밀도가 작은 물질은 위에 뜬다
(2)물질의 상태와 밀도의 변화
①고체와 액체의 밀도
-압력에 따른 부피 변화가 거의 없으므로 압력에 따른 밀도의 변화가 거의 없다.
-온도가 높아짐에 따라 부피가 약간 증가하므로 온도가 높아질수록 밀도가 조금씩 작아진다
②기체의 밀도
-압력이 높아짐에 따라 부피가 작아지므로 압력이 높아질수록 밀도가 증가한다
-온도가 높아짐에 따라 부피가 증가하므로 온도가 높아질수록 밀도가 작아진다
-기체의 밀도는 고체나 액체의 밀도에 비해 매우 작으며, 기체의 밀도를 나타낼때는 온도와 압력을 함께 표시한다.
(3)우리의 생활과 밀도의 이용
①밀도를 작게하여 이용하는 경우: 위로 뜨게 할 때
②밀도를 크게하여 이용하는 경우: 아래로 가라앉게 할 때
03. 용해도
1. 용해와 용액
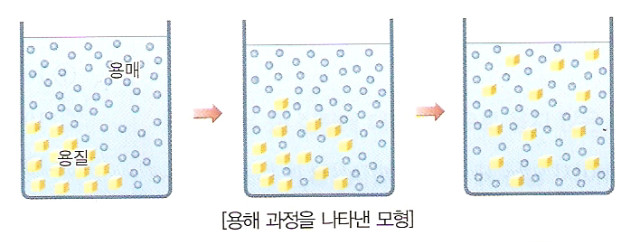
(1)용해: 한 물질이 다른물질에 녹아서 고르게 섞이는 현상
(2)용액: 용해에 의해 한 물질이 다른물질에 고르게 섞여 있는 혼합물이다
①용매: 다른 물질을 녹이는 물질이다
②용질: 다른 물질에 녹아 들어가는 물질이다
(3)용액의 특징
①용질 입자가 보이지 않는다
②거름종이로 걸러도 걸러지는 것이 없다
③오랫동안 놓아두어도 가라앉는 것이 없다
④섞이기 전의 물질의 성질을 그대로 가지고 있다
⑤대부분 무색투명하고 색깔이 있는 투명한 액체도 있다
⑥용매 입자와 용질입자가 고루섞여 있어 용액의 어느부분이나 색이나 맛, 밀도 등이 같다
⑦용액을 증발시키면 용질을 얻을수 있다 즉 용질은 작은 입자로 나뉘어 용매에 퍼져 있을 뿐이지 없어지는 것은 아니다
2. 용해될 때의 부피와 질량변화
(1)부피변화: 작은 입자가 큰 입자사이에 끼어들어 입자사이의 빈 공간이 줄어들기 때문에 용해 후 부피가 감소한다
(용질의 부피+용매의 부피)>용액의 부피
(2)질량 변화: 용질과 용매의 입자수가 변하지 않기 때문에 용해후 질량은 변하지 않는다
(용질의 질량+용매의 질량)=용액의 질량
3. 용액의 농도
(1)농도: 용액 속에 용질이 얼마나 녹아 있는가를 나타내는 값, 즉 용액의 묽고 진한 정도를 말한다
①농도에 따라 용액의맛, 색,밀도,어는점,끓는점이 달라진다
②같은 물질이라도 농도가 달라질수 있으므로 농도는 물질의 특성이 아니다
(2)퍼센트(%)농도: 용액 100g속에 녹아있는 용질의 g수를 백분율로 나타낸 값이다
퍼센트(%)농도=용질의 질량/용액의 질량×100
=용질의 질량/용질의 질량+용매의 질량×100
4. 용해도
(1)포화 상태
①일정량의 용매에 최대한 녹을 수 있는 용질의 양에는 한계가 있다. 따라서 이 양보다 용질을 더 넣으면 용질은 녹지 않는다
②포화: 어떤 온도에서 일정한 양의 용매에 용질이 최대한 녹아 있어 더 이상 용해되지 않는 상태
-포화용액: 포화상태에 있는 용액
-불포화 용액: 용매에 용질이 더 녹을수 있는 용액
-과포화 용액: 용매에 용질이 포화상태보다 더 많이 녹아있는 용액
(2)용해도: 어떤 온도에서 용매 100g에 최대로 녹을수 있는 용질의 g수이다
①같은 용질이라도 온도 및 용매의 종류에 따라 용해도가 달라진다
②같은 온도에서 같은 용매에 대한 용해도는 용질의 종류에 따라 다르므로 용해도는 물질의 특성이다
(3)용해도 곡선: 어떤 물질의 온도에 따른 용해도 변화를 그래프로 나타낸 것이다
①용해도 곡선 상에 있는 용액은 포화상태, 용해도 곡선 아래에 있는 용액은 불포화 상태이다
②용해도 곡선의 기울기가 급할수록 온도에 따른 용해도 변화가 크다
③용해도 곡선을 이용하면 어떤 용액을 냉각시킬때 석출되는 결정의 양을 알수 있다
5. 물질의 상태와 용해도
(1)고체와 액체의 용해도
①온도가 높을수록 용해도가 증가한다
②압력에 따른 용해도의 변화가 거의 없다
③고체와 액체의 용해도를 나타낼 때는 온도를 함께 표시한다
(2)기체의 용해도
①온도가 높을수록 용해도가 감소한다
②압력이 높을수록 용해도가 증가한다
③기체의 용해도를 나타낼때는 온도와 압력을 함께 표시한다