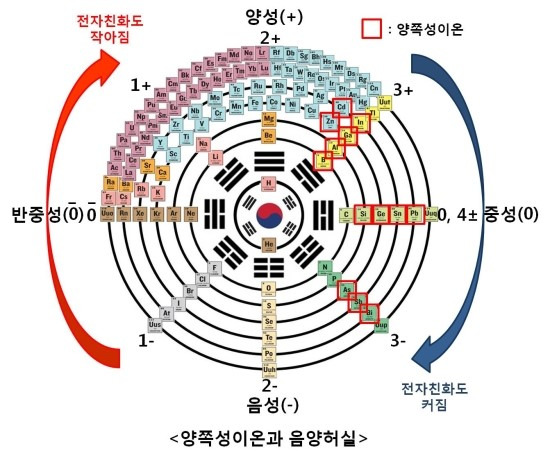
양쪽성이온(쯔비터이온,amphoteric ion,zwitterion)은 산성에 대해서는 염기성을, 염기성에 대해서는 산성을 나타내는 이온으로써 산성과 염기성에 모두 작용합니다.
양쪽성이온은 위의 그림과 같이 중성(0)상태를 기점으로 음(陰,-)과 양(陽,+)의 크기에 큰 차이가 없는 원소들입니다. 금속원소와 비금속원소의 중간상태이며, 전기적으로도 거의 중성이고 산화수(number)가 중간입니다.
물과 아미노산 등은 대표적인 양쪽성 화합물입니다. 이들은 산과 염기성에 모두 반응을 하여 중화반응을 합니다. 중화반응은 산과 염기가 만나서 염(흰가루)과 물을 만드는 반응인데, 결국 중성화시키는 과정입니다. 따라서 양쪽성화합물들은 산성과 염기성이 약합니다.
양쪽성이온은 단지 양쪽성화합물(amphoteric compound)과는 비슷하지만 약간 다릅니다. 양쪽성화합물은 외부적인 요인에 의해 음이온(anion)과 양이온(cation)이 결정된 것이지만(즉, 결합에 의해), 양쪽성이온은 좀더 자발적으로 음이온과 양이온을 외부 영향없이 같은 분자에서 가질 수 있습니다. 물론 양쪽성이온이 양쪽성화합물을 만들어 냅니다.
금속산화물은 대부분 염기성산화물이고, 비금속산화물은 대부분 산성산화물인데 양쪽성산화물은 각각 따로 반응합니다. 산화물은 비활성기체를 제외한 원소들이 산소와 결합된 화합물인데, 지구상에 산소와 물이 풍부하고 산소는 친화력도 강해 대부분의 원소들은 산화물을 형성합니다.
물은 대표적인 self-ionizable compounds이며 양쪽성화합물인데 아래처럼,
H2O + HCl → H3O+ + Cl− 물이 산성(HCl)을 만나 → 염기성처럼 행동합니다.
H2O + NH3 → NH4+ + OH− 물이 염기성(NH3)을 만나 → 산성처럼 행동합니다.
브뢴스테드-로우리의 정의에 의하면 수소이온(H+)을 받는쪽이 염기이고, 주는쪽이 산성입니다. (브뢴스테드-로우리의 산-염기는 상대적 개념이므로 어떤 물질은 염기가 있어야 산으로서 작용하며, 마찬가지로 산이 있어야 염기로 작용할 수 있습니다. 따라서 산성 물질은 양성자를 잃어 산의 짝염기인 염기를 만들고, 염기성 물질이 양성자를 얻으면 염기의 짝산인 산을 만듭니다. 앞의 내용과 반대인것 같지만 이것은 주는 쪽과 받는 쪽의 기준을 어디에 두냐에 따라 다릅니다.)
<참고문헌 : 브뢴스테드-로우리의 정의 - 위키백과>
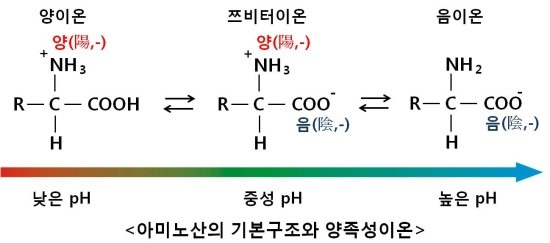
아미노산도 양쪽성화합물입니다. 아미노산이 양쪽성화합물이 될 수 있는 이유는 아미노산의 기본구조가 양성(+)의 아미노기(NH3)와 음성(-)의 카르복실기(COOH)로 구성되어 있기 때문입니다.
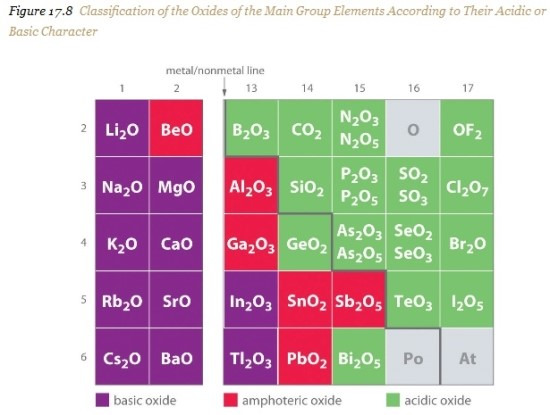
산화물(oxides)과 양쪽성산화물(amphoteric oxides)이 다른 점은 위의 그림과 같은 산소로 구성된 기본적인 산화물은 금속원소와 산소의 결합 또는 비금속원소와 산소의 결합을 통한 화합물인데 반해서 양쪽성화합물은 Al, Si, Sn, Pb, As, Zn 등과 같이 금속원소일수도 비금속원소일수도 있는 원소가 산소와 결합된 산화물인 경우가 대부분입니다. 빨간색이 양쪽성원소와 결합한 양쪽성산화물입니다.
ZnO는 산성(2H+)과 만나 전자(O)를 잃고 자신은 산성이 됩니다(주변을 염기성으로 만듬). 염기성(H2O 등)을 만나 전자(O)를 얻고 염기성이 됩니다. 물 역시 때에 따라서 산성이며 염기성인 양쪽성산화물입니다.
위와같은 물과 작용하는 양쪽성산화물이 아닌 이온에서도 양쪽성이온(물분자가 없음)이 가능합니다.
HSO4- 는 산성에서 수소이온을 받아들여 염기로 작용하였고, 염기에서 수소이온을 내보내 산으로 작용하였습니다.
양쪽성이온이든 양쪽성산화물이든 H+ 와 OH- 의 작용이 필요합니다. 그래야 양성자나 전자를 주거나 받거나 할 수 있습니다.
양쪽성산화물(화합물)이 아닌 금속산화물과 비금속산화물은 스스로 중성상태를 이룰 수 없어 산소(O) 또는 물(H2O)의 도움이 필요합니다. 산화물이 아닌 수소화물의 경우는 수소(H)가 그 역할을 합니다. 이것은 양쪽성이온과 양쪽성산화물도 마찬가지 입니다. 다만 금속산화물과 비금속산화물은 산성과 염기성이 이미 결정되어 있지만 양쪽성산화물은 그 자신이 음(陰,-)과 양(陽,+)을 모두 가지고 있으므로 두 가지 상태를 모두 경험할 수 있습니다.