Adenosine in the spinal cord and periphery(release and regulation of pain)
작성자문형철작성시간10.06.15조회수377 목록 댓글 0이 내용을 정확하게 이해해야 침에 의한 아데노신. 아데노신 수용체와 관련된 통증 억제를 알 수 있다.
![]() Adenosine_in_the_spinal_cord_and_periphery..pdf
Adenosine_in_the_spinal_cord_and_periphery..pdf
panic bird..
abstract
중추신경에서 아데노신은 중요한 neuromodulator이고 세포외액의 아데노신 A1, A2A, A2B, A3수용체의 작용에 의해 신경성, 비신경성 세포기능을 조절한다. 아데노신의 세포외액 농도는 아데노신의 재흡수, 분비, 대사, 합성에 의해 조절된다. 아데노신은 또한 척수와 말초신경에서 통증전달을 조절한다. 그리고 많은 요소들이 아데노신의 extracellular availability를 변경시킬 수 있고, 그 결과로 adenosin A1 receptor의 활성화에 의해 통증전달을 조절할 수 있다. 캡사이신의 사용으로 이러한 과정을 이해할 수 있다.
척수에서 아데노신의 이용성과 분비는
1) 탈분극에 의해서 증강. 탈분극은 K+, 캡사이신, 물질 P, NMDA에 의해 발생 - 염증반응
2) 아데노신의 대사와 재흡수의 억제에 의해서 증강됨(AK 억제제, AD, equilibrative transporter) - 아데노신 대사과정
3) receptor-operated mechanism(opioids, serotonin, noradrenaline)에 의해서 증강됨 - 호르몬에 의해
이들 물질중 일부는 세포내(k+, morphin) 아데노신 생성을 관장하는 equilibrative transporter에 영향을 받아 아데노신을 분비하는데, 다른 물질은 ecto-5'-nucleotidase(capsacin, 5HT)에 의해 세포외액에서 아데노신으로 변하는 nucleotide를 분비한다. 아데노신 분비는 capsaicin-sensitive할 수 있고, Ca(2+) 의존성일 수 있고, G-protein과 관련될 수 있는데, 이는 c-fiber내에서 ca(2+) 의존성 세포내 과정이 아데노신의 분비와 생산을 조절한다는 의미이다.
말단에서 아데노신은 신경성(neuronal)과 비신경성(non-neuronal) 인자로부터 분비된다. capsacin-sensitive afferents로부터 분비되는 신경성 분비는 글루타메이트, 신경인성 염증(캡사이신, 저농도의 formalin)에 의해서 유도되는데, 교감신경후신경 뉴런에 의해 보통 염증반응보다 더 염증 발생유도한다. 이러한 분비는 AK억제와 AD에 의해서 조절된다.
그런데 신경이 손상되면, capsaicin-sensitive adenosine 분비기전이 변경된다. 즉 아데노신의 척수분비가 opioid에 덜 반응하고, 반면 말단분비는 대사억제에 덜 반응한다.
염증이 있을때는 다양한 세포로부터의 아데노신이 분비된다. 예를 들어 endothelial cell, neutrophils, mast cells, fibroblast등의 세포에서
ATP는 척수와 말단에서 염증과 신경손상시에 모두 분비되어, ecto-5-nucleotidase가 아데노신으로 변화한다.
척수와 말단부에서 아데노신의 분비는 통증전달의 억제역할을 한다. 척수에서 아데노신의 세포외 농도 증가를 유도하는 morphine, 5-HT, substance p, AK 억제제에 의해서 통증전달을 억제한다. 말단에서는 AK 억제제와 AD 억제제에 의해서..
세포외 아데노신 이용성의 증가는 또한 methotrexate, sulfasalazine, salicylate, AK inhibitor에 의해 항염증반응에 기여하는 역할을 한다. 이러한 항염증 효과때문에 2차적으로 만성염증에서 통증전달을 억제한다.
이 논문의 목적은 척수와 말단에서 아데노신의 세포외 이용성을 조절하는 인자에 대하여 review하고, 아데노신이 통증전달을 어떻게 억제하는지를 알아보고자 한다.
1. 도입
중추신경계내에서 아데노신은 중요한 신경전달물질로 새롭게 인식되고 있다. 각성, 수면, 흥분, 인지, 기억 등의 조절과 관련하여.
trauma, ischemia, seizure 등의 병리적 상황에서 아데노신은 뉴론에 작용하여 중요한 neuroprotective 역할을 하고, 뇌척수액의 조절, 중풍, 뇌출혈, 간질 등의 상황에서 central inflammatory cell의 활성을 억제한다. 아데노신은 중추신경계내에서 내인성 물질로 이러한 내인성 level은 아데노신의 생성, 대사, 이동과 관련이 있다. 아데노신이 세포외 공간으로 분비되면 아데노신은 기능을 발휘하는데, 아데노신 A1, A2a, A2b, A3 수용체의 활성과 관련이 있다.
아데노신 A1 수용체는 뉴론에서 inhibitory neuromodulation and neuroprotection과 관련이 있다.
아데노신 A2a 수용체는 뉴론에서 excitatory action을 하고, brain injury를 악화시킬 수 있다. 면역 세포가 보호역할을 할 수 있지만
아데노신 A2b 수용체는 glial function을 조절하여 central inflammatory process를 발현한다.
아데노신 A3 수용체는 보호와 손상효과를 동시에 가지고 있다.
중추신경계내에서 아데노신의 세포외액 이용성은 다음과 같은 것에 의해서 증가한다.
1) neuronal excitation such as synaptic stimulation, seizures or depolarization (K+, veratridine, electrical stimulation)
2) reduced oxygen availability (hypoxia, anoxia, global and focal ischemia)
3) inhibition of metabolism by adenosine kinase (AK) and adenosine deaminase (AD)
4) receptor-operated mechanisms (e.g. ionotropic and metabotropic glutamate (GLU) receptors, opioid receptors)
추가로 아데노신은 spinal, supraspinal, peripheral site에서 통증전달을 조절하는 역할을 한다. 염증성 통증, 신경병증성 통증 둘다
첫번째 단계에서 통증전달은 c-fiber 신경에 존재하는 수용체의 활성을 조절하여 통증 전달을 조절. 또한 말단에서 항염증 세포에 작용하여 통증 조절하고 중추신경계의 glia 에서 아데노신 A2a, A2b, A3 수용체에 작용하여 간접적으로 통증을 조절
endogenous 아데노신은 척수와 말단조직에서 분비될 수 있다. 그리고 다양한 인자에 의해서 그러한 분비가 조절됨. 그리하여 뉴런의 아데노신 A1 수용체 활성화를 통해 통증 전달을 변경시킬 수 있다.
2. sensory afferent neurons and pain signalling
2.1 sensory afferent의 활성과 분류
- 조직이 손상돼 염증이 발생하면 염증물질이 분비되는데, 이 물질을 살펴보면 protons, adenosin5-triphosphate(ATP), 브라디키닌, 세로토닌, 히스타민, 프로스타글란딘, 물질 P, 아데노신 등이다. 이러한 물질중에서 H+, ATP, 5-HT3은 ligand gated cation channel에 작용하여 기능을 하고, 다른 물질들(프로스타글란딘, 브라디키닌, 5-HT1/2은 G-protein-coupled receptors(GPCRs)에 작용하여 기능을 함.
- 유해자극 구심성 뉴런의 흥분성의 변화는 sensory neuron specific Na+ channel의 인산화와 연관된 intracellular protein kinase의 활성화때문.
- 유해자극의 구심성 전달은 두가지(neuropeptide와 receptor)로 분류됨. 하나는 물질 p, CGRP(calcitonin gene-related peptide), tyrosine kinase A receptor를 발현하여 nerve growth factor(NGF)에 반응하여 구심성전달을 하고, 다른 하나는 isolectin B4 binding site와 P2X3 수용체를 발현하여 glial-derived neurotrophic factor에 반응하여 라미나 2에 종지하여 구심성 전달.
- 이 두가지는 vanilloid receptor(VR-1)을 express하고 캡사이신에 sensitive함.
=> 찾아라.. 몰라.. VR-1????
2.2 신경손상에 따른 sensory afferents의 변화
신경이 손상되면 유해하지 않은 자극이 증폭되어 유해자극으로 전달되어, 자발적 방전(spontaneous discharge), 이소성 활성화(etopic activity)이 발생하고, 교감신경 활성화에 의해 비정상적으로 조절됨.
Aβ섬유 자극은 척수의 심부(lamina III-V)에 innervate하는데, 염증은 Aβ섬유의 표현형을 바꿔 물질 P는 Aβ섬유에 영향을 주고 염증반응을 악화시키는 역할을 함. 그리하여 Aβ섬유는 VR-1 수용체에 반응하여 통증이 악화됨.
게다가 Aβ섬유는 척수의 천층부에 sprout함.
Aβ섬유의 표현형 변화와 Aβ섬유의 종지변화는 만지는 자극을 통증으로 느끼게 하는데 이를 이질통(allodynia)라고 함.
2.3 척수에서의 중추감작
- c 섬유자극전달과정에서 척수내에서 흥분성 아미노산, 물질 P, neurokinin(NK) A, CGRP의 분비는 통증의 central signalling에 중요한 역할.
- intensive or persistant 유해자극은 흥분성 신경전달물질의 분비를 증강, 연장시켜 시냅스 후 전달의 누적적인 탈분극을 야기함. 그리고 이것은 NMDA-gated channel의 활성화와 Mg2+ block제거를 유도함.
- NMDA 수용체의 활성화는 Ca2+ 유입을 유도하여 세포내액의 ca2+ 수준을 높여 cascade of change를 활성화시킴. 막수용체와 이온채널의 인산화를 야기하여 척수에서 흥분성 전달을 증가시키는 multiple protein kinase의 활성화를 포함하여....
- 새포내 ca2+ 증가는 전사(transcriptional)와 전환(translational)경로를 활성화하고, 새로운 단백질, 새로운 수용체를 만들어 내어 long-term plastic change를 유도함. 이렇게 말초와 중추감작이 되면 비정상적인 sympathetic/sensory coupling과 intrinsic and descending inhibition 기능이 감소하여 만성통증이 됨.
2.4 neurogenic inflammation in peripheral tissue
- c fiber sensory neuron이 활성화 되면 antidromic 자극에 의해 efferent기능이 유도되어 말단조직에 부종, 혈관확장같은 신경인성 염증이 발생
- sensory neuron의 말단에서 물질 p, CGRP같은 물질이 분비되고, 이러한 물질들은 extravasation과 vasodilation을 야기하여 염증물질인 히스타민, 프로스타노이드, 사이토카인 등을 비만세포, leukocyte에서 분비함. 이러한 신경펩티드의 분비는 구심성자극을 직접 활성화하여 ..
2.5. sensory afferent neuron을 특징짓는 도구로서 캡사이신
- 캡사이신은 VR-1수용체를 활성화 할 수 있는 물질로 C-fiber(some Aδ)를 선택적으로 express. 이 수용체는 ligand-gated cation channel로서 heat, proton, lipid medictor에 의해 활성화.
- VR-1 수용체의 활성화는 entry of cations(Na+, Ca+)을 야기하여 탈분극을 일으켜 afferent 자극을 전달.
- 동물실험에서 캡사이신에 노출되면 유해성 구심성 활성화가 야기됨
- ca2+ influx가 유해성 뉴런에 들어가면 이들 뉴런에서 신경펩타이드를 분비함. 세포실험에서 캡사이신에 노출되면 온도, 기계적 자극에 유해성 구심성 역치가 감소하여 유해성 구심성에 민감해지고, 통증에 민감해짐.
- VR-1 수용체 활성화는 유해자극 구심성의 원심성기능을 유발하여 말초의 혈관확장과 조직부종을 야기함.
- 캡사이신에 급성적으로 노출되면 기능적 탈감작을 일으켜 화학적, 열, 압박 등의 자극에 반응성이 줄어듬.
- Ca2+ dependent phosphatase calcineurin은 이러한 탈감작에 관여함.
- 게다가 탈감작은 ....
- 동물, 세포실험에서 캡사이신의 사용은 유해성 뉴런의 역할을 조사하기 위해 중요한 수단.
- 캡사이신은 척수와 말초부분으로부터 아데노신 분비를 특징짓는 중요한 역할. 내인성 아데노신이 척수와 말초에서 통증전달에 중요한 역할을 하는데 통찰력을 제공.
3. 아데노신의 formation, metabolism, transport
3.1 아데노신에 대한 일반론
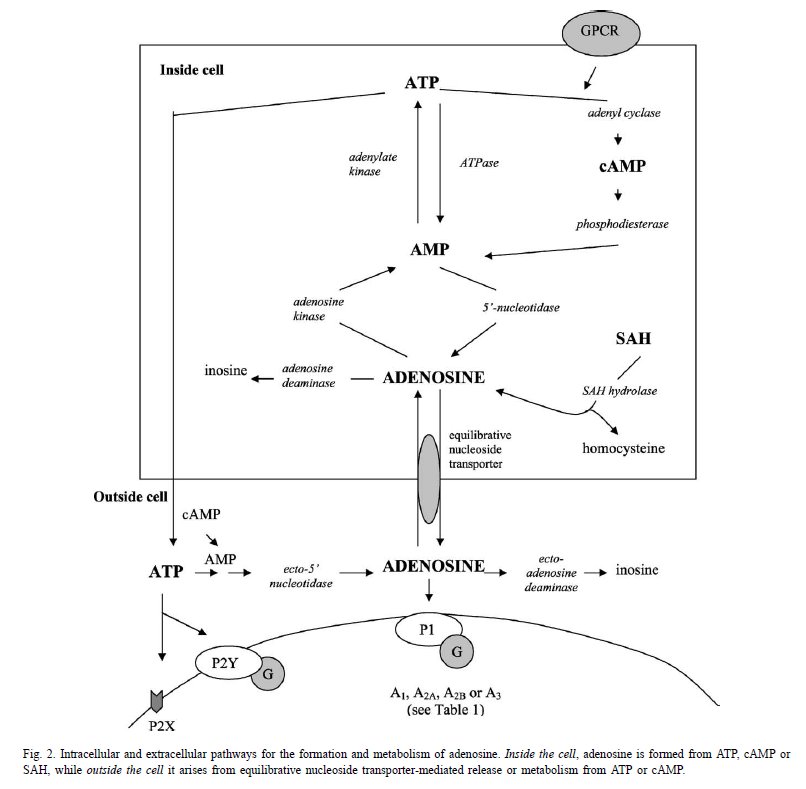
- 중추신경에서 아데노신의 생성과 분비에 관여하는 요소는 최근에 분석되고 있음. 세포내에서 아데노신은 ATP로부터 만들어지고 세포외에서 대사.. 그림 참조
- 세포내에서 ATP의 농도는 아데노신 5-monophosphate의 농도보다 50배 높고, ATP농도의 small variation은 AMP의 높은 증가를 야기. 두가지 세포내 5-NUCLEOTIDASE 효소는 cloned되고, ..대사..
3.2 아데노신 transport
- 아데노신이 한번 세포외로 빠져 나오면, 특이한 nucleoside transporter 물질에 의해 세포벽을 가로질저 재흡수되어 제거됨
- ENTs와 CNTs 두가지 형태의 nucleoside transporter가 있는데, ENTs(equilibrative nucleoside transporter)는 농도 기울기차에 따라서 직접 세포벽을 가로질러 이동하고, CNTs(concentrative nucleoside transporter)는 transmembrane Na+ 기울기와 농도기울기에 따라 necleoside의 유입을 매개하여 이동.
- ENT의 두가지 형태가 일어나면 ENT 1은 NBMPR의 저농도에도 민감하고, ENT2는 NBMPR의 억제에 덜 민감함. 두가지 이동은 dipyridamole에 의해 억제됨.
- 최신의 교잡(hylbridization)연구에 의하면 ENT1, 2 모두 중추신경계에서 나타나고, ENT2는 쥐의 뇌에서 우월하게 작용.
- CNT는 5가지가 있는데 ENT처럼 특징을 나누기 힘듬.
3.3 아데노신 대사
- 세포네 아데노신은 AK에 의해 AMP로 인산화되고, AD에 의해 이노신으로 deaminate됨.
- AK는 cytosolic enzyme으로 뇌에 많이 분포되어 있고, cytosolic과 뇌와 척수의 특정부위 세포외 enzyme에 널리 분포됨.
- 세포내에서 AD는 대사기능을 나타내는데, 세포외에서는 extra-enzymatic effect를 나타냄. 이는 아데노신 A1 수용체에 ligand binding의 조절과 관련되고, ,또한 endocytosis)세포막의 함입에 의한 외부 물질흡수작용)와 수요체 활성화의 조절과 관련됨.
- 중추신경에서 AK억제는 basal and evoked 아데노신 분비를 증강시킴. 하지만 AD의 억제는 좀더 다양한 효과를 생성함.
- AK와 AD 억제의 서로 다른 효과는 다양한 실험적 조건에서 아데노신의 다양한 기능을 반영함.
4. 척수에서 아데노신 분비
4.1 아데노신의 spinal analgesia
- 아데노신에 의한 척수에서의 통증조절은 1984년 Post의 연구에 의해서 시작됨. 그는 5-N-ethylcarboxamidoadenosine(NECA)가 척수에서 analgesia효과가 나타냄을 증명. 이는 methylxantine adenosin 수용체 antagonist에 의해 block됨을 증명.
- 당시 많은 연구는 아데노신의 척수작용이 anagesia를 유발한다는 것.
- 흥미롭게, 아데노신 analog(유사물)는 신경손상의 조건에서 특별한 효과를 나타내는데, 이는 말초신경의 구심성기능을 변경시키기 때문이고, 중추감작을 recruit하기 때문. 이러한 활성화를 매개하는 기전은 잘 알려지지 않았지만 척수감작에 중요한 역할을 함. 게다가 neuroprotective effect를 하고 .....
- 설치류에서 아데노신의 척수투여는 그 자체로 weak analgesic effect를 생성. 왜냐하면 uptake and metabolic degradation때문 .
- neuropathic pain모델에서 아데노신은 long-lasting analgesia를 유발.
- 사람에게서 아데노신의 척수투여도 통증감작에 의한 만성통증에 analgesic 효과가 있음. 아데노신에 의한 spinal analgesia는 아데노신 A1 수용체와 관련. 다양한 방식으로 증명됨.
- 아데노신 A1 수용체의 Immunohistochemistry 연구에 의하면 척수의 라미나 2층의 cell body에 강한 염색효과.
- 척수에서 아데노신 A1수용체의 활성화는 hyperpolirization과 K+ channel의 활성화에 기인하여 postsynaptic inhibition of excitatory transmission을 야기하여 통증 완화. dorsal root를 잘라내면 아데노신 수용체의 유해자극 구심성 효과는 보이지 않을지라도 trigeninal ganglion neuron에서는 확인됨. 다양한 연구에 의하여 확인..
- 최근에는 아데노신 A2,3 수용체는 척수에서 통증조절 증거가 부족하다는 것이 밝혀지고 있음.
4.2 아데노신 분비의 방법
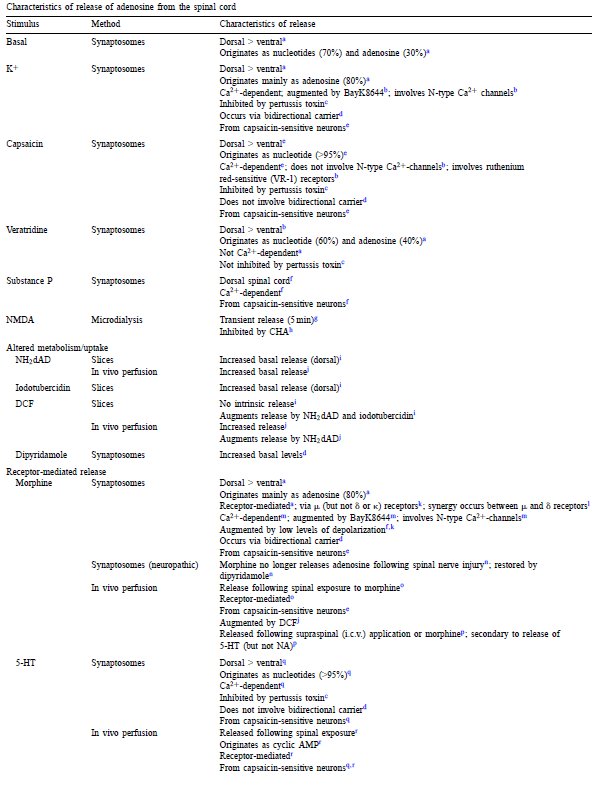
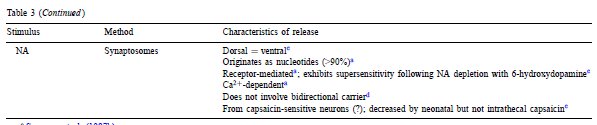
- 통증을 조절하기 위해서 척수에서 아데노신의 분비가 중요한데, 여러가지 실험적인 상황에서 분비. 아래 표로 정리됨.
4.3. 탈분극에 의한 아데노신 분비
- 척수에서 신경으로부터 다양한 형태의 탈분극은 아데노신을 분비하게 함.
- 증가된 K+ 농도는 dorsal spinal cord synaptosomes로부터 아데노신을 분비하게 하는데 이는 Ca2+의존성이고, N-type Ca2+ channels가 관여하고 capsaicin-sensitive neuron으로부터 시작됨.
- 이러한 분비는 ENTs에 의존적이고...
- 캡사이신은 아데노신을 nucleotide형태로 분비하고 이는 세포외에서 아데노신으로 바뀜.
- capsaicin-induced release는 또한 ca2+ 의존적이고, N-type ca2+ channel과는 관여없이, 하지만 VR-1 수용체를 통하여 Ca2+ 유입을 반영함. 이러한 분비는 분명하게 capsicin-sensitive neuron으로부터 originate함.
- 아데노신과 탈분극으로 유도된 nuclotide분비는 pertussis(파상풍) toxin에 senstive하고,