Open AccessReview
Contributions of Gamma-Aminobutyric Acid (GABA) Produced by Lactic Acid Bacteria on Food Quality and Human Health: Current Applications and Future Prospects
by
Mehmet Arif Icer
1,*,
Buse Sarikaya
1,
Emine Kocyigit
2

,
Büşra Atabilen
3

,
Menşure Nur Çelik
4,
Raffaele Capasso
5

,
Duygu Ağagündüz
6

and
Ferenc Budán
7,*

1
Department of Nutrition and Dietetics, Faculty of Health Sciences, Amasya University, Amasya 05100, Turkey
2
Department of Nutrition and Dietetics, Faculty of Health Sciences, Ordu University, Ordu 52000, Turkey
3
Department of Nutrition and Dietetics, Faculty of Health Sciences, Karamanoğlu Mehmetbey University, Karaman 70100, Turkey
4
Department of Nutrition and Dietetics, Faculty of Health Sciences, Ondokuz Mayıs University, Samsun 55000, Turkey
5
Department of Agricultural Sciences, University of Naples Federico II, 80055 Portici, Italy
6
Department of Nutrition and Dietetics, Faculty of Health Sciences, Gazi University, Emek, Ankara 06490, Turkey
7
Institute of Physiology, Medical School, University of Pécs, H-7624 Pécs, Hungary
*
Authors to whom correspondence should be addressed.
Foods 2024, 13(15), 2437; https://doi.org/10.3390/foods13152437
Submission received: 10 June 2024 / Revised: 20 July 2024 / Accepted: 29 July 2024 / Published: 1 August 2024
(This article belongs to the Special Issue Lactobacillus as a Biotechnological Tool to Improve Food Quality and Human Health)
Downloadkeyboard_arrow_down
Abstract
The need to increase food safety and improve human health has led to a worldwide increase in interest in gamma-aminobutyric acid (GABA), produced by lactic acid bacteria (LABs). GABA, produced from glutamic acid in a reaction catalyzed by glutamate decarboxylase (GAD), is a four-carbon, non-protein amino acid that is increasingly used in the food industry to improve the safety/quality of foods. In addition to the possible positive effects of GABA, called a postbiotic, on neuroprotection, improving sleep quality, alleviating depression and relieving pain, the various health benefits of GABA-enriched foods such as antidiabetic, antihypertension, and anti-inflammatory effects are also being investigated. For all these reasons, it is not surprising that efforts to identify LAB strains with a high GABA productivity and to increase GABA production from LABs through genetic engineering to increase GABA yield are accelerating. However, GABA’s contributions to food safety/quality and human health have not yet been fully discussed in the literature. Therefore, this current review highlights the synthesis and food applications of GABA produced from LABs, discusses its health benefits such as, for example, alleviating drug withdrawal syndromes and regulating obesity and overeating. Still, other potential food and drug interactions (among others) remain unanswered questions to be elucidated in the future. Hence, this review paves the way toward further studies.
초록
식품 안전성 향상과 인간 건강 개선의 필요성은
유산균(LABs)에 의해 생성되는
감마-아미노부티르산(GABA)에 대한 전 세계적인 관심을 증가시켰습니다.
GABA는 글루타메이트 디카르복실라제(GAD)에 의해 촉매되는 반응을 통해
글루타메이트에서 생성되는 4탄소 비단백질 아미노산으로,
식품 산업에서 식품의 안전성/품질 개선을 위해 점점 더 널리 사용되고 있습니다.
GABA의 포스트바이오틱스로 알려진
신경 보호 효과, 수면 품질 개선, 우울증 완화, 통증 완화 등 잠재적 긍정적 효과 외에도,
GABA 함유 식품의 다양한 건강 혜택(항당뇨, 항고혈압, 항염증 효과 등)이 연구되고 있습니다.
이러한 모든 이유로,
LAB에서 GABA 생산성을 높이는 LAB 균주 식별 및 유전자 공학을 통해
LAB로부터 GABA 생산량을 증가시켜
GABA 수율을 높이는 노력들이 가속화되고 있습니다.
그러나
GABA가 식품 안전성/품질 및 인간 건강에 미치는 기여는
문헌에서 아직 충분히 논의되지 않았습니다.
따라서
본 리뷰는 LAB에서 생산된 GABA의 합성 및 식품 응용을 강조하며,
약물 금단 증상 완화, 비만 및 과식 조절 등 건강 혜택에 대해 논의합니다.
그럼에도 불구하고
식품 및 약물 상호작용 등 다른 잠재적 문제는 미래에 밝혀져야 할 미해결 과제입니다.
따라서 본 리뷰는 추가 연구의 길을 열기 위해 기여합니다.
Keywords:
lactic acid bacteria; gamma-aminobutyric acid; food quality; human health
1. Introduction
Humans need safe and nutritious food in their life. However, challenges like population growth, urbanization, climate change, and conflicts affect food safety and security, leading to significant food loss. The short shelf life foods adds to this problem [1]. The spoilage process makes food unsuitable for consumption. About one-third of the world’s food is lost due to spoilage or waste, leading to significant environmental and economic consequences [2]. Unwanted microorganisms can contaminate food throughout the production and supply chains (the production, processing, distribution, or preparation stages) [3]. Strategies to control spoilage-causing microorganisms and foodborne pathogens in food products involve managing intrinsic factors such as pH, water activity, NaCl content, and nutrient components, as well as extrinsic factors, including temperature, relative humidity, and the preservation methods required for microbial growth in the food product. Chemical compounds—synthetic and natural—and antimicrobials of biological origin can be utilized to manage pathogens and extend the shelf life of food products [4,5]. Lactic acid bacteria (LABs), their metabolites, or both, are often used to prevent the growth of undesirable microorganisms and improve food safety and quality [3]. LABs are a group of bacteria generally recognized as safe (GRAS), functioning as natural bio-protectants and health promoters [3,6]. They are known for their role in fermenting food and are being explored as a way to preserve food naturally [7,8]. They produce antimicrobial substances that can help prevent spoilage and the growth of foodborne pathogens [9,10]. Most LAB species including Levilactobacillus brevis, Lacticaseibacillus paracasei, Lactiplantibacillus plantarum, and Lactococcus lactis produce γ-amino butyric acid (GABA) via α-decarboxylation of glutamate by the enzymatic reaction of glutamate decarboxylase (GAD) [11,12], a pyridoxal 5′-phosphate (PLP-dependent enzyme) [11]. The demand for GABA production suitable for food applications has risen with its commercial utilization [13]. Although GABA is widely present in plants, animals, and microorganisms, its concentrations in plants are generally low [14]. Microorganisms serve as a significant source of GABA, with many microorganisms, including yeast, fungi, and bacteria, demonstrating the capacity to synthesize GABA [15,16]. It has been reported that Lactococci can synthesize significant amounts of GABA, but the highest-performing GABA producers have been reported among Lactobacilli, specifically Levilactobacillus brevis, Lactobacillus delbreuckii subsp. bulgaricus, Lentilactobacillus buchneri, Limosilacobacillus fermentum, Lactobacillus helveticus, Lacticaseibacillus paracasei, and Lactiplantibacillus plantarum [17]. Microbial fermentation is an effective process for GABA accumulation. LABs, in particular, are one of the most essential GABA producers due to their food-available and high GAD activity for GABA production [18].
1. 소개
인간은 삶에서 안전하고 영양가 있는 식품이 필요합니다. 그러나 인구 증가, 도시화, 기후 변화, 분쟁 등 다양한 도전 과제가 식품 안전과 안보를 위협하며 심각한 식품 손실을 초래합니다. 짧은 유통기한을 가진 식품은 이 문제를 더욱 악화시킵니다 [1]. 부패 과정은 식품을 섭취에 부적합하게 만듭니다. 세계 식품의 약 1/3이 부패나 폐기로 인해 손실되며, 이는 심각한 환경적 및 경제적 영향을 초래합니다 [2]. 원치 않는 미생물은 생산 및 공급망(생산, 가공, 유통, 또는 준비 단계) 전반에 걸쳐 식품을 오염시킬 수 있습니다 [3]. 식품 제품에서 부패를 유발하는 미생물과 식품borne 병원체를 통제하기 위한 전략은 pH, 수분 활동, NaCl 함량, 영양 성분과 같은 내인적 요인과 온도, 상대 습도, 식품 제품 내 미생물 성장에 필요한 보존 방법과 같은 외인적 요인을 관리하는 것을 포함합니다. 합성 및 천연 화합물과 생물학적 기원 항균제는 병원체를 관리하고 식품 제품의 유통기한을 연장하기 위해 활용될 수 있습니다 [4,5].
젖산균(LABs),
그 대사산물, 또는 둘 다는 유해 미생물의 성장을 방지하고
식품 안전성과 품질을 개선하기 위해 자주 사용됩니다 [3].
LABs는 일반적으로 안전하다고 인정된 미생물(GRAS)로,
자연적인 생물학적 보호제 및 건강 증진제로 기능합니다 [3,6].
이들은 식품 발효에 역할을 하며 자연적인 식품 보존 방법으로 탐구되고 있습니다 [7,8].
그들은 식품 부패와 식품borne 병원균의 성장을 방지하는 데 도움이 되는 항균 물질을 생산합니다 [9,10].
대부분의 LAB 종,
예를 들어
Levilactobacillus brevis,
Lacticaseibacillus paracasei,
Lactiplantibacillus plantarum, 및
Lactococcus lactis는
글루타메이트 디카르복실라제(GAD)의 효소 반응을 통해
글루타메이트의 α-디카르복실화 반응으로 γ-아미노 부티르산(GABA)을 생성합니다[11,12],
이는 피리독살 5′-인산(PLP 의존성 효소)에 의존합니다[11].
식품 응용에 적합한 GABA 생산에 대한 수요는
상업적 활용과 함께 증가했습니다 [13].
GABA는
식물, 동물, 미생물에서 널리 존재하지만,
식물에서의 농도는 일반적으로 낮습니다 [14].
미생물은 GABA의 중요한 원천으로,
효모, 곰팡이, 세균 등 많은 미생물이 GABA 합성 능력을 보여줍니다 [15,16].
Lactococci가 상당량의 GABA를 합성할 수 있다는 보고가 있지만,
가장 높은 생산량을 보이는 GABA 생산균은
Lactobacilli 속, 특히 Levilactobacillus brevis, Lactobacillus delbreuckii subsp. bulgaricus, Lentilactobacillus buchneri, Limosilacobacillus fermentum, Lactobacillus helveticus, Lacticaseibacillus paracasei, 및 Lactiplantibacillus plantarum [17]에서 보고되었습니다.
미생물 발효는
GABA 축적에 효과적인 과정입니다.
특히 LAB는 식품에 존재하는 GAD 활성이 높아
GABA 생산에 필수적인 미생물 중 하나입니다 [18].
With LABs being widely accepted as GRAS and having a high potential for application in the fermentation industry, GABA-producing LABs in the food industry have attracted great interest in recent years. Many GABA-producing LABs have been isolated from fermented foods and are used to produce natural health-oriented foods enriched with GABA [18].
The widespread use of GABA is attributed to the gradual elucidation of its physiological functions. GABA and its receptors have also been found in the peripheral nervous system, the endocrine system, and other non-neural organs, which are involved in oxidative metabolism [19]. The mechanism of GABA’s action on various diseases is mainly suggested by its presence in the central nervous system and the nerves around various organs, thus regulating human functions through nerve signal transmission and various receptors [20]. It is a potent pain reliever, beneficial for cardiovascular function, and treatment of various neurological diseases, including Parkinson’s disease, Huntington’s chorea, and Alzheimer’s disease [19,21]. GABA exhibits significant health benefits, including anti-hypertensive, anti-diabetic, and anti-inflammatory properties. Moreover, its potential anticancer effects, by stimulating cancer cell death and inhibiting growth, offer hope for its future applications in cancer treatment [13,22].
LAB가 GRAS로 널리 인정받고 발효 산업에서의 높은 적용 가능성을 갖추면서,
식품 산업에서 GABA를 생산하는 LAB에 대한 관심이 최근 급증하고 있습니다.
발효 식품에서 많은 GABA 생산 LABs가 분리되어
GABA가 풍부한 자연 건강 식품 생산에 활용되고 있습니다 [18].
GABA의 광범위한 사용은
그 생리적 기능의 점진적인 규명에 기인합니다.
GABA와 그 수용체는
산화 대사 과정에 관여하는 말초 신경계, 내분비계, 기타 비신경 기관에서도 발견되었습니다 [19].
GABA의 다양한 질병에 대한 작용 메커니즘은
주로 중추 신경계와 다양한 장기 주변 신경에 존재하여
신경 신호 전달과 다양한 수용체를 통해 인간 기능을 조절한다는 점에서 제안되고 있습니다 [20].
GABA는
강력한 진통제이며, 심혈관 기능 개선에 유익하며,
파킨슨병, 헌팅턴 병, 알츠하이머 병 등 다양한 신경 질환의 치료에 유용합니다 [19,21].
GABA는
항고혈압, 항당뇨, 항염증 효과를 포함해 다양한 건강 혜택을 제공합니다.
또한 암 세포 사멸을 자극하고 성장 억제를 통해
암 치료에 대한 잠재적 항암 효과를 보여주어
미래 암 치료 분야에서의 적용 가능성을 제시합니다 [13,22].
From the point of view of market consumption, GABA-rich foods are becoming increasingly popular due to the various physiological activities of GABA [23]. Currently, GABA-enriched foods include mostly grain-based staple foods, beverages, dairy products, and some snacks. The health claims of these GABA-rich products are mostly associated with relieving insomnia or improving sleep, lowering blood pressure, and relieving stress [24]. GABA impacts cognitive functions such as cognition, emotion, and memory and controls central nervous system activity. Therefore, it is necessary to draw attention to how important GABA function is in regulating neuronal activity and maintaining a healthy and functional neurological system [19]. It has also been reported that GABA-enriched foods have other health benefits, such as relieving stress and fatigue, hepatoprotective effects, and protection against cisplatin-induced nephrotoxicity [24].
This review aims to detail the process of obtaining GABA from LABs, the factors affecting this process, the use of GABA in the food sector, and its possible health benefits in light of the current literature. Given the significant role of GABA in the food sector and the growing body of evidence supporting its beneficial effects on health, this review will provide a comprehensive understanding of the process.
시장 소비 측면에서 GABA가 풍부한 식품은
GABA의 다양한 생리적 활동으로 인해 점점 더 인기를 얻고 있습니다 [23].
현재 GABA 강화 식품은
주로 곡물 기반 주곡 식품, 음료, 유제품, 일부 간식류로 구성되어 있습니다.
이 GABA 풍부한 제품의 건강 주장은
주로 불면증 완화 또는 수면 개선, 혈압 감소, 스트레스 완화와 연관되어 있습니다 [24].
GABA는
인지, 감정, 기억과 같은 인지 기능에 영향을 미치고
중추 신경계 활동을 조절합니다.
따라서
신경 활동 조절과 건강한 신경계 유지에 GABA 기능의 중요성에 주목할 필요가 있습니다 [19].
또한 GABA 강화 식품은
스트레스와 피로 완화, 간 보호 효과, 시스플라틴 유발 신장 독성 보호 등 다른 건강 혜택이 보고되었습니다 [24].
이 리뷰는 현재 문헌을 바탕으로 LAB에서 GABA를 추출하는 과정,
이 과정에 영향을 미치는 요인, 식품 산업에서의 GABA 활용,
그리고 건강에 대한 잠재적 이점을 상세히 설명하는 것을 목표로 합니다.
GABA가 식품 산업에서 차지하는 중요한 역할과 건강에 대한 유익한 효과를 지원하는 증거가 증가함에 따라,
이 리뷰는 해당 과정에 대한 포괄적인 이해를 제공할 것입니다.
2. Biosynthesis of GABA by LABs
GABA is a non-protein amino acid produced mainly by plants, animals, and microorganisms [25] and has different functions depending on the producing organism [26]. Several LAB strains producing GABA have been isolated from traditional fermented foods such as cheese, kimchi, paocai, yogurt, and fermented soya beans [18]. In a recent systematic review, GABA-producing Lactobacillus species were compiled as Levilactobacillus brevis, Lentilactobacillus buchneri, Lactobacillus delbreuckii subsp. bulgaricus, Limosilactobacillus fermentum, Lactobacillus helveticus, Lacticaseibacillus paracasei, Lactiplantibacillus plantarum, Lactococcus lactis, etc. [18]. The GABA production capacity of different species is highly variable. Levilactobacillus brevis is able to produce higher amounts of GABA compared to other LAB species [27]. At the same time, various strains of a species also have marked differences in GABA productivity [27,28,29,30].
Some microorganisms use Putrescine (Puu) or GAD pathways for GABA biosynthesis [31]. The Puu pathway is a route used by some microorganisms (Escherichia coli [32] and Aspergillus oryzae, a fungus [33]) to obtain GABA [34,35]. In another pathway, the GAD pathway, GABA can be synthesized by a wide variety of microorganisms, including Lactobacillus spp. [36], Escherichia coli [37], Listeria monocytogenes [38], and Aspergillus oryzae [39]. Since this review focuses on GABA synthesis by LABs, the GAD pathway is detailed. The first step of the GAD pathway is carried out by an L-Glutamate (Glu)/GABA antiporter encoded by a gadC gene [40]. This antiporter pumps the precursor Glu or its monosodium glutamate (MSG) into the microorganism [41]. Subsequently, a PLP-dependent GAD enzyme catalyzes the conversion of the precursor to GABA, which is then transferred to the extracellular matrix by the action of the Glu/GABA antiporter [42,43]. L-glutamate precursor, a-ketoglutarate, is synthesized from glucose via the glycolysis pathway and part of the Krebs cycle and then converted to L-glutamate by L-glutamate dehydrogenase [18]. The GAD enzyme is encoded by a gadB gene that usually binds to PLP [37]. In most Lactobacillus strains (Lacticaseibacillus rhamnosus, Lactiplantibacillus plantarum, Lacticaseibacillus casei, and Latilactobacillus sakei), GAD is encoded by a gadB gene [44]. However, Levilactobacillus brevis also possesses a gadA, which presents a similar structure to the gadB gene. Although both genes play the same role in GAD expression, deletion of gadB is reported to be associated with a more pronounced decrease in GABA production than deletion of gadA [45]. The metabolic pathway GABA production is given in Figure 1.
2. LAB에 의한 GABA의 생합성
GABA는
주로 식물, 동물, 미생물에 의해 생성되는 비단백질 아미노산으로 [25],
생성하는 생물체에 따라 다양한 기능을 갖습니다 [26].
GABA is a non-protein amino acid produced mainly by
plants, animals, and microorganisms [25]
and has different functions depending on the producing organism
치즈, 김치, 파오차이, 요거트, 발효 콩 등
전통 발효 식품에서 GABA를 생성하는 여러 LAB 균주가 분리되었습니다 [18].
non-protein amino acid
GABA 외에도 다양한 비단백질 아미노산이 존재하며, 각각 독특한 기능을 수행합니다.
카르니틴은 지방산을 미토콘드리아로 운반하여 에너지 생성에 중요한 역할을 하며,
오르니틴은 요소 회로에서 암모니아를 제거하는 데 관여.
시트룰린은 혈관 확장 및 혈류 개선에 도움을 줄 수 있으며,
테아닌은 녹차에 풍부하며 신경 안정 및 집중력 향상에 기여할.
이러한 비단백질 아미노산들은 우리 몸에서 다양한 생리적 기능을 조절하며, 건강 유지에 필수적인 역할.
https://pmc.ncbi.nlm.nih.gov/articles/PMC7544725/

최근 체계적 검토에서
GABA를 생산하는 Lactobacillus 종은
Levilactobacillus brevis, Lentilactobacillus buchneri,
Lactobacillus delbreuckii subsp. bulgaricus, Limosilactobacillus fermentum,
Lactobacillus helveticus, Lacticaseibacillus paracasei, Lactiplantibacillus plantarum, Lactococcus lactis 등으로
분류되었습니다. [18].
다양한 종의 GABA 생산 능력은
매우 다양합니다.
Levilactobacillus brevis는
다른 LAB 종에 비해 더 많은 양의 GABA를 생산할 수 있습니다 [].
동시에, 같은 종의 다양한 균주도
GABA 생산량에 현저한 차이를 보입니다 [, , ].
일부 미생물은
GABA 생합성에 푸트레신(Puu) 또는 GAD 경로를 사용합니다 [31].
Puu 경로는
일부 미생물(Escherichia coli [32] 및 곰팡이 Aspergillus oryzae [33])이
GABA를 얻기 위해 사용하는 경로입니다 [34,35].
다른 경로인 GAD 경로를 통해 GABA는
Lactobacillus spp. [36], Escherichia coli [37], Listeria monocytogenes [38], 및 Aspergillus oryzae [39]를 포함한
다양한 미생물에 의해 합성될 수 있습니다.
이 리뷰는
LABs에 의한 GABA 합성에 초점을 맞추고 있으므로
GAD 경로가 상세히 설명됩니다.
GAD 경로의 첫 번째 단계는
gadC 유전자에 의해 암호화된 L-글루타메이트(Glu)/GABA 안티포터에 의해 수행됩니다 [40].
이 안티포터는
전구체 Glu 또는 그 모노소듐 글루타메이트(MSG)를 미생물 내로 펌핑합니다 [41].
이후 PLP 의존성 GAD 효소가 전구체를
GABA로 전환하며,
이는 Glu/GABA 안티포터의 작용으로 세포외 기질로 전달됩니다 [42,43].
L-글루타메이트 전구체인 α-케토글루타레이트는
글루코스에서 글리코시스 경로를 통해 일부 크렙스 회로를 거쳐 합성되며,
이후 L-글루타메이트 탈수소효소에 의해 L-글루타메이트로 전환됩니다 [18].
GAD 효소는
일반적으로 PLP에 결합하는 gadB 유전자에 의해암호화됩니다 [37].
대부분의 락토바실러스 균주(Lacticaseibacillus rhamnosus, Lactiplantibacillus plantarum, Lacticaseibacillus casei, 및 Latilactobacillus sakei)에서
GAD는 gadB 유전자에 의해암호화됩니다 [44].
그러나
Levilactobacillus brevis는
gadB 유전자와 유사한 구조를 가진 gadA 유전자를 추가로 보유하고 있습니다.
두 유전자는 GAD 발현에서 동일한 역할을 하지만,
gadB 유전자의 삭제는 gadA 유전자의 삭제보다
GABA 생산량의 감소가 더 두드러지게 나타난다는 보고가 있습니다 [45].
GABA 생산의 대사 경로는 그림 1에
제시되어 있습니다.
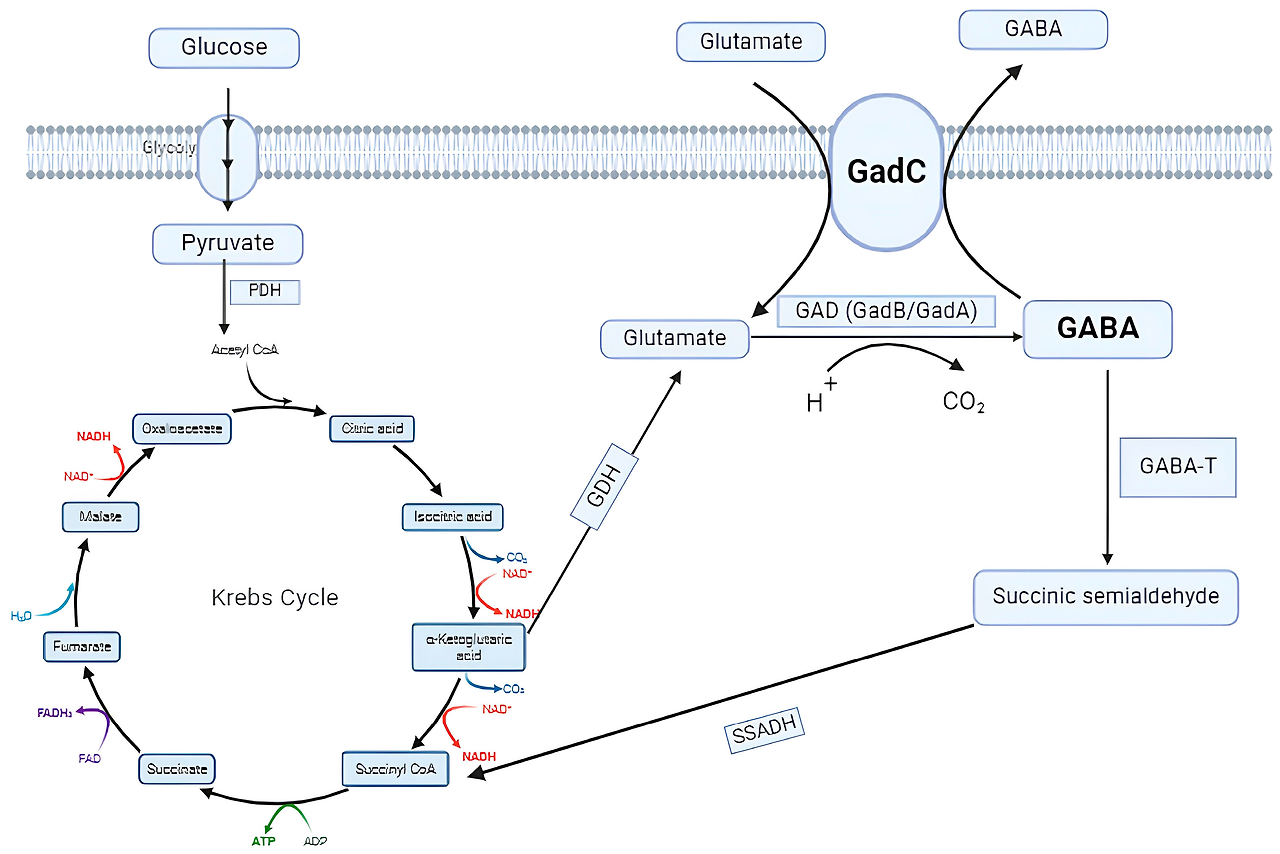
Figure 1. Metabolic pathway GABA production (Adapted from [18,46]). Abbreviations: PDH, pyruvate dehydrogenase; GDH, glutamate dehydrogenase; GAD, glutamate decarboxylase; GABA-T, GABA transaminase; SSADH, succinic semialdehyde dehydrogenase.
2.1. Factors Affecting GABA Synthesis
Lactobacillus has attracted significant interest due to its many GABA-producing strains (e.g., Lactiplantibacillus plantarum, Levilactobacillus brevis, Latilactobacillus sakeii, Lacticaseibacillus paracasei, Lactobacillus delbreuckii subsp. bulgaricus, Levilactobacillus zymae, Companilactobacillus futsaii, Lentilactobacillus buchneri, Lentilactobacillus parabuchneri, Levilactobacillus namurensis, Lacticaseibacillus rhamnosus, and Limosylactobacillus fermentum) [13]. Depending on the natural environment of each Lactobacillus strain, different parameters influence the expression of GAD genes and, thus, GABA production [47]. These factors are explained below.
2.1.1. pH and Temperature
pH and temperature are the main environmental factors that can modulate GAD gene expression [48]. The pH value is a key factor for GABA biosynthesis by LABs and affects the growth of the bacteria and GAD activity [22,45,49,50,51]. Changes in pH enhance GAD pathway activation, a key mechanism for maintaining cell homeostasis [27,52]. Some studies have shown that the initial pH of the fermentation medium affects GABA synthesis [22,51]. In a study analyzing how initial pH affects GABA production by Lactiplantibacillus plantarum, the best GABA concentration was found at pH 5.5, and it was reported that, at this pH, twice the amount of GABA obtained at pH 4.0 could be obtained [53]. In general, acid environment (as in Korean kimchi and Chinese paocai) has been reported to be beneficial for the growth of GABA-producing LABs [18]. Therefore, the optimal conditions for fermenting microorganisms vary according to the different properties of GADs, and the optimum pH is reported to be 3.5–5.0 [18]. Low pH must be maintained for effective GABA production [54,55]. It is also known that GAD activity is significantly lost at near-neutral pH (pH 7.0) [18].
At the same time, temperature also affects GABA production due to its relationship with GAD activation [53]. The researchers summarized the optimal temperatures and pH values for various Lactobacillus species. Accordingly, Latilactobacillus sakei showed the highest GAD activity at 55 °C and pH 5, while 40 °C and pH 4.5 were reported as the best values for Lactiplantibacillus plantarum GAD activity. In addition, different strains of L. brevis show optimum activity between 30 and 48 °C and at a pH of 4.2–5.2 [56,57]. The optimal temperatures of GADs ranged from 30 to 60 °C in different LAB species [18].
2.1.2. Effect of Medium Composition
GAD activity is the key factor determining the GABA yield of a strain. Not only pH and temperature but also adding various media additives, such as L-glutamic acid and PLP, can modulate GABA synthesis. L-glutamic acid, the substrate of GAD, is an indispensable compound in the medium for the synthesis of GABA by LABs since LABs cannot synthesize sufficient L-glutamic acid for GABA production. Monosodium glutamate (MSG) is usually used in GABA production because it can produce L-glutamic acid by hydrolysis [18]. By increasing MSG, the aim is to stimulate GABA production of GAD via the GABA shunt pathway. At the same time, some researchers have shown that excessive MSG can inhibit cell growth and reduce GABA production. The optimal MSG concentrations for various microorganisms in GABA production are different [30,43,54]. The concentration of the Glu or MSG precursors strongly alters GABA synthesis [58]. In one study, the relationship between the amount of GABA produced Lactiplantibacillus plantarum and the effect of Glu concentration was measured in the range of 0–600 mM, and it was found that GABA production increased sharply until a 400 mM Glu concentration was reached [59]. Another study evaluating how different MSG concentrations affect GABA production by Lactiplantibacillus plantarum reported that the optimum Glu concentration to obtain the best GABA results was 20 g/L [53]. In a study in which a range of 0 to 400 mM MSG was used to evaluate the GABA yield of Levilactobacillus brevis, the best result was obtained at 270 mM [43]. Despite the effectiveness of the direct addition of Glu or MSG, alternatives were sought to reduce economic costs [26]. Woraharn et al. (2016) used the fungus Hericium erinaceus as a source of Glu combined with a co-culture of two Lactobacillus strains. Levilactobacillus brevis was used to hydrolyze L-glutamine to Glu using an L-glutaminase, and L. fermentum was added to convert this Glu to GABA. Another technique to promote the secretion of Glu without external support is co-cultivation with a microorganism that synthesizes Glu [60]. Yang et al. (2015) used a strain of Corynebacterium glutamicum to produce Glu, which was then converted to GABA by Lactiplantibacillus plantarum via the fermentation of cassava powder [61].
PLP can increase GAD activity by acting as a cofactor for the GAD enzyme. The effect of PLP varies according to the time of the addition of PLP. It was found that PLP can greatly promote the GABA production of Lacticaseibacillus paracasei at concentrations of 10 or 100 µM in the initial culture medium [55]. In addition to coenzyme PLP supplementation [62], other procedures, such as regulation of Tween-80 concentration [27] and the addition of metal ions, can be used to increase GAD activity [48].
Furthermore, adding different carbon and nitrogen sources can help improve bacterial metabolism and thus enhance GABA synthesis. Zareian et al. (2012) used glucose (carbon source) and nitrogen to enhance the bacterial production of Glu without any other supplementation [63]. However, the optimal carbon and nitrogen source varies depending on the Lactobacillus species. Several studies have shown that glucose is the most efficient carbon source for Lactiplantibacillus plantarum [64] and Levilactobacillus brevis [58]. Similarly, Zhao et al. (2015) reported that Lentilactobacillus buchneri produced higher amounts of GABA in the presence of xylose [65]. Yi Song and Yu Chui (2017) observed that Lacticaseibacillus rhamnosus synthesized high amounts of this amino acid using galactose [66].
2.1.3. Effect of Cultivation Time
The point at which optimum GABA production was reached varied depending on the Lactobacillus strain used. In one study, the highest GABA yield was detected after 60 h of cultivation using Lactiplantibacillus plantarum [59], while another study reported a higher GABA yield at 35 h when using another Lactiplantibacillus plantarum strain [62]. A study on Levilactobacillus brevis reported that the highest amount of GABA was reached in 30 h [67].
2.1. GABA 합성에 영향을 미치는 요인
Lactobacillus는
많은 GABA 생성 균주(예: Lactiplantibacillus plantarum, Levilactobacillus brevis, Latilactobacillus sakeii, Lacticaseibacillus paracasei, Lactobacillus delbreuckii subsp. bulgaricus, Levilactobacillus zymae, Companilactobacillus futsaii, Lentilactobacillus buchneri, Lentilactobacillus parabuchneri, Levilactobacillus namurensis, Lacticaseibacillus rhamnosus, 및 Limosylactobacillus fermentum) [13].
각 Lactobacillus 균주의 자연 환경에 따라
GAD 유전자 발현에 영향을 미치는 다양한 파라미터가 존재하며,
이는 결국 GABA 생산에 영향을 미칩니다 [47].
이러한 요인들은 아래에서 설명됩니다.
2.1.1. pH 및 온도
pH 및 온도는
GAD 유전자 발현을 조절하는 주요 환경 요인입니다 [48].
pH 값은
LAB에 의한 GABA 생합성의 핵심 요인으로,
세균의 성장과 GAD 활성에 영향을 미칩니다 [22,45,49,50,51].
pH 변화는
세포 내 환경 균형을 유지하는 핵심 메커니즘인
일부 연구에서는 발효 매체의 초기 pH가 GABA 합성에 영향을 미친다는 것이 보고되었습니다 [22,51]. Lactiplantibacillus plantarum의 GABA 생산에 초기 pH가 미치는 영향을 분석한 연구에서, pH 5.5에서 가장 높은 GABA 농도가 관찰되었으며, 이 pH에서 pH 4.0에서 얻은 양의 두 배가 얻을 수 있다고 보고되었습니다 [53]. 일반적으로 산성 환경(한국 김치와 중국 파오차이와 같은)은 GABA 생성 LAB의 성장에 유익하다고 보고되었습니다 [18]. 따라서 발효 미생물의 최적 조건은 GAD의 다양한 특성에 따라 다르며, 최적 pH는 3.5–5.0으로 보고되었습니다 [18]. 효과적인 GABA 생산을 위해 낮은 pH를 유지해야 합니다 [54,55]. 또한 GAD 활성은 중성 pH(pH 7.0) 근처에서 크게 감소한다는 것이 알려져 있습니다 [18].
동시에 온도도 GAD 활성화와의 관계로 인해 GABA 생산에 영향을 미칩니다 [53]. 연구자들은 다양한 Lactobacillus 종의 최적 온도와 pH 값을 요약했습니다. 이에 따르면 Latilactobacillus sakei는 55°C와 pH 5에서 가장 높은 GAD 활성을 보였으며, Lactiplantibacillus plantarum의 GAD 활성에 대한 최적 조건은 40°C와 pH 4.5로 보고되었습니다. 또한 L. brevis의 다양한 균주는 30~48°C와 pH 4.2~5.2에서 최적 활성을 보였습니다 [56,57]. GAD의 최적 온도는 다양한 LAB 종에서 30~60°C 사이로 다양했습니다 [
2.1.2. 배지 조성의 영향
GAD 활성은 균주의 GABA 수율을 결정하는 핵심 요인입니다.
pH와 온도뿐만 아니라 L-글루탐산과 PLP와 같은
다양한 배지 첨가물을 추가하는 것도
GABA 합성을 조절할 수 있습니다.
L-글루탐산은 GAD의 기질로, LAB가 GABA 생산에 필요한 충분한 L-글루탐산을 합성하지 못하기 때문에 LAB의 GABA 합성에 필수적인 성분입니다. 모노소듐 글루타메이트(MSG)는 가수분해로 L-글루탐산을 생성하기 때문에 GABA 생산에 일반적으로 사용됩니다 [
[18]. MSG를 증가시키는 것은 GABA 분비 경로를 통해 GAD의 GABA 생산을 자극하는 것을 목표로 합니다. 동시에 일부 연구자들은 과도한 MSG가 세포 성장 억제와 GABA 생산 감소로 이어질 수 있음을 보여주었습니다. GABA 생산에 사용되는 다양한 미생물에 대한 최적의 MSG 농도는 다릅니다 [30, 43, 54]. 글루타메이트 또는 MSG 전구체의 농도는 GABA 합성에 크게 영향을 미칩니다 [58].
한 연구에서 Lactiplantibacillus plantarum이 생산하는 GABA의 양과 글루타믹산 농도의 관계를 0–600 mM 범위에서 측정했으며, 글루타믹산 농도가 400 mM에 도달할 때까지 GABA 생산량이 급격히 증가하는 것으로 확인되었습니다 [59]. 또 다른 연구에서는 MSG 농도가 Lactiplantibacillus plantarum의 GABA 생산에 미치는 영향을 평가했으며, 최상의 GABA 결과를 얻기 위한 최적의 Glu 농도는 20 g/L [53]. Levilactobacillus brevis의 GABA 수율을 평가하기 위해 0~400 mM의 MSG 범위를 사용한 연구에서 최상의 결과는 270 mM에서 얻어졌습니다 [43]. 글루타메이트 또는 MSG의 직접 추가의 효과에도 불구하고 경제적 비용을 줄이기 위한 대안이 모색되었습니다 [26]. Woraharn 등(2016)은 곰팡이 Hericium erinaceus를 Glu의 원천으로 사용하며 두 가지 Lactobacillus 균주의 공배양을 결합했습니다. Levilactobacillus brevis는 L-글루타민을 Glu로 가수분해하기 위해 L-글루타민아제를 사용했으며, L. fermentum을 추가하여 이 글루타메이트를 GABA로 전환했습니다. 외부 지원 없이 글루타메이트 분비를 촉진하는 또 다른 기술은 글루타메이트를 합성하는 미생물과의 공배양입니다 [60]. Yang 등 (2015)은 Corynebacterium glutamicum 균주를 사용하여 Glu를 생산한 후, 이 Glu를 Lactiplantibacillus plantarum을 통해 cassava 분말 발효를 통해 GABA로 전환했습니다 [61].
PLP는 GAD 효소의 보조인자로 작용하여 GAD 활성을 증가시킬 수 있습니다. PLP의 효과는 PLP 추가 시점에 따라 다릅니다. PLP는 초기 배지 농도 10 또는 100 µM에서 Lacticaseibacillus paracasei의 GABA 생산을 크게 촉진한다는 것이 확인되었습니다 [55]. PLP 보충 외에도 [62], Tween-80 농도 조절 [27] 및 금속 이온 추가와 같은 다른 방법도 GAD 활성을 증가시키는 데 사용될 수 있습니다 [48].
또한, 다양한 탄소 및 질소 원료를 추가하면 세균 대사 과정을 개선하여 GABA 합성을 증진시킬 수 있습니다. Zareian 등(2012)은 다른 보충 없이 글루코스(탄소 원료)와 질소를 사용하여 세균의 Glu 생산을 증진시켰습니다 [63]. 그러나 최적의 탄소 및 질소 원천은 Lactobacillus 종에 따라 다릅니다. 여러 연구에서 글루코스가 Lactiplantibacillus plantarum [64]과 Levilactobacillus brevis [58]에 대한 가장 효율적인 탄소 원천으로 확인되었습니다. 同様に, Zhao 등(2015)은 Lentilactobacillus buchneri가 xylose 존재 하에서 더 많은 양의 GABA를 생산했다고 보고했습니다[65]. Yi Song과 Yu Chui(2017)는 Lacticaseibacillus rhamnosus가 galactose를 사용하여 이 아미노산을 높은 양으로 합성했다고 관찰했습니다[66].
2.1.3. 배양 시간의 영향
최적의 GABA 생산 시점은 사용된 Lactobacillus 균주에 따라 달랐습니다. 한 연구에서는 Lactiplantibacillus plantarum을 사용해 배양 60시간 후에 가장 높은 GABA 수율을 검출했으며 [59], 다른 연구에서는 다른 Lactiplantibacillus plantarum 균주를 사용해 배양 35시간 후에 더 높은 GABA 수율을 보고했습니다 [62]. Levilactobacillus brevis에 대한 연구에서는 30시간에 가장 높은 GABA 양이 달성되었다고 보고되었습니다 [67].
2.2. Mechanisms and Techniques to Improve GABA Production
The GABA production capacity of strains is significantly affected by culture conditions. Numerous studies have been conducted to increase GABA yield by optimizing fermentation conditions, such as optimizing the initial pH of the culture medium, fermentation temperature, fermentation time, L-glutamic acid concentration, PLP, media additives, carbon source, nitrogen source, etc. [43,51,68].
Several LAB strains have shown potential for industrial GABA production. However, there is a need to improve the production efficiency of LAB-derived GABA. Several strategies have been used to improve GABA synthesis by LAB strains [69]. These strategies can be grouped under two headings: strategies dependent on modern biotechnology and traditional fermentation optimizations [70,71,72,73]. As a modern strategy, genetic improvement based on understanding cell physiology can effectively increase GABA production by LAB strains [74]. Conventional optimization has also proven to be an effective way to increase GABA production of LAB strains [65,75,76]. LABs often face various environmental stresses, including acid, cold, heat, drying, oxidative stress, etc., during fermentation and industry application [77,78]. In response to these challenges, LAB strains need good metabolic capabilities, strong physiological endurance, and environmental suitability [79,80,81]. Physiology-driven engineering has become an important way to increase the productivity of industrially applicable strains by improving their physiological performance [81].
Genetic engineering is an important strategy to improve GABA bioconversion and increase GABA yield through directed modulation of metabolic pathways. The direct approach is overexpression of the key enzyme GAD. Genes encoding GAD have been identified to be heterologously or homologously overexpressed in model LAB strains (Latilactobacillus sakei, Lactiplantibacillus plantarum, and so forth) [18,82,83]. A recombinant C. glutamicum was constructed by co-expression of two GAD genes (gadB1 and gadB2) from L. brevis Lb85. Compared to strains with a single expression of gadB1 or gadB2, this co-expressing strain increased GABA production more than twofold [82]. In addition to the overexpression of the GAD gene, glutamate in the GABA synthesis pathway, GABA antiporter gene gadC, and the regulatory gene gadR can also be used as a pathway for overproduction to increase GABA efficiency in the species [83].
The key to genetically modifying LABs is recombinant protein production gene therapy and genome engineering of the DNA molecules of plasmids used to deliver the genes of interest [84]. Since LABs have a thick peptide-glycan layer that acts as a barrier for transferring exogenous DNA into cells, the use of plasmids is often limited by transformation efficiency [85]. Additionally, factors such as low plasmid copy number, endonuclease activity within cells, and species-to-species variation limit the use of plasmids in LABs [86]. Alternatively, using genome engineering tools to insert the gene of interest into the LAB chromosome can increase the genetic stability of these constructs [87].
The Cre-lox system is another pathway for genetic recombination in LABs [88]. It offers flexibility and high recombination efficiency by allowing the deletion or insertion of a specific gene in any region of the bacterial chromosome [89]. There are limitations to the use of the Cre-lox system, such as iterative screening procedures, off-target effects, and high rates of false positive colonies causing genomic instability [90]. Alternatively, clustered regularly interspaced short palindromic repeats (CRISPR)-Cas systems, which make lethal double-strand breaks in the targeted region to eliminate false positive or wild-type colonies during screening, have been developed to provide a high-throughput screening and genome editing platform [91,92]. Rapid progress is being made in genetic engineering of LABs using recombination and CRISPR-based systems [84]. The most common genera used in the field of genetic engineering of LABs are Lactococcus and Lactobacillus [93,94].
However, the use of genetically modified LABs in food production is limited, due to concerns related to the dissemination of modified strains, plasmids, and recombinant genes, and especially due to a lack of public acceptance. Therefore, the use of genetically modified LABs is not approved and requires legal regulation [9].
Increased GABA biosynthesis efficiency and GABA productivity can also be achieved by inactivating the competing pathways of GABA production. The GABA aminotransferase enzyme gadT directs GABA to the Krebs cycle and causes GABA degradation. When gadB and gadC genes are co-overexpressed in the gadT mutant strain, the final GABA concentration is found to be increased [95].
A sufficient amount of precursor substance (L-glutamate) is needed for GABA production. However, since GABA-producing LABs cannot synthesize high concentrations of this compound naturally, exogenous L-glutamate must be supplied. Therefore, some L-glutamate recombinant strains have been developed to provide L-glutamate [96,97]. It was also found that GABA production was significantly increased by improving L-glutamate supplementation through deletion of the 2-oxoglutarate decarboxylase subunit gene odhA or the pyruvate carboxylase gene pyc [98].
In addition, using multiple microorganisms is currently popular in the fermentation industry as some substances produced by co-culture strains can enhance each other’s growth [99,100]. Co-fermentation with different strains is therefore considered a crucial and promising route for high yields of GABA [18].
2.2. GABA 생산을 개선하기 위한 메커니즘과 기술
균주의 GABA 생산 능력은
배양 조건에 크게 영향을 받습니다.
배양 조건을 최적화하여
GABA 수율을 증가시키기 위한 다양한 연구가 진행되었습니다.
예를 들어,
배양 매체의 초기 pH, 발효 온도, 발효 시간, L-글루탐산 농도, PLP, 배지 첨가물, 탄소 원천, 질소 원천 등을
여러 LAB 균주는 산업용 GABA 생산에 잠재력을 보여주었습니다. 그러나 LAB 유래 GABA의 생산 효율성을 향상시킬 필요가 있습니다. LAB 균주의 GABA 합성을 향상시키기 위해 여러 전략이 사용되었습니다 [69]. 이러한 전략은 현대 생물공학에 의존하는 전략과 전통적인 발효 최적화 전략으로 두 가지로 분류될 수 있습니다 [70,71,72,73]. 현대적 전략으로, 세포 생리학 이해를 기반으로 한 유전적 개선은 LAB 균주의 GABA 생산량을 효과적으로 증가시킬 수 있습니다 [74]. 전통적인 최적화도 LAB 균주의 GABA 생산량을 증가시키는 효과적인 방법으로 입증되었습니다 [65,75,76]. LAB는 발효 및 산업 적용 과정에서 산성, 저온, 고온, 건조, 산화 스트레스 등 다양한 환경 스트레스에 직면합니다 [77,78]. 이러한 도전 과제에 대응하기 위해 LAB 균주는 우수한 대사 능력, 강한 생리적 내성, 환경 적응성을 갖추어야 합니다 [79,80,81]. 생리학 기반 공학은 균주의 생리적 성능을 개선하여 산업 적용 가능한 균주의 생산성을 높이는 중요한 방법으로 부상했습니다 [81].
유전공학은 대사 경로의 선택적 조절을 통해
GABA 생체 전환을 개선하고
GABA 수율을 증가시키는 중요한 전략입니다.
직접적인 접근 방식은
핵심 효소 GAD의 과발현입니다.
GAD를암호화하는 유전자는 모델 LAB 균주(Latilactobacillus sakei, Lactiplantibacillus plantarum 등)에서 이종 또는 동종 과발현으로 확인되었습니다 [18,82,83]. L. brevis Lb85에서 유래한 두 개의 GAD 유전자(gadB1과 gadB2)를 공동 발현한 재조합 C. glutamicum이 구축되었습니다. 단일 유전자(gadB1 또는 gadB2)를 발현한 균주에 비해 이 공동 발현 균주는 GABA 생산량을 두 배 이상 증가시켰습니다 [82]. GABA 합성 경로에 있는 글루타메이트, GABA 항운반체 유전자 gadC, 및 조절 유전자 gadR의 과발현 외에도, 종의 GABA 효율을 높이기 위한 과생산 경로로 활용될 수 있습니다 [83].
LAB의 유전적 변형의 핵심은 재조합 단백질 생산 유전자 치료와 관심 유전자를 전달하는 플라스미드의 DNA 분자 유전체 공학입니다 [84]. LAB는 세포 내로 외래 DNA를 전달하는 장벽으로 작용하는 두꺼운 펩타이드-글리칸 층을 가지고 있어 플라스미드의 사용은 변환 효율성에 의해 제한됩니다 [85]. 또한 플라스미드 복제 수의 저하, 세포 내 엔도뉴클레이스 활성, 종 간 변이 등 요인이 LAB에서 플라스미드 사용을 제한합니다 [86]. 대안으로 유전체 공학 도구를 활용해 관심 유전자를 LAB 염색체에 삽입하면 이러한 구조물의 유전적 안정성을 높일 수 있습니다 [87].
Cre-lox 시스템은 LAB에서 유전적 재조합을 위한 또 다른 경로입니다 [88]. 이 시스템은 세균 염색체의 특정 지역에서 특정 유전자의 삭제 또는 삽입을 허용함으로써 유연성과 높은 재조합 효율성을 제공합니다 [89]. Cre-lox 시스템의 사용에는 반복적인 스크리닝 절차, 오프-타겟 효과, 가짜 양성 콜로니의 높은 발생률로 인한 유전체 불안정성 등 제한 사항이 있습니다 [90]. 대안으로, 표적 지역에서 치명적인 이중 가닥 절단을 유발하여 스크리닝 과정에서 가짜 양성 또는 야생형 콜로니를 제거하는 클러스터드 정규 간격 단일 염기 반복(CRISPR)-Cas 시스템이 개발되었습니다. 이는 고효율 스크리닝 및 유전체 편집 플랫폼을 제공합니다 [91,92]. 재조합 및 CRISPR 기반 시스템을 활용한 LAB 유전공학 분야에서 빠른 진전이 이루어지고 있습니다 [84]. LAB 유전공학 분야에서 가장 널리 사용되는 속은 Lactococcus와 Lactobacillus입니다 [93,94].
그러나 유전자 변형 LAB의 식품 생산 활용은 변형된 균주, 플라스미드, 재조합 유전자의 확산에 대한 우려, 특히 공공 수용 부족으로 인해 제한적입니다. 따라서 유전자 변형 LAB의 사용은 승인되지 않았으며 법적 규제가 필요합니다 [9].
GABA 생합성 효율과 GABA 생산량을 증가시키기 위해
GABA 생산의 경쟁 경로를 불활성화하는 방법도 있습니다.
GABA 아미노전달효소 gadT는
GABA를 크렙스 회로로 유도하여
GABA 분해를 유발합니다.
gadT 돌연변이 균주에서 gadB와 gadC 유전자를 동시에 과발현시키면
최종 GABA 농도가 증가하는 것으로 확인되었습니다 [95].
GABA 생산에는 충분한 전구체 물질(L-글루타메이트)이 필요합니다. 그러나 GABA 생산 LAB은 이 화합물을 자연적으로 고농도로 합성할 수 없기 때문에 외부에서 L-글루타메이트를 공급해야 합니다. 따라서 L-글루타메이트를 공급하기 위해 일부 L-글루타메이트 재조합 균주가 개발되었습니다 [96,97]. 또한 2-옥소글루타르산 탈카복실화 효소 서브유닛 유전자 odhA 또는 피루vate 카복실화 효소 유전자 pyc를 삭제함으로써 L-글루타메이트 보충을 개선하면 GABA 생산이 유의미하게 증가한다는 것이 발견되었습니다 [98].
또한, 일부 공배양 균주에서 생성되는 물질이 서로의 성장을 촉진할 수 있기 때문에 다중 미생물을 사용하는 것이 발효 산업에서 현재 인기 있습니다 [99,100]. 따라서 서로 다른 균주와의 공발효는 GABA의 고수율 생산을 위한 중요한 잠재적 경로로 고려되고 있습니다 [18].
3. Food Applications of GABA Derived from LABs
The production of foods and beverages fermented by LABs is becoming increasingly widespread because the metabolites produced as a result of their activities improve product quality and health consequences [101]. GABA is one of these metabolites that bacteria synthesize from the L-glutamate found in foods with the enzyme glutamate decarboxylase in order to increase their tolerance to acidic environments [12]. Levilactobacillus brevis, Lentilactobacillus buchneri, Lactobacillus delbreuckii subsp. bulgaricus, Limosilactobacillus fermentum, Lactobacillus helveticus, Lacticaseibacillus paracasei, and Lactiplantibacillus plantarum are important LABs for GABA production. Some strains of Streptococcus thermophilus and Lactococcus lactis are prominent in the production of GABA-rich dairy products. In recent years, it has been found that some species belonging to the Enterococcus, Leuconostoc, Pediococcus, and Weissella genera can also produce GABA [18]. The GABA production capacity of different species is highly variable. Compared to other LABs, it has been reported that Levilactobacillus brevis can produce high amounts of GABA (205 g/L). However, there may be marked differences in the GABA efficiency of various strains of a bacteria species [27]. Therefore, the use of strains with high GABA productivity as starter cultures in some fermented foods can be used as an alternative technique in the production of functional foods that offer significant health effects [102].
In the food industry, the production of functional foods enriched with GABA is becoming widespread. Examples of these functional foods include GABA-enriched beverages, such as Gabaron Tea, white tea, fruit juice; GABA-enriched dairy products, such as fermented milk, yogurt, cheese; GABA-enriched cereal-based products, such as brown rice, fermented oat, wheat-based sourdough, quinoa flakes; and GABA-enriched legumes and soy products, such as adzuki beans, black soybeans, tempeh, fermented soybeans, etc. [103,104]. Among these products Gabaron Tea, for example, was a common GABA-enriched functional beverage that was commercially produced in Japan in the 1980s and black raspberry juice enriched with GABA is included in the list of GRAS. GABA can also be used as a food additive in some foods such as chocolates, potato snacks, bread, and biscuits [104]. The advantage of using LAB fermentation in foods is its high enrichment effect and suitability for the mass production of GABA [105]. However, the problem with GABA production from LABs is that it requires a controlled fermentation process [102]. In addition, disadvantages of LAB fermentation include its high cost and strain safety issues [105].
3. LAB에서 유래한 GABA의 식품 응용
LAB에 의해 발효된 식품 및 음료의 생산은
그들의 활동으로 생성되는 대사산물이 제품 품질과 건강에 긍정적인 영향을 미치기 때문에
점점 더 널리 확산되고 있습니다 [101].
GABA는
식품에 존재하는 L-글루타메이트를 글루타메이트 디카르복실라제 효소를 통해
산성 환경에 대한 내성을 높이기 위해 박테리아가 합성하는 대사산물 중 하나입니다 [12].
Levilactobacillus brevis, Lentilactobacillus buchneri, Lactobacillus delbreuckii subsp. bulgaricus, Limosilactobacillus fermentum, Lactobacillus helveticus, Lacticaseibacillus paracasei, 및 Lactiplantibacillus plantarum은 GABA 생산에 중요한 LAB입니다.
Streptococcus thermophilus와 Lactococcus lactis의 일부 균주는
GABA 함량이 높은 유제품 생산에 두드러집니다.
최근 연구에서 Enterococcus, Leuconostoc, Pediococcus, 및 Weissella 속의 일부 종도 GABA를 생산할 수 있다는 것이 밝혀졌습니다 [18]. 다양한 종의 GABA 생산 능력은 매우 다양합니다. 다른 LAB에 비해 Levilactobacillus brevis는 높은 양의 GABA(205 g/L)를 생산할 수 있다는 보고가 있습니다. 그러나 동일한 세균 종의 다양한 균주 간 GABA 효율성에 큰 차이가 있을 수 있습니다 [27]. 따라서, 일부 발효 식품의 스타터 문화로 GABA 생산 능력이 높은 균주를 사용하는 것은 건강에 유익한 효과를 제공하는 기능성 식품 생산을 위한 대체 기술로 활용될 수 있습니다 [102].
식품 산업에서 GABA가 풍부한 기능성 식품의 생산이 널리 확산되고 있습니다.
이러한 기능성 식품의 예시로는
GABA 강화 음료(Gabaron Tea, 백차, 과일 주스),
GABA 강화 유제품(발효 우유, 요거트, 치즈),
GABA 강화 곡물 기반 제품(현미, 발효 오트, 밀 기반 사워도우, 퀴노아 플레이크) 등이 있습니다.
GABA 강화 콩류 및 콩 제품으로는
적두, 검은 콩, 템페, 발효 콩 등이 있습니다 [103,104].
이 중 Gabaron Tea는
1980년대 일본에서 상업적으로 생산된 대표적인 GABA 강화 기능성 음료이며,
GABA 강화 검은 라즈베리 주스는 GRAS 목록에 포함되어 있습니다.
GABA는
초콜릿, 감자 스낵, 빵, 비스킷 등 일부 식품의 식품 첨가물로도
사용될 수 있습니다 [104].
LAB 발효를 식품에 사용하는 장점은
GABA의 높은 풍부화 효과와 대량 생산에 적합하다는 점입니다 [105].
그러나
LAB에서 GABA를 생산하는 문제는 발효 과정을 엄격히 제어해야 한다는 점입니다 [102].
또한
LAB 발효의 단점으로는
높은 비용과 균주 안전성 문제가 있습니다 [105].
3.1. Applications of GABA Produced by LABs in the Baking Industry and Cereal-Based Products
Plant foods are dietary sources of naturally occurring GABA. For example, while the GABA content in wheat is quite low and insignificant compared to other grain products (0.7 mg/100 g for wheat flour), the food with the highest GABA content was recorded as whole grain oat (57.1 mg/100 g). The GABA contents of different rice types also vary. The foods with the highest GABA content among pseudocereals are stated as Tartary Buckwheat and quinoa (10.34 mg/100 g and 7.8 mg/100 g, respectively) [106].
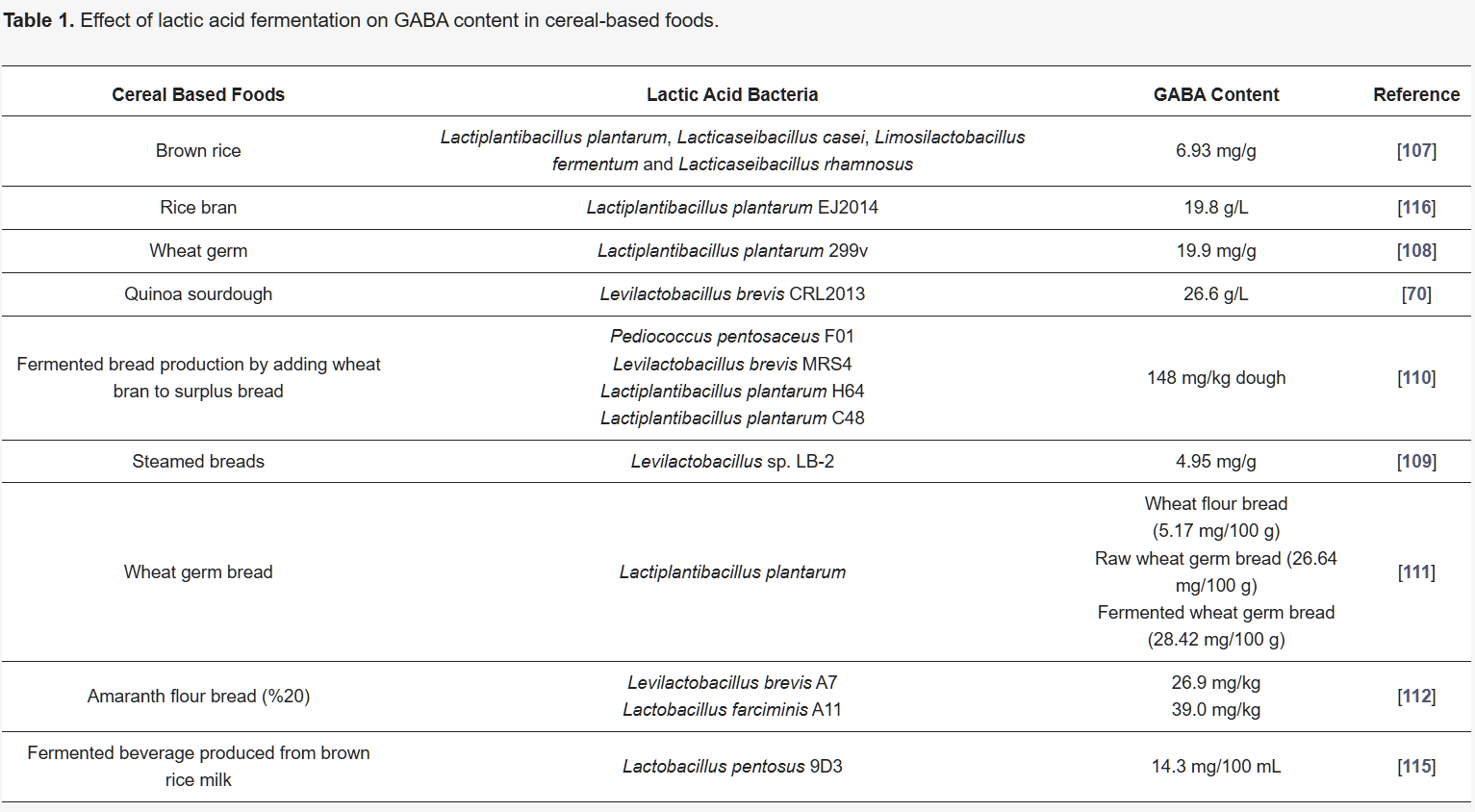
Since the amount of GABA naturally found in foods is low, the GABA content in cereal-based foods can be increased through the fermentation process using LABs. When a brown rice was fermented with 1 × 107 CFU/mL LAB (Lactiplantibacillus plantarum, Lacticaseibacillus casei, Limosilactobacillus fermentum, and Lacticaseibacillus rhamnosus) at 36 °C for 48 h, the GABA content increased from 4.64 mg/g to 6.93 mg/g (49%) [107]. Although the amount of GABA naturally found in wheat is low (0.7 mg/100 g for wheat flour) [106], the GABA content was increased to 19.9 mg/g in wheat germ as a result of the fermentation with Lactiplantibacillus plantarum 299v [108]. Similarly, an increase in GABA content has been reported in breads prepared by fermenting with LABs [109,110,111] and in fermented products prepared using pseudocereals [70,112]. Table 1 summarizes the GABA content increase in cereal-based products fermented by LABs.
Applications increasing GABA content in cereal-based products should be considered in terms of their effects on product quality as well as their effects on health. The fermentation process with LABs is important in terms of improving taste, flavor, aroma, and texture in cereal-based and bakery industry products [113]. At the end of the fermentation process, an improvement in the volume, color, brightness, and taste of the bread product was demonstrated [109,111]. Fermentation plays a role in improving the bioavailability of micronutrients by providing optimal conditions for the enzymatic degradation of phytates. Improving protein digestibility causes an increase in the levels of free amino acids, especially lysine, methionine, and tryptophan [114]. Due to their antimicrobial effects, fermentation with LABs is also important in the detoxification of harmful components such as toxins [113]. Additionally, the production of gluten-free cereal-based fermented beverages may be a good option for people with celiac disease or gluten sensitivity [115].
3.1. LAB에서 생산된 GABA의 제과 산업 및 곡물 기반 제품에 대한 응용
식물성 식품은 자연적으로 발생하는
GABA의 식이 공급원입니다.
예를 들어,
밀의 GABA 함량은 다른 곡물 제품에 비해 매우 낮고 미미합니다(밀 가루 0.7 mg/100 g).
반면, 가장 높은 GABA 함량을 기록한 식품은
전체 곡물 오트밀(57.1 mg/100 g)입니다.
다양한 쌀 종류의 GABA 함량도 차이가 있습니다.
곡물 중 GABA 함량이 가장 높은 식품은
타르타리 보리(10.34 mg/100 g)와 퀴노아(7.8 mg/100 g)로 보고되었습니다
GABA는 식품에 자연적으로 존재하는 양이 적기 때문에,
곡물 기반 식품의 GABA 함량은 LAB를 이용한 발효 과정을 통해 증가시킬 수 있습니다.
갈색 쌀을 1 × 107 CFU의 LAB로 발효시켰을 때
GABA 함량이 증가했습니다.
식품에 자연적으로 존재하는 GABA의 양이 적기 때문에,
LAB을 이용한 발효 과정을 통해
곡물 기반 식품의 GABA 함량을 증가시킬 수 있습니다.
갈색 쌀을
1 × 10⁷ CFU/mL의 LAB (Lactiplantibacillus plantarum, Lacticaseibacillus casei, Limosilactobacillus fermentum, 및 Lacticaseibacillus rhamnosus)로 36°C에서 48시간 발효시킨 결과,
GABA 함량은 4.64 mg/g에서 6.93 mg/g(49%)로 증가했습니다 [107].
밀에 자연적으로 존재하는
GABA의 양은 낮습니다(밀 가루 100 g당 0.7 mg) [106],
그러나
Lactiplantibacillus plantarum 299v로 발효한 결과
밀 배아의 GABA 함량이 19.9 mg/g로 증가했습니다 [108].
마찬가지로,
LABs로 발효한 빵에서 GABA 함량 증가가 보고되었으며 [109,110,111],
가짜 곡물을 사용한 발효 제품에서도 증가가 관찰되었습니다 [70,112].
표 1은 LABs로 발효한 곡물 기반 제품의 GABA 함량 증가를 요약합니다.
곡물 기반 제품의 GABA 함량을 증가시키는 응용 기술은 제품 품질에 미치는 영향뿐만 아니라 건강에 미치는 영향 측면에서도 고려되어야 합니다. LABs를 이용한 발효 과정은 곡물 기반 제품 및 제과 산업 제품의 맛, 향, 향기, 텍스처 개선 측면에서 중요합니다 [113].
발효 과정 종료 시
빵 제품의 부피, 색상, 밝기, 맛이 개선되었다는 것이 입증되었습니다 [109,111].
발효는
피타트의 효소적 분해에 최적의 조건을 제공함으로써
미량 영양소의 생체 이용률을 향상시키는 역할을 합니다.
단백질 소화율 개선은
특히 라이신, 메티오닌, 트립토판과 같은 자유 아미노산 수준을 증가시킵니다 [114].
LABs를 이용한 발효는
독소와 같은 유해 성분의 해독에 중요한 역할을 합니다 [113].
또한 글루텐이 없는 곡물 기반 발효 음료의 생산은
셀리악병이나 글루텐 민감증을 가진 사람들에게 좋은 옵션이 될 수 있습니다 [115].
Table 1. Effect of lactic acid fermentation on GABA content in cereal-based foods.
3.2. Applications of GABA Produced by LABs in Dairy Products
Lactobacillus, Streptococcus, Leuconostoc, Pediococcus, and Lactococcus are LABs that play a role in the fermentation of dairy products. During the fermentation process, various biochemical changes occur that increase food quality, such as the conversion of lactose to lactic acid, the release of fatty acids, improvements in sensory properties such as taste and texture, and the production of bioactive compounds [117]. In addition, the breakdown of proteins into casein and whey peptides and the increase in the shelf life of the dairy products are among the other positive results of the fermentation with LABs [118].
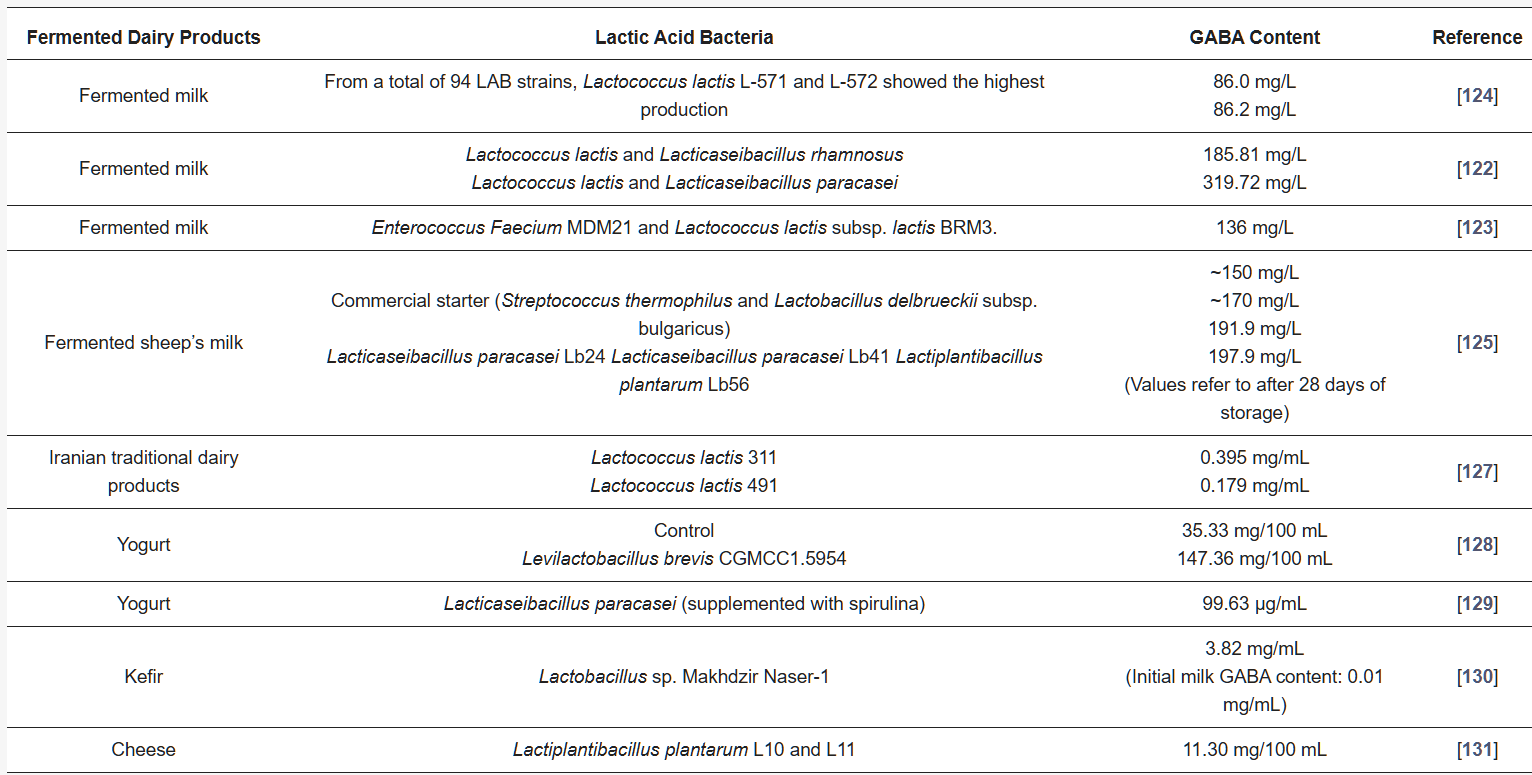
The use of probiotic LABs in dairy products is important in the production of functional foods that can reduce cholesterol and support the diet with GABA. Additionally, LABs can reduce oxidative stress by increasing the level of antioxidant components [119]. Animal studies have shown that the GABA in fermented dairy products may have anti-insomnia [120] and anti-diabetic [121] effects. Studies on fermented dairy products show that the use of more than one bacterial strain together increases the GABA content compared to a single bacterial strain [122,123,124]. In addition, the increase in GABA content continues during storage, and the sensory characteristics of fermented dairy products are better than the control group [125]. However, especially in cheeses, proteolysis can stimulate the release of free amino acids that can be converted to toxic biogenic amines. The accumulation of biogenic amines such as histamine and tyramine can have adverse effects on health. In a study evaluating the safety of starter cultures in cheese, it was reported that the Levilactobacillus brevis TAUL1567 strain could produce tyramine (193.15 μg/mL). Also, the Lactococcus lactis TAUL88 and TAUL8000 strains and the Levilactobacillus brevis TAUL1567 strain have been shown to be capable of producing putrescine [126]. Therefore, it is important to use starter cultures that do not produce biogenic amines in the fermented foods. The effect of LAB fermentation on GABA content in fermented dairy products is given in Table 2.
3.2. 유산균에 의해 생성된 GABA의 유제품 적용
Lactobacillus, Streptococcus, Leuconostoc, Pediococcus, 및 Lactococcus는
유제품 발효에 역할을 하는 LABs입니다.
발효 과정에서 유당을 젖산으로 전환,
지방산 방출, 맛과 텍스처 등 감각적 특성 개선, 생물활성 화합물 생산 등
식품 품질을 향상시키는 다양한 생화학적 변화가 발생합니다 [117].
또한,
단백질의 카제인과 유청 펩타이드로 분해되고 유제품의 유통기한이 연장되는 것도
LABs 발효의 다른 긍정적인 결과입니다 [118].
유제품에 프로바이오틱 LABs를 사용하는 것은
콜레스테롤을 감소시키고
GABA로 식단을 지원하는 기능성 식품 생산에 중요합니다.
또한,
LABs는 항산화 성분의 수준을 증가시켜 산화 스트레스를 감소시킬 수 있습니다 [119].
동물 연구에서 발효 유제품의 GABA는
불면증 억제 [120] 및 당뇨병 억제 [121] 효과를 가질 수 있음을 보여주었습니다.
발효 유제품에 대한 연구에서
단일 세균 균주보다 여러 세균 균주를 함께 사용했을 때
GABA 함량이 증가함을 보여주었습니다 [122,123,124].
또한 GABA 함량은 저장 중에도 증가하며,
발효 유제품의 감각적 특성은 대조군보다 우수합니다 [125].
그러나
특히 치즈에서는 단백질 분해가 독성 생물학적 아민으로 전환될 수 있는
자유 아미노산의 방출을 자극할 수 있습니다.
히스타민과 티라민과 같은 생물학적 아민의 축적은
건강에 유해한 영향을 미칠 수 있습니다.
치즈에서 스타터 배양액의 안전성을 평가한 연구에서
Levilactobacillus brevis TAUL1567 균주가
티라민(193.15 μg/mL)을 생성할 수 있다는 보고가 있었습니다.
또한 Lactococcus lactis TAUL88 및 TAUL8000 균주와 Levilactobacillus brevis TAUL1567 균주는 푸트레신 생성이 가능함이 확인되었습니다 [126]. 따라서 발효 식품에는 생물학적 아민을 생성하지 않는 스타터 배양균을 사용하는 것이 중요합니다. LAB 발효가 발효 유제품의 GABA 함량에 미치는 영향은 표 2에 제시되어 있습니다.
Table 2. Effect of lactic acid fermentation on GABA content in fermented dairy products.
3.3. Applications of GABA Produced by LABs in the Other Food Sources
LABs are also widely used in the fermentation of meat products. LABs metabolize the proteins, lipids, and glycogen in meat into smaller molecules through enzyme systems and are responsible for the development of a special taste in the final product. In addition, the fermentation process improves the physical and chemical properties of meat products and increases antioxidant and antibacterial metabolites and nitrite breakdown [132]. During fermentation, the product is also enriched with GABA. Related studies have shown that LABs increase the amount of GABA in the Vietnamese traditional fermented meat product Nem Chua [133], fermented sausage [134], and fermented fish products [135,136].
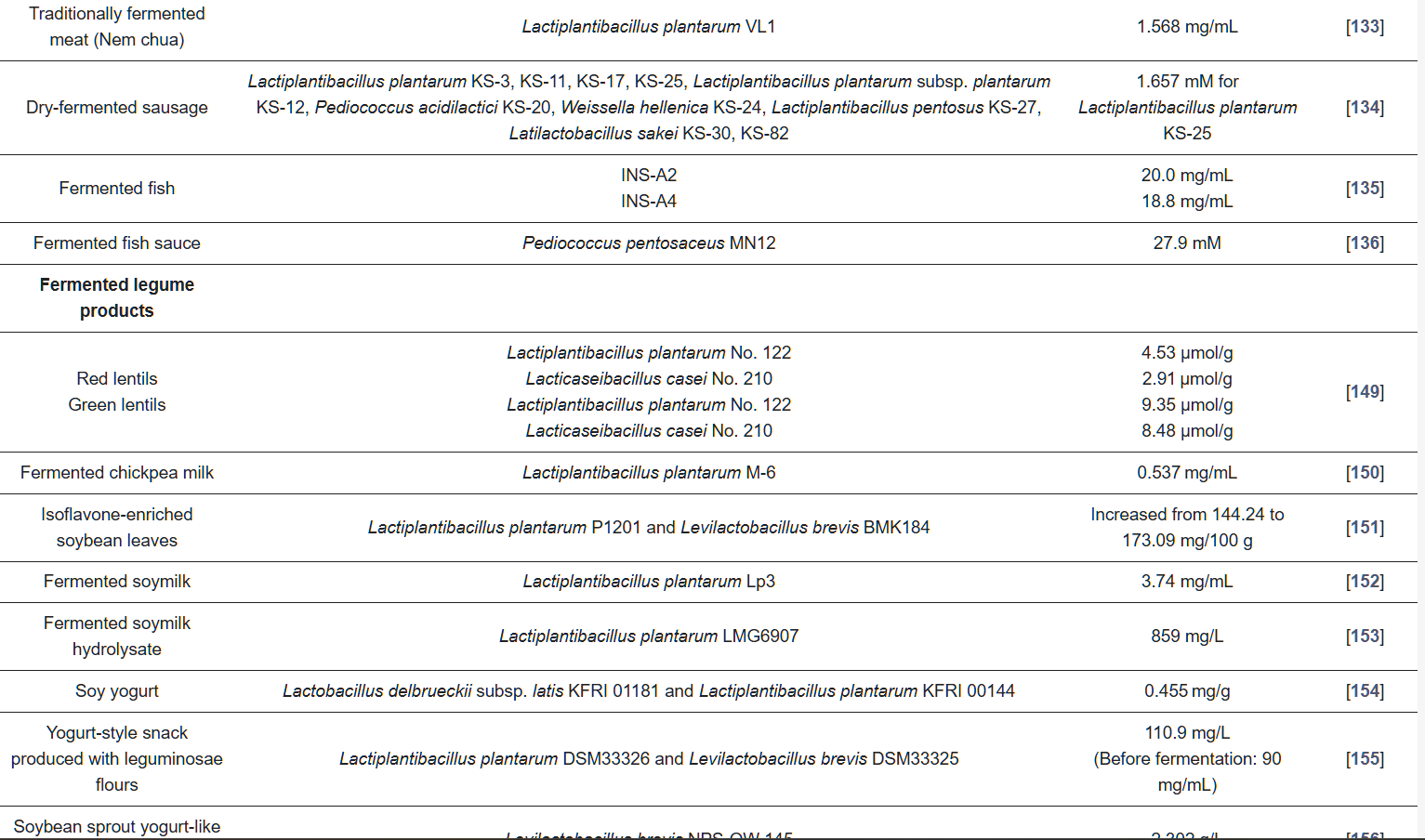
Legumes are a source of natural prebiotic ingredients including oligosaccharides, resistant starch, polyphenols, and isoflavones. These compounds provide various important physiological benefits due to their anti-inflammatory and immune system regulation as well as anti-cancer properties [137]. In a study conducted on mice with depressive-like behavior, it was shown that the GABA content in fermented Adzuki bean sprouts increased serotonin and norepinephrine levels and improved social interaction [138]. However, applications for legumes are still limited due to the presence of undesirable compounds such as phytic acid and saponin and their unpleasant sensory qualities [139]. Fermentation of legumes with LABs is important in reducing undesirable nutritional components such as phytic acid and in developing a healthier and technologically adapted symbiotic product [137,139]. Protein solubility, water and oil retention capacity, emulsification, and gel formation properties can change during the fermentation process; thus, the technological properties of the products can be improved. In addition, fermentation with LABs is important in the degradation of aromatic components, reducing undesirable taste and allergenic properties [139]. By fermenting legumes, snacks and beverages with enhanced GABA, such as bread, pasta, and yogurt, can be produced [137]. The effect of lactic acid fermentation on GABA content in other food sources is shown in Table 3.
Similarly, fermentation of fruits and vegetables with LABs can have positive effects on health through the production of bioactive components [140]. In a study, it was reported that strawberry juice with enhanced GABA had an anti-inflammatory effect and reduced serum TNF-α and IL-6 levels in mice [141]. In another study, the GABA in fermented Hovenia dulcis extract was shown to have liver-protective properties in mice [142]. In addition to its health effects, fermentation also improves the quality of the foods. The fermentation extends the shelf life of products by reducing or inhibiting foodborne pathogens in fruits and vegetables [143]. Fruit juices fermented by LABs have higher viscosity, enhanced aroma with the production of new compounds, and increased stability of phenolic compounds through the production of organic acids [101]. Recently, the production of vegan fermented fruit and vegetable juices that can be easily used by individuals with lactose intolerance or allergies has been at the forefront. In a systematic review, it was stated that these products offer strong antimicrobial and antioxidant properties, high vitamin, total phenolic substance, amino acid, exopolysaccharide content, and unique sensory quality [144]. Fermentation of fruit and vegetable juices with LABs is also effective in increasing the GABA content of the products [145,146,147,148].
3.3. LAB에 의해 생성된 GABA의 다른 식품 원료에 대한 응용
LAB는
육류 제품 발효에도 널리 사용됩니다.
LAB는
효소 시스템을 통해 육류의 단백질, 지방, 글리코겐을 작은 분자로 분해하며,
최종 제품의 특수한 맛 형성에 기여합니다.
또한 발효 과정은 육류 제품의 물리적 및 화학적 특성을 개선하고
항산화 및 항균 대사산물과 니트리트 분해량을 증가시킵니다 [132].
발효 과정에서 제품에는
GABA가 풍부해집니다.
관련 연구 결과, LAB는 베트남 전통 발효 육류 제품인 Nem Chua [133], 발효 소시지 [134], 발효 어류 제품 [135,136]에서 GABA의 양을 증가시키는 것으로 나타났습니다.
콩류는 올리고당, 저항성 전분, 폴리페놀, 이소플라본 등 자연적인 프리바이오틱 성분의 원천입니다. 이러한 화합물은 항염증 및 면역 체계 조절, 항암 특성으로 인해 다양한 중요한 생리적 혜택을 제공합니다 [137]. 우울증 유사 행동을 보이는 쥐를 대상으로 한 연구에서 발효된 아즈키 콩 새싹의 GABA 함량이 세로토닌과 노르에피네프린 수치를 증가시키고 사회적 상호작용을 개선했다는 결과가 나왔습니다 [138]. 그러나 콩류의 응용은 피틴산과 사포닌과 같은 유해 성분 및 불쾌한 감각 특성으로 인해 여전히 제한적입니다 [139]. 콩류의 LAB 발효는 피틴산과 같은 유해 영양 성분을 감소시키고 건강에 이로운 기술적으로 적응된 공생 제품을 개발하는 데 중요합니다 [137,139]. 발효 과정에서 단백질 용해도, 수분 및 지방 유지 능력, 유화 능력, 젤 형성 특성 등이 변화할 수 있으며, 이는 제품의 기술적 특성을 개선할 수 있습니다. 또한 LABs를 이용한 발효는 향기 성분의 분해, 불쾌한 맛과 알레르기 성질 감소에 중요합니다 [139]. 콩류, 스낵, 음료 등을 발효시켜 GABA 함량이 증가한 제품(예: 빵, 파스타, 요거트)을 생산할 수 있습니다 [137]. 유산균 발효가 다른 식품 원료의 GABA 함량에 미치는 영향은 표 3에 제시되어 있습니다.
同様に, LABs를 이용한 과일 및 채소의 발효는 생체활성 성분 생산을 통해 건강에 긍정적인 영향을 미칠 수 있습니다 [140]. 한 연구에서 GABA 함량이 증가한 딸기 주스가 쥐에서 항염증 효과를 보이고 혈청 TNF-α 및 IL-6 수치를 감소시켰다는 보고가 있습니다 [141]. 다른 연구에서는 발효된 Hovenia dulcis 추출물의 GABA가 쥐에서 간 보호 효과를 나타냈습니다 [142]. 건강 효과 외에도 발효는 식품의 품질을 향상시킵니다. 발효는 과일과 채소에서의 식품borne 병원균을 감소시키거나 억제함으로써 제품의 유통기한을 연장합니다 [143]. LABs로 발효된 과일 주스는 새로운 화합물의 생산을 통해 점도가 증가하고 향이 향상되며, 유기산 생산을 통해 페놀 화합물의 안정성이 증가합니다 [101]. 최근에는 유당 불내증이나 알레르기가 있는 사람들이 쉽게 섭취할 수 있는 비건 발효 과일 및 채소 주스의 생산이 주목받고 있습니다. 체계적 문헌 고찰에서 이러한 제품이 강력한 항균 및 항산화 특성, 높은 비타민, 총 페놀성 물질, 아미노산, 외부 다당류 함량, 독특한 감각적 품질을 제공한다고 보고되었습니다 [144]. LAB를 이용한 과일 및 채소 주스의 발효는 제품의 GABA 함량을 증가시키는 데도 효과적입니다 [145,146,147,148].
Table 3. Effect of lactic acid fermentation on GABA content in other food sources.
3.4. Potential Adverse Effects of High GABA Intake
The literature regarding the potential side effects of GABA produced by LAB fermentation is limited. It is known that some toxic components (such as biogenic amines) can be produced during lactic acid fermentation. Identification of strains that produce beneficial metabolites but do not increase toxic compounds may expand the use of these bacteria in the health and food industries [160]. On the other hand, the effects of GABA as a dietary supplement or as a naturally occurring ingredient in fermented milk or soy matrices were studied in clinical trials. Data at dosages up to 18 g/d for 4 days and in longer studies at intakes of 120 mg/d for 12 weeks indicated no significant side effects related to GABA. It is possible that using GABA concurrently with anti-hypertensive drugs could raise the risk of hypotension because GABA may cause a drop in blood pressure. Caution is advised for pregnant and lactating women since GABA can impact neurotransmitters and the endocrine system, which includes elevated levels of prolactin and growth hormone [23].
3.4. 고농도 GABA 섭취의 잠재적 부작용
LAB 발효로 생성된 GABA의 잠재적 부작용에 대한 문헌은 제한적입니다. 젖산 발효 과정에서 일부 독성 성분(예: 생물학적 아민)이 생성될 수 있다는 것이 알려져 있습니다. 유익한 대사물을 생성하지만 독성 화합물을 증가시키지 않는 균주를 식별하는 것은 이러한 세균의 건강 및 식품 산업에서의 활용 범위를 확대할 수 있습니다 [160]. 반면, GABA를 식이 보충제나 발효 유제품 또는 대두 매트릭스 내 자연 발생 성분으로 사용한 임상 시험에서 그 효과가 연구되었습니다. 4일 동안 18g/일 또는 12주 동안 120mg/일의 용량에서 GABA와 관련된 유의미한 부작용은 관찰되지 않았습니다. GABA를 항고혈압제와 동시에 복용할 경우 혈압 저하 위험이 증가할 수 있습니다. GABA가 혈압을 낮출 수 있기 때문입니다. 임신 및 수유 중인 여성은 GABA가 신경전달물질과 내분비계에 영향을 미칠 수 있으며, 이는 프로락틴과 성장 호르몬 수치 상승을 포함할 수 있으므로 주의가 필요합니다 [23].
4. Human Health Benefits of GABA
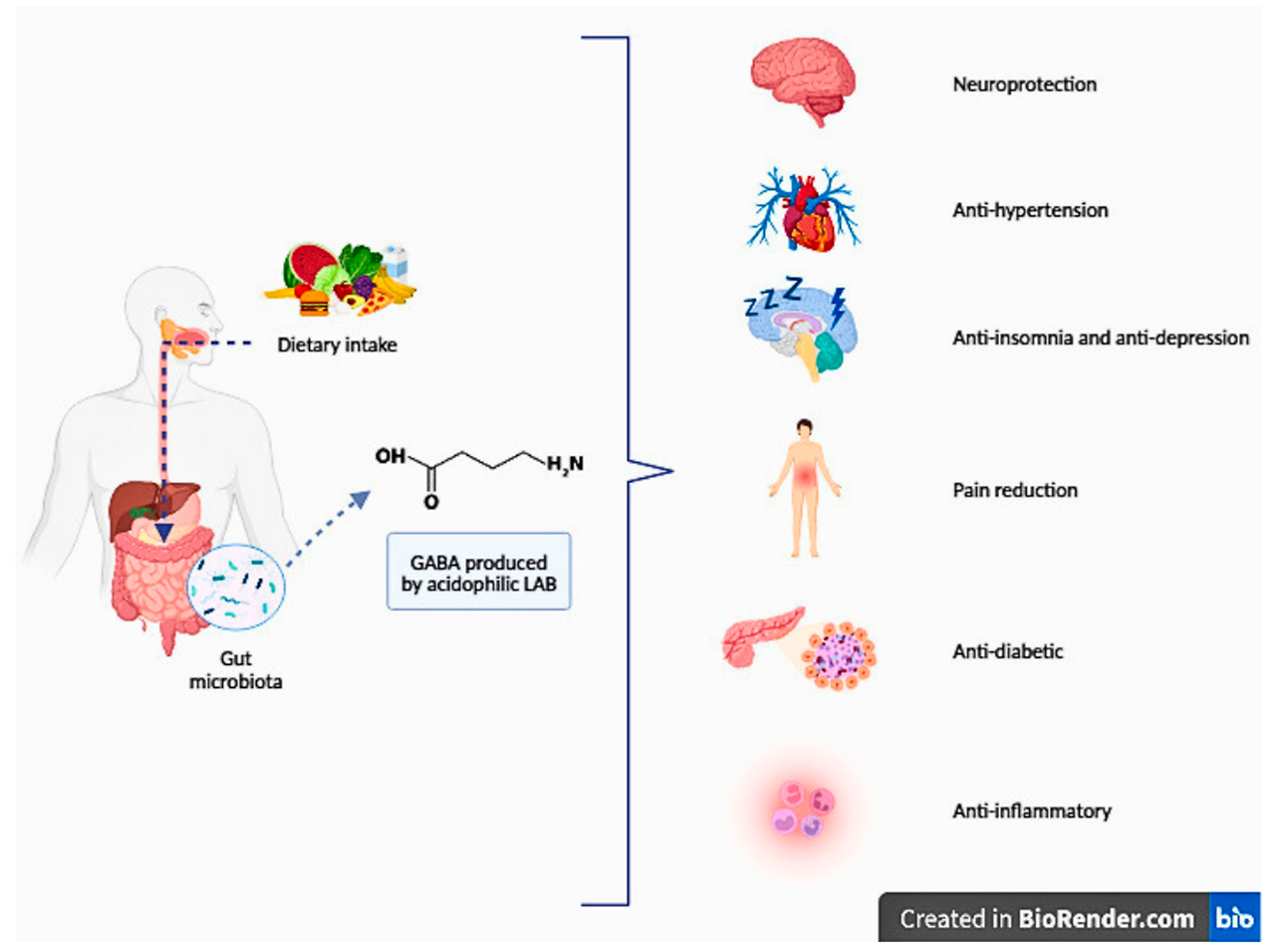
In recent years, numerous studies have demonstrated the beneficial effects of GABA produced by LABs, referred to as a postbiotic, on neuroprotection, improvement of sleep quality, alleviation of depression, and pain relief (see Table 4). Foods enriched with GABA have been found to possess various health benefits, such as anti-diabetic, anti-hypertensive, and anti-inflammatory properties [24]. Despite its effects on different organs, GABA primarily exerts its influence through the brain–gut axis [161]. The positive effects of GABA on health are shown in Figure 2.
4. GABA의 인간 건강 혜택
최근 연구에서 LAB(유산균)에 의해 생성된 GABA(포스트바이오틱스)가 신경 보호, 수면 품질 개선, 우울증 완화, 통증 완화 등에 유익한 효과를 나타낸다는 것이 입증되었습니다 (표 4 참조). GABA가 풍부한 식품은 항당뇨, 항고혈압, 항염증 등 다양한 건강 혜택을 지니는 것으로 밝혀졌습니다 [24]. 다양한 장기에게 영향을 미치지만, GABA는 주로 뇌-장 축을 통해 그 영향을 발휘합니다 [161]. GABA의 건강에 대한 긍정적 효과는 그림 2에 표시되어 있습니다.
Figure 2. Potential health advantages of foods enriched with GABA (adapted from [24,162]).
4.1. Neuroprotection
The inflammatory response to nerve tissue damage disrupts the balance of electrical activities between excitatory and inhibitory neurotransmitter systems in the brain by leading to the release of various inflammatory mediators such as reactive oxygen species (ROS), nitric oxide (NO), and cytokines [163,164]. This condition contributes to various neurological disorders, including epilepsy, Alzheimer’s, cerebrovascular diseases, multiple sclerosis, Parkinson’s, neuroinfections, and insomnia [165,166,167].
GABA is a significant inhibitory neurotransmitter in the nervous system and plays a critical role in transmitting information, neuronal development, and regulation of neurological disorders [168,169]. The impact of GABA on various diseases is attributed to its regulation of numerous functions through neuronal signal transmission and various receptors via its distribution in the central nervous system and peripheral organs [20]. Low GABA concentrations in the brain, imbalances in the GABAergic system, and alterations in GABA neurotransmitter activity, have been observed to lead to dysfunctions in ion transport functionality, synaptic connections, and modulation of the central nervous system [170,171]. Additionally, it has been noted that permanent damage to GABA function resulting from hypoxic–ischemic events during fetal development may lead to the emergence of learning and memory deficits [172].
The therapeutic effects of GABA as a dietary supplement have been extensively studied, showing its potential to enhance memory and cognitive functions by suppressing neurodegeneration [50,150,173,174,175,176,177,178,179]. It has been suggested that GABA supplements may reduce the severity of epileptic seizures and could be utilized for the prevention or mitigation of cerebral stroke damage [180,181]. However, in particular studies, the neuroprotective effect of GABA was not observed in cerebral ischemia [182,183]. In a study conducted on mice, significant neuroprotection could not be achieved when GABA transporters were inhibited following focal cerebral ischemia [183]. Similarly, consistent with the previous study, GABA did not exhibit a significant difference in functional or histological measurements following ischemia in the rat suture model, indicating no neuroprotective effect [182].
GABA produced by Lentilactobacillus buchneri isolated from kimchi protects against neurotoxic-induced cell death [50]. Additionally, GABA produced by another LAB, Lactobacillus sakei B216, isolated from kimchi, has improved long-term memory loss in cognitively impaired mice and increased the proliferation of in vitro neuroendocrine PC-12 cells [173]. Pre-germinated brown rice extract with enhanced levels of GABA has been observed to effectively inhibit apoptosis-associated DNA fragmentation and intracellular ROS formation, thereby significantly reducing the proliferation and apoptosis of human neuroblastoma cells [174]. Neuroprotective effects observed in mice fed with fermented rice flour containing 750.55 ± 26.03 mg GABA/100 g have been linked to increased activities of antioxidant enzymes superoxide dismutase and catalase in the cortex and cerebellum regions, along with a decrease in oxidative stress [175].
GABA-enriched fermented sea tangle (Laminaria japonica) fermented with Levilactobacillus brevis BJ20 has been shown to provide a protective effect against cognitive decline in dementia model mice and the elderly, potentially enhancing neuroplasticity [176,177]. Another study revealed that GABA-enriched fermented sea tangle with Levilactobacillus brevis BJ20 effectively increased neurotrophic factor levels associated with reduced risk of dementia and Alzheimer’s disease in middle-aged women [184]. GABA produced by Lactiplantibacillus plantarum from novel fermented chickpea milk has been reported to protect neuroendocrine PC-12 cells from MnCl2-induced damage and enhance cell viability, thus providing neuroprotective effects [150].
In conclusion, the neuroprotective effects of GABA may stem from its ability to improve long-term memory loss, support the proliferation of neuroendocrine cells, protect against neurotoxic-induced cell death, inhibit the proliferation and apoptosis of neuroblastoma cells, reduce ROS and oxidative stress levels, increase neuroplasticity and neurotrophic factor levels, and protect neuroendocrine cells.
4.2. Anti-Hypertension Activity
Hypertension, a condition where blood vessels are consistently under high pressure, typically arises from the narrowing or stiffening of the vessels [185]. Angiotensin-converting enzyme (ACE) plays a significant role in regulating blood pressure by converting angiotensin I to the potent vasoconstrictor angiotensin II; ACE inhibitors hinder this conversion, leading to vasodilation and consequently lowering blood pressure, thus proving effective in hypertension treatment [186,187,188]. It is noted that GABA found in foods fermented by LABs exhibits antihypertensive effects through ACE inhibitory activity, thereby playing a role in central blood pressure control in the cerebral renin-angiotensin system [20].
Skimmed milk fermented by the ND01 strain LAB demonstrated antihypertensive potential due to its high ACE inhibitor activities, with the Lactobacillus helveticus ND01 strain showing an ACE inhibitory activity of 67.18% [189]. GABA produced by Lactococcus lactis DIBCA2 and Lactiplantibacillus plantarum PU11 bacteria from fermented milk showed 0.70 ± 0.07 mg/mL ACE inhibitor activity [190]. Similarly, high ACE inhibitor activity has been observed in GABA produced by Lactiplantibacillus plantarum NTU 102 bacteria from fermented milk [191]. The production of 113.35 mg/L of GABA from skimmed milk by Lactobacillus helveticus has possible uses in the treatment of hypertension [187]. Additionally, 77.4 mg/kg of GABA obtained from milk fermentation with Lactiplantibacillus plantarum strain, when combined with other LABs, reaches a concentration of 144.5 mg/kg, thus providing an effective dosage for hypertensive effects [190]. Furthermore, yogurts containing GABA produced from Lactobacillus helveticus or Lacticaseibacillus rhamnosus have also shown antihypertensive effects [192].
The antihypertensive effects of GABA produced from fermented dairy products have been confirmed in rats [193,194] and humans [195,196]. In spontaneously hypertensive rats, after eight weeks of oral administration of GABA-enriched low-fat milk fermented by Lactiplantibacillus plantarum (80.6 mg/100 g), a decrease in systolic and diastolic blood pressure was observed [194]. Additionally, this effect of GABA from fermented milk was seen in another study involving both spontaneously hypertensive and normotensive rats [193]. In a study involving twenty-three adult men, daily consumption of 50 g of Cheddar cheese containing 16 mg of GABA prepared with Lactococcus lactis ssp. lactis strain over 12 weeks decreased 3.5 ± 2.8 mmHg in blood pressure and 5.5 ± 3.9 mmHg in systolic blood pressure [196]. Another randomized placebo-controlled study conducted in mildly hypertensive patients showed that supplementation of 10–12 mg of GABA in 100 mL of fermented milk significantly reduced blood pressure within 2 or 4 weeks [195].
It has been reported that GABA-enriched wheat-based fermented rice, fermented brown rice, and buckwheat exhibit a strong ACE inhibitory effect, with buckwheat’s maximum ACE inhibition percentage being 2.57 times higher than that of pure buckwheat [197,198,199]. Studies on GABA-enriched rice [199,200,201,202,203], idli [204], and purple sweet potatoes [205,206] have consistently shown antihypertensive effects in both humans and animals. It has been observed that GABA produced by Lactiplantibacillus plantarum MNZ from wheat-based fermented rice prevents the increase in blood pressure in spontaneously hypertensive rats. Additionally, a decrease in aortic endothelin-1 protein expression was observed in these rats [199]. It has been reported that supplementation of idli, a fermented rice and black lentil meal, significantly reduced systolic blood pressure in spontaneously hypertensive rats. The blood pressure-lowering effects of idli were attributed to reduced gene expressions of ET-1, HSP70, NF-κB, and iNOS in the aorta of spontaneously hypertensive rats [204]. In a randomized, double-blind, placebo-controlled clinical trial involving 39 mildly hypertensive adults, 150 g/day of GABA-enriched rice decreased morning blood pressure after the first week and between the sixth and eighth weeks compared to placebo rice [200]. GABA-enriched rice reduced blood pressure by approximately 20 mmHg in spontaneously hypertensive rats. However, it did not show a significant hypotensive effect in normotensive rats [201]. Similarly, the antihypertensive effect of GABA-rich brown rice has been demonstrated in spontaneously hypertensive rats [202,203]. Moreover, the blood pressure of patients with mild to moderate hypertension decreased significantly during daily consumption of 120 g of GABA-rich bread [207].
Research indicates that GABA derived from plant proteins such as beans, soybeans, and lentils exhibits high ACE inhibitor activity and has positive effects on hypertension [208,209,210,211]. Fermented soybeans with approximately 1.9 g/kg GABA produced by Levilactobacillus brevis were found to have higher ACE inhibitor activity than traditional soybeans [208]. Kimchi LABs fermented soybeans under optimized conditions, GABA content reached up to 1.3 mg/g and exhibited up to 43% ACE inhibitor activity [209]. An extract of 10.42 mg/g GABA obtained from fermented lentils showed a potent ACE inhibitor activity of 92% [211]. Significant systolic and diastolic blood pressure decreases were achieved in spontaneously hypertensive rats fed with GABA-enriched lentils [210]. On the other hand, the amount of GABA in foods needs to reach an effective dose for it to exhibit an antihypertensive effect. In a study evaluating the antihypertensive effects of eggplant, the GABA content in eggplants did not exhibit a hypotensive effect in spontaneously hypertensive rats [212].
GABA produced by purple sweet potato milk fermentation with LABs (Lactococcus acidophilus BCRC 14065, Lactococcus delbrueckii ssp. lactis BCRC 12256, and Lactococcus gasseri BCRC 14619) reduced both systolic and diastolic blood pressure. They showed positive effects on cardiac hypertrophy in spontaneously hypertensive rats [205,206]. Similarly, it has been shown that a GABA-rich tomato significantly reduces blood pressure in spontaneously hypertensive rats [213]. These findings confirm the ACE inhibitor activity of GABA found in fermented products and its ability to reduce blood pressure, supporting the consideration of fermented products as a potential alternative or adjunct therapy in hypertension management.
4.3. Management of Stress and Sleep
Insomnia, characterized by difficulty initiating sleep, poor sleep quality, and impaired daytime functioning, adversely affects individuals’ quality of life, mood, cognitive function, and health [214]. In individuals experiencing insomnia, GABA’s inhibitory function may be impaired, and reduced expression levels of GABAA receptor α1 and α2 subunit mRNA may indicate sleep disorders [215].
Research on the effectiveness of GABA in reducing stress and improving sleep quality has yielded mixed results. While in a recent study on 19 sleep-disorder patients who took 700 mg/day GABA supplementation, the sleep score did not exhibit a statistically significant difference [216], others, mostly in animals, have demonstrated its potential to increase sleep duration [120,217,218,219], reduced sleep latency [120,219], and enhanced sleep quality both in animal and human studies [169,220]. Oral administration of GABA-rich fermented milk with Levilactobacillus brevis to mice induced with sodium pentobarbital or sodium barbital has increased sleep duration and reduced sleep latency [120]. Another study on mice showed that GABA derived from fermented rice seed extracts prevented caffeine-induced sleep disturbances, increased sleep duration, and mildly neutralized anxiety-like behaviors [217]. The alleviation of fatigue following the consumption of GABA-containing beverages has been demonstrated in both rats [221] and humans [222,223]. Oral administration of GABA Maoyecha tea extracts at a low dose (0.83 g/kg) for 30 days has significantly increased sleep duration and reduced sleep latency via GABAergic neurotransmission in mice induced with sodium pentobarbital [219]. Another study found that high-dose (3.33 g/kg) intake of GABA-rich black tea extracts for 15 days significantly increased sleep duration and proportion in mice induced with sodium pentobarbital. However, it did not significantly affect sleep latency [218].
Stress and anxiety are standard emotional states that impact people’s lives. Stress emerges as a response to external stimuli and is characterized by increased adrenergic activity [224]. Anxiety, on the other hand, is a personal response to prolonged or excessive stress, often defined as intense tension, worry, or anxiety associated with future adverse events [225,226]. Stress and anxiety have physical, psychological, and behavioral symptoms that can affect daily life and sometimes lead to pathological conditions. Therefore, maintaining an optimal stress level is essential for sustaining normal life processes [227]. Stress and anxiety are typically treated with lifestyle changes, psychotherapy, antidepressants, and anxiolytics [228].
The pathophysiology of anxiety is not entirely clear; however, research has shown that alterations in the GABA system are effective and that GABA improves mood [168,229]. Since the GABA receptor is the active site of anxiolytic drugs, GABA participates in depression and anxiety processes [230,231]. Therefore, it has been suggested that anxiety and depressive disorders can be treated with antidepressant drugs that regulate GABAergic transmission or GABA receptors. Additionally, it is noted that GABA tends to be less addictive compared to other antidepressants [230,231]. Furthermore, evidence suggests that oral GABA supplementation, when reaching concentrations that can produce biological effects in the brain, positively influences mood and sleep biology and plays a role in stress, anxiety, and depression [180,232,233]. Hence, it is recommended that GABA-containing foods and beverages could offer an alternative to pharmaceuticals in alleviating these conditions.
Animal studies have indicated reduced psychological and physical stress in animals fed with GABA-containing foods [219,234,235]. Rats fed with fermented black soybean milk containing GABA and subjected to forced swimming tests exhibited antidepressant-like effects without showing side effects such as loss of appetite or weight loss [234]. GABA-rich monascus, found on fermented rice or other grains, improved the levels of monoamines in the hippocampus of rats subjected to forced swimming tests, indicating an antidepressant effect [235]. In mice fed with GABA (3.43 mg/kg) produced by Levilactobacillus brevis J1 bacteria from fermented milk of adzuki bean sprouts for ten days, a decrease in mild depression-like symptoms was observed along with increased social interaction and mental activities [138].
A study on adults suggested that GABA increases alpha waves, decreases beta waves, and increases IgA levels under stressful conditions, implying that GABA can provide relaxation and reduce anxiety in stressful conditions [223]. Additionally, it is noted that GABA found in foods and beverages has a stress-reducing effect on acute and chronic stress in adults [236]. Supplementation with GABA-enriched yeast extract has been reported to alter human cortical excitation and inhibition balance [237]. Moreover, in more than 65% of 20 women consuming approximately 80 g of defatted rice germ enriched with GABA, the most common mental symptoms observed before menopause and in old age were significantly improved [238]. Another study showed that a single dose of chocolate containing 28 g of GABA produced by Lactobacillus hilgardii K-3 bacteria had a stress-reducing effect [239]. In contrast to previous studies, Konno et al. found that, in adults with sleep problems, the combination of GABA (700 g/day) and L-theanine (200 mg/day) significantly improved the Pittsburgh Sleep Quality Index score and Fitbit Charge 5 sleep improvement scores. Nevertheless, the sleep score did not exhibit a statistically significant difference. It has been reported that this might be attributed to a significant quantity of missing data about sleep duration and stage variables [216].
Studies conducted on animals and humans have demonstrated the effectiveness of GABA-fortified tea in alleviating stress, anxiety, and depression and relieving insomnia [240,241,242,243]. In studies on mice with post-ischemic stroke depression, both intraperitoneal injection and oral administration of GABA green tea via gavage have been shown to reduce depressive behaviors in mice. These reductions were determined by increased climbing and swimming times and decreased immobility time in forced swimming and tail suspension tests [241,242,243]. Additionally, it has been found that GABA green tea may increase GABAergic neurotransmission in the brains of mice [242]. In a study involving thirty young male participants, GABA-fortified tea was observed to reduce both acute and chronic stress and increase parasympathetic activity, thereby slowing down the heart rate. Moreover, it was noted that this effect was more pronounced in participants with higher levels of chronic stress [240]. In light of all these reports, it can be concluded that GABA has positive effects on sleep regulation, stress, and anxiety; therefore, consuming GABA-containing foods and beverages may benefit health and well-being.
4.4. Pain Reduction
Pain is a natural defense mechanism of the body that arises from nociceptors and includes the interaction of several neuroanatomical and neurochemical systems [244]. The International Association for the Study of Pain defines pain as “an unpleasant sensory and emotional experience related to actual or potential damage to body tissues”. Pain, which has a widespread impact on millions of individuals globally, has challenges in terms of treatment and can significantly influence one’s emotional well-being, social life, and profession. Pain is a multifaceted phenomenon encompassing several aspects, such as nociception, emotions, cognition, and social factors. It is a subjective experience that varies from person to person [245].
The etiology of pain is classified as nociceptive, inflammatory, or neuropathic. Pain arises from the interplay between receptors, neurotransmitters responsible for regulating the sense of pain, emotions associated with pain, and memories. Acute pain is a warning mechanism that protects us from tissue damage. On the other hand, chronic pain lasts for 3–6 months or more. It is a continuous pain linked to injuries, disorders, or diseases such as arthritis, gastrointestinal disorders, inflammatory bowel diseases, diabetes, and tumor growth. Chronic pain may result from nerve fiber damage, causing alterations in neurotransmitter function [246]. Research has shown that chronic pain problems are common in the general population. Based on the latest findings by the Centers for Disease Control and Prevention, it has been determined that a significant number of 51.6 million people in the United States are currently experiencing chronic pain [247]. A comprehensive survey of 52 nations revealed that the incidence of pain was documented at 28% [248]. The complete understanding of the molecular and cellular pathways that underlie persistent pathological pain remains incomplete. There is a need for clinically proven, well-tolerated, and effective treatment methods for chronic pain.
Recent research indicates that the gut microbiota significantly affects pain regulation [249,250]. The gut microbiota synthesizes neuroactive compounds such as GABA, tryptophan, and its metabolites, serotonin, and catecholamines. These compounds can communicate with the host through receptors on gut cells or neurocrine pathways [251]. Inhibiting the activity of ion channels in sensory neurons and blocking the transmission of C- and A-afferent fibers in the dorsal root ganglion (DRG) is regarded as an essential approach to decreasing hypersensitivity, increasing excitability, and alleviating the persistence of pain. Gut microbiota mediators, which include metabolites (SCFAs), neurotransmitters (glutamate, GABA, 5-HT), and pathogen-associated molecular patterns (PAMPs), control the excitability of nociceptive DRG neurons that act on pain-related receptors or ion channels (e.g., TRLs, TRP channels, ionotropic and metabotropic glutamate receptors, GABA receptors). They also lessen the activation of immune cells that secrete proinflammatory cytokines (TNF-α, IL-1, IL-6) and chemokines (CCL2, CXCL1) [249]. SCFAs can modulate pain sensitization by binding to their receptor FFAR2/3, which in turn regulates the synthesis of TNF-α, IL-2, IL-6, IL-10, and chemokines (such as C-C motif chemokine ligand 2, CCL2) by leukocytes [252]. The various metabolic pathways indicate that the gut microbiota could potentially significantly impact the regulation of neuronal excitability in the peripheral nervous system during chronic pain.
The gut microbiota can produce neurotransmitters influencing pain signaling [253]. LAB species, including Lactobacillus spp., Lactococcus spp., Streptococcus spp., Bifidobacterium spp., and Bifidobacterium dentium, produce GABA by using enzymes to remove a carboxyl group from glutamate [12,254]. The activation of the GABAA receptor causes a chloride influx to cause hyperpolarization of the post-synaptic neuron. In contrast, GABAB receptor activation decreases the likelihood of presynaptic neurons to release neurotransmitters, especially glutamate [255,256]. This inhibits the triggering of a neuron’s action potential and the release of synaptic vesicles. Gabapentin, a structural analog of GABA, has been used in medical practice for many years to alleviate thermal and mechanical pain [257]. Gabapentin and pregabalin have shown analgesic properties in individuals with pancreatitis, irritable bowel syndrome (IBS), and inflammatory bowel disorders. Also, they can alleviate abdominal wall discomfort and concomitant fibromyalgia [258,259,260]. Metagenomic research has revealed decreased Lactobacillus and Bifidobacterium in individuals suffering from visceral hyperalgesia and IBS [261,262]. In vivo studies have demonstrated that probiotics, including strains from the Lactobacillus and Bifidobacterium families, have a positive effect on lowering visceral pain [263,264]. Lactobacillus and Bifidobacterium are species that express the enzyme glutamate decarboxylase β (GadB), which decarboxylates glutamate to GABA [265,266]. GABA is capable of relieving pain. However, more research is required to determine if certain types of microbes can make GABA or similar molecules, as well as what effects this signaling has on the development and relief of chronic pain.
4.5. Modulation of Glucose Homeostasis
Diabetes mellitus (DM) is a chronic, endocrine, and metabolic condition characterized by elevated glucose levels and linked to the disruption of carbohydrate metabolism, either due to insufficient insulin production or a failure of the utilization of insulin [267]. GABA and GABA-enriched products can potentially be valuable therapeutic agents for controlling impaired glucose homeostasis [268].
GABA may play a crucial role in the pancreatic islet by regulating hormone secretions, suppressing the immune response, enhancing the survival of β cells, and facilitating the conversion of pancreatic α cells into β cells [269]. Furthermore, GABA has demonstrated its involvement in the control of insulin and glucagon secretions and its role in protecting and regenerating β-cells and promoting neogenesis. GABA suppresses immunological activation and inflammation in individuals with diabetes mellitus, resulting in the management of glucose homeostasis and a decrease in diabetic complications. According to in vivo studies, GABA enhances the reproduction and number of human β-cells and promotes the activation of growth and survival mechanisms by initiating PI3-K/Akt activation in β-cell islets [270]. Hosseini Dastgerdi et al. [271] found that administering GABA can decrease hepatic insulin resistance in pregnant diabetic rats and their offspring. This effect is achieved by modulating the insulin signaling and gluconeogenesis pathways. Administration of GABA to pregnant diabetic rats for 12 weeks resulted in a considerable reduction in plasma glucose levels in both the rats and their offspring. Another study found that empagliflozin and GABA, as the only treatment in streptozotocin induced diabetic mice, had beneficial effects on the preservation or growth of β-cell mass [272].
GABA-rich foods have been shown in several studies to have antidiabetic properties. In recent years, several clinical and animal studies have demonstrated the effectiveness of pre-germinated foods in improving DM. One contributing factor to their efficacy is the positive impact on GABA levels [273,274]. Research demonstrated notable improvements in administering GABA-rich-germinated adzuki beans to mice with type 2 DM. Specifically, fasting blood glucose levels decreased and there were significant enhancements in HOMA-β and HOMA-IR scores [275]. Li et al. [121] treated mice with streptozotocin-induced type 2 DM with GABA-rich yogurt and observed that this increased blood insulin levels, HOMA-β (a measure of β-cell activity), and better insulin sensitivity. C57BL/6J mice produced by a high-fat diet + streptozotocin (STZ) showed a drop in fasting blood glucose levels and improved glycolipid metabolism when supplemented with GABA-enriched germinated adzuki bean [276]. It was reported that GABA-rich fermented camel milk produced by Levilactobacillus brevis showed hypoglycaemic activity and decreased postprandial blood glucose levels in STZ-induced C57BL/6J mice [277]. Additionally, it has been suggested that the production of GABA by LAB strains has a noticeable impact on lowering glucose and insulin levels in the bloodstream during in vivo trials. This suggests there is potential for using GABA in pharmaceutical and food applications to decrease the occurrence of type 1 DM [278]. Furthermore, GABA-enriched fermented foods may regulate blood glucose levels in rats with type 2 DM by decreasing the activity of antioxidant enzymes, including glutathione, catalase, and superoxide dismutase. In the short term (6 weeks), fecal microbiota transplantation from healthy donors can successfully alleviate peripheral insulin resistance in patients, as evidenced by decreased HbA1c and increased plasma GABA [279]. Researchers are currently seeking safer and more efficient alternatives for the treatment of DM, considering its growing global prevalence and the adverse effects of current treatments. The human gut microbiota serves as a potent reservoir of bacteria that produce GABA. Hence, investigating the modulation of gut bacteria that produce GABA has great promise for future study. Although more research both in vitro and in vivo has shown that GABA has anti-diabetic properties, there is presently inadequate clinical data to support the use of GABA or GABA-rich diets in the treatment of DM. As a result, more clinical research is necessary to confirm the potential of GABA as an anti-diabetic agent and explore the transplantation of GABA-producing gut microbiota into diabetic patients.
4.6. Immunoregulatory Effects
Inflammation is the immune system’s response to external stressors, including physical injury, UV irradiation, microbial invasion, and immunological responses, etc. [280]. Inflammation has been associated with the synthesizing of many proinflammatory agents, including cytokines, NO, PGE2, and TNF-α. The prevalence of autoimmune diseases and immune response-related conditions, such as DM type I, atherosclerosis, and obesity, is on the rise. However, there is a scarcity of novel therapeutic strategies for these ailments. A growing body of research has examined the immunomodulatory function of microorganisms since it was discovered that gut microbiota protects immunological homeostasis. The immunological activities of the host are regulated by GABA, which LABs produce. GABA has been shown as an anti-inflammatory agent, as it inhibits the synthesis of proinflammatory mediators and improves symptoms associated with inflammation. GABA acts as a neurotransmitter inhibitor and significantly modulates the immune system [13,24]. Han et al. [281] found that GABA had anti-inflammatory activity by suppressing the synthesis and expression of iNOS, IL-1β, and TNF-α in RAW 264.7 cells treated with LPS. GABA improved the reduction of overall healing duration and promoted early wound healing. It has been shown that in LPS-induced mouse macrophage RAW 264.7 cells, NO generation and NO synthase expression are suppressed by GABA-enriched sea tangle L. japonica extract [282]. GABA-rich germinated brown rice reduced the release of IL-8, MCP-1, and ROS from Caco-2 human intestinal cells stimulated by IL-1 and H2O2 [283].
GABA-rich fermented Aronia melanocarpa extract was found to have anti-inflammatory properties through immune response modulation in Balb/c mice and inhibition of proinflammatory cytokines in RAW 264.7 cells. The findings from the in vivo experiments demonstrated that consuming fermented Aronia melanocarpa extract, which is rich in GABA, significantly impacted various immune parameters. Specifically, oral administration of doses (125, 250, and 500 mg/kg body weight) for 21 days resulted in enhanced proliferation of splenocytes and lymphocytes. Moreover, there was an increase in the expression of CD4+ and CD8+ T-cells, while the levels of TNF-α and IL-6 were reduced in a dose-dependent manner [284]. Likewise, the anti-inflammatory properties of GABA-enriched fermented strawberry juice were assessed, and findings revealed that COX-2 gene expression in LPS-stimulated RAW 264.7 macrophages reduced TNF-α, IL-6, and CXCL1 levels in mice given intraperitoneal LPS [141]. The GABA-rich extract derived from the red microalgae Rhodosorus marinus has been found to have an adverse effect on the expression and release of the proinflammatory cytokine IL-1α in normal human keratinocytes that have been stimulated with phorbol myristate acetate. This suggests the extract can treat sensitive skin, atopy, and dermatitis [285].
4.1. 신경 보호
신경 조직 손상에 대한 염증 반응은 활성 산소 종(ROS), 일산화질소(NO), 사이토카인 등 다양한 염증 매개체의 방출을 유발하여 뇌 내 흥분성 및 억제성 신경전달물질 시스템 간의 전기적 활동 균형을 깨뜨립니다 [163,164]. 이 상태는 간질, 알츠하이머병, 뇌혈관 질환, 다발성 경화증, 파킨슨병, 신경감염, 불면증 등 다양한 신경학적 장애에 기여합니다[165,166,167].
GABA는 신경계에서 중요한 억제성 신경전달물질로, 정보 전달, 신경 발달, 신경학적 장애 조절에 핵심적인 역할을 합니다[168,169]. GABA가 다양한 질환에 미치는 영향은 중추 신경계와 주변 기관에 분포된 GABA의 신경 신호 전달과 다양한 수용체를 통해 수많은 기능을 조절하기 때문입니다 [20]. 뇌 내 GABA 농도 감소, GABAergic 시스템의 불균형, GABA 신경전달물질 활동의 변화는 이온 운반 기능 장애, 시냅스 연결 장애, 중추 신경계 조절 장애를 초래하는 것으로 관찰되었습니다 [170,171]. 또한 태아 발달 기간 중 저산소-허혈 사건으로 인한 GABA 기능의 영구적 손상이 학습 및 기억 장애의 발생으로 이어질 수 있다는 점이 지적되었습니다 [172].
GABA를 식이 보충제로서의 치료 효과는 광범위하게 연구되어 신경 퇴화를 억제함으로써 기억력과 인지 기능을 향상시키는 잠재력을 보여주었습니다 [50,150,173,174,175,176,177,178,179]. GABA 보충제가 간질 발작의 심각성을 줄일 수 있으며 뇌졸중 손상의 예방 또는 완화에 활용될 수 있다는 제안이 있습니다 [180,181]. 그러나 특정 연구에서는 뇌 허혈 시 GABA의 신경 보호 효과가 관찰되지 않았습니다 [182,183]. 쥐를 대상으로 한 연구에서, 초점성 뇌 허혈 후 GABA 운반체를 억제했을 때 유의미한 신경 보호 효과가 달성되지 않았습니다 [183]. 마찬가지로, 이전 연구와 일치하게, 쥐의 봉합 모델에서 허혈 후 기능적 또는 조직학적 측정에서 GABA는 유의미한 차이를 보이지 않았으며, 이는 신경 보호 효과가 없음을 나타냅니다 [182].
김치에서 분리된 Lentilactobacillus buchneri에 의해 생성된 GABA는 신경독성 유발 세포 사멸로부터 보호합니다 [50]. 또한 김치에서 분리된 다른 LAB인 Lactobacillus sakei B216에 의해 생성된 GABA는 인지 장애 쥐의 장기 기억력 저하를 개선하고 체외 신경내분비 PC-12 세포의 증식을 증가시켰습니다 [173]. GABA 함량이 증가된 사전 발아된 현미 추출물은 인간 신경모세포종 세포의 세포 사멸과 관련된 DNA 분열 및 세포 내 ROS 형성을 효과적으로 억제하여 세포 증식 및 세포 사멸을 유의미하게 감소시켰습니다 [174]발효 쌀 가루에 750.55 ± 26.03 mg GABA/100 g을 함유한 사료를 섭취한 쥐에서 관찰된 신경 보호 효과는 대뇌 피질과 소뇌 부위에서 항산화 효소인 슈퍼옥사이드 디스뮤타제와 카탈라제의 활성 증가 및 산화 스트레스 감소와 연관되었습니다 [175].
GABA가 풍부한 발효 해조류(Laminaria japonica)를 Levilactobacillus brevis BJ20으로 발효시킨 제품은 치매 모델 쥐와 노인에서 인지 기능 저하에 대한 보호 효과를 보여주었으며, 신경 가소성 향상 가능성을 시사했습니다 [176,177]. 또 다른 연구에서는 Levilactobacillus brevis BJ20로 발효된 GABA 풍부 발효 해조류가 중년 여성에서 치매 및 알츠하이머 병 위험 감소와 관련된 신경 영양 인자 수치를 효과적으로 증가시켰습니다 [184]. Lactiplantibacillus plantarum에서 생산된 GABA는 새로운 발효 병아리콩 우유에서 MnCl2로 유발된 손상으로부터 신경내분비 PC-12 세포를 보호하고 세포 생존율을 향상시켜 신경 보호 효과를 제공한다는 보고가 있습니다 [150].
결론적으로, GABA의 신경 보호 효과는 장기 기억력 저하 개선, 신경 내분비 세포 증식 지원, 신경 독성 유발 세포 사멸 방지, 신경모세포종 세포의 증식 및 사멸 억제, 활성산소종(ROS) 및 산화 스트레스 수준 감소, 신경 가소성 및 신경 영양 인자 수준 증가, 신경 내분비 세포 보호 등에서 기인할 수 있습니다.
4.2. 항고혈압 활성
고혈압은 혈관이 지속적으로 높은 압력에 노출되는 상태로, 일반적으로 혈관의 협착이나 경화로 인해 발생합니다 [185]. 안지오텐신 전환 효소(ACE)는 안지오텐신 I을 강력한 혈관 수축제인 안지오텐신 II로 전환함으로써 혈압 조절에 중요한 역할을 합니다; ACE 억제제는 이 전환을 방해하여 혈관 확장 효과를 유발하고 결국 혈압을 낮추며, 이는 고혈압 치료에 효과적임을 입증했습니다 [186,187,188]. LAB에 의해 발효된 식품에 함유된 GABA는 ACE 억제 활성을 통해 항고혈압 효과를 나타내며, 뇌의 레닌-안지오텐신 시스템에서 중앙 혈압 조절에 역할을 합니다 [20].
ND01 균주 LAB로 발효된 저지방 우유는 높은 ACE 억제 활성으로 인해 항고혈압 잠재력을 보여주었으며, Lactobacillus helveticus ND01 균주는 67.18%의 ACE 억제 활성을 나타냈습니다 [189]. Lactococcus lactis DIBCA2 및 Lactiplantibacillus plantarum PU11 박테리아가 발효 우유에서 생산한 GABA는 0.70 ± 0.07 mg/mL의 ACE 억제 활성을 나타냈습니다 [190]. 마찬가지로, Lactiplantibacillus plantarum NTU 102 박테리아가 발효 우유에서 생산한 GABA에서도 높은 ACE 억제 활성이 관찰되었습니다 [191]. Lactobacillus helveticus를 사용하여 탈지유에서 생산된 113.35 mg/L의 GABA는 고혈압 치료에 활용될 가능성이 있습니다 [187]. 또한 Lactiplantibacillus plantarum 균주로 발효된 우유에서 얻은 GABA 77.4 mg/kg은 다른 LABs와 결합 시 144.5 mg/kg의 농도에 도달하여 고혈압 효과에 효과적인 용량을 제공합니다 [190]. 또한, Lactobacillus helveticus 또는 Lacticaseibacillus rhamnosus로 생산된 GABA를 함유한 요거트는 항고혈압 효과를 나타냈습니다 [192].
발효 유제품에서 생산된 GABA의 항고혈압 효과는 쥐 [193,194]와 인간 [195,196]에서 확인되었습니다. 자발성 고혈압 쥐에서 Lactiplantibacillus plantarum으로 발효된 GABA 강화 저지방 우유(80.6 mg/100 g)를 8주간 경구 투여한 결과, 수축기 및 이완기 혈압이 감소했습니다 [194]. 또한 발효 우유에서 유래한 GABA의 이 효과는 자발성 고혈압 쥐와 정상 혈압 쥐를 포함한 다른 연구에서도 관찰되었습니다 [193]. 23명의 성인 남성을 대상으로 한 연구에서 Lactococcus lactis ssp. lactis 균주로 제조된 GABA 16mg을 함유한 체다 치즈 50g을 12주간 매일 섭취한 결과, 혈압이 3.5 ± 2.8 mmHg, 수축기 혈압이 5.5 ± 3.9 mmHg 감소했습니다 [196]. 경도 고혈압 환자를 대상으로 한 무작위 위약 대조 연구에서 발효 우유 100mL에 GABA 10–12mg을 보충한 결과, 2주 또는 4주 내에 혈압이 유의미하게 감소했습니다 [195].
GABA가 풍부한 밀 기반 발효 쌀, 발효 현미, 그리고 메밀은 강한 ACE 억제 효과를 나타내며, 메밀의 최대 ACE 억제율은 순수 메밀보다 2.57배 높았습니다 [197,198,199]. GABA 강화 쌀 [199,200,201,202,203], 이디리 [204], 및 자색 고구마 [205,206]에 대한 연구는 인간과 동물 모두에서 항고혈압 효과를 일관되게 보여주었습니다. 밀 기반 발효 쌀에서 Lactiplantibacillus plantarum MNZ에 의해 생성된 GABA가 자발성 고혈압 쥐의 혈압 상승을 방지한다는 것이 관찰되었습니다. 또한 이 쥐에서 대동맥 내 엔도테린-1 단백질 발현이 감소했다는 것이 관찰되었습니다 [199]. 발효 쌀과 검은 렌틸콩 가루로 만든 이드리가 자발성 고혈압 쥐의 수축기 혈압을 유의미하게 감소시켰다는 보고가 있습니다. 이드리의 혈압 강하 효과는 자발성 고혈압 쥐의 대동맥에서 ET-1, HSP70, NF-κB, 및 iNOS 유전자 발현 감소에 기인한 것으로 추정되었습니다 [204]. 39명의 경도 고혈압 성인 대상 무작위 이중 맹검 위약 대조 임상 시험에서 GABA 강화 쌀 150g/일을 섭취한 그룹은 위약 쌀 대비 첫 주 후 및 6~8주 사이에 아침 혈압이 감소했습니다 [200]. GABA 강화 쌀은 자발성 고혈압 쥐의 혈압을 약 20 mmHg 감소시켰습니다. 그러나 정상 혈압 쥐에서는 유의미한 혈압 강하 효과가 관찰되지 않았습니다 [201]. 마찬가지로, GABA가 풍부한 현미의 항고혈압 효과는 자발성 고혈압 쥐에서 입증되었습니다 [202,203]. 또한, 경도에서 중등도 고혈압 환자의 혈압은 매일 120g의 GABA가 풍부한 빵을 섭취한 후 유의미하게 감소했습니다 [207].
연구 결과, 콩, 대두, 렌틸콩 등 식물 단백질에서 유래한 GABA는 높은 ACE 억제 활성을 나타내며 고혈압에 긍정적인 영향을 미친다는 것이 밝혀졌습니다 [208,209,210,211]. Levilactobacillus brevis로 발효된 대두는 1.9 g/kg의 GABA를 함유하며 전통적인 대두보다 높은 ACE 억제 활성을 나타냈습니다 [208]. 최적화된 조건에서 김치 LABs로 발효된 대두는 GABA 함량이 최대 1.3 mg/g에 달했으며 최대 43%의 ACE 억제 활성을 나타냈습니다 [209]. 발효 렌틸콩에서 추출된 10.42 mg/g의 GABA는 92%의 강력한 ACE 억제 활성을 보였습니다 [211]. GABA가 풍부한 렌틸콩을 섭취한 자발성 고혈압 쥐에서 수축기 및 이완기 혈압이 유의미하게 감소했습니다 [210]. 반면, 식품 내 GABA의 양은 항고혈압 효과를 나타내기 위해 효과적인 용량에 도달해야 합니다. 가지의 항고혈압 효과를 평가한 연구에서, 가지의 GABA 함량은 자발성 고혈압 쥐에서 저혈압 효과를 나타내지 않았습니다 [212].
LAB(Lactococcus acidophilus BCRC 14065, Lactococcus delbrueckii ssp. lactis BCRC 12256, 및 Lactococcus gasseri BCRC 14619)로 발효된 자색 고구마 우유에서 생성된 GABA는 수축기 및 이완기 혈압을 모두 감소시켰습니다. 이들은 자발성 고혈압 쥐에서 심장 비대증에 긍정적인 효과를 나타냈습니다 [205,206]. 마찬가지로, GABA가 풍부한 토마토가 자발성 고혈압 쥐의 혈압을 유의미하게 감소시킨다는 것이 밝혀졌습니다 [213]. 이러한 결과는 발효 제품에 함유된 GABA의 ACE 억제 활성과 혈압 감소 능력을 확인하며, 고혈압 관리에서 발효 제품을 잠재적 대체 또는 보조 치료제로 고려하는 것을 지지합니다.
4.3. 스트레스 및 수면 관리
불면증은 수면 시작 어려움, 수면 품질 저하, 낮 시간 기능 장애로 특징지어지며, 개인의 삶의 질, 기분, 인지 기능, 건강에 부정적인 영향을 미칩니다 [214]. 불면증을 겪는 개인에서 GABA의 억제 기능이 손상될 수 있으며, GABAA 수용체 α1 및 α2 서브유닛 mRNA의 발현 수준 감소는 수면 장애를 나타낼 수 있습니다 [215].
GABA가 스트레스 감소와 수면 품질 개선에 미치는 효과에 대한 연구 결과는 혼합된 결과를 보여줍니다. 최근 19명의 수면 장애 환자를 대상으로 하루 700mg의 GABA 보충제를 복용한 연구에서 수면 점수는 통계적으로 유의미한 차이를 보이지 않았습니다 [216], 반면 주로 동물 연구에서는 수면 시간 증가 [120,217,218,219], 수면 지연 감소 [120,219], 동물 및 인간 연구에서 수면 품질 개선 [169,220]을 보여주는 결과가 보고되었습니다. 나트륨 펜토바르비탈 또는 나트륨 바르비탈로 유도된 쥐에게 GABA가 풍부한 발효 우유에 Levilactobacillus brevis를 투여한 결과, 수면 시간이 증가하고 수면 지연 시간이 감소했습니다 [120]. 또 다른 연구에서 발효 쌀 종자 추출물에서 유래한 GABA는 카페인이 유발한 수면 장애를 예방하고 수면 시간을 연장하며 불안 유사 행동을 경미하게 중화시켰습니다 [217]. GABA 함유 음료 섭취 후 피로 완화는 쥐 [221]와 인간 [222,223]에서 모두 입증되었습니다. 나트륨 펜토바르비탈로 유도된 쥐에게 GABA 마오예차 차 추출물을 저용량(0.83 g/kg)로 30일간 경구 투여한 결과, GABA 신경전달을 통해 수면 지속 시간을 유의미하게 증가시키고 수면 지연을 감소시켰습니다 [219]. 또 다른 연구에서는 나트륨 펜토바르비탈로 유도된 쥐에게 고용량(3.33 g/kg)의 GABA 풍부한 검은 차 추출물을 15일 동안 투여한 결과, 수면 시간과 비율이 유의미하게 증가했지만 수면 지연에는 유의미한 영향을 미치지 않았습니다 [218].
스트레스와 불안은 사람들의 삶에 영향을 미치는 표준적인 감정 상태입니다. 스트레스는 외부 자극에 대한 반응으로 발생하며, 부신피질 호르몬 분비 증가로 특징지어집니다 [224]. 반면 불안은 장기간 또는 과도한 스트레스에 대한 개인적 반응으로, 미래의 부정적 사건과 관련된 강렬한 긴장, 걱정, 또는 불안으로 정의됩니다 [225,226]. 스트레스와 불안은 신체적, 심리적, 행동적 증상을 동반하며 일상 생활에 영향을 미치고 때로는 병리적 상태로 이어질 수 있습니다. 따라서 정상적인 생명 과정을 유지하기 위해 최적의 스트레스 수준을 유지하는 것이 필수적입니다 [227]. 스트레스와 불안은 일반적으로 생활 방식 변경, 심리 치료, 항우울제, 불안 완화제로 치료됩니다 [228].
불안의 병리생리학은 완전히 명확하지 않지만, 연구 결과 GABA 시스템의 변화가 효과적이며 GABA가 기분을 개선한다는 것이 밝혀졌습니다 [168,229]. GABA 수용체는 항불안 약물의 활성 부위이므로 GABA는 우울증과 불안 과정에 참여합니다 [230,231]. 따라서 GABAergic 전달이나 GABA 수용체를 조절하는 항우울제 약물로 불안 및 우울 장애를 치료할 수 있다는 제안이 제기되었습니다. 또한 GABA는 다른 항우울제에 비해 중독성이 덜하다는 점이 지적되었습니다 [230,231]. 또한, 뇌에서 생물학적 효과를 유발할 수 있는 농도에 도달할 때 구강 GABA 보충이 기분과 수면 생리학에 긍정적인 영향을 미치고 스트레스, 불안, 우울증에 역할을 한다는 증거가 있습니다 [180,232,233]. 따라서 GABA를 함유한 식품과 음료가 이러한 증상을 완화하는 데 약물의 대안으로 제안되고 있습니다.
동물 연구에서는 GABA를 함유한 식품을 섭취한 동물에서 심리적 및 신체적 스트레스가 감소했다는 결과가 보고되었습니다 [219,234,235]. GABA를 함유한 발효 검은 콩 우유를 섭취한 쥐에게 강제 수영 테스트를 실시한 결과, 식욕 감소나 체중 감소와 같은 부작용 없이 항우울제 유사 효과를 나타냈습니다 [234]. 발효 쌀이나 다른 곡물에서 발견된 GABA가 풍부한 모나스쿠스는 강제 수영 테스트를 받은 쥐의 해마에서 모노아민 수치를 개선하여 항우울제 효과를 나타냈습니다 [235]. 아즈키 콩 싹 발효 우유에서 Levilactobacillus brevis J1 박테리아로 생산된 GABA (3.43 mg/kg)를 10일 동안 섭취한 쥐에서 경미한 우울증 유사 증상이 감소하고 사회적 상호작용 및 정신 활동이 증가했습니다 [138].
성인을 대상으로 한 연구에서 GABA는 스트레스 조건 하에서 알파 파를 증가시키고 베타 파를 감소시키며 IgA 수치를 증가시켜 스트레스 조건에서 이완을 제공하고 불안감을 줄일 수 있음을 시사했습니다 [223]. 또한 식품 및 음료에 함유된 GABA는 성인에서 급성 및 만성 스트레스에 대한 스트레스 감소 효과를 갖는 것으로 보고되었습니다 [236]. GABA가 풍부한 효모 추출물을 보충한 경우 인간 뇌피질의 흥분과 억제 균형이 변화한다는 보고가 있습니다 [237]. 또한, GABA가 풍부한 탈지 쌀 배아를 약 80g 섭취한 20명의 여성 중 65% 이상에서 폐경 전과 노년기에 가장 흔히 관찰되는 정신적 증상이 유의미하게 개선되었습니다 [238]. 또 다른 연구에서는 Lactobacillus hilgardii K-3 박테리아로 생산된 GABA 28g을 함유한 초콜릿의 단일 투여가 스트레스 감소 효과를 보였습니다 [239]. 이전 연구와 달리 Konno 등[240]은 수면 문제를 가진 성인에서 GABA (700g/일)와 L-테아닌 (200mg/일)의 조합이 피츠버그 수면 품질 지수(Pittsburgh Sleep Quality Index) 점수와 Fitbit Charge 5 수면 개선 점수를 유의미하게 개선했습니다. 그러나 수면 점수는 통계적으로 유의미한 차이를 보이지 않았습니다. 이는 수면 지속 시간과 단계 변수에 대한 데이터 부족이 원인일 수 있다는 보고가 있습니다 [216].
동물과 인간을 대상으로 한 연구에서 GABA 강화 차가 스트레스, 불안, 우울증을 완화하고 불면을 완화하는 데 효과적임을 입증했습니다 [240,241,242,243]. 뇌졸중 후 우울증을 가진 쥐를 대상으로 한 연구에서, 복강 내 주사 및 경구 투여를 통해 GABA 녹차를 투여한 결과 쥐의 우울 행동이 감소했습니다. 이 감소는 강제 수영 테스트와 꼬리 현수 테스트에서 등반 및 수영 시간 증가와 무동작 시간 감소로 확인되었습니다 [241,242,243]. 또한 GABA 녹차가 쥐의 뇌에서 GABA 신경전달을 증가시킬 수 있다는 것이 발견되었습니다 [242]. 30명의 젊은 남성 참가자를 대상으로 한 연구에서 GABA 강화 차는 급성 및 만성 스트레스를 감소시키고 부교감 신경 활동을 증가시켜 심장 박동수를 늦추는 것으로 관찰되었습니다. 또한 이 효과는 만성 스트레스 수준이 높은 참가자에서 더 두드러지게 나타났습니다 [240]. 이러한 모든 보고서를 고려할 때, GABA는 수면 조절, 스트레스 및 불안에 긍정적인 영향을 미치며, 따라서 GABA를 함유한 식품 및 음료를 섭취하는 것이 건강과 웰빙에 도움이 될 수 있다고 결론지을 수 있습니다.
4.4. 통증 감소
통증은 통각 수용체에서 발생하는 신체의 자연적인 방어 메커니즘으로, 여러 신경 해부학적 및 신경 화학적 시스템의 상호 작용을 포함합니다 [244]. 국제 통증 연구 협회(IASP)는 통증을 “신체 조직의 실제 또는 잠재적 손상과 관련된 불쾌한 감각적 및 정서적 경험”으로 정의합니다. 전 세계 수백만 명에게 영향을 미치는 통증은 치료에 어려움이 있으며, 개인의 정서적 웰빙, 사회적 생활, 직업에 크게 영향을 미칠 수 있습니다. 통증은 통각, 감정, 인지, 사회적 요인 등 여러 측면을 포함하는 다면적인 현상입니다. 이는 개인마다 다르게 경험되는 주관적인 현상입니다 [245].
통증의 원인은 통각성, 염증성, 신경병성으로 분류됩니다. 통증은 통각 수용체, 통각을 조절하는 신경전달물질, 통증과 관련된 감정, 기억 사이의 상호작용에서 발생합니다. 급성 통증은 조직 손상으로부터 우리를 보호하는 경고 메커니즘입니다. 반면 만성 통증은 3개월 이상 지속됩니다. 이는 관절염, 위장 장애, 염증성 장 질환, 당뇨병, 종양 성장 등과 같은 손상, 장애, 또는 질환과 관련된 지속적인 통증입니다. 만성 통증은 신경 섬유 손상으로 인해 신경전달물질 기능의 변화로 인해 발생할 수 있습니다 [246]. 연구 결과, 만성 통증 문제는 일반 인구에서 흔히 발생합니다. 미국 질병통제예방센터(CDC)의 최신 연구 결과에 따르면, 미국에서 현재 5,160만 명이 만성 통증을 겪고 있는 것으로 추정됩니다[247]. 52개국을 대상으로 한 포괄적인 조사에서는 통증 발생률이 28%로 기록되었습니다[248]. 지속적인 병리학적 통증의 분자적 및 세포적 기전을 완전히 이해하는 것은 아직 미완성 상태입니다. 만성 통증에 대한 임상적으로 입증된, 잘 견디며 효과적인 치료 방법이 필요합니다.
최근 연구는 장 미생물이 통증 조절에 크게 영향을 미친다는 것을 보여줍니다 [249,250]. 장 미생물은 GABA, 트립토판 및 그 대사산물인 세로토닌과 카테콜아민과 같은 신경활성 화합물을 합성합니다. 이 화합물은 장 세포의 수용체나 신경내분비 경로를 통해 호스트와 소통할 수 있습니다 [251]. 감각 신경의 이온 채널 활성을 억제하고 등쪽 뿌리 신경절(DRG)에서 C- 및 A-구심성 섬유의 전달을 차단하는 것은 과민성 감소, 흥분성 증가, 통증 지속 완화를 위한 필수적인 접근법으로 간주됩니다. 장 미생물 매개체는 대사산물(SCFAs), 신경전달물질(글루타메이트, GABA, 5-HT), 병원체 관련 분자 패턴(PAMPs)을 포함하며, 통증 관련 수용체나 이온 채널(예: TRLs, TRP 채널, 이온성 및 대사성 글루타메이트 수용체, GABA 수용체)에 작용하는 통각성 DRG 신경세포의 흥분성을 조절합니다. 또한 염증성 사이토킨(TNF-α, IL-1, IL-6)과 케모카인(CCL2, CXCL1)을 분비하는 면역 세포의 활성화를 감소시킵니다 [ SCFAs는 FFAR2/3 수용체에 결합하여 백혈구의 TNF-α, IL-2, IL-6, IL-10 및 화학유인물질(예: C-C 모티프 화학유인물질 리간드 2, CCL2) 합성을 조절함으로써 통증 감작을 조절할 수 있습니다 [252]. 다양한 대사 경로는 장내 미생물이 만성 통증 동안 말초 신경계의 신경 흥분성 조절에 잠재적으로 중요한 영향을 미칠 수 있음을 나타냅니다.
장내 미생물은 통증 신호에 영향을 미치는 신경 전달 물질을 생성할 수 있습니다 [253]. LAB 종(Lactobacillus spp., Lactococcus spp., Streptococcus spp., Bifidobacterium spp., Bifidobacterium dentium)은 글루타메이트에서 카르복실 그룹을 제거하는 효소를 사용하여 GABA를 생성합니다[12,254]. GABAA 수용체의 활성화는 포스트시냅스 신경세포의 과분극화를 유발하는 염화물 이온의 유입을 초래합니다. 반면, GABAB 수용체의 활성화는 전시냅신 신경세포가 신경전달물질, 특히 글루타메이트를 방출할 가능성을 감소시킵니다 [255,256]. 이는 신경세포의 활동 전위 유발과 시냅스 소포 방출을 억제합니다. GABA의 구조적 유사체인 가바펜틴은 열적 및 기계적 통증을 완화하기 위해 의료 분야에서 수십 년간 사용되어 왔습니다 [257]. 가바펜틴과 프레가발린은 췌장염, 과민성 대장 증후군(IBS), 염증성 장 질환을 가진 개인에서 진통 효과를 나타냈습니다. 또한 복벽 불편감과 동반된 섬유근육통을 완화시킬 수 있습니다 [258,259,260]. 메타게노믹 연구는 내장 과민증과 IBS를 앓는 개인에서 락토바실러스와 비피도박테리움의 감소가 관찰되었다고 보고했습니다 [261,262]. in vivo 연구에서 Lactobacillus와 Bifidobacterium 속의 균주를 포함한 프로바이오틱스가 내장 통증 감소에 긍정적인 영향을 미친다는 것이 입증되었습니다 [263,264]. Lactobacillus와 Bifidobacterium은 글루타메이트를 GABA로 탈카복실화하는 효소 글루타메이트 탈카복실화 효소 β (GadB)를 발현하는 종입니다 [265,266]. GABA는 통증을 완화하는 능력을 가지고 있습니다. 그러나 특정 미생물이 GABA 또는 유사 분자를 생성할 수 있는지, 그리고 이 신호 전달이 만성 통증의 발생과 완화에 어떤 영향을 미치는지 추가 연구가 필요합니다.
4.5. 글루코스 균형 조절
당뇨병(DM)은 혈당 수치 상승을 특징으로 하는 만성 내분비 대사 질환으로, 탄수화물 대사 장애로 인해 인슐린 생산 부족 또는 인슐린 작용 장애로 인해 발생합니다 [267]. GABA 및 GABA 함유 제품은 손상된 글루코스 균형을 조절하는 데 유용한 치료제로 잠재력을 가지고 있습니다 [268].
GABA는 췌장 섬에서 호르몬 분비 조절, 면역 반응 억제, β 세포 생존 증진, 췌장 α 세포에서 β 세포로의 전환 촉진 등을 통해 중요한 역할을 할 수 있습니다 [269]. 또한 GABA는 인슐린과 글루카곤 분비 조절, β 세포 보호 및 재생, 신생성 촉진에 관여하는 것으로 나타났습니다. GABA는 당뇨병 환자의 면역 활성화와 염증을 억제하여 혈당 균형을 관리하고 당뇨병 합병증을 감소시킵니다. in vivo 연구에 따르면 GABA는 인간 β 세포의 재생산과 수를 증가시키고, β 세포 섬에서 PI3-K/Akt 활성화를 통해 성장 및 생존 메커니즘을 활성화합니다 [270]. Hosseini Dastgerdi 등 [271]은 임신한 당뇨병 쥐와 그 후손에게 GABA를 투여하면 간 인슐린 저항성이 감소한다는 사실을 발견했습니다. 이 효과는 인슐린 신호전달 경로와 글루코네오제네시스 경로를 조절함으로써 달성됩니다. 임신한 당뇨병 쥐에게 12주간 GABA를 투여한 결과, 쥐와 그 후손의 혈장 포도당 수치가 크게 감소했습니다. 또 다른 연구에서는 스트렙토조토신으로 유도된 당뇨병 쥐에서 empagliflozin과 GABA를 단독 치료제로 투여했을 때 β-세포 질량의 유지 또는 증가에 유익한 효과가 있음을 발견했습니다 [272].
GABA가 풍부한 식품은 여러 연구에서 항당뇨병 효과를 나타냈습니다. 최근 몇 년간 임상 및 동물 연구에서 발아 식품이 당뇨병 개선에 효과적임을 입증했습니다. 이 효과의 주요 요인 중 하나는 GABA 수치에 미치는 긍정적인 영향입니다 [273,274]. 연구 결과, 제2형 당뇨병을 가진 쥐에게 GABA가 풍부한 발아 아즈키 콩을 투여했을 때 눈에 띄는 개선이 관찰되었습니다. 구체적으로, 공복 혈당 수치가 감소했으며 HOMA-β 및 HOMA-IR 점수가 유의미하게 개선되었습니다 [275]. Li 등 [121]은 스트렙토조토신으로 유도된 제2형 당뇨병을 가진 쥐에게 GABA 풍부한 요거트를 투여한 결과, 혈중 인슐린 수치, HOMA-β(β-세포 활동의 지표)가 증가했으며 인슐린 감수성이 개선되었습니다. 고지방 식이 + 스트렙토조토신(STZ)으로 유도된 C57BL/6J 쥐는 GABA 풍부 발아 적두를 보충했을 때 공복 혈당 수치가 감소하고 글리코리피드 대사 개선이 관찰되었습니다 [276]. Levilactobacillus brevis로 발효된 GABA 풍부한 낙타 우유가 STZ 유도 C57BL/6J 쥐에서 혈당 강하 활성을 보이고 식후 혈당 수치를 감소시켰다는 보고가 있습니다 [277]. 또한, LAB 균주에 의한 GABA 생산이 체내 실험에서 혈중 글루코스 및 인슐린 수치를 낮추는 데 유의미한 영향을 미친다는 제안이 있습니다. 이는 GABA를 제약 및 식품 응용 분야에서 제1형 당뇨병 발생을 감소시키는 데 활용할 잠재력이 있음을 시사합니다 [278]. 또한 GABA가 풍부한 발효 식품은 글루타티온, 카탈라제, 슈퍼옥사이드 디스뮤타제 등 항산화 효소의 활성을 감소시켜 제2형 당뇨병을 가진 쥐의 혈당 수치를 조절할 수 있습니다. 단기(6주) 연구에서 건강한 기부자로부터의 분변 미생물 이식술은 혈당 조절 지표인 HbA1c 감소와 혈장 GABA 증가를 통해 환자의 말초 인슐린 저항성을 성공적으로 완화시켰습니다 [279]. 연구자들은 당뇨병의 전 세계적 유병률 증가와 현재 치료법의 부작용을 고려해 더 안전하고 효율적인 치료법을 탐색 중입니다. 인간 장내 미생물은 GABA를 생산하는 세균의 강력한 저장고 역할을 합니다. 따라서 GABA를 생산하는 장내 세균의 조절을 연구하는 것은 미래 연구에 큰 잠재력을 가지고 있습니다. 체외 및 체내 연구에서 GABA가 항당뇨병 성질을 가지고 있음을 보여주는 연구가 더 많이 진행되었지만, 현재 당뇨병 치료에 GABA 또는 GABA 풍부한 식단을 사용하는 것을 뒷받침하는 임상 데이터는 부족합니다. 따라서 GABA의 항당뇨병제 잠재력을 확인하고 당뇨병 환자에게 GABA를 생성하는 장내 미생물 군집을 이식하는 것을 탐구하기 위해 추가적인 임상 연구가 필요합니다.
4.6. 면역 조절 효과
염증은 신체적 손상, 자외선 조사, 미생물 침입, 면역 반응 등 외부 스트레스 요인에 대한 면역계의 반응입니다. [280]. 염증은 사이토킨, NO, PGE2, TNF-α 등 많은 염증 유발 물질의 합성과 연관되어 있습니다. 제1형 당뇨병, 동맥경화증, 비만 등 자가면역 질환과 면역 반응 관련 질환의 유병률이 증가하고 있습니다. 그러나 이러한 질환에 대한 새로운 치료 전략은 부족합니다. 장내 미생물이 면역 균형을 보호한다는 사실이 밝혀진 후, 미생물의 면역 조절 기능에 대한 연구가 증가하고 있습니다. LAB(젖산균)이 생성하는 GABA는 호스트의 면역 활동을 조절합니다. GABA는 염증 매개체의 합성을 억제하고 염증 관련 증상을 개선함으로써 항염증 작용을 나타냅니다. GABA는 신경전달물질 억제제로 작용하며 면역 시스템을 크게 조절합니다 [13,24]. Han 등 [281]은 LPS로 처리된 RAW 264.7 세포에서 GABA가 iNOS, IL-1β, TNF-α의 합성과 발현을 억제함으로써 항염증 활성을 나타냈다고 보고했습니다. GABA는 전체 치유 기간의 단축을 촉진하고 조기 상처 치유를 촉진했습니다. LPS로 유도된 마우스 대식세포 RAW 264.7 세포에서 GABA가 풍부한 해조류 L. japonica 추출물이 NO 생성 및 NO 합성효소 발현을 억제한다는 것이 밝혀졌습니다 [282]. GABA가 풍부한 발아 현미는 IL-1과 H₂O₂로 자극받은 Caco-2 인간 장 세포에서 IL-8, MCP-1 및 ROS의 방출을 감소시켰습니다 [283].
GABA가 풍부한 발효된 Aronia melanocarpa 추출물은 Balb/c 마우스에서의 면역 반응 조절을 통해 항염증 효과를 나타냈으며, RAW 264.7 세포에서의 염증성 사이토카인 억제를 통해 이 효과를 확인했습니다. in vivo 실험 결과, GABA가 풍부한 발효된 Aronia melanocarpa 추출물을 섭취한 경우 다양한 면역 매개변수에 유의미한 영향을 미쳤습니다. 구체적으로, 21일 동안 체중당 125, 250, 500 mg의 용량을 경구 투여한 결과, 비장 세포와 림프구의 증식이 증가했습니다. 또한 CD4+ 및 CD8+ T 세포의 발현이 증가했으며, TNF-α 및 IL-6의 수준은 용량 의존적으로 감소했습니다 [284]. 또한 GABA가 풍부한 발효 딸기 주스의 항염증 효과가 평가되었으며, LPS로 자극받은 RAW 264.7 대식세포에서 COX-2 유전자 발현이 감소하고 TNF-α, IL-6, 및 CXCL1 수준이 감소한 것으로 나타났습니다 [141]. 붉은 미세조류 Rhodosorus marinus에서 추출된 GABA 풍부 추출물은 포르볼 마이리스테이트 아세테이트로 자극받은 정상 인간 각질세포에서 염증성 사이토킨 IL-1α의 발현과 분비에 부정적인 영향을 미치는 것으로 확인되었습니다. 이는 해당 추출물이 민감성 피부, 아토피, 피부염 치료에 효과적일 수 있음을 시사합니다 [285].
Table 4. In vitro and in vivo studies of the effects of GABA produced by LAB.
5. Conclusions
Some metabolites of LABs, which are the most commonly used microorganisms in the food industry, can also be used for similar purposes to improve food safety and quality. GABA, one of these metabolites known to be synthesized at different levels by many LABs, helps improve the taste, flavor, aroma, and texture of the food it contains, and increases protein digestibility. Moreover, it can extend the shelf life of foods by preventing the proliferation of pathogenic microorganisms. Foods with increased GABA content can be produced as a result of the fermentation of meat, grains, milk, fruits, vegetables, and legumes with LABs. With the demonstration of these advantages they provide to foods, the use of GABA-producing LABs in the food industry has attracted great attention in recent years. However, it should not be ignored that some microorganisms may cause spoilage in foods, and strains with high GABA efficiency and proven safety should be preferred.
The positive effects of GABA, produced by LABs and called postbiotic, on neuroprotection, improving sleep quality, alleviating depression, and relieving pain have accelerated efforts to increase GABA production. Moreover, considering the various health benefits of GABA-enriched foods such as antidiabetics, antihypertension, and anti-inflammatory, their use will become more widespread in the coming years.
On the other hand, it should not be ignored that during the fermentation of foods with some LABs, some toxic biogenic amines such as histamine and tyramine, which can have negative effects on health, may be produced. For this reason, more comprehensive studies involving in vitro and in vivo analyses and animal and human subjects should be conducted to identify LAB strains that do not form biogenic amines, have high GABA yield, and are safe. Moreover, the oral intake of GABA theoretically could cause food–drug interactions by increasing the sedative effect of barbiturates or benzodiazepines. On the other hand, GABA intake can alleviate the symptoms of barbiturate withdrawal. Also, it is important to mention that GABA intake through nutrition can regulate the lateral hypothalamus (the so-called hunger center) and thereby could positively influence obesity and overeating disorders.
In summary, this review draws attention to the synthesis of GABA produced from LABs, the factors affecting its synthesis, and efforts to improve GABA production, underlines its areas of use in the food industry and the benefits it provides to the foods it contains. Thus, it is predicted that this review article will pave the way toward serving for future studies on increasing GABA production and developing GABA-rich functional products.
5. 결론
식품 산업에서 가장 널리 사용되는 미생물인 LAB의 일부 대사산물은 식품 안전성과 품질 개선을 위해 유사한 목적으로 활용될 수 있습니다. LAB에 의해 다양한 수준에서 합성되는 대사산물 중 하나인 GABA는 식품의 맛, 향, 향기, 텍스처를 개선하고 단백질 소화율을 높입니다. 또한 병원성 미생물의 증식을 억제하여 식품의 유통기한을 연장합니다. LAB과 함께 육류, 곡물, 우유, 과일, 채소, 콩류 등을 발효시켜 GABA 함량이 증가한 식품을 생산할 수 있습니다. 이러한 장점을 식품에 제공하는 것이 입증됨에 따라, GABA를 생산하는 LAB의 식품 산업 활용은 최근 몇 년간 큰 관심을 끌고 있습니다. 그러나 일부 미생물이 식품의 부패를 유발할 수 있다는 점을 무시해서는 안 되며, 높은 GABA 효율과 안전성이 입증된 균주를 선호해야 합니다.
LAB에 의해 생성되는 GABA(포스트바이오틱스)의 신경 보호, 수면 품질 개선, 우울증 완화, 통증 완화 등 긍정적인 효과는 GABA 생산 증대 노력을 가속화하고 있습니다. 또한 GABA 강화 식품의 다양한 건강 혜택(항당뇨, 항고혈압, 항염증 등)을 고려할 때, 향후 몇 년간 그 활용이 더욱 확산될 것으로 예상됩니다.
반면, 일부 LABs로 발효된 식품에서 히스타민과 티라민과 같은 건강에 해로운 생물학적 아민이 생성될 수 있다는 점을 무시해서는 안 됩니다. 이 때문에 생물학적 아민을 생성하지 않으며 GABA 수율이 높고 안전한 LAB 균주를 식별하기 위해 체외 및 체내 분석을 포함한 동물 및 인간 대상 연구가 더 많이 진행되어야 합니다. 또한, GABA의 경구 섭취는 바르비투르산염이나 벤조디아제핀의 진정 효과를 증가시켜 식품-약물 상호작용을 유발할 수 있습니다. 반면, GABA 섭취는 바르비투르산염 금단 증상을 완화시킬 수 있습니다. 또한, 영양을 통해 GABA를 섭취하면 측두하수체(소위 식욕 중추)를 조절하여 비만 및 과식 장애에 긍정적인 영향을 미칠 수 있다는 점도 중요합니다.
요약하자면, 이 리뷰는 LAB에서 생성되는 GABA의 합성, 합성에 영향을 미치는 요인, GABA 생산 개선을 위한 노력에 주목하며, 식품 산업에서의 활용 분야와 함유 식품에 제공하는 이점을 강조합니다. 따라서 이 리뷰 논문은 GABA 생산 증대와 GABA 풍부 기능성 제품 개발을 위한 미래 연구의 기반을 마련할 것으로 예상됩니다.
Author Contributions
Conceptualization, M.A.I.; writing—original draft preparation, M.A.I., B.S., E.K., B.A. and M.N.Ç.; writing—review and editing, M.A.I., D.A., R.C. and F.B. visualization, B.S., E.K., B.A. and M.N.Ç.; supervision, M.A.I., D.A., R.C. and F.B. All authors have read and agreed to the published version of the manuscript.
Funding
This research received no external funding.
Institutional Review Board Statement
Not applicable.
Informed Consent Statement
Not applicable.
Data Availability Statement
No new data were created or analyzed in this study. Data sharing is not applicable to this article.
Conflicts of Interest
The authors declare no conflicts of interest.
References
- Ishangulyyev, R.; Kim, S.; Lee, S.H. Understanding food loss and waste—Why are we losing and wasting food? Foods 2019, 8, 297. [Google Scholar] [CrossRef] [PubMed]
- FAO. The State of Food and Agriculture 2020: Overcoming Water Challenges in Agriculture; FAO: Rome, Italy, 2020. [Google Scholar]