Re: 세포건강 지킴이 Exerkines in health, resilience and disease 2023 네이처!!!
작성자문형철작성시간25.08.17조회수168 목록 댓글 0

Nat Rev Endocrinol
. Author manuscript; available in PMC: 2023 May 1.
Published in final edited form as: Nat Rev Endocrinol. 2022 Mar 18;18(5):273–289. doi: 10.1038/s41574-022-00641-2
Exerkines in health, resilience and disease
Lisa S Chow 1, Robert E Gerszten 2, Joan M Taylor 3, Bente K Pedersen 4, Henriette van Praag 5, Scott Trappe 6, Mark A Febbraio 7, Zorina S Galis 8, Yunling Gao 8, Jacob M Haus 9, Ian R Lanza 10, Carl J Lavie 11, Chih-Hao Lee 12, Alejandro Lucia 13,14,15, Cedric Moro 16,17, Ambarish Pandey 18, Jeremy M Robbins 2, Kristin I Stanford 19, Alice E Thackray 20, Saul Villeda 21, Matthew J Watt 22, Ashley Xia 23, Juleen R Zierath 24,25, Bret H Goodpaster 26, Michael P Snyder 27
- Author information
- Article notes
- Copyright and License information
PMCID: PMC9554896 NIHMSID: NIHMS1829603 PMID: 35304603
The publisher's version of this article is available at Nat Rev Endocrinol
Abstract
The health benefits of exercise are well-recognized and are observed across multiple organ systems. These beneficial effects enhance overall resilience, healthspan and longevity. The molecular mechanisms that underlie the beneficial effects of exercise, however, remain poorly understood. Since the discovery in 2000 that muscle contraction releases IL-6, the number of exercise-associated signalling molecules that have been identified has multiplied. Exerkines are defined as signalling moieties released in response to acute and/or chronic exercise, which exert their effects through endocrine, paracrine and/or autocrine pathways. A multitude of organs, cells and tissues release these factors, including skeletal muscle (myokines), the heart (cardiokines), liver (hepatokines), white adipose tissue (adipokines), brown adipose tissue (baptokines) and neurons (neurokines). Exerkines have potential roles in improving cardiovascular, metabolic, immune and neurological health. As such, exerkines have potential for the treatment of cardiovascular disease, type 2 diabetes mellitus and obesity, and possibly in the facilitation of healthy ageing. This Review summarizes the importance and current state of exerkine research, prevailing challenges and future directions.
초록
운동의 건강 혜택은 널리 인정되며
다양한 장기 시스템에서 관찰됩니다.
이러한 유익한 효과는
전반적인 회복력, 건강 수명 및 수명을 향상시킵니다.
그러나
운동의 유익한 효과에 기초한 분자적 메커니즘은
여전히 잘 이해되지 않고 있습니다.
2000년 근육 수축이 IL-6를 방출한다는 발견 이후,
운동과 관련된 신호 분자의 수는 급격히 증가했습니다.
엑서카인은
급성 및/또는 만성 운동에 반응하여 분비되는 신호 전달 물질로,
내분비,
파라크린 및/또는 오토크린 경로를 통해 그 효과를 발휘합니다.
골격근(미오카인),
심장(카디오카인),
간(헤파토카인),
백색 지방 조직 (아디포카인),
갈색 지방 조직 (바프토카인) 및
뉴런 (뉴로카인)을 비롯한 수많은 기관, 세포 및 조직에서 분비됩니다.
엑서카인은
심혈관, 대사, 면역 및 신경 건강을 개선하는 데 잠재적인 역할을 합니다.
따라서
엑서카인은 심혈관 질환, 제2형 당뇨병 및 비만 치료에 잠재력이 있으며,
건강한 노화를 촉진할 가능성도 있습니다.
이 리뷰는
엑서카인 연구의 중요성과 현재 상태, 주요 과제 및 향후 방향에 대해 요약합니다.
Irrefutable evidence supports the importance of physical activity, exercise and cardiorespiratory fitness in the prevention and treatment of chronic diseases, such as cardiovascular disease, obesity, type 2 diabetes mellitus, cognitive decline and many cancers, while enhancing the immune system, healthspan, longevity and resilience1 (FIG. 1). Conversely, physical inactivity poses a major public health threat, as it is associated with increased mortality2 and a notable economic burden3. Moreover, the COVID-19 pandemic clearly reinforces the relevance of physical activity for health, due to the effects of COVID-19-related reductions in physical activity4 and increases in sedentary behaviour, especially due to COVID-19-related quarantine4. Moreover, physical inactivity is associated with increased risk of severe COVID-19 outcomes5.
신체 활동, 운동 및 심폐 기능의 중요성은
만성 질환(심혈관 질환, 비만, 제2형 당뇨병, 인지 기능 저하, 다양한 암 등)의 예방 및 치료에 있어
확실한 증거로 뒷받침되며,
면역 체계 강화, 건강 수명, 장수 및 회복력 향상에도 기여합니다1 (그림 1).
반면, 신체 활동 부족은
주요 공중 보건 위협으로 작용합니다.
또한 COVID-19 팬데믹은
COVID-19 관련 신체 활동 감소4 및 특히 COVID-19 관련 격리 조치로 인한 좌식 행동 증가로 인해
건강에 대한 신체 활동의 중요성을 명확히 강조했습니다.
또한 신체 활동 부족은 심각한 COVID-19 결과의 위험 증가와 연관되어 있습니다5.
Fig. 1 |. The systemic effects of exercise.
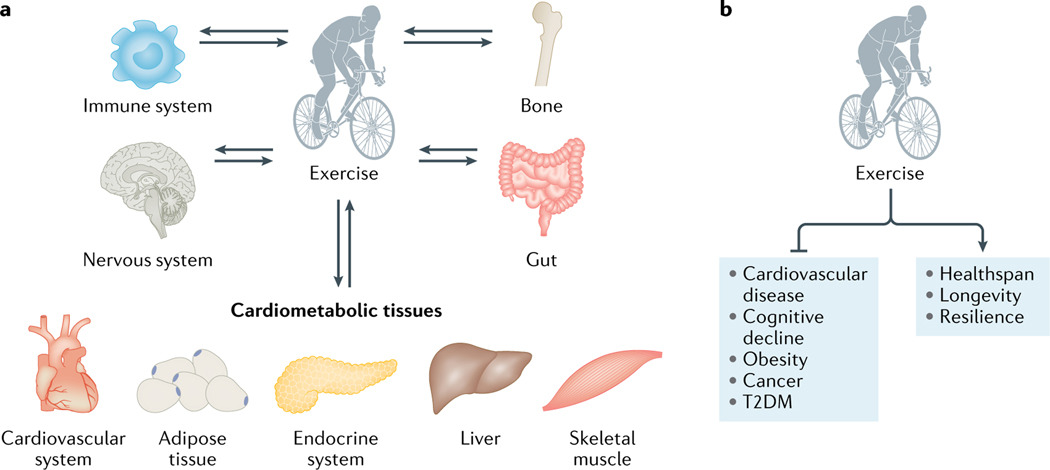
a | Organs and tissues that can serve as source of exerkines and that are directly affected by exercise. b | Exercise results in profound health benefits, including reductions in the presence or severity of certain diseases, as well as increases in healthspan, longevity and resilience. T2DM, type 2 diabetes mellitus.
Although the terms ‘exercise’ and ‘physical activity’ are commonly used interchangeably, exercise is typically regarded as intentional physical activity, such as aerobic training1, resistance training1 or high-intensity interval training6,7. By contrast, physical activity encompasses exercise as well as usual occupational and/or domestic activity1. Promoting physical activity remains a critical intervention to reduce the incidence and prevalence of common metabolic diseases. In the USA, official guidelines for physical activity were first published in 1995 and recommended that every US adult should accumulate at least 30 min of moderate intensity physical activity on most, preferably all, days of the week8. Subsequently, these guidelines have evolved1. In 2020, the World Health Organization stated that that all adults should aim for 150–300 min of moderate intensity physical activity per week or 75–150 min of vigorous intensity physical activity per week or an equivalent combination of moderate intensity and vigorous intensity physical activity per week9. Despite these recommendations, objective data obtained with accelerometers of physical activity in the US population indicated poor adherence to recommended guidelines, with only 5% of US adults having more than 30 min of moderate intensity physical activity per day10.
In this Review, we focus on the potential role of exerkines in driving the established benefits of exercise, such as preventing and mitigating disease, promoting health and increasing resilience. The term exerkine was coined in 2016 (REF.11), although the concept of humoral factors mediating the benefit of exercise has long been recognized. A prime example is lactic acid; its secretion from skeletal muscle was identified over 100 years ago12. In 1961, Goldstein speculated about the existence of a non-insulin humoral factor that regulates the effect of exercise on skeletal muscle and liver glucose utilization13. For the purposes of this Review, we define an exerkine as a signalling moiety released in response to acute exercise and/or chronic exercise, exerting its effects through endocrine, paracrine and/or autocrine pathways.
As skeletal muscle comprises approximately one third of body mass and has an important role in exercise14, the effects of physical activity (FIG. 1) were initially attributed to blood-borne factors, particularly muscle-secreted hormones (myokines)15. Of the myokines, IL-6 has been the most extensively studied since its discovery in 2000 (REF.16). Subsequent exerkine work has broadened to include exercise-related humoral factors arising from the heart (cardiokines), liver (hepatokines), white adipose tissue (WAT; adipokines) and brown adipose tissue (BAT; batokines) and the nervous system (neurokines), with local autocrine effects (affecting the cell of origin) and paracrine effects (affecting adjacent cells) (Table 1). Exerkines are increasingly recognized to include a broad range of signalling moieties, including cytokines, nucleic acids (microRNA17, mRNA and mitochondrial DNA), lipids and metabolites, which are frequently driven by cell-specific extracellular vesicle secretion18.
‘운동’과 ‘신체 활동’이라는 용어는 일반적으로 혼용되지만,
운동은 일반적으로 의도적인 신체 활동으로 간주되며,
예를 들어 유산소 운동1, 저항 운동1 또는 고강도 간격 운동6,7 등이 포함됩니다.
‘exercise’ and ‘physical activity’
intentional physical activity = 운동, exercise
반면 신체 활동은 운동뿐만 아니라
일상적인 직업적 및/또는 가정 내 활동을 포함합니다1.
신체 활동 촉진은
일반적인 대사 질환의 발생률과 유병률을 감소시키는 중요한 개입 수단으로 남아 있습니다.
미국에서는 1995년에 신체 활동에 대한 공식 지침이 처음 발표되었으며,
모든 미국 성인은 주간 대부분의 날, 가능하면
모든 날에 중간 강도의 신체 활동을 최소 30분 이상 누적하도록 권장했습니다8.
이후 이 지침은 발전되었습니다1.
2020년 세계보건기구(WHO)는
모든 성인이 주당 150–300분의 중간 강도 신체 활동 또는
주당 75–150분의 고강도 신체 활동 또는
중간 강도와 고강도 신체 활동의 동등한 조합을 주당 목표로 삼아야 한다고 밝혔습니다9.
이러한 권장 사항에도 불구하고,
미국 인구에서 가속도계를 통해 수집된 객관적 데이터는
권장 지침 준수율이 낮음을 보여주었습니다.
미국 성인의 5%만이
하루에 30분 이상의 중등도 강도 신체 활동을 수행한 것으로 나타났습니다10.
이 리뷰에서는
질병 예방 및 완화, 건강 증진, 회복력 향상 등
운동의 입증된 이점을 촉진하는 엑서카인의 잠재적 역할에 초점을 맞출 것입니다.
엑서카인이라는 용어는
2016년에 만들어졌지만(참고 문헌 11),
운동의 이점을 매개하는 체액 인자의 개념은 오랫동안 알려져 왔습니다.
대표적인 예로는 젖산이 있습니다. 젖산의 골격근 분비는 100년 이상 전에 발견되었습니다12. 1961년에 Goldstein은 골격근과 간에서 포도당 이용에 대한 운동의 효과를 조절하는 비인슐린 체액 인자의 존재를 추측했습니다13.
이 리뷰의 목적상,
엑서카인은 급성 운동 및/또는 만성 운동에 반응하여 분비되어
내분비, 파라크린 및/또는 오토크린 경로를 통해 효과를 발휘하는 신호 전달 단편으로 정의합니다.
골격근은
체중의 약 1/3을 차지하며 운동에 중요한 역할을 합니다14.
따라서
신체 활동의 효과(그림 1)는 초기에는 혈액 매개 인자,
특히 근육 분비 호르몬(마이오킨)에 기인한다고
여겨졌습니다15.
마이오킨 중에서는
2000년 발견 이후 가장 광범위하게 연구된
IL-6가 대표적입니다(참조16).
이후 엑서카인에 대한 연구는
심장(카디오카인), 간(헤파토카인),
백색 지방 조직(WAT, 아디포카인) 및 갈색 지방 조직 (BAT; 바토키네스) 및
신경계(신경키네스)에서 발생하는
운동 관련 체액성 요인을 포함하게 되었으며,
이는 국소적 자가지배 효과(원천 세포에 영향을 미치는)와
이웃 세포에 영향을 미치는 파라크린 효과를 포함합니다(표 1).
엑서카인은
사이토카인, 핵산(마이크로RNA17, mRNA 및 미토콘드리아 DNA),
지질 및 대사 산물 등 광범위한 신호 전달 분자를 포함하는 것으로 점점 더 인식되고 있으며,
이러한 분자는 세포 특이적인 세포외 소포 분비에 의해 자주 유도됩니다18.
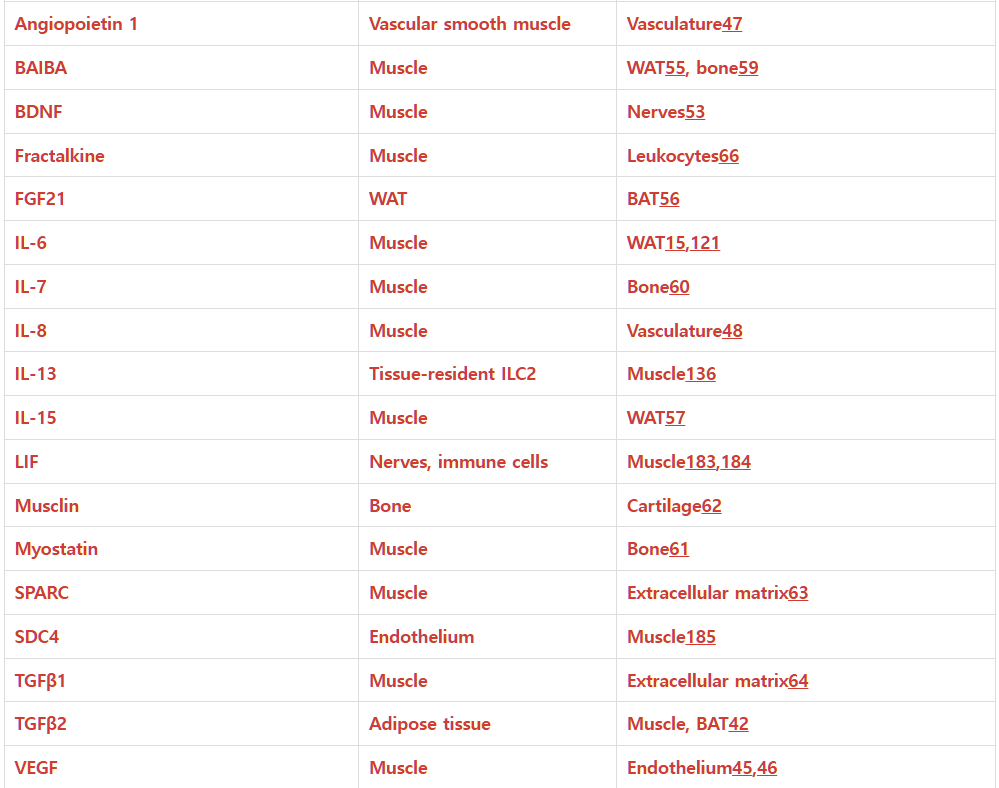
Table 1 |.
Examples of paracrine and autocrine effects of exerkines
Exerkinea Source tissue Affected tissue
| Autocrine effects b | ||
| 12,13-diHOME | - | BAT91,169 |
| Apelin | - | Muscle94,96 |
| Adiponectin | - | WAT153 |
| BDNF | - | Brain170, muscle171 |
| FGF21 | - | WAT56,172 |
| HSP72 | - | Muscle107,173 |
| IL-6 | - | Muscle15,54,120 |
| IL-7 | - | Muscle102 |
| IL-15 | - | Muscle174 |
| Lactate | - | Muscle175 |
| LIF | - | Muscle103 |
| Musclin (also known as osteocrin) | - | Muscle43,176, bone62,177, brain178 |
| Myostatin | - | Muscle44 |
| Nitric oxide | - | Endothelium179 |
| Reactive oxygen species | - | Muscle180 |
| SPARC | - | Muscle63,181 |
| SDC4 | - | Muscle104 |
| TGFβ1 | - | Muscle182 |
| Paracrine effects | ||
| Adiponectin | Adipose tissue | Muscle58 |
| Angiopoietin 1 | Vascular smooth muscle | Vasculature47 |
| BAIBA | Muscle | WAT55, bone59 |
| BDNF | Muscle | Nerves53 |
| Fractalkine | Muscle | Leukocytes66 |
| FGF21 | WAT | BAT56 |
| IL-6 | Muscle | WAT15,121 |
| IL-7 | Muscle | Bone60 |
| IL-8 | Muscle | Vasculature48 |
| IL-13 | Tissue-resident ILC2 | Muscle136 |
| IL-15 | Muscle | WAT57 |
| LIF | Nerves, immune cells | Muscle183,184 |
| Musclin | Bone | Cartilage62 |
| Myostatin | Muscle | Bone61 |
| SPARC | Muscle | Extracellular matrix63 |
| SDC4 | Endothelium | Muscle185 |
| TGFβ1 | Muscle | Extracellular matrix64 |
| TGFβ2 | Adipose tissue | Muscle, BAT42 |
| VEGF | Muscle | Endothelium45,46 |
12,13-diHOME, 12,13-dihydroxy-9Z-octadecenoic acid; BAIBA, β-aminoisobutyric acid; BAT, brown adipose tissue; BDNF, brain-derived neurotrophic factor; FGF21, fibroblast growth factor 21; HSP72, heat shock protein 72; ILC2, type 2 innate lymphoid cells; LIF, leukaemia inhibitory factor; SDC4, syndecan 4; SPARC, secreted protein acidic and rich in cysteine; TGFβ1, transforming growth factor-β1; TGFβ2, transforming growth factor-β2; VEGF, vascular endothelial growth factor; WAT, white adipose tissue.
a
Although exerkine effects are commonly thought to be distant (endocrine) from the originating tissue, exerkines also exert local effects within the originating tissue (autocrine) and neighbouring tissues (paracrine). More details and relevant references are provided in Supplementary Table 1.
b
For exerkines with autocrine effects, the source tissue is indicated as ‘–’, as the source tissue and affected tissue are the same.
Understanding the role of exerkines in the physiological and biological response to exercise is a principal objective of many investigations sponsored by the National Institutes of Health (NIH)19, given the demonstrated benefits of exercise in enhancing and prolonging human health across the lifespan. In 2020, the National Heart, Lung, and Blood Institute and the National Institute of Diabetes and Digestive and Kidney Diseases convened a virtual 2-day public workshop inviting 21 international experts to discuss “Exerkines in Health, Resilience, and Diseases”. The workshop executive summary was published online20, laying the foundation for this article. In this Review, we summarize the importance and current state of exerkine research, the prevailing challenges and future directions.
12,13-diHOME, 12,13-dihydroxy-9Z-octadecenoic acid; BAIBA, β-aminoisobutyric acid; BAT, 갈색 지방 조직; BDNF, 뇌유래 신경 영양 인자; FGF21, 섬유아세포 성장 인자 21; HSP72, 열 충격 단백질 72; ILC2, 유형 2 선천성 림프구 세포; LIF, 백혈병 억제 인자; SDC4, 신데칸 4; SPARC, 시스테인 풍부한 산성 분비 단백질; TGFβ1, 변형 성장 인자-β1; TGFβ2, 변형 성장 인자-β2; VEGF, 혈관 내피 성장 인자; WAT, 백색 지방 조직.
a 엑서카인의 효과는 일반적으로 원발 조직에서 멀리 떨어진 곳(내분비)에서 나타나는 것으로 알려져 있지만, 엑서카인은 원발 조직(자율 신경) 및 인접 조직(부신경) 내에서도 국소적인 효과를 발휘합니다. 자세한 내용과 관련 참고 문헌은 보충 표 1에 나와 있습니다.
b 자율 신경 효과를 가진 엑서카인의 경우, 원발 조직과 영향을 받는 조직이 동일하기 때문에 원발 조직은 '–'로 표시되어 있습니다.
운동이
인간의 건강을 향상시키고 수명을 연장하는 데 도움이 된다는 것이 입증됨에 따라,
운동에 대한 생리적 및 생물학적 반응에서 엑서카인의 역할을 이해하는 것은
국립보건원(NIH)이 후원하는 많은 연구의 주요 목표입니다19.
2020년에 국립 심장,
폐 및 혈액 연구소(National Heart, Lung, and Blood Institute)와
국립 당뇨병 및 소화기 및 신장 질환 연구소(National Institute of Diabetes and Digestive and Kidney Diseases)는
21명의 국제 전문가들을 초청하여 “건강, 회복력 및 질병에 대한 엑서카인”을 주제로
2일간의 가상 공개 워크숍을 개최했습니다.
워크숍의 요약본이
온라인으로20에 발표되어 이 기사의 토대가 되었습니다.
이 리뷰에서는
엑서카인 연구의 중요성과 현재 상태, 주요 과제 및 향후 방향에 대해 요약합니다.
Exercise response variability
Potential role for exerkines
The majority of exercise research has been limited to studies with genetically homogeneous animal models and/or small numbers of human participants. Moreover, the physiological response to a structured exercise training stimulus remains highly variable in humans and animals owing to a multitude of external and internal factors. In terms of external factors, the context of exercise matters, as exercise timing relative to circadian rhythms21, fed-fasting status22 or post-exercise dietary composition23 might influence metabolic outcomes. This variability is well-detailed in a study published in 2022, which included an atlas describing the time-dependent effects of exercise across multiple tissues after a single bout of treadmill exercise24. Addressing these external factors will require careful consideration of the exercise exposure, controlling the exercise exposure’s environmental context and serial sampling of blood and tissue prior, during and after exercise. This level of rigor is needed to ‘reduce the noise’ and facilitate interpretation of the temporal signatures of circulating and tissue-specific exerkines. In terms of internal factors, genetics have a critical role in the response to exercise. The Health, Risk Factors, Exercise Training and Genetics (HERITAGE) family study involved 20 weeks of supervised aerobic exercise training in 481 sedentary, healthy, white adults from 98 two-generation families, and found that the maximal heritability estimate for the aerobic capacity response was roughly 47%25. Furthermore, chronic exercise training elicited a ‘non-response’ in terms of improved aerobic capacity in ~20% of individuals25. In addition, 7–15% of individuals demonstrated an ‘adverse response’ regarding alterations in systolic blood pressure, as well as in fasting levels of HDL cholesterol, triglycerides and insulin25,26.
운동 반응의 다양성
엑서카인의 잠재적 역할
대부분의 운동 연구는 유전적으로 동질적인 동물 모델과/또는 소수의 인간 참가자를 대상으로 한 연구에 한정되어 왔습니다. 또한 구조화된 운동 훈련 자극에 대한 생리적 반응은 인간과 동물에서 다양한 외부 및 내부 요인으로 인해 매우 변동성이 큽니다.
외부 요인 측면에서 운동의 맥락이 중요하며,
운동 시간과 생체 리듬의 관계21,
식사 상태(식후/공복)22 또는 운동 후 식이 구성23이 대사 결과에 영향을 미칠 수 있습니다.
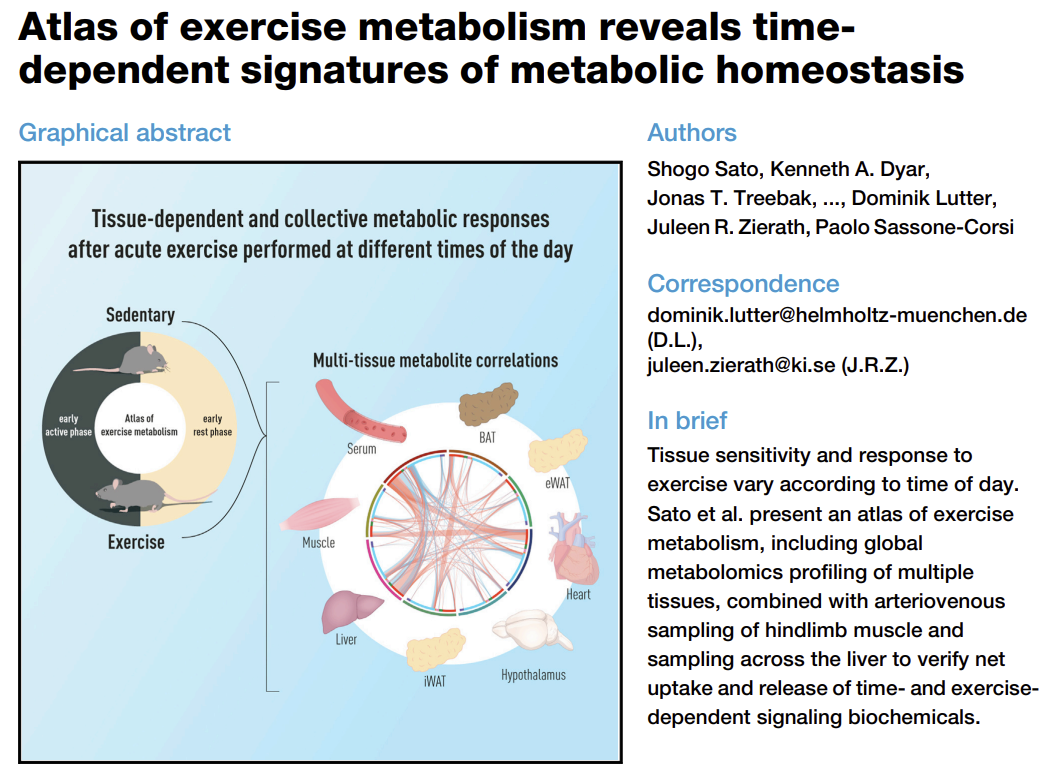
이 변동성은 2022년에 발표된 연구에서 상세히 설명되었으며,
이 연구는 단일 회차의 트레드밀 운동 후 여러 조직에서 운동의 시간 의존적 효과를 설명하는
아틀라스를 포함했습니다24.
https://www.cell.com/cell-metabolism/pdf/S1550-4131(21)00635-5.pdf
이러한 외부 요인을 해결하려면
운동 노출을 신중하게 고려하고,
운동 노출의 환경적 맥락을 통제하며,
운동 전, 운동 중 및 운동 후에 혈액과 조직을 연속적으로 채취해야 합니다.
이러한 수준의 엄격함은
‘노이즈를 줄이고’ 순환 및 조직별 엑서카인의 시간적 특징을 쉽게 해석하기 위해 필요합니다.
내부 요인의 측면에서,
유전학은 운동에 대한 반응에 중요한 역할을 합니다.
건강, 위험 요인, 운동 훈련 및 유전학(HERITAGE) 가족 연구는
98개 2세대 가족의 481명 비활동적 건강한 백인 성인을 대상으로
20주간의 감독 하에 진행된 유산소 운동 훈련을 포함했으며,
유산소 용량 반응의 최대 유전율 추정치는 약 47%였습니다25.
또한 만성 운동 훈련은
약 20%의 개인에서 유산소 능력 개선 측면에서 '비반응'을 유발했습니다25.
또한 7–15%의 개인은
수축기 혈압 변화, 공복 시 HDL 콜레스테롤, 트리글리세라이드 및 인슐린 수치 변화와 관련된
To drive the application of precision medicine to exercise, investigations into the mechanisms underlying the response variability to exercise are sorely needed. The contribution of exerkines to the variation in exercise response remains under active research and will be a key focus of the Molecular Transducers of Physical Activity Consortium (MoTrPAC; NCT03960827). This NIH-supported research consortium is designed to discover and broadly characterize the range of molecular transducers that underlie the variable effects of exercise in humans and animals. For humans, MoTrPAC has several unique features: its size (2,280 estimated participants); its recruitment of sedentary participants who will undergo a 12-week programme of aerobic exercise, resistance exercise or no exercise (control), with a comparison group of highly active endurance exercise or resistance exercise participants; and its time course analysis of changes in tissue (muscle and adipose tissue) and plasma metabolites19. In animals (~800 studied), the unique feature of MoTrPAC will be its focus on detailed biospecimen analysis across multiple time points and organs, which cannot be easily replicated in humans, in young (6 months) and old (18 months) male and female rats after an acute (single session) bout of treadmill exercise, or after chronic treadmill exercise (8 weeks) versus non-exercised control rats19. Identification of an exerkine or a panel of exerkines, which capture the benefits of exercise, would have potential implications for improving the health of those unable to exercise, such as those with ageing-associated exercise intolerance.
운동에 정밀 의학을 적용하기 위해 운동 반응의 변이성을 underlying하는 메커니즘에 대한 연구가 시급히 필요합니다. 운동 반응의 변화에 대한 엑서카인의 기여도는 여전히 활발한 연구 대상이며, Molecular Transducers of Physical Activity Consortium (MoTrPAC; NCT03960827)의 주요 연구 주제입니다.
NIH가 지원하는 이 연구 컨소시엄은
인간과 동물에서 운동의 다양한 효과의 기반이 되는 분자 변환기의 범위를 발견하고
광범위하게 특성화하기 위해 설계되었습니다.
인간을 대상으로 한 MoTrPAC은 다음과 같은 독특한 특징을 가지고 있습니다:
참가자 규모(추정 2,280명);
운동을 하지 않는 참가자를 모집하여 12주간의 유산소 운동, 저항 운동 또는
운동을 하지 않는 대조군(대조군)으로 나누어 진행하며,
고강도 내구 운동 또는 저항 운동을 하는 고활동군과 비교합니다;
조직(근육 및 지방 조직)과 혈장 대사물의 변화를
시간 경과에 따라 분석합니다19.
동물 (약 800마리 연구), MoTrPAC의 독특한 특징은
인간에서 쉽게 재현하기 어려운 젊은(6개월) 및 노령(18개월) 수컷과 암컷 쥐에서
급성(단일 세션) 트레드밀 운동 후 또는
만성 트레드밀 운동(8주) 후 운동을 하지 않은 대조군 쥐를 대상으로
다중 시간점 및 장기별 상세한 생체 시료 분석에 초점을 맞추는 점입니다19.
운동의 이점을 포착하는 엑서카인 또는 엑서카인 패널을 확인하면,
노화와 관련된 운동 불내증 등
운동이 불가능한 사람들의 건강을 개선하는 데 잠재적인 의미가 있을 것입니다.
Influence of exercise exposure
Exerkines are secreted in response to acute exercise, which is usually a single episode of either aerobic or resistance exercise. Chronic exercise is also associated with altered humoral factors, even in the resting state, suggesting that exerkine alterations can reflect the effects of chronic training27.
The acute exerkine response is influenced by the type of exercise, duration of exercise, underlying fitness, fed-fasting status and sample timing after exercise. In a human model, the blood concentration of glucose typically remains stable during acute exercise, with the liver releasing glucose for brain and skeletal muscle usage28. During exercise, skeletal muscle also uses lipid as fuel, which originates from the triglycerides stored in muscle and free fatty acids (FFAs) released from WAT29. The classic exerkines released during acute exercise, as found in human and animal models, include IL-6, IL-8, IL-1 receptor antagonist (IL-1RA) and IL-10. In a study in humans in which blood samples were collected before and after a marathon, plasma levels of several cytokines (IL-6, IL-1RA, IL-10 and tumour necrosis factor (TNF)) were higher than baseline levels when collected immediately after exercise, peaking 1–2 h after exercise and remaining elevated for ~4 h after exercise30. Certainly, the type and intensity of exercise matters. As an example, the exerkine response to high-intensity interval training depends on exercise intensity; higher exercise intensity corresponds with higher plasma levels of IL-6, while IL-10 levels remain unchanged compared with the levels before exercise6. Supplementary Table 1 shows examples of singular exerkine alterations. Currently, exerkine research is evolving from measuring singular exerkine changes to characterizing metabolic profiles31, for which challenges in analysis and interpretation remain (TABLE 2).
운동 노출의 영향
엑서카인은
급성 운동, 즉
일반적으로 단일 에피소드의 유산소 운동 또는 저항 운동에 반응하여 분비됩니다.
만성 운동은
휴식 상태에서도 체액 인자의 변화와 관련이 있으며,
이는 엑서카인의 변화가 만성 훈련의 효과를 반영할 수 있음을 시사합니다27.
급성 엑서카인 반응은
운동의 유형, 운동 시간, 기본 체력, 식후 또는 공복 상태, 운동 후 샘플 채취 시점 등에 의해 영향을 받습니다.
인간 모델에서,
급성 운동 중에는 혈중 포도당 농도가 일반적으로 안정적으로 유지되며,
간은 뇌와 골격근에 사용할 포도당을 방출합니다28.
운동 중에는 골격근도 연료로 지질을 사용하며,
이 지질은 근육에 저장된 트리글리세리드와 WAT에서 방출된
유리 지방산(FFA)에서 유래합니다29.
인간 및 동물 모델에서 발견된
급성 운동 중에 분비되는 전형적인 엑서카인에는
IL-6, IL-8, IL-1 수용체 길항제(IL-1RA) 및 IL-10이 있습니다.
인간을 대상으로 한 연구에서 마라톤 전후에 혈액 샘플을 채취한 결과,
운동 직후 채취된 혈장 내 여러 사이토카인(IL-6, IL-1RA, IL-10 및 종양 괴사 인자(TNF))의 농도는 기저치보다 높았으며,
운동 후 1–2시간에 정점을 찍고
운동 후 약 4시간 동안 높은 수준을 유지했습니다30.
물론 운동의 유형과 강도도
중요합니다.
예를 들어,
고강도 인터벌 트레이닝에 대한 엑서카인 반응은
운동 강도에 따라 달라집니다.
운동 강도가 높을수록
혈장 내 IL-6 수치가 높아지는
반면, IL-10 수치는 운동 전과 비교하여 변함이 없습니다6.
보충표 1은 단일 엑서카인 변화의 예를 보여줍니다. 현재 엑서카인 연구는 단일 엑서카인 변화의 측정에서 대사 프로파일의 특성화로 발전하고 있습니다31. 그러나 분석 및 해석에 대한 과제가 남아 있습니다 (표 2).
Table 2 |.
Common platforms for exerkine measurement
PlatformCommonly measured exerkinesAdvantagesDisadvantagesRefs
| Untargeted mass spectrometry | Lipidomics; metabolomics; proteomics | Profiles large numbers of molecules (>1,000 for metabolites and lipids; over 5,000 proteins); fairly inexpensive | Relative quantification rather than absolute quantification; bias towards abundant molecules; throughput lower than targeted assays | 31 |
| Targeted mass spectrometry | Lipidomics; metabolomics; proteomics | Accurate and absolute quantification; fast | Fewer molecules than untargeted assays | 31 |
| Immunoassays | Proteins (including cytokines) and metabolites | Accurate and absolute quantification; measures low-abundance molecules | Fewer molecules than untargeted assays | 31 |
| RNA-seq | Transcripts; splicing isoforms | Comprehensive (>10,000 genes); accurate absolute quantification | Does not reflect protein levels or protein modification | 31,33 |
| Methyl-seq | DNA methylation | Measures stable epigenome changes | Expensive | 31,33 |
| ATAC-seq | Open chromatin | Measures chromatin epigenome changes; easy to perform | Does not reflect RNA or protein expression levels | 31,33 |
ATAC-seq, assay for transposase-accessible chromatin using sequencing; Methyl-seq, methylation sequencing; RNA-seq, RNA sequencing.
Notably, the acute exerkine response does not necessarily parallel the chronic exerkine response (Supplementary Table 1). Typically, acute exercise exposure is associated with responses focused on the maintenance of metabolic homeostasis, with acute inflammation balanced by anti-inflammatory mediators30 and accommodating shifts in fuel utilization. By contrast, chronic exercise exposure is associated with responses focused on long-term metabolic adaptations and decreased inflammation27. However, when investigating chronic exercise exposure, the caveats of recent (24–72 hours prior to exercise) acute exercise or dietary composition, underlying fitness, fed-fasting status, circadian timing and training modality need to be considered. Moreover, the effects of exercise could also be influenced by alterations at the level of the exerkine receptor, in addition to alterations in plasma levels of exerkines. For example, in humans, chronic exercise training reduces plasma concentrations of IL-6; however, this effect could be partially mitigated by increased skeletal muscle mRNA expression of IL-6 receptor32.
특히,
급성 엑서카인 반응이
반드시 만성 엑서카인 반응과 평행하지는 않습니다 (보충표 1).
일반적으로 급성 운동 노출은
항염증 매개체에 의해 균형을 이루는 급성 염증30 및 연료 이용의 변화를 수용하는,
대사 항상성 유지에 집중된 반응과 관련이 있습니다.
반면, 만성 운동 노출은
장기적인 대사 적응과 염증 감소에 초점을 맞춘 반응과 연관됩니다27.
그러나
만성 운동 노출을 조사할 때,
최근(운동 전 24–72시간) 급성 운동이나 식이 구성, 기초 체력, 식사 상태, 생체 리듬, 훈련 방식 등의
제한 사항을 고려해야 합니다.
또한, 운동의 효과는
엑서카인 수치의 변화 외에도 엑서카인 수용체 수준의 변화에 의해 영향을 받을 수도 있습니다.
예를 들어,
인간에서 만성 운동 훈련은 혈장 내 IL-6 농도를 감소시킵니다.
그러나,
이 효과는 IL-6 수용체의 골격근 mRNA 발현 증가에 의해 부분적으로 완화될 수 있습니다32.
Exerkines: technical considerations
Discovery techniques
Exerkine research is increasingly focused on measuring changes across a broad swathe of factors rather than singular change. Specifically, interest is increasing in ‘omics’ technology to capture exercise-related changes in lipids (lipidomics), metabolites (metabolomics), proteins (proteomics), gene expression (transcriptomics) and DNA alterations (epigenomics)31 (TABLE 2). A paper in 2020 studied humans across the spectrum of insulin sensitivity (n = 36, ranging from people with high insulin sensitivity to patients with diabetes mellitus) who performed an acute bout of treadmill-based exercise to reach peak oxygen uptake. This exercise exposure altered >50% of measured molecules, spanning platforms based on lipidomics, metabolomics, proteomics, transcriptomics and epigenomics31. TABLE 2 lists commonly used platforms for exerkine analysis, including their relative advantages and disadvantages. Mass spectrometry is often used for targeted and untargeted omics analysis, whereas immunoassays are commonly used for analysis of proteins and metabolites. Genetic analyses include RNA sequencing, methylation sequencing (Methyl-seq) and assay for transposase-accessible chromatin with high-throughput sequencing (ATAC-seq)33. Together, these platforms provide a rich profile of the molecular and epigenomic changes that occur in response to acute and chronic exercise.
엑서카인: 기술적 고려 사항
발견 기술
엑서카인 연구는
단일한 변화보다는 광범위한 요인의 변화를 측정하는 데 점점 더 집중되고 있습니다.
특히,
운동과 관련된
지질(지질체학), 대사 산물(대사체학), 단백질(단백질체학), 유전자 발현(전사체학) 및
DNA 변화(후성 유전학)의 변화를 포착하는
‘오믹스’ 기술에 대한 관심이 증가하고 있습니다31 (표 2).
2020년 연구에서는
인슐린 민감도 스펙트럼 전반에 걸친 인간 대상(n = 36, 고인슐린 민감도부터 당뇨병 환자까지)이
트레드밀 기반 운동을 수행해 최대 산소 섭취량에 도달하도록 했습니다.
이 운동 노출은
지질체학, 대사체학, 단백질체학, 전사체학, 에피게노믹스 기반 플랫폼에서
측정된 분자의 50% 이상을 변화시켰습니다31.
표 2에는
엑서카인 분석에 일반적으로 사용되는 플랫폼과
그 상대적인 장단점이 나열되어 있습니다.
질량 분석법은
표적 및 비표적 오믹스 분석에 자주 사용되는 반면,
면역 분석법은
단백질 및 대사 산물의 분석에 일반적으로 사용됩니다.
유전 분석에는 RNA 시퀀싱, 메틸화 시퀀싱(Methyl-seq) 및 고처리량 시퀀싱을 이용한 트랜스포제이스 접근성 염색질 분석(ATAC-seq)이 포함됩니다33. 이러한 플랫폼을 함께 사용하면 급성 및 만성 운동에 반응하여 발생하는 분자 및 후성 유전학적 변화에 대한 풍부한 프로파일을 얻을 수 있습니다.
Extracellular vesicles
In the exerkine field, interest is also intensifying in the role of extracellular vesicles as important carriers of molecular signals and drivers of inter-organ crosstalk related to exercise18. Extracellular vesicles are membranous structures that are released from almost all cell types, with cell-specific profiles. They vary in size, ranging from 150 nm to 1,000 nm, and carry an assortment of material, including proteins, nucleic acids and lipids18,34. The content of extracellular vesicles reflects the unique and varied composition of the cells from which they are released. As an example of extracellular vesicles acting as an exerkine in humans, acute exercise increases plasma levels of various microRNAs after exercise, and chronic exercise increases various microRNAs in the resting state17, supporting the possibility of microRNAs exerting their endocrine effects via extracellular vesicle-based transport11,34.
Extracellular vesicles can be routinely isolated and profiled from cell culture media. Studying the molecular cargo of plasma-derived extracellular vesicles, however, remains uniquely challenging. Critical to extracellular vesicle analysis is the careful consideration of pre-analytical steps, including proper collection and isolation. Isolation techniques include ultracentrifugation (using a differential density gradient), ultrafiltration, size exclusion chromatography, high-resolution mass spectrometry, capillary electrophoresis, asymmetric-flow field-flow fractionation and immunoaffinity capture35. Moreover, contamination at the time of collection needs to be considered as extracellular vesicles can arise from ex vivo platelet activation36,37. A 2021 paper presented an optimized size-exclusion chromatography method for proteomic analysis of plasma-derived extracellular vesicles from platelet-poor plasma; this technique has greater precision than conventional extracellular vesicle techniques and demonstrates a distinct exosome protein cargo profile after acute exercise in humans37.
세포외 소포
엑서카인 분야에서는
운동과 관련된 분자 신호의 중요한 전달체이자
기관 간 교차 통신을 촉진하는 세포외 소포의 역할에 대한 관심도 높아지고 있습니다18.
세포외 소포는
거의 모든 세포 유형에서 방출되는 막 구조물로,
세포 특이적 프로파일을 가지고 있습니다.
크기는 150 nm에서 1,000 nm까지 다양하며,
단백질, 핵산, 지질 등 다양한 물질을 운반합니다18,34.
세포외 소포의 내용은
이를 방출한 세포의 독특하고 다양한 구성을 반영합니다.
인간에서 엑서카인 역할을 하는 세포외 소포의 예로,
급격한 운동은 운동 후 혈장 내 다양한 마이크로RNA의 농도를 증가시키고,
만성 운동은 휴식 상태에서 다양한 마이크로RNA를 증가시킵니다17.
이는 마이크로RNA가
세포외 소포를 통한 수송을 통해 내분비 효과를 발휘할 가능성을 뒷받침합니다11,34.
세포 배양 매체에서 세포외 소포를
일상적으로 분리하고 프로파일링하는 것은 가능합니다.
그러나
혈장 유래 세포외 소포의 분자적 화물을 연구하는 것은
여전히 독특한 도전 과제입니다.
세포외 소포 분석에서 중요한 것은
적절한 수집 및 분리 등 사전 분석 단계를 신중히 고려하는 것입니다.
분리 기술에는 차등 밀도 그라디언트를 사용한 초고속 원심분리, 초여과, 크기 배제 크로마토그래피, 고해상도 질량 분석법, 모세관 전기영동, 비대칭 유동 필드 플로우 분획법 및 면역 친화성 포집35가 포함됩니다. 또한 수집 시 오염을 고려해야 합니다. 세포외 소포는 체외 혈소판 활성화에서 발생할 수 있기 때문입니다36,37. 2021년 논문에서는 혈소판이 적은 혈장에서 유래한 혈장 유래 세포외 소포의 프로테오믹스 분석을 위한 최적화된 크기 배제 크로마토그래피 방법을 제시했습니다. 이 기술은 전통적인 세포외 소포 기술보다 높은 정밀도를 보여주며, 인간에서 급성 운동 후 엑소좀 단백질 화물 프로파일이 명확히 구분됩니다37.
Autocrine, paracrine and/or endocrine effects
Initially, exerkine research focused on changes in plasma levels of cytokines, especially before and after an acute exercise exposure30. The classic exerkines are cytokines, of which IL-6 has been the most extensively studied since its identification as a myokine in 2000 (REF.16). Subsequently, the field evolved into examining the endocrine effects of exerkines, where molecules secreted from the source tissue, traditionally viewed as skeletal muscle, affect distant tissues15. Especially within the past 15 years, interest has been increasing in the local effects of exerkines, either on the secreting tissue (autocrine) or the adjacent environment (paracrine)38 (TABLE 1), non-muscle exerkine sources39 (Supplementary Table 1) and exerkine profiling rather than on singular exerkine alterations31 (TABLE 2).
A common perception among the general scientific community is the view of exerkines as a cytokine exerting its effects in an endocrine fashion, affecting tissues distant from the originating tissue. Exerkines are not merely cytokines, however, as hormones, neurotransmitters or metabolites associated with exercise, such as catecholamines40, lactate41 or FFAs29, can also serve as exerkines with endocrine signalling potential42.
From an autocrine standpoint, exerkines affect their origin cells by coupling local energy balance to tissue growth and metabolic homeostasis (TABLE 1). For example, in skeletal muscle, myocytes secrete factors such as lactate41, musclin43 and myostatin44 that couple exercise to changes in mitochondrial biogenesis and myocyte substrate utilization.
Muscle and other highly metabolically active tissues can also secrete exerkines that exert local (paracrine) effects38. For example, muscle secretes vascular endothelial growth factor (VEGF)45,46, angiopoietin 1 (REF.47) and IL-8 (REF.48) to regulate tissue angiogenesis, modulate blood flow and increase nutrient availability to support tissue growth27,49–52 (TABLE 1). Exercise-related paracrine effects are also observed in the nervous system53, adipose tissue42,54–58, bone59–61, cartilage62, extracellular matrix63,64 and the immune system65,66.
autocrine, 파라크린 및/또는 내분비 효과
처음에 엑서카인 연구는
특히 급격한 운동 노출 전후의 혈장 내 사이토카인 농도의 변화에 초점을 두었습니다30.
고전적인 엑서카인은 사이토카인이며,
그 중 IL-6는 2000년에 미오카인으로 확인된 이후
가장 광범위하게 연구되어 왔습니다 (참고 문헌 16).
그 후,
이 분야는 엑서카인의 내분비 효과를 연구하는 방향으로 발전하여,
전통적으로 골격근으로 여겨지던 원천 조직에서 분비된 분자가
멀리 떨어진 조직에 영향을 미치는 현상이 밝혀졌습니다15.
특히 지난 15년 동안,
분비 조직(자크린) 또는 인접한 환경(파라크린)에 대한 엑서카인의
국소적 효과에 대한 관심이 증가하고 있습니다38 (표 1),
비근육 엑서카인 공급원39 (보충 표 1) 및 단일 엑서카인 변화보다는
엑서카인 프로파일링31 (표 2)에 대한 연구가 진행되고 있습니다.
일반 과학계에서 엑서카인은
내분비 방식으로 효과를 발휘하여
기원의 조직에서 멀리 떨어진 조직에 영향을 미치는 사이토카인으로 인식되고 있습니다.
그러나
엑서카인은 호르몬과 같은
단순한 사이토카인이 아닙니다.
운동과 관련된 신경 전달 물질이나
대사 산물도 내분비 신호 전달 가능성이 있는
엑서카인으로 작용할 수 있습니다42.
자각적 관점에서, 엑서카인은
국소 에너지 균형을 조직 성장 및 대사 항상성(표 1)에 연결하여
기원의 세포에 영향을 미칩니다.
예를 들어,
골격근에서 근육 세포는 젖산41, 무스클린43 및 미오스타틴44와 같은 인자를 분비하여
운동과 미토콘드리아 생성과 근육 세포 기질 이용의 변화를 연결합니다.
근육 및 기타 대사 활동이 활발한 조직도
국소(파라크린) 효과를 발휘하는 엑서카인을 분비할 수 있습니다38.
예를 들어,
안지오포이에틴 1(REF.47) 및 IL-8(REF.48)을 분비하여
조직 혈관新生을 조절하고 혈류량을 조절하며
영양소 가용성을 증가시켜 조직 성장을 지원합니다27,49–52 (표 1).
운동 관련 파라크라인 효과는
신경계53, 지방 조직42,54–58, 뼈59–61, 연골62, 세포외 기질63,64 및 면역계65,66에서도
관찰됩니다.
Tissue-specific exerkine relationships
The cardiovascular system
Physical activity reduces the risk of cardiometabolic disease and mortality. Although exercise mitigates traditional cardiovascular risk factors, such as obesity and dyslipidaemia, these benefits incompletely account for the effects of exercise on cardiometabolic health. Studies in both humans and animal models support a role for exerkines potentially enhancing cardiometabolic health (FIG. 2; TABLE 3; Supplementary Table 1). Exerkines could also oppose multiple mechanisms associated with cardiovascular disease, such as persistent systemic inflammation, dysregulated energy balance and fuel utilization. Furthermore, the enhanced angiogenesis associated with certain exerkines could mitigate ischaemia. Notably, exercise might improve endothelial function. As the vascular endothelium lies at the interface between blood and tissue, its wide-ranging distribution and strategic positioning supports its potential role as an initiator and recipient of exerkine-related effects. For example, interplay between the endothelium and established exerkines, such as nitric oxide52 and VEGF27, has been shown to influence vascular tone, inflammation, regeneration and thrombosis, and has an important role in cardiovascular and overall resilience67.
조직별 엑서카인 관계
심혈관계
신체 활동은
심혈관 대사 질환 및 사망 위험을 감소시킵니다.
운동은 비만 및 이상 지질 혈증과 같은 전통적인 심혈관 위험 요인을 완화하지만,
이러한 이점은 운동이 심혈관 대사 건강에 미치는 영향을 완전히 설명하지는 못합니다.
인간과 동물 모델에 대한 연구들은
엑서카인이 심혈관 대사 건강을 향상시킬 가능성이 있다는 것을 뒷받침합니다 (그림 2; 표 3; 보충 표 1).
엑서카인은
또한 지속적인 전신 염증, 에너지 균형 및 연료 이용의 조절 장애와 같은
심혈관 질환과 관련된 여러 메커니즘에 대항할 수도 있습니다.
또한,
특정 엑서카인과 관련된 혈관 신생 강화는
허혈을 완화할 수 있습니다.
특히,
운동은 내피 기능을 개선할 수 있습니다.
혈관 내피는 혈액과 조직의 경계면에 위치하기 때문에,
그 광범위한 분포와 전략적인 위치는 엑서카인 관련 효과의 개시자 및 수용체로서의 잠재적 역할을 뒷받침합니다.
예를 들어,
내피와 산화질소(Nitric oxide)52 및 VEGF27와 같은
확립된 엑서카인 사이의 상호 작용이
혈관 긴장도, 염증, 재생 및 혈전증에 영향을 미치고,
심혈관 및 전반적인 회복력에 중요한 역할을 하는 것으로 나타났습니다67.
Fig. 2 |. Examples of exerkines that affect the cardiometabolic system.
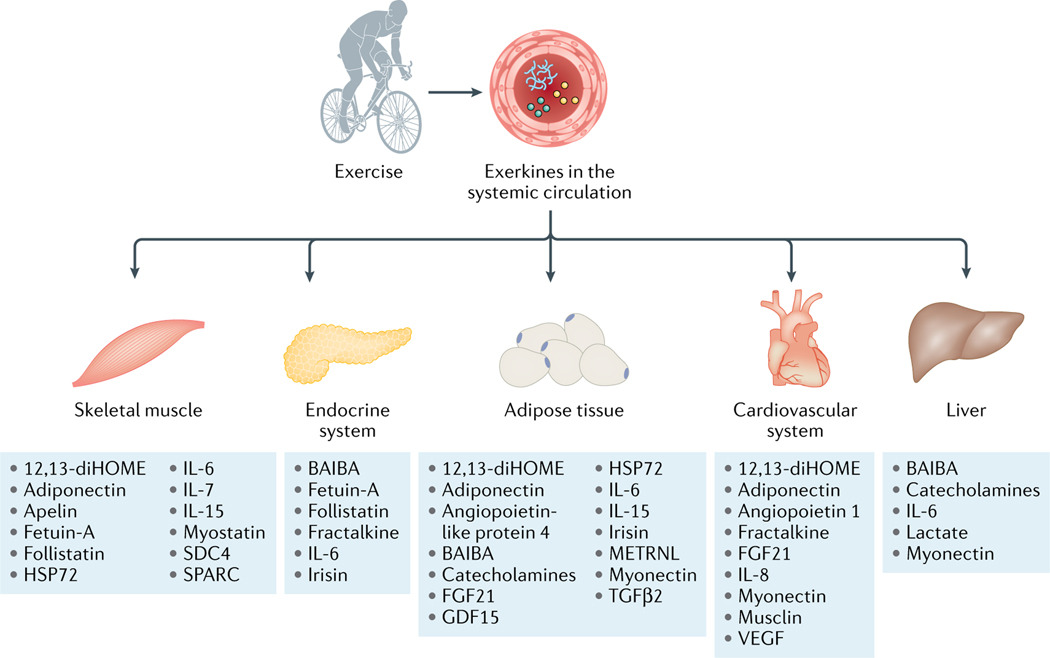
Exerkines released after exercise into the systemic circulation (see TABLE 3 for tissue sources, detailed effects and relevant references), including proteins (blue lines), metabolites (yellow circles) and extracellular vesicles (green circles), affect the cardiometabolic system. The effects are wide-ranging and systemic. In the cardiovascular system, exerkines enhance vascularization and angiogenesis, as well as improve blood pressure, endothelial function and overall fitness, resulting in cardioprotection. In adipose tissue, exerkines increase fatty acid uptake, enhancing lipolysis, thermogenesis and glucose metabolism. In the liver, exerkines enhance glucose metabolism and fatty acid uptake. In skeletal muscle, exerkines enhance muscle formation, maintenance and repair, glucose uptake, lipid oxidation, mitochondrial biogenesis and muscle capillarization. In the pancreas, exerkines enhance cell viability and influence insulin secretion. Commonly described exerkines are noted.
12,13-diHOME, 12,13-dihydroxy-9Z-octadecenoic acid; BAIBA, β-aminoisobutyric acid; FGF21, fibroblast growth factor 21; GDF15, growth and differentiation factor 15; HSP72, heat shock protein 72; METRNL, meteorin-like; SDC4, syndecan 4; SPARC, secreted protein acidic and cysteine rich; TGFβ2, transforming growth factor-β2; VEGF, vascular endothelial growth factor.
운동 후 전신 순환으로 방출되는 엑서카인(조직 출처, 자세한 효과 및 관련 참고 문헌은 표 3 참조)은
단백질(파란색 선), 대사 산물(노란색 원) 및 세포외 소포(녹색 원)를 포함하며,
심혈관 대사 시스템에 영향을 미칩니다.
그 효과는 광범위하고 전신에 걸쳐 나타납니다.
심혈관계에서 엑서카인은
혈관 신생 및 혈관 신생을 촉진하고,
혈압, 내피 기능 및 전반적인 체력을 개선하여 심장을 보호합니다.
지방 조직에서 엑서카인은
지방산 흡수를 증가시켜 지방 분해, 열 생성 및 포도당 대사를 향상시킵니다.
간에서 엑서카인은 포도당 대사와 지방산 흡수를 향상시킵니다.
골격근에서 엑서카인은
근육 형성, 유지 및 복구, 포도당 흡수, 지질 산화, 미토콘드리아 생합성 및 근육 모세관화를
향상시킵니다.
췌장에서 엑서카인은
세포의 생존력을 향상시키고 인슐린 분비에 영향을 미칩니다.
일반적으로 알려진 엑서카인이 언급되어 있습니다.
12,13-diHOME, 12,13-dihydroxy-9Z-octadecenoic acid; BAIBA, β-aminoisobutyric acid; FGF21, 섬유아세포 성장 인자 21; GDF15, 성장 및 분화 인자 15; HSP72, 열 충격 단백질 72; METRNL, 메테오린 유사; SDC4, 신데칸 4; SPARC, 분비형 산성 시스테인 풍부 단백질; TGFβ2, 변형 성장 인자-β2; VEGF, 혈관 내피 성장 인자.
Table 3 |.
Examples of exerkines that affect the cardiometabolic system
NameSpecies or modelaMain tissue of originMain target tissueEffectbMain biological actionResponse to acute exercise boutcResponse to chronic trainingcRefs
| 12,13-diHOME | H, A, C | BAT | BAT, skeletal muscle, heart | A, E | Increases fatty acid uptake | ↑ | ↑ | 91,93,169 |
| Adiponectin | H, A, C | WAT | Many tissues, including liver, muscle, heart | A, P, E | Enhances glucose and lipid utilization | ↑ | ↑,↔ | 58,153,186 |
| Angiopoietin I | H, A, C | Skeletal muscle | Vasculature | P | Enhances angiogenesis | ↑,↔ | ↑,↓ | 47,68,69 |
| Angiopoietin-like protein 4 | H, A | Liver, | WAT | E | Decreases lipoprotein lipase activity and enhance WAT lipolysis to increase plasma FFAs and triglycerides | ↑ | ↑,↔ | 39,68,79 |
| Apelin | H, A, C | WAT, skeletal muscle | Skeletal muscle, | A, E | Enhances skeletal muscle mass and mitochondria | ↑ | ↑,↔ | 94–96 |
| BAIBA | H, A, C | Skeletal muscle | WAT, Liver, β-cells | E, P | Enhances ‘browning’ of white adipocytes and β-oxidation in liver; attenuates insulin secretion from β-cells | ↑ | ↑ | 55,113,187 |
| Catecholamines | H | Adrenal | Skeletal muscle, WAT | E | Stimulates glycogenolysis; stimulates lipolysis of WAT | ↑ | ↔ | 40 |
| Fetuin-A | H | Liver | Skeletal muscle, pancreas | E | Impedes β-cell function; increases insulin resistance | ↓,↔ | ↓ | 39,72,97,101,115 |
| Fractalkine (also known as CX3CL1) | H, A, C | Skeletal muscle | Leukocytes, endothelium, myocytes, β-cells | P, E | Increases inflammatory, angiogenic, and chemotactic factors; regulates β-cell secretion | ↑ | ↔ | 66,70,71,114 |
| FGF21 | H, A | Many tissues, especially liver; also WAT | Many tissues, including heart and WAT | E, A, P | Augments fuel utilization (glucose, lipid); protects from apoptosis | ↑ | ↔ | 56,72,73,106,172,188 |
| Follistatin | H, A | Many tissues, especially liver | Skeletal muscle | E | Decreases serum levels of myostatin to enhance skeletal muscle growth; might affect glucose homeostasis | ↑ | ↑ | 39,97,98,100,116,189 |
| GDF15 | H, A | Many sites | Many sites | E | Marker of stress response, promotes WAT lipolysis | ↑ | ↑ | 80,190 |
| HSP72 | H, A | Many tissues, especially liver | Many sites | A, E | Maintains cellular homeostasis; protects cells from stress | ↑ | ↑ | 107,173 |
| IL-6 | H, A, C | Primarily skeletal muscle | Many sites | A, P, E | Multiple effects: including enhancing WAT lipolysis; lipid oxidation; glucose homeostasis; anti-inflammatory response; skeletal muscle growth | ↑ | ↓ | 15,16,30,78,81,119–121 |
| IL-7 | H, A, C | Skeletal muscle | Skeletal muscle, bone | A, P | Regulates skeletal muscle development | ↑ | ↔ | 102,191 |
| IL-8 | H, A, C | Skeletal muscle | Endothelium | P | Regulates tissue angiogenesis and blood flow | ↑,↔ | ↔ | 48,50,74 |
| IL-15 | H, A, C | Many tissues, especially immune cells | Many tissues, especially immune cells | A, P, E | Regulates immune cell functioning and might reduce WAT mass; improves glucose homeostasis; promotes skeletal muscle growth | ↑,↔ | ↔ | 57,99,174 |
| Irisin (also known as FNDC5) | H, A | Skeletal muscle | WAT, bone, β-cells, brain | E | Benefits primarily in animal models: increases fatty acid uptake; beiging of WAT; improves insulin secretion | ↑ | ↓,↔ | 84,117,167 |
| Lactate | H | Skeletal muscle | Many tissues, including central nervous system | A, E | Provides substrate for hepatic gluconeogenesis | ↑ | ↔ | 41,175 |
| METRNL | H, A, C | Many tissues, including WAT and skeletal muscle | Immune cells | E | Increases energy expenditure; improves glucose tolerance | ↑ | ↑ | 134,192,193 |
| Myonectin (CTRP15) | H, A | Skeletal muscle | Liver, WAT, heart | E | Promotes fatty acid uptake; might be cardioprotective | ↑,↔ | ↔ | 27,75,82,194 |
| Musclin (also known as osteocrin) | H, A, C | Skeletal muscle, bone, brain | Skeletal muscle, heart, vasculature, cartilage, brain | A, P, E | Regulates mitochondrial biogenesis and might exacerbate insulin resistance | ↑ | ↓ | 27,43,176,195 |
| Myostatin (also known as GDF8) | H, A, C | Many tissues, especially skeletal muscle and WAT | Many tissues, especially skeletal muscle and bone | A, P, E | Blunts skeletal muscle growth and glucose uptake | ↑,↔ | ↔ | 44,73,99,189 |
| SPARC | H, A, C | Many tissues | Many tissues | A, P, E | Regulates cell function and tissue remodelling | ↑,↔ | ↔ | 63,181 |
| SDC4 | H | Many tissues | Immune system | A, P, E | Involved in cell–extracellular matrix crosstalk, inflammation and skeletal muscle growth | ↑ | ↑ | 104,185,196,197 |
| TGFβ1 | H, A, C | Many tissues | Many tissues especially immune cells | A, P, E | Chemotactic factor for immune cells; affects skeletal muscle growth | ↑ | ↑ | 64,65,182,198,199 |
| TGFβ2 | H, A, C | Adipose tissue | Many tissues, especially muscle and immune cells | P, E | Promotes glucose and fatty acid metabolism; reduces inflammation | ↑ | ↑ | 42 |
| VEGF | H, A, C | Many tissues, especially skeletal muscle | Vascular endothelium | P, E | Promotes angiogenesis and exercise-induced neurogenesis | ↑,↔ | ↑ | 27,45,46 |
12,13-diHOME H, A, C BAT BAT, 골격근, 심장 A, E 지방산 흡수 증가 ↑ ↑ 91,93,169
아디포넥틴 H, A, C WAT 간, 근육, 심장 등 다양한 조직 A, P, E 포도당 및 지질 이용을 향상시킴 ↑ ↑,↔ 58,153,186
안지오포이에틴 I H, A, C 골격근 혈관 P 혈관新生을 촉진함 ↑,↔ ↑,↓ 47,68,69
안지오포이에틴 유사 단백질 4 H, A 간, WAT E 지단백질 리파아제 활성을 감소시키고 WAT 지방 분해를 촉진하여 혈장 FFAs 및 트리글리세라이드를 증가시킵니다. ↑ ↑,↔ 39,68,79
아펠린 H, A, C WAT, 골격근 골격근, A, E 골격근 질량 및 미토콘드리아를 증가시킵니다. ↑ ↑,↔ 94–96
BAIBA H, A, C 골격근 WAT, 간,
β-세포 E, P 백색 지방세포의 ‘갈색화’ 및 간에서 β-산화를 강화하고, β-세포에서 인슐린 분비를 약화시킵니다.
카테콜아민 H 부신 골격근, WAT E 글리코겐 분해를 자극하고 WAT의 지방 분해를 촉진 ↑ ↔ 40
페투인-A H 간 골격근, 췌장 E β-세포 기능을 방해; 인슐린 저항성을 증가 ↓,↔ ↓ 39,72,97,101,115
프랙탈킨 (CX3CL1이라고도 함) H, A, C 골격근 백혈구, 내피, 근육 세포,
β-세포 P, E 염증, 혈관 신생 및 화학 주성 인자를 증가시킵니다. β-세포 분비를 조절합니다. ↑ ↔ 66,70,71,114
FGF21 H, A 많은 조직, 특히 간; 또한 WAT 심장 및 WAT를 포함한 많은 조직 E, A, P 연료 이용률(포도당, 지질)을 증가시킴; 세포 사멸로부터 보호 ↑ ↔ 56,72,73,106,172,188
Follistatin H, A 많은 조직, 특히 간 골격근 E 혈청 내 마이오스타틴 수치를 감소시켜 골격근 성장 촉진; 포도당 균형에 영향을 미칠 수 있음 ↑ ↑ 39,97,98,100,116,189
GDF15 H, A 많은 부위 많은 부위 E 스트레스 반응의 지표, WAT 지방 분해 촉진 ↑ ↑ 80,190
HSP72 H, A 여러 조직, 특히 간 여러 부위 A, E 세포의 항상성을 유지하고 스트레스로부터 세포를 보호합니다. ↑ ↑ 107,173
IL-6 H, A, C 주로 골격근 여러 부위 A, P, E 여러 효과: WAT 지방 분해 촉진, 지질 산화, 포도당 항상성, 항염증 반응; 골격근 성장 ↑ ↓ 15,16,30,78,81,119–121
IL-7 H, A, C 골격근 골격근, 뼈 A, P 골격근 발달 조절 ↑ ↔ 102,191
IL-8 H, A, C 골격근 내피 P 조직 혈관 신생 및 혈류 조절 ↑,↔ ↔ 48,50,74
IL-15 H, A, C 여러 조직, 특히 면역 세포 여러 조직, 특히 면역 세포 A, P, E 면역 세포 기능을 조절하고 WAT 질량을 감소시킬 수 있음; 포도당 항상성을 개선함; 골격근 성장을 촉진함 ↑,↔ ↔ 57,99,174
이리신 (FNDC5라고도 함) H, A 골격근 WAT, 뼈,
β-세포, 뇌 E 주로 동물 모델에서 유익함: 지방산 흡수 증가; WAT의 베이지화; 인슐린 분비 개선 ↑ ↓,↔ 84,117,167
젖산 H 골격근 중추 신경계를 포함한 여러 조직 A, E 간 포도당 생합성에 필요한 기질을 공급 ↑ ↔ 41,175
METRNL H, A, C WAT 및 골격근을 포함한 여러 조직 면역 세포 E 에너지 소비를 증가시키고, 포도당 내성을 개선 ↑ ↑ 134,192,193
Myonectin (CTRP15) H, A 골격근 간, WAT, 심장 E 지방산 흡수 촉진; 심장 보호 효과 가능 ↑,↔ ↔ 27,75,82,194
Musclin (osteocrin이라고도 함) H, A, C 골격근, 뼈, 뇌 골격근, 심장, 혈관, 연골, 뇌 A, P, E 미토콘드리아 생성을 조절하고 인슐린 저항성을 악화시킬 수 있음 ↑ ↓ 27,43,176,195
미오스타틴 (GDF8라고도 함) H, A, C 여러 조직, 특히 골격근 및 WAT 여러 조직, 특히 골격근 및 뼈 A, P, E 골격근의 성장 및 포도당 흡수를 둔화시킵니다. ↑,↔ ↔ 44,73,99,189
SPARC H, A, C 여러 조직 여러 조직 A, P, E 세포 기능 및 조직 재구성을 조절합니다. ↑,↔ ↔ 63,181
SDC4 H 여러 조직 면역 체계 A, P, E 세포-세포외 기질 교차 통신, 염증 및 골격근 성장에 관여합니다. ↑ ↑ 104,185,196,197
TGFβ1 H, A, C 여러 조직 여러 조직, 특히 면역 세포 A, P, E 면역 세포의 화학유인인자; 골격근 성장에 영향을 미침 ↑ ↑ 64,65,182,198,199
TGFβ2 H, A, C 지방 조직 여러 조직, 특히 근육 및 면역 세포 P, E 포도당 및 지방산 대사 촉진; 염증 감소 ↑ ↑ 42
VEGF H, A, C 여러 조직, 특히 골격근 혈관 내피 P, E 혈관 신생 및 운동에 의한 신경 발생 촉진 ↑,↔ ↑ 27,45,46
12,13-diHOME, 12,13-dihydroxy-9Z-octadecenoic acid; BAIBA, β-aminoisobutyric acid; BAT, brown adipose tissue; CTRP15, complement C1q tumour necrosis factor-related protein 15; CX3CL1, chemokine (C-X3-C motif) ligand 1; FFAs, free fatty acids; FGF21, fibroblast growth factor 21; FNDC5, fibronectin type III domain containing 5; GDF8, growth and differentiation factor 8; GDF15, growth and differentiation factor 15; HSP72, heat shock protein 72; METRNL, meteorin-like; SDC4, syndecan 4; SPARC, secreted protein acidic and cysteine rich; TGFβ1, transforming growth factor-β1; TGFβ2, transforming growth factor-β2; VEGF, vascular endothelial growth factor; WAT, white adipose tissue.
a
Relevant species or models are human (H), animal (A) or cell (C).
b
Effects are autocrine (A), paracrine (P) or endocrine (E).
c
Arrows indicate: ↑, plasma levels increase; ↓, plasma levels decrease; ↔, plasma levels remain the same.
Contracting skeletal muscle produces many molecules that can enhance the cardiovascular system. Studies in humans15,45,68–74 and animal models15,43,49,75,76 have shown that the exerkines angiopoietin 1 (REFS49,68,69), fractalkine70,71, fibroblast growth factor 21 (FGF21)72,73, IL-6 (REF.15), IL-8 (REFS50,74), musclin43, myonectin75 and VEGF27,45,76 are generally increased with acute exercise; however, the exerkine response to chronic training, as measured by assessing exerkines in plasma during the resting state, can be quite variable and discrepant from the acute effects. As shown in TABLE 3 and Supplementary Table 1, examples include angiopoietin68,69, FGF21 (REFS73,77), fractalkine, IL-6 (REFS30,78) and IL-8 (REFS50,74).
수축하는 골격근은
심혈관 시스템을 강화할 수 있는 많은 분자를 생성합니다.
인간15,45,68–74 및 동물 모델15,43,49,75,76에 대한 연구에 따르면
엑서카인 안지오포이에틴 1 (REFS49,68,69),
섬유모세포 성장 인자 21 (FGF21)72,73,
IL-6 (REF.15), IL-8 (REFS50,74), musclin43, myonectin75 및 VEGF27,45,76은
일반적으로 급성 운동으로 증가하지만,
휴식 상태에서 혈장 내 엑서카인을 평가하여 측정된 만성 훈련에 대한 엑서카인 반응은
매우 다양하고 급성 효과와 불일치할 수 있습니다.
안지오포이에틴68,69, FGF21 (REFS73,77), 프랙탈킨,
IL-6 (REFS30,78) 및 IL-8 (REFS50,74)이 포함됩니다.
Adipose tissue
Exercise facilitates WAT lipolysis to provide FFA for utilization as fuel29. Although this lipolysis was typically attributed to adrenaline release40, acute exercise in humans also releases additional molecules79, such as growth and differentiation factor 15 (GDF15)80 and IL-6 (REF.81), which also affect lipolysis (TABLE 3; Supplementary Table 1). Lipolysis is not the only avenue by which exerkines can affect adipose tissue mass. For example, in myonectin knockout mice, WAT lipolysis is unaffected; however, dietary lipid clearance is impaired compared with lipid clearance in wild-type mice, resulting in increased WAT mass and decreased liver steatosis82.
A potential effect of exercise on WAT is ‘browning’, where WAT increases mitochondrial content, metabolic rate and heat production. WAT browning might have metabolic importance, as individuals with PET-CT-defined BAT had a decreased prevalence of cardiometabolic disease, particularly if they had overweight or obesity83. In a mouse model, fibronectin type III domain containing 5 is cleaved in the muscle cell and secreted as irisin, which induces WAT browning to increase energy expenditure and consequently reduce obesity84. Transgenic mice that overexpress muscle peroxisome proliferator-activated receptor-γ coactivator 1-α (PGClα) have higher circulating levels of irisin and increased WAT browning than control mice84. Hence, the initial excitement regarding irisin as an exerkine, as exercise generally increases muscle PGClα expression in both animal models85 and humans86.
As the irisin findings and exercise-induced browning of WAT concepts were re-evaluated in humans, the initial excitement was subsequently tempered. Although acute exercise in humans generally increases plasma levels of irisin87, the effect of chronic exercise training remains highly variable. A meta-analysis of several randomized controlled trials even showed lower levels of irisin after training than before training88. Trained athletes have lower BAT activity and no difference in WAT browning markers compared with lean, sedentary men89; this observation is supported by a study in humans of chronic exercise training, which did not find any browning of WAT (as assessed by biopsy)90. Thus, whether exercise can brown WAT in humans, especially through an irisin-mediated pathway, remains controversial55,83,84,90.
Adipose tissue can also secrete exerkines. A prime example is 12,13-dihydroxy-9Z-octadecenoic acid (12,13-diHOME), which is secreted from BAT and increases skeletal muscle oxidative capacity91. In humans, circulating levels of 12,13-diHOME are inversely associated with adipose tissue mass, fasting blood levels of insulin and blood levels of triacylglycerol92. A 2021 study showed that BAT transplantation in mice increased plasma levels of 12,13-diHOME and improved cardiac haemodynamics93. These findings suggest that a sustained increase in plasma levels of 12,13-diHOME preserves cardiac function and remodelling and increases cardiac haemodynamics through a direct effect on the cardiomyocyte. These findings were reinforced by observations in humans, in whom the presence of cardiovascular disease is associated with decreased plasma levels of 12,13-diHOME93.
Interestingly, skeletal muscle can influence the adipose tissue response to exercise via lactate secretion. The prototypical example is transforming growth factor-β2 (TGFβ2)42. In a mouse model, specific lactate exposure in vitro and in vivo increased adipocyte expression of TGFβ2 (REF.42). Furthermore, the same study found that in a mouse model of chronic exercise, increased adipocyte levels of TGFβ2 expression and secretion were associated with improvements in glucose metabolism, lipid oxidation and a possible reduction of adipose tissue inflammation. Parallel findings were also observed in humans undertaking chronic exercise, albeit to a less pronounced degree than the animal model observations42. Nevertheless, these findings demonstrate the possibility of lactate mediating tissue-to-tissue communication during exercise.
지방 조직
운동은
WAT의 지방 분해를 촉진하여 연료로 사용되는
자유 지방산(FFA)을 공급합니다29.
이 지방 분해는
일반적으로 아드레날린 분비에 기인한다고 여겨져 왔지만40,
인간에서 급성 운동은 추가 분자79(예: 성장 및 분화 인자 15(GDF15)80 및 IL-6(REF.81))를 분비하며,
이 분자들도 지방 분해에 영향을 미칩니다(표 3; 보충 표 1).
지방 분해는
엑서카인이 지방 조직의 질량에 영향을 미칠 수 있는 유일한 경로는 아닙니다.
예를 들어,
미오넥틴 녹아웃 마우스에서는 WAT 지방 분해는 영향을 받지 않지만,
식이 지질 제거는 야생형 마우스에 비해 지질 제거가 저하되어 WAT 질량이 증가하고 간 지방증이 감소합니다82.
운동이 WAT에 미치는 잠재적인 효과는
'브라우닝'으로, WAT가 미토콘드리아 함량, 대사율 및 열 생산을 증가시키는 현상입니다.
WAT 브라운닝은 대사적 중요성을 가질 수 있습니다.
PET-CT로 정의된 BAT를 가진 개인은
특히 과체중 또는 비만인 경우 심혈관 대사 질환의 유병률이 감소했습니다83.
마우스 모델에서 근육 세포에서 분해되어 분비되는 피브로네ктиן 유형 III 도메인 포함 5는 이리신을 생성하여 WAT 브라운닝을 유도해 에너지 소비를 증가시키고 결과적으로 비만을 감소시킵니다84. 근육 퍼옥시좀 증식제 활성화 수용체-γ 코액티베이터 1-α (PGClα)를 과발현하는 형질전환 마우스는 대조군 마우스에 비해 순환 이리신 수치가 높고 WAT 브라우닝이 증가했습니다84. 따라서, 운동은 동물 모델85과 인간86 모두에서 일반적으로 근육 PGClα 발현을 증가시키기 때문에, 엑서카인으로서의 이리신에 대한 초기 흥분이 일었습니다.
인간에서 이리신 연구 결과와 운동 유발 WAT 갈색화 개념이 재평가되면서 초기 기대는 점차 줄어들었습니다. 인간에서 급성 운동은 일반적으로 혈장 내 이리신 수치를 증가시킵니다87, 그러나 만성 운동 훈련의 효과는 매우 변동성이 큽니다. 여러 무작위 대조 시험의 메타분석은 훈련 후 이리신 수치가 훈련 전보다 낮다는 결과를 보여주었습니다88. 훈련받은 운동 선수는 마른 비활동적 남성보다 BAT 활동이 낮으며 WAT 갈색화 지표에서도 차이가 없습니다89; 이 관찰은 인간을 대상으로 한 만성 운동 훈련 연구에서도 생검을 통해 WAT 갈색화가 관찰되지 않았다는 결과로 뒷받침됩니다90. 따라서 인간에서 운동이 WAT를 갈색화할 수 있는지, 특히 이리신 매개 경로를 통해 가능할지는 여전히 논란의 여지가 있습니다55,83,84,90.
지방 조직은 또한 엑서카인을 분비할 수 있습니다. 대표적인 예로 12,13-디하이드록시-9Z-옥타데세노산(12,13-diHOME)이 있으며, 이는 BAT에서 분비되어 골격근의 산화 능력을 증가시킵니다91. 인간에서 12,13-diHOME의 혈중 농도는 지방 조직량, 공복 혈당 수치 및 트리아실글리세롤 혈중 농도와 역상관 관계를 보입니다92. 2021년 연구에서는 쥐에 BAT 이식을 통해 12,13-diHOME의 혈장 농도가 증가하고 심장 혈역학이 개선되었다는 결과가 나왔습니다93. 이러한 결과는 혈장 내 12,13-diHOME 수치의 지속적인 증가가 심근 세포에 대한 직접적인 영향을 통해 심장 기능과 재형성을 유지하고 심장 혈역학을 개선한다는 것을 시사합니다. 이러한 결과는 인간에서 심혈관 질환의 존재가 12,13-diHOME 혈장 수치 감소와 연관되어 있다는 관찰 결과로 강화되었습니다93.
흥미롭게도 골격근은 젖산 분비를 통해 지방 조직의 운동 반응에 영향을 미칠 수 있습니다. 대표적인 예는 변형 성장 인자-β2 (TGFβ2)42입니다. 쥐 모델에서 체외 및 체내에서 특정 젖산 노출은 지방 세포의 TGFβ2 발현을 증가시켰습니다 (REF.42). 또한 동일한 연구에서 만성 운동 마우스 모델에서 지방세포의 TGFβ2 발현 및 분비 증가가 포도당 대사 개선, 지방 산화 증가 및 지방 조직 염증 감소와 연관되었다고 보고되었습니다. 인간에서 만성 운동을 수행한 경우에도 유사한 결과가 관찰되었으나, 동물 모델에서의 관찰보다 덜 두드러졌습니다42. 그럼에도 불구하고 이러한 결과는 운동 중 조직 간 통신을 매개하는 젖산의 가능성을 보여줍니다.
Skeletal muscle
Exerkines originating from multiple tissues have demonstrated the capacity to improve skeletal muscle function and growth (TABLE 3; Supplementary Table 1). Apelin is an example of a myokine affecting muscle function. In both humans and animal models, exercise increases muscle mRNA levels of apelin94 and possibly serum levels of apelin95,96. In an animal model, skeletal muscle95,96 served as a source of apelin secretion, which improved skeletal muscle function in the setting of ageing, supporting the potential of apelin as a therapeutic to combat age-related sarcopenia94–96. Specifically in old mice, increased apelin exposure (by daily injection or skeletal muscle overexpression) stimulated muscle mitochondrial biogenesis, muscle protein synthesis and enhancement of muscle stem cells to stimulate muscle regeneration96. 12,13-diHOME is an example of a batokine with muscle effects. In both humans and mouse models, exercise facilitates BAT secretion of 12,13-diHOME, which enhances skeletal muscle FFA uptake and oxidation91. The hepatokines follistatin and fetuin-A also affect muscle function. For example, in both humans97–99 and mouse models100, acute exercise97,100 and chronic exercise98 increase liver-secreted follistatin, which has been reported to antagonize the effects of myostatin99. Decreased function of myostatin enhances skeletal muscle growth and improves whole-body glycaemic control44,99. Furthermore, fetuin-A worsens peripheral insulin resistance by reducing insulin signalling and glucose transporter type 4 trafficking39. Although acute exercise in humans does not alter plasma levels of fetuin-A97, chronic exercise might decrease plasma levels of fetuin-A72,101. Additional exerkines involved in muscle growth and development include the following: IL-7 (REF.102), IL-15 (REF.99), follistatin97, leukaemia inhibitory factor103, syndecan 4 (REF.104) and myostatin44,73.
골격근
여러 조직에서 생성되는 엑서카인은
골격근의 기능과 성장을 개선하는 능력이 입증되었습니다 (표 3; 보충 표 1).
아펠린은
근육 기능에 영향을 미치는 미오카인의 한 예입니다.
인간과 동물 모델 모두에서 운동은
아펠린의 근육 mRNA 수준94 및 아마도 혈청 아펠린 수준95,96을 증가시킵니다.
동물 모델에서 골격근95,96은 아펠린 분비의 원천으로 작용하여
노화 환경에서 골격근 기능을 개선했으며,
이는 아펠린이 노화 관련 근감소증 치료제로서의 잠재성을 뒷받침합니다94–96.
특히 노화 마우스에서 아펠린 노출 증가(일일 주사 또는 골격근 과발현을 통해)는
근육 미토콘드리아 생합성, 근육 단백질 합성 및 근육 줄기세포 활성화를 자극하여
근육 재생 촉진 효과를 나타냈습니다96.
12,13-diHOME은 근육에 영향을 미치는 바토킨의 예시입니다.
인간과 쥐 모델에서 운동은
BAT에서 12,13-diHOME 분비를 촉진하며,
이는 골격근의 자유 지방산(FFA) 흡수 및 산화를 증가시킵니다91.
간에서 분비되는 헤파토킨인 폴리스타틴과 페투인-A도 근육 기능에 영향을 미칩니다.
예를 들어, 인간97–99 및 쥐 모델100에서 급성 운동97,100 및 만성 운동98은 간에서 분비되는 폴리스타틴을 증가시키며, 이는 마이오스타틴의 효과를 억제하는 것으로 보고되었습니다99. 마이오스타틴 기능 저하는 골격근 성장과 전신 혈당 조절을 개선합니다44,99. 또한 페투인-A는 인슐린 신호전달과 글루코스 운반체 유형 4의 이동을 감소시켜 말초 인슐린 저항성을 악화시킵니다39. 인간에서 급성 운동은 페투인-A 혈장 농도를 변화시키지 않습니다97, 그러나 만성 운동은 페투인-A 혈장 농도를 감소시킬 수 있습니다72,101.
근육의 성장과 발달에 관여하는 추가적인 엑서카인에는
IL-7 (REF.102), IL-15 (REF.99), 폴리스타틴97, 백혈병 억제 인자103,
신데칸 4 (REF.104) 및 미오스타틴44,73이 있습니다.
The liver and the gut
Exercise reduces hepatic steatosis independently of weight loss105. The liver is recognized as a source for many circulating proteins, with ~2,500 liver-secreted proteins identified using modern liquid chromatography and mass spectroscopy technologies39. Not surprisingly, the liver is the source of many acute exercise-responsive cytokines (Supplementary Table 1). These exerkines affect glucose and/or lipid metabolism (for example, angiopoietin-like protein 4 in humans and animal models39,79), browning of WAT (FGF21 in a mouse model106), lipolysis (FGF21 in humans and a mouse model77) and the maintenance of cellular homeostasis (heat shock protein 72 in humans107).
Exercise also alters the gut microbiome108. Chronic exercise in humans and animal models alters the composition and functional capacity of the gut microbiota, independently of diet; these exercise-dependent changes in the microbiota might be independent of weight while being contingent on exercise intensity, modality and sustainment108. In humans, chronic exercise altered the gut microbiome to increase availability of short chain fatty acids, particularly butyrate109. Once these participants ceased training, exercise-induced changes in the microbiota were largely reversed when re-measured after a 6-week sedentary period109. The mechanisms by which exercise might alter the gut microbiome remain numerous, including altering the gene expression of intraepithelial lymphocytes for a more favourable inflammatory profile110, influencing blood flow in the gut111 or changing bile acid excretion112.
간과 장
운동은
체중 감소와 무관하게 간 지방증을 감소시킵니다105.
간은
많은 순환 단백질의 원천으로 알려져 있으며,
현대적인 액체 크로마토그래피와 질량 분광법 기술을 사용하여
약 2,500개의 간 분비 단백질이 식별되었습니다39.
예상대로,
간은 많은 급성 운동 반응성 사이토카인의 원천입니다 (보충 표 1).
이러한 엑서카인은 포도당 및/또는 지질 대사에 영향을 미칩니다(예: 인간 및 동물 모델에서 안지오포이에틴과 유사한 단백질 439,79), WAT의 갈변(마우스 모델에서 FGF21106), 지방 분해(인간 및 마우스 모델에서 FGF2177) 및 세포의 항상성 유지(인간에서 열 충격 단백질 72107).
운동은
장 미생물군집을 변화시킵니다108.
인간과 동물 모델에서 만성 운동은
식이 요인과 무관하게 장 미생물군집의 구성과 기능적 능력을 변화시킵니다.
이러한 운동 의존적 미생물군집 변화는
체중과 무관할 수 있지만
운동 강도, 유형 및 지속성에 따라 달라질 수 있습니다108.
인간에서 만성 운동은
장 미생물군집을 변화시켜
단쇄 지방산, 특히 부티레이트의 가용성을 증가시켰습니다109.
참가자들이 훈련을 중단한 후,
운동으로 인한 미생물군집 변화는 6주간의 활동 부족 기간 후 재측정 시 대부분 역전되었습니다109.
운동이 장내 미생물군집을 변화시키는 메커니즘은 다양하며,
상피 내 림프구의 유전자 발현을 변경하여 더 유리한 염증 프로필을 유도하는 것110,
장 내 혈류에 영향을 미치는 것111 또는 담즙산 배설을 변경하는 것112 등이 포함됩니다.
The endocrine system
As exercise has established benefits in improving dysglycaemia, this section focuses specifically on exerkines affecting glucose homeostasis (TABLE 3; Supplementary Table 1). In humans, circulating levels of β-aminoisobutyric acid (BAIBA) increased with chronic training55 and inversely correlated with insulin resistance55. In wild-type mice, BAIBA treatment reduced insulin resistance and suppressed inflammation55. In another study using C2C12 mouse myocytes and a wild-type mouse model (palmitate or high-fat diet exposure), BAIBA treatment attenuated insulin resistance, reduced inflammation and increased fatty acid oxidation through AMP-activated protein kinase (AMPK) and a AMPK-PPARδ-dependent pathway in skeletal muscle113. Limited human data show that an acute exercise bout increases plasma and muscle expression levels of fractalkine (encoded by CX3CL1)70, which is a chemokine that favourably regulates glucose-stimulated insulin secretion by enhancing β-cell function114. Chronic exercise in humans also reduces circulating levels of fetulin-A72,101. Fetulin-A has been shown to impair β-cell sensing by reducing glucose-stimulated insulin secretion115.
In humans, both acute exercise97 and chronic exercise98 increase circulating levels of follistatin. The extent to which follistatin might improve glycaemic measures remains controversial. After bariatric surgery, improvements in HbA1c have been observed in the setting of reduced levels of follistatin116. Furthermore, inactivating hepatic follistatin in a mouse model improved WAT sensitivity and reduced hepatic glucose production116. In vitro, irisin prevented excessive lipogenesis of mouse islets under glucolipotoxic conditions, resulting in improved insulin secretion, inhibition of apoptosis and restored β-cell function-related gene expression117.
The myokine IL-6 is also associated with favourable alterations in glucose homeostasis. In humans, IL-6 infusion delays gastric emptying and lowers postprandial glucose levels118. In rodents, increasing IL-6 by exercise or by IL-6 injection increases the production of glucagon-like peptide 1 by intestinal L cells and pancreatic α-cells to enhance glucose-stimulated insulin secretion. These benefits of IL-6 in enhancing insulin secretion were seen across multiple rodent models of T2DM119. In healthy humans, IL-6 infusion to levels similar to those seen with strenuous exercise enhances insulin-stimulated glucose-uptake but does not alter whole-body lipolysis or lipid oxidation120. However, another study of IL-6 infusion into humans found that IL-6 stimulates lipolysis and lipid oxidation54,121. Further research into these seemingly conflicting findings is warranted to establish the effect of exerkines on glucose metabolism.
내분비계
운동이
당 대사 장애 개선에 효과가 있는 것으로 입증되었으므로,
이 섹션에서는 포도당 항상성에 영향을 미치는 엑서카인에 대해 구체적으로 살펴보겠습니다 (표 3; 보충 표 1).
인간에서,
β-아미노이소부티르산 (BAIBA)의 순환 수준은
만성 훈련에 따라 증가했으며55
인슐린 저항성과 반비례하는 상관 관계가 있었습니다55.
β-aminoisobutyric acid

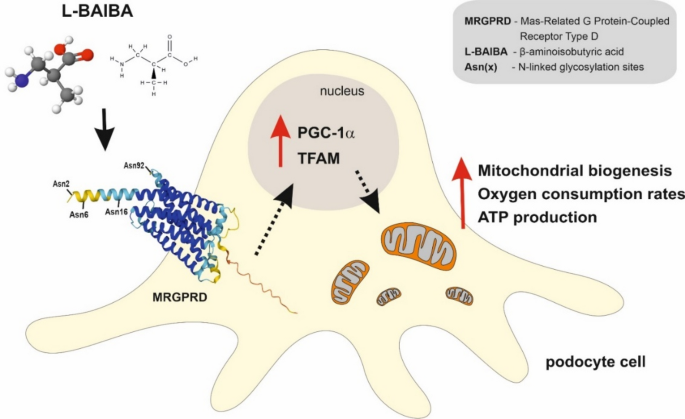
야생형 마우스에서 BAIBA 투여는
인슐린 저항성을 감소시키고 염증을 억제했습니다55.
다른 연구에서 C2C12 마우스 근육 세포와 야생형 마우스 모델(팔미트산 또는 고지방 식이 노출)을 사용한 결과, BAIBA 투여는 AMP-활성화 단백질 키나제(AMPK) 및 AMPK-PPARδ 의존적 경로를 통해 골격근에서 인슐린 저항성을 완화하고 염증을 감소시키며 지방산 산화를 증가시켰습니다113. 제한된 인간 데이터에 따르면, 급격한 운동은 CX3CL1에 의해 암호화되는 프랙탈킨(fractalkine)의 혈장 및 근육 발현 수준을 증가시킵니다70. 프랙탈킨은 β 세포 기능을 강화하여 포도당에 의해 자극된 인슐린 분비를 유리하게 조절하는 케모카인입니다114. 인간에게 만성적인 운동은 또한 순환하는 페툴린-A의 수준을 감소시킵니다72,101. 페투린-A는 포도당 자극성 인슐린 분비를 감소시켜 β-세포 감지를 저해하는 것으로 나타났습니다115.
순환하는 폴리스틴 수치를 증가시킵니다.
폴리스틴이 혈당 조절을 개선하는 정도는 여전히 논란의 여지가 있습니다. 비만 수술 후 폴리스틴 수치가 감소한 상황에서 HbA1c 개선이 관찰되었습니다116. 또한, 쥐 모델에서 간 follistatin을 불활성화시키면 백색 지방 조직(WAT)의 감수성이 개선되고 간 포도당 생산이 감소했습니다116. 체외 실험에서 irisin은 글루코리포톡신 조건 하에서 쥐의 섬세포에서 과도한 지방 생성을 방지하여 인슐린 분비 개선, 세포 사멸 억제 및 β-세포 기능 관련 유전자 발현 회복을 유도했습니다117.
미오킨 IL-6도 포도당 대사 균형의 유리한 변화와 연관되어 있습니다. 인간에서 IL-6 투여는 위 배출을 지연시키고 식후 혈당 수치를 낮춥니다118. 설치류에서 운동이나 IL-6 주사로 IL-6 수치를 증가시키면 장 L 세포와 췌장 α-세포에서 글루카곤 유사 펩티드 1(GLP-1) 생산이 증가하여 포도당 자극성 인슐린 분비가 향상됩니다. IL-6의 인슐린 분비 향상 효과는 T2DM 설치류 모델에서 다중 모델에서 관찰되었습니다119. 건강한 인간에게 격렬한 운동으로 나타나는 수준과 유사한 수준의 IL-6를 주입하면 인슐린에 의해 자극된 포도당 흡수가 향상되지만 전신 지방 분해나 지질 산화는 변화하지 않습니다120. 그러나 인간에게 IL-6를 주입한 또 다른 연구에서는 IL-6가 지방 분해와 지질 산화를 자극한다는 것이 밝혀졌습니다54,121. 이러한 상반된 연구 결과를 확인하기 위해서는 엑서카인이 포도당 대사에 미치는 영향을 확인하기 위한 추가 연구가 필요합니다.
The immune system
The broad effects of exercise on immune function implicate mobilization and altered function of cytokines and immune cells, such as neutrophils, leukocytes and natural killer cells (FIG. 3; Supplementary Table 1)30,122,123. The effects of chronic exercise on the immune system might depend on intensity, with immune enhancement by moderate exercise and possible impairment by strenuous exercise124. As shown in humans, an acute bout of exercise might be initially pro-inflammatory, but subsequently this effect is offset by an anti-inflammatory response30,124. The exercise-induced acute increase in circulating levels of IL-6 increases plasma levels of anti-inflammatory cytokines, such as IL-1RA and IL-10 (REF.125). IL-1RA inhibits IL-1β signal transduction126, whereas IL-10 inhibits production of pro-inflammatory cytokines, such as TNF127. In healthy humans, one bout of exercise or an IL-6 infusion blunted the increase in circulating levels of TNF induced by infusion of lipopolysaccharide128. Thus, an acute bout of exercise induces anti-inflammatory effects that might in part be mediated by IL-6, possibly in conjunction with other known anti-inflammatory factors, such as adrenaline and cortisol122. As a pleiotropic factor, the effect of IL-6 on metabolism and inflammation remains context-dependent. Although IL-6 is transiently increased after acute exercise, the baseline (or ‘resting’) circulating levels of IL-6 are lower in exercise-trained individuals than in untrained individuals78. Future studies focusing on tissue and cell type-specific effects as well as different exercise regimens will help delineate the temporal and spatial requirement of IL-6 in mediating exercise benefits.
면역 체계
운동이 면역 기능에 미치는 광범위한 영향은
사이토카인과 면역 세포(예: 중성구, 백혈구, 자연살해 세포)의 동원 및 기능 변화와
관련이 있습니다(그림 3; 보충 표 1)30,122,123.
만성 운동이 면역 체계에 미치는 영향은
강도에 따라 달라질 수 있으며,
중간 강도의 운동은 면역 기능을 강화할 수 있지만,
과도한 운동은 면역 기능을 저하시킬 수 있습니다124.
인간에서 보여지듯이,
급성 운동은 초기에는 염증 촉진 효과가 있을 수 있지만,
이후 이 효과는 항염증 반응에 의해 상쇄됩니다30,124.
운동으로 인한 순환 IL-6 수준의 급격한 증가는
IL-1RA 및 IL-10과 같은 항염증성 사이토카인의 혈장 수준을 증가시킵니다(REF.125).
IL-1RA는
IL-1β 신호 전달을 억제합니다126,
반면
IL-10은 TNF와 같은 염증성 사이토카인의 생성을 억제합니다127.
건강한 인간에서 단일 운동 세션이나 IL-6 투여는
리포폴리사카라이드 투여로 유발된 TNF의 순환 수준 증가를 억제했습니다128.
따라서
급성 운동 세션은 IL-6를 통해 부분적으로 매개될 수 있는 항염증 효과를 유발하며,
아드레날린과 코르티솔과 같은 다른 알려진 항염증 인자와 함께 작용할 수 있습니다122.
다기능 인자로서 IL-6의 대사 및 염증에 대한 영향은
맥락에 따라 달라집니다.
급성 운동 후 IL-6는 일시적으로 증가하지만,
운동 훈련을 받은 개인의 기초(또는 ‘휴식’) 순환 IL-6 수준은
운동을 하지 않은 개인보다 낮습니다78.
조직 및 세포 유형별 효과와 다양한 운동 요법에 초점을 맞춘 향후 연구는
운동의 이점을 매개하는 IL-6의 시간적 및 공간적 요구 사항을 명확히 하는 데 도움이 될 것입니다.
Fig. 3 |. Effects of exercise on the immune system.
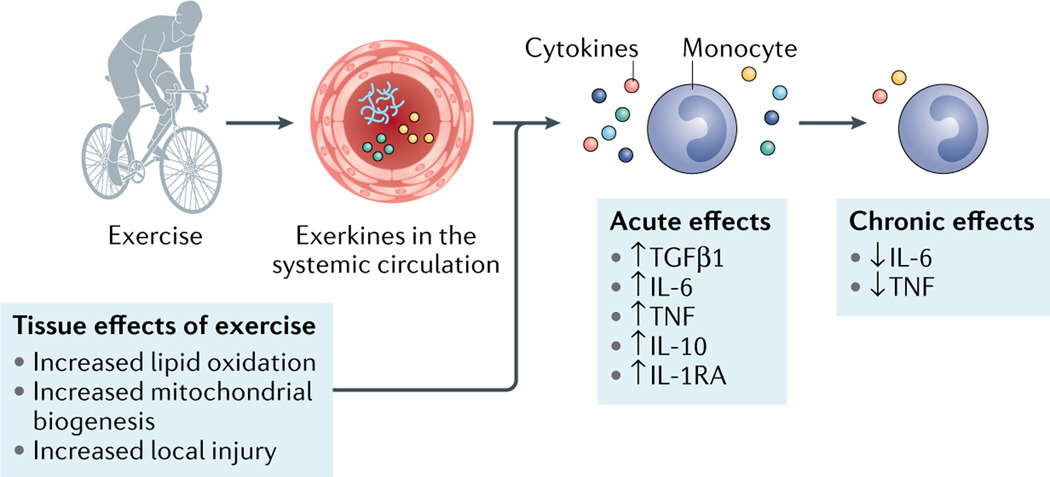
Exercise induces lipid oxidation, mitochondrial biogenesis and local injury, which stimulates exerkine release into the circulation to influence the immune system. See Supplementary Table 1 for detailed effects and relevant references. These include proteins (blue lines), metabolites (yellow circles) and extracellular vesicles (green circles), which have a multitude of effects on the immune system (generically represented by a monocyte). Acutely, exercise increases cytokines such as circulating levels of transforming growth factor β1 (TGFβ1) and IL-6 relative to the resting state. This change results in acute inflammation, characterized by increases in tumour necrosis factor (TNF) and IL-6. Once the acute exercise-induced effects have diminished, an increase in anti-inflammatory cytokines (such as IL-10 and IL-1 receptor antagonist (IL-1RA)) occurs in response to the acute inflammatory response. Chronic training is associated with a reduction in systemic and tissue inflammation, as characterized by lower circulating levels of TNF and IL-6 in the resting state, relative to sedentary individuals. Reduced insulin resistance and tumour growth has been attributed to the effects of chronic training on decreasing systemic and/or tissue inflammation.
운동은
지질 산화, 미토콘드리아 생합성 및 국소 손상을 유도하여
엑서카인의 순환으로의 방출을 자극하여 면역 체계에 영향을 미칩니다.
자세한 효과와 관련 참고 문헌은 보충 표 1을 참조하세요.
이에는 단백질(파란 선), 대사산물(노란 원), 세포외 소포(녹색 원)가 포함되며, 이는 면역 체계(일반적으로 단핵구로 표시됨)에 다양한 영향을 미칩니다. 급성적으로 운동은 휴식 상태에 비해 순환하는 변형 성장 인자 β1(TGFβ1) 및 IL-6와 같은 사이토카인의 수준을 증가시킵니다. 이 변화는 종양 괴사 인자(TNF)와 IL-6의 증가로 특징지어지는 급성 염증을 유발합니다.
급성 운동 유발 효과가 감소한 후, 급성 염증 반응에 대한 반응으로 항염증성 사이토킨(예: IL-10 및 IL-1 수용체 억제제(IL-1RA))의 증가가 발생합니다. 만성 훈련은 휴식 상태에서 TNF와 IL-6의 순환 수준이 감소하는 것으로 특징지어지는 전신 및 조직 염증의 감소와 연관되어 있습니다. 만성 훈련이 전신 및/또는 조직 염증을 감소시키는 효과로 인해 인슐린 저항성과 종양 성장 감소가 보고되었습니다.
An emerging frontier in exercise biology involves exerkine-induced immune effects in increasing resilience to cancer or as co-adjuvant to cancer therapy. The anticancer effects of exercise might not be limited to its effect on body weight. A meta-analysis pooled data from 12 prospective cohorts with self-reported physical activity and found that increased physical activity levels are associated with decreased risk of incident cancer across multiple types; many of these associations remained even after adjusting for BMI129. Acute exercise creates a unique exerkine milieu that lasts several hours after exercise cessation, which provides a temporal window for immune function stimulation31. For this reason, exercise could potentially serve as a co-adjuvant treatment for cancer therapy. In tumour-bearing mouse models (across five tumour models), mice that undertook voluntary wheel running had a reduction of more than 60% in tumour incidence and tumour growth compared with sedentary mice. Further analysis of these mouse models showed that adrenaline and IL-6 induced natural killer cell mobilization, redistribution and tumour infiltration to inhibit tumour growth123. Another mouse model found that exercise metabolites such as lactate and possibly tricarboxylic acid intermediates enhance the antitumour effector profile of CD8+ lymphocytes130. Of note, exercise is associated with enhanced secreted protein acidic and rich in cysteine (SPARC) secretion in humans and animal models131; this matricellular protein regulates cell function and tissue remodelling, while inhibiting proliferation and promoting apoptosis of a mouse colon cancer cell line132.
Crosstalk exists between skeletal muscle and the immune system. Contemporary views towards skeletal muscle now consider muscle as an immunoregulatory organ that especially affects lymphocyte and neutrophil trafficking and inflammation. During acute exercise, immune cells are mobilized by muscle secretion of exerkines such as fractalkine to enhance regeneration (in humans)133 or meteorin-like (METRNL) to increase beige adipose tissue thermogenesis (animal model)134. As previously noted, one bout of exercise or an IL-6 infusion in humans blunts the increase in circulating levels of TNF that are induced by lipopolysaccharide infusion128.
IL-13 is an important main T helper 2 (TH2) cell cytokine that mediates the anti-inflammatory polarization of resident macrophages in WAT135. IL-13 is also an exerkine, increasing in the circulation after exercise training in humans and mice136. Mice lacking IL-13 show reduced running capacity and do not show certain beneficial effects of exercise training, such as improvements in glucose tolerance and endurance running capacity136. Unlike IL-6, IL-13 is produced by type 2 innate lymphoid cells (ILC2s) in skeletal muscle. As IL-13-deficient mice show defective muscle fatty acid utilization after acute exercise and fail to show increased muscle mitochondrial biogenesis after chronic exercise, the ILC2 to IL-13 axis might have an important role in the metabolic adaptation to exercise training136. Interestingly, ILC2 and TH2 cell cytokines also control beige adipocyte recruitment in rodents137, suggesting that ILC2 to TH2 signalling might partially mediate exercise-induced beiging of WAT. The stimulants within skeletal muscle or WAT that activate ILC2s during exercise remain to be identified.
운동 생물학의 새로운 분야로는
암에 대한 저항력을 높이는 엑서카인 유도 면역 효과 또는 암 치료의 보조제로서의
엑서카인 유도 면역 효과가 있습니다.
운동의 항암 효과는
체중에 미치는 영향에만 국한되지 않을 수도 있습니다.
자기 보고에 의한 신체 활동을 조사한 12개의 전향적 코호트 데이터를 통합한 메타 분석에 따르면,
신체 활동 수준이 높을수록 여러 유형의 암 발병 위험이 감소하는 것으로 나타났습니다.
이러한 관련성은
BMI를 조정한 후에도 대부분 유지되었습니다129.
급격한 운동은
운동이 끝난 후 몇 시간 동안 지속되는 독특한 엑서카인 환경을 조성하여
면역 기능을 자극할 수 있는 일시적인 기회를 제공합니다31.
이러한 이유로 운동은 암 치료의 보조 요법으로 사용될 가능성이 있습니다. 종양이 있는 마우스 모델(5가지 종양 모델)에서 자발적으로 휠을 달린 마우스는 앉아만 있는 마우스에 비해 종양 발생률과 종양 성장률이 60% 이상 감소했습니다. 이 마우스 모델의 추가 분석 결과, 아드레날린과 IL-6이 자연살해 세포의 동원, 재분배 및 종양 침투를 촉진하여 종양 성장을 억제하는 것으로 나타났습니다123. 다른 마우스 모델에서는 운동 대사산물인 젖산과 트리카르복실산 중간체가 CD8+ 림프구의 항종양 효과 프로파일을 강화하는 것으로 확인되었습니다130. 특히 주목할 점은 운동이 인간과 동물 모델에서 분비 단백질 산성 및 시스테인 풍부 단백질(SPARC) 분비를 증가시킨다는 점입니다131; 이 매트릭셀 단백질은 세포 기능과 조직 재모델링을 조절하며, 쥐 대장 암 세포 라인에서 증식을 억제하고 아포토시스를 촉진합니다132.
골격근과 면역 체계 사이에는 상호작용이 존재합니다. 근골격근에 대한 현대적인 견해는 근육을 특히 림프구와 호중구 이동 및 염증에 영향을 미치는 면역 조절 기관으로 간주합니다. 급성 운동 중에는 근육이 프랙탈킨과 같은 엑서카인을 분비하여 면역 세포를 동원하여 재생(인간)을 촉진하거나133, 메테오린과 유사한 물질(METRNL)을 분비하여 베이지색 지방 조직의 열 생성을 증가시킵니다(동물 모델)134. 앞서 언급된 바와 같이, 인간에서 단일 운동 세션이나 IL-6 주입은 리포폴리사카라이드 주입에 의해 유발되는 순환 혈중 TNF 수치의 증가를 억제합니다128.
IL-13은 WAT 내 거주성 대식세포의 항염증성 분화를 매개하는 주요 T helper 2 (TH2) 세포 사이토킨입니다135. IL-13은 또한 엑서카인(exerkine)으로, 인간과 쥐에서 운동 훈련 후 순환에서 증가합니다136. IL-13이 결핍된 쥐는 달리기 능력이 저하되고, 포도당 내성 및 지구력 달리기 능력 개선과 같은 운동 훈련의 특정 유익한 효과가 나타나지 않습니다136. IL-6과 달리, IL-13은 골격근의 제 2형 선천성 림프구 세포(ILC2)에 의해 생성됩니다. IL-13 결핍 마우스는 급성 운동 후 근육 지방산 이용이 결손되며, 만성 운동 후 근육 미토콘드리아 생성이 증가하지 않습니다. 따라서 ILC2에서 IL-13로 이어지는 축은 운동 훈련에 대한 대사적 적응에 중요한 역할을 할 수 있습니다136. 흥미롭게도 ILC2와 TH2 세포 사이토카인은 설치류에서 베이지 지방세포 모집을 조절합니다137, 이는 ILC2에서 TH2로의 신호전달이 운동 유발성 WAT의 베이지화를 부분적으로 매개할 수 있음을 시사합니다. 운동 중 골격근 또는 WAT 내 ILC2를 활성화하는 자극제는 아직 밝혀지지 않았습니다.
The nervous system
Exercise is a promising non-pharmacological strategy to maintain and improve brain function138. FIGURE 4 presents an overview of the purported effects of exercise on the nervous system (Supplementary Table 1). Of note, evidence for the benefits of exercise on cognition remains variable, probably owing to the lack of randomized controlled trials throughout the lifespan with standardized exercise interventions and comparable methods for cognitive assessment139–142. The effects of exercise on the brain are most apparent in the hippocampus, a part of the brain involved in learning and memory143. In older adults (aged 55–80 years), participation in an aerobic walking programme increased hippocampal volume and improved memory144. Moreover, accumulating evidence suggests that physical activity, as shown in preclinical, observational and interventional studies in humans, can prevent or delay the onset of neurodegenerative conditions138. In humans, acute exercise increases plasma levels of brain-derived neurotrophic factor (BDNF)7, whereas chronic exercise training has been shown to not alter140, increase or even decrease plasma levels of BDNF140,145. In rodents, chronic exercise upregulates BDNF in the hippocampus, which is essential for adult hippocampal neurogenesis and neural plasticity146. Chronic exercise in rodents also enhances hippocampal synaptic plasticity, adult neurogenesis and neurotrophin levels, as well as memory function147. In addition, voluntary wheel running in rodents increases the number of new hippocampal neurons, enhances morphological maturation, such as dendritic branching and spine density, and alters the circuitry of adult-born neurons147.
신경계
운동은
뇌 기능을 유지하고 개선하는 유망한 비약물적 전략입니다138.
그림 4는
운동이 신경계에 미치는 것으로 추정되는 효과를 개괄적으로 보여줍니다(보충 표 1).
주목할 점은
운동의 인지 기능에 대한 이점이 여전히 변동성이 크며,
이는 생애 전반에 걸쳐 표준화된 운동 개입과 인지 평가를 위한 비교 가능한 방법을 갖춘
무작위 대조 시험이 부족하기 때문일 가능성이 높습니다139–142.
운동이 뇌에 미치는 영향은 학습과 기억에 관여하는
뇌의 일부인 해마에서 가장 명확히 나타납니다143.
55세에서 80세 사이의 노인에서 유산소 걷기 프로그램에 참여한 경우
해마 부피가 증가하고 기억력이 개선되었습니다144.

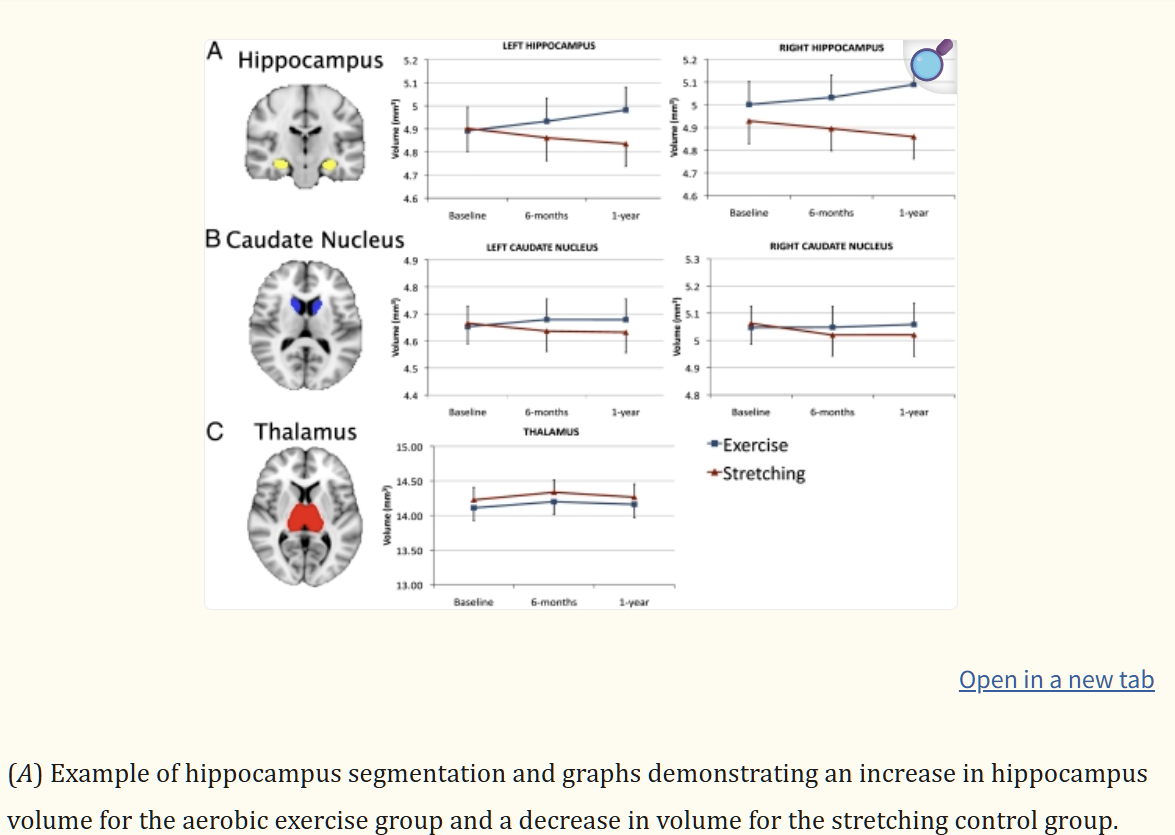
또한,
전임상 연구, 관찰 연구 및 인간 대상 개입 연구에서 축적된 증거는
신체 활동이 신경퇴행성 질환의 발병을 예방하거나 지연시킬 수 있음을 시사합니다138.
인간에서 급성 운동은
뇌유래 신경 영양 인자(BDNF)의 혈장 수치를 증가시킵니다7,
반면 만성 운동 훈련은
BDNF의 혈장 수치를 변화시키지 않거나140 증가시키거나 심지어 감소시킬 수 있습니다140,145.
설치류에서 만성 운동은 해마에서의 BDNF 발현을 증가시키며, 이는 성인 해마 신경 발생과 신경 가소성에 필수적입니다146. 쥐에서 만성 운동은 해마 시냅스 가소성, 성인 신경 발생, 신경 영양 인자 수준 및 기억 기능을 향상시킵니다147. 또한 쥐의 자발적 휠 달리기는 새로운 해마 신경세포의 수를 증가시키고, 수상돌기 분지 및 척추 밀도와 같은 형태학적 성숙을 촉진하며, 성인 생성 신경세포의 회로 구조를 변화시킵니다147.
Fig. 4 |. Effects of exercise on the nervous system.
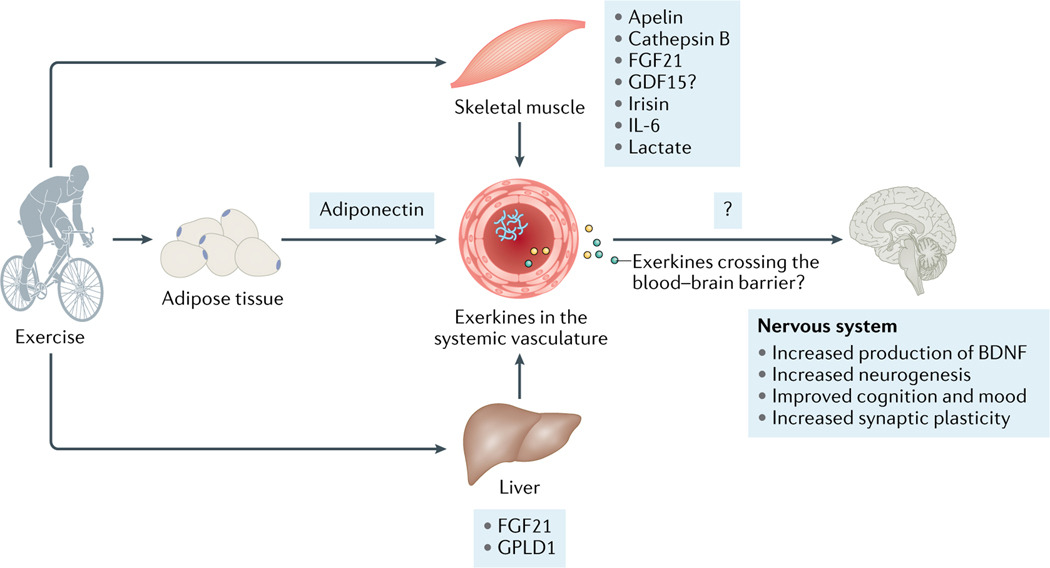
Exercise stimulates the production of exerkines from tissues, such as skeletal muscle, adipose tissue or the liver, to affect the nervous system. See Supplementary Table 1 for detailed effects and relevant references. These exerkines are released into the circulation and include proteins (blue lines), metabolites (yellow circles) and extracellular vesicles (green circles), which have a multitude of purported effects on the nervous system. These effects include increasing production of brain-derived neurotrophic factor (BDNF), enhancing neurogenesis (even in adults), cognition, mood and synaptic plasticity. The extent to which exerkines cross the blood-brain barrier to exert their effects remains unknown, symbolized by the question mark. There is uncertainty with GDF15, as symbolized by the question mark, as pharmacological GDF15 inhibits appetite and reduces activity, whereas physiological induction of GDF15 by exercise does not200. Commonly described exerkines are noted.
FGF21, fibroblast growth factors 21; GDF15, growth and differentiation factor 15; GPLD1, glycosylphosphatidylinositol-specific phospholipase D1.
운동은
골격근, 지방 조직 또는 간과 같은 조직에서 엑서카인의 생성을 자극하여
신경계에 영향을 미칩니다.
자세한 효과 및 관련 참고 문헌은 보충 표 1을 참조하십시오.
이러한 엑서카인은 혈류로 방출되며,
단백질(파란색 선), 대사 산물(노란색 원) 및 세포외 소포(녹색 원)를 포함하며,
신경계에 다양한 영향을 미치는 것으로 알려져 있습니다.
이러한 효과에는
뇌에서 분비되는 신경 영양 인자(BDNF)의 생성 증가,
신경 발생(성인에서도) 강화, 인지 기능, 기분 및 시냅스 가소성 향상 등이 있습니다.
엑서카인이 혈액 뇌 장벽을 통과하여 그
효과를 발휘하는 정도는 아직 알려지지 않았으며,
물음표로 표시되어 있습니다.
GDF15는 약리학적인 GDF15는 식욕을 억제하고 활동을 감소시키는 반면,
운동에 의한 생리적인 GDF15의 유도는
그러한 효과가 없기 때문에 불확실성이 있습니다200.
일반적으로 설명되는 엑서카인이 언급되어 있습니다.
FGF21, 섬유아세포 성장 인자 21; GDF15, 성장 및 분화 인자 15; GPLD1, 글리코실포스파티딜인오실 특이적 포스포리파제 D1.
There is increasing recognition that peripheral factors might trigger the effects of exercise on the brain. In the past 20 years, researchers have begun to test the hypothesis that metabolites, peptides and proteins released from liver, adipocytes, blood cells (particularly platelets) and muscle might influence the central nervous system138,148,149. Since 2020, several studies have transferred plasma from exercised animals into sedentary animals, with subsequent improvements in cognitive function, supporting the presence of a transferable factor in improving cognitive function148,149. Evidence is now accumulating that factors released from non-neuronal tissue148–152 and delivered via the vasculature to the brain might have important roles in synaptic plasticity, memory function and mood regulation150. Adiponectin is an adipocyte-secreted protein that seems to have neuroprotective effects151, in addition to its insulin-sensitizing, anti-inflammatory and anti-atherogenic effects151,153. In mice, adiponectin was demonstrated to pass through the blood-brain barrier and was associated with increased neurogenesis and reduced depression-like behaviours151. Interestingly, discrepancies can exist between the plasma levels of adiponectin and levels in the cerebrospinal fluid. For example, in humans, acute exercise increases plasma levels of adiponectin but decreases cerebrospinal fluid levels of adiponectin154. The mechanisms underlying the beneficial effects of exercise on brain structure and function remain an active area of investigation.
최근 주변 요인이
운동의 뇌에 미치는 효과를 유발할 수 있다는 인식이 증가하고 있습니다.
지난 20년간 연구자들은
간, 지방세포, 혈액 세포(특히 혈소판) 및 근육에서 방출되는 대사산물,
펩타이드 및 단백질이 중추 신경계에 영향을 미칠 수 있다는 가설을 검증하기 시작했습니다138,148,149.
2020년 이후 여러 연구에서
운동한 동물의 혈장을 운동하지 않은 동물에게 이식한 결과 인지 기능이 개선되었으며,
이는 인지 기능 개선에 기여하는 전이 가능한 요인의 존재를 지지합니다148,149.
혈관을 통해 뇌로 전달되는 요소가
시냅스 가소성, 기억 기능 및 기분 조절에 중요한 역할을 할 수 있다는 증거가 축적되고 있습니다150.
아디포넥틴은 지방세포에서 분비되는 단백질로,
인슐린 감수성 향상, 항염증 및 항동맥경화 효과 외에도
쥐 실험에서 아디포넥틴은 혈액-뇌 장벽을 통과해 신경 발생 증가와 우울증 유사 행동 감소와 연관되었습니다151. 흥미롭게도, 혈장 내 아디포넥틴 농도와 뇌척수액 내 농도 사이에 차이가 존재할 수 있습니다. 예를 들어, 인간에서 급성 운동은 혈장 내 아디포넥틴 농도를 증가시키지만 뇌척수액 내 아디포넥틴 농도는 감소시킵니다154. 운동이 뇌 구조와 기능에 미치는 유익한 효과의 기전은 여전히 활발히 연구 중인 분야입니다.
Muscle-brain crosstalk.
Myokines seem to have an important role in hippocampal neurogenesis (animal model) and neurotrophin levels (animal model), and enhanced cognition and mood (animal model and humans) (Supplementary Table 1). For instance, in mice, increasing intrinsic irisin expression in neurons or increasing plasma levels of irisin elevates hippocampal Bdnf gene expression152. Irisin administration in a mouse model of Alzheimer disease improves synaptic plasticity and memory function155,156. In both animal models and humans, plasma levels of cathepsin B, a lysosomal thiol proteinase produced by muscle, is positively associated with hippocampus-dependent memory145,157. Studies in humans have shown that acute exercise does not clearly increase plasma levels of cathepsin B7, although chronic exercise does increase plasma levels of cathepsin B145,157. These same studies also showed that acute exercise increases plasma levels of BDNF7, whereas chronic exercise does not increase BDNF140,145 suggesting that investigation of local neuronal effects remains warranted.
근육-뇌 교신.
마이오킨은
해마 신경 발생(동물 모델)과 신경 영양 인자 수준(동물 모델),
인지 기능 및 기분 개선(동물 모델 및 인간)에 중요한 역할을 하는 것으로 보입니다(보충 표 1).
예를 들어, 쥐에서 신경세포 내 내인성 이리신 발현을 증가시키거나 혈장 내 이리신 수치를 증가시키면 해마 Bdnf 유전자 발현이 증가합니다152. 알츠하이머 병 동물 모델에서 이리신 투여는 시냅스 가소성과 기억 기능을 개선합니다155,156. 동물 모델과 인간 모두에서 근육에서 생성되는 리소좀 티올 프로테아제인 카테프신 B의 혈장 수준은 해마 의존적 기억과 양의 상관관계를 보입니다145,157.
인간 연구에서는 급성 운동이
카테프신 B의 혈장 수준을 명확히 증가시키지 않지만7,
만성 운동은 카테프신 B의 혈장 수준을 증가시킵니다145,157.
같은 연구에서 급성 운동은 BDNF7 혈장 수치를 증가시키지만,
국소 신경 세포 효과에 대한 추가 연구가 필요함을 시사합니다.
Liver-brain crosstalk.
The liver secretes factors that are important for brain function. Kynurenine is a metabolite of the amino acid L-tryptophan and is primarily synthesized in the liver. In both mice and humans, chronic aerobic training increases muscle expression of kynurenine aminotransferase, which facilitates conversion of kynurenine into kynurenic acid, a metabolite that is unable to cross the blood-brain barrier. This shift in kynurenine metabolism is able to protect the brain from stress-induced depression150.
Exchanging plasma from exercising aged mice to sedentary aged mice enhances adult hippocampal neurogenesis and memory function148. Upon further investigation, plasma proteomic analysis led to the identification of a novel hepatokine, glycosylphosphatidylinositol-specific phospholipase D1 (GPLD1), which increases after exercise and correlates with improved cognitive function in aged mice. These findings are supported in humans, as concentrations of GPLD1 in blood were higher in active, healthy older adults (n = 20, >66 years old) than in their sedentary counterparts148. Investigations into the underlying mechanisms indicate that GPLD1 does not cross the blood-brain barrier148. Hence, the benefit of GPLD1 (REF.148) and other exerkines on brain structure and function might relate to its peripheral effects, such as the complement signalling cascade149,158, or coagulation159. Additional exercise studies are needed to better appreciate the exercise-liver-brain axis.
간-뇌 교차 작용.
간은 뇌 기능에 중요한 인자를 분비합니다.
키누레닌은
아미노산 L-트립토판의 대사산물로 주로 간에서 합성됩니다.
쥐와 인간 모두에서 만성 유산소 운동은 근육 내 키누레닌 아미노전달효소 발현을 증가시켜 키누레닌이 혈액-뇌 장벽을 통과할 수 없는 대사산물인 키누레닉 산으로 전환되는 것을 촉진합니다. 이 키누레닌 대사 변화는 스트레스 유발 우울증으로부터 뇌를 보호하는 것으로 나타났습니다150.
운동을 하는 노화 마우스의 혈장을 운동을 하지 않는 노화 마우스에게 교환하면 성인 해마 신경 발생과 기억 기능이 향상됩니다148. 추가 연구에서 혈장 단백질체 분석을 통해 운동 후 증가하고 노화 마우스의 인지 기능 개선과 상관관계가 있는 새로운 간유래 인자(hepatokine)인 글리코실포스파티딜인오실 특이적 포스포리파제 D1(GPLD1)이 식별되었습니다. 이 결과는 인간에서도 확인되었으며, 활동적인 건강한 노인(n = 20, 66세 이상)의 혈중 GPLD1 농도가 비활동적인 노인보다 높았습니다148. 근본적인 메커니즘에 대한 연구에 따르면 GPLD1은 혈액-뇌 장벽을 통과하지 않는 것으로 나타났습니다148. 따라서 GPLD1 (REF.148) 및 기타 엑서카인이 뇌 구조 및 기능에 미치는 이점은 보체 신호 전달149,158 또는 응고159와 같은 말초 효과와 관련이 있을 수 있습니다. 운동-간-뇌 축을 더 잘 이해하기 위해서는 추가적인 운동 연구가 필요합니다.
Bone
Exercise, especially resistance exercise, increases bone mineral desnity160. Multiple mechanisms exist, although mechanical loading is considered a major factor161. Noted exercise-associated bone-derived factors affecting bone formation include TGFβ1 (REF.162) and sclerostin163. Sclerostin inhibits bone formation163,164 and blood levels of sclerostin are lower in highly active humans than in sedentary humans163. Emerging data demonstrate that crosstalk exists between bone and muscle, probably mediated by secretory factors165. Noted myokines affecting the bone include apelin166, myostatin61, irisin167, IL-6 (REF.168), IL-7 (REF.60) and BAIBA59 (Supplementary Table 1).
Gaps and future opportunitiesGaps in exerkine science
Contentious questions remain that temper the enthusiasm regarding exerkines (BOX 1). These controversies include the lack of consistency between the acute and chronic exercise response, discrepancies between humans and animal models of exercise and interpretation challenges due to variability in outcomes and sampling. These knowledge gaps set the stage for future opportunities in exerkine research.
뼈
운동, 특히 저항 운동은 골밀도를 증가시킵니다160. 다양한 메커니즘이 존재하지만, 기계적 부하가 주요 요인으로 간주됩니다161. 운동과 관련된 뼈 유래 인자 중 뼈 형성에 영향을 미치는 것으로 알려진 것에는 TGFβ1 (REF.162)과 스클레로스틴163이 있습니다. 스클레로스틴은 뼈 형성을 억제합니다163,164이며, 활동적인 인간의 혈중 스클레로스틴 수치는 비활동적인 인간보다 낮습니다163. 최근 연구 결과는 뼈와 근육 사이에 교차 작용이 존재하며, 이는 분비 인자에 의해 매개될 가능성이 높다는 것을 보여줍니다165. 뼈에 영향을 미치는 주요 마이오킨에는 아펠린166, 마이오스타틴61, 이리신167, IL-6 (REF.168), IL-7 (REF.60) 및 BAIBA59 (보충 표 1)가 있습니다.
격차와 미래의 기회 엑서카인 과학의 격차
엑서카인에 대한 열정을 식히는 논쟁의 여지가 있는 질문들이 남아 있습니다 (BOX 1). 이러한 논쟁에는 급성 및 만성 운동 반응의 일관성 부족, 인간과 동물 운동 모델 간의 불일치, 결과 및 샘플링의 변동성으로 인한 해석의 어려움 등이 있습니다. 이러한 지식의 격차는 엑서카인 연구의 미래 기회를 위한 무대를 마련합니다.
Box 1 |. Contentious questions regarding exerkines.
Overenthusiasm about the potential of exerkines needs to be tempered, as controversies remain.
Inconsistency between the acute and chronic exerkine response
As demonstrated in Supplementary Table 1, the acute exerkine response does not necessarily parallel and could even contradict the chronic exercise response, as exemplified by brain-derived neurotropic factor (BDNF), IL-6, irisin and musclin. Hence, the question arises as to whether the discrepancy reflects the difference in mechanism between acute versus chronic perturbation, or more pragmatically, remains unrelated to the observed exercise-induced changes.
Inconsistency between studies in animals and humans
As demonstrated in Supplementary Table 1, the exerkine response in animals does not necessarily parallel the exerkine response in humans, as exemplified by angiopoietin, BDNF, follistatin, IL-7, IL-8, IL-10, irisin, leukaemia inhibitory factor, myonectin, musclin, myostatin and secreted protein acidic and rich in cysteine (SPARC). Hence, the question arises as to whether the excitement generated from discoveries in animal models will translate to specific human populations or more pragmatically, whether animal findings remain unrelated to observed changes in humans.
급성 및 만성 엑서카인 반응의 불일치
보충 표 1에서 볼 수 있듯이, 급성 엑서카인 반응은 반드시 만성 운동 반응과 평행하지는 않으며, 뇌에서 분비되는 신경 영양 인자(BDNF), IL-6, 이리신 및 머스클린의 예에서 볼 수 있듯이 만성 운동 반응과 모순될 수도 있습니다.
따라서 이 불일치가 급성과 만성적 교란 간의 메커니즘 차이를 반영하는지, 아니면 더 실용적으로 운동 유발 변화와 무관한지 의문이 제기됩니다.
동물과 인간 연구 간의 불일치
보충표 1에서 볼 수 있듯이, 동물에서 나타나는 엑서카인 반응은 인간에서 나타나는 엑서카인 반응과 반드시 일치하지는 않습니다. 안지오포이에틴, BDNF, 폴리스타틴, IL-7, IL-8, IL-10, 이리신, 백혈병 억제 인자, 미오넥틴, 머스클린, 미오스타틴 및 분비 단백질 산성 및 시스테인 풍부 단백질(SPARC)이 그 예입니다. 따라서 동물 모델에서 발견된 흥분이 특정 인간 인구 집단에 적용될 수 있는지, 또는 더 실용적으로 말해 동물 연구 결과가 인간에서 관찰된 변화와 무관한지 여부가 질문으로 제기됩니다.
Variability of outcomes and sampling, which hinder interpretation
The literature is replete with studies showing variable, if not conflicting, benefits from exercise, commonly attributed to differences in selected populations, exercise type, exercise intensity and exercise duration141,142,201. However, even when an exercise exposure is fixed, as exemplified by a clinical trial setting, the cardiovascular response can be ostensibly disassociated from the metabolic response25,26,202. Hence, the question arises as to whether these discrepancies can be explained by differences in the exerkine response. If alterations in exerkines might explain the observed findings, even more questions arise regarding sampling relative to the timing of exercise exposure (during versus after), sampled tissue (soft tissue versus blood) and context (fasted or fed22, or circadian rhythm21,24) Hence, the question arises as to the translational relevance of the exerkine literature to date, given the inconsistency of observed exercise effects and highly variable sampling protocols.
Despite the acceleration in exerkine-related research since the identification of IL-6 as a myokine in 2000 (REF.16), much remains to be done in the scientific areas of research, technology and therapeutic interventions (BOX 1). Specifically, a critical need exists to move beyond the ‘skeletal muscle-centric’ view of exerkines and focus more on their roles in inter-organ communication, tissue regeneration, immune regulation, metabolic adaptation, cardiovascular fitness, psychological health and overall health across the lifespan. The vasculature and endothelium are emerging as a probable central facilitator, which enables systemic exerkines to exert their specific effects within the various local environments, as well as being a direct target and source of exerkines. Understanding the system-wide effects of exercise and the myriad of exercise-related improvements is essential for understanding resilience. Such knowledge will provide new translational research opportunities to develop novel, targeted interventions that increase physiological reserve, maintain and/or enhance resiliency and thus promote healthy ageing, as well as interventions that prevent and treat comorbidities and chronic disease.
Many more exerkines, and their sources, targets and mechanisms, remain to be discovered. In 2016, the MoTrPAC project was launched to uncover novel exerkines through deep omics profiling of biomaterial from humans and rodents before and after acute exercise as well as chronic exercise training. As potential candidate transducers are uncovered, follow-up mechanistic studies will be required to delineate their function. In addition to molecular discoveries, substantial work remains to decipher the dosage and type of exercise needed to elicit positive health outcomes. Intervention studies are needed to investigate the effect of different types of exercise on resilience to various conditions, with guidance available from the NIH in designing resilience-based studies. To address these knowledge gaps, detailed studies are needed to identify and validate the exerkine responses after exercise (acute, chronic or intermittent) exposure, including a detailed post-exercise response. Certainly, the demographics and phenotypes of the population will matter, as the response in healthy participants can vary greatly from that in participants with comorbidities. Further work in these areas will advance our understanding of ageing, health and disease prevention.
결과와 표본 채취의 변동성, 해석을 방해하는 요인
문헌에는 운동의 이점이 변동적이거나 심지어 상반된 결과를 보이는 연구가 많으며, 이는 주로 선택된 인구 집단, 운동 유형, 운동 강도 및 운동 지속 시간의 차이에 기인한다고 설명됩니다141,142,201. 그러나 임상 시험 환경에서와 같이 운동 노출이 고정된 경우에도, 심혈관 반응은 대사 반응과 명백하게 분리될 수 있습니다25,26,202. 따라서 이러한 불일치는 엑서카인 반응의 차이로 설명될 수 있는지 여부에 대한 의문이 제기됩니다. 엑서카인의 변화가 관찰된 결과를 설명할 수 있다면, 운동 노출의 시점(운동 중 대 운동 후), 샘플링된 조직(연조직 대 혈액) 및 상황(공복 대 식후22, 또는 일주기 리듬21,24)과 관련된 샘플링에 대해 더 많은 의문이 제기됩니다. 따라서, 관찰된 운동 효과의 불일치와 매우 다양한 샘플링 프로토콜을 고려할 때, 현재까지 발표된 엑서카인 관련 문헌의 번역적 관련성에 대한 의문이 제기됩니다.
2000년에 IL-6이 미오카인으로 확인된 이후 엑서카인 관련 연구가 가속화되었지만 (참고 문헌 16), 과학적 연구, 기술 및 치료적 개입 분야에서는 아직 해야 할 일이 많습니다 (박스 1). 특히, 엑서카인에 대한 '골격근 중심'의 관점을 넘어, 기관 간 통신, 조직 재생, 면역 조절, 대사 적응, 심혈관 건강, 심리적 건강 및 생애 전반에 걸친 전반적인 건강에 대한 엑서카인의 역할에 더 초점을 맞출 필요가 있습니다. 혈관과 내피는 전신 엑서카인이 다양한 국소 환경에서 특정한 효과를 발휘할 수 있게 하는 중심적인 촉진제 역할을 할 가능성이 대두되고 있으며, 엑서카인의 직접적인 표적 및 공급원으로도 작용합니다. 운동의 전신적 효과와 운동과 관련된 무수한 개선 사항을 이해하는 것은 회복력을 이해하는 데 필수적입니다. 이러한 지식은 생리적 예비 능력을 증가시키고, 회복력을 유지 및/또는 향상시켜 건강한 노화를 촉진하며, 동반 질환 및 만성 질환을 예방하고 치료하는 새로운 맞춤형 개입 방법을 개발하기 위한 새로운 번역 연구 기회를 제공할 것입니다.
더 많은 엑서카인과 그 공급원, 표적 및 메커니즘이 아직 발견되지 않았습니다. 2016년에는 급성 운동 및 만성 운동 훈련 전후의 인간과 설치류의 생체 물질을 심층 오믹스 프로파일링하여 새로운 엑서카인을 발견하기 위한 MoTrPAC 프로젝트가 시작되었습니다. 잠재적인 변환기 후보가 발견되면, 그 기능을 규명하기 위한 후속 메커니즘 연구가 필요할 것입니다. 분자적 발견 외에도, 긍정적인 건강 결과를 유발하기 위해 필요한 운동의 용량과 유형을 규명하는 작업이 여전히 많이 남아 있습니다. 다양한 조건에 대한 회복력에 대한 운동의 효과를 조사하기 위해 개입 연구가 필요하며, NIH에서 회복력 기반 연구 설계에 대한 지침이 제공될 수 있습니다. 이러한 지식의 격차를 해소하기 위해서는 운동(급성, 만성 또는 간헐적) 노출 후 엑서카인 반응을 확인하고 검증하기 위한 상세한 연구가 필요합니다. 물론, 건강한 참가자의 반응은 동반 질환이 있는 참가자의 반응과 크게 다를 수 있으므로, 인구의 인구 통계학적 특성과 표현형이 중요할 것입니다. 이러한 분야에서의 추가 연구는 노화, 건강 및 질병 예방에 대한 우리의 이해를 발전시킬 것입니다.
Opportunities for new technologies
Technology gaps also remain in exerkine research. One emerging area is the use of wearable technologies and devices to capture quantitative and dynamic phenotypes over long periods of time in healthy individuals as well as in those with mild or severe diseases. For instance, wearable technology could provide valuable information regarding physical activity levels and exercise capacity during and following COVID-19 illness and recovery, adding to the description of post-acute sequelae of SARS-CoV-2 infection, which is under active investigation. Currently, non-invasive and minimally invasive devices have enabled the monitoring of many behavioural and physiological phenotypes, including heart rate and electrical activity in the heart (ECG), body temperature, physical activity and sedentary behaviour, peripheral blood oxygen saturation and blood concentrations of glucose. These devices enable the real-time monitoring of the effects of exercise in natural and controlled settings at an unprecedented level. Moreover, wearable technologies can be scaled to the analysis of over a million people and can enable ‘citizen science’ whereby individuals with devices can readily participate in studies. These measurements, when combined with molecular measurements such as exerkines, have the potential to greatly improve our understanding of exercise adaptations in large cohorts with deep phenotyping across a broad age range.
Although wearable devices are powerful, multiple challenges remain in data interpretation and analysis. These challenges include device accuracy as well as device standardization and a lack of readily available high-resolution data from the manufacturers. In addition, many wearable devices do not characterize the environmental context associated with data capture. For example, if a device does not sense any physical activity, one explanation could be the lack of movement by the wearer while another explanation could be device removal. A remaining challenge entails approval and regulation from entities such as the FDA before widespread use of wearables as therapeutic interventions.
In addition to wearables, the technology, analysis and approach for exerkine discovery needs to be further developed. Deep omics profiling (transcriptome, metabolome, proteome and lipidome) of human and animal-based exerkines is occurring in MoTrPAC; this effort is expected to reveal novel molecules and mechanisms involved in exercise by providing a more comprehensive view of the multi-omics landscape of exerkines to the research community. Extracellular vesicle analysis, especially of exosomes, will be a critical component of MoTrPAC’s analysis owing to burgeoning interest in the role of extracellular vesicles as carriers of molecular signals and drivers of inter-organ crosstalk.
신기술의 기회
엑서카인 연구에도 기술적 격차가 남아 있습니다. 새로운 분야 중 하나는 웨어러블 기술과 기기를 사용하여 건강한 사람과 경증 또는 중증 질환이 있는 사람의 양적 및 동적 표현형을 장기간에 걸쳐 포착하는 것입니다. 예를 들어, 웨어러블 기술은 COVID-19 감염 및 회복 기간과 그 이후의 신체 활동 수준과 운동 능력에 대한 귀중한 정보를 제공하여, 현재 활발하게 연구되고 있는 SARS-CoV-2 감염의 급성기 후유증에 대한 설명을 보강할 수 있습니다. 현재 비침습적 및 최소 침습적 장치는 심박수, 심장 전기 활동(ECG), 체온, 신체 활동, 앉아 있는 시간, 말초 혈중 산소 포화도, 혈당 농도 등 다양한 행동 및 생리적 형질을 모니터링할 수 있습니다. 이러한 장치는 자연 환경과 통제된 환경에서 운동의 영향을 실시간으로 모니터링하는 데 전례 없는 수준을 달성했습니다. 또한 웨어러블 기술은 백만 명 이상의 사람들을 분석할 수 있도록 확장될 수 있으며, 기기를 보유한 개인이 연구에 쉽게 참여할 수 있는 '시민 과학'을 가능하게 합니다. 이러한 측정값을 엑서카인(exerkines)과 같은 분자 측정값과 결합하면, 광범위한 연령대의 심층적인 표현형 분석을 통해 대규모 코호트에서 운동 적응에 대한 이해를 크게 향상시킬 수 있습니다.
웨어러블 기기는 강력하지만, 데이터 해석 및 분석에는 여러 가지 과제가 남아 있습니다. 이러한 과제에는 장치의 정확성, 장치 표준화, 제조업체로부터 쉽게 접근 가능한 고해상도 데이터의 부족이 포함됩니다. 또한 많은 웨어러블 장치는 데이터 수집 시 환경적 맥락을 특성화하지 않습니다. 예를 들어, 장치가 신체 활동을 감지하지 않는 경우, 이는 착용자의 움직임 부족 때문일 수 있지만, 장치 제거 때문일 수도 있습니다. 웨어러블을 치료적 개입으로 널리 사용하기 전에 FDA와 같은 기관의 승인 및 규제가 필요한 점도 남아 있습니다.
웨어러블 기기 외에도 엑서카인 발견을 위한 기술, 분석 및 접근 방식이 더욱 개발되어야 합니다. MoTrPAC에서는 인간 및 동물 기반 엑서카인의 심층 오믹스 프로파일링(전사체, 대사체, 단백질체 및 지질체)이 진행되고 있습니다. 이 노력은 연구 커뮤니티에 엑서카인의 다중 오믹스 지형을 보다 포괄적으로 파악할 수 있게 함으로써 운동과 관련된 새로운 분자와 메커니즘을 밝혀낼 것으로 기대됩니다. 세포외 소포 분석, 특히 엑소좀 분석은 세포외 소포가 분자 신호 전달체 및 장기 간 교차 작용의 촉진제로서의 역할에 대한 관심 증가로 인해 MoTrPAC 분석의 핵심 요소로 작용할 것입니다.
Data reporting and data sharing
To promote comparison between studies and enhance translation, a crucial need exists for the establishment of community-wide standards for data reporting and data sharing. As an example, capturing physical activity and body composition (for example, adipose tissue mass) in the electronic health record will facilitate electronic health record data mining to examine clinical outcomes outside a structured clinical study. Cross-study comparisons of exercise studies will be facilitated by setting standards for a minimum metadata set, for consistent documentation and of covariates, such as time of day, diet or exercise exposure. Advances in computational modelling will accelerate our understanding of the physiological process of exercise and exerkine effects. Establishing a uniform knowledge base remains a critical next step in driving this process.
Exerkines as therapeutics
The health benefits of exercise are well documented. However, not all individuals are able to benefit from exercise owing to physical limitations, such as paraplegia, or imposed limitations, such as quarantining during the current COVID-19 pandemic. Moreover, in humans, metabolic non-response or even adverse responses to exercise have been described26. As the role of exerkines and their biological effects are increasingly clarified, exerkines could potentially be harnessed to mimic the benefits of exercise in individuals who are limited in their exercise capacity or to counterbalance a metabolic non-response or adverse response to exercise. Although this ‘exercise in a pill’ is currently wishful thinking, it remains a tantalizing goal for future research directions.
데이터 보고 및 데이터 공유
연구 간 비교를 촉진하고 번역을 강화하기 위해 데이터 보고 및 데이터 공유에 대한 커뮤니티 전체 표준 수립이 필수적입니다. 예를 들어, 전자 건강 기록에 신체 활동과 체성분(예: 지방 조직량)을 기록하면 구조화된 임상 연구 외부의 임상 결과를 분석하기 위한 전자 건강 기록 데이터 마이닝이 용이해집니다. 운동 연구 간의 비교는 시간대, 식이요법 또는 운동 노출과 같은 공변인의 일관된 기록을 위한 최소 메타데이터 세트 표준을 설정함으로써 용이해집니다. 계산 모델링의 발전은 운동의 생리학적 과정과 엑서카인의 효과에 대한 우리의 이해를 가속화할 것입니다. 이 과정을 추진하기 위해서는 통일된 지식 기반을 구축하는 것이 중요한 다음 단계로 남아 있습니다.
치료제로서의 엑서카인
운동의 건강상의 이점은 잘 알려져 있습니다. 그러나 하반신 마비 등 신체적 제한이나 현재 코로나19 대유행으로 인한 격리 조치 등 외부적 제한으로 인해 모든 사람이 운동의 이점을 누릴 수 있는 것은 아닙니다. 또한, 인간에서는 운동에 대한 대사적 무반응 또는 심지어는 부작용이 보고된 바 있습니다26. 엑서카인의 역할과 생물학적 효과가 점점 더 명확해짐에 따라, 엑서카인은 운동 능력이 제한된 개인에게 운동의 이점을 모방하거나 운동에 대한 대사적 무반응 또는 부작용을 상쇄하기 위해 활용될 가능성이 있습니다. 현재 이 '알약 형태의 운동'은 아직 꿈에 불과하지만, 미래 연구 방향의 유망한 목표로 남아 있습니다.
Conclusions
Although exercise exerts many beneficial effects across multiple organ systems, our understanding of the mechanisms driving the benefits of exercise and the variability in these benefits remains rudimentary. Much of the initial exerkine research has been focused on skeletal muscle; however, contemporary research is now rapidly expanding to include non-skeletal muscle-based sources and targets for exerkines that contribute to maintaining and restoring health. Exerkines are increasingly recognized as critical mediators of exercise-related changes and health benefits, particularly in their role in inter-organ and systemic communication and coordination. Yet, much remains to be done. To improve translation of results, the heterogeneity across studies needs to be minimized by reducing exposure variability and using standardized, consistent outcome measures. Large-scale, structured studies will be key resources in providing a structured environment to pursue future exerkine-related questions. In summary, exerkines are a highly promising direction for future research initiatives, with high potential as biomarkers to predict outcomes, facilitate personalized exercise programmes to improve health, reduce disease and promote resilience across the lifespan.
결론
운동은 다양한 장기 시스템에 걸쳐 많은 유익한 효과를 발휘하지만,
운동의 이점을 驱动하는 메커니즘과 이러한 이점의 변이성에 대한 이해는 여전히 미흡합니다.
초기 엑서카인 연구의 대부분은 골격근에 집중되어 있었지만,
최근에는 건강 유지 및 회복에 기여하는 엑서카인의 비골격근 기반 공급원과 표적에 대한 연구가 빠르게 확대되고 있습니다.
엑서카인은 운동과 관련된 변화 및 건강상의 이점,
특히 기관 간 및 전신적 소통과 협응력에서 중요한 매개체로 점점 더 인정받고 있습니다.
그러나 아직 해야 할 일이 많습니다.
결과를 더 잘 적용하기 위해서는 노출의 변동성을 줄이고 표준화되고 일관된 결과 측정 방법을 사용하여
연구 간의 이질성을 최소화해야 합니다.
대규모의 체계적인 연구는 엑서카인과 관련된 향후의 의문을 추구하기 위한
체계적인 환경을 제공하는 데 중요한 자원이 될 것입니다.
요약하면,
엑서카인은 향후 연구 이니셔티브를 위한 매우 유망한 방향이며,
결과를 예측하고, 건강을 개선하고, 질병을 예방하며,
생애 전반에 걸쳐 회복력을 증진하기 위한 개인 맞춤형 운동 프로그램을 촉진하는
바이오마커로서 높은 잠재력을 가지고 있습니다.
Supplementary Material
Supplementary Material
NIHMS1829603-supplement-Supplementary_Material.pdf (651KB, pdf)
Key points.
Acknowledgements
The authors thank A. Honkala (Stanford University) and N. C. Oldenburg (University of Minnesota) for their assistance with the manuscript. The workshop that set the foundation for this Review article was supported by the National Heart, Lung, and Blood Institute (NHLBI) and the National Institute of Diabetes and Digestive and Kidney Diseases, National Institutes of Health (NIH). The listed authors acknowledge the support of the following grants. L.S.C.: NIH grant R01DK098203; B.H.G.: NIH grant U01AR071133; A.L.: Spanish Ministry of Economy and Competitiveness and Fondos FEDER (PI18/00139); C.M.: European Federation of the Study of Diabetes/MSD, Occitanie Region/FEDER funds (DIABKINES, MP0021755 and Enterosys); B.K.P.: TrygFonden for the Centre for PA Research (CFAS); A.P.: Texas Health Resources Clinical Scholarship, Gilead Sciences Research Scholar Program, NIH National Institute of Aging GEMSSTAR grant (1R03AG067960-01), and Applied Therapeutics; J.M.R.: NIH grant HL150327-01A1; H.v.P: NIH National Institute on Aging (NIA)/NIH IRP and the FDOH Ed and Ethel Moore Alzheimer’s Disease Research program; K.I.S.: NIH grants R01-HL138738 and R01-AG060542; A.E.T.: National Institute for Health Research (NIHR) Leicester Biomedical Research Centre; J.M.T.: NIH grant 1R01HL142879; S.T.: NIH grants U01AR071133; J.R.Z.: Swedish Research Council for Sport Science (P2018-0097), Swedish Research Council (Vetenskapsrådet) (2015-00165), and Novo Nordisk Foundation Center for Basic Metabolic Research at the University of Copenhagen (NNF18CC0034900); M.P.S.: NIH grants U24DK112348 and U54DK102556. The views expressed in this manuscript are those of the authors and do not necessarily represent the views of the National Heart, Lung, and Blood Institute; the National Institutes of Health; or the U.S. Department of Health and Human Services.
L.S.C. has received a Dexcom investigator initiated grant (product only). C.J.L. is a consultant for PAIhealth on their Personalized Activity Intelligence applications. A.P. is on the advisory board of Roche Diagnostics. M.P.S. is a cofounder and scientific advisory board member of Personalis, SensOmics, Qbio, January, Filtricine, Protos, NiMo, Mirvie, and an advisor for Genapsys.
GlossaryResilience
Resilience is the ability of the body to resist, adapt to, recover or grow in response to stressors.
High-intensity interval training
High-intensity interval training is a form of exercise training characterized by bursts of high-intensity activity followed by less intense recovery periods.
Exerkines
Exerkines encompass a broad variety of signalling moieties that are released in response to acute and/or chronic exercise that exert their effects through endocrine, paracrine and/or autocrine pathways.
Acute exercise
Acute exercise is typically considered a single episode of exercise (often resistant or aerobic exercise) that is completed during one visit.
Chronic exercise
Chronic exercise is typically described as multiple exercise episodes (often resistant or aerobic exercise) performed over the course of weeks to months.
MicroRNA
MicroRNAs are non-protein-coding RNA molecules that are regulated in a transcriptional or post-transcriptional fashion to affect mRNA transcription and/or degradation.
Exosomes
Exosomes are a type of extracellular vesicle released by parent cells, which contain RNAs, proteins and lipids, to facilitate crosstalk between tissues.
RELATED LINKS
Molecular Transducers of Physical Activity Consortium: https://www.motrpac.org/
Resilience: https://ods.od.nih.gov/Research/resilience.aspx#defining
Footnotes
Peer review information
Nature Reviews Endocrinology thanks P. Atherton who co-reviewed the manuscript with D. Wilkinson, M. Fukui and E. Ziemann for their contribution to the peer review of this work.
Supplementary information
The online version contains supplementary material available at https://doi.org/10.1038/s41574-022-00641-2.
Competing interests
The other authors declare no competing interests.
References
- 1.Piercy KL. et al. The physical activity guidelines for Americans. J. Am. Med. Assoc 320, 2020–2028 (2018). [DOI] [PMC free article] [PubMed] [Google Scholar]
- 2.Katzmarzyk PT, Church TS, Craig CL & Bouchard C.Sitting time and mortality from all causes, cardiovascular disease, and cancer. Med. Sci. Sports Exerc 41, 998–1005 (2009). [DOI] [PubMed] [Google Scholar]
- 3.Ding D.et al. The economic burden of physical inactivity: a global analysis of major non-communicable diseases. Lancet 388, 1311–1324 (2016). [DOI] [PubMed] [Google Scholar]
- 4.Trabelsi K.et al. Globally altered sleep patterns and physical activity levels by confinement in 5056 individuals: ECLB COVID-19 international online survey. Biol. Sport 38, 495–506 (2021). [DOI] [PMC free article] [PubMed] [Google Scholar]