와우!
언젠가 꼭 한번 읽고 싶은 자료다
immobilization시 근절의 변화
1. 짧아진 상태에서의 고정은 sarcomere subtroaction
2. 길어진 상태에서의 고정은 myofibrillorgenesis
아래에서 과학적 근거를 바탕으로 자세히 설명하겠습니다. (주로 동물 실험 기반 연구 결과입니다.)
1. 기본 개념: 근육 Immobilization이란?
- 근육 immobilization은 부상 치료나 실험에서 관절을 고정하여 근육이 특정 길이(짧아진 상태 또는 길어진 상태)로 유지되게 하는 것입니다.
- 근육은 사용되지 않으면 적응(adaptation)이 일어나며, 이는 사르코미어의 수 변화로 나타납니다. 사르코미어는 근육 섬유의 반복 단위로, 직렬(serial)로 연결되어 근육 길이를 결정합니다.
- 고정 기간(보통 1-4주)이 길어질수록 변화가 뚜렷해지며, 근육 위축(atrophy)이나 관절 운동 범위 감소(contracture)가 동반될 수 있습니다.
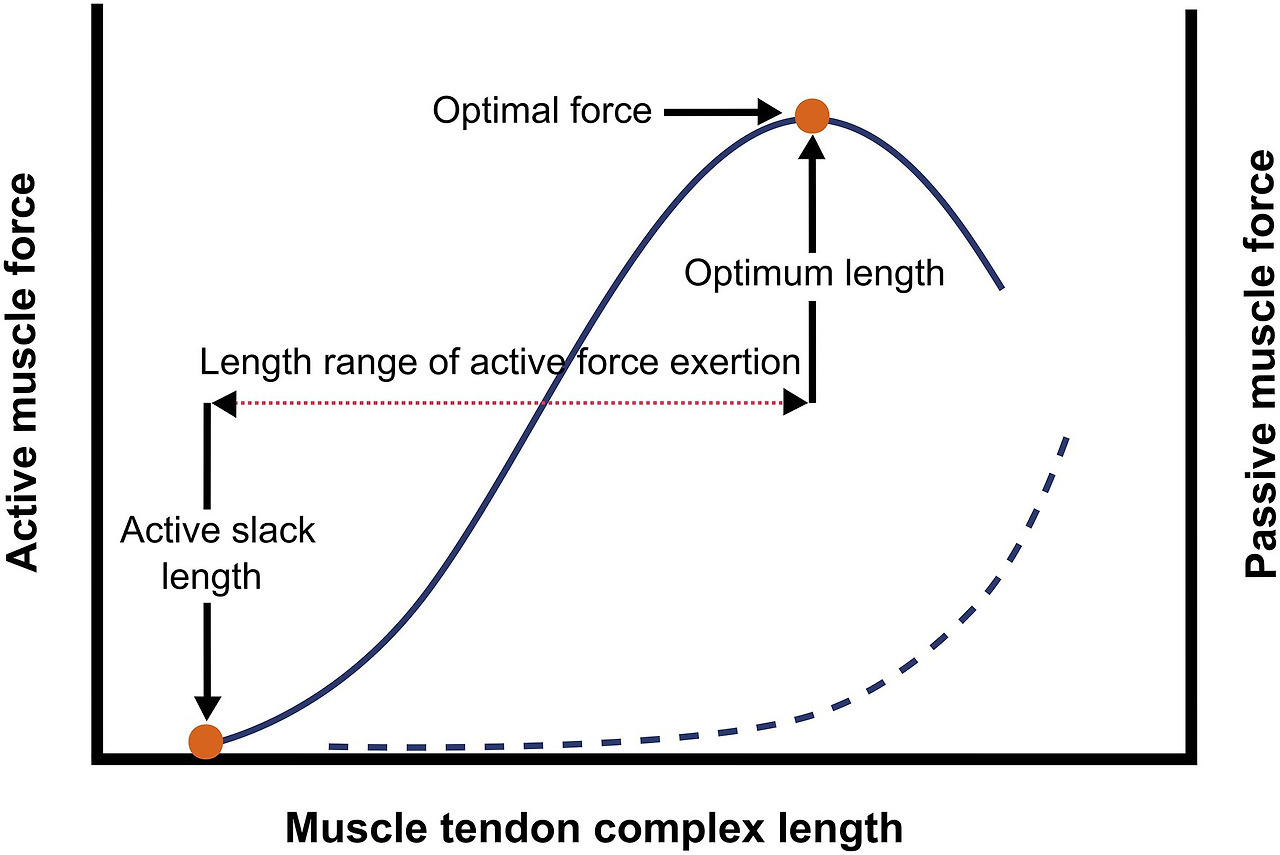
- 핵심: 근육은 최적의 길이-힘 관계(length-tension relationship)를 유지하려고 사르코미어 수를 조절합니다. 각 사르코미어의 최적 길이는 약 2.2-2.5 μm로, 이 범위에서 최대 힘을 발휘합니다.
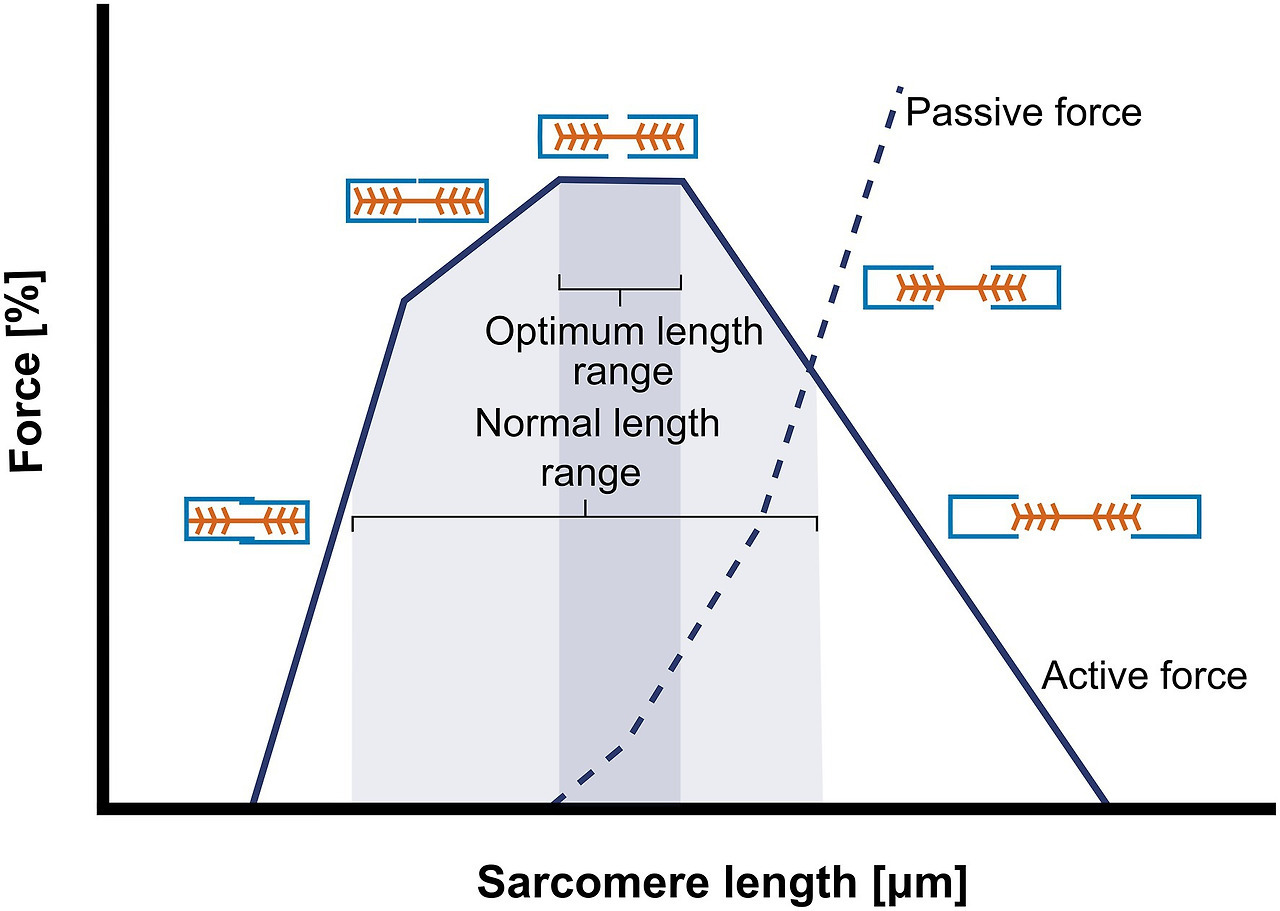
Frontiers | Stimuli for Adaptations in Muscle Length and the Length Range of Active Force Exertion—A Narrative Review
(사르코미어 길이-힘 곡선: 최적 범위에서 능동/수동 힘이 최대.)
2. 짧아진 상태(shortened position)에서의 고정: Sarcomere Abruption (Sarcomere Subtraction/감소)
- 변화 설명: 근육이 짧아진 위치(예: 무릎을 구부린 상태로 고정)로 immobilization되면, 사르코미어 수가 직렬로 감소합니다. 이는 근육 섬유 길이가 짧아지게 하여, 고정된 짧은 길이에 적응하려는 과정입니다.
- 결과: 근육 길이 감소, 위축(atrophy), 콜라겐 증가로 근육 강직도(stiffness) 상승.
- 예: 항중력 근육(anti-gravity muscles, e.g., soleus)은 더 빨리 사르코미어 손실이 일어납니다. 4주 고정 시 35% 정도 사르코미어 감소 가능.
- 메커니즘: 사용 부족으로 사르코미어가 분해되고, 연결 조직이 증가하여 근육이 짧아진 상태를 유지합니다. 이는 관절 운동 범위 감소(contracture)를 유발하며, 1주 후부터 시작됩니다.
- 임상적 의미: 깁스 치료 후 근육 약화나 구축 현상. 예방: 짧은 스트레칭(하루 30분)이 사르코미어 손실을 막을 수 있습니다.
3. 길어진 상태(lengthened position)에서의 고정: Myofibrillogenesis (근원섬유 생성/Sarcomere Addition)
- 변화 설명: 근육이 길어진 위치(예: 무릎을 펴서 고정)로 immobilization되면, 사르코미어 수가 직렬로 증가합니다. 이는 myofibrillogenesis 과정(새로운 근원섬유 및 사르코미어 형성)을 통해 일어나며, 고정된 긴 길이에 적응합니다.
- 결과: 근육 섬유 길이 증가, 개별 사르코미어 길이 단축(짧아진 사르코미어로 인해 전체 길이 유지). 4주 고정 시 25% 사르코미어 증가 가능.
- 메커니즘: 긴장(tension) 자극으로 새로운 사르코미어가 추가되며, 세포 외 기질(ECM, e.g., 콜라겐) 증식도 동반됩니다. 이는 근육이 최적 길이로 재조정되는 과정입니다.
- 임상적 의미: 재활에서 길어진 고정은 근육 길이 회복에 도움이 되지만, 과도하면 위축이나 힘 감소가 발생할 수 있습니다. 중립 위치(neutral) 고정은 사르코미어 수를 유지합니다.
요약 표: Immobilization에 따른 변화 비교
고정 상태주요 변화사르코미어 영향추가 효과예방/치료
| 짧아진(shortened) | 근육 길이 감소, 위축 | 사르코미어 수 감소 (subtraction) | 콜라겐 증가, 강직도 ↑, contracture | 간헐적 스트레칭 (e.g., 30분/일) |
| 길어진(lengthened) | 근육 길이 증가, 적응 | 사르코미어 수 증가 (addition via myofibrillogenesis) | ECM 증식, 개별 사르코미어 단축 | 활동 재개 후 점진적 단축 훈련 |
| 중립(neutral) | 최소 변화 | 사르코미어 수 유지 | 약간의 위축 가능 | 일반적 |
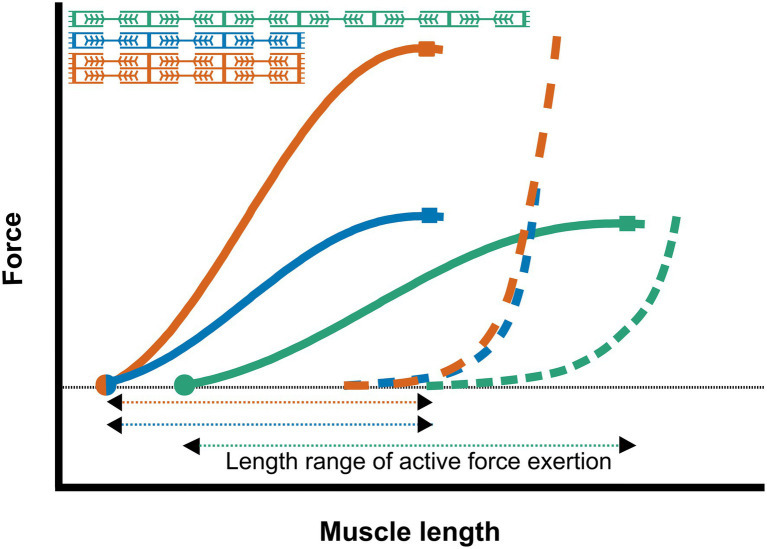
Frontiers | Stimuli for Adaptations in Muscle Length and the Length Range of Active Force Exertion—A Narrative Review
(근육 길이-힘 곡선: immobilization 후 최적 길이 변화 예시.)
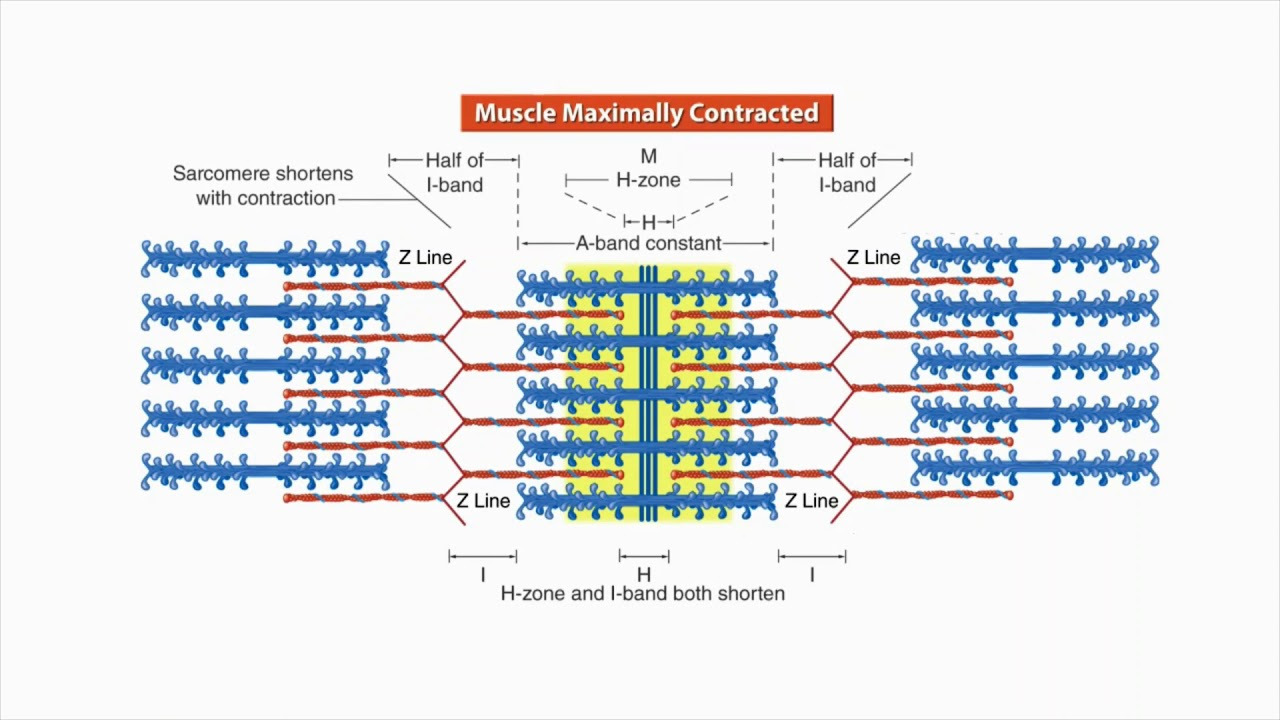
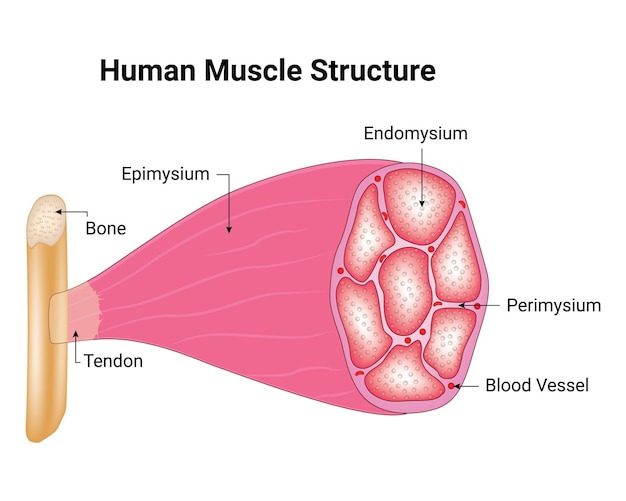
Structure and function of a sarcomere | Physiology of Sport and Exercise
(사르코미어 구조 변화: 수축 시와 유사하게 immobilization에서 길이 적응.)
이 자료를 찾다가 근절의 분자생물학적 수준에서의 근수축에 대한 놀라운 논문을 찾았다.
panic bird..










Slide 1: 제목 슬라이드
- 제목: Sarcomere의 분자 구조 (Molecular Structure of the Sarcomere)
- 저자: Roger W. Craig & Raúl Padrón
- 출처: Myology, 3rd Edition (2004, McGraw-Hill)
- 발표자: 형철
- 목적: 횡격근(striated muscle)의 사르코미어 구조를 통해 수축 메커니즘 이해
- 배경: 사르코미어는 다단백질 복합체로, 수축(contractile), 조절(regulatory), 구조(structural) 단백질로 구성됨.
Slide 2: 서론 (Introduction)
- 핵심 내용: 횡격근은 빠른 움직임과 힘 생성에 특화된 기관. 사르코미어는 기본 수축 단위로, 고도로 정렬된 구조.
- 주요 속성:
- 빠르고 효율적인 단축(shortening).
- 밀리초 단위의 on/off 스위칭.
- 정밀한 자가 조립(self-assembly).
- 단백질 분류:
- 수축: Myosin, actin.
- 조절: Troponin, tropomyosin.
- 구조: Titin, nebulin, α-actinin 등.
- 발표 개요: 근섬유 구조 → 슬라이딩 필라멘트 모델 → Thick/Thin 필라멘트 → M/Z 라인 → 중간 필라멘트 → 질환.
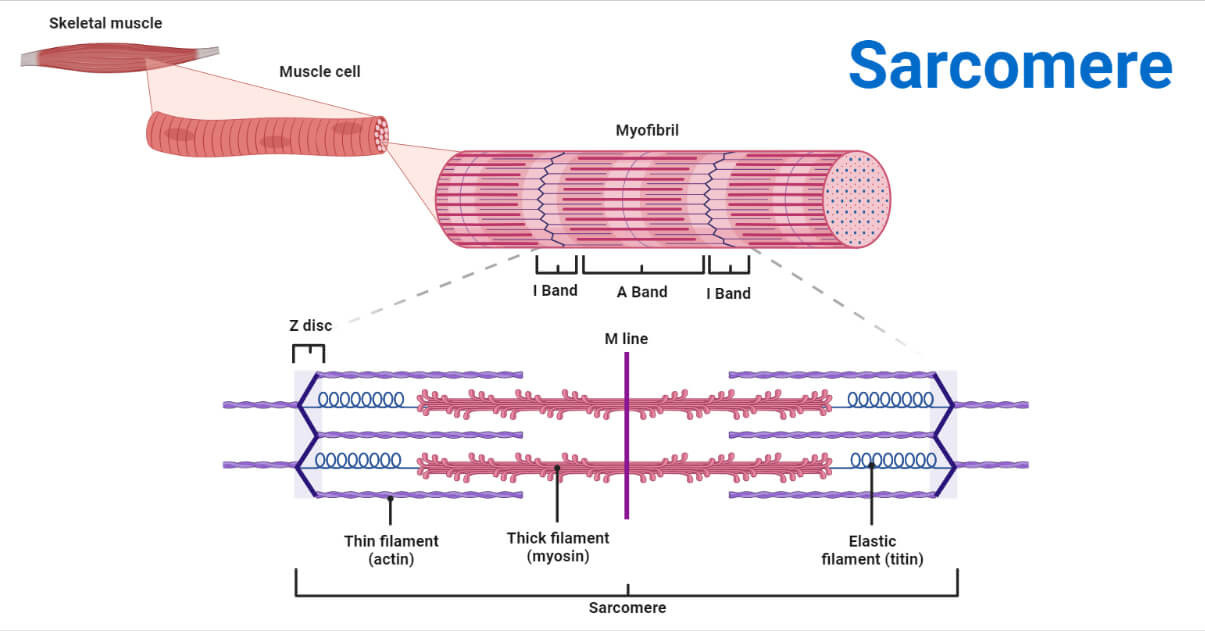
Sarcomere: Structure, Function & Role in Muscle Contraction
(이미지: Sarcomere의 전체 구조 다이어그램 - 근섬유부터 A/I 밴드까지 시각화.)
Slide 3: 횡격근 섬유의 구조 (Structure of Striated Muscle Fiber)
- A 밴드: Thick 필라멘트 (myosin, 15 nm, 1.6 μm).
- I 밴드: Thin 필라멘트 (actin, 10 nm, 1 μm).
- H 존: Thin 필라멘트 없음.
- M 라인: Thick 필라멘트 연결.
- ProteinMW (kDa)LocationFunction
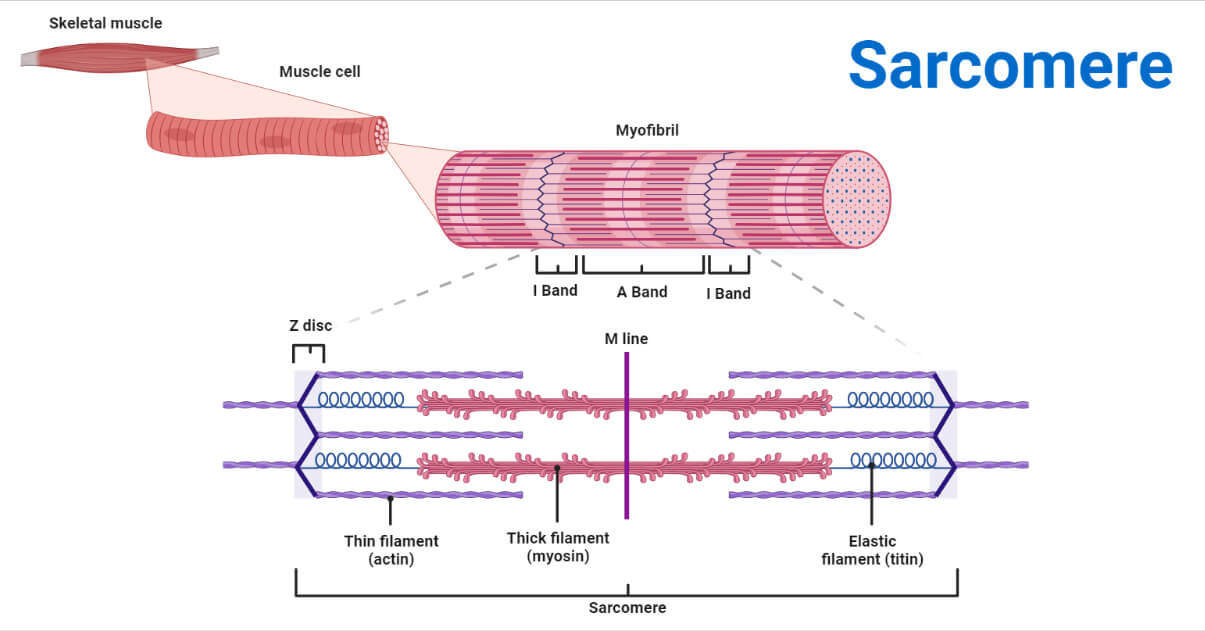
Sarcomere: Structure, Function & Role in Muscle Contraction
(이미지: Sarcomere의 상세 구조 - 밴드와 필라멘트 배열.)
Slide 4: 슬라이딩 필라멘트 모델 (Sliding Filament Model)
- 메커니즘: 수축 시 필라멘트 길이不变, 슬라이딩으로 오버랩 증가.
- 증거:
- 광학/EM: A 밴드 길이 일정, I/H 단축.
- X-ray: 분자 간격不变.
- 크로스브릿지 사이클: Myosin 헤드가 actin에 결합-변형-분리 반복, ATP 가수분해로 힘 생성.
- 그림 설명: 휴지 → 수축 상태 전환 (Fig. 7-5).
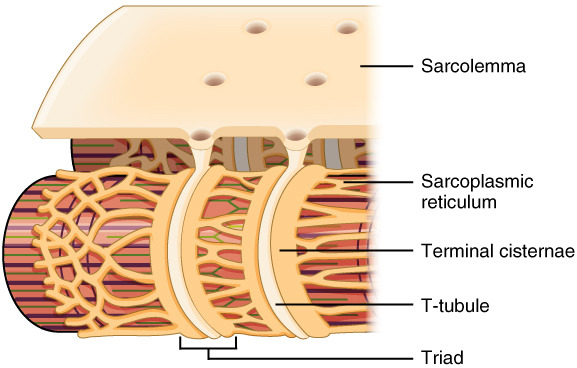
1. 전체 그림 구조 개요
- Sarcolemma (근육막): 가장 바깥쪽 세포막. 전기 신호(활동전위, action potential)가 전달되는 출발점.
- T-tubule (횡관, transverse tubule): sarcolemma가 근육 섬유 내부로 깊이 함입된 관 모양 구조. A 밴드와 I 밴드 경계(A-I junction) 근처에 위치.
- Sarcoplasmic reticulum (SR, 근소포체): 근육 섬유 내부의 특화된 소포체. Ca²⁺(칼슘 이온)를 저장하는 주요 저장소.
- Terminal cisternae (종단 시스턴네): SR의 확대된 끝부분. T-tubule 양쪽에 하나씩 붙어 triad를 형성.
- Triad (삼중체): T-tubule 1개 + terminal cisternae 2개가 나란히 붙은 구조. 골격근에서 가장 중요한 신호 전달 단위.
2. 주요 구성 요소 라벨링 설명
- Sarcolemma → 표면 막. 신경 말단에서 오는 신호를 받아 활동전위 발생.
- T-tubule → 깊숙이 침투한 관. 활동전위를 근육 섬유 중심부까지 빠르게 전달 (전기적 신호 전달).
- Sarcoplasmic reticulum → 네트워크처럼 퍼져 있는 막 구조. Ca²⁺ 저장.
- Terminal cisternae → SR의 bulb 모양 확대부. 여기서 Ca²⁺가 가장 많이 저장됨.
- Triad → T-tubule + 양쪽 terminal cisternae. 이곳에서 전기 신호 → 화학 신호(Ca²⁺ 방출)로 변환됨.
3. 기능적 의미: Excitation-Contraction Coupling 과정
- 신경 말단 → neuromuscular junction에서 ACh 방출 → sarcolemma 탈분극 → 활동전위 발생.
- 활동전위가 sarcolemma → T-tubule 을 따라 빠르게 전파 (근육 섬유 깊숙이까지 도달, 지연 없이).
- T-tubule 막의 DHPR (dihydropyridine receptor, voltage-gated Ca²⁺ channel) 이 전압 감지 → 기계적 coupling.
- DHPR가 인접한 RYR1 (ryanodine receptor) (terminal cisternae에 위치) 을 물리적으로 활성화.
- RYR1 열림 → terminal cisternae 에서 대량의 Ca²⁺ 방출 → sarcomere 내로 확산.
- Ca²⁺가 troponin C 에 결합 → tropomyosin 이동 → actin-myosin 결합 허용 → cross-bridge cycle → 근육 수축.
- 이완 시: Ca²⁺가 SR로 재흡수 (SERCA 펌프) → 수축 종료.
→ Triad는 전기 신호를 화학 신호(Ca²⁺)로 변환하는 핵심 구조로, 밀리초 단위의 빠른 수축을 가능하게 합니다.
4. 왜 중요한가? (골격근 특성)
- 골격근은 cardiac muscle과 달리 T-tubule이 잘 발달되어 triad가 명확.
- Cardiac muscle은 diad (T-tubule 1개 + SR 1개) 구조로, Ca²⁺ 유입이 더 중요.
- Triad 덕분에 근육 섬유 전체가 거의 동시에 수축 → 힘을 강하고 빠르게 발생.
5. 시각적 보완 (비슷한 그림들)
아래는 유사한 구조를 보여주는 그림들입니다. (검색 기반으로 선별)
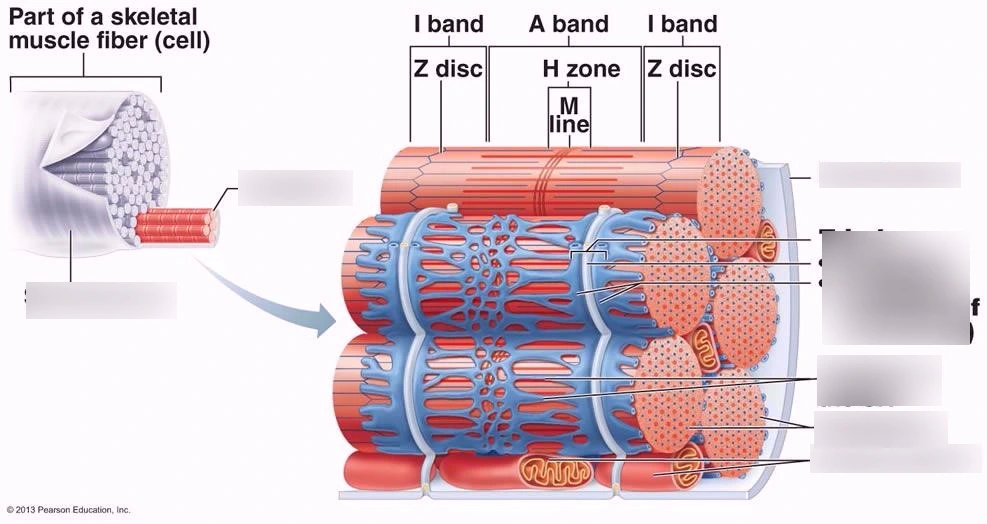
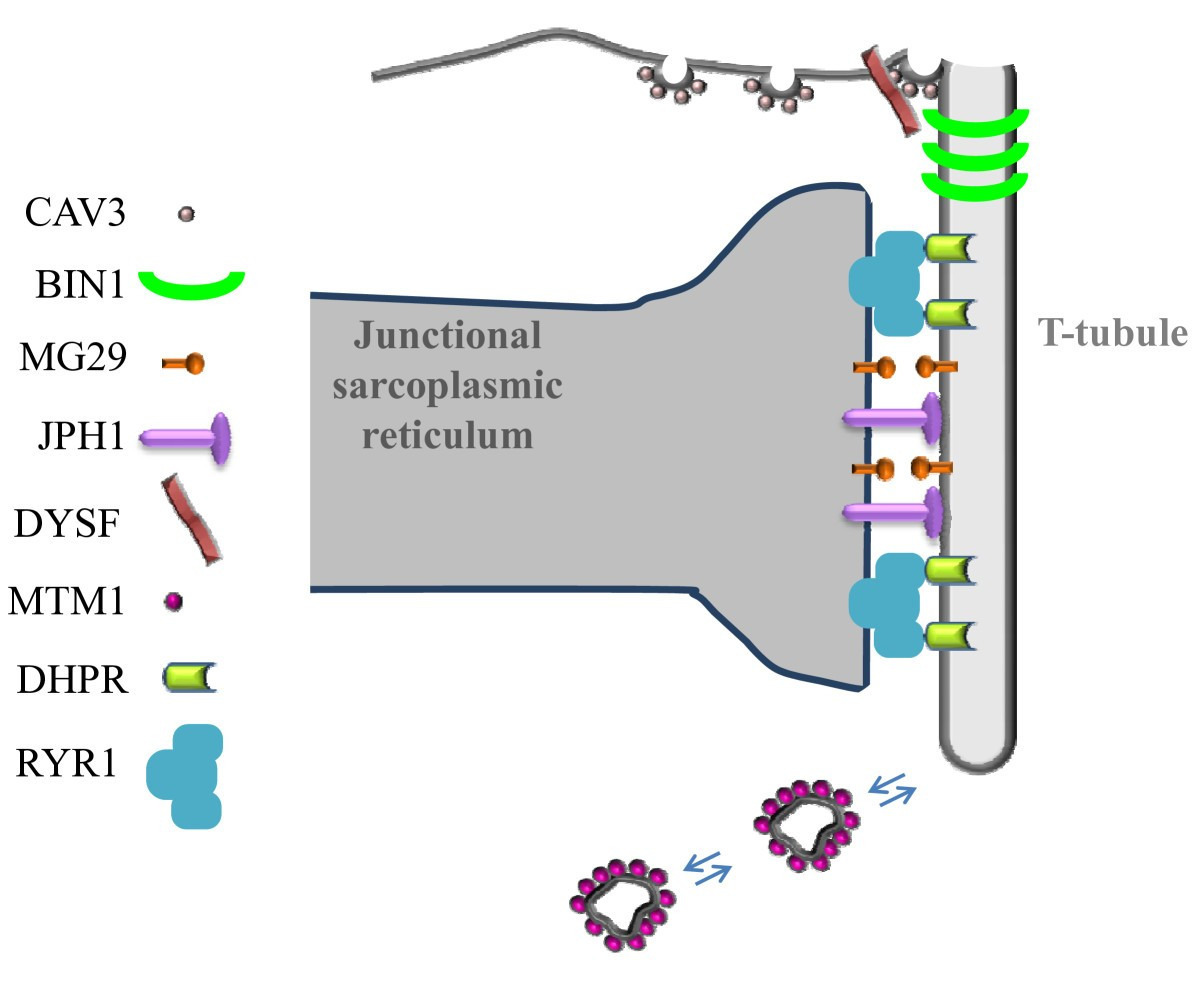
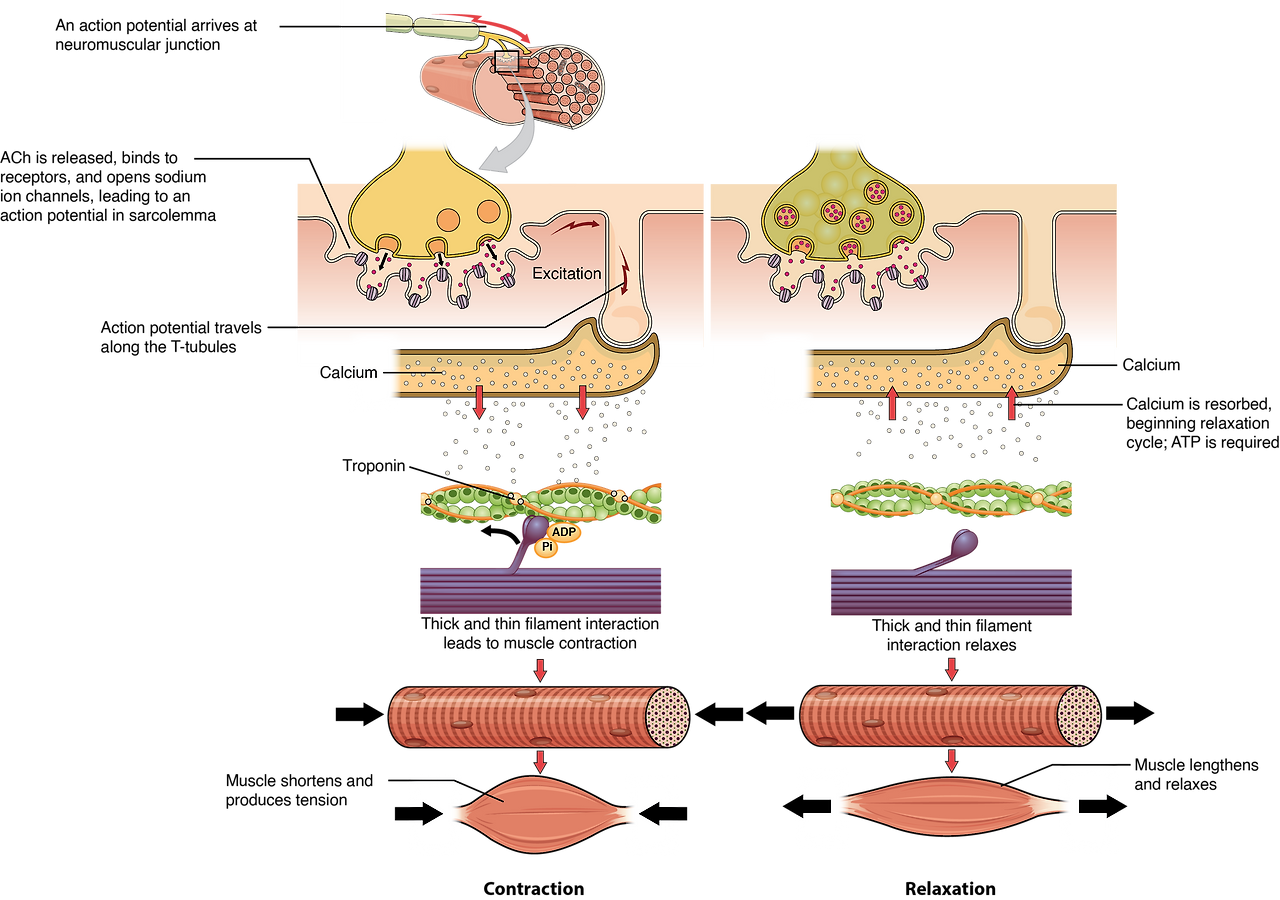
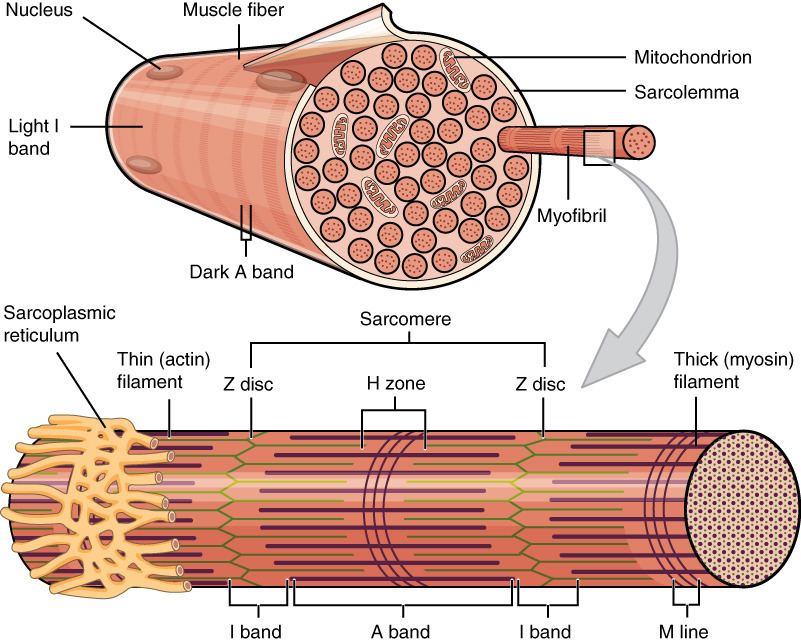
(이 그림들은 triad의 3D-like 배치, 단백질 위치, excitation-contraction coupling 과정을 더 잘 보여줍니다.)
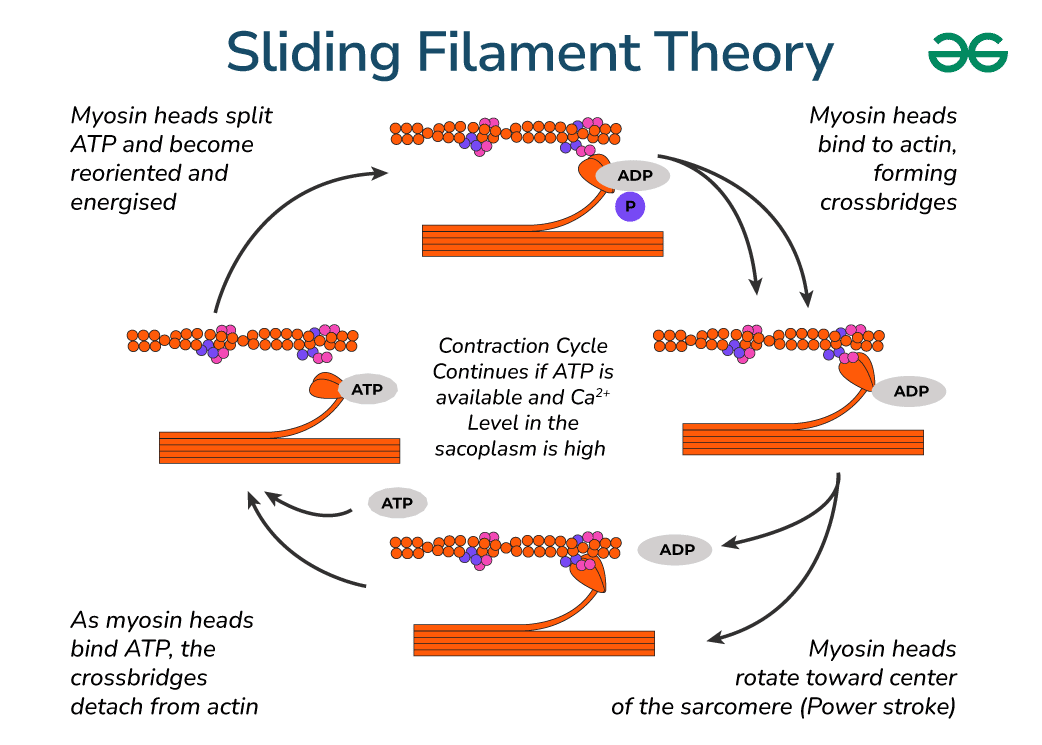
전체 사이클 개요
- 주요 플레이어:
- Thin filament: Actin (주황색 구슬처럼 보이는 것) + tropomyosin/troponin (Ca²⁺ 의존적 조절).
- Thick filament: Myosin (헤드 부분이 주황색 팔처럼 돌출).
- Cross-bridge: Myosin head가 actin에 결합한 상태.
- 에너지원: ATP (아데노신 삼인산) → 가수분해로 에너지 공급.
- 조건: Sarcoplasmic reticulum (SR)에서 Ca²⁺가 방출되어야 시작 (triad에서 온 신호).
- 결과: Thin filament가 thick filament 위로 미끄러지며 사르코미어 길이 단축 → 근육 수축.
단계별 설명 (그림의 순환 화살표 따라 번호 매김)
- Myosin head가 ATP를 가수분해하고 energized 상태
- Myosin head가 ATP를 분해 → ADP + Pi (무기인산) 방출.
- 이 과정에서 head가 high-energy conformation (높은 에너지 상태)으로 재배향 (cocked position).
- 그림: 왼쪽 위 → "Myosin heads split ATP and become reoriented and energized" 부분. → ATP가 에너지를 저장한 "스프링"처럼 head를 준비시킴.
- Myosin head가 actin에 결합 → cross-bridge 형성
- Energized head가 actin의 결합 사이트에 붙음 (Ca²⁺가 tropomyosin을 이동시켜 사이트 노출된 상태).
- 그림: 오른쪽 위 → "Myosin heads bind to actin, forming crossbridges". → Pi (P)가 아직 붙어 있음.
- Power stroke (힘 발생 행정)
- Pi가 방출되면서 myosin head가 회전 (rotate toward center of sarcomere).
- 이 회전으로 thin filament를 Z-line 쪽으로 끌어당김 (sliding).
- 그림: 아래쪽 → "Myosin heads rotate toward center... (Power stroke)". → ADP가 아직 붙어 있음. 이 단계가 실제 힘을 생성하는 순간!
- Cross-bridge detachment (분리)
- 새로운 ATP가 myosin head에 결합 → affinity 변화로 actin에서 떼어짐.
- 그림: 왼쪽 아래 → "As myosin heads bind ATP, the crossbridges detach from actin". → ATP가 없으면 rigor mortis처럼 붙은 상태 유지 (죽은 후 근육 경직).
- Cycle restart (사이클 반복)
- ATP 가수분해 → 다시 energized 상태로 돌아감 (1단계로 복귀).
- 그림: 전체 화살표가 순환. → ATP와 Ca²⁺가 충분하면 계속 반복 → 지속 수축 (tetanus). → Ca²⁺ 낮아지면 troponin-tropomyosin이 사이트 차단 → 이완.
그림에서 강조된 핵심 포인트
- Ca²⁺ 의존성: "Continues if ATP is available and Ca²⁺ level in the sarcoplasm is high" → Ca²⁺ 없으면 cross-bridge 형성 불가 (이완 상태).
- ATP 역할: ① Energizing, ② Detachment, ③ Cycle 유지 → ATP 고갈 시 수축 불가.
- 슬라이딩 결과: Thick filament 길이不变, thin filament가 중앙으로 끌려들어감 → I-band와 H-zone 단축, A-band不变 (Fig. 7-1, 7-5 참조).
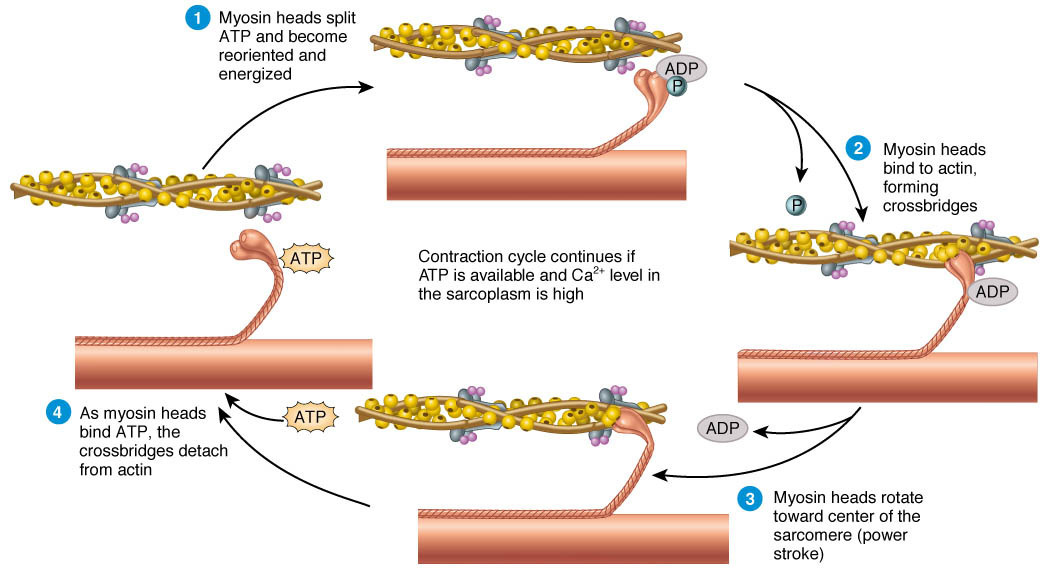
(이미지: Sliding filament cycle과 myosin-actin 상호작용.)
Slide 5: Thick 필라멘트 (Thick Filament)
- 구조: Bipolar, 1.6 μm, 15 nm, ~300 myosin 분자.
- Myosin: 2 heavy chain (223 kDa), 4 light chain; 헤드(ATPase)와 tail.
- 조립: Antiparallel bare zone, parallel 추가 (Fig. 7-9).
- 헤드 배열: 3-strand helix, 14.3 nm 간격, 43 nm 반복 (Fig. 7-12).
- 백본: Myosin tail 팩킹, subfilament 모델 (Fig. 7-15).
- MyBP-C 등: C-zone 스트라이프, 구조/조절 역할.
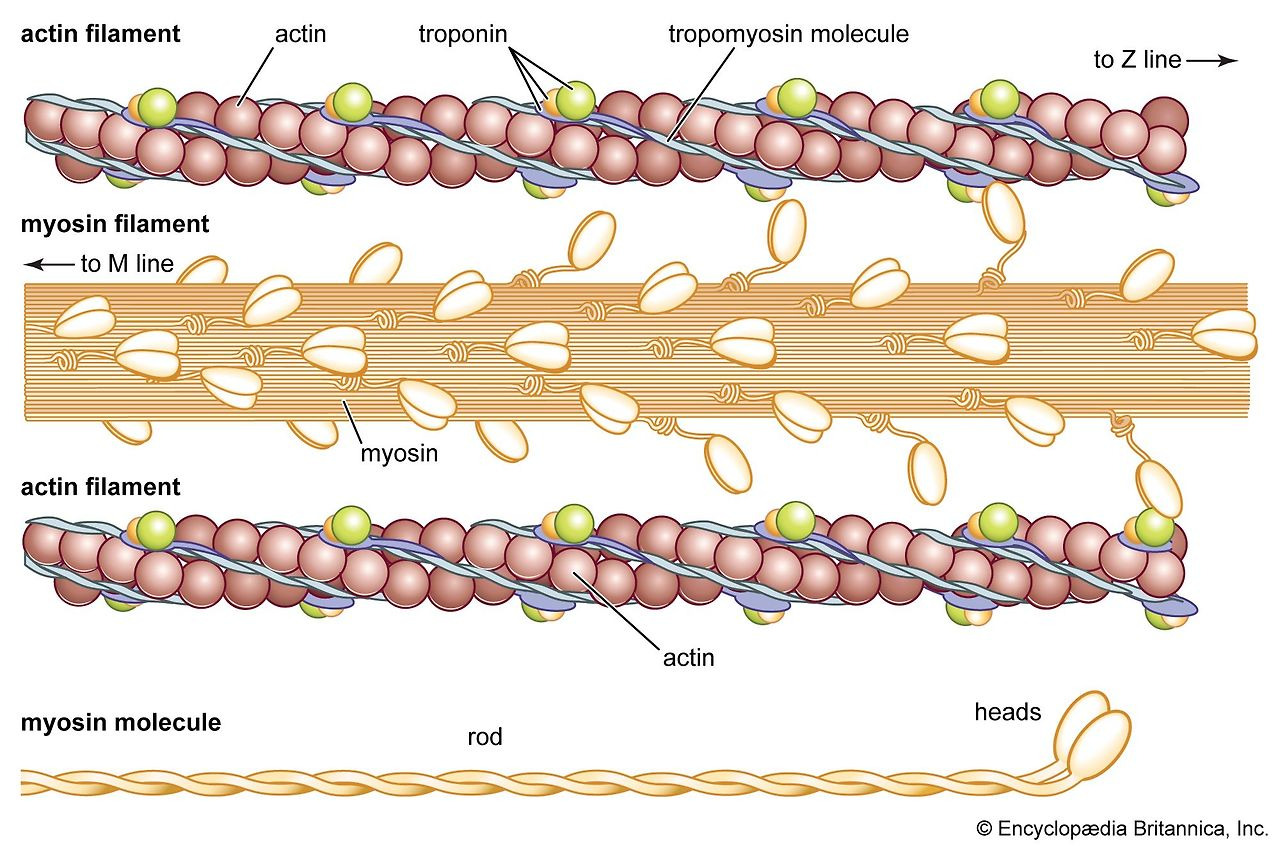
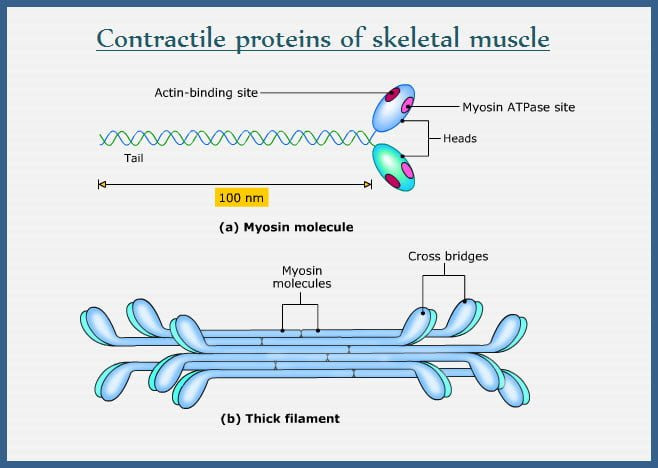
(이미지: Myosin 구조와 thick 필라멘트.)
Slide 6: M 라인 (M Line)
- 구조: Thick 필라멘트 연결, 80 nm 폭, 3-5 라인 (Fig. 7-21).
- 단백질: Myomesin, M protein, creatine kinase.
- 모델: Myomesin이 브릿지 형성, titin/myosin 연결.
- 기능: A 밴드 안정화, ATP 버퍼.
Slide 7: Titin 필라멘트 (Titin Filaments)
- 구조: 3 MDa, 1 μm 길이, Z-M 스팬 (Fig. 7-22).
- 모듈: Ig/Fn 도메인, PEVK (탄성).
- 기능: 사르코미어 템플릿 (조립), 탄성 (I-band, Fig. 7-23).
- 아이소폼: Cardiac/skeletal 다름, 수동 장력 조절.
Slide 8: Thin 필라멘트 (Thin Filament)
- Actin: G-actin → F-actin (double helix, polar, Fig. 7-24).
- Tropomyosin: Coiled-coil, actin groove 따라.
- Troponin: TnC (Ca-binding), TnI (inhibitory), TnT (binding, Fig. 7-30).
- Nebulin: 길이 결정 (Fig. 7-36).
- 캡핑: CapZ (barbed), Tmod (pointed, Fig. 7-37).
Slide 9: 조절 메커니즘 (Regulation)
- Steric blocking 모델: Low Ca - Tm 외부 도메인, myosin 차단; High Ca - 내부 이동, 노출 (Fig. 7-33, 7-34).
- Troponin 역할: Ca 결합 → TnI-actin 분리 → Tm 이동 (Fig. 7-35).
- 협력적: Myosin 강결합 추가 이동 유도.
Slide 10: Z 라인 (Z Line)
- 구조: Thin 필라멘트 연결, 지그재그/바스켓 (Fig. 7-38).
- 단백질: α-actinin (cross-link), titin, nebulin 등 (Fig. 7-39).
- 기능: 필라멘트 정렬, 힘 전달.
Slide 11: 중간 필라멘트 (Intermediate Filaments)
- 구조: 10 nm, Z 라인 둘러싸고 myofibril 연결 (Fig. 7-40).
- 단백질: Desmin, synemin, plectin.
- 기능: 세포 강화, 힘 전달, myofibril 정렬.
Slide 12: 사르코미어 관련 질환 (Diseases of the Sarcomere)
- FHC (Familial Hypertrophic Cardiomyopathy): Sarcomeric 단백질 돌연변이 (myosin, TnT, MyBP-C 등).
- 기타: Nemaline myopathy (actin, Tm, nebulin), Desmin myopathy.
- 메커니즘: Poison polypeptide → 사르코미어 불안정 → 비대/부정맥.
Slide 13: 결론 (Conclusion)
- 사르코미어: 모듈러 단백질 기반의 정교한 기계.
- 구조 이해 → 수축 메커니즘, 발달, 질환 해명.
- 미래 연구: 고해상도 구조 (cryo-EM), 돌연변이 치료.