

- nature
- spinal cord
- review articles
- article
Clinical signs and symptoms for degenerative cervical myelopathy: a scoping review of case-control studies to facilitate early diagnosis among healthcare professionals with stakeholder engagement
- Review Article
- Open access
- Published: 26 February 2025
Clinical signs and symptoms for degenerative cervical myelopathy: a scoping review of case-control studies to facilitate early diagnosis among healthcare professionals with stakeholder engagement
Spinal Cord volume 63, pages171–180 (2025)Cite this article
Abstract
Study design
Scoping Review.
Objective
Degenerative cervical myelopathy (DCM) is a leading cause of chronic spinal cord dysfunction, with diverse clinical presentations that complicate diagnosis. Therefore, it is important to identify the signs and symptoms of DCM that demonstrate high diagnostic accuracy. This review aims to evaluate the sensitivity and specificity of signs and symptoms in diagnosing DCM.
Methods
Articles up to June 2024 were retrieved from PubMed, EMBASE, and Cochrane databases using search terms like “degenerative cervical myelopathy”, “cervical spondylotic myelopathy”, “sensitivity”, “specificity”, and related signs and symptoms. Studies were screened based on selection criteria assessing the sensitivity and specificity of signs or symptoms using an appropriate control group.
Results
Sixteen studies were included. The most sensitive signs were Tromner sign (93–97%) and hyperreflexia (15–85%). Specific signs included the Babinski sign (93–100%), Tromner sign (79–100%), clonus (96–99%), and inverted supinator sign (78–99%). Neck pain had a sensitivity of 76–94% and specificity of 11–73%. Hand incoordination showed 52% sensitivity and 92% specificity. Altered hand sensation had 76% sensitivity and 90% specificity. Upper extremity weakness had 51–75% sensitivity and 18–95% specificity. Gait imbalance exhibited 56–63% sensitivity and 52–95% specificity.
Conclusion
Sensitive signs like the Tromner sign and hyperreflexia are useful for screening, while specific signs such as Babinski, clonus, and the inverted supinator sign aid in confirmation of DCM. Symptoms like neck pain, hand incoordination, and altered hand sensation should heighten suspicion and guide differential diagnosis. Early and accurate diagnosis using these indicators can improve patient outcomes and reduce diagnostic delays.
목적
퇴행성 경추 척수증(DCM)은
만성 척수 기능 장애의 주요 원인이며,
다양한 임상 증상으로 진단이 복잡합니다.
따라서
높은 진단 정확도를 보이는 DCM의 징후와 증상을 식별하는 것이 중요합니다.
본 검토는 DCM 진단에서 징후와 증상의 민감도와 특이도를 평가하는 것을 목표로 합니다.
방법
2024년 6월까지의 논문들을 PubMed, EMBASE, Cochrane 데이터베이스에서 “퇴행성 경추성 척수증”, “경추 척추증성 척수증”, ‘민감도’, “특이도” 및 관련 징후와 증상을 검색어로 검색하였다. 적절한 대조군을 사용하여 징후나 증상의 민감도와 특이도를 평가한 연구들을 선별 기준으로 검토하였다.
결과
16건의 연구가 포함되었다.
가장 민감한 징후는
트롬너 징후(93–97%)와 과반사(15–85%)였다.
https://www.youtube.com/watch?v=kE40_tx2SeI

특이적인 징후로는
바빈스키 징후(93–100%), 트롬너 징후(79–100%),
경련반사(96–99%), 역상완근 징후(78–99%)가 있었다.
목 통증은
민감도 76~94%, 특이도 11~73%를 보였다.
손 운동 불협응은
민감도 52%, 특이도 92%를 나타냈다.
손 감각 이상은 민감도 76%,
특이도 90%였다.
상지 근력 약화는 민감도 51~75%,
특이도 18~95%를 보였다.
보행 불균형은 56–63%의 민감도와 52–95%의 특이도를 나타냈다.
결론
트롬너 징후 및 과반사와 같은 민감한 징후는 선별 검사에 유용한 반면,
바빈스키 반사, 클로누스, 역전된 회전근 징후와 같은 특이적인 징후는
퇴행성 경추 척수병증(DCM)의 확인에 도움이 된다.
목 통증, 손의 운동 조정 장애, 손 감각 이상과 같은 증상은 의심을 높이고 감별 진단을 안내해야 한다. 이러한 지표를 활용한 조기 및 정확한 진단은 환자 예후를 개선하고 진단 지연을 줄일 수 있다.
Similar content being viewed by others

Article Open access09 October 2021
Decreased angiogenesis as a possible pathomechanism in cervical degenerative myelopathy
Article Open access28 January 2021
Article Open access21 December 2023
Introduction
Degenerative cervical myelopathy (DCM) is a progressive neck region spinal condition first introduced in 2015 and the leading cause of chronic, non-traumatic spinal cord dysfunction worldwide [1, 2]. Despite its prevalence, the diagnosis of DCM remains a significant challenge for practitioners due to its diverse clinical presentations [3, 4]. Consequently, DCM is frequently misdiagnosed, leading to delays in specialist assessment and appropriate management. These diagnostic delays can result in severe consequences, including incomplete post-operative recovery, diminished quality of life, and significant disability, such as the inability to work [5,6,7]. Research indicates that 20–62% of DCM patients experience clinical deterioration within 3–6 years if surgical intervention was not performed [8]. While surgical treatment is often recommended, patient outcomes depend on the severity of preoperative functional impairment and the duration of symptoms [9,10,11]. A retrospective study reported that the average time from symptom onset to DCM diagnosis was 2.2 ± 2.3 years [12]. Given the potential for disease progression, prompt diagnosis and timely referral to a specialist are essential to optimize patient outcomes [13]. While DCM’s firm diagnosis requires a clinical radiological concordance (Fig. 1), the importance of DCM suspicion and a sensitivity to considering it as a differential diagnosis in non-specialist situations is an imperative.
서론
퇴행성 경추 척수증(DCM)은
2015년에 처음 소개된 진행성 경추 척추 질환으로,
전 세계적으로 만성 비외상성 척수 기능 장애의 주요 원인이다[1, 2].
그 유병률에도 불구하고,
DCM의 진단은 다양한 임상 증상으로 인해
결과적으로
DCM은 종종 오진되어 전문의 평가 및 적절한 치료가 지연된다.
이러한 진단 지연은
수술 후 불완전한 회복, 삶의 질 저하, 근로 불능과 같은
중대한 장애 등 심각한 결과를 초래할 수 있다[5,6,7].
연구에 따르면,
수술적 개입이 이루어지지 않은 경우
DCM 환자의 20~62%가 3~6년 이내에 임상적 악화를 경험하는 것으로 나타났습니다[8].
수술적 치료가 종종 권장되지만,
환자의 예후는 수술 전 기능적 장애의 중증도와 증상 지속 기간에 따라 달라집니다[9,10,11].
한 후향적 연구에 따르면
증상 발현부터 DCM 진단까지의 평균 기간은
2.2±2.3년 [12].
질병 진행 가능성을 고려할 때,
환자 예후를 최적화하기 위해서는 신속한 진단과 전문의로의 적시 의뢰가 필수적이다[13].


DCM의 확정적 진단에는 임상적·방사선학적 일치(그림 1)가 필요하지만,
비전문 환경에서 DCM을 의심하고 감별진단으로 고려하는
민감성을 갖는 것이 매우 중요하다.
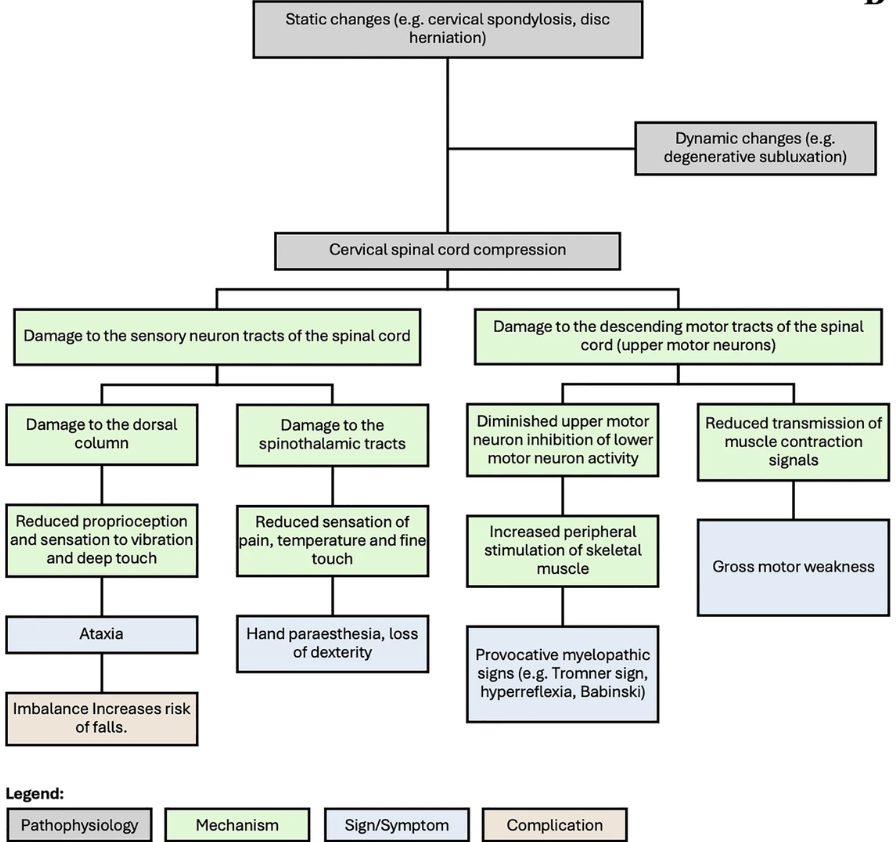
Fig. 1: MRI Findings and Pathophysiological Overview of DCM.
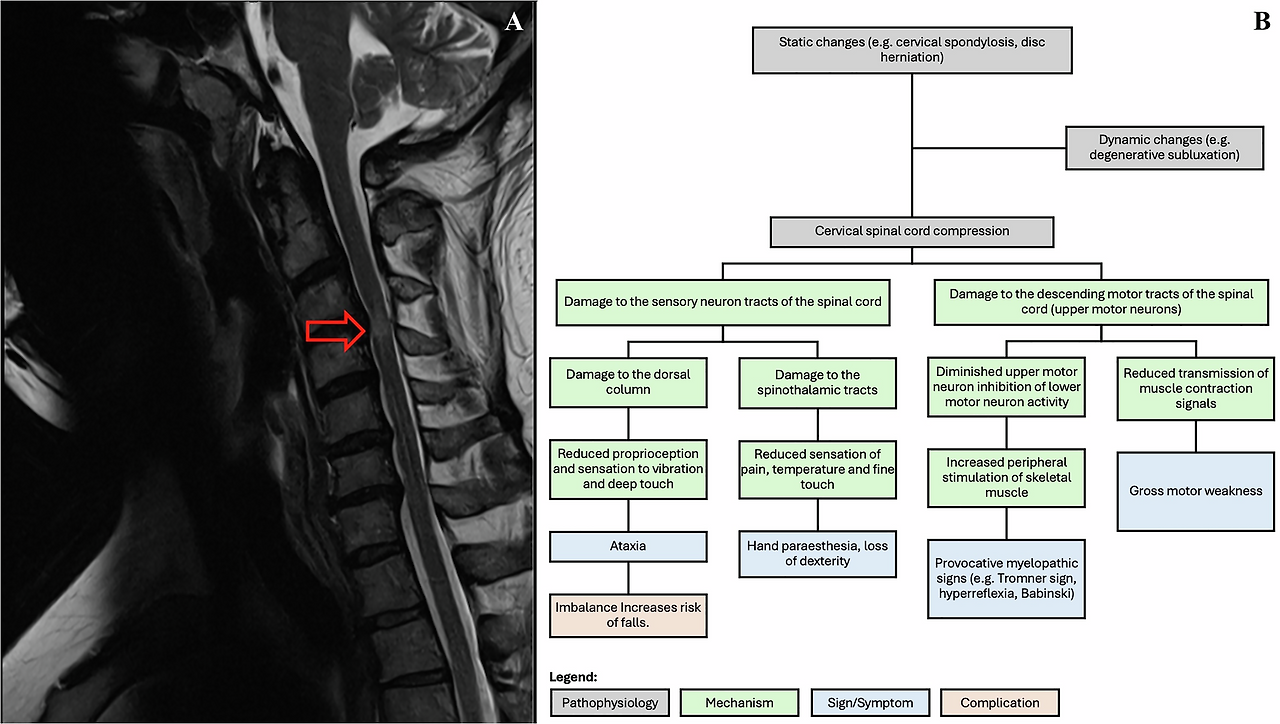
A T2-weighted sagittal MRI of a 45-year-old male with DCM, showing signal cord changes (indicated by red arrow). B An overview of the pathophysiological mechanisms, signs, symptoms, and complications associated with cervical spinal cord compression, including both static and dynamic changes.
To evaluate the clinical utility of signs and symptoms in diagnosing DCM, it is essential to assess their sensitivity and specificity. Sensitivity refers to a clinical sign’s ability to correctly identify patients with DCM, calculated as the proportion of true positives among all patients with the condition. Specificity measures a sign’s effectiveness in correctly identifying patients without DCM, based on the proportion of true negatives among all patients without the condition [14]. These metrics ensure that healthcare professionals make informed decisions, thereby improving patient outcomes through timely and accurate diagnosis.
While systematic reviews and meta-analysis are an important part of translating research to practice, a lack of stakeholder engagement can be a significant obstacle, potentially hindering the implementation of research findings within clinical settings. This scoping review aims to synthesize current research and clinical findings to identify the clinical signs and symptoms of DCM with high diagnostic accuracy, addressing the need for stakeholder engagement in translating research to practice.
DCM 진단에서 징후와 증상의 임상적 유용성을 평가하려면 그 민감도와 특이도를 평가하는 것이 필수적이다. 민감도는 임상 징후가 DCM 환자를 정확히 식별하는 능력을 의미하며, 해당 질환을 가진 모든 환자 중 진양성(true positive)의 비율로 계산됩니다. 특이도는 DCM이 없는 환자를 정확히 식별하는 징후의 효과를 측정하며, 해당 질환이 없는 모든 환자 중 진음성(true negative)의 비율을 기반으로 합니다 [14]. 이러한 지표들은 의료진이 정보에 기반한 결정을 내리도록 보장하여, 시기적절하고 정확한 진단을 통해 환자 예후를 개선합니다.
체계적 문헌고찰과 메타분석은 연구를 실무에 적용하는 데 중요한 부분이지만, 이해관계자 참여 부족은 임상 현장에서 연구 결과를 적용하는 데 잠재적 장애물이 될 수 있다. 본 탐색적 문헌고찰은 현재의 연구 및 임상 결과를 종합하여 진단 정확도가 높은 DCM의 임상 징후와 증상을 규명하고, 연구를 실무에 적용하는 과정에서 이해관계자 참여의 필요성을 다루고자 한다.
Methods
Identifying relevant studies
To systematically identify relevant studies on the clinical signs and symptoms of DCM and their diagnostic accuracy, a comprehensive search strategy following the Preferred Reporting Items for Systematic Reviews and Meta-Analysis Extension for Scoping Reviews (PRISMA-ScR) statement was employed across multiple databases, including PubMed, EMBASE, and Cochrane [15]. Publications were retrieved up to June 2024. The search terms were selected to include both MeSH and Emtree terms and free-text keywords, ensuring a broad capture of pertinent literature. The search strategy combined terms for the condition (e.g., “degenerative cervical myelopathy” and “cervical spondylotic myelopathy”) with terms related to clinical signs and symptoms. Diagnostic accuracy terms such as “sensitivity” and “specificity” were incorporated to focus on relevant studies. To exclude irrelevant studies, terms related to imaging techniques (e.g., “MRI” and “CT scan”) were excluded. Only English-language studies were included.
관련 연구 식별
DCM의 임상적 징후 및 증상과 그 진단 정확도에 관한 관련 연구를 체계적으로 식별하기 위해, PubMed, EMBASE, Cochrane 등 여러 데이터베이스에 걸쳐 체계적 문헌고찰 및 메타분석을 위한 선호 보고 항목 확장(PRISMA-ScR) 지침을 따른 포괄적인 검색 전략을 적용하였다[15]. 2024년 6월까지의 출판물을 검색하였다. 검색어는 MeSH 및 Emtree 용어와 자유 텍스트 키워드를 모두 포함하도록 선정하여 관련 문헌을 폭넓게 포착할 수 있도록 하였다.
검색 전략은 질환 관련 용어(예: “퇴행성 경추 척수병증” 및 “경추 척추증성 척수병증”)와 임상 징후 및 증상 관련 용어를 결합하였다. 관련 연구에 집중하기 위해 “민감도” 및 “특이도”와 같은 진단 정확도 용어를 포함시켰습니다. 관련 없는 연구를 배제하기 위해 영상 기법 관련 용어(예: ‘MRI’ 및 “CT 스캔”)는 제외했습니다. 영어로 된 연구만 포함했습니다.
Eligibility criteria
Table 1 outlines the inclusion and exclusion criteria for selecting the studies included in this review. Table 2 describes the results of individual studies assessing the diagnostic accuracy of clinical signs and symptoms of DCM.
Table 1 Inclusion and exclusion criteria.
CharacteristicInclusionExclusion
| Population | ‐ Patient with cervical myelopathy ‐ Patients 18 years old or more | ‐ Patients with spondylosis but do not exhibit myelopathy ‐ Thoracic or lumbar myelopathy ‐ Patients with traumatic cervical spinal cord injury ‐ Patients with tumour or infection |
| Clinical sign | ‐ Tromner’s’ sign ‐ Babinski ‐ Hoffmann ‐ Clonus ‐ Inverted supinator ‐ Hyperreflexia (biceps, triceps, patella, brachioradialis, Achilles) ‐ Tandem gait ‐ Other clinical signs | ‐ Studies using imaging modalities to diagnose DCM ‐ Patient (e.g., neck disability index, Visual Analog Scale, SF-36) or clinician (e.g., Nurick grade, mJOA score) reported outcome measures |
| Symptom | ‐ Neck pain ‐ Autonomic dysfunction ‐ Hand numbness ‐ Hand paraesthesia ‐ Upper extremity weakness ‐ Loss of dexterity(손재주 장애) ‐ Other symptoms | |
| Outcomes | ‐ Sensitivity and specificity of clinical signs and symptoms | ‐ Studies reporting only frequencies for clinical signs and symptoms |
| Study Design | ‐ Case – controlled studies with suitable control groups (e.g., individuals with cervical radiculopathy or axial neck pain who do not exhibit myelopathic symptoms) | ‐ Review articles ‐ Studies with no control group ‐ Animal studies ‐ Case series, reports |
Table 2 Results of individual studies assessing the diagnostic accuracy of clinical signs and symptoms in DCM.
Clinical SignAuthorsSensitivity (%)Specificity (%)
| Tromner’s sign | Chaiyamongkol et al. [26] | 94 | 79 |
| Chang et al. [23] | 93.5 | 100 | |
| Soufi et al. [34] | 97 | 35 | |
| Babinski | Chaiyamongkol et al. [26] | 36 | 100 |
| Cook et al. [19] | 7 | 100 | |
| Cook et al. [18] | 33 | 93 | |
| Rhee et al. [24] | 13 | 100 | |
| Harrop et al. [28] | 44 | Not reported | |
| Hoffmann | Cao et al. [16] | 61.6 | 85.7 |
| Chaiyamongkol et al. [26] | 75 | 93 | |
| Grijalva et al. [30] | 59.2 | 49.5 | |
| Chang et al. [23] | 89.1 | 100 | |
| Cook et al. [19] | 31 | 73 | |
| Cook et al. [18] | 44 | 74 | |
| Rhee et al. [24] | 59 | 84 | |
| Glaser et al. [29] | 58 | 78 | |
| Soufi et al. [34] | 89 | 41 | |
| Harrop et al. [28] | 83 | Not reported | |
| Clonus | Cook et al. [19] | 11 | 99 |
| Cook et al. [18] | 7 | 96 | |
| Rhee et al. [24] | 13 | 100 | |
| Inverted supinator sign | Chaiyamongkol et al. [26] | 75 | 86 |
| Cook et al. [19] | 18 | 99 | |
| Cook et al. [18] | 61 | 78 | |
| Rhee et al. [24] | 51 | 81 | |
| Hyperreflexia | Rhee et al. [24] | 72 | 43 |
| Harrop et al. [28] | 85 | Not reported | |
| Hyperreflexia of the biceps and triceps | Cook et al. [18] | 44 | 70 |
| Hyperreflexia of the biceps | Cook et al. [19] | 18 | 96 |
| Rhee et al. [24] | 62 | 49 | |
| Soufi et al. [34] | 61 | 74 | |
| Hyperreflexia of the triceps | Rhee et al. [24] | 36 | 78 |
| Soufi et al. [34] | 40 | 92 | |
| Hyperreflexia at the patella | Cook et al. [19] | 22 | 97 |
| Rhee et al. [24] | 33 | 76 | |
| Hyperreflexia at the Achilles | Cook et al. [19] | 15 | 98 |
| Rhee et al. [24] | 26 | 81 | |
| Hyperreflexia at brachioradialis | Rhee et al. [24] | 21 | 89 |
| Suprapatellar reflex | Cook et al. [18] | 56 | 33 |
| Absence of deep tendon reflexes | Philips [33] | 13 | 84 |
| Hand withdrawal reflex | Cook et al. [18] | 39 | 63 |
| Gait deviation | Cook et al. [19] | 19 | 94 |
| Tandem gait | Soufi et al. [34] | 66 | 84 |
| Sensory impairment | Harrop et al. [28] | 72 | 88 |
| Philips [33] | 40 | 46 | |
| Motor impairment | Archer et al. [32] | 53 | 64 |
| Philips [33] | 75 | 18 | |
| Weakness and wasting of deltoid muscles and shoulder girdle | Philips [33] | 17 | 88 |
| Grip release test and grip strength | Kobayashi et al. [20] | 88.2 | 78.1 |
| 10 s step test | Machino et al. [31] | 92.3 | 67.8 |
| 10 s grip and release test | Machino et al. [31] | 77.3 | 58.8 |
SymptomAuthorsSensitivity (%)Specificity (%)
| Neck pain | Soufi et al. [34] | 81 | 73 |
| Cheung et al. [35] | 76 | 11 | |
| Cook et al. [18] | 93 | 18 | |
| Neck stiffness | Hori et al. [36] | 11 | 87 |
| Gait abnormalities/disturbance | Soufi et al. [34] | 63 | 95 |
| Cook et al. [18] | 56 | 52 | |
| Autonomic dysfunction | Soufi et al. [34] | 24 | 95 |
| Loss of dexterity | Cook et al. [18] | 72 | 26 |
| Soufi et al. [34] | 52 | 92 | |
| Hand numbness | Cook et al. [18] | 57 | 67 |
| Hand paraesthesia | Soufi et al. [34] | 76 | 90 |
| Upper extremity weakness | Soufi et al. [34] | 51 | 95 |
| Numbness | Hori et al. [36] | 61 | 60 |
| Pain | Hori et al. [36] | 61 | 60 |
| Tremor | Hori et al. [36] | 11 | 93 |
| Cervical vertigo | Hori et al. [36] | 6 | 87 |
| Hypalgesia | Hori et al. [36] | 6 | 87 |
| Jitteriness | Hori et al. [36] | 0 | 93 |
| Apraxia | Hori et al. [36] | 6 | 93 |
| Difficulty lifting heavy objects | Soufi et al. [34] | 75 | 87 |
| Heightened neck pain when driving or reading | Soufi et al. [34] | Driving: 70 Reading: 71 | Driving: 90 Reading: 78 |
Data extraction
Following the search process detailed in Fig. 2, data was extracted from relevant studies included in this scoping review. The key data extracted from each study included the authors, year of publication, title, study design, patient demographics, and the reported symptoms and clinical signs associated with DCM. Additionally, the sensitivity and specificity of each clinical sign and symptom were extracted for inclusion in the results section.
Fig. 2: Literature Search Flowchart.
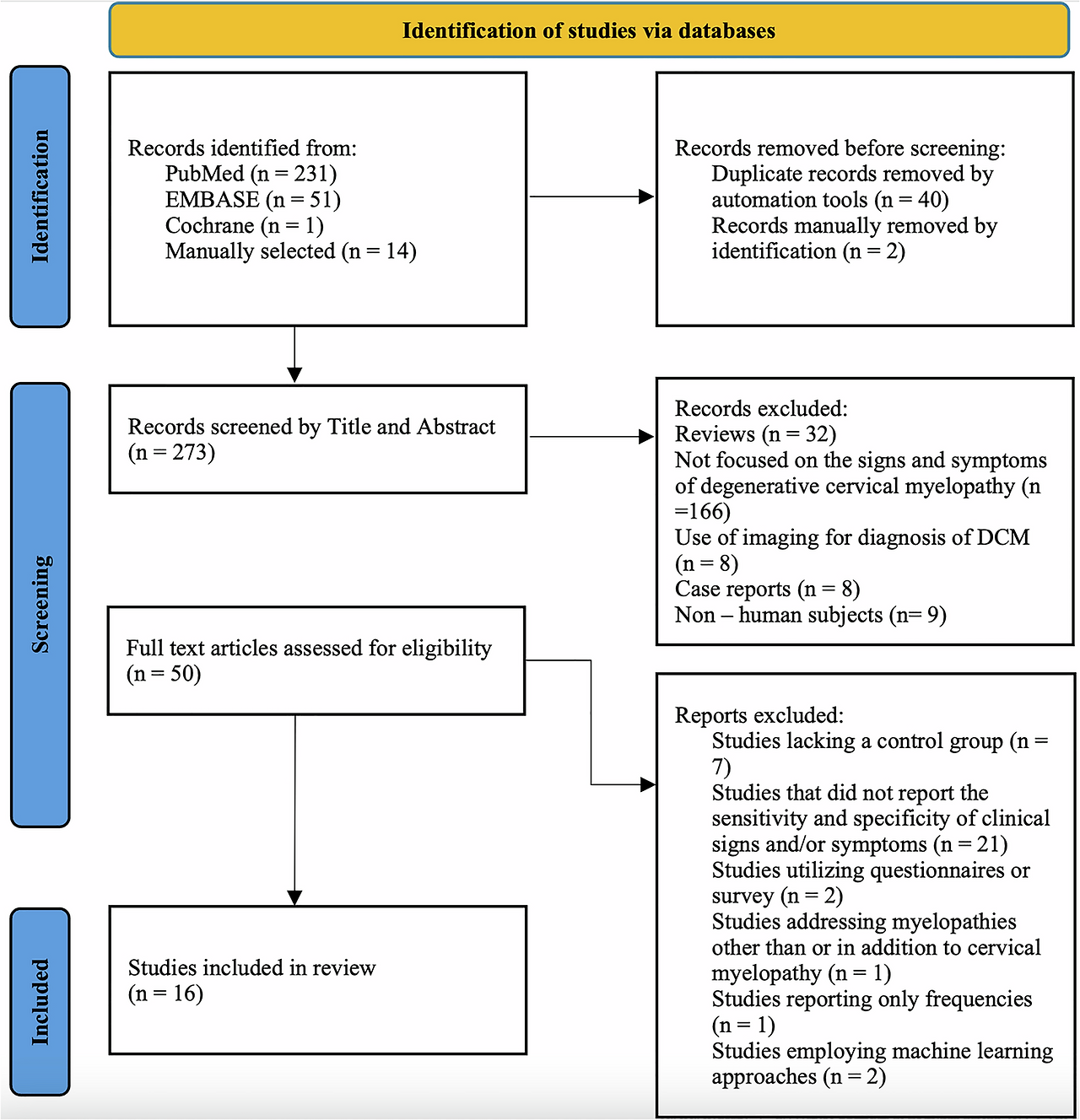
Adapted from PRISMA Scoping Review protocol.
Collection of codes
Research articles on clinical signs and symptoms for DCM [16,17,18,19,20,21,22,23,24,25,26] were distributed via email to neurosurgeons and spine surgeons (n = 11). The collection of codes involved systematically identifying relevant clinical signs and symptoms of DCM from the included studies as detailed in Table 3 to develop evidence-based clinical recommendations for DCM. These codes were refined through discussions among the research team, focusing on clarity, naming conventions, and relationships between codes, as outlined by Mak and Thomas [27].
Table 3 Codebook for diagnostic clinical signs and symptoms in DCM.
Code No.Code LabelDescriptionExcerpt TextComments
| 1 | Clinical Diagnosis | The process of diagnosing degenerative cervical myelopathy based on patient history, physical examination, and imaging studies. | ‐ “Despite significant advances in the understanding of the disorder, cervical myelopathy remains a clinical diagnosis. Commonly used criteria in establishing the diagnosis include a history of myelopathic complaints, physical examination demonstrating myelopathic signs, and advanced imaging studies showing correlative compression of the cervical cord.” ‐ “While the presence of these clinical signs is helpful, examination findings may be absent entirely and a diagnosis of DCM can still be made using a combination of patient-reported symptoms and imaging findings.” | Emphasizes the importance of clinical diagnosis despite advancements in imaging. |
| 2 | Imaging Confirmation | Any deformation of the cervical spinal cord due to a compressive lesion observed on CT myelogram or MRI. | ‐ “Cervical cord compression was defined as any deformation of the spinal cord due to a compressive lesion on CT myelogram or MRI.” | Imaging evidence is critical for confirming cervical cord compression. |
| 3 | Absence of Upper Motor Neuron Signs | Diagnosis of DCM can still be made even if upper motor neuron signs are absent. | ‐ “The absence of upper motor neuron signs does not rule out a diagnosis of DCM.” | A diagnosis of DCM should not be excluded solely based on the absence of upper motor neuron signs. |
| 4 | Sensitivity of Clinical Tests for DCM | The effectiveness of clinical tests in correctly identifying patients with DCM. | ‐ “The most sensitive clinical tests for diagnosing DCM are the Tromner sign and hyperreflexia.” ‐ “Most sensitive clinical examination: Tromner and hyperreflexia.” | Tromner sign and hyperreflexia are the most effective tests for initial screening of DCM. |
| 5 | Specificity of Clinical Tests for DCM | The effectiveness of clinical tests in correctly identifying patients without DCM. | ‐ “The most specific tests are the Babinski, Tromner sign, clonus and inverted supinator sign.” ‐ “Only the inverted supinator sign and the Babinski sign demonstrated significant diagnostic accuracy.” ‐ “Clonus most specific.” ‐ “Most specific clinical examination: Babinski, Tromner, clonus and inverted supinator sign.” | Babinski, Tromner, clonus, and inverted supinator sign are crucial for confirming DCM diagnosis. |
| 6 | Diagnostic Accuracy of Clinical Signs in DCM Diagnosis | The reliability of specific clinical signs in diagnosing DCM. | ‐ “Only the inverted supinator sign and the Babinski sign demonstrated significant diagnostic accuracy.” ‐ “The most accurate finding to confirm the presence of myelopathy on MRI was the Babinski sign in isolation. Combinations of findings did not improve the diagnostic accuracy of the tests at a rate greater than the standalone test of the Babinski sign.” ‐ “Hoffman may not be present.” ‐ “The Hoffmann sign may modestly increase the predicted probability of cervical spinal cord compression and offer a modest contribution to the overall diagnosis, it is not foolproof for the diagnosis of cervical spinal cord compression.” | Individual signs vary in reliability; combined findings often do not significantly enhance diagnostic accuracy. |
| 7 | Clinical Signs and Disease Severity | The relationship between various clinical signs and the severity of DCM. | ‐ “There was no definite association between Hoffmann sign, Babinski sign or hyperreflexia and disease severity. | Indicates no clear link between certain clinical signs and disease severity. |
| 8 | Clinical Examination Preferences | Preferences for specific clinical signs during examination. | ‐ “I always look for the inverted supinator reflex.” ‐ “Hoffmann and clonus”. | Spine surgeons may have preferences for specific signs, such as the inverted supinator reflex, due to their diagnostic value. |
| 9 | Sensitive Symptoms for DCM | Symptoms with high sensitivity for diagnosing DCM. | ‐ “Hand numbness is frequently reported in DCM patients.” ‐ “Hand paresthesias are a commonly reported symptom in DCM.” ‐ “Loss of dexterity is a sensitive indicator for DCM, particularly in hand function.” ‐ “Neck pain is moderately to highly sensitive for diagnosing DCM, but not specific.” ‐ “Gait abnormalities are often present due to upper motor neuron and proprioceptive dysfunction.” | High sensitivity symptoms should raise suspicion of DCM. |
| 10 | Specific Symptoms for DCM | Symptoms with high specificity for diagnosing DCM. | ‐ “Autonomic dysfunction is a rare but highly specific symptom for DCM.” ‐ “Bladder dysfunction is uncommon but more frequent than bowel or sexual impairment.” | Specific symptoms, though less sensitive, are still crucial to recognise. |
Results
Study selection
A total of 283 articles were identified using the literature search strategy, along with 14 articles selected manually (Fig. 2). Following the removal of 40 duplicate records through automation tools and 2 duplicates manually, 273 records remained. These records (n = 273) were subsequently screened by title and abstract according to the inclusion and exclusion criteria, resulting in 50 articles being selected for full-text eligibility screening. After a detailed evaluation of each article, 16 articles were deemed eligible for inclusion in the analysis. The complete database search strategy is detailed in Supplementary Table 1.
Study characteristics
Sample sizes of the included studies ranged from 32–7629. All studies calculated sensitivity and specificity for at least one clinical sign or symptom. Control groups included normal volunteers and patients with cervical spine complaints but no signs of myelopathy or evidence of cord compression. Of the included studies, 62% were prospective and 38% were retrospective. Detailed study characteristics are reported in Supplementary Table 2.
The sensitivity and specificity of clinical signs of degenerative cervical myelopathy
The study by Rhee et al. [24] found that hyperreflexia had the highest sensitivity (62%), followed by Hoffmann sign (59%) and inverted brachioradialis (51%). In contrast, Babinski and clonus, in conjunction with brachioradialis hyperreflexia, were comparatively less prevalent, with sensitivities recorded at 13 and 21%, respectively.
Two studies published by Cook et al. [18, 19] examined the diagnostic accuracy of various clinical indicators for diagnosing DCM. In the first study, it was demonstrated that the inverted supinator sign had the highest sensitivity (61%), followed by the suprapatellar tendon reflex (56%), while Babinski (93%) and clonus (96%) had the highest specificity. In their second study, the authors sought to develop a prediction model aimed at DCM diagnosis. Based on their results, the combination of gait deviation, Hoffmann, inverted supinator sign, Babinski, and age over 45, were significantly important indicators for DCM diagnosis. Whilst the individual clinical signs had low sensitivity, they exhibited high specificity.
In the retrospective analysis by Harrop et al. [28] sensory loss was the only clinical sign in this study to have both sensitivity and specificity values reported, which were 72 and 88%, respectively. Other signs had only their sensitivity calculated, including gait abnormality (91%), hyperreflexia (85%), Hoffmann sign (83%), lower extremity hyperreflexia (81%), and Babinski sign (44%).
There were two studies that examined the diagnostic value of the Tromner sign specifically in DCM [23, 26]. The sensitivity of this clinical sign ranged from 93–94%, whilst the specificity was 79 and 100%. Furthermore, three studies specifically examined the clinical utility of the Hoffmann sign in DCM diagnosis [16, 29, 30]. The Hoffmann sign demonstrated sensitivity between 58 and 62% and specificity between 78 and 86%.
Kobayashi et al. [20] reported that the 10-s grip and release test had a sensitivity of 88.2% and a specificity of 78.1%. Machino et al. [31] found that the same test had a sensitivity of 77.3% and a specificity of 58.8%. Machino et al. [31] also evaluated the 10-s step test, reporting a sensitivity of 92.3% and a specificity of 67.8%.
Two studies examining the extent of motor and sensory impairment found that motor impairment ranged from 53–75%, whilst specificity ranged from 18–64% [32, 33].
Lastly, a prospective study by Soufi et al. [34] evaluated the most discriminative clinical signs in patients with DCM. They reported that Tromner’s sign had a sensitivity of 97% and a specificity of 35%. The Hoffmann sign demonstrated a sensitivity of 89% and a specificity of 41%, while hyperreflexia of the biceps and triceps showed a sensitivity of 61% and a specificity of 74%. Tandem gait had a sensitivity of 66% and a specificity of 84%.
These findings are summarised in Table 2.
The sensitivity and specificity of symptoms of degenerative cervical myelopathy
Cook et al. [18] reported that the most sensitive symptoms for diagnosis DCM was neck pain (94%), followed by the loss of dexterity (72%). Conversely, the specificity of these symptoms were low, with 26% for loss of dexterity and 18% for neck pain. Gait clumsiness and hand numbness were both reported to have a sensitivity of 56%. The results of Cheung et al. [35] indicated that the sensitivity of neck or shoulder pain was 76%, with a low specificity at 11%.
In a prospective study by Hori et al. [36], the findings demonstrated that numbness and pain had moderate sensitivity (61%) and specificity (60%) for diagnosing DCM, whilst other reported symptoms had low sensitivity but high specificity.
Soufi et al. [34] reported that neck pain (81%) was the most sensitive symptom for diagnosing DCM, followed by limitations in daily activities (77%). Other symptoms, such as hand incoordination (52%), altered hand sensation (76%), upper extremity weakness (51%), gait imbalance (63%), difficulty lifting heavy objects (75%), and exacerbation of neck pain during driving (70%) or reading (71%), also showed high sensitivity but varying degrees of specificity. Autonomic dysfunction had low sensitivity (24%) but high specificity (95%), making it a more specific but less sensitive indicator of DCM.
These findings are summarised in Table 2.
Thematic analysis of diagnostic clinical signs and symptoms in degenerative cervical myelopathy
The thematic analysis of the selected studies elucidated key patterns and themes pertinent to the diagnosis of DCM (Table 3).
The Tromner sign and hyperreflexia were identified as highly sensitive clinical signs, demonstrating significant efficacy in the initial screening and identification of patients with DCM. Conversely, specific clinical signs such as the Babinski, Tromner sign, clonus, and inverted supinator sign were noted for their high specificity, making them essential for confirming the diagnosis by effectively excluding patients without DCM. However, no clear association was observed between certain clinical signs, including the Hoffmann sign, Babinski sign, and hyperreflexia, and the severity of the disease. This finding indicates that while these signs are valuable for diagnosis, they do not necessarily correlate with the severity of DCM.
Furthermore, the analysis identified hand numbness, hand paresthesias, loss of dexterity, gait abnormalities, and neck pain as highly sensitive symptoms for diagnosing DCM. Conversely, autonomic dysfunction demonstrated high specificity.
연구 선정
문헌 검색 전략을 통해 총 283편의 논문이 확인되었으며, 여기에 수동으로 선정된 14편의 논문이 추가되었다(그림 2). 자동화 도구를 통해 중복 기록 40건을 제거하고 수동으로 중복 2건을 추가 제거한 후, 273건의 기록이 남았다. 이 기록들(n = 273)은 포함 및 제외 기준에 따라 제목과 초록을 통해 선별되었으며, 그 결과 50편의 논문이 전문 적격성 선별 대상으로 선정되었습니다. 각 논문에 대한 상세한 평가 후, 16편의 논문이 분석에 포함될 적격성이 있다고 판단되었습니다. 완전한 데이터베이스 검색 전략은 보충 자료 표 1에 상세히 기술되어 있습니다.
연구 특성
포함된 연구의 표본 크기는 32명에서 7629명 사이였습니다. 모든 연구는 적어도 하나의 임상 징후 또는 증상에 대해 민감도와 특이도를 계산했습니다. 대조군에는 정상 대조군과 경추 통증 증상이 있으나 척수병증 징후나 척수 압박 증거가 없는 환자가 포함되었습니다. 포함된 연구 중 62%는 전향적 연구였고 38%는 후향적 연구였습니다. 상세한 연구 특성은 보충 자료 표 2에 보고되어 있습니다.
퇴행성 경추성 척수병증의 임상 징후에 대한 민감도와 특이도
Rhee 등[24]의 연구에 따르면, 반사과다증이 가장 높은 민감도(62%)를 보였으며, 호프만 징후(59%)와 역상완요골근 반사(51%)가 그 뒤를 이었다. 반면, 바빈스키 반사와 경련 반사는 상완요골근 반사과잉과 함께 상대적으로 덜 흔했으며, 각각 13%와 21%의 민감도를 기록했다.
Cook 등[18, 19]이 발표한 두 연구는 퇴행성 경추 척수병증(DCM) 진단에 대한 다양한 임상 지표의 진단 정확도를 평가했다. 첫 번째 연구에서는 역회전근 징후가 가장 높은 민감도(61%)를 보였으며, 슬개건 반사(56%)가 그 뒤를 이었고, 바빈스키 반사(93%)와 경련(96%)이 가장 높은 특이도를 나타냄을 입증하였다. 두 번째 연구에서는 DCM 진단을 위한 예측 모델 개발을 목표로 하였다. 그들의 결과에 따르면, 보행 이상, 호프만 징후, 역회전근 징후, 바빈스키 징후, 그리고 45세 이상 연령의 조합이 DCM 진단에 있어 상당히 중요한 지표였다. 개별 임상 징후들은 낮은 민감도를 보였으나 높은 특이도를 나타냈다.
Harrop 등[28]의 후향적 분석에서 감각 상실은 이 연구에서 민감도와 특이도 값이 모두 보고된 유일한 임상 징후였으며, 각각 72%와 88%였다. 다른 징후들은 민감도만 계산되었는데, 보행 이상(91%), 과반사(85%), 호프만 징후(83%), 하지 과반사(81%), 바빈스키 징후(44%)가 포함된다.
트롬너 징후의 진단적 가치를
DCM에서 구체적으로 검토한 연구는 두 건이었다[23, 26].
이 임상 징후의 민감도는
93~94% 범위를 보였으며,
특이도는 79%와 100%였다.
또한 호프만 징후의 DCM 진단에서의 임상적 유용성을 구체적으로 검토한 연구는 세 건이었다[16, 29, 30]. 호프만 징후는 58~62%의 민감도와 78~86%의 특이도를 보였다.
코바야시 등[20]은 10초 쥐고 놓기 검사의 민감도가 88.2%, 특이도가 78.1%라고 보고했다. 마치노 등[31]은 동일한 검사의 민감도가 77.3%, 특이도가 58.8%임을 발견했다. 마치노 등[31]은 또한 10초 보행 검사를 평가하여 민감도 92.3%, 특이도 67.8%를 보고했다.
운동 및 감각 장애 정도를 조사한 두 연구에서는 운동 장애가 53~75% 범위인 반면 특이도는 18~64% 범위로 나타났다[32, 33].
마지막으로 Soufi 등[34]의 전향적 연구는 DCM 환자에게서 가장 차별적인 임상 징후를 평가했다. Tromner 징후는 민감도 97%, 특이도 35%를 보였다고 보고했다. Hoffmann 징후는 민감도 89%, 특이도 41%를 보였으며, 이두근 및 삼두근 반사 과반사는 민감도 61%, 특이도 74%를 나타냈다. 탠덤 보행은 민감도 66%, 특이도 84%를 기록했다.
이러한 결과는 표 2에 요약되어 있다.
퇴행성 경추 척수증 증상의 민감도와 특이도
Cook 등[18]은 DCM 진단에 가장 민감한 증상이 목 통증(94%)이며, 그다음으로 손재주 상실(72%)이라고 보고했다. 반면, 이러한 증상의 특이도는 낮았는데, 손재주 상실은 26%, 목 통증은 18%였다. 보행 서투름과 손 저림은 모두 56%의 민감도를 보인 것으로 보고되었다. Cheung 등[35]의 연구 결과에 따르면 목 또는 어깨 통증의 민감도는 76%였으나 특이도는 11%로 낮았다.
Hori 등[36]의 전향적 연구 결과, 저림과 통증은 DCM 진단에 대해 중간 수준의 민감도(61%)와 특이도(60%)를 보인 반면, 다른 보고된 증상들은 민감도는 낮으나 특이도는 높았다.
Soufi 등[34]은 목 통증(81%)이 DCM 진단에 가장 민감한 증상이며, 일상생활 제한(77%)이 그다음으로 민감하다고 보고했다 . 손의 협응력 저하(52%), 손 감각 이상(76%), 상지 근력 약화(51%), 보행 불균형(63%), 무거운 물건 들기 어려움(75%), 운전 중(70%) 또는 독서 중(71%) 목 통증 악화 등 다른 증상들도 높은 민감도를 보였으나 특이도는 다양했다. 자율신경 기능 장애는 민감도는 낮았으나(24%) 특이도는 높았으며(95%), 이는 퇴행성 경추 척수증의 특이도는 높으나 민감도는 낮은 지표임을 시사한다.
이러한 결과는 표 2에 요약되어 있다.
퇴행성 경추 척수증의 진단적 임상 징후 및 증상에 대한 주제 분석
선정된 연구에 대한 주제 분석은 퇴행성 경추 척수증 진단과 관련된 핵심 패턴 및 주제를 규명하였다 (표 3).
트롬너 징후와 과반사는 높은 민감도를 보이는 임상 징후로 확인되어, DCM 환자의 초기 선별 및 식별에 상당한 효능을 입증하였다. 반대로 바빈스키 반사, 트롬너 징후, 클로누스, 역상완근 반사 등의 특이적 임상 징후는 높은 특이도로 주목받았으며, DCM이 없는 환자를 효과적으로 배제함으로써 진단을 확정하는 데 필수적이었다. 그러나 호프만 징후, 바빈스키 징후, 과반사 등 특정 임상 징후와 질환 중증도 간에는 명확한 연관성이 관찰되지 않았다. 이는 해당 징후들이 진단에는 유용하나 DCM 중증도와 반드시 상관관계가 있지는 않음을 시사한다.
또한 분석 결과, 손 저림, 손 감각 이상, 손재주 상실, 보행 이상, 목 통증이 DCM 진단에 매우 민감한 증상으로 확인되었다. 반대로 자율신경 기능 장애는 높은 특이도를 보였다.
Discussion
Establishing diagnostic criteria for DCM is invaluable for clinical practice, akin to the Wells’ Score for Pulmonary Embolus [37], as it enhances the triage of high-risk DCM patients. With an aging global population, the incidence of degenerative spinal conditions is expected to rise, underscoring the necessity for early and accurate diagnosis. The AO Spine RECODE-DCM (Research Objectives and Common Data Elements for Degenerative Cervical Myelopathy) project has identified this as a research priority [38, 39]. Given the clinical-radiological nature of DCM, there is a significant gap in clinical knowledge regarding which signs and symptoms are most predictive of the condition. Hence, this scoping review aims to outline the clinical signs and symptoms essential for inclusion in DCM diagnostic criteria. Through systematic refinement and stakeholder engagement, these evidence-based clinical recommendations will assist healthcare professionals, particularly primary care physicians, in accurately identifying DCM, even when it presents subtly. Early detection is crucial, as it significantly impacts surgical and patient outcomes.
The development of a codebook in this review represents a significant step toward improving the translation of research into clinical practice. Using thematic analysis, text excerpts from the included studies were examined to identify their relationship to the research question, with codes iteratively refined through data analysis. This process grouped similar codes into categories and broader themes, creating a structured framework for understanding diagnostic features of DCM. Stakeholder consultation played a pivotal role in shaping the codebook, providing valuable input to refine findings, address gaps in the literature, and ensure the results were both evidence-based and clinically relevant. This structured and collaborative approach bridges the gap between research and practical application, facilitating the integration of findings into clinical workflows.
Based on the results of the thematic analysis, three key themes emerged to encapsulate the diagnostic utility of the clinical signs and symptoms of DCM across the included studies. The first theme, High Sensitivity Signs, included Tromner’s sign and hyperreflexia, both identified as highly sensitive indicators useful for initial screening of DCM. The Tromner sign, an alternative clinical test to the Hoffman sign, demonstrated superiority in both sensitivity (93–97%) and specificity (35–100%) compared to the Hoffmann sign. Moreover, the Tromner sign’s diagnostic sensitivity remained high across varying degrees of myelopathy, highlighting its clinical utility [26]. While hyperreflexia is noted to be a highly sensitive sign for DCM diagnosis, its sensitivity varies by location of the lesion. Evaluation of individual reflexes demonstrated a wide range of sensitivities: biceps (18–62%), triceps (36–40%), brachioradialis (21%), patellar (22–33%), Achilles (15–26%), and suprapatellar reflex (56%).
The second theme, High Specificity Signs, encompassed the Babinski sign, Tromner sign, clonus, and the inverted supinator sign, all noted for their high specificity and value in confirming a DCM diagnosis. Among these, the Babinski sign and clonus have low sensitivity but high specificity, consistent with previous studies [18]. Though the Babinski sign was highly specific among the case-controlled studies in this review, the control groups were either healthy participants or patients with cervical spine complaints without imaging evidence of spinal cord compression or myelomalacia. Consequently, the specificity values for the Babinski sign might be falsely high, as this clinical sign can also be found in patients without cervical or spondylotic disorders causing upper motor neuron dysfunction. Additionally, variability in assessment methods and interrater reliability across different studies may impact the reported specificity values, underscoring the need for standardized diagnostic protocols in future research.
Lastly, the third theme, Symptom Sensitivity and Specificity, identified hand numbness, hand paresthesias, loss of dexterity, gait abnormalities, and neck pain as highly sensitive symptoms of DCM. Although less common, autonomic dysfunction and bladder dysfunction are noted for their high specificity in severe DCM cases. While bladder and bowel dysfunction were less frequently reported in the included studies, they serve as important markers of advanced disease and should be considered during diagnosis. Among the symptoms, it has been reported that 85% of DCM patients may present with at least one symptom involving their hands [40]. However, the specificity of neck pain is relatively low, with estimates indicating that 30–50% of adults experience neck pain annually [41]. On average, a primary care practitioner will encounter seven cases of neck-related symptoms per week, underscoring the importance of examining patients with neck pain for evidence of myelopathy [42].
Patients with DCM often present with subtle gait abnormalities, such as instability. Though not assessed in this review, it is crucial to consider recurrent falls in DCM patients, particularly the elderly [43]. This demographic may perceive gait instability as a natural aspect of aging and, consequently, may not report it when questioned about symptoms. Functional tests like tandem walk and Rhomberg sign could aid in assessing balance and coordination deficits. However, similar abnormalities can be observed in other neurodegenerative conditions, such as multiple sclerosis, Parkinson’s disease, or peripheral neuropathies, necessitating a thorough differential diagnosis [44]. Grip release tests, though reported variably, may provide additional diagnostic utility when used alongside other clinical signs and symptoms. Therefore, when taking patient history, it is essential to critically evaluate hand function and fine motor skills, gait abnormalities, neck pain, and autonomic dysfunction.
Importantly, the diagnostic accuracy of DCM may be enhanced by combining specific signs and symptoms. For instance, pairing highly sensitive signs, such as hyperreflexia and Tromner sign, with highly specific signs, such as the Babinski sign and clonus, could provide a more robust framework for diagnosis. Similarly, incorporating symptoms like hand incoordination with confirmatory signs like the inverted supinator sign could improve diagnostic confidence. Multimodal assessments, rather than evaluating signs or symptoms in isolation, are critical to achieving higher diagnostic accuracy. This combined approach underscores the need for further research into how paired or grouped findings can optimize diagnostic strategies for DCM.
Moreover, the lack of studies comparing the sensitivity and specificity of symptoms between DCM patients and healthy controls means that there is limited information on the specificity values of symptoms for DCM. This is likely due to poorly defined inclusion criteria or reliance on the absence of imaging findings, such as cervical spinal cord compression or hyperintensity on T2-weighted MRI images in these studies. Secondly, the heterogeneity in control groups, ranging from healthy individuals to those with non-myelopathic cervical spine complaints, may skew the reported sensitivity and specificity values. Nonetheless, this scoping review provides a diagnostic framework that will aid healthcare professionals in identifying DCM.
Conclusion
Highly sensitive signs, such as the Tromner sign and hyperreflexia can be employed as screening tools for DCM. Whilst high specificity signs such as Babinski, clonus and inverted supinator sign are recommended in confirming DCM diagnosis. Symptoms like neck pain, hand incoordination, and altered hand sensation should heighten the index of suspicion and guide the clinical differential diagnosis of DCM and reduce diagnostic delays.
논의
DCM 진단 기준 수립은 폐색전증에 대한 웰스 점수[37]와 마찬가지로 임상 실무에 매우 가치 있다. 이는 고위험 DCM 환자의 분류를 향상시키기 때문이다. 전 세계 인구 고령화로 퇴행성 척추 질환 발생률이 증가할 것으로 예상됨에 따라 조기 및 정확한 진단의 필요성이 부각된다. [37]과 마찬가지로 고위험 DCM 환자의 분류를 향상시키므로 임상적으로 매우 중요합니다. 전 세계 인구 고령화로 퇴행성 척추 질환의 발생률이 증가할 것으로 예상됨에 따라 조기 및 정확한 진단의 필요성이 강조됩니다. AO Spine RECODE-DCM(퇴행성 경추 척수증에 대한 연구 목표 및 공통 데이터 요소) 프로젝트는 이를 연구 우선순위로 지정했습니다[38, 39] . DCM의 임상-방사선학적 특성상, 이 질환을 가장 잘 예측하는 징후와 증상에 관한 임상 지식에는 상당한 공백이 존재한다. 따라서 본 탐색적 문헌고찰은 DCM 진단 기준에 포함되어야 할 핵심 임상 징후 및 증상을 개괄하는 것을 목표로 한다. 체계적인 정제와 이해관계자 참여를 통해 도출된 이러한 근거 기반 임상 권고사항은 의료진, 특히 일차 진료 의사들이 DCM이 미묘하게 나타날 때조차 정확히 식별하는 데 도움을 줄 것이다. 조기 발견은 수술 결과와 환자 예후에 중대한 영향을 미치므로 매우 중요하다.
본 연구에서 개발된 코드북은 연구 결과를 임상 실무로 전환하는 데 중요한 진전을 의미한다. 주제 분석을 통해 포함된 연구의 텍스트 발췌문을 검토하여 연구 질문과의 연관성을 확인하고, 데이터 분석을 통해 코드를 반복적으로 정제하였다. 이 과정을 통해 유사한 코드를 범주와 광범위한 주제로 그룹화하여 DCM의 진단적 특징을 이해하기 위한 구조화된 틀을 구축하였다. 코드북 구성에는 이해관계자 협의가 중추적 역할을 수행하여 연구 결과를 정교화하고 문헌의 공백을 메우며, 증거 기반이면서 임상적으로 관련성 있는 결과를 보장하는 데 귀중한 의견을 제공했습니다. 이러한 체계적이고 협력적인 접근법은 연구와 실제 적용 간의 격차를 해소하여 연구 결과를 임상 업무 흐름에 통합하는 데 기여합니다.
주제 분석 결과를 바탕으로 포함된 연구 전반에 걸쳐 DCM의 임상적 징후 및 증상의 진단적 유용성을 요약하는 세 가지 핵심 주제가 도출되었습니다. 첫 번째 주제인 '고감도 징후'에는 트롬너 징후와 과반사가 포함되었으며, 둘 다 DCM 초기 선별에 유용한 고감도 지표로 확인되었습니다.
호프만 징후의 대체 임상 검사인 트롬너 징후는 호프만 징후 대비 감도(93~97%)와 특이도(35~100%) 모두에서 우월성을 보였습니다. 또한 Tromner 징후의 진단 민감도는 다양한 척수병증 단계에서 높은 수준을 유지하여 임상적 유용성을 입증하였다[26].
과반사는
DCM 진단에 매우 민감한 징후로 알려져 있으나,
병변 위치에 따라 민감도가 달라진다.
개별 반사 평가 결과 광범위한
민감도가 확인되었다:
이두근 반사(18–62%),
삼두근 반사(36–40%),
상완요골근 반사(21%),
슬개골 반사(22–33%),
아킬레스 반사(15–26%),
슬개골상 반사(56%).
두 번째 주제인 '높은 특이도 징후'에는
바빈스키 징후, 트롬너 징후, 클로누스, 역회전반사 징후가 포함되었으며,
이들 모두 높은 특이도와 DCM 진단 확정에 있어 가치가 있는 것으로 알려져 있다.
이 중 바빈스키 징후와 클로누스는
기존 연구와 일관되게 낮은 민감도와 높은 특이도를 보였다[18].
본 문헌고찰의 사례대조군 연구에서 바빈스키 증상은 높은 특이도를 보였으나,
대조군은 건강한 참가자이거나 척수 압박 또는 척수연화증의 영상학적 증거가 없는
경추 증상 환자들로 구성되었다.
따라서
상부 운동뉴런 기능장애를 유발하는 경추 또는 척추관협착증이 없는 환자에서도
이 임상 징후가 관찰될 수 있으므로
바빈스키 증상의 특이도 값은 과대평가되었을 가능성이 있다.
또한, 연구 간 평가 방법의 변동성과 평가자 간 신뢰도 차이는 보고된 특이도 값에 영향을 미칠 수 있어
향후 연구에서 표준화된 진단 프로토콜의 필요성을 강조한다.
마지막으로 세 번째 주제인
증상 민감도와 특이도에서는
손 저림, 손 감각 이상, 손재주 상실, 보행 이상, 목 통증이
DCM의 높은 민감도를 보이는 증상으로 확인되었다.
비록 흔하지는 않지만,
자율신경 기능 장애와 방광 기능 장애는 중증 DCM 사례에서
높은 특이도를 보이는 것으로 알려져 있다.
포함된 연구에서 방광 및 장 기능 장애는 덜 보고되었지만,
이들은 진행성 질환의 중요한 지표 역할을 하므로 진단 시 고려되어야 한다.
이러한 증상 중 DCM 환자의 85%가 손과 관련된 증상을
적어도 하나 이상 경험할 수 있다고 보고되었습니다[40].
그러나 목 통증의 특이도는 상대적으로 낮으며,
성인의 30~50%가 매년 목 통증을 경험한다는 추정치가 있습니다[41].
일반적으로 일차 진료 의사는
주당 평균 7건의 목 관련 증상을 접하게 되며,
이는 목 통증이 있는 환자에게 척수병증의 증거를 검사하는 것이 중요함을 강조한다[42].
DCM 환자는 종종 불안정성과 같은 미묘한 보행 이상을 보입니다. 본 리뷰에서는 평가되지 않았지만, 특히 노인 DCM 환자에서 반복적인 낙상을 고려하는 것이 중요합니다[43]. 이 연령층은 보행 불안정성을 노화의 자연스러운 측면으로 인식할 수 있으며, 결과적으로 증상에 대해 질문받을 때 이를 보고하지 않을 수 있습니다. 탠덤 보행 및 롬베르크 징후와 같은 기능적 검사는 균형 및 조정력 결핍 평가에 도움이 될 수 있습니다. 그러나 다발성 경화증, 파킨슨병 또는 말초 신경병증과 같은 다른 신경퇴행성 질환에서도 유사한 이상이 관찰될 수 있으므로 철저한 감별 진단이 필요합니다[44]. 그립 릴리즈 검사는 보고에 따라 결과가 다양하지만, 다른 임상 징후 및 증상과 함께 사용할 경우 추가적인 진단적 유용성을 제공할 수 있습니다. 따라서 환자 병력을 수집할 때 손 기능 및 미세 운동 능력, 보행 이상, 목 통증, 자율신경 기능 장애를 비판적으로 평가하는 것이 필수적입니다.
중요한 점은 DCM의 진단 정확도는 특정 징후와 증상을 결합함으로써 향상될 수 있다는 것이다. 예를 들어, 과반사나 트롬너 징후와 같은 고감도 징후를 바빈스키 징후나 클로누스와 같은 고특이도 징후와 함께 사용하면 더 견고한 진단 프레임워크를 제공할 수 있다. 마찬가지로, 손의 운동조화 장애와 같은 증상과 역회전근 징후와 같은 확인 징후를 통합하면 진단 확신을 높일 수 있다. 단일 징후나 증상을 평가하기보다는 다중 평가 방식이 진단 정확도 향상에 핵심적이다. 이러한 복합적 접근법은 DCM 진단 전략을 최적화하기 위해 쌍을 이루거나 그룹화된 소견의 활용 방안에 대한 추가 연구 필요성을 강조한다.
또한, DCM 환자와 건강한 대조군 간 증상의 민감도와 특이도를 비교한 연구가 부족하여 DCM에 대한 증상의 특이도 값에 대한 정보가 제한적이다. 이는 연구에서 포함 기준이 불명확하거나 경추 척수 압박이나 T2 가중 MRI 영상의 고신호 강도와 같은 영상 소견 부재에 의존했기 때문일 가능성이 높다. 둘째, 대조군의 이질성(건강한 개인부터 비척수병증성 경추 증상을 가진 환자까지 포함)은 보고된 민감도와 특이도 값을 왜곡할 수 있습니다. 그럼에도 불구하고, 본 탐색적 문헌고찰은 의료진이 DCM을 식별하는 데 도움이 될 진단적 틀을 제공합니다.
결론
트롬너 징후(Tromner sign) 및 과반사(hyperreflexia)와 같은 고감도 징후는
DCM 선별 도구로 활용될 수 있습니다.
반면 바빈스키 반사, 클로누스, 역상완반사 같은 고특이도 징후는
DCM 진단 확정에 권장된다.
목 통증, 손 운동 불협조, 손 감각 이상 같은 증상은
DCM에 대한 의심을 높이고 임상적 감별진단을 유도하여 진단 지연을 줄여야 한다.
References