REVIEW article
Front. Physiol., 02 May 2022
Sec. Striated Muscle Physiology
Volume 13 - 2022 | https://doi.org/10.3389/fphys.2022.872277
Diaphragm Dysfunction and Rehabilitation Strategy in Patients With Chronic Obstructive Pulmonary Disease




Xiaodan Liu2*

- 1Department of Sports Rehabilitation, Shanghai University of Sport, Shanghai, China
- 2School of Rehabilitation Medicine, Shanghai University of Traditional Chinese Medicine, Shanghai, China
Chronic obstructive pulmonary disease (COPD) affects the whole body and causes many extrapulmonary adverse effects, amongst which diaphragm dysfunction is one of the prominent manifestations. Diaphragm dysfunction in patients with COPD is manifested as structural changes, such as diaphragm atrophy, single-fibre dysfunction, sarcomere injury and fibre type transformation, and functional changes such as muscle strength decline, endurance change, diaphragm fatigue, decreased diaphragm mobility, etc. Diaphragm dysfunction directly affects the respiratory efficiency of patients and is one of the important pathological mechanisms leading to progressive exacerbation of COPD and respiratory failure, which is closely related to disease mortality. At present, the possible mechanisms of diaphragm dysfunction in patients with COPD include systemic inflammation, oxidative stress, hyperinflation, chronic hypoxia and malnutrition. However, the specific mechanism of diaphragm dysfunction in COPD is still unclear, which, to some extent, increases the difficulty of treatment and rehabilitation. Therefore, on the basis of the review of changes in the structure and function of COPD diaphragm, the potential mechanism of diaphragm dysfunction in COPD was discussed, the current effective rehabilitation methods were also summarised in this paper. In order to provide direction reference and new ideas for the mechanism research and rehabilitation treatment of diaphragm dysfunction in COPD.
만성 폐쇄성 폐질환(COPD)은
전신에 영향을 미치며 폐 외부의 다양한 부작용을 유발하는데,
그중 횡격막 기능 장애가 대표적인 증상 중 하나이다.
COPD 환자의 횡격막 기능 장애는
횡격막 위축, 단일 섬유 기능 장애, 근절 손상 및 섬유 유형 변형과 같은 구조적 변화와
근력 감소, 지구력 변화, 횡격막 피로, 횡격막 가동성 감소 등과 같은 기능적 변화로 나타난다.
횡격막 기능 장애는 환자의 호흡 효율에 직접적인 영향을 미치며,
COPD의 진행성 악화와 호흡 부전으로 이어지는 중요한 병리학적 기전 중 하나로,
이는 질병 사망률과 밀접한 관련이 있습니다.
현재 COPD 환자의 횡격막 기능 장애 가능성 있는 기전으로는
전신성 염증, 산화 스트레스, 과팽창, 만성 저산소증 및 영양실조 등이 제시되고 있다.
그러나
COPD에서 횡격막 기능 장애의 구체적 기전은 아직 명확하지 않아
어느 정도 치료 및 재활의 난이도를 높이고 있다.
따라서
본 논문에서는 COPD 횡격막의 구조 및 기능 변화에 대한 문헌 고찰을 바탕으로
COPD에서 횡격막 기능 장애의 잠재적 기전을 논의하고,
현재 효과적인 재활 방법도 종합하였다.
이는 COPD에서
횡격막 기능 장애의 기전 연구 및 재활 치료에 방향성 참고 자료와
새로운 아이디어를 제공하기 위함이다.
1 Introduction
COPD is a common respiratory disease caused by exposure to harmful particles or gases, characterised by persistent respiratory symptoms and restricted airflow (Singh et al., 2019). According to the World Health Organization statistical report, COPD is the third leading cause of death in the world, causing 3.23 million deaths in 2019. The high incidence and mortality of COPD make it the fifth disease aggravating the global economic burden. In addition to damaging the airway, alveoli and pulmonary vessels, COPD also damages the circulatory system, nervous system, motor system and other systems, resulting in remarkable extrapulmonary adverse effects (Vanfleteren et al., 2016). Diaphragm dysfunction is present at all stages of COPD development (Donaldson et al., 2012). The diaphragm is the most important inspiratory muscle and the maximum inspiratory pressure is an independent determinant of survival in patients with severe COPD. Diaphragm dysfunction directly leads to dyspnoea and respiratory failure (Elsawy, 2017). It is also associated with increased risk of hospitalisation and increased disease mortality due to acute exacerbation of COPD (Vilaró et al., 2010). Diaphragm dysfunction in patients with COPD is mainly manifested in structural and functional changes, including negative changes and positive adaptive changes. The mechanism of diaphragm dysfunction may be related to systemic inflammation, oxidative stress, hyperinflation, chronic hypoxia, and malnutrition. These factors interact to affect the diaphragm function. Rehabilitation is an individualised and comprehensive treatment plan that is based on existing rehabilitation methods after the assessment of patients’ physique and disease progression. Pulmonary rehabilitation has been shown to be the most effective treatment strategy for improving health outcomes and exercise tolerance in patients with COPD according to the 2022 Global Initiative on Chronic Obstructive Pulmonary Disease guidelines. Studies have shown that rehabilitation could increase diaphragmatic endurance and strength, reduce airflow resistance and improve dyspnoea in patients with COPD, thereby reducing the incidence of diaphragm dysfunction (Gosselink et al., 2011). Therefore, in the present paper, the structural and functional changes and mechanisms of diaphragm dysfunction in COPD were discussed. The common rehabilitation treatment methods of diaphragm dysfunction in COPD, such as Inspiratory muscle training (IMT), exercise intervention and nutritional support, were also summarised to provide reference and new ideas for the rehabilitation and research direction of diaphragm dysfunction in COPD.
1 서론
COPD는
유해 입자나 가스 노출로 발생하는 흔한 호흡기 질환으로,
지속적인 호흡기 증상과 폐쇄성 폐질환(COPD)의 특징인
공기 흐름 제한이 나타난다(Singh et al., 2019).
세계보건기구(WHO) 통계 보고서에 따르면,
COPD는 전 세계 사망 원인 3위로,
2019년 323만 명의 사망자를 발생시켰다.
COPD의 높은 발병률과 사망률은
이를 전 세계 경제 부담을 가중시키는 5대 질환으로 만들었다.
기도, 폐포 및 폐혈관 손상 외에도 COPD는
순환계, 신경계, 운동계 등 다른 시스템에도 손상을 입혀
현저한 폐외 부작용을 초래한다(Vanfleteren et al., 2016).
횡격막 기능 장애는
COPD 진행의 모든 단계에서 관찰됩니다(Donaldson et al., 2012).
횡격막은 가장 중요한 흡기근이며,
최대 흡기압은 중증 COPD 환자의 생존을 결정하는 독립적 요인입니다.
횡격막 기능 장애는
직접적으로 호흡곤란과 호흡부전을 초래합니다(Elsawy, 2017).
또한
COPD 급성 악화로 인한 입원 위험 증가 및 질병 사망률 증가와 연관되어 있다(Vilaró et al., 2010).
COPD 환자의 횡격막 기능 장애는
주로 구조적·기능적 변화(부정적 변화 및 긍정적 적응 변화 포함)로 나타난다.
횡격막 기능 장애의 기전은
전신성 염증, 산화 스트레스, 과팽창, 만성 저산소증, 영양실조와 관련될 수 있다.
이러한 요인들이
상호작용하여 횡격막 기능에 영향을 미칩니다.
재활은 환자의 체격과 질병 진행 정도를 평가한 후 기존 재활 방법을 기반으로
한 개인 맞춤형 종합 치료 계획입니다.
2022년 만성폐쇄성폐질환 글로벌 이니셔티브(GOLD) 지침에 따르면,
폐 재활은 COPD 환자의 건강 결과 및 운동 내성 개선에
가장 효과적인 치료 전략으로 입증되었습니다.
연구에 따르면 재활은
COPD 환자의 횡격막 지구력과 근력을 증가시키고,
기류 저항을 감소시키며,
호흡곤란을 개선하여 횡격막 기능 장애 발생률을 낮출 수 있다(Gosselink et al., 2011).
따라서
본 논문에서는 COPD에서 횡격막 기능 장애의 구조적·기능적 변화와 기전에 대해 논의하였다.
또한 흡기근 훈련(IMT), 운동 중재, 영양 지원 등
COPD에서 횡격막 기능 장애의 일반적인 재활 치료 방법을 요약하여
COPD 횡격막 기능 장애의 재활 및 연구 방향에 대한 참고 자료와 새로운 아이디어를 제공한다.
2 Manifestations of Diaphragm Dysfunction in COPD
2.1 Structural Changes of the Diaphragm
The function of diaphragm depends largely on its physiological characteristics at the structural level. Negative changes and positive adaptive changes exist at the same time in the structural changes of diaphragm in patients with COPD. The balance between negative changes and positive changes is closely related to the functional performance and changes of diaphragm in each stage of the disease, which has a profound impact on diaphragm dysfunction and disease progression.
Amongst the negative structural changes of diaphragm in patients with COPD, diaphragmatic atrophy is an important pathological basis of dysfunction (Ottenheijm et al., 2005). Studies have shown a 30% reduction in myosin heavy chain content in patients with mild to moderate COPD and a 30%–40% reduction in diaphragmatic muscle fibre cross-sectional area in patients with severe COPD (Levine et al., 2013). These findings suggested that diaphragmatic atrophy occurs early in the disease and may be present at all stages of the disease. In addition, reduced myosin content in the diaphragm induced changes in the contractile properties and passive properties of diaphragm single fibres in COPD patients. Levine and colleagues’ study showed a 35% reduction in the force generated by diaphragm fibres in patients with severe COPD, indicating a decrease in the contractile properties of diaphragm single fibres (Levine et al., 2003). Moore and colleagues’ data indicated that diaphragmatic fibres exhibit less passive tension during fibre stretching in patients with mild to moderate COPD than in patients without COPD, suggesting a reduction in the diaphragmatic single fibre elasticity (Moore et al., 2006). Sarcomere is the basic structure and function unit of muscle. Patients with COPD have a deletion of serial sarcomeres (Levine et al., 2013). Sarcomere disruption is more evident in patients with moderate and severe COPD(Orozco-Levi et al., 2001). With chronic hyperinflation, there is a 10%–15% loss of sarcomeres in the diaphragmatic muscle fibres (De Troyer, 1997). The biomechanical defects of diaphragm due to changes in diaphragm shape are the main negative factors for diaphragm dysfunction. Pulmonary hyperinflation and deformation of the thorax cause the diaphragm to drop in position, shorten and flatten the normal dome shape (Salito et al., 2015; Laghi et al., 2021). These changes put the diaphragm at a mechanical disadvantage, resulting in a reduced ability of the diaphragm to generate flow and pressure, increasing respiratory work, and causing diaphragmatic fatigue (Hellebrandová et al., 2016).
In addition to the negative changes, there are some positive adaptive structural changes in the diaphragm of patients with COPD. Due to pulmonary hyperinflation, the length of diaphragm muscle segments is shortened in patients with COPD and the greater the lung volume, the shorter the muscle segments are (Orozco-Levi et al., 1999). Muscle segments shortening may result in a partial reversal of the displacement of the diaphragm’s length-tension curve, increasing its ability to maintain tension (Gea et al., 2013), and enhance endurance. The transformation of diaphragm fibre type is the most remarkable structural and physiological characteristic of diaphragm in patients with COPD. The contraction rate and main metabolic types of muscle fibres determine its antifatigue ability. Studies have shown that the diaphragm type II fibres in patients with COPD are transformed into type I fibres with higher oxidation degree, resulting in an increase in the proportion of type I fibres (Nguyen et al., 2000; Levine et al., 2002). To some extent, this transformation is a positive adaptation of the diaphragm muscle. The peripheral vascular network of type I fibre is richer than that of type II fibre and it contains more myoglobin and mitochondria than that of type II fibre. The increase of capillary density, myoglobin content and mitochondrial density can improve the oxygen supply efficiency of diaphragm. Therefore, it compensatively increases the endurance and fatigue resistance of diaphragm (Levine et al., 2003). To some extent, they help the diaphragm adapt to the high load due to increased airway resistance that lowers airflow. However, beyond the compensatory range could cause a decrease in diaphragm endurance. The experimental data of rats show that type I fibres produced less force than type II fibres (Geiger et al., 2000), possibly leading to decreased diaphragm strength in patients with mild to severe COPD.
Therefore, in summary, although positive adaptive changes in diaphragm structure could be found in patients with COPD, negative structural changes still dominate (Levine et al., 2013). In the early and middle stages of the disease, a balance exists between positive and negative changes (Barreiro and Gea, 2015). However, this balance quickly shifts towards negative outcomes as the disease progresses (Gayan-Ramirez and Decramer, 2013).
2 COPD에서 횡격막 기능 장애의 증상
2.1 횡격막의 구조적 변화
횡격막의 기능은
구조적 차원의 생리적 특성에 크게 좌우된다.
COPD 환자의 횡격막 구조 변화에는
부정적 변화와 긍정적 적응 변화가 동시에 존재한다.
부정적 변화와 긍정적 변화의 균형은
질병 각 단계에서 횡격막의 기능적 수행 및 변화와 밀접하게 연관되어 있으며,
이는 횡격막 기능 장애와 질병 진행에 중대한 영향을 미친다.
COPD 환자의 횡격막 부정적 구조적 변화 중 횡격막 위축은
기능 장애의 중요한 병리학적 근거이다(Ottenheijm et al., 2005)
연구에 따르면
경증에서 중등도 COPD 환자의 미오신 중쇄 함량은 30% 감소했으며,
중증 COPD 환자의 횡격막 근섬유 단면적은 30~40% 감소한 것으로 나타났다(Levine et al., 2013).
이러한 결과는
횡격막 위축이 질병 초기 단계에서 발생하며
모든 병기에 걸쳐 존재할 수 있음을 시사한다.
또한 횡격막 내 미오신 함량 감소는
COPD 환자의 횡격막 단일 섬유 수축 특성과 수동적 특성에 변화를 유발했다.
Levine과 동료들의 연구는
중증 COPD 환자에서 횡격막 섬유가 생성하는 힘이 35% 감소함을 보여주어
횡격막 단일 섬유의 수축 특성 저하를 시사했다(Levine et al., 2003).
Moore와 동료들의 데이터는
경증에서 중등도 COPD 환자에서 횡격막 섬유가
COPD가 없는 환자보다 섬유 신장 시 수동적 장력을 덜 나타냄을 보여주며,
이는 횡격막 단일 섬유의 탄력성 감소를 시사합니다(Moore et al., 2006).
근절은
근육의 기본 구조 및 기능 단위입니다.
COPD 환자는
연속적인 근절의 결손이 있습니다 (Levine et al., 2013).
중등도 및 중증 COPD 환자에서 근절 손상은
더욱 뚜렷하다(Orozco-Levi et al., 2001).
만성 과팽창 시 횡격막 근섬유에서 근절이
10%–15% 감소한다(De Troyer, 1997).
횡격막 형태 변화로 인한 생체역학적 결함은
횡격막 기능 장애의 주요 부정적 요인이다.
폐 과팽창과 흉곽 변형은
횡격막의 위치 하강을 유발하며,
정상적인 돔 형태를 단축 및 평탄화시킨다(Salito et al., 2015; Laghi et al., 2021).
이러한 변화는 횡격막에 기계적 불리함을 초래하여,
횡격막의 유량 및 압력 생성 능력이 감소하고
호흡 작업량이 증가하며 횡격막 피로를 유발합니다(Hellebrandová et al., 2016).
이러한 부정적 변화 외에도,
COPD 환자의 횡격막에는 일부 긍정적인 적응적 구조적 변화가 존재한다.
폐 과팽창으로 인해 COPD 환자의 횡격막 근육 단편 길이는 단축되며,
폐 용적이 클수록 근육 단편은 더 짧아진다(Orozco-Levi et al., 1999).
근육 단편의 단축은
횡격막 길이-장력 곡선의 변위를 부분적으로 역전시켜
장력 유지 능력(Gea et al., 2013)과 지구력을 향상시킬 수 있습니다.
횡격막 섬유 유형의 변형은
COPD 환자의 횡격막에서 가장 두드러진 구조적·생리학적 특징입니다.
근섬유의 수축 속도와 주요 대사 유형은
피로 저항 능력을 결정합니다.
연구에 따르면 COPD 환자의 횡격막 II형 섬유는
산화도가 더 높은 I형 섬유로 변형되어 I형 섬유의 비율이 증가한다(Nguyen et al., 2000; Levine et al., 2002).
어느 정도 이 변형은
횡격막 근육의 긍정적 적응이다.
제1형 섬유의 말초 혈관망은 제2형 섬유보다 풍부하며,
제2형 섬유보다 더 많은 미오글로빈과 미토콘드리아를 함유한다.
모세혈관 밀도, 미오글로빈 함량 및 미토콘드리아 밀도의 증가는
횡격막의 산소 공급 효율을 향상시킬 수 있다.
따라서
이는 횡격막의 지구력과 피로 저항성을 보상적으로 증가시킨다(Levine et al., 2003).
어느 정도 이들은
기류량을 감소시키는 기도 저항 증가로 인한 높은 부하에 횡격막이 적응하도록 돕습니다.
그러나
보상 범위를 초과하면 횡격막 내구력 감소로 이어질 수 있습니다.
쥐 실험 데이터에 따르면
제1형 섬유는 제2형 섬유보다 적은 힘을 생성했습니다(Geiger et al., 2000),
이는 경증에서 중증 COPD 환자에서 횡격막 강도 감소를 초래할 수 있습니다.
따라서 요약하면,
COPD 환자에서 횡격막 구조의 긍정적 적응 변화가 발견될 수 있지만,
부정적 구조적 변화가 여전히 우세하다(Levine et al., 2013).
질병 초기 및 중기에는
긍정적 변화와 부정적 변화 사이의 균형이 존재한다(Barreiro and Gea, 2015).
그러나
질환이 진행됨에 따라
이 균형은 빠르게 부정적인 결과 쪽으로 기울어집니다(Gayan-Ramirez and Decramer, 2013).
2.2 Functional Changes in Diaphragm
Diaphragm dysfunction could be classified as partial or total loss of diaphragmatic function and it may involve one or both hemidiaphragms (McCool and Tzelepis, 2012). Diaphragm dysfunction in patients with COPD is mostly unilateral diaphragmatic paralysis, which is usually asymptomatic. However, dyspnoea may occur during exertion and supine. (Hart et al., 2002; Steier et al., 2008). From the specific function, patients with COPD with diaphragm dysfunction is mainly manifested as decreased diaphragm muscle strength, endurance changes, reduced mobility, and diaphragm fatigue.
Diaphragm muscle strength mainly depends on muscle fibre cross-sectional area, muscle fibre type and initial length (Mathur et al., 2014). The cross-sectional area of diaphragm muscle fibre in patients with COPD decreases, the muscle fibre type changes from fast twitch muscle to slow twitch muscle and the pulmonary hyperinflation shortens the length of diaphragm muscle (Finucane et al., 2005), resulting in the decline of diaphragm muscle strength in patients with COPD. Levine and colleagues found that although the type conversion of diaphragm fibres increased the ATP production capacity, the utilisation rate of ATP decreased, the specific force decreased, resulting in the weakening of the pressure-generating ability (Levine et al., 2003). Transdiaphragmatic pressure (Pdi) is a more direct indicator of diaphragm muscle strength. The maximum Pdi in patients with severe COPD is only 60% of that in healthy controls (McCool and Tzelepis, 2012). Increased lung volume and altered chest wall geometry led to diaphragm shortening (Silva et al., 2013). An early pioneering study found that the diaphragm of patients was on average 28% shorter than that of healthy subjects (Rochester and Braun, 1985). The diaphragm is shortened to the suboptimal length, which makes the conversion of diaphragm tension into trans-diaphragm pressure ineffective, so as to reduce the pressure-generating ability. Furthermore, pulmonary hyperinflation shortens the operation length of diaphragm and changes the mechanical linkage between its various parts, damaging the muscle strength of diaphragm (Nair et al., 2019).
Patients with COPD showed fragile positive fitness for diaphragm endurance (Papavramidis et al., 2011). The respiratory controller imposes a shorter duty cycle, and the transformation of diaphragm fibre to type II muscle fibre with higher oxidation degree is the main reason for the increase of endurance (Wijnhoven et al., 2006). However, studies have shown that patients with stable COPD have a lower mean diaphragm tension-time index (which indicates the ability of the inspiratory muscles to maintain sufficient pressure generation over time) than normal subjects (Ceriana et al., 2017), indicating decreased diaphragm endurance in patients with COPD. The enhanced endurance adaptations may only be maintained within a certain range. The reasons for this are the low ATP utilization in the diaphragm and the fact that the load on the diaphragm continues to rise with disease severity. Eventually, diaphragmatic endurance is further impaired due to increased muscle weakness and a series of factors that limit regeneration (Macgowan et al., 2001).
2.2 횡격막의 기능적 변화
횡격막 기능 장애는 횡격막 기능의 부분적 또는 완전한 상실로 분류될 수 있으며, 한쪽 또는 양쪽 횡격막 반쪽에 영향을 미칠 수 있습니다(McCool and Tzelepis, 2012). COPD 환자의 횡격막 기능 장애는 대부분 일측성 횡격막 마비이며, 일반적으로 무증상이다. 그러나 운동 시 및 앙와위 자세에서 호흡곤란이 발생할 수 있다(Hart et al., 2002; Steier et al., 2008). 특정 기능 측면에서, 횡격막 기능 장애를 동반한 COPD 환자는 주로 횡격막 근력 감소, 지구력 변화, 가동성 저하 및 횡격막 피로로 나타난다.
횡격막 근력은 주로 근섬유 단면적, 근섬유 유형 및 초기 길이에 의존한다(Mathur et al., 2014). COPD 환자의 횡격막 근섬유 단면적은 감소하고, 근섬유 유형은 속근섬유에서 지근섬유로 변화하며, 폐 과팽창은 횡격막 근육의 길이를 단축시킵니다(Finucane et al., 2005). 이로 인해 COPD 환자의 횡격막 근력이 저하됩니다. Levine 등은 횡격막 섬유의 유형 전환이 ATP 생산 능력을 증가시켰지만, ATP 이용률은 감소하고 특정 힘은 감소하여 압력 생성 능력이 약화되었다는 것을 발견했습니다(Levine et al., 2003). 횡격막 압력(Pdi)은 횡격막 근력을 더 직접적으로 나타내는 지표이다. 중증 COPD 환자의 최대 Pdi는 건강한 대조군의 60%에 불과하다(McCool and Tzelepis, 2012). 폐 용적 증가와 흉벽 기하학적 구조 변화는 횡격막 단축을 초래한다(Silva et al., 2013). 초기 선구적 연구에 따르면 환자의 횡격막은 건강한 피험자에 비해 평균 28% 더 짧았습니다(Rochester and Braun, 1985). 횡격막은 최적 길이에 미치지 못하는 상태로 단축되어, 횡격막 장력이 횡격막 압력으로 전환되는 과정이 비효율적으로 변하며 결과적으로 압력 생성 능력이 감소한다. 또한 폐 과팽창은 횡격막의 작동 길이를 단축시키고 각 부분 간의 기계적 연결을 변화시켜 횡격막 근력을 손상시킨다(Nair et al., 2019).
만성폐쇄성폐질환(COPD) 환자는 횡격막 지구력에 대해 취약한 양의 피트니스(fitness)를 보였다(Papavramidis et al., 2011). 호흡 조절기는 더 짧은 듀티 사이클을 부과하며, 횡격막 섬유가 더 높은 산화도를 가진 II형 근섬유로 전환되는 것이 지구력 증가의 주요 원인이다(Wijnhoven et al., 2006). 그러나 연구에 따르면 안정기 COPD 환자는 정상인에 비해 평균 횡격막 장력-시간 지수(흡기근이 시간 경과에 따라 충분한 압력 생성을 유지하는 능력을 나타냄)가 낮아 COPD 환자의 횡격막 지구력이 감소했음을 시사한다(Ceriana et al., 2017). 향상된 지구력 적응은 특정 범위 내에서만 유지될 수 있다. 그 이유는 횡격막의 낮은 ATP 이용률과 질병 중증도에 따라 횡격막 부하가 지속적으로 증가한다는 사실이다. 결국 근육 약화 증가와 재생을 제한하는 일련의 요인으로 인해 횡격막 지구력이 더욱 손상된다(Macgowan et al., 2001).
Compared with healthy individuals, patients with COPD had reduced diaphragmatic mobility (Gonçalves et al., 2018). Reduced diaphragmatic mobility has been found to be an important factor in decreased exercise tolerance and increased dyspnoea in patients with COPD(Paulin et al., 2007). The maximum level of diaphragm excursion (DEmax) can fully predict improvement in exercise tolerance in patients with COPD. Another study found a strong correlation between diaphragmatic mobility and maximal voluntary ventilation (MVV) in COPD patients, suggesting that greater diaphragmatic mobility was associated with better ventilatory capacity (Rocha et al., 2017). Increased airway resistance, pulmonary hyperinflation and air trapping are the main factors affecting diaphragm activity. Rocha et al. found that the decrease of diaphragm mobility in patients with COPD was related to airway obstruction (Rocha et al., 2017). Shiraishi et al. (2021). found that reduced diaphragmatic mobility may be associated with a range of symptoms associated with dynamic pulmonary hyperinflation. However, another study suggested that diaphragm mobility correlated strongly with pulmonary function parameters that quantify air trapping, moderately with airway resistance and weakly with pulmonary hyperinflation (Dos Santos Yamaguti et al., 2008).
Diaphragmatic fatigue in patients with COPD is characterized by reversible weakening of diaphragmatic contractility and decrease of contractile speed. rom an overall point of view, it is the change of muscle output power. Due to hyperinflation and long-term unfavourable mechanical position, the diaphragm is forced to remain in a state of contraction, which is easy to cause the decline of diaphragm compliance and contraction force, leading to diaphragm fatigue (De Troyer, 1997). Additionally, muscle fibre atrophy and damage to the airway and lung parenchymal structure in patients with COPD lead to increased laborious respiratory movement, resulting in reduced fatigue resistance (McKenzie et al., 2009) (Figure 1).
건강한 사람에 비해 COPD 환자는 횡격막 가동성이 감소했습니다(Gonçalves et al., 2018). 횡격막 가동성 감소는 COPD 환자의 운동 내성 저하 및 호흡곤란 증가의 중요한 요인으로 밝혀졌습니다(Paulin et al., 2007). 최대 횡격막 이동량(DEmax)은 COPD 환자의 운동 내성 개선을 완전히 예측할 수 있다. 또 다른 연구에서는 COPD 환자에서 횡격막 가동성과 최대 자발적 환기량(MVV) 사이에 강한 상관관계가 있음을 발견하여, 더 큰 횡격막 가동성이 더 나은 환기 능력과 연관되어 있음을 시사했다(Rocha et al., 2017). 기도 저항 증가, 폐 과팽창 및 공기 포획은 횡격막 활동에 영향을 미치는 주요 요인이다. Rocha 등은 COPD 환자의 횡격막 가동성 감소가 기도 폐쇄와 관련이 있음을 발견했다(Rocha et al., 2017). Shiraishi et al. (2021)은 횡격막 가동성 감소가 동적 폐 과팽창과 관련된 다양한 증상과 연관될 수 있음을 발견했습니다. 그러나 다른 연구에서는 횡격막 가동성이 공기 포집을 정량화하는 폐 기능 매개변수와 강하게, 기도 저항과 중간 정도로, 폐 과팽창과 약하게 상관관계를 보인다고 제안했습니다(Dos Santos Yamaguti et al., 2008).
COPD 환자의 횡격막 피로는 가역적인 횡격막 수축력 약화와 수축 속도 감소를 특징으로 한다. 전반적으로 근육 출력력의 변화로 볼 수 있다. 과팽창과 장기간의 불리한 기계적 위치로 인해 횡격막은 수축 상태를 유지해야 하며, 이는 횡격막 순응도와 수축력 감소를 쉽게 유발하여 횡격막 피로를 초래한다(De Troyer, 1997). 또한 COPD 환자의 근섬유 위축 및 기도 및 폐 실질 구조 손상은 호흡 운동의 부담을 증가시켜 피로 저항성을 감소시킵니다(McKenzie et al., 2009) (그림 1).
FIGURE 1
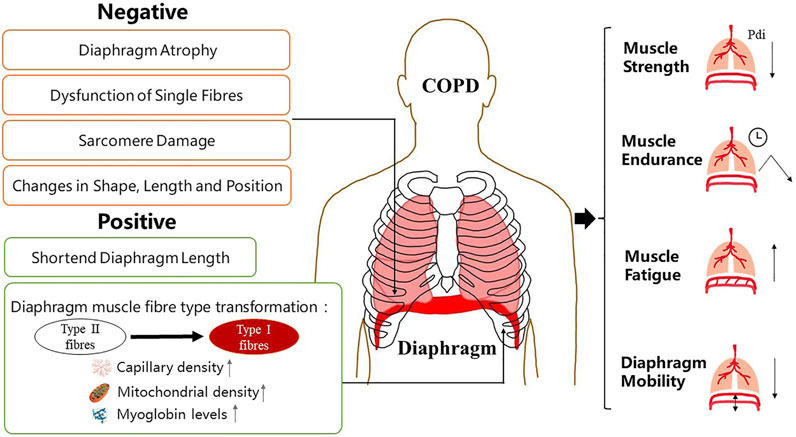
FIGURE 1. Manifestations of diaphragm dysfunction in COPD. Diaphragm dysfunction in patients with COPD is mainly manifested in structural and functional changes. Changes in diaphragm structure include both negative and positive changes. The function of diaphragm depends largely on its physiological characteristics at the structural level. COPD, chronic obstructive pulmonary disease.
그림 1. COPD에서 횡격막 기능 장애의 양상. COPD 환자의 횡격막 기능 장애는 주로 구조적 및 기능적 변화로 나타난다. 횡격막 구조 변화에는 부정적 변화와 긍정적 변화가 모두 포함된다. 횡격막 기능은 구조적 수준에서의 생리적 특성에 크게 좌우된다. COPD: 만성 폐쇄성 폐질환.
3 Mechanisms of Diaphragm Dysfunction in COPD
3.1 Systemic Inflammation and Diaphragm Dysfunction in COPD
According to recent studies, COPD is a systemic disease involving chronic low-grade inflammation and altered protein metabolism throughout the body (Mador and Sethi, 2013). Studies have shown that patients with COPD have a systemic inflammatory response, including the activation of inflammatory cells and increased levels of multiple circulating inflammatory factors, such as tumour necrosis factor-α (TNF-α), interleukin (IL)-1, IL-6, IL-8, and C-reactive protein (Huang et al., 2016). Elevated levels of inflammatory cytokines TNF-α and IL-6 were also found in the diaphragm in patients with severe COPD (Barreiro et al., 2011). Studies have shown that the levels of inflammatory factors are negatively correlated with diaphragm quality and muscle strength, suggesting that systemic inflammation is involved in the occurrence and development of diaphragm dysfunction in patients with COPD (Lin et al., 2010). Different studies have found that the negative effects of systemic inflammation on diaphragm dysfunction in COPD may be caused by multiple pathways.
TNF-α plays a major role in diaphragmatic catabolism and the levels of TNF-α in serum and diaphragm of COPD rats are higher than those of the normal control group, leading to diaphragmatic atrophy. TNF-α may directly stimulate total muscle protein, resulting in decreased protein content and loss of muscle-specific protein. It interacts with its receptor to activate caspase-8, thereby initiating the apoptosis pathway. It also activates the nuclear factor-κB (NF-κB) signalling pathway and induces apoptosis or muscle degradation.
3 COPD에서 횡격막 기능 장애의 기전
3.1 COPD에서의 전신성 염증과 횡격막 기능 장애
최근 연구에 따르면, COPD는 전신에 걸쳐 만성적인 저등급 염증과 단백질 대사 변화를 수반하는 전신성 질환이다(Mador and Sethi, 2013). 연구에 따르면 COPD 환자는 종양 괴사 인자-α(TNF-α), 인터루킨(IL)-1, IL-6, IL-8 및 C-반응성 단백질(Huang et al., 2016)과 같은 여러 순환 염증 인자의 수준 증가 및 염증 세포의 활성화를 포함한 전신 염증 반응을 보입니다. 심한 COPD 환자에서는 횡격막에서도 염증성 사이토카인인 TNF-α와 IL-6의 수치가 상승한 것으로 나타났습니다(Barreiro et al., 2011). 연구에 따르면 염증 인자의 수준은 횡격막의 질과 근력과 음의 상관관계가 있어, 전신 염증이 COPD 환자의 횡격막 기능 장애의 발생 및 진행에 관여함을 시사한다(Lin et al., 2010). 여러 연구에서 COPD에서 전신 염증이 횡격막 기능 장애에 미치는 부정적인 영향은 여러 경로를 통해 발생할 수 있음을 발견했다.
TNF-α는 횡격막 이화 작용에서 주요 역할을 하며, COPD 쥐의 혈청 및 횡격막 내 TNF-α 수치는 정상 대조군보다 높아 횡격막 위축을 유발한다. TNF-α는 총 근육 단백질을 직접 자극하여 단백질 함량 감소 및 근육 특이적 단백질 손실을 초래할 수 있다. 또한 수용체와 상호작용하여 카스파제-8을 활성화함으로써 세포사멸 경로를 개시한다. 또한 핵인자-κB(NF-κB) 신호전달 경로를 활성화하여 세포사멸 또는 근육 분해를 유도합니다.
NF-κB is an important signalling pathway involved in diaphragmatic mass depletion. Haegens and colleagues’ study reported that NF-κB activation and ubiquitin-proteasome system (UPS) mediated protein degradation are required for pulmonary inflammation-induced diaphragm atrophy (Haegens et al., 2012). Genetic studies have shown that inhibition of NF-κB activity promotes muscle regeneration (Mourkioti et al., 2006). Inflammatory factors may upregulate the expression of E3 ubiquitin ligase atrogin-1/MAFbx and muscle ring finger protein 1 (MURF-1) by influencing the NF-κB signalling pathway, so as to accelerate muscle protein decomposition (Attaix et al., 2005). Activation of NF-κB decreased the expression of MyoD mRNA, disrupted the stability of MyoD protein, and decreased the level of MyoD protein (Shirakawa et al., 2021). It could also inhibit muscle formation by suppressing the expression of growth-stimulating molecules, thus interfering with the regeneration of diaphragm and eventually leading to diaphragm dysfunction (Vogiatzis et al., 2007).
In addition, systemic inflammatory mediators indirectly contribute to muscle atrophy through dysregulation of tissue and organ systems, including GCs via the hypothalamic-pituitary-adrenal (HPA) axis, digestion leading to anorexia-cachexia, and altered liver and adipocyte behaviour, all of which subsequently lead to the development of diaphragmatic atrophy (Webster et al., 2020). The exact relationship between systemic inflammation and the process of diaphragmatic atrophy in COPD patients is currently unknown due to the lack of longitudinal data. The specific mechanisms of inflammatory response involved in diaphragm dysfunction have also not been fully elucidated and should be further investigated.
NF-κB는 횡격막 질량 감소에 관여하는 중요한 신호전달 경로입니다. Haegens 등의 연구에 따르면, 폐 염증에 의한 횡격막 위축에는 NF-κB 활성화와 유비퀴틴-프로테아좀 시스템(UPS) 매개 단백질 분해가 필수적이다(Haegens et al., 2012). 유전학적 연구는 NF-κB 활성 억제가 근육 재생을 촉진함을 보여주었다(Mourkioti et al., 2006). 염증 인자는 NF-κB 신호 전달 경로에 영향을 미쳐 E3 유비퀴틴 리가제 아트로긴-1/MAFbx 및 근육 링 핑거 단백질 1(MURF-1)의 발현을 상향 조절하여 근육 단백질 분해를 가속화할 수 있다(Attaix et al., 2005).. NF-κB의 활성화는 MyoD mRNA의 발현을 감소시키고, MyoD 단백질의 안정성을 파괴하며, MyoD 단백질의 수준을 감소시켰습니다 (Shirakawa et al., 2021). 또한 성장 촉진 분자의 발현을 억제하여 근육 형성을 저해함으로써 횡격막의 재생을 방해하고 결국 횡격막 기능 장애를 초래할 수 있습니다 (Vogiatzis et al., 2007).
또한 전신성 염증 매개체는 시상하부-뇌하수체-부신(HPA) 축을 통한 GC를 비롯한 조직 및 장기 시스템의 조절 장애, 식욕부진-악액질을 유발하는 소화 장애, 간 및 지방세포 행동의 변화를 통해 간접적으로 근육 위축에 기여하며, 이 모든 것이 결국 횡격막 위축의 발병으로 이어집니다(Webster et al., 2020). COPD 환자에서 전신 염증과 횡격막 위축 과정 간의 정확한 관계는 종단적 데이터 부족으로 현재 알려지지 않았다. 횡격막 기능 장애에 관여하는 염증 반응의 구체적 기전 또한 완전히 규명되지 않았으며 추가 연구가 필요하다.
3.2 Oxidative Stress and Diaphragm Dysfunction in COPD
Oxidative stress refers to a state of imbalance between oxidation and antioxidant effects in the body. For the first time, Barreiro and colleagues detected higher levels of oxidative stress in the diaphragm of patients with severe COPD than in control muscles, resulting in increased diaphragmatic muscle depletion and diaphragm dysfunction (Barreiro et al., 2005). Reactive oxygen species (ROS) and reactive nitrogen species (RNS) are the triggering factors of diaphragm dysfunction. A certain amount of reactive oxides has a certain effect on muscle fibre adaptation to exercise or disuse state (Ábrigo et al., 2018). However, high levels of ROS and RNS over a long period of time could lead to proteolysis and potential apoptosis (Ji et al., 2006). Oxidative stress promotes muscle atrophy by activating various proteolytic pathways. UPS is the main pathway for intracellular protein degradation and oxidative stress increases protein degradation in the diaphragm by activating the UPS, resulting in diaphragmatic atrophy (Gomes-Marcondes and Tisdale, 2002; Pomiès et al., 2016). Calprotease is a Ca2+-dependent cysteine protease, which could catalyse the restricted hydrolysis of various substrates and plays an important role in the occurrence and development of muscular dystrophy. High ROS levels inhibit sarcoplasmic Ca2+-ATPase activity and prevent Ca2+ reabsorption into the sarcoplasmic reticulum, thus increasing intracellular free Ca2+ concentration and leading to calprotease activation, which promotes muscle degradation (Powers and Jackson, 2008; Whidden et al., 2010). Caspase is closely related to apoptosis and it participates in the apoptosis regulation of muscle cells (Kuwano and Hara, 2000). Oxidative stress can also activate caspase-3 in muscle cells and promote degradation of the complete actin-myosin complex and apoptosis of muscle nucleus cells, resulting in muscle atrophy and loss of muscle nucleus (Du et al., 2004). In addition to the activation of proteolytic enzymes, ROS and RNS modify the diaphragm with protein oxidation, which results in reduced protein activity and makes it more vulnerable to protease degradation. Oxidative damage to muscle proteins prior to characteristic respiratory changes may lead to muscle loss and dysfunction in patients with COPD (Barreiro et al., 2010). Additionally, muscle redox disorder caused by oxidative stress and altered expression of redox-sensitive genes may be responsible for increased susceptibility to diaphragm fatigue (Orozco-Levi, 2003). In conclusion, oxidative stress activates multiple proteolytic pathways, increases protein oxidation and results in altered expression of redox-sensitive genes, leading to diaphragm dysfunction.
3.2 COPD에서의 산화 스트레스와 횡격막 기능 장애
산화 스트레스는 체내 산화 작용과 항산화 효과 간의 불균형 상태를 의미한다. Barreiro 등은 처음으로 중증 COPD 환자의 횡격막에서 대조군 근육보다 높은 수준의 산화 스트레스를 검출했으며, 이는 횡격막 근육의 고갈과 횡격막 기능 장애를 증가시켰습니다(Barreiro et al., 2005). 활성산소종(ROS)과 활성질소종(RNS)은 횡격막 기능 장애의 유발 인자입니다. 일정량의 활성산소는 운동 또는 미사용 상태에 대한 근섬유 적응에 특정 영향을 미친다(Ábrigo et al., 2018). 그러나 장기간 높은 수준의 ROS 및 RNS는 단백질 분해와 잠재적 세포사멸을 유발할 수 있다(Ji et al., 2006). 산화 스트레스는 다양한 단백질 분해 경로를 활성화하여 근육 위축을 촉진한다. UPS(유사소체-프로테아좀 시스템)는 세포 내 단백질 분해의 주요 경로이며, 산화 스트레스는 UPS를 활성화하여 횡격막의 단백질 분해를 증가시켜 횡격막 위축을 초래한다(Gomes-Marcondes and Tisdale, 2002; Pomiès et al., 2016). 칼프로테아제는 Ca2+ 의존성 시스테인 프로테아제로, 다양한 기질의 제한적 가수분해를 촉매하며 근이영양증의 발생 및 진행에 중요한 역할을 합니다. 높은 ROS 수준은 근질 내 Ca2+-ATPase 활성을 억제하고 Ca2+의 근질 내막 재흡수를 방해하여 세포 내 유리 Ca2+ 농도를 증가시키고, 이는 칼프로테아제 활성화를 유발하여 근육 분해를 촉진합니다(Powers and Jackson, 2008; Whidden et al., 2010). 카스파제는 세포 사멸과 밀접한 관련이 있으며 근육 세포의 세포 사멸 조절에 관여한다(Kuwano and Hara, 2000). 산화 스트레스는 또한 근육 세포에서 카스파제-3을 활성화시켜 완전한 액틴-미오신 복합체의 분해와 근육 핵 세포의 세포 사멸을 촉진하여 근육 위축과 근육 핵 손실을 초래한다(Du et al., 2004). 단백질 분해 효소 활성화 외에도, ROS 및 RNS는 단백질 산화를 통해 횡격막을 변형시켜 단백질 활성을 감소시키고 프로테아제 분해에 더 취약하게 만듭니다. 특징적인 호흡 변화 이전에 발생하는 근육 단백질의 산화적 손상은 COPD 환자에서 근육 손실 및 기능 장애를 초래할 수 있습니다(Barreiro et al., 2010). 또한 산화 스트레스와 산화환원 민감 유전자 발현 변화로 인한 근육 산화환원 장애가 횡격막 피로에 대한 감수성 증가의 원인이 될 수 있다(Orozco-Levi, 2003). 결론적으로, 산화 스트레스는 다중 단백질 분해 경로를 활성화하고 단백질 산화를 증가시키며 산화환원 민감 유전자 발현 변화를 초래하여 횡격막 기능 장애를 유발한다.
3.3 Hyperinflation and Diaphragm Dysfunction in COPD
Pulmonary hyperinflation can be due to loss of lung elastic recoil and airway closure at higher volumes, which significantly increases the mechanical load of the diaphragm (Krieger, 2009). The respiratory work of healthy individuals is relatively small and the diaphragm could easily maintain this level of power output. However, the increase of airway resistance places higher demands on diaphragm endurance, which could lead to dyspnoea and reduced exercise tolerance. Hyperinflation results in energy loss and breakdown of muscle proteins, leading to diaphragm atrophy, which makes it even less able to withstand increased stress. Increases in acute and chronic stresses lead to fibre damage and fibrosis of the diaphragm (Scott et al., 2006). During exacerbations of COPD, additional damage to sarcomere may occur when patients are faced with acute diaphragm load, which may further impair diaphragm function (Orozco-Levi et al., 2001), leading to respiratory failure. The increased workload on the diaphragm of patients with severe COPD may also induce oxidative stress and aggravate diaphragm wear by increasing the production of oxidants (Barreiro et al., 2005). Meanwhile, hyperinflation results in changes in diaphragm shape in patients with COPD. A normal diaphragm is located between the thoracoabdominal cavity and it closes the lower thoracic orifice. It is a thin fornix muscle with a flat central part and upward protruding on both sides. The fornix is low on the left and high on the right. By using chest radiographs and spiral CT, Sverzellati et al. found that excessive ventilation resulted in an increase in the radius of curvature of the diaphragm (Sverzellati et al., 2013). Thus, the shape of the diaphragm is nearly flat (Laghi et al., 2021). Normal dome shape plays an important role in diaphragm function. In patients with COPD, diaphragm shape changes and position downshifts away from the optimal mechanical position, resulting in increased respiratory work and diaphragm fatigue (Gayan-Ramirez and Decramer, 2013). In summary, pulmonary hyperinflation increases the dynamic load on the diaphragm, leading to varying degrees of damage and loss of function of the diaphragm cells and subcellular structures. Overloading increases diaphragmatic oxidative stress, leading to biomechanical defects in the diaphragm and ultimately to diaphragmatic dysfunction.
3.3 COPD에서의 과팽창과 횡격막 기능 장애
폐 과팽창은 폐 탄성 반발력 상실과 높은 용적에서의 기도 폐쇄로 인해 발생할 수 있으며, 이는 횡격막의 기계적 부하를 현저히 증가시킵니다(Krieger, 2009). 건강한 개인의 호흡 작업량은 상대적으로 작으며 횡격막은 이 수준의 출력을 쉽게 유지할 수 있습니다. 그러나 기도 저항 증가로 횡격막 내구력에 대한 요구가 높아져 호흡곤란과 운동 내성 감소를 초래할 수 있다. 과팽창은 에너지 손실과 근육 단백질 분해를 유발하여 횡격막 위축을 일으키며, 이는 증가된 스트레스에 대한 저항력을 더욱 약화시킨다. 급성 및 만성 스트레스 증가는 횡격막 섬유 손상과 섬유화를 초래한다(Scott et al., 2006). 만성폐쇄성폐질환(COPD) 악화 시, 환자가 급성 횡격막 부하에 직면하면 추가적인 근절 손상이 발생할 수 있으며, 이는 횡격막 기능을 더욱 저하시켜(Orozco-Levi et al., 2001) 호흡부전으로 이어질 수 있습니다. 중증 COPD 환자의 횡격막에 가해지는 증가된 작업 부하는 또한 산화 스트레스를 유발하고 산화제 생성을 증가시켜 횡격막 마모를 악화시킬 수 있습니다 (Barreiro et al., 2005). 한편, 과팽창은 COPD 환자의 횡격막 형태 변화를 초래한다. 정상 횡격막은 흉복강 사이에 위치하며 하부 흉강 개구부를 막는다. 이는 중앙부가 평평하고 양측이 위쪽으로 돌출된 얇은 포닉스 근육이다. 포닉스는 좌측이 낮고 우측이 높다. Sverzellati 등은 흉부 X선과 나선형 CT를 활용하여 과도한 환기가 횡격막의 곡률 반경을 증가시킨다는 사실을 발견했다(Sverzellati et al., 2013). 따라서 횡격막의 형태는 거의 평평해진다(Laghi et al., 2021). 정상적인 돔 형태는 횡격막 기능에 중요한 역할을 한다. 만성폐쇄성폐질환(COPD) 환자의 경우 횡격막 형태가 변화하고 최적의 기계적 위치에서 하방으로 이동하여 호흡 작업량 증가와 횡격막 피로를 유발한다(Gayan-Ramirez and Decramer, 2013). 요약하면, 폐 과팽창은 횡격막에 가해지는 동적 부하를 증가시켜 횡격막 세포 및 세포 내 구조물의 다양한 정도의 손상과 기능 상실을 초래한다. 과부하는 횡격막의 산화 스트레스를 증가시켜 횡격막의 생체역학적 결함을 초래하고 궁극적으로 횡격막 기능 장애로 이어집니다.
3.4 Chronic Hypoxia and Diaphragm Dysfunction in COPD
Patients with COPD suffer from chronic hypoxia with varying degrees of hypoxemia and hypercapnia due to prolonged expiratory flow obstruction, dysfunction of ventilation and retention of sputum. Studies have shown that chronic hypoxia could reduce the aerobic capacity of the diaphragm, resulting in changes in the histological morphology, contractile properties, and metabolism of the diaphragm (Shiota et al., 2004), causing the diaphragm to be unable to cope with the increased load, which may cause diaphragm dysfunction. Histologically, a reduction in muscle fibre cross-sectional area has been observed in the diaphragm in animal models of chronic hypoxia (McMorrow et al., 2011; Gamboa and Andrade, 2012), decreased mitochondrial density and related protein loss in diaphragm muscle (Gamboa and Andrade, 2010). In terms of contractile properties, chronic hypoxia could reduce the rate of diaphragmatic contraction, inhibit the diaphragmatic isotonic properties and power output and reduce the endurance time during repeated isotonic contractions (Machiels et al., 2001). Metabolically, chronic hypoxia reduces diaphragmatic oxygen consumption and ATP production and it may increase dependence on fatty acid oxidation. Activation of hypoxia-inducible factor (HIF), activation of atrophy signal transduction and increased proteolysis due to chronic hypoxia are the main causes of diaphragm dysfunction (Lewis and O'Halloran, 2016). Hif-1 α, the subunit comprising HIF-1, is a major regulator of the adaptive response of cells to hypoxia stress and its increased expression limits muscle regeneration (Semenza, 2010). In addition, studies have shown that chronic hypoxia activates TNF-α, induces the formation of ROS, and induces high expression of myostatin. These factors can exacerbate systemic inflammation, oxidative stress, and inhibition of myogenesis, respectively (Remels et al., 2007; Gayan-Ramirez and Decramer, 2013), thereby aggravating the damage to diaphragm function. Archiza and colleagues found that female diaphragms were more prone to fatigue under acute hypoxia, which may be related to gender differences in diaphragm metabolism, such as fibre type composition, systolic properties, substrate utilisation and blood perfusion (Archiza et al., 2021). A notable detail that chronic hypoxia could lead to diaphragm dysfunction in patients with COPD, which in turn leads to further hypoxia in a vicious cycle (Bradford, 2004).
3.4 COPD에서의 만성 저산소증과 횡격막 기능 장애
COPD 환자는 장기간의 호기 유량 폐쇄, 환기 기능 장애 및 가래 정체로 인해 다양한 정도의 저산소증과 고탄산혈증을 동반한 만성 저산소증을 겪습니다. 연구에 따르면 만성 저산소증은 횡격막의 유산소 능력을 감소시켜 횡격막의 조직학적 형태, 수축 특성 및 대사에 변화를 일으킬 수 있으며(Shiota et al., 2004), 이로 인해 횡격막이 증가된 부하를 감당하지 못하여 횡격막 기능 장애를 유발할 수 있습니다. 조직학적으로, 만성 저산소증 동물 모델에서 횡격막의 근섬유 단면적 감소가 관찰되었으며(McMorrow et al., 2011; Gamboa and Andrade, 2012), 횡격막 근육에서 미토콘드리아 밀도 감소 및 관련 단백질 손실이 확인되었습니다(Gamboa and Andrade, 2010). 수축 특성에 있어, 만성 저산소증은 횡격막 수축 속도를 감소시키고, 횡격막의 등장성 특성과 출력을 억제하며, 반복적인 등장성 수축 동안의 지구력을 감소시킬 수 있다(Machiels et al., 2001). 대사적으로 만성 저산소증은 횡격막의 산소 소비량과 ATP 생산을 감소시키고 지방산 산화에 대한 의존성을 증가시킬 수 있습니다. 만성 저산소증으로 인한 저산소증 유도 인자(HIF) 활성화, 위축 신호 전달 활성화 및 단백질 분해 증가는 횡격막 기능 장애의 주요 원인입니다(Lewis and O'Halloran, 2016). HIF-1을 구성하는 하위 단위인 Hif-1 α는 저산소 스트레스에 대한 세포의 적응 반응을 조절하는 주요 인자이며, 그 발현 증가는 근육 재생을 제한합니다 (Semenza, 2010). 또한 연구에 따르면 만성 저산소증은 TNF-α를 활성화하고, 활성산소종(ROS) 형성을 유도하며, 미오스타틴의 높은 발현을 유발합니다. 이러한 인자들은 각각 전신 염증, 산화 스트레스, 근육 생성 억제를 악화시킬 수 있습니다(Remels et al., 2007; Gayan-Ramirez and Decramer, 2013), 이로 인해 횡격막 기능 손상이 심화됩니다. Archiza와 동료들은 급성 저산소 상태에서 여성 횡격막이 피로에 더 취약하다는 사실을 발견했는데, 이는 섬유 유형 구성, 수축 특성, 기질 이용 및 혈액 관류와 같은 횡격막 대사의 성별 차이와 관련이 있을 수 있습니다 (Archiza et al., 2021). 만성 저산소증이 COPD 환자에게 횡격막 기능 장애를 유발할 수 있으며, 이는 악순환 속에서 더 심각한 저산소증을 초래할 수 있다는 점이 주목할 만한 세부 사항입니다(Bradford, 2004).
3.5 Malnutrition and Diaphragm Dysfunction in COPD
Patients with COPD often suffer from malnutrition due to inadequate energy and nutrient intake, gastrointestinal digestive and absorption dysfunction, increased energy expenditure and enhanced catabolism (Holst et al., 2019; Kaluźniak-Szymanowska et al., 2021). According to statistics, 25%–40% of patients with COPD are malnourished (Cano et al., 2004; Vermeeren et al., 2006). Malnutrition causes COPD patients to gradually develop a negative nitrogen balance. The massive consumption of fat and protein causes muscle atrophy and reduced muscle mass. The structural and functional changes of diaphragm caused by malnutrition may evolve into diaphragm dysfunction. At the structural level, malnutrition could directly lead to increased muscle consumption (Xie et al., 2021). Malnutrition is associated with increased diaphragmatic diastolic ratio, decreased muscle weight, decreased fibre size, decreased percentage of type II fibre, and consumption of energy-rich compounds (Orozco-Levi, 2003). At the functional level, malnutrition causes an imbalance in the energy supply and demand of the diaphragm, along with damage to the respiratory system and the body’s defense system. Malnutrition may lead to a reduction in the mass of the diaphragm, which reduces the power to maintain normal ventilation and decreases muscle strength and endurance (Sahebjami and Sathianpitayakul, 2000). In general, malnutrition mainly affects the activity of glycolytic enzymes but it does not impair the function of oxidative pathways. A notable detail that although malnutrition may be associated with diaphragm dysfunction, it is also associated with the severity of malnutrition and its effect is clinically relevant only in some patients. Hamnegard studied diaphragm strength in two groups of 10 patients with severe COPD and found that the levels of malnutrition did not cause diaphragm weakness (Hamnegard et al., 2002), possibly because these changes are related to changes in diaphragm structure without affecting the overall changes in diaphragm function. Structural damage does not necessarily lead to loss of function.
The mechanisms of diaphragm dysfunction in patients with COPD are correlated. For example, oxidative stress could serve as a signal for the expression of inflammatory mediators and inflammation could regulate ROS production and thus oxidative stress levels (Thoma and Lightfoot, 2018). The increased load caused by hyperinflation could induce oxidative stress and aggravate diaphragm wear (Barreiro et al., 2005). Inflammatory factors have been shown to be involved in the development of malnutrition through the fusion of multiple mechanisms (Laviano et al., 2003). Hyperinflation plays an important role in chronic hypoxia and hypercapnia (Zysman et al., 2021). Such interactions may further complicate the condition of diaphragmatic dysfunction. But it also means that partial improvement in each factor has the potential to improve the overall situation. Well-organized rehabilitation has been proven to have a positive effect on diaphragmatic dysfunction in COPD by eliminating adverse triggers and improving functional performance of the diaphragm.
3.5 COPD에서의 영양실조와 횡격막 기능 장애
COPD 환자는 에너지 및 영양소 섭취 부족, 위장관 소화 및 흡수 기능 장애, 에너지 소비 증가, 강화된 이화 작용으로 인해 종종 영양실조를 겪습니다(Holst et al., 2019; Kaluźniak-Szymanowska et al., 2021). 통계에 따르면, COPD 환자의 25%~40%가 영양실조 상태입니다(Cano et al., 2004; Vermeeren et al., 2006). 영양실조는 COPD 환자에게 점진적인 음의 질소 균형을 유발합니다. 지방과 단백질의 과도한 소비는 근육 위축과 근육량 감소를 초래합니다. 영양실조로 인한 횡격막의 구조적·기능적 변화는 횡격막 기능 장애로 발전할 수 있습니다. 구조적 수준에서 영양실조는 직접적으로 근육 소모 증가를 유발할 수 있습니다(Xie et al., 2021). 영양실조는 횡격막 이완기 비율 증가, 근육량 감소, 섬유 크기 감소, II형 섬유 비율 감소 및 고에너지 화합물 소모와 관련이 있습니다(Orozco-Levi, 2003). 기능적 수준에서는 영양실조가 횡격막의 에너지 공급과 수요 불균형을 초래하며, 호흡계 및 신체 방어 체계 손상을 동반한다. 영양실조는 횡격막 질량 감소를 유발하여 정상적인 환기 유지 능력을 저하시키고 근력과 지구력을 감소시킬 수 있다(Sahebjami and Sathianpitayakul, 2000). 일반적으로 영양실조는 주로 당분해 효소 활성에 영향을 미치지만 산화 경로의 기능에는 손상을 주지 않습니다. 주목할 점은 영양실조가 횡격막 기능 장애와 연관될 수 있지만, 이는 영양실조의 중증도와 관련이 있으며 그 영향은 일부 환자에서만 임상적으로 의미가 있다는 것입니다. Hamnegard는 중증 COPD 환자 10명씩 두 그룹에서 횡격막 강도를 연구한 결과, 영양실조 수준이 횡격막 약화를 유발하지 않는다는 사실을 발견했습니다(Hamnegard et al., 2002). 이는 이러한 변화가 횡격막 기능의 전반적 변화에는 영향을 미치지 않으면서 횡격막 구조의 변화와 관련되어 있기 때문일 수 있습니다. 구조적 손상이 반드시 기능 상실로 이어지지는 않습니다.
COPD 환자의 횡격막 기능 장애 메커니즘은 상호 연관되어 있다. 예를 들어, 산화 스트레스는 염증 매개체 발현의 신호 역할을 할 수 있으며, 염증은 ROS 생성을 조절하여 산화 스트레스 수준을 변화시킬 수 있다(Thoma and Lightfoot, 2018). 과팽창으로 인한 부하 증가는 산화 스트레스를 유발하고 횡격막 마모를 악화시킬 수 있다(Barreiro et al., 2005). 염증 인자는 여러 기전의 융합을 통해 영양실조 발생에 관여하는 것으로 밝혀졌습니다(Laviano et al., 2003). 과팽창은 만성 저산소증 및 고이산화탄소혈증에 중요한 역할을 합니다(Zysman et al., 2021). 이러한 상호작용은 횡격막 기능 장애 상태를 더욱 복잡하게 만들 수 있습니다. 그러나 이는 각 요인의 부분적 개선이 전체 상황 개선 가능성을 시사하기도 합니다. 잘 조직된 재활은 불리한 유발 요인을 제거하고 횡격막의 기능적 성능을 향상시킴으로써 COPD에서 횡격막 기능 장애에 긍정적인 영향을 미치는 것으로 입증되었습니다.
4 Rehabilitation Treatment of Diaphragm Dysfunction in COPD
To date, the clinical attention paid to the prevention and treatment of diaphragm dysfunction in patients with COPD is not sufficient. Certain clinical interventions could even aggravate diaphragm dysfunction. For instance, long-term mechanical ventilation could further aggravate diaphragm dysfunction and even makes it difficult to get off the ventilator (Marchioni et al., 2019). IMT, exercise intervention and nutritional support are the main rehabilitation treatment that have been proven to be effective in improving diaphragm function. They are expected to improve diaphragm strength and endurance, enhance the exercise tolerance of patient and improve symptoms such as dyspnoea, overall, improve health-related quality of life (HRQL).
4 COPD에서 횡격막 기능 장애의 재활 치료
현재까지 COPD 환자의 횡격막 기능 장애 예방 및 치료에 대한
임상적 관심은 충분하지 않습니다.
일부 임상적 개입은
횡격막 기능 장애를 악화시킬 수도 있습니다.
예를 들어,
장기적인 기계적 인공호흡은 횡격막 기능 장애를 더욱 악화시키고
인공호흡기에서 벗어나는 것을 어렵게 만들 수도 있습니다(Marchioni et al., 2019).
IMT, 운동 중재 및 영양 지원은
횡격막 기능 개선에 효과적인 것으로 입증된 주요 재활 치료법입니다.
이러한 치료법은 횡격막의 힘과 지구력을 향상시키고,
환자의 운동 내성을 증진시키며,
호흡곤란과 같은 증상을 개선하여 전반적으로 건강 관련 삶의 질(HRQL)을 향상시킬 것으로 기대됩니다.
4.1 Inspiratory Muscle Training
IMT applies a load to the diaphragm and accessory inspiratory muscles to increase their strength and endurance. It has been proven to improve inspiratory muscle strength, relieve dyspnoea, and improve exercise capacity in COPD patients (Beckerman et al., 2005; Hill et al., 2006; Magadle et al., 2007). The American Thoracic Society/European Respiratory Society (ATS/ERS) guidelines for pulmonary rehabilitation recommend IMT as an effective adjunct to pulmonary rehabilitation. Breathing techniques and neuromuscular electrical stimulation can reinforce and complement the effects of diaphragmatic training. Strengthening of the intercostal muscle synergistically improves diaphragm function and increases the functional reserve of the inspiratory muscles.
4.1 흡기근 훈련
흡기근 훈련(IMT)은
횡격막과 보조 흡기근에 부하를 가해 그 힘과 지구력을 증가시킵니다.
이 훈련은 흡기근 강도를 향상시키고,
호흡곤란을 완화하며,
만성 폐쇄성 폐질환(COPD) 환자의 운동 능력을 개선하는 것으로 입증되었습니다(Beckerman et al., 2005; Hill et al., 2006; Magadle et al., 2007).
미국흉부학회/유럽호흡기학회(ATS/ERS)의 폐 재활 지침은
폐 재활의 효과적인 보조 수단으로 IMT를 권장합니다.
호흡 기술과 신경근 전기 자극은
횡격막 훈련의 효과를 강화하고 보완할 수 있습니다.
늑간근 강화는
횡격막 기능을 시너지적으로 개선하고
흡기근의 기능적 예비력을 증가시킵니다.
4.1.1 Diaphragm Training
Diaphragm training is performed via devices that impose resistive or threshold loads, including inspiratory resistive training and threshold pressure training. Inspiratory resistive training is a method of continuous resistance breathing on the resistive load device at a normal breathing rate. The amount of inspiratory resistance during training depends on the amount of air the patient is breathing. Studies have shown that inspiratory resistive training could combat diaphragm fatigue, increase diaphragm strength and endurance and relieve dyspnoea (Madariaga et al., 2007). In threshold pressure training, the threshold inspiratory muscle trainer is used to set the given domain pressure and the patient’s respiratory work could only reach a certain threshold to open the channel in the trainer and make air flow. Studies have shown that threshold pressure training could enhance the muscle strength and endurance of the diaphragm to relieve dyspnoea and improve lung function (Sturdy et al., 2003; Lee et al., 2021). The threshold pressure training has better effect than inspiratory resistive training (Wu et al., 2017). Notably, recent studies have shown that long-term diaphragm training with high resistance load could lead to diaphragmatic injury, especially in patients with advanced COPD(Bertoni et al., 2019). During diaphragmatic training, patients are usually unable to maintain a high constant load training for a long time due to factors, such as anaerobic respiration, lactic acid accumulation and inadequate perfusion adjustment (Louvaris et al., 2021). In view of this situation, low load should be selected for diaphragm training, which could usually be set to 15–50% of the maximum suction negative pressure, to achieve a relatively safe and efficient improvement of diaphragm function.
4.1.1 횡격막 훈련
횡격막 훈련은
흡기 저항 훈련 및 역치 압력 훈련을 포함하여
저항성 또는 역치 부하를 가하는 장치를 통해 수행됩니다.
흡기 저항 훈련은
정상 호흡 속도로 저항 부하 장치에 대한 지속적 저항 호흡을 수행하는 방법이다.
훈련 중 흡기 저항량은
환자가 호흡하는 공기량에 따라 달라진다.
연구에 따르면 흡기 저항 훈련은
횡격막 피로를 완화하고,
횡격막 근력과 지구력을 향상시키며, 호흡곤란을 완화할 수 있다(Madariaga et al., 2007).
역치 압력 훈련에서는
역치 흡기 근육 트레이너를 사용하여 주어진 영역 압력을 설정하며,
환자의 호흡 작업은 트레이너 내 채널을 열고 공기 흐름을 발생시키기 위해 특정 역치에 도달해야만 한다.
연구에 따르면
역치 압력 훈련은 횡격막의 근력과 지구력을 향상시켜
호흡곤란을 완화하고 폐 기능을 개선할 수 있다(Sturdy et al., 2003; Lee et al., 2021).
역치 압력 훈련은
흡기 저항 훈련보다 더 우수한 효과를 보인다(Wu et al., 2017).
특히 최근 연구에 따르면,
고저항 부하를 이용한 장기적인 횡격막 훈련은
특히 중증 COPD 환자에서 횡격막 손상을 유발할 수 있다(Bertoni et al., 2019).
횡격막 훈련 중 환자들은
무산소 호흡, 젖산 축적, 불충분한 관류 조절 등의 요인으로 인해
일반적으로 높은 일정 부하 훈련을 장시간 유지하지 못한다(Louvaris et al., 2021).
이러한 상황을 고려하여 횡격막 훈련에는
낮은 부하를 선택해야 하며,
이는 일반적으로 최대 흡입 음압의 15~50%로 설정하여
비교적 안전하고 효율적인 횡격막 기능 개선을 달성할 수 있습니다.
Breathing techniques include diaphragmatic breathing and pursed-lips breathing, which can be utilised as compensatory therapy for patients who are unable to exercise (Mendes et al., 2019). Diaphragmatic breathing minimises the respiratory demand of the disease, improving breathing patterns and ventilation efficiency without causing respiratory dyspnoea (Fernandes et al., 2011).Diaphragmatic breathing enables the diaphragm to be fully exercised, thus increasing muscle strength and endurance. Pursed-lips breathing could prevent premature closure of small airways, improve gas exchange and relieve hypoxia symptoms of patients. Studies have shown that pursed-lips breathing could effectively reduce the minute ventilation and respiratory rate during exercise in patients with COPD (Mayer et al., 2018). Pursed-lips breathing can reduce dynamic hyperinflation (de Araujo et al., 2015), thereby reducing the diaphragm load. It could also improve patients’ exercise tolerance (Cabral et al., 2015). Studies have shown that diaphragmatic breathing combined with pursed-lips breathing could increase tidal volume, improve chest wall volume by shortening breathing cycle and relieve diaphragm fatigue by reducing breathing rate (Mendes et al., 2019). Due to the simplicity of implementation and the low incidence of serious adverse effects during training, breathing techniques are suitable for patients with COPD at all stages.
Neuromuscular electrical stimulation trains muscle strength by stimulating the diaphragm and related nerves with a controllable current (Vieira et al., 2014). Studies have shown that neuromuscular electrical stimulation could promote muscle protein synthesis, increase muscle mass and improve diaphragm muscle strength and fatigue resistance (Maddocks et al., 2016), especially for patients with moderate and severe COPD with limited exercise capacity. However, because it is passive training, neuromuscular electrical stimulation should be combined with active exercise to achieve enhanced rehabilitation effect as an alternative to routine rehabilitation exercise.
호흡 기법에는 횡격막 호흡과 입술을 오므린 호흡이 있으며,
운동이 불가능한 환자에게 보상 요법으로 활용될 수 있습니다(Mendes et al., 2019).
횡격막 호흡은
호흡 곤란을 유발하지 않으면서
호흡 패턴과 환기 효율을 개선하여 질환의 호흡 요구량을 최소화한다(Fernandes et al., 2011).
횡격막 호흡은
횡격막을 완전히 운동시켜 근력과 지구력을 증가시킨다.
입술 오므리기 호흡은
소기도의 조기 폐쇄를 방지하고,
가스 교환을 개선하며, 환자의 저산소증 증상을 완화할 수 있다.
연구에 따르면 입술 오므리기 호흡은
COPD 환자의 운동 중 분당 환기량과 호흡수를 효과적으로 감소시킬 수 있다(Mayer et al., 2018).
입술 오므리기 호흡은
동적 과팽창을 줄여(de Araujo et al., 2015) 횡격막 부하를 감소시킬 수 있으며,
환자의 운동 내성을 향상시킬 수 있다(Cabral et al., 2015).
연구에 따르면,
횡격막 호흡과 입술 오므리기 호흡을 병행하면 호흡량을 증가시키고
호흡 주기를 단축하여 흉벽 용적을 개선하며 호흡수를 감소시켜
횡격막 피로를 완화할 수 있다(Mendes et al., 2019).
실행이 간편하고 훈련 중 심각한 부작용 발생률이 낮기 때문에,
호흡 기법은 모든 단계의 COPD 환자에게 적합하다.
신경근 전기 자극은
제어 가능한 전류로 횡격막 및 관련 신경을 자극하여 근력을 훈련합니다(Vieira 외, 2014).
연구에 따르면 신경근 전기 자극은
근육 단백질 합성을 촉진하고 근육량을 증가시키며,
특히 운동 능력이 제한된 중증 및 중등도 COPD 환자의 횡격막 근력 및 피로 저항성을 향상시킬 수 있습니다(Maddocks et al., 2016).
그러나
수동적 훈련이기 때문에 신경근 전기 자극은
일상 재활 운동의 대체 수단으로 강화된 재활 효과를 얻기 위해 능동적 운동과 병행해야 합니다.
4.1.2 Intercostal Muscle Training
The contraction of intercostal muscles causes the ribs to move outward and upward, assisting the diaphragm in the coordination of inspiratory completion (Rohrbach et al., 2003). Training the intercostal muscles could increase their strength, endurance and mobility, thereby improving their ability to resist high-load exercise and reducing the load on the diaphragm. Intercostal muscle training mostly adopts exercise that promote upper body activities, such as chest expansion, rotation, swimming and various ball games (Zhou and Sun, 2021). Intercostal muscle training has high compliance requirements for patients and it is suitable for patients with mild to moderate COPD.
4.1.2 늑간근 훈련
늑간근 수축은
늑골을 바깥쪽과 위쪽으로 움직여 횡격막이 호흡 완료를 협응하는 데 도움을 줍니다(Rohrbach et al., 2003).
늑간근 훈련은 근력, 지구력 및 가동성을 증가시켜
고부하 운동에 대한 저항 능력을 향상시키고 횡격막에 가해지는 부하를 줄일 수 있습니다.
늑간근 훈련은
주로 상체 활동을 촉진하는 운동(가슴 확장, 회전, 수영, 다양한 볼 게임 등)을 채택한다(Zhou and Sun, 2021).
늑간근 훈련은 환자의 순응도가 높아
경증에서 중등도 COPD 환자에게 적합하다.
4.2 Exercise Intervention
Exercise is the core content of pulmonary rehabilitation treatment of COPD. Personalised strength and endurance training plan is the cornerstone of pulmonary rehabilitation. It could effectively improve the diaphragm dysfunction of patients with COPD. Studies have shown that exercise could improve local muscle inflammation and even systemic inflammation in patients with COPD by significantly reducing the levels of inflammatory factors, such as TNF-α, in muscle and increasing the levels of anti-inflammatory factors, such as IL-10 (Toledo-Arruda et al., 2017). Exercise also improves oxidative stress in patients with COPD by increasing antioxidant capacity (Vieira Ramos et al., 2018), reducing the activity of oxidase and improving mitochondrial function (Zhang et al., 2021). Long-term exercise could correct chronic hypoxia by improving the oxygen utilisation efficiency of the body. Nutritional status could be improved by increasing appetite and regulating intestinal flora (Donati Zeppa et al., 2021). Thus, exercise could improve diaphragm dysfunction by reducing adverse factors that lead to negative changes in diaphragmatic structure and function as a whole. In addition to the positive effects of direct action on the diaphragm, exercise interventions can train the supporting muscles of the abdomen, back and limbs. These muscles play a better supporting and supportive role during respiration, reducing the fatigue of the diaphragm and thus improving its function.
4.2 운동 중재
운동은
COPD의 폐 재활 치료 핵심 내용이다.
개인 맞춤형 근력 및 지구력 훈련 계획은 폐 재활의 초석으로,
COPD 환자의 횡격막 기능 장애를 효과적으로 개선할 수 있다.
연구에 따르면
운동은 근육 내 TNF-α와 같은 염증 인자 수치를 현저히 감소시키고
IL-10과 같은 항염증 인자 수치를 증가시켜
COPD 환자의 국소 근육 염증 및 전신 염증을 개선할 수 있다(Toledo-Arruda et al., 2017).
운동은 또한 항산화 능력 향상(Vieira Ramos et al., 2018),
산화효소 활성 감소 및 미토콘드리아 기능 개선(Zhang et al., 2021)을 통해
COPD 환자의 산화 스트레스를 개선합니다.
장기적인 운동은
신체의 산소 이용 효율을 향상시켜 만성 저산소증을 교정할 수 있습니다.
영양 상태는
식욕 증진과 장내 미생물군 조절을 통해 개선될 수 있습니다(Donati Zeppa et al., 2021).
따라서 운동은 횡격막 구조와 기능 전반에 부정적 변화를 초래하는 유해 요인을 감소시켜 횡격막 기능 장애를 개선할 수 있습니다. 횡격막에 대한 직접적 작용의 긍정적 효과 외에도, 운동 중재는 복부, 등 및 사지의 보조 근육을 훈련시킬 수 있습니다. 이러한 근육들은 호흡 시 더 나은 지지 및 보조 역할을 수행하여 횡격막의 피로를 줄이고 그 기능을 향상시킵니다.
훈련 계획의 운동 처방 구성 요소에는 운동 형태, 강도, 빈도 및 지속 시간이 포함됩니다. 유산소 운동과 저항 운동은 COPD 환자 재활에 가장 흔히 사용되는 운동 형태입니다. 유산소 운동은 전신 주요 근육군을 동원하는 주기적이고 동적인 활동입니다. 이는 폐 재활 표준 훈련의 기초가 됩니다. 자전거 타기나 걷기와 같은 하지 지구력 훈련이 가장 흔히 사용되는 유산소 운동입니다. 연구에 따르면 유산소 운동은 횡격막 지구력과 주요 근육군의 근력을 향상시키고 횡격막 피로를 완화합니다(Wada et al., 2016; Burtch et al., 2017). 저항 운동은 외부 저항을 극복하기 위한 근육의 능동적 움직임을 의미하며, 일반적으로 덤벨, 탄성 밴드 및 기타 저항 훈련 장비를 활용한다(Hoff et al., 2007). Spruit 등은 저항 운동이 환자의 호흡근 근력, 운동 능력 및 건강 관련 삶의 질(HRQL)을 유의미하게 개선한다고 보고하였다(Spruit et al., 2002).
Panton 등은 저항 운동이 유산소 운동의 유용한 보완 수단이 될 수 있으며, 근육 약화와 위축을 효과적으로 개선할 수 있음을 발견했다(Panton et al., 2004). 저항 운동을 추가하면 현재 유산소 운동 프로그램에 참여 중인 만성 폐쇄성 폐질환(COPD) 환자의 기능적 결과가 개선되었다(Skumlien et al., 2007). 횡격막에 대한 직접적인 긍정적 효과 외에도, 운동은 복부, 등 및 사지의 보조 근육을 훈련시켜 호흡 과정에서 더 나은 보조 및 지지 역할을 수행하게 하고, 횡격막 피로를 완화하며, 횡격막 기능 장애를 개선할 수 있습니다.
The constituent elements of the exercise prescription of the training plan include the form, intensity, frequency, and duration of exercise. Aerobic and resistance exercise are the most common forms of exercise used in the rehabilitation of COPD patients. Aerobic exercise is a periodic and dynamic activity involving the major muscle groups of the whole body. It is the basis of the standard training of pulmonary rehabilitation. Lower-extremity endurance training, such as cycling or walking, is the most commonly used aerobic exercise. Studies have shown that aerobic exercise enhances diaphragm endurance and the muscle strength of major muscle groups and relieve diaphragm fatigue (Wada et al., 2016; Burtch et al., 2017). Resistance exercise refers to the active movement of muscles to overcome external resistance, usually with the help of dumbbells, elastic bands and other impedance training equipment (Hoff et al., 2007). Spruit and colleagues reported that resistance exercise significantly improves respiratory muscle strength, exercise capacity and HRQL in patients (Spruit et al., 2002). Panton et al. found that resistance exercise can be a useful supplement to aerobic exercise, effectively improving muscle weakness and atrophy (Panton et al., 2004). The addition of resistance exercise improved functional outcomes in COPD patients currently participating in an aerobic exercise programme (Skumlien et al., 2007). In addition to the positive effect of direct action on the diaphragm, exercise could train the auxiliary muscles in the abdomen, back and limbs for these muscles to play a better auxiliary and supporting role in the breathing process, relieve diaphragm fatigue, and improve diaphragm dysfunction.
With regard to exercise intensity, studies have shown that patients with stable COPD have better clinical outcomes with high-intensity training than with low-intensity training. Higher intensity exercise significantly improves respiratory muscle strength (Gimenez et al., 2000), reduces minute ventilation (Ve), and reduces dyspnoea (Vallet et al., 1997). High intensity here refers to the exercise close to the individual’s peak level, which is operationally defined as reaching at least 60%–85% of the peak working speed during the incremental maximum exercise test, rather than training at high absolute work levels. Similarly, low intensity refers to 20%–40% of the peak working speed during the incremental maximum exercise test (Norton et al., 2010). A single bout of strenuous exercise may increase the level of oxidative stress in the diaphragm in patients with COPD, leading to diaphragm fatigue (Itoh et al., 2004). In addition to being based on objective data, exercise intensity can be developed by the degree of respiratory distress perceived by the patient during exercise. The recommended intensity for resistance training consists of performing one to four sets of 40%–50% resistance of one repetition maximum (RM) for 10 to 15 repetitions ≥2 days per week (Garvey et al., 2016).
Regarding exercise frequency, it is recommended that aerobic exercise is 3–5 times a week and resistance exercise is at least 2 times a week (Spruit et al., 2013). In terms of duration, a 6–12 weeks training program is recommended (Bolton et al., 2013). Some studies have shown that longer-term programs may provide more lasting benefits (du Moulin et al., 2009; Beauchamp et al., 2013).
Noninvasive positive-pressure ventilation (NPPV) includes continuous positive airway pressure, pressure support and proportional assist ventilation (PAV). NPPV is particularly suitable for COPD patients with hypercapnia and mild to moderate respiratory failure (Lightowler et al., 2003; Köhnlein et al., 2014), and can be an important adjunct to exercise training in COPD patients. Hawkins et al. found that compared to spontaneous breathing, the use of PAV in conjunction with exercise training significantly improved exercise capacity and reduced exercise fatigue (Hawkins et al., 2002). Garrod and colleagues report that the use of NPPV as an adjunct to exercise training in COPD patients can help improve exercise tolerance and health status (Garrod et al., 2000). Non-invasive ventilation can reduce hyperinflation (Dennis et al., 2021).The main objective of NPPV in patients with severe COPD is to improve gas exchange and to provide adequate rest for the respiratory muscles after periods of fatigue (García et al., 2011). NPPV assists the diaphragm in respiratory movements, which helps to relieve the burden on the diaphragm, reduce respiratory work and promote the recovery of diaphragmatic dysfunction (Duiverman et al., 2016). However, as it is passive ventilation, the effect of training the diaphragm to contract on its own is lost to a certain extent. It is recommended as an adjunct to exercise training and is not recommended for long-term use.
운동 강도에 관해 연구들은 안정기 COPD 환자가 저강도 훈련보다 고강도 훈련 시 더 나은 임상 결과를 보인다는 점을 보여주었다. 고강도 운동은 호흡근 강도를 유의미하게 향상시키고(Gimenez et al., 2000), 분당 환기량(Ve)을 감소시키며, 호흡곤란을 완화시킨다(Vallet et al., 1997). 여기서 고강도란 개인의 최대 수준에 근접한 운동을 의미하며, 절대적인 고강도 훈련이 아닌 점진적 최대 운동 검사 중 최대 작업 속도의 최소 60%~85%에 도달하는 것으로 정의된다. 마찬가지로 저강도는 점진적 최대 운동 검사 중 최대 작업 속도의 20%~40%에 해당하는 수준을 말한다(Norton et al., 2010). 한 번의 격렬한 운동은 COPD 환자의 횡격막에서 산화 스트레스 수준을 증가시켜 횡격막 피로를 유발할 수 있습니다(Itoh et al., 2004). 운동 강도는 객관적 데이터에 기반할 뿐만 아니라, 운동 중 환자가 인지하는 호흡 곤란 정도에 따라 설정될 수 있습니다. 저항 운동의 권장 강도는 1회 최대 반복량(RM)의 40~50% 저항으로 10~15회 반복을 1~4세트 수행하며, 주당 2일 이상 실시하는 것입니다(Garvey et al., 2016).
운동 빈도에 관해서는 유산소 운동은 주 3~5회, 저항 운동은 주 2회 이상 실시할 것을 권장합니다(Spruit et al., 2013). 기간 측면에서는 6~12주 훈련 프로그램이 권장됩니다(Bolton et al., 2013). 일부 연구에 따르면 장기 프로그램이 더 지속적인 효과를 제공할 수 있습니다(du Moulin et al., 2009; Beauchamp et al., 2013).
비침습적 양압 환기(NPPV)에는 지속적 양압 호흡(CPAP), 압력 지원(PS) 및 비례 보조 환기(PAV)가 포함됩니다. NPPV는 고탄산혈증과 경증에서 중등도의 호흡부전을 동반한 만성폐쇄성폐질환(COPD) 환자에게 특히 적합하며(Lightowler et al., 2003; Köhnlein et al., 2014), COPD 환자의 운동 훈련에 중요한 보조 수단이 될 수 있습니다. Hawkins 등은 자발 호흡에 비해 운동 훈련과 병행한 PAV 사용이 운동 능력을 유의하게 향상시키고 운동 피로를 감소시킨다는 사실을 발견했다(Hawkins et al., 2002). Garrod 등은 COPD 환자에서 운동 훈련 보조 수단으로 NPPV를 사용하면 운동 내성과 건강 상태 개선에 도움이 될 수 있다고 보고했다(Garrod et al., 2000). 비침습적 인공호흡은 과팽창을 감소시킬 수 있다(Dennis et al., 2021). 중증 COPD 환자에서 NPPV의 주요 목적은 가스 교환을 개선하고 피로 후 호흡근에 충분한 휴식을 제공하는 것이다(García et al., 2011). NPPV는 호흡 운동에서 횡격막을 보조하여 횡격막의 부담을 덜어주고, 호흡 작업을 줄이며, 횡격막 기능 장애의 회복을 촉진하는 데 도움이 됩니다(Duiverman et al., 2016). 그러나 수동적 인공호흡이기 때문에 횡격막이 스스로 수축하도록 훈련하는 효과는 어느 정도 상실됩니다. 운동 훈련의 보조 수단으로 권장되며 장기 사용은 권장되지 않습니다.
4.3 Nutritional Support
As mentioned above, chronic malnutrition is an important factor in diaphragm dysfunction, and even respiratory failure. Studies have shown that appropriate nutritional support can significantly improve calorie and protein intake, enhance inspiratory muscle function, improve exercise capacity and alleviate dyspnoea symptoms (Weekes et al., 2009; Collins et al., 2013). Nutritional support can improve diaphragm dysfunction in patients with COPD by regulating inflammation, improving oxidative stress and regulating carbon dioxide production (Broekhuizen et al., 2005; Marín-Hinojosa et al., 2021).The main forms of nutritional support include dietary strategy and oral nutritional supplement (ONS).
The dietary strategy is to adjust the daily dietary structure of patients, and provide personalized food fortification, food snacks and dietary suggestions according to the age, illness and nutritional status of patients. Patients with COPD are often complicated with protein-energy malnutrition, so the diet should be supplied with sufficient calories (Akner and Cederholm, 2001). The respiratory quotient (RQ) of carbohydrates is high, which will produce more CO2 after oxidation in the body, causing or aggravating CO2 retention, aggravating dyspnoea and the burden of diaphragm, so the diet of COPD patients should reduce the energy supply ratio of carbohydrates (Anker et al., 2006). The carbohydrate intake of patients with stable COPD should account for 50%–60% of the total energy, while the carbohydrate intake of patients with acute exacerbation should account for 35%–50%, but the whole day carbohydrate should not be less than 150 g. The RQ of fat is very low. The proportion of fat intake can be appropriately increased. The fat supply of COPD patients in stable stage can account for 20%–30% of the total energy. Patients with COPD suffer from hyperproteinysis, which is also an important factor in diaphragm atrophy. Therefore, a high protein diet should be provided to promote anabolism. Protein supply can be calculated as 1.2–1.5 g/kg body weight per day, accounting for 15%–20% of total energy (Schols et al., 2014). Moreover, adequate vitamins, minerals, and trace elements should also be supplied in the diet.
4.3 영양 지원
앞서 언급한 바와 같이 만성 영양실조는 횡격막 기능 장애, 심지어 호흡 부전의 중요한 요인입니다. 연구에 따르면 적절한 영양 지원은 칼로리 및 단백질 섭취를 크게 개선하고, 흡기 근육 기능을 강화하며, 운동 능력을 향상시키고 호흡곤란 증상을 완화시킬 수 있습니다(Weekes et al., 2009; Collins et al., 2013). 영양 지원은 염증 조절, 산화 스트레스 개선, 이산화탄소 생성 조절을 통해 COPD 환자의 횡격막 기능 장애를 개선할 수 있습니다(Broekhuizen et al., 2005; Marín-Hinojosa et al., 2021). 영양 지원의 주요 형태로는 식이 전략과 경구 영양 보충제(ONS)가 있습니다.
식이 전략은 환자의 연령, 질환 및 영양 상태에 따라 일일 식이 구조를 조정하고 맞춤형 식품 강화, 간식 및 식이 권장사항을 제공하는 것이다. COPD 환자는 종종 단백질-에너지 영양실조가 동반되므로 식이에는 충분한 열량이 공급되어야 한다(Akner and Cederholm, 2001). 탄수화물의 호흡상수(RQ)는 높아 체내에서 산화 후 더 많은 CO2를 생성하여 CO2 저류를 유발하거나 악화시키고, 호흡곤란과 횡격막 부담을 가중시키므로 COPD 환자의 식이에서는 탄수화물의 에너지 공급 비율을 줄여야 합니다(Anker et al., 2006). 안정기 COPD 환자의 탄수화물 섭취량은 총 에너지의 50~60%를 차지해야 하며, 급성 악화기 환자의 탄수화물 섭취량은 35~50%를 차지해야 하지만 하루 전체 탄수화물 섭취량은 150g 미만이어서는 안 됩니다. 지방의 호흡상수는 매우 낮습니다. 지방 섭취 비율은 적절히 증가시킬 수 있습니다. 안정기 COPD 환자의 지방 공급은 총 에너지의 20%–30%를 차지할 수 있습니다. COPD 환자는 고단백질 분해증을 앓고 있으며, 이는 횡격막 위축의 중요한 요인입니다. 따라서 동화작용 촉진을 위해 고단백 식이를 제공해야 한다. 단백질 공급량은 체중 kg당 1.2~1.5g/일(총 에너지의 15~20%에 해당)로 계산할 수 있다(Schols et al., 2014). 또한 식이에서 충분한 비타민, 미네랄 및 미량 원소도 공급해야 한다.
In order to increase oral nutritional intake, nutritional liquid, semi-solid or powder preparations rich in a variety of macronutrients and micronutrients are added to drinks and foods for oral administration. ONS is often used to supplement intake when food is insufficient to meet the body’s needs. Similarly, ONS can be used as a sole source of nutrition. Sugawara‘s study found that low-intensity exercise therapy with nutritional supplements containing whey peptide can inhibit systemic inflammation, increase muscle strength and improve exercise tolerance in elderly patients with stable COPD (Sugawara et al., 2012). Studies have shown that nutritional supplements such as polyunsaturated fatty acids (PUFAs) and respifor have anti-inflammatory effects and can improve muscle strength and exercise capacity in patients with COPD (Steiner et al., 2003; Broekhuizen et al., 2005). Another study found that L-carnitine could improve exercise tolerance and inspiratory muscle strength in patients with COPD(Borghi-Silva et al., 2006). However, due to the differences in nutritional supplement regimen and effect measurement, more evidence is still needed on the effect of nutritional support therapy in improving diaphragm dysfunction in patients with COPD (Table 1).
경구 영양 섭취량을 증가시키기 위해 다양한 다량영양소와 미량영양소가 풍부한 영양액, 반고형 또는 분말 제제를 음료나 경구 투여 식품에 첨가한다. 음식만으로 신체 요구량을 충족시키기 어려운 경우 ONS(경구영양제)를 보충제로 자주 사용한다. 마찬가지로 ONS는 단독 영양 공급원으로 사용될 수 있습니다. 스가와라(Sugawara)의 연구에 따르면, 유청 펩타이드를 함유한 영양 보충제와 함께 저강도 운동 요법을 병행할 경우 안정된 만성 폐쇄성 폐질환(COPD) 노인 환자의 전신 염증을 억제하고 근력을 증가시키며 운동 내성을 개선할 수 있습니다(Sugawara et al., 2012).
연구에 따르면 다불포화 지방산(PUFAs) 및 레스피포르(RespiFor)와 같은 영양 보충제는 항염증 효과를 가지며, COPD 환자의 근력과 운동 능력을 향상시킬 수 있습니다(Steiner et al., 2003; Broekhuizen et al., 2005).
또 다른 연구에서는 L-카르니틴이 COPD 환자의 운동 내성과 흡기 근력을 개선할 수 있음을 발견하였다(Borghi-Silva et al., 2006). 그러나 영양 보충 요법의 처방 및 효과 측정 방법의 차이로 인해, COPD 환자의 횡격막 기능 장애 개선에 대한 영양 지원 요법의 효과에 대해서는 여전히 더 많은 증거가 필요하다(표 1).
TABLE 1
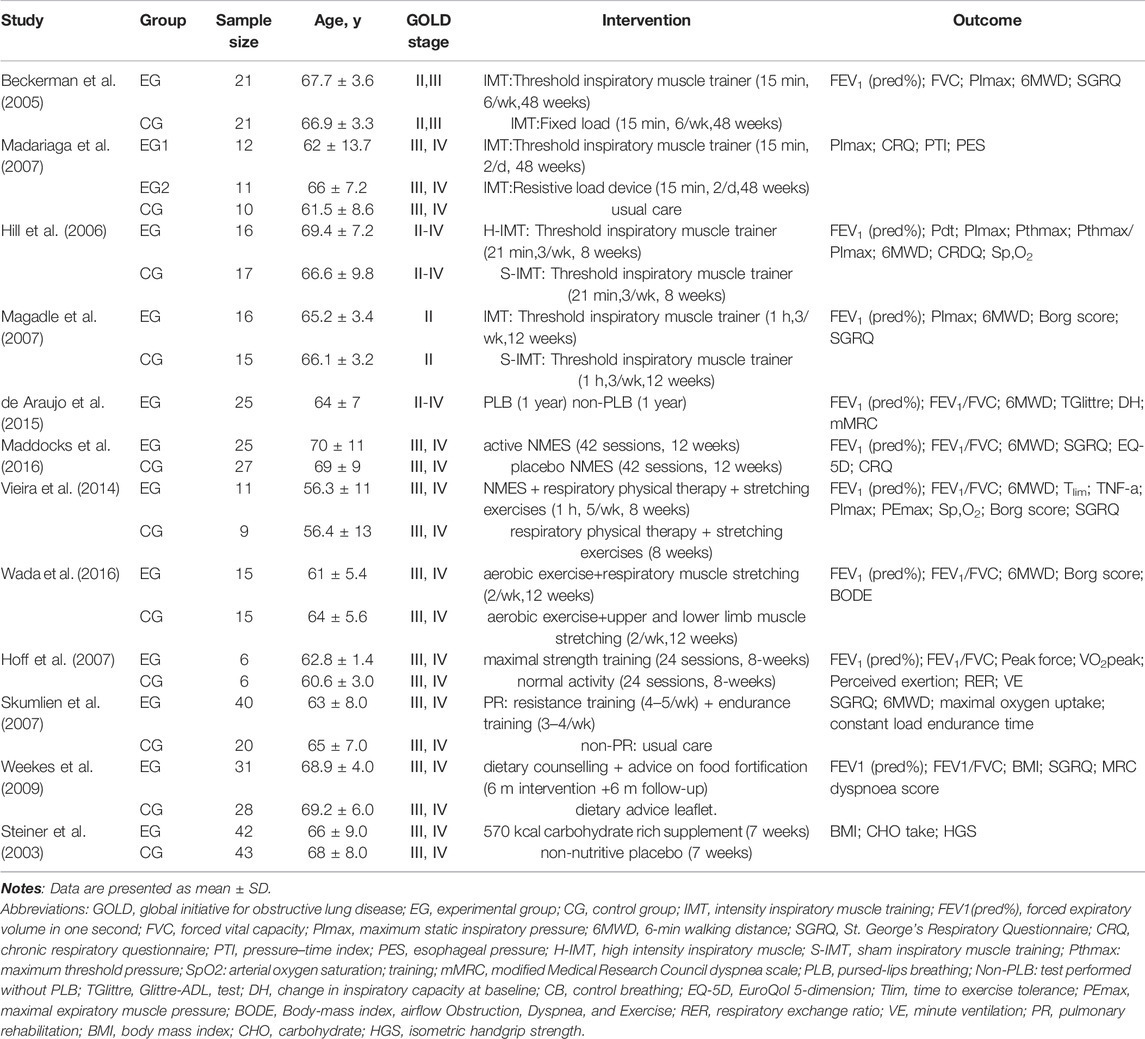
TABLE 1. Characteristics of included studies.
5 Conclusion and Prospect
In summary, COPD combined with diaphragm dysfunction is a common phenomenon that directly affects patients’ respiratory status and quality of life and it is closely related to poor prognosis. In stable patients, diaphragmatic injury and adaptation achieved a special balance (Barreiro and Gea, 2015). However, these positive adaptations are not sufficient to restore normal muscle strength and endurance, resulting in increased susceptibility to fatigue and injury and leading to diaphragm dysfunction. No single factor could not fully explain its occurrence. The mechanism of diaphragmatic muscle dysfunction in patients with COPD is a pathway induced by various pathological factors and mechanisms involved in complex processes. Various factors induce protein breakdown, accelerate cell apoptosis, resulting in the loss of diaphragm muscle fibre, leading to diaphragm dysfunction. Rehabilitation methods, such as IMT, exercise intervention and nutritional support can eliminate the risk factors of diaphragm dysfunction to a certain extent, exercise the diaphragm and respiratory auxiliary muscle group locally and as a whole, improve the overall condition, and have a clear rehabilitation effect on COPD patients with diaphragm dysfunction, which can be used as a reference for clinical treatment of COPD patients with diaphragm dysfunction.
5 결론 및 전망
요약하면, 횡격막 기능 장애를 동반한 COPD는 환자의 호흡 상태와 삶의 질에 직접적인 영향을 미치는 흔한 현상이며, 불량한 예후와 밀접한 관련이 있습니다. 안정된 환자에서는 횡격막 손상과 적응이 특별한 균형을 이루었다(Barreiro and Gea, 2015). 그러나 이러한 긍정적 적응만으로는 정상적인 근력과 지구력을 회복시키기에 충분하지 않아 피로와 손상에 대한 취약성이 증가하고 결국 횡격막 기능 장애로 이어진다. 단일 요인으로는 그 발생을 완전히 설명할 수 없다. COPD 환자의 횡격막 근육 기능 장애 기전은 다양한 병리적 요인과 복잡한 과정에 관여하는 메커니즘에 의해 유발되는 경로이다. 여러 요인이 단백질 분해를 유도하고 세포 사멸을 촉진하여 횡격막 근섬유 손실을 초래함으로써 횡격막 기능 장애를 일으킨다. IMT(근육 강화 운동), 운동 중재 및 영양 지원과 같은 재활 방법은 횡격막 기능 장애의 위험 요인을 어느 정도 제거하고, 횡격막 및 호흡 보조 근육군을 국소적 및 전체적으로 운동시켜 전반적인 상태를 개선하며, 횡격막 기능 장애를 동반한 COPD 환자에게 뚜렷한 재활 효과를 나타내므로, 횡격막 기능 장애를 동반한 COPD 환자의 임상 치료에 참고 자료로 활용될 수 있다.
In the future, diaphragm dysfunction in patients with mild to moderate COPD should be the focus of research. In terms of the structure and function of diaphragm dysfunction, studies to determine the causal relationship between the presence and severity of COPD and changes in diaphragm structure and function are still lacking. On the one hand, the specific mechanism of inflammatory response, oxidative stress, chronic hypoxia and other factors playing a role in diaphragm dysfunction has not been fully clarified and each theory is not sufficient to fully explain the mechanism of diaphragm dysfunction. On the other hand, most of the current research is animal experimental research and clinical research and dynamic observation are lacking. In the study of rehabilitation treatment of diaphragm dysfunction, the rehabilitation treatment methods have not been unified and a complete and systematic pulmonary rehabilitation training prescription has not been formed. Large-scale clinical trials could be carried out in the future to explore the most suitable individualised rehabilitation programme for patients from clinical practice and to form standardised and unified operation and evaluation standards. A longitudinal dynamic follow-up study could be conducted to explore the correlation between the severity of diaphragm dysfunction and different stages of disease to provide a prospective basis for the early discovery of diaphragm dysfunction.
향후 경증에서 중등도 COPD 환자의 횡격막 기능 장애가 연구의 초점이 되어야 합니다. 횡격막 기능 장애의 구조 및 기능 측면에서, COPD의 존재 및 중증도와 횡격막 구조·기능 변화 간의 인과관계를 규명하는 연구는 여전히 부족하다. 한편, 염증 반응, 산화 스트레스, 만성 저산소증 등 횡격막 기능 장애에 관여하는 요인의 구체적 기전은 완전히 규명되지 않았으며, 각 이론만으로는 횡격막 기능 장애의 기전을 충분히 설명하기 어렵다. 다른 한편으로는 현재 연구 대부분이 동물 실험 연구에 그쳐 임상 연구 및 동적 관찰이 부족하다. 횡격막 기능 장애 재활 치료 연구에서는 재활 치료 방법이 통일되지 않았으며 완전하고 체계적인 폐 재활 훈련 처방이 형성되지 않았다. 향후 대규모 임상 시험을 통해 임상 현장에서 환자에게 가장 적합한 맞춤형 재활 프로그램을 탐구하고 표준화된 통일된 운영 및 평가 기준을 수립할 수 있을 것이다. 종단적 동적 추적 관찰 연구를 수행하여 횡격막 기능 장애의 중증도와 질병의 다양한 단계 간의 상관관계를 규명함으로써 횡격막 기능 장애의 조기 발견을 위한 전망적 근거를 마련할 수 있을 것이다.
Author Contributions
WW, XL, and YC contributed to the design of this review. YC, PL, and YW conducted the literature search selection and completed data extraction. YC completed data analysis and wrote the initial draft of the manuscript. PL and YW contributed important intellectual content and put forward suggestions for revision. YC and PL revised the article. WW, XL, and PL supervised the quality of articles. All authors have read and approved the submitted version.
Funding
This review was supported by the National Natural Science Foundation of China (No 82072551, 81902307).
Conflict of Interest
The authors declare that the research was conducted in the absence of any commercial or financial relationships that could be construed as a potential conflict of interest.
Publisher’s Note
All claims expressed in this article are solely those of the authors and do not necessarily represent those of their affiliated organizations, or those of the publisher, the editors and the reviewers. Any product that may be evaluated in this article, or claim that may be made by its manufacturer, is not guaranteed or endorsed by the publisher.
References
Ábrigo J., Elorza A. A., Riedel C. A., Vilos C., Simon F., Cabrera D., et al. (2018). Role of Oxidative Stress as Key Regulator of Muscle Wasting during Cachexia. Oxid. Med. Cell Longev. 2018, 1–17. doi:10.1155/2018/2063179
CrossRef Full Text | Google Scholar
Akner G., Cederholm T. (2001). Treatment of Protein-Energy Malnutrition in Chronic Nonmalignant Disorders. Am. J. Clin. Nutr. 74, 6–24. doi:10.1093/ajcn/74.1.6
PubMed Abstract | CrossRef Full Text | Google Scholar
Anker S. D., John M., Pedersen P. U., Raguso C., Cicoira M., Dardai E., et al. (2006). ESPEN Guidelines on Enteral Nutrition: Cardiology and Pulmonology. Clin. Nutr. 25, 311–318. doi:10.1016/j.clnu.2006.01.017
PubMed Abstract | CrossRef Full Text | Google Scholar
Archiza B., Reinhard P. A., Welch J. F., Sheel A. W. (2021). Sex Differences in Diaphragmatic Fatigue: Effects of Hypoxia during Inspiratory Loading. J. Physiol. 599, 1319–1333. doi:10.1113/JP280704
PubMed Abstract | CrossRef Full Text | Google Scholar
Attaix D., Ventadour S., Codran A., Béchet D., Taillandier D., Combaret L. (2005). The Ubiquitin-Proteasome System and Skeletal Muscle Wasting. Essays Biochem. 41, 173–186. doi:10.1042/bse0410173
PubMed Abstract | CrossRef Full Text | Google Scholar
Barreiro E., Gea J. (2015). Respiratory and Limb Muscle Dysfunction in COPD. COPD J. Chronic Obstructive Pulm. Dis. 12, 413–426. doi:10.3109/15412555.2014.974737
PubMed Abstract | CrossRef Full Text | Google Scholar
Barreiro E., de la Puente B., Minguella J., Corominas J. M., Serrano S., Hussain S. N. A., et al. (2005). Oxidative Stress and Respiratory Muscle Dysfunction in Severe Chronic Obstructive Pulmonary Disease. Am. J. Respir. Crit. Care Med. 171, 1116–1124. doi:10.1164/rccm.200407-887OC
PubMed Abstract | CrossRef Full Text | Google Scholar
Barreiro E., Peinado V. I., Galdiz J. B., Ferrer E., Marin-Corral J., Sánchez F., et al. (2010). Cigarette Smoke-Induced Oxidative Stress: A Role in Chronic Obstructive Pulmonary Disease Skeletal Muscle Dysfunction. Am. J. Respir. Crit. Care Med. 182, 477–488. doi:10.1164/rccm.200908-1220OC