beyond reason

서 론
소포체(endoplasmic reticulum, ER)는 단백질 및 지질 의 합성, 칼슘의 저장, 신호전달 등을 담당하는 중요 세포소 기관이다[1]. 세포는 각자의 주어진 기능을 수행하기 위해 서 단백질을 생산하는데, 이는 환경 변화에 따라 선택적이고 정교하게 조절되어진다. 소포체는 단백질들의 “quality control”을 담당하는 소기관으로서 단백질들은 구조 형성 및 변형을 거친 후 적절한 위치로 운송되어진다. 소포체 내 에 미접힘 단백질이 증가하는 소포체 스트레스(ER stress) 는 단백질의 항상성 네트워크를 변화시키는 다양한 원인에 의해 발생한다. 최근 퇴행성 신경질환, 암, 대사질환, 염증성 질환 등에서 만성적인 소포체 스트레스가 발생하고 있고, 이는 질병들의 주요 병리기작과 관련이 있다는 많은 연구가 보고되고 있다. 그래서 소포체 스트레스의 신호전달 기작인 미접힘 단백질 반응(unfolded protein response, UPR)의 조절에 대한 연구의 증가와 더불어 이를 타깃으로 하여 치료 방법 을 개발하려는 시도가 다양하게 이뤄지고 있다. 이 글을 통해 소포체 스트레스의 감지부터 하위 신호 전달을 통한 세 포의 기능 조절에 이르는 UPR의 분자적 기작에 대해 분석하고, 이 중 가장 잘 연구되어있는 IRE1/XBP1의 다양한 생물학적 기능에 대해 알아보고자 한다.
소포체 스트레스와 미접힘 단백질 반응
소포체는 콜레스테롤, 지방산과 같은 지질의 합성과 더불어 칼슘의 저장 및 신호 전달에 중요한 역할을 한다(그림1). 또한 소포체는 단백질의 합성과 접힘을 담당하는 중요한 세 포소기관으로서 단백질의 기능에 필수적인 다양한 번역 후 변형(post-translational modification)을 수행한다[1]. 소포체내로 들어온 신생 단백질은 폴데이즈(foldase), 샤페론 (chaperone) 및 보조인자들로 이루어진 복잡한 네트워크에 의해 접힘이 일어나고 당화과정(glycosylation) 같은 변형을 통해 기능을 할 수 있는 3차구조를 만든다[2]. 이처럼 소포체에서 “quality control” 과정을 통과한 단백질은 다양 한 세포소기관 및 세포막 또는 외부로 이동을 하게 된다[3].
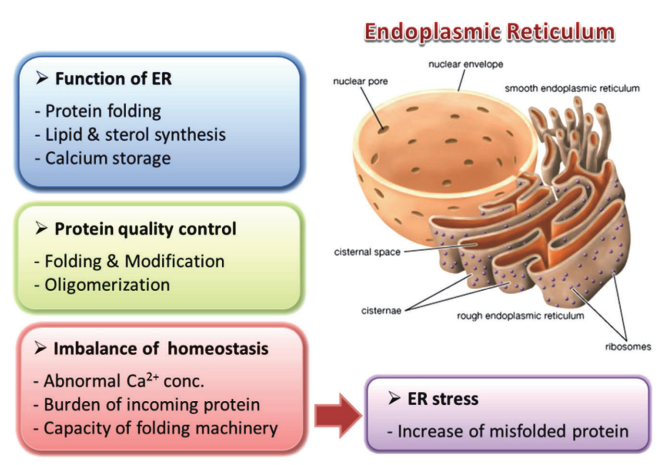
소포체내에 단백질이 급격하게 유입되어 소포체의 단백질 접힘 능력의 한계를 벗어나거나 또는 다양한 생리학적•병리학적 원인에 의해 소포체 내의 항상성이 무너지게 되면 단백질 접힘 과정에 문제가 발생하여 잘못 접힘(misfolding) 또는 미접힘(unfolding) 단백질이 증가하는 소포체 스트레스를 발생시킨다(그림1)[4, 5]. 이러한 원인에는 단백질 합성의 과도한 증가, 단백질 성숙의 방해, 샤페론 분자의 기능 저하, 질병 관련 이상 단백질의 과발현, 소포체내 칼슘 농도 감소, 산화 스트레스, 바이러스 감염 등이 있다(그림2).
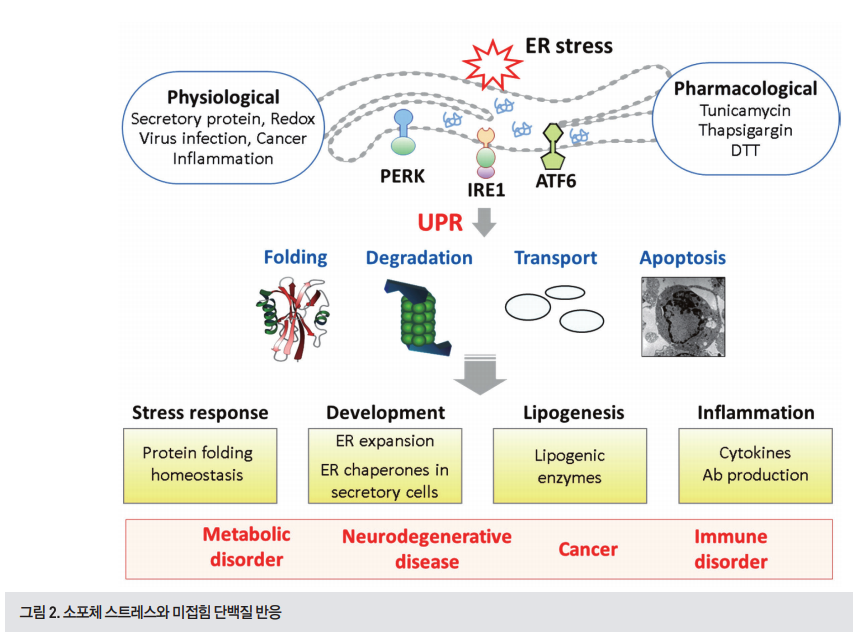
실험적으로는 당화과정을 억제하는 Tunicamycin, 소포체내 칼슘을 결핍시키는 Thapsigargin, 이황화결합을 억제하는 DTT와 같은 시약의 처리를 통해 소포체 스트레스를 유도할 수 있다. 세포는 이러한 소포체 스트레스를 해결하기 위한 일련의 과정을 활성화시키는데, 이를 미접힘 단백질 반응(UPR)이 라고 한다(그림2)[4, 5]. UPR은 복잡한 신호전달 시스템으로
1)소포체의 단백질 접힘 능력을 증가시키는 동시에
2)단백질의 유입을 줄이거나
3)미접힘 단백질을 분해하여 스트레스를 감소시킨다.
그러나 이러한 기작으로도 소포체의 항상성을 회복하기에 부족하다면
4)세포는 apoptosis를 일으켜 죽음에 이른다.
UPR을 통해 스트레스 반응, 세포의 발달 및 분화, 지질생합성, 염증반응 등 다양한 측면의 생물학적 기능이 조절된다는 것이 보고되었다. 이러한 결과들은 다양한 질환에서 소포체 스트레스가 중요한 신호 네트워크로 작용할 가능성을 보여주고 있다. 소포체 스트레스는 B세포, 췌장의 베타세포(β-cell), 침샘의 샘꽈리세포(acinar cell)와 같은 전문화된 분비 세포의 기능에 필수적인 것으로 알려져 있다. 분비 세포의 발달과 분화에 따라 요구되는 단백질 합성과 분비 능력의 증가는 적절한 수준의 소포체 스트레스를 발생시키고, 이는 UPR을 통한 단백질 항상성 유지에 중요한 역할을 한다.
UPR의 신호전달 기작
일반적으로 진핵생물의 UPR은 소포체 막에 위치하여 소포체 스트레스를 감지하는 센서 단백질인 IRE1α/β (inositol-requiring endonuclease), PERK(PKR-like ER kinase), ATF6α/β(activating transcription factor 6)에 의해 매개된다(그림3)[5, 6].
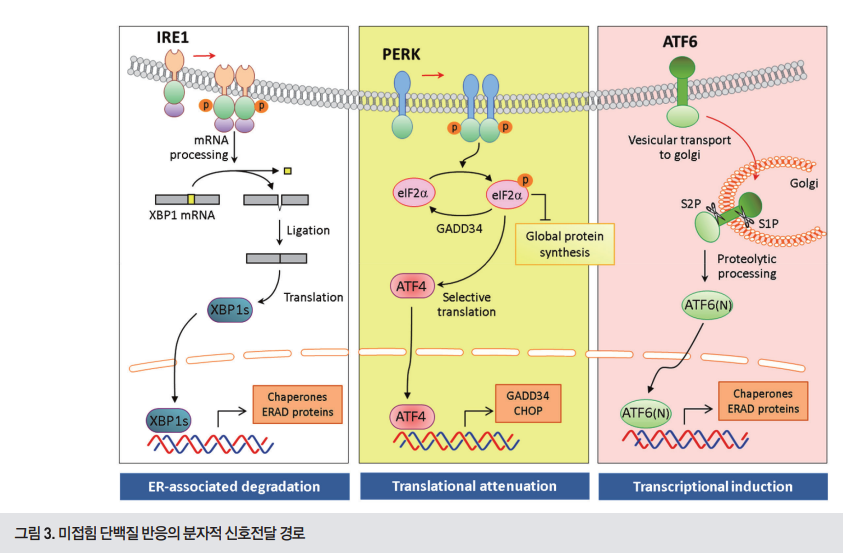
UPR의 기능은
1)전사 증가를 통한 소포체 기능과 관련된 유전자 발현,
2)단백질 번역 억제를 통한 새로운 단백질의 합성 중단,
3)ERAD를 통한 미접힘 단백질들을 분해시키는 과정으로 분류할 수 있다.
3개의 스트레스 센서 단백질은 각각의 특정 신호 전 달 경로와 하위 전사 인자들의 활성화를 통해 단백질 항상성 조절과 관련된 다양한 유전자들의 발현을 조절하여 소포체 스트레스에 대한 반응을 나타낸다. 여러 유전자 분석 연구들은 UPR에 의해 주로 소포체 안으로의 단백질 이동, 접힘, 당화과정, 단백질 분해, 지질 생합성, 소포 수송, 산화환원 대사과정 등과 관련된 유전자들이 조절된다는 것을 규명하였다.
그러나 각 신호 기작의 타깃 유전자들은 세포 종류 및 소포체 스트레스가 발생하는 외부 환경 요건에 따라 다를 것으로 예상되므로, 각 UPR의 센서 단백질이나 전사 인자들이 결핍된 생쥐나 세포를 이용한 체계적인 분석이 필요하다.
1. IRE1/XBP1
IRE1/XBP1은 진핵생물 사이에서 가장 잘 보존된 UPR 신호 기작으로 IRE1은 Ser/Thr protein kinase와 endoribonuclease의 기능을 가지고 있다(그림3)[5, 6]. 소포체 내 미접힘 단백질의 증가로 IRE1α가 자가인산화되어 활성화되면 XBP1(X-box binding protein 1) mRNA의 2차구조를 인식한 IRE1α에 의해 splicing이 세포질에서 일어난다. IRE1α는 XBP1 mRNA에서 26bp 크기의 인트론을 제거하는데, 이는 ORF(open reading frame)에 변화를 주어 새로운 C-말단을 가지는 XBP1s라는 단백질을 발현시킨다. XBP1s는 bZIP domain을 가진 전사인자로서 단백질의 접 힘을 증가시키는 샤페론 분자들과 더불어 미접힘 단백질을 분해하는 ERAD(ER-associated degradation)와 관련된 유전자들의 전사를 증가시킨다[7]. 이외에도 인지질 생합성 과 관련된 효소들의 전사를 증가시켜 소포체와 골지체 등의 생성에도 중요한 역할을 한다[8].
2. PERK
PERK는 type I transmembrane protein kinase로서 소포체 스트레스 증가 시 자가인산화를 통해 활성화되고 eIF2α(eukaryotic initiation factor 2 alpha subunit) 의 51번 serine을 인산화시켜 일반적인 단백질 번역 과정을 저해(translational attenuation)한다(그림3)[5, 6]. eIF2α의 인산화는 GDP-GTP 교 환을 도와주는 eIF2B의 활성을 억제하여 단백질 번역 시작 에 중요한 복합체의 형성을 방해하고, 이를 통해 소포체 내 로 들어오는 미접힘 단백질의 양을 줄여준다. 이와는 반대로 5′ UTR(untranslated region) 지역에 여러 개의 ORF 를 가지고 있어 평상 시 번역이 억제되었던 유전자인 ATF4 는 eIF2α 인산화에 의해 단백질로의 번역이 증가한다. 전사 인자인 ATF4는 타깃 유전자인 GADD34의 전사를 증가시 켜 PP1(protein phosphatase 1)과 함께 eIF2α의 탈인산화를 유도하여 중단된 단백질 번역이 다시 재개되도록 한다. 또한 ATF4는 CHOP의 전사도 증가시켜 apoptosis를 유도하기도 한다[9].
3. ATF6
ATF6는 소포체막에 존재하는 type II transmembrane 단백질로서 소포체 스트레스 증가에 의해 골지체로 이동한 뒤 S1P(site 1 protease)와 S2P(site 2 protease)에 의해 절단된다(그림3)[5, 10]. 이런 단백질 가공과정을 거쳐 세포질 쪽에 위치한 N-말단이 분리되어 bZIP 도메인을 가진 전사 인자 ATF6(N)이 생성된다. 핵 안으로 이동한 ATF6(N)는 XBP1s와 비슷하게 샤페론 분자 및 ERAD와 관련된 유전자들의 전사를 증가시킨다[11]. -> protein folding ability증가시킴.
IRE1/XBP1에 의한 유전자 조절
1. XBP1s의 타깃 유전자 전사 조절
XBP1s는 프로모터 부근에 존재하는 ESRE(ER stress responsive element)에 결합하며, 주로 단백질의 접힘, ERAD에 관련된 유전자들의 전사를 조절한다[6, 12]. 또한 XBP1s는 인지질 합성과 관련된 유전자들의 전사를 유도하 여 소포체의 확장 및 크기를 조절하는 것으로 알려져있다. 지금까지 밝혀진 XBP1s의 타깃 유전자들을 살펴보면 소포 체내 단백질 이동을 조절하는 유전자(Sec61, Derl1), 단백 질 접힘을 조절하는 샤페론 분자(ERdj3, ERdj4, p58IPK , Grp78, Grp94, PDI), ERAD련 유전자 (EDEM, Herp, Hrd1, Mannosidase I), 당화과정과 관련된 RAMP4 등이 있다(그림5)[7, 13]. 유전자 발현 양상 분석을 보면 XBP1s 의 타깃 유전자들이 세포 종류와 스트레스 자극에 따라 다 양할 것으로 예상되고 있다. 최근에는 DNA 손상 및 복구와 관련된 유전자를 포함하여 질병과 밀접히 관련된 XBP1s 타 깃 유전자들을 찾아내기 위해 노력 중이다. 다른 전사인자와의 상호작용을 통해서 세포 특이적인 유전자 조절이 가능 하므로, XBP1의 파트너를 찾는 연구도 활발히 진행 중이다.
2. RIDD (Regulated IRE1-depanednt decay)
IRE1은 소포체 막에 위치하는 단백질로, luminal, transmembrane, cytosolic 부분으로 구성되어있다. 소포체 스트레스에 의해 세포질에 위치한 IRE1의 kinase, endoribonuclease의 기능이 활성화되면 XBP1 mRNA에 있는 2개의 stem-loop 구조와 5’-CUGCAG-3’라는 특정 시퀀스를 인식하여 splicing을 일으킨다(그림4).
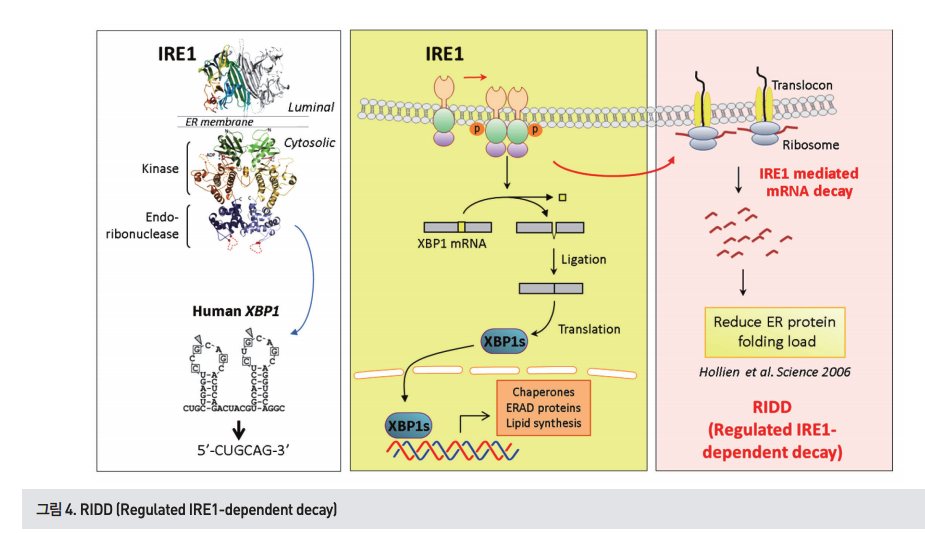
2006년 초파리를 이용한 연구에서, XBP1에 추가하여 IRE1이 다양한 mRNA를 타깃 유전자로 인식한 후 RNase 활성을 이용하여 분해하는 것을 발견하였는데, 이러한 과정을 “Regulated IRE1-dependent decay(RIDD)”라고 한다[14, 15]. 소포체 스트레스 상황에서 소포체로 유입되는 단백질을 암호화하 는 유전자를 IRE1이 분해하는데, 이를 통해 미접힘 단백질의 부담을 완화하려는 방법으로 생각되어졌다. 이후 여러 연구들을 통해서 IRE1 타깃 유전자들을 분석한 결과 XBP1 과 비슷한 stem-loop 2차 구조와 5’-CUGCAG-3’ 시퀀스 를 가지고 있음이 밝혀졌다[16]. 최근 연구에 따르면 이러한 IRE1 타깃 유전자 역시 조직이나 세포마나 다르며, RIDD 의 생리학적 기능이 다양한 질병 모델을 이용해서 밝혀지고 있다.
IRE1/XBP1의 생리학적 기능
유전학적으로 변형시킨 생쥐를 이용하여 다양한 생리학 적 과정 및 질병에서 IRE1/XBP1 신호전달의 근본적인 기능들을 분석할 수 있게 되었다. XBP1은 다양한 조직에서 분비 세포들의 기능 조절에 주요한 역할을 담당하고 있으며, 이 외에도 지질대사, 글루코스 항상성, 염증성 반응 등에도 참여한다. 특히, 간 또는 장에서 XBP1이 결핍된 생쥐의 경우, IRE1α이 과활성화되어 RNase activity가 증가하는데, 이는 RIDD의 생리학적 기능을 분석할 수 있는 좋은 동물모델로 생각된다.
1. 분비 세포의 기능과 분화 조절
여러 분비 세포의 기능 및 분화에서 XBP1의 중요성은 기존에 알려진 소포체 및 골지체의 생성과 인지질 합성을 조절하는 XBP1의 기능에서 충분히 예측할 수가 있다 (그림5).
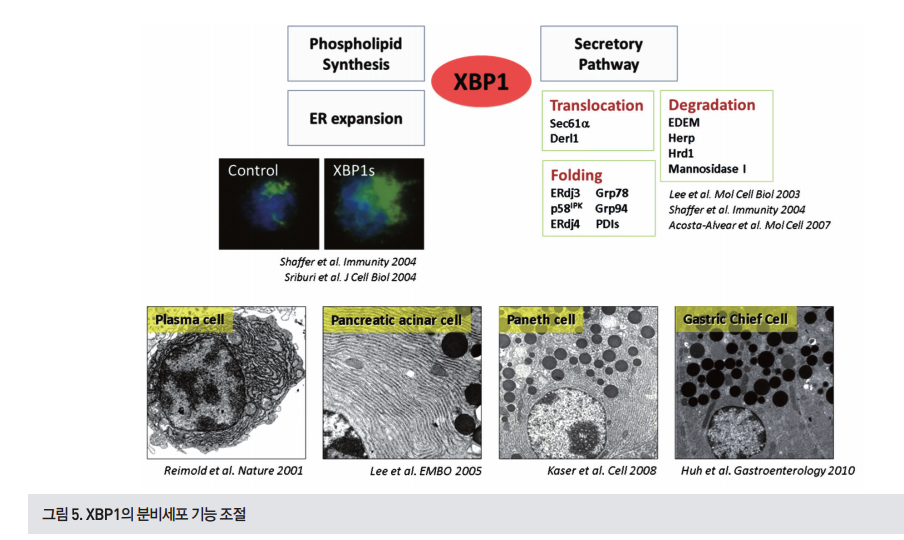
분비 세포에서 XBP1의 중요성은 14년전 XBP1이 결핍된 B 세포가 항체를 생산하는 플라즈마세포로 분화를 할 수 없다는 결과로 확인되었다[17]. B세포에서 XBP1s의 발현의 유도는 소포체, 리소좀, 미토콘드리아와 같은 세포 소기관 및 세포의 크기를 증가시키고 단백질 분비와 관련된 유전자들 의 전사를 증가시켰다[13]. XBP1 결핍시 침샘의 샘꽈리세 포, 췌장의 베타세포, 소장의 파네스세포(Paneth cell), 위 의 주세포(zymogenic cell)에서 분비 기능 및 세포 구조 의 이상이 확인되었으며, 위 연구들을 통해 분비세포에서 XBP1의 중요성을 다시 확인할 수 있었다[18-20]. 소장에서 박테리아 항원에 노출 시 파네스세포는 항박테 리아 기능의 펩타이드를 생산하여 방어막을 구축한다. 그러 나 소장 상피세포에서 XBP1이 결핍되면 파네스세포의 이상 으로 항박테리아 펩타이드 생산이 감소하고 장염이 발생하 게된다[18, 21]. 마찬가지로 IRE1α의 결핍 역시 췌장과 침 샘 조직의 구조적 이상을 보이는 동시에 혈청내의 항체 생 산을 억제하였다[22]. 최근 XBP1이 알러지 반응에 관여하 는 호산구(eosinophil)의 분화에도 필수적이라는 결과가 보 고되었으며, XBP1 결핍 시 생존에 필요한 주요 과립 단백질 들의 번역 후 변형 과정에 문제가 발생해 호산구 발달과 관 련된 전사 프로그램이 억제되었다[23].
2. 지질대사
XBP1은 비전문 분비세포들의 기능과 항상성 조절에도 중요하며, 특히 간에서 XBP1의 발현은 정상적인 지질의 합성에 필수적이다(그림6)[24, 25]. 고탄수화물 식이는 간에서 XBP1을 활성화하여 주요 지질합성 관련 유전자의 전사 를 증가시킨다. 그러나 간에서 XBP1의 결핍은 혈액 내의 트 리글리세리드, 콜레스테롤, 지방산의 양을 현저하게 낮추었다. 이는 간에서 XBP1이 직접적으로 Dgat2, Scd1, Acc2와 같은 지질합성 관련 유전자들의 전사를 조절하면서 나타나는 결과이다.
3. 면역반응
분비세포와 지질대사 이외에, XBP1은 선천성 면역반응 조절에도 관여한다고 알려져있다. XBP1은 수지상세포(dendritic cell)의 발달과 생존에 중요하며, 대식세포 (macrophage)에서는 TLR(toll-like receptor)을 통해 인 식되는 병원체에 대한 면역반응을 조절한다[26, 27]. 대식 세포에서 TLR4/TLR2에 의한 병원체 인식은 IRE1α-XBP1 경로를 활성화시켜 염증성 사이토카인의 발현을 증가시켰 다. 그러나 이러한 IRE1α 신호 경로의 자극은 소포체 스트 레스 관련 유전자들의 전사는 증가시키지 못했다. TLR2를 활성화시키는 병원체인 Francisella tularensis를 XBP1 결 핍 생쥐에게 감염시킨 경우 면역반응이 줄어들어 박테리아 를 효과적으로 제거하지 못했다. 이와는 반대로, 최근 XBP1이 수지상세포에서 암에 대한 면역 반응을 억제하는 것으로 보고되었다[28]. 암세포 주변 의 수지상세포에서 XBP1이 활성화되면 트리글리세리드의 합성을 증가시키고, 이러한 지질의 축적은 암에 대한 T세포 의 면역 반응을 돕는 수지상세포의 기능을 억제하였다. 수 지상세포 특이적으로 XBP1 결핍시 면역반응을 증가시켜 암 세포의 성장을 효과적으로 막아주었다.
4. IRE1 – RIDD의 생리학적 기능
최근 IRE1의 RIDD 기능이 지질 합성, 간독성, 인슐린 생 성 등을 조절한다는 것이 밝혀졌다[29, 30]. 간에서 XBP1 을 결핍 시킨 경우 지질 합성과 관련된 유전자들의 전사가 억제되어 혈액내의 트리글리세리드와 콜레스테롤과 같은 지질의 양이 현저하게 줄어든다. 이는 XBP1 결핍 시 활성 화된 IRE1이 간에서 리파아제를 억제하는 Angptl3 유전자 및 지질 합성 관련 유전자들을 분해하여 나타나는 결과이다 (그림6)[31].
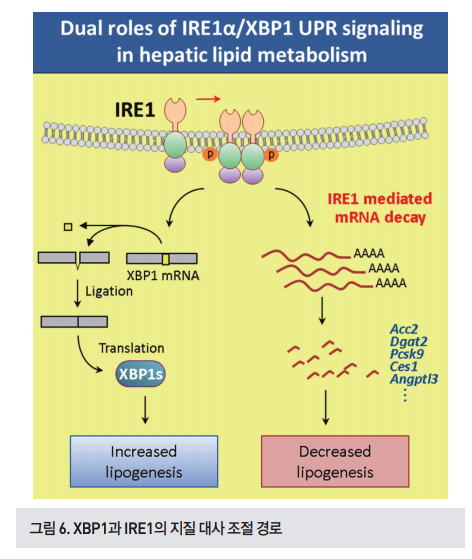
정상 생쥐에게 고농도의 아세트아미노펜을 투 여하면 간독성에 의해 ALT가 급격히 증가하지만, XBP1 결 핍 생쥐는 ALT가 거의 증가하지 않는다[32]. 이는 아세트 아미노펜을 독성 대사체로 전환하는 Cyp1a2, Cyp2e1의 효 소를 암호화하는 유전자들이 활성화된 IRE1에 의해 분해되 기 때문이다. 췌장의 베타세포에 고농도의 글루코스를 처리 하면 소포체 스트레스가 일어나고 활성화된 IRE1에 의해 인 슐린 mRNA가 분해된다[33, 34]. 이외에도 활성화된 IRE1 은 eIF2α 탈인산화효소 조절자인 CReP/Ppp1r15b 유전자 를 분해하여 소포체 스트레스 발생 시 PERK에 의한 eIF2α 인산화를 도와주어 단백질 번역을 억제한다[35]. 이외에도 RIDD는 세포의 apoptosis 유도, pre-miRNA의 분해, 소 포체 항상성 유지 등을 통해 다양한 생리학적 기능을 가질 것으로 예상되며, 이들이 다양한 질병과 관련하여 어떠한 조절 능력을 가지는지 체계적인 분석이 필요하다[36].
맺음말
미국에서 가장 권위있는 의학상인 “라스커상”의 2014년 수상자로 소포체 스트레스를 연구한 미국의 피터 월터 교수 와 일본의 모리 가즈토시 교수가 선정됐다. 약 20년정도 연구가 진행되었지만 아직까지 풀지 못한 수많은 과제들이 남아있다. 각각의 질병, 세포 및 환경에서 발생하는 소포체 스트레스의 원인을 포함하여 UPR 기작 중 어떠한 신호전달 기작이 일어나는지, 각각의 신호 강도는 어느 정도인지, 또한 타깃 유전자들은 어떤 것들이 있는지 등의 깊이있는 의 문점들을 풀어야할 시점이다. 이처럼 소포체 스트레스는 많 은 의생명 과학자들의 관심을 받고 있는 분야이며 암, 대사질환, 염증성 질환 등 각종 질병에 관여할 것으로 예상되고 있어, 이를 타깃으로 신약 개발을 위한 연구가 활발하게 진행 중이다.