
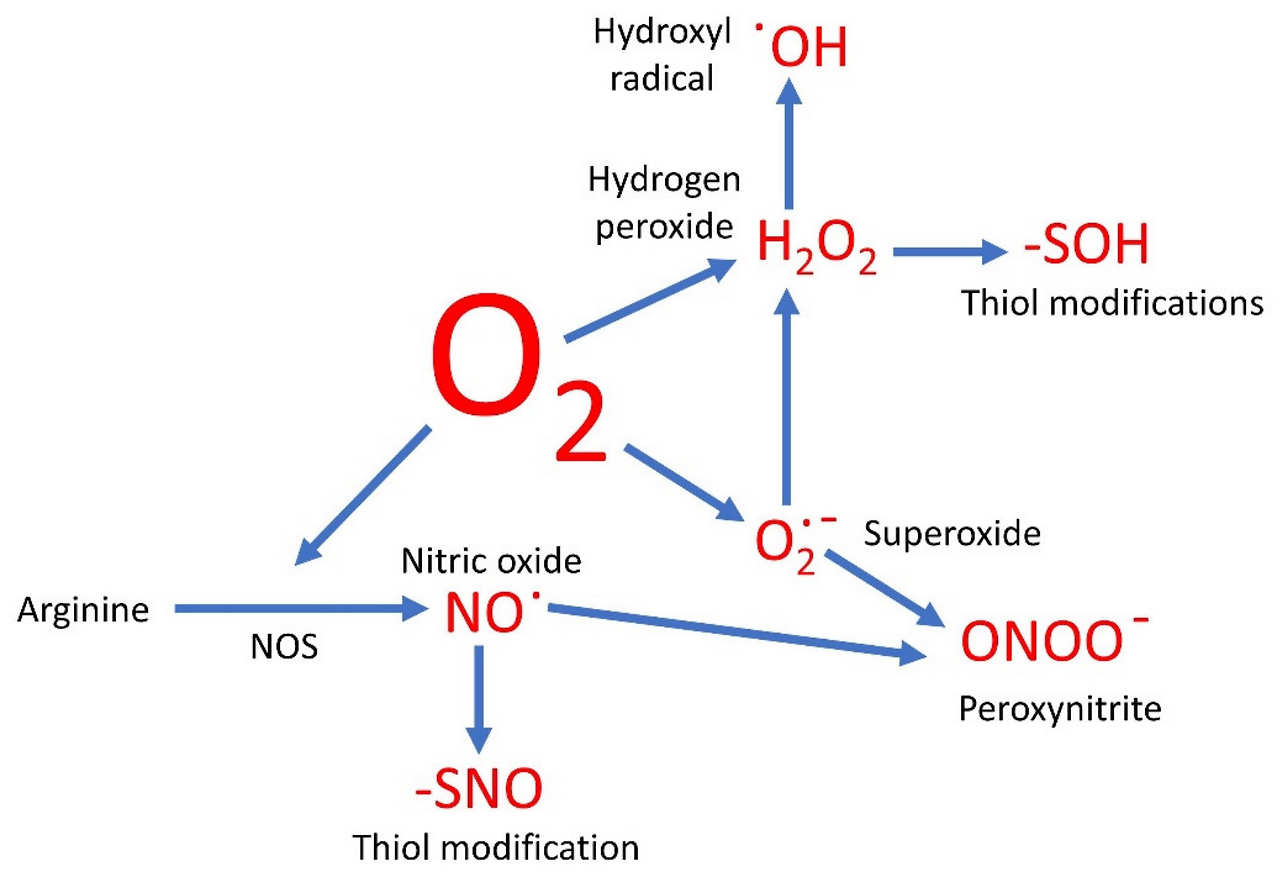
H2O2+NO --> Hydroxyl radical
NO + O2 --> NO2- AND Peroxynitrite

Open AccessFeature PaperReview
Free Radical Properties, Source and Targets, Antioxidant Consumption and Health
by
Giovanni Martemucci
1,
Ciro Costagliola
2

,
Michele Mariano
3
and
Angela Gabriella D’Alessandro
1
1
Department of Agricultural and Environmental Sciences, University of Bari Aldo Moro, Via G. Amendola, 70126 Bari, Italy
2
Department of Neurosciences, Reproductive Sciences and Dentistry, University of Naples Federico II, 80131 Naples, Italy
3
Unità Operativa Complessa di Radiodiagnostica Universitaria—Policlinico di Bari, 70122 Bari, Italy
4
Department of Medicine and Health Sciences “Vincenzo Tiberio”, Università del Molise, 86100 Campobasso, Italy
*
Author to whom correspondence should be addressed.
Oxygen 2022, 2(2), 48-78; https://doi.org/10.3390/oxygen2020006
Submission received: 27 February 2022 / Revised: 3 April 2022 / Accepted: 6 April 2022 / Published: 12 April 2022
(This article belongs to the Special Issue Feature Papers in Oxygen)
Downloadkeyboard_arrow_down
Abstract
Free radicals have acquired growing importance in the fields of biology and medicine. They are produced during many different endogenous and exogenous processes. Mitochondria are the main source of endogenous reactive oxygen species (ROS) produced at cell level. The overproduction of free radicals can damage macromolecules such as nucleic acids, proteins and lipids. This leads to tissue damage in various chronic and degenerative diseases. Antioxidants play a crucial role in the body’s defense against free radicals. This review concerns the main properties of free radicals, their sources and deleterious effects. It highlights the potential role of the dietary supplementation of antioxidants and discusses unsolved problems regarding antioxidant supplements in the prevention and therapy of diseases.
초록
자유 라디칼은
생물학 및 의학 분야에서 점점 더 중요해지고 있다.
이들은 다양한 내인성 및 외인성 과정에서 생성된다.
미토콘드리아는
세포 수준에서 생성되는 내인성 활성산소종(ROS)의 주요 공급원이다.
자유 라디칼의 과잉 생산은
핵산, 단백질, 지질과 같은 거대분자를 손상시킬 수 있다.
이는 다양한 만성 및 퇴행성 질환에서 조직 손상으로 이어진다.
항산화제는
체내에서 자유 라디칼에 대항하는 방어 체계에서 핵심적인 역할을 수행한다.
본 리뷰는
자유 라디칼의 주요 특성, 발생 원천 및 유해한 영향에 대해 다루며,
항산화제 식이 보충제의 잠재적 역할에 주목하고
질병 예방 및 치료 측면에서 항산화제 보충제와 관련된 미해결 문제들을 논의한다.
Keywords:
free radicals; reactive oxygen species; reactive nitrogen species; molecular targets; physiopathology; antioxidant supplementation
1. Introduction
In recent years, there has been growing interest in the prevention of disease, with particular reference to the role of free radicals. The biology and medicine of free radicals are expanding rapidly because they are profoundly relevant to health and disease and, therefore, quality of life. Free radicals were discovered more than a century ago, when it seemed that all oxidation reactions involving organic molecules were mediated by free radicals [1]. In the 1950s, free radicals were detected in biological systems and were proposed to be involved in human diseases [2]. In 1969, McCord and Fridovich [3] discovered the enzyme superoxide dismutase (SOD), demonstrating that living organisms have protective systems. This finding was sustained by subsequent discoveries of other antioxidant enzymes and antioxidant protein metabolites. It became clear that the deleterious effects of free radicals can be controlled by specific antioxidant systems. Most research on free radicals concerns oxygen radicals, which, together with some forms of active non-radical oxygen, are collectively called reactive oxygen species (ROS). In 1971, it was discovered [4] that reactive oxygen species are generated in cell metabolic respiration; later, Halliwell and Gutteridge [5] reported that ROS included free radical and non-radical derivatives of oxygen. In the 1980s, free radical nitric oxide (•NO) was identified in blood vessels and gave rise to studies on the biochemistry of reactive nitrogen species (RNS) [6]. More recently, it has been found that free radicals also play a positive biological role; ROS and reactive nitrogen species (RNS) operate in concert with reactive halogen species as part of the cell immune response to infection by microorganisms [7]. The signaling functions of ROS and RNS are the latest major biological discovery on free radicals [8].
Here, we provide an overview of the properties, generation and molecular targets of free radicals and their implications in diseases. The potential role of antioxidant supplementation for health maintenance is also discussed.
1. 서론
최근 몇 년간 질병 예방,
특히 자유 라디칼의 역할에 대한 관심이 증가하고 있다.
자유 라디칼의 생물학과 의학은
건강과 질병, 그리고 삶의 질과 깊이 관련되어 있기 때문에 급속히 확장되고 있다.
자유 라디칼은
1세기 이상 전에 발견되었으며,
당시에는 유기 분자를 포함한 모든 산화 반응이 자유 라디칼에 의해 매개되는 것으로 여겨졌다 [1].
1950년대에는 생물학적 시스템에서 자유 라디칼이 검출되었으며,
인간 질병에 관여한다는 제안이 제기되었다[2].
1969년 McCord와 Fridovich[3]는
슈퍼옥사이드 디스뮤타제(SOD) 효소를 발견하여
생물체가 보호 시스템을 갖추고 있음을 입증했다.
이 발견은 이후
다른 항산화 효소와 항산화 단백질 대사 산물의 발견으로 뒷받침되었다.
자유 라디칼의 유해한 영향이
특정 항산화 시스템에 의해 제어될 수 있음이 분명해졌다.
자유 라디칼에 대한 대부분의 연구는
산소 라디칼을 다루며,
이는 일부 활성 비라디칼 산소 형태와 함께 반응성 산소 종(ROS)으로 통칭된다.
1971년,
반응성 산소 종이 세포 대사 호흡 과정에서 생성된다는 사실이
발견되었다[4];
이후 할리웰과 거터리지[5]는
ROS가 산소의 자유 라디칼 및 비라디칼 유도체를 포함한다고 보고했다.
1980년대에는
혈관에서 자유 라디칼 산화질소(•NO)가 확인되어
반응성 질소종(RNS)의 생화학 연구가 시작되었다[6].
최근에는
자유 라디칼이 긍정적인 생물학적 역할도 한다는 사실이
밝혀졌다;
ROS와 반응성 질소 종(RNS)은
미생물 감염에 대한 세포 면역 반응의 일환으로
반응성 할로겐 종과 함께 작용한다[7].
ROS와 RNS의 신호 전달 기능은
자유 라디칼에 관한 최신 주요 생물학적 발견이다[8].
본고에서는
자유 라디칼의 특성, 생성, 분자 표적 및 질병에서의 의미를 개괄한다.
건강 유지에 대한 항산화제 보충제의
잠재적 역할도 논의한다.
2. Free Radicals
In the history of the Earth, the evolutionary selection of oxygen has depended on its ready availability, high energy of oxidation, easy distribution and solubility in biocomponents. However, there are negative aspects, since breathing pure oxygen (100% O2, 1 atm) instead of air (20% O2, 1 atm) is harmful to living organisms. Oxygen is essential for the life of aerobic organisms. The ability to use oxygen has enabled humans and animals to metabolize fats, proteins and carbohydrates to produce energy, albeit not without a cost since, paradoxically, the use of oxygen contributes to human aging and illness. Free radicals are products of normal cell metabolism. When cells use oxygen, the redox process generates free radicals, normally ROS and RNS [9].
Free radicals can be defined as molecular entities or molecular fragments, capable of independent existence (hence “free”). They contain one or more unpaired electrons in an outer atomic orbital or molecular orbital (hence “radical”) [10]. The negative electrical charge of electron(s) may be counterbalanced by the positive nuclear charge of positrons, resulting in a neutral particle; otherwise, we have anion or cation radicals. The unpaired electron of a free radical is denoted by a point on the atom or group in which it predominantly resides, for example •H (hydrogen atom), •OH (hydroxyl), •CH3 (methyl) and •CH2CH3 (ethyl). In oxygen radicals, the unpaired electron is located predominantly on an oxygen atom, e.g., superoxide (O2•−), hydroxyl (•OH), peroxyl (ROO•). The odd number of electron(s) of a free radical makes it unstable, short-lived and highly reactive. This characteristic is responsible for chain reactions. Free radicals attempt to bond with other molecules, atoms or even individual electrons to create a stable compound. They either donate or accept an electron from other molecules, acting as oxidizing or reducing agents [10].
2. 자유 라디칼
지구 역사에서 산소의 진화적 선택은
그 가용성, 높은 산화 에너지, 생체 구성 요소 내 용이한 분포 및 용해성에 의존해 왔다.
그러나
공기(20% O2, 1 atm) 대신 순수 산소를 호흡하는 것은 생물체에 해롭다.
산소는
호기성 생물의 생명에 필수적이다.
산소 이용 능력은
인간과 동물이 지방, 단백질, 탄수화물을 대사하여 에너지를 생산할 수 있게 했으나,
역설적으로 산소 이용이 인간의 노화와 질병에 기여한다는 점에서
대가를 치르지 않은 것은 아니다.
자유 라디칼은
정상적인 세포 대사의 부산물이다.
세포가 산소를 이용할 때
산화환원 과정은 자유 라디칼,
일반적으로 ROS(반응성 산소 종) 및 RNS(반응성 질소 종)를 생성한다 [9].
자유 라디칼은
독립적으로 존재할 수 있는 분자 실체 또는
분자 단편으로 정의될 수 있습니다(따라서 “자유”).
이들은
외부 원자 궤도 또는 분자 궤도에
하나 이상의 짝을 이루지 않은 전자를 포함합니다(따라서 “라디칼”) [10].
전자의 음전하가 양전자를 통해 핵의 양전하와 상쇄될 경우 중성 입자가 되며,
그렇지 않으면 음이온 또는 양이온 라디칼이 생성됩니다.
자유 라디칼의 짝을 이루지 않은 전자는
주로 존재하는 원자나 그룹 위에 점(•)으로 표시됩니다.
예를 들어
•H(수소 원자), •OH (하이드록실), •CH3 (메틸), •CH2CH3 (에틸) 등이 있습니다.
산소 라디칼의 경우,
불쌍 전자들은 주로 산소 원자에 위치합니다.
예를 들어,
슈퍼옥사이드(O2•−), 하이드록실(•OH), 페록실(ROO•) 등이 있습니다.
자유 라디칼의 홀수 전자 수는 이를 불안정하고
수명이 짧으며 반응성이 매우 높게 만듭니다.
이 특성은 연쇄 반응의 원인이 됩니다.
자유 라디칼은
안정된 화합물을 생성하기 위해
다른 분자, 원자 또는 심지어 개별 전자와 결합하려 합니다.
그들은 다른 분자로부터 전자를 기증하거나 수락함으로써
산화제 또는 환원제로 작용합니다 [10].
Reactive oxygen and nitrogen species may be radicals or non-radical compounds [11,12] (Table 1). Reactive oxygen species include the three chemical species of the Fenton/Haber-Weiss pathway (O2•− superoxide radical, H2O2 hydrogen peroxide and HO• hydroxyl radical), products of the partial reduction of oxygen. Four-electron reduction of molecular oxygen leads to the formation of water without the generation of ROS, whereas one-electron reduction leads to the formation of the superoxide radical, hydrogen peroxide and the hydroxyl radical [13]. O2•− and HO• have unpaired electrons in external orbitals and are therefore defined as free radicals, whereas H2O2 does not have unpaired electrons and is therefore not a radical. Non-radical derivatives of oxygen include hydrogen peroxide (H2O2), ozone (O3) and singlet oxygen (1O2). Reactive nitrogen species are nitrogen-based radicals, including the three chemical species of the Beckman-Radi-Freeman pathway (NO• nitric oxide, ONOO• peroxynitrite and NO2• nitrogen dioxide) [10,14]. Collectively, the radicals include superoxide (O2•−), oxygen radical (O2••), hydroxyl (•OH), alkoxy radical (RO•), peroxyl radical (ROO•), nitric oxide (or nitrogen monoxide) (NO•) and nitrogen dioxide (NO2•) [11,12]. The non- radical species include hydrogen peroxide (H2O2), hypochlorous acid (HOCl), hypobromous acid (HOBr), ozone (O3), singlet oxygen (1O2), nitrous acid (HNO2), nitrosyl cation (NO+), nitroxyl anion (NO−), dinitrogen trioxide (N2O3), dinitrogen tetroxide (N2O4), nitronium (nitryl) cation (NO2+), organic peroxides (ROOH), aldehydes (HCOR) and peroxynitrite (ONOO−) [11,12]. These non- radical species are not free radicals, but they are readily trigger free radical reactions in living organisms [15]. The different types of free radicals vary widely in their reactivity; for example, the reactivity of ROS in decreasing order is: HO• > O2•− > H2O2 [10]. The chemical reactivity of free radicals is directly associated with their potential to damage biological molecules. •OH is much more reactive than the other species and reacts rapidly with almost all chemical species, while H2O2, NO• and O2•− react quickly with a few molecules. Other species, such as RO2•, NO3•, RO•, HOCl, NO2•, ONOO−, NO2• and O3, show intermediate reactivities. RO• is more reactive than ROO•, the main products of lipid peroxidation. Regarding RNS, the reactivity of NO2• is between those of NO• and ONOO−. NO• has a rather low chemical reactivity, and its toxicity is therefore not high. However, when it reacts with O2•−, it produces a highly toxic species ONOO− capable of damaging lipids, proteins and DNA. The term ROS is used to include not only radicals but also non-radical species. However, biological systems are mainly damaged by radicals generated from oxygen.
활성산소종 및 활성질소종은
라디칼 형태이거나 비라디칼 화합물일 수 있다 [11,12] (표 1).
| non 라디칼’로 분류되는 대표적인 ROS, RNS에는 과산화수소(H2O2), 아질산(N2O3), 그리고 퍼옥시나이트라이트(ONOO-) 같은 것들. 이런 물질들은 전자 배치가 비교적 안정적이고, 자유 라디칼처럼 홀전자를 가지지 않기 때문에 ‘넌 라디칼 컴파운드’로 분류. 즉, 반응성이 상대적으로 낮고, 주로 다른 라디칼들과 반응하면서 2차 산물을 만들어내는 역할 |
활성산소종에는
산소의 부분적 환원 생성물인 펜튼/하버-바이스 경로의
세 가지 화학적 종(O2•− 과산화물 라디칼, H2O2 과산화수소, HO• 하이드록실 라디칼)이 포함됩니다.
분자 산소의 4전자 환원은
ROS 생성 없이 물의 형성을 초래하는 반면,
1전자 환원은 과산화물 라디칼, 과산화수소 및 하이드록실 라디칼의 형성을 초래합니다 [13].
O2•−와 HO•는
외부 궤도에 짝을 이루지 않은 전자를 가지므로 자유 라디칼로 정의되는 반면,
H2O2는
짝을 이루지 않은 전자를 가지지 않아 라디칼이 아닙니다.
산소의 비라디칼 유도체로는
과산화수소(H2O2), 오존(O3), 일중항 산소(1O2)가 있다.
반응성 질소 종은
질소 기반 라디칼로, 베크만-라디-프리먼 경로의
세 가지 화학적 종(NO• 일산화질소, ONOO• 과산화질산염, NO2• 이산화질소)을 포함한다 [10,14].
라디칼에는 총체적으로
과산화물(O2•−),
산소 라디칼(O2••),
하이드록실(•OH),
알콕시 라디칼(RO•),
퍼옥실 라디칼(ROO•),
일산화질소(NO•),
비라디칼 종에는
과산화수소(H2O2), 차염소산(HOCl), 차브롬산(HOBr), 오존(O3), 일중항 산소(1O2),
아질산(HNO2),
니트로실 양이온(NO+),
니트로실 음이온(NO−),
삼산화이질소(N2O3), 사산화이질소(N2O4),
니트로늄(니트릴) 양이온(NO2+),
유기 과산화물(ROOH), 알데하이드(HCOR), 과산화질산염(ONOO−) 등이 있다 [11,12].
radical - 근본적이고 강한 영향력을 가진 존재
이러한 비라디칼 종들은 자유 라디칼은 아니지만,
생물체 내에서 자유 라디칼 반응을 쉽게 유발한다 [15].
다양한 유형의 자유 라디칼은 반응성이 크게 다르며,
예를 들어 ROS의 반응성은 감소 순서로 다음과 같다:
HO• > O2•− > H2O2 [10] .
자유 라디칼의 화학적 반응성은 생물학적 분자를 손상시킬 잠재력과 직접적으로 연관된다.
•OH는 다른 종들보다 훨씬 반응성이 높으며
거의 모든 화학적 종과 신속히 반응하는 반면,
H2O2, NO• 및 O2•−는 소수의 분자와 빠르게 반응한다.
RO2•, NO3•, RO•, HOCl, NO2•, ONOO−, NO2• 및 O3와 같은
다른 종들은 중간 정도의 반응성을 보인다.
지질 과산화의 주요 생성물인
ROO•보다 RO•가 더 반응성이 높다.
RNS의 경우,
NO2•의 반응성은 NO•와 ONOO− 사이이다.
NO•는
화학 반응성이 상당히 낮아 독성도 높지 않다.
그러나 O2•−와 반응하면
지질, 단백질 및 DNA를 손상시킬 수 있는 고독성 종인 ONOO−를 생성한다.
ROS라는 용어는
라디칼뿐만 아니라 비라디칼 종도 포함하는 데 사용됩니다.
그러나 생물학적 시스템은
주로 산소에서 생성된 라디칼에 의해 손상됩니다.
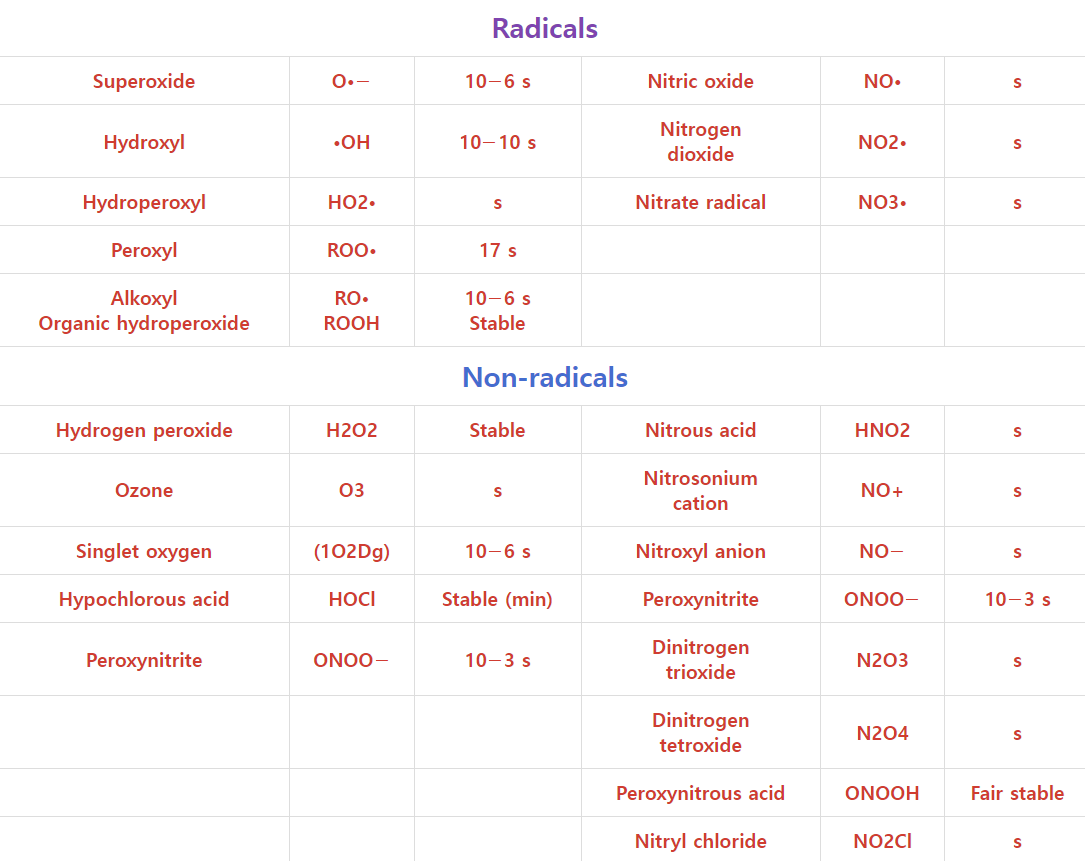
Table 1. Main reactive oxygen and nitrogen species generated during metabolism [11,12].
Reactive Oxygen Species (ROS)Reactive NitrogenSpecies (RNS)NameSymbolHalf-Life (s)NameSymbolHalf-Life 1
| Radicals | |||||
| Superoxide | O•− | 10−6 s | Nitric oxide | NO• | s |
| Hydroxyl | •OH | 10−10 s | Nitrogen dioxide | NO2• | s |
| Hydroperoxyl | HO2• | s | Nitrate radical | NO3• | s |
| Peroxyl | ROO• | 17 s | |||
| Alkoxyl Organic hydroperoxide | RO• ROOH | 10−6 s Stable | |||
| Non-radicals | |||||
| Hydrogen peroxide | H2O2 | Stable | Nitrous acid | HNO2 | s |
| Ozone | O3 | s | Nitrosonium cation | NO+ | s |
| Singlet oxygen | (1O2Dg) | 10−6 s | Nitroxyl anion | NO− | s |
| Hypochlorous acid | HOCl | Stable (min) | Peroxynitrite | ONOO− | 10−3 s |
| Peroxynitrite | ONOO− | 10−3 s | Dinitrogen trioxide | N2O3 | s |
| Dinitrogen tetroxide | N2O4 | s | |||
| Peroxynitrous acid | ONOOH | Fair stable | |||
| Nitryl chloride | NO2Cl | s | |||
The abundance of free radicals in decreasing order is reactive oxygen species > reactive nitrogen species > reactive sulfur species [12,16] (Table 2).
Table 2. List of the common reactive oxygen species, nitrogen species and sulfur species of biological interest [12,16].
Reactive Oxygen Species (ROS)Reactive Nitrogen Species (RNS)Reactive Sulfur Species (RSS)NameSymbolNameSymbolNameSymbol
| Radicals | |||||
| Oxygen (bi-radical) | O2·· | Nitric oxide | NO• | Thiyl radical S• | RS• |
| Hydroxyl | •OH | Nitrogen dioxide | NO2• | ||
| Hydroperoxyl | HO2• | Nitrate radical | NO3• | ||
| Carbonate | CO3•− | ||||
| Peroxyl | ROO• | ||||
| Alkoxyl | RO• | ||||
| Carbon dioxide radical | CO2•− | ||||
| Non-radicals | |||||
| Hydrogen peroxide | H2O2 | Nitrosyl cation | NO+ | Hydrogen sulfide | H2S |
| Ozone | O3 | Nitrous acid | HNO2 | Disulfide | RSSR |
| Singlet oxygen | 1O2 | Nitroxyl anion | NO− | Disulfide-S-monoxide | RS(O)SR |
| Hypobromous acid | HOBr | Dinitrogen trioxide | N2O3 | Disulfide-S-dioxide | RS(O)2SR |
| Hypochlorous acid | HOCl | Dinitrogen tetroxide | N2O4 | Sulfenic acid | RSOH |
| Hypoiodous acid | HOI | Dinitrogen pentoxide | N2O5 | Thiol/sulfide | RSR |
| Organic peroxides | ROOH | Alkyl peroxynitrites | ROONO | ||
| Peroxynitrite | ONOO− | Alkyl peroxynitrates | RO2ONO | ||
| Peroxynitrate | O2NOO− | Nitryl chloride | NO2Cl | ||
| Peroxynitrous acid | ONOOH | Peroxyacetyl nitrate | CH3C(O)OONO2 | ||
| Peroxomono-carbonate | HOOCO2− | ||||
| Carbon monoxide | CO | ||||
2.1. Properties of Free Radicals
2.1.1. Superoxide Anion Radical (O2•−)
The superoxide anion (O2•−) is a reduced form of molecular oxygen created by receiving an electron in a π* antibonding orbital [10]. With only one unpaired electron, superoxide is less radical than O2, and despite its super name, its reactivity with biomolecules is not very sustained [17]. The addition of another electron to O2•− produces O2−, the peroxide ion, a non-radical (no unpaired electrons) with a weaker oxygen–oxygen bond. The addition of another two electrons to O22− completely eliminates the bond, producing two O2− (oxide ions). In biology, the two-electron reduction product of O2 is H2O2, and the four-electron product is water. It is mostly produced in the mitochondrial electron transport chain in the course of oxidative phosphorylation, which produces adenosine triphosphate (ATP) [18,19]. The superoxide anion can be produced by enzymic or non-enzymic activity, by the direct transfer of electrons to an oxygen molecule [20] or by photochemical means [21]; in biological systems, it is the main precursor of highly reactive species such as HO•, 1O2, CO3•−, ONOO•, HOCl and GSSG•− (glutathione disulfide) [10,22]. The enzymes that produce superoxide include oxygenases dependent on cytochrome P450 and xanthine oxidase dependent on lipoxygenase, cyclooxygenase and nicotinamide adenine dinucleotide phosphate (NADPH) oxidase [20]. A superoxide radical, as a moderately reactive free radical, can react with another superoxide radical to produce hydrogen peroxide (H2O2), which can be reduced to water or partially reduced to the extremely reactive hydroxyl radical (HO•). Dismutation of the superoxide radical can be spontaneous or catalyzed by enzymes known as superoxide dismutases. The formation of HO• is possible by the decomposition of H2O2, catalyzed by transition metal ions in the lower valence state, such as Fe2+ or Cu+ (Fenton reaction), or by the reaction of H2O2 with a superoxide radical (Haber–Weiss reaction); oxidized transitional metals from the Fenton reaction may be re-reduced by O2•− [23].
Since superoxide is a highly reactive free radical, it can damage molecules (DNA, proteins and lipids) [10]. It may be generated by the immune system to kill invading microorganisms; phagocytes, such as neutrophils, monocytes, macrophages, mast cells and dendritic cells, are mobilized by chemotaxis to the site of bacterial infection and mediate damage through their surface receptors. The phagocytosed bacteria are killed by a process involving O2•− [17].
2.1. 자유 라디칼의 특성
2.1.1. 슈퍼옥사이드 음이온 라디칼 (O2•−)
초산화물 음이온(O2•−)은
π* 반결합 궤도에서 전자를 받아 생성된 분자 산소의 환원 형태이다[10].
단 하나의 짝을 이루지 않은 전자를 가진 초산화물은
O2보다 라디칼 특성이 약하며,
'초(超)'라는 이름에도 불구하고 생체 분자와의 반응성은 그리 지속적이지 않다[17] .
O2•−에 전자를 하나 더 추가하면
과산화 이온인 O2−가 생성되는데,
이는 비라디칼(불쌍 전자 없음)이며
산소-산소 결합이 더 약하다. O2−에 전자를 두 개 더 추가하면 결합이 완전히 제거되어
두 개의 O2−(산화 이온)이 생성된다.
생물학에서
O2의 2전자 환원 생성물은
H2O2이며,
4전자 생성물은 물이다.
| 2전자 생성물’은 반응에서 전자가 생기는 쪽, 그러니까 O2가 전자를 받아들여서 H2O2를 만들면 그 과정에서 전자가 생겨나는 쪽. 반대로 ‘4전자 생성물’은 전자를 잃어버리는 쪽, 즉 물(H2O)이 되는 쪽을 의미 |
이는 주로 산화적 인산화 과정에서 미토콘드리아 전자 전달계에서 생성되며,
이 과정에서 아데노신 삼인산(ATP)이 생성된다[18,19].
슈퍼옥사이드 음이온은
효소적 또는 비효소적 활성, 산소 분자로의 직접적인 전자 전달[20],
또는 광화학적 수단[21]을 통해 생성될 수 있다.
생물학적 시스템에서 이는
HO•, 1O2, CO3•−, ONOO•, HOCl 및 GSSG•−(글루타티온 디설파이드)의
슈퍼옥사이드를 생성하는 효소에는
시토크롬 P450에 의존하는 산소화효소,
리폭시게나제,
사이클로옥시게나제 및 니코틴아미드 아데닌 디뉴클레오티드 포스페이트(NADPH) 산화효소에 의존하는
크산틴 산화효소가 포함된다[20] .
| 사이토크롬 P450은 우리 몸에 있는 아주 중요한 효소 계열. 주로 간에 많이 존재하고, 여러 가지 약물, 독성 물질, 호르몬 같은 다양한 화합물을 대사하고 분해하는 역할. 쉽게 말해서, 몸에 들어온 약물이나 독소를 더 잘 배출할 수 있도록 변환해주는 효소들 |
| 크산틴 산화효소는 퓨린 대사 과정에서 중요한 역할을 하는 효소. 주로 하이폭산틴을 크산틴으로, 또 크산틴을 요산으로 변환하는 반응을 촉매 https://www.nature.com/articles/s41440-021-00724-z 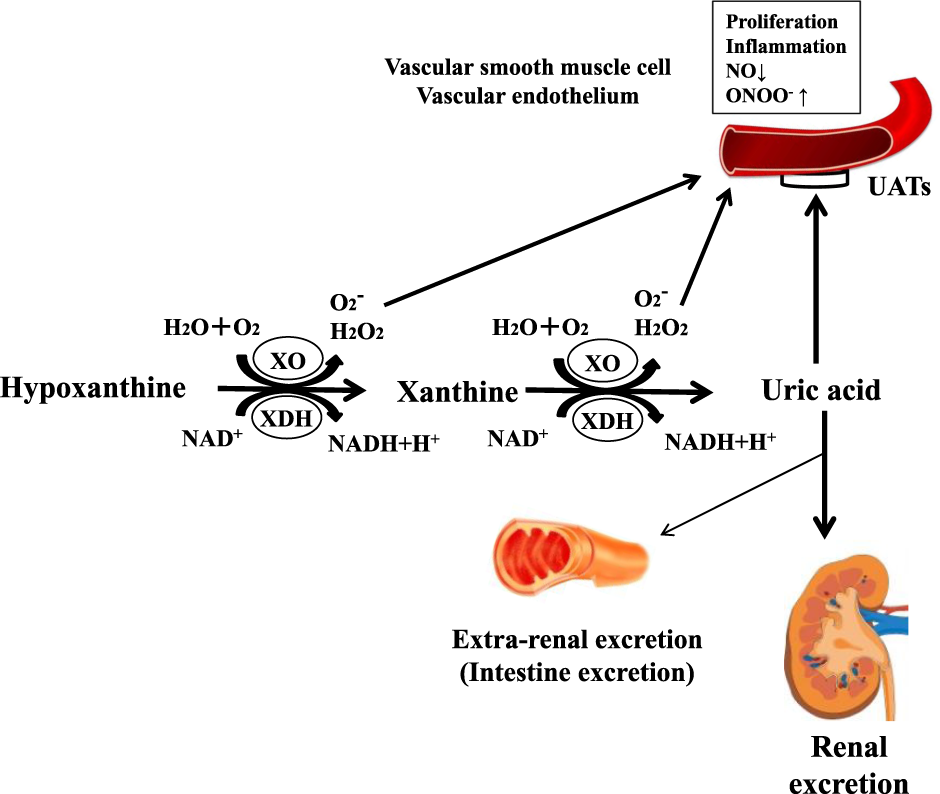 이 효소에는 두 가지 형태가 있는데, 바로 크산틴 탈수소효소(xanthine dehydrogenase)와 크산틴 산화효소(xanthine oxidase). 이 둘은 공유된 단백질 구조를 가지는데, 산소 분압이나 세포 내 조건에 따라 상호전환될 수 있어요. 크산틴 산화효소(XO)는 산소를 전자 수용체로 사용해서 요산을 만들어내고, 이 과정에서 활성산소(슈퍼옥사이드 라디컬이나 과산화수소 같은 것들)을 생성합니다. 반면, 크산틴 탈수소효소(XDH)는 NAD+를 전자 수용체로 사용해서 NADH를 생산하는 방식으로 전환을 이끌어내요. 이렇게 두 형태가 서로 다른 조건에서 기능하면서, 우리 몸의 산화적 스트레스 조절에도 영향을 미치고, 통풍 같은 질환과도 관련 |
https://pmc.ncbi.nlm.nih.gov/articles/PMC6235219/

중간 반응성을 지닌 자유 라디칼인 슈퍼옥사이드 라디칼은 다른 슈퍼옥사이드 라디칼과 반응하여 과산화수소(H2O2)를 생성할 수 있으며, 이는 물로 환원되거나 극도로 반응성이 높은 하이드록실 라디칼(HO•)로 부분 환원될 수 있다 . 슈퍼옥사이드 라디칼의 이중분해는 자발적으로 발생하거나 슈퍼옥사이드 디스뮤타아제(SOD)로 알려진 효소에 의해 촉매될 수 있다. HO•의 생성은 H2O2의 분해를 통해 가능하며, 이는 Fe2+ 또는 Cu+와 같은 낮은 원자가 상태의 전이 금속 이온에 의해 촉매되거나(펜튼 반응), H2O2와 슈퍼옥사이드 라디칼의 반응을 통해 발생할 수 있다(하버-바이스 반응); 펜튼 반응에서 산화된 전이 금속은 O2•−에 의해 재환원될 수 있다 [23].
슈퍼옥사이드가 고도로 반응성 자유 라디칼이기 때문에 분자(DNA, 단백질 및 지질)를 손상시킬 수 있다[10]. 침입한 미생물을 사멸시키기 위해 면역 체계에 의해 생성될 수 있으며, 호중구, 단핵구, 대식세포, 비만세포 및 수지상 세포와 같은 식세포는 세균 감염 부위로의 화학주행에 의해 동원되어 표면 수용체를 통해 손상을 매개한다. 포식된 박테리아는 O2•−가 관여하는 과정으로 사멸됩니다 [17].
2.1.2. Hydroxyl Radical (HO•)
The hydroxyl radical (HO•) is, chemically, the most reactive free radical formed in vivo. It is formed by the Fenton reaction, in which free iron (Fe2+) reacts with hydrogen peroxide (H2O2), and by the Haber–Weiss reaction of superoxide with ferric iron (Fe3+), producing Fe2+. The reaction is not limited to iron, but it may involve several other ions (Cu2+, Fe3+, Ti4+ and Co3+), which can be recycled by interaction with superoxide anion to form O2 [24]. It is estimated that a cell produces around 50 hydroxyl radicals per second [25]; since hydroxyl radicals have the highest one-electron reduction potential (2310 mV), they can react with anything in living organisms with rate constants from 109 to 1010/M/s [26] and are considered the most harmful free species, since they attack any molecule less than a few nanometers from where they are generated.
The hydroxyl radical reacts strongly with most organic and inorganic molecules (DNA, proteins, lipids, amino acids, sugars, vitamins and metals) faster than its speed of generation [27]. These reactions involve the abstraction of hydrogen and the addition and transfer of electrons [10,11]. In saturated compounds, a hydroxyl radical abstracts a hydrogen atom from the weaker C–H bond to produce a free radical [26]. The resulting radicals may react with oxygen and generate other free radicals. Hydroxyl radicals are easily added to double bonds. All mitochondrial enzyme proteins are susceptible to inactivation by HO•, while all amino acid residues of proteins can be oxidized by HO• [28]. It is estimated that ·OH is responsible for 60–70% of the tissue damage caused by ionizing radiation [29]. Hydroxyl radicals are also involved in disorders, such as cardiovascular disease [30] and cancer [31].
2.1.2. 하이드록실 라디칼 (HO•)
하이드록실 라디칼(HO•)은 생체 내에서 생성되는 화학적으로 가장 반응성이 높은 자유 라디칼입니다. 이는 자유 철(Fe2+)이 과산화수소(H2O2)와 반응하는 펜튼 반응과, 과산화물이 철(III) 이온(Fe3+)과 반응하여 Fe2+를 생성하는 하버-바이스 반응에 의해 생성됩니다. 이 반응은 철에 국한되지 않으며, 여러 다른 이온(Cu2+, Fe3+, Ti4+ 및 Co3+)도 포함될 수 있으며, 이들은 과산화수소 음이온과의 상호작용을 통해 O2 [24]를 형성하며 재활용될 수 있다. 세포는 초당 약 50개의 하이드록실 라디칼을 생성하는 것으로 추정된다 [25]; 하이드록실 라디칼은 가장 높은 1전자 환원 전위(2310 mV)를 가지므로, 생물체 내 모든 물질과 10⁹~10¹⁰/M/s의 속도 상수로 반응할 수 있으며[26], 생성 지점에서 몇 나노미터 이내의 모든 분자를 공격하기 때문에 가장 유해한 자유 라디칼로 간주됩니다.
하이드록실 라디칼은 생성 속도보다 빠르게 대부분의 유기 및 무기 분자(DNA, 단백질, 지질, 아미노산, 당류, 비타민 및 금속)와 강력하게 반응합니다[27]. 이러한 반응에는 수소 원자 추출과 전자 첨가 및 전이가 포함됩니다[10,11]. 포화 화합물에서 하이드록실 라디칼은 더 약한 C–H 결합으로부터 수소 원자를 추출하여 자유 라디칼을 생성합니다[26]. 생성된 라디칼은 산소와 반응하여 다른 자유 라디칼을 생성할 수 있습니다. 하이드록실 라디칼은 이중 결합에 쉽게 첨가됩니다. 모든 미토콘드리아 효소 단백질은 HO•에 의해 비활성화되기 쉬우며, 단백질의 모든 아미노산 잔기는 HO•에 의해 산화될 수 있습니다 [28]. ·OH는 이온화 방사선에 의해 유발되는 조직 손상의 60~70%를 차지하는 것으로 추정됩니다 [29]. 하이드록실 라디칼은 또한 심혈관 질환[30] 및 암[31]과 같은 질환에도 관여한다.
2.1.3. Peroxyl Radical (ROO•)
The alkoxyl (RO•) and peroxyl (ROO•) radicals are oxygen-centered organic radicals. They tend to accept electrons and then undergo reduction, having highly positive reduction potentials (1000 to 1600 mV) [32]. Peroxyl and alkoxyl radicals can be generated by the decomposition of alkyl peroxides (ROOH) induced by heat, radiation or a reaction with transition metal ions and other oxidants capable of subtracting hydrogen [32]. They can also be generated by the oxidation of proteins and nucleic acid [33]. These carbon-centered radicals react directly with biological molecules, such as DNA and albumin -SH-groups. They can abstract hydrogen from other molecules that have a lower standard reduction potential, as observed in the propagation phase of lipid peroxidation. The alkyl radical formed by this reaction may react with oxygen to form another peroxyl radical, resulting in a chain reaction. The RO• radicals formed by the reduction of peroxides are significantly more reactive than ROO• but less reactive than •OH [34]. ROO• may diffuse to remote parts of cells. Their half-lives are of the order of seconds, and they are generally less reactive than HOO• when R is an alkyl or an alkenyl group [35]. Some peroxyl radicals cleave, releasing superoxide anion, or react with each other to generate singlet oxygen [10].
2.1.3. 퍼옥실 라디칼 (ROO•)
알콕실 (RO•) 및 퍼옥실 (ROO•) 라디칼은 산소 중심의 유기 라디칼이다. 이들은 전자를 받아들이고 환원되는 경향이 있으며, 매우 양의 환원 전위(1000~1600 mV)를 가진다 [32]. 과산화 라디칼과 알콕실 라디칼은 열, 방사선 또는 전이 금속 이온 및 수소를 빼낼 수 있는 다른 산화제와의 반응에 의해 유도된 알킬 과산화물(ROOH)의 분해로 생성될 수 있다[32]. 또한 단백질과 핵산의 산화에 의해 생성될 수도 있다[33]. 이러한 탄소 중심 라디칼은 DNA 및 알부민 -SH- 그룹과 같은 생물학적 분자와 직접 반응한다. 지질 과산화 반응의 진행 단계에서 관찰되듯이, 이들은 표준 환원 전위가 더 낮은 다른 분자에서 수소를 추출할 수 있다. 이 반응으로 생성된 알킬 라디칼은 산소와 반응하여 또 다른 퍼옥실 라디칼을 형성할 수 있으며, 이는 연쇄 반응을 초래한다. 과산화물의 환원으로 생성된 RO• 라디칼은 ROO•보다 반응성이 현저히 높지만 •OH보다는 반응성이 낮다 [34]. ROO•는 세포의 먼 부분까지 확산될 수 있습니다. 이들의 반감기는 초 단위이며, R이 알킬 또는 알켄일 그룹일 때 일반적으로 HOO•보다 반응성이 낮습니다 [35]. 일부 퍼옥실 라디칼은 분해되어 슈퍼옥사이드 음이온을 방출하거나, 서로 반응하여 일중항 산소를 생성합니다 [10].
2.1.4. Hydroperoxyl Radical (HO2•)
HO2•, usually termed hydroperoxyl radical or perhydroxyl radical, is the simplest form of a peroxyl radical, produced by the protonation of the superoxide anion radical or by the decomposition of hydroperoxide; approximately 0.3% of superoxide present in the cell cytosol exists in the protonated form [36]. The hydroperoxyl radical produces H2O2, which can react with active redox metals, including iron and copper, to trigger Fenton or Haber–Weiss reactions. The hydroperoxyl radical can also extract hydrogen atoms from NADH or glyceraldehyde-3-phosphate dehydrogenase–NADH, forming H2O2 [37]. Its reactions are slower than HO• but competitive with organic peroxyl radicals. The hydroperoxyl radical plays an important role in the chemistry of lipid peroxidation. It is a much stronger oxidant than superoxide anion due to its ability to extract hydrogen atoms from linoleic, linolenic and arachidonic fatty acids, suggesting a role in the initiation of lipid oxidation [10,37].
2.1.4. 하이드로퍼옥실 라디칼 (HO2•)
HO2•는 일반적으로 하이드로퍼옥실 라디칼 또는 퍼하이드록실 라디칼이라 불리며, 과산화수소 이온 라디칼의 양성자화 또는 하이드로퍼옥사이드의 분해로 생성되는 가장 단순한 형태의 퍼옥실 라디칼이다. 세포질 내 존재하는 과산화수소 이온의 약 0.3%가 양성자화된 형태로 존재한다 [36]. 하이드로퍼옥실 라디칼은 H2O2를 생성하며, 이는 철과 구리를 포함한 활성 산화환원 금속과 반응하여 펜튼 반응 또는 하버-바이스 반응을 유발할 수 있다. 하이드로퍼옥실 라디칼은 또한 NADH 또는 글리세랄데하이드-3-인산 탈수소효소-NADH로부터 수소 원자를 추출하여 H2O2를 형성할 수 있다 [37]. 그 반응 속도는 HO•보다 느리지만 유기 과산화 라디칼과는 경쟁적이다. 하이드로퍼옥실 라디칼은 지질 과산화 반응에서 중요한 역할을 한다. 리놀레산, 리놀렌산, 아라키돈산 지방산으로부터 수소 원자를 추출할 수 있는 능력으로 인해 과산화수소 음이온보다 훨씬 강력한 산화제로, 지질 산화 개시에 관여함을 시사한다 [10,37].
2.1.5. Hydrogen Peroxide (H2O2)
Hydrogen peroxide can be generated by the dismutation of O2•− or by the direct reduction of O2, and it is mainly produced by enzyme reactions [38]. The presence of oxidases (urate oxidase, glucose oxidase, D- amino acid oxidase) may lead to the direct synthesis of hydrogen peroxide by the transfer of two electrons to molecular oxygen; these enzymes are found in microsomes, peroxisomes and mitochondria [38]. Hydrogen peroxide is liposoluble and can therefore diffuse through the cell membrane. Being weakly reactive, this non-free-radical cannot readily oxidize most lipids, proteins and nucleic acids. The threat posed by H2O2 lies in its conversion to the hydroxyl radical (HO•) by homolytic fission, induced by UV or by the interaction with transition metal ions (Fenton reaction) [39]. Hydrogen peroxide may produce singlet oxygen through a reaction with a superoxide anion or with HOCl or chloramines in living systems [22]. The direct action of H2O2 involves an attack on the structure of heme proteins with the release of iron, enzyme inactivation and oxidation of DNA, lipids, -SH groups and keto-acids [11].
2.1.5. 과산화수소 (H2O2)
과산화수소는 O2•−의 이중분해 또는 O2의 직접 환원을 통해 생성될 수 있으며, 주로 효소 반응에 의해 생성됩니다 [38]. 산화효소(요산산화효소, 포도당산화효소, D-아미노산산화효소)의 존재는 두 개의 전자를 분자 산소로 전달함으로써 과산화수소의 직접 합성을 유발할 수 있으며, 이러한 효소들은 미세소체, 퍼옥시좀 및 미토콘드리아에서 발견된다[38]. 과산화수소는 지용성이므로 세포막을 통해 확산될 수 있다. 반응성이 약한 이 비자유라디칼은 대부분의 지질, 단백질 및 핵산을 쉽게 산화시키지 못한다. H2O2가 초래하는 위협은 자외선 또는 전이 금속 이온과의 상호작용(펜튼 반응)에 의해 유도된 동해성 분열을 통해 하이드록실 라디칼(HO•)로 전환되는 데 있다[39]. 과산화수소는 생체 내에서 슈퍼옥사이드 음이온 또는 HOCl, 클로라민과의 반응을 통해 일중항 산소를 생성할 수 있다[22]. H2O2의 직접 작용은 헤모 단백질 구조를 공격하여 철을 방출하고, 효소 비활성화 및 DNA, 지질, -SH 그룹 및 케토산의 산화를 유발한다[11].
2.1.6. Molecular Oxygen (O2••) and Singlet Oxygen (1O2)
In the evolutionary history of the Earth, oxygen appeared two billion years ago, what we call the ‘’Great Oxidation Event’’, by virtue of the photosynthesis of cyanobacteria, which used solar energy to split water [40]. Oxygen, a metabolic by-product, was released into the atmosphere [25], where it formed the ozone (O3) that shields the Earth from the radiation. Oxygen removed ferrous iron (Fe2+) from aqueous environments by forming deposits of insoluble ferric complexes, leaving only traces of soluble iron in sea and river water [25]. Since animals, including humans, need O2, a toxic mutagenic gas for the mitochondria to efficiently produce energy, only advanced antioxidant defenses allow them to survive. In fact, all aerobic organisms, including plants, aerobic bacteria, animals and humans, suffer damage if exposed to higher-than-normal concentrations of O2 [10]. This means that their antioxidant defenses are limited. According to the theory of superoxide toxicity, O2 toxicity is due to excessive superoxide radical formation [17]. From the biological point of view, molecular oxygen, in its diatomic (O2) ground state, is a bi-radical because it contains two unpaired electrons, each of which is located in a different π antibonding orbital. It is indicated as “triplet oxygen” because the spin of these electrons has three possible alignments with an external field [41]. Triplet oxygen, the more abundant form of oxygen, is the common oxygen we breathe. It carries a “spin restriction” against reacting with most organic molecules. Molecular oxygen is not very reactive because its electrons are in the lowest energy configuration.
When the two unpaired electrons from triplet oxygen enter two different orbitals, the result is a powerful oxidant named singlet oxygen (1Δg, 1O2) [42]. The 1Δg state, which is 92 kJmol−1 above the ground state, carries an empty π* orbital where it can accommodate a pair of electrons. This ability gives singlet oxygen strong acidic properties. It is therefore a strong electrophile, which reacts with reagents that have high electron density regions, oxidizing them.
Photosensitizers, such as hematoporphyrins, riboflavin and myoglobin, may form singlet oxygen from triplet oxygen in the presence of light by two basic types of photo- oxidation [21]. In the type I reaction, the photosensitizer absorbs light, enabling the excited triplet to react directly with the substrate; while in the type II reaction, it first interacts with the molecular oxygen ground-state (3O2) to produce 1O2, and the excited triplet returns to its ground state. The speed of the type I or II reaction depends on sensitizer type [21,43] and on the substrate and concentrations of substrate and oxygen in the reaction environment. Additionally, 1O2 is produced in vivo by the activation of eosinophils, macrophages and neutrophils [43] and by the enzyme reactions and activities of different peroxidases [42].
Singlet oxygen is very reactive because the “spin restriction” is removed, allowing the species to react as an electrophilic oxidant [21,44] and making it a potential aggressor when it is produced inside the cell [45]. This is indicated especially by its ability to damage DNA, components of guanine and nucleic acids, leading to toxic and mutagenic effects and tissue damage [43]. It is also involved in the oxidation of cholesterol [46] and proteins with high electron density amino acid residues, such as cysteine, methionine, tryptophan, tyrosine and histidine [28]. Singlet oxygen can also play a role in generating cell signals to modify gene expression [43] and can be used to fight cancer cells and various pathogens such as microbes and viruses [22].
2.1.6. 분자 산소(O2••) 및 일중항 산소(1O2)
지구 진화 역사에서 산소는 20억 년 전, 즉 '대산화사건'이라 불리는 시기에 청록색 박테리아의 광합성에 의해 태양 에너지를 이용해 물을 분해하면서 등장했습니다[40]. 대사 부산물인 산소는 대기 중으로 방출되어 [25]에서 방출되었으며, 여기서 지구를 방사선으로부터 보호하는 오존(O3)을 형성했습니다. 산소는 용해되지 않는 제2철 복합체의 침전물을 형성함으로써 수중 환경에서 제2철(Fe2+)을 제거하여 바다와 강물에 용해성 철의 흔적만 남겼습니다 [25]. 인간을 포함한 동물은 미토콘드리아가 효율적으로 에너지를 생산하기 위해 독성 돌연변이 유발 가스인 O2가 필요하기 때문에, 진보된 항산화 방어 체계만이 그들의 생존을 가능하게 합니다. 사실 식물, 호기성 세균, 동물 및 인간을 포함한 모든 호기성 생물은 정상보다 높은 농도의 O2에 노출되면 손상을 입습니다[10]. 이는 그들의 항산화 방어 체계가 한계가 있음을 의미합니다. 슈퍼옥사이드 독성 이론에 따르면, O2 독성은 과도한 슈퍼옥사이드 라디칼 생성에 기인합니다 [17]. 생물학적 관점에서, 분자 산소는 이원자(O2) 기저 상태에서 두 개의 짝을 이루지 않은 전자를 포함하고 있으며, 각 전자는 서로 다른 π 반결합 궤도에 위치하기 때문에 이중 라디칼이다. 이 산소는 외부 자기장 하에서 전자 스핀이 세 가지 배열 상태를 가질 수 있어 “삼중항 산소”로 명명된다[41]. 삼중항 산소는 더 풍부한 형태의 산소로, 우리가 호흡하는 일반적인 산소이다. 이 산소는 대부분의 유기 분자와 반응하는 데 “스핀 제한”을 지닌다. 분자 산소는 전자가 최저 에너지 상태에 위치하므로 반응성이 높지 않다.
삼중항 산소의 두 개의 짝을 이루지 않은 전자가 서로 다른 두 개의 궤도에 들어가면, 일중항 산소(1Δg, 1O2)라는 강력한 산화제가 생성됩니다[42]. 기저 상태보다 92 kJmol−1 높은 1Δg 상태는 한 쌍의 전자를 수용할 수 있는 빈 π* 궤도를 가지고 있습니다. 이러한 능력 덕분에 일중항 산소는 강한 산성 특성을 지닙니다. 따라서 이는 강한 친전자체로서, 높은 전자 밀도 영역을 가진 시약과 반응하여 이를 산화시킵니다.
헤마토포르피린, 리보플라빈, 미오글로빈과 같은 광감작제는 빛의 존재 하에서 두 가지 기본 유형의 광산화 반응을 통해 삼중항 산소로부터 일중항 산소를 생성할 수 있습니다[21] . 제1형 반응에서는 광감작제가 빛을 흡수하여 여기된 삼중항 상태가 기질과 직접 반응하게 합니다. 반면 제2형 반응에서는 먼저 분자 산소 기저 상태(3O2)와 상호작용하여 1O2를 생성하고, 그리고 여기된 삼중항 산소는 기저 상태로 돌아간다. 제1형 또는 제2형 반응의 속도는 감광제 유형[21,43]과 기질, 그리고 반응 환경 내 기질과 산소의 농도에 따라 달라진다. 또한, 1O2는 호산구, 대식세포 및 호중구의 활성화[43]와 다양한 과산화효소의 효소 반응 및 활성에 의해 생체 내에서 생성된다[42].
일중항 산소는 “스핀 제한”이 제거되어 매우 반응성이 높으며, 이는 해당 종이 친전자성 산화제로 반응할 수 있게 하여[21,44] 세포 내에서 생성될 때 잠재적 공격자가 되게 합니다[45]. 이는 특히 DNA, 구아닌 및 핵산 구성 요소를 손상시켜 독성 및 변이원성 효과와 조직 손상을 초래하는 능력으로 나타납니다[43]. 또한 콜레스테롤[46]과 시스테인, 메티오닌, 트립토판, 티로신, 히스티딘과 같은 전자 밀도가 높은 아미노산 잔기를 가진 단백질의 산화에도 관여한다[28]. 일중항 산소는 유전자 발현을 조절하는 세포 신호 생성[43]에도 역할을 할 수 있으며, 암세포 및 미생물과 바이러스 같은 다양한 병원체와 싸우는 데 활용될 수 있다[22].
2.1.7. Ozone (O3)
In the history of the Earth, ozone was formed from O2 by the action of high energy electromagnetic radiation and electrical discharges [25]. It is slightly less reactive than HO• and a much stronger oxidizing agent than oxygen [46]. It can form free radicals by oxidizing biological molecules and causes oxidative damage to lipids [47], proteins and nucleic acids [48]. Ozone also plays an important role in inflammatory processes [49].
2.1.8. Hypochlorous Acid (HOCl)
Hypochlorous acid (HOCl) is a highly reactive species involved in oxidation reactions and chlorination of the protein and lipid components. It is generated by hydrogen peroxide and the chloride anion in a reaction catalyzed by myeloperoxidase in macrophages and neutrophils at sites of inflammation [50]. It can oxidize thiols and other biological molecules, including ascorbate, urate, pyridine nucleotides and tryptophan [50]. HOCl chlorinate compounds such as amines to chloramines, residues of tyrosyl to ring chlorinated products, cholesterol and unsaturated lipids to chlorohydrins and may also chlorinate DNA [51].
2.1.7. 오존 (O3)
지구 역사에서 오존은 고에너지 전자기 복사 및 전기 방전의 작용으로 O2로부터 생성되었습니다 [25]. HO•보다 반응성이 약간 낮으며 산소보다 훨씬 강력한 산화제이다 [46]. 생물학적 분자를 산화시켜 자유 라디칼을 형성할 수 있으며 지질 [47], 단백질 및 핵산 [48]에 산화적 손상을 유발한다. 오존은 또한 염증 과정에서도 중요한 역할을 한다 [49].
2.1.8. 차아염소산(HOCl)
차아염소산(HOCl)은 단백질 및 지질 성분의 산화 반응과 염소화에 관여하는 고반응성 물질이다. 염증 부위에서 대식세포와 호중구의 골수과산화효소에 의해 촉매되는 반응에서 과산화수소와 염화물 음이온에 의해 생성된다[50]. 티올 및 아스코르브산염, 요산염, 피리딘 뉴클레오티드, 트립토판 등 기타 생물학적 분자를 산화시킬 수 있다[50]. HOCl은 아민을 클로라민으로, 티로실 잔기를 고리형 염소화 생성물로, 콜레스테롤 및 불포화 지질을 클로로하이드린으로 염소화하며 DNA도 염소화할 수 있다[51].
2.1.9. Carbonate Radical Anion (CO3•−)
The carbonate radical anion (CO3•−) may be produced by the radiolysis of aqueous solutions of bicarbonate/carbonate [52]; it can also be formed when •OH reacts with carbonate or bicarbonate ions. Levels of bicarbonate are high (25 mM) in blood plasma, enabling the reaction [53]. Although not as strong an oxidizing agent as the hydroxyl radical, the carbonate radical anion is a strong one-electron oxidant that acts by electron transfer and hydrogen abstraction [33]. It has a much longer half-life than •OH and can therefore spread further and oxidatively modify distant cell targets. A wide variety of biomolecules can be oxidized by CO3•−. Regarded as a major oxidant of proteins and nucleic acids, it oxidizes DNA guanine bases by a one-electron transfer process that leads to the formation of stable guanine oxidation products [54]. The carbonate radical anion has been proposed as a key mediator of oxidative damage derived from peroxynitrite production [33,55], xanthine oxidase turnover and superoxide dismutase activity [56]. It is known to play an important role in the modification of selective amino acids in proteins under conditions of oxidative stress, aging and inflammation [57]. The kinetics of tyrosine nitration in the presence of CO2 suggest a specific role of CO3•− in MnSOD nitration by peroxynitrite [58]. The nitration of tyrosine has been observed in neurodegenerative conditions, cardiovascular disorders and diabetes [59].
2.1.9. 탄산 라디칼 음이온 (CO3•−)
탄산 라디칼 음이온(CO3•−)은 중탄산염/탄산염 수용액의 방사분해에 의해 생성될 수 있다[52]; 또한 •OH가 탄산염 또는 중탄산염 이온과 반응할 때도 형성될 수 있다. 혈장 내 중탄산염 농도는 높으며(25 mM), 이로 인해 반응이 가능해진다 [53]. 하이드록실 라디칼만큼 강력한 산화제는 아니지만, 탄산 라디칼 음이온은 전자 전달과 수소 추출을 통해 작용하는 강력한 1전자 산화제이다 [33]. •OH보다 훨씬 긴 반감기를 가지므로 더 멀리 확산되어 원거리 세포 표적을 산화적으로 변형시킬 수 있다. CO3•−에 의해 다양한 생체 분자가 산화될 수 있다. 단백질과 핵산의 주요 산화제로 간주되며, 안정된 구아닌 산화 생성물 형성으로 이어지는 1전자 전달 과정을 통해 DNA 구아닌 염기를 산화시킨다 [54]. 탄산 라디칼 음이온은 퍼옥시나이트라이트 생성[33,55], 크산틴 산화효소 전환 및 슈퍼옥사이드 디스뮤타제 활성[56]에서 비롯된 산화적 손상의 핵심 매개체로 제안되었다. 이는 산화 스트레스, 노화 및 염증 조건 하에서 단백질 내 특정 아미노산의 변형에 중요한 역할을 하는 것으로 알려져 있다[57]. CO2 존재 하에서의 티로신 니트레이션 동역학은 과산화질소에 의한 MnSOD 니트레이션에서 CO3•−의 특이적 역할을 시사한다[58]. 티로신의 니트레이션은 신경퇴행성 질환, 심혈관 장애 및 당뇨병에서 관찰되었다[59].
2.1.10. Nitric Oxide (NO•)
Nitric oxide (NO•), nitrogen dioxide (NO2•) and peroxynitrite (ONOO−), as well as non-radicals such as nitrous acid HNO2 and N2O4 (dinitrogen tetroxide), are included in the collective term reactive nitrogen species (RNS). Nitric oxide or nitrogen monoxide (NO•) is a free radical with a single unpaired electron. The chemical reactivity of NO• is rather limited, and consequently its direct toxicity is less than that of ROS. However, it reacts with O2•−, producing peroxynitrite anion (ONOO−) [55], a very damaging species for proteins, lipids and DNA [60]. Nitric oxide also reacts with molecular oxygen and nitrogen to form nitrogen dioxide or dinitrogen trioxide, both toxic oxidizing and nitrosating agents [55]. Nitric oxide is generated in biological tissues by specific nitric oxide synthases [61], through the reaction of H2O2 with arginine [62] or through the decomposition of S-nitroso thiols in the presence of metal ions [63].
Nitric oxide is soluble in water and fat, and it therefore diffuses readily through the cytoplasm and plasma membrane. If human blood plasma is exposed to NO•, ascorbic acid and uric acid concentrations become depleted and lipid peroxidation is triggered [10]. Nitric oxide-derived species in cell membranes and lipoproteins react quickly with fatty acids and lipid peroxyl radicals during lipid oxidation, generating oxidized and nitrated products of free lipids and esterified cholesterol [64]. Nitric oxide is also involved in many physiological processes, such as neuro-transmission, relaxation of smooth muscle, vasodilation and regulation of blood pressure, gene expression, defense mechanisms, cell function and regulation of inflammatory and immune mechanisms, as well as in pathological processes such as neurodegenerative disorders and heart diseases [14].
2.1.10. 일산화질소 (NO•)
일산화질소 (NO•), 이산화질소 (NO2•), 과산화질소 (ONOO−) 및 아질산 HNO2, N2O4 (이산화질소)와 같은 비라디칼은 반응성 질소 종 (RNS)이라는 총칭에 포함됩니다. (RNS)에 포함된다. 일산화질소 또는 질소 일산화물(NO•)은 단일 비결합 전자를 가진 자유 라디칼이다. NO•의 화학적 반응성은 상당히 제한적이며, 따라서 그 직접적인 독성은 ROS보다 낮다. 그러나 이는 O2•−와 반응하여 과산화질소 음이온(ONOO−)을 생성한다[55], 이는 단백질, 지질 및 DNA에 매우 유해한 물질이다[60]. 일산화질소는 또한 분자 산소 및 질소와 반응하여 이산화질소 또는 삼산화질소를 형성하는데, 이 둘 모두 독성 산화제 및 니트로화제이다 [55]. 일산화질소는 생물학적 조직 내에서 특정 일산화질소 합성효소 [61]에 의해, H2O2와 아르기닌의 반응 [62]을 통해, 또는 금속 이온 존재 하에서 S-니트로소 티올의 분해를 통해 생성된다 [63].
일산화질소는 물과 지방에 용해되므로 세포질과 세포막을 통해 쉽게 확산됩니다. 인체 혈장이 NO•에 노출되면 아스코르브산과 요산 농도가 감소하고 지질 과산화가 촉발된다[10]. 세포막과 지단백질 내 일산화질소 유래 물질은 지질 산화 과정에서 지방산 및 지질 과산화 라디칼과 신속히 반응하여 자유 지질과 에스테르화 콜레스테롤의 산화 및 질산화 생성물을 생성한다[64] . 일산화질소는 또한 신경 전달, 평활근 이완, 혈관 확장 및 혈압 조절, 유전자 발현, 방어 기전, 세포 기능, 염증 및 면역 기전 조절과 같은 많은 생리적 과정과 신경퇴행성 장애 및 심장 질환과 같은 병리학적 과정에도 관여한다 [14].
2.1.11. Nitrogen Dioxide (NO2•)
Unlike nitrous oxide (N2O), nitrogen dioxide (NO2•) can be considered a free radical because the electrons are not paired. It is formed by the reaction of the peroxyl radical and NO in polluted air and smoke [65]. Nitrogen dioxide is a moderately strong oxidant, with reactivity between those of NO• and ONOO− [10]. NO2• reacts with organic molecules at rates ranging from ~104 to 106 M/s, depending on pH [33]. Two NO2• radicals can be dimerized to the highly reactive dinitrogen tetroxide (N2O4). Nitrogen dioxide can affect antioxidant mechanisms, causing the oxidation of ascorbic acid, which leads to lipid peroxidation and free radical production [66].
2.1.12. Peroxynitrite (ONOO−)
Peroxynitrite (ONOO−) is formed by the reaction of nitric oxide and superoxide anion. It is highly toxic and can react directly with CO2 to form other highly reactive nitroso-peroxo-carboxylates (ONOOCO2−) or peroxynitrous acid (ONOOH), which may undergo further homolysis to form •OH and NO2• or rearrange to form NO3 [67]. Peroxynitrite diffuses readily across cell membranes [24]; it can oxidize lipids, methionine residues and tyrosine in proteins and DNA to nitroguanine [11,60]. It acts as an oxidant in a similar way to the hydroxyl radical [10]. Nitrotyrosine residues are considered markers of cell damage induced by peroxynitrite and have been associated with tissues aging [11,24]. Peroxynitrite causes tissue injury and oxidizes low-density lipoprotein (LDL); it seems to be generated at sites of inflammation [24,66].
2.1.11. 이산화질소 (NO2•)
일산화질소(N2O)와 달리 이산화질소(NO2•)는 전자가 짝을 이루지 않아 자유 라디칼로 간주될 수 있습니다. 이는 오염된 공기 및 연기 속에서 퍼옥실 라디칼과 NO의 반응을 통해 생성됩니다[65]. 이산화질소는 중간 정도의 강한 산화제로, 반응성은 NO•와 ONOO− 사이의 수준입니다[10]. NO2•는 pH에 따라 ~10⁴~10⁶ M/s 범위의 속도로 유기 분자와 반응한다 [33]. 두 개의 NO2• 라디칼은 고반응성 이산화질소(N2O4)로 이량화될 수 있다. 이산화질소는 항산화 기전에 영향을 미쳐 아스코르브산의 산화를 유발하며, 이는 지질 과산화 및 자유 라디칼 생성을 초래한다[66].
2.1.12. 과산화질산염(ONOO−)
과산화질소(ONOO−)는 일산화질소와 과산화물 음이온의 반응으로 생성된다. 이는 매우 독성이 강하며, 이산화탄소(CO2)와 직접 반응하여 다른 고반응성 질소-과산화-카복실산염(ONOOCO2−) 또는 과산화질소산(ONOOH)을 형성할 수 있다. 이 물질들은 추가적인 동분해(homolysis)를 통해 •OH와 NO2•를 생성하거나 재배열되어 NO3를 형성할 수 있다[67]. . 퍼옥시나이트라이트는 세포막을 쉽게 확산한다[24]; 지질, 메티오닌 잔기, 단백질 내 티로신 및 DNA를 산화시켜 니트로구아닌으로 전환시킬 수 있다[11,60]. 이는 하이드록실 라디칼과 유사한 방식으로 산화제로 작용한다[10]. 니트로티로신 잔기는 퍼옥시나이트라이트에 의해 유발된 세포 손상의 지표로 간주되며 조직 노화와 연관되어 있다 [11,24]. 퍼옥시나이트라이트는 조직 손상을 유발하고 저밀도 지단백질(LDL)을 산화시키며, 염증 부위에서 생성되는 것으로 보인다 [24,66].
2.1.13. Reactive Sulfur Species
Sulfur is very abundant in nature and in the human body, and it has been implicated in the origin of life [68]. Organic derivatives of sulfur can form thiols (−2), disulfides (−1), sulfenic acids or sulfoxides (0), sulfinic acid (+2) and sulfonic acids (+4). By analogy with ROS and RNS, these compounds are identified as reactive sulfur species (RSS) [16]. Thiols can generate free radicals. In the presence of traces of transition metal ions, thiol compounds are oxidized to thiyl radicals (RS•) and reactive oxygen species. Pro-oxidative action takes place by means of reduction of transition metals such as Fe3+ to Fe2+, leading to the formation of thiyl radicals and the generation of a superoxide radical anion. The biochemistry of thiols, hydrogen sulfide (H2S) and its sulfane sulfur derivatives enables roles in protein structure/folding, cell redox homeostasis, signaling, metal ligation, cell protection, enzymology, metabolism and mitochondrial function [69]. Humans and animals are continuously exposed to many exogenous thiols and related disulfides. Thiol compounds can be found in food, contaminants and products in which sulfur-containing substances are breaking down.
Hydrogen sulfide (H2S) is the hydrogenated sulfur compound with the lowest oxidation state (−2). It is slightly hydrophobic and soluble in lipid membranes, which it crosses rapidly, diffusing between compartments. H2S exerts many physiological activities with potential health benefits [68]. It is mostly synthesized enzymatically, but also non-enzymatically in mammalian tissues [70], and it is produced via different pathways, in mitochondria [71], the kidneys and the brain [72]. Hydrogen sulfide has traditionally been considered toxic to mammals because of its inhibitory effect on cytochrome c oxidase, interrupting oxidative phosphorylation [73]. Since the identification of nitric oxide (NO) and carbon monoxide (CO) as gasotransmitters, H2S has been recognized as the third gasotransmitter [69]. Similar to NO and CO, H2S was considered to regulate various physiological and pathological processes.
Recently, the biological action and signaling of hydrogen sulfide [68] have stimulated interest in species related to H2S and/or as possible mediators/biological effectors derived from it. The biological effects mediated by H2S have mainly been attributed to the persulfidation of proteins, as shown by its vasorelaxant effect mediated by the activation of ATP-sensitive K+ [74]. H2S also blocks the generation of mitochondrial ROS through the induction of p66Shc persulfidation [75] and reduces the advanced toxicity of glycation end products through persulfidation of their receptor [76]. It is involved in inflammatory processes [77], inhibiting leukocyte adherence [78] and in carcinogenesis [79]. Polysulfides protect neurons from oxidative stress through the activation of the Keap1/Nrf2 (Kelch-like ECH associated protein 1/transcription nuclear factor erythroid 2-related factor 2) system and also induce neurite growth [80]. H2S appears to inhibit atherogenesis and platelet aggregation [81], and it has been shown to protect against ischemia-reperfusion damage by the preservation of mitochondrial function [82]. It is stressed that, in biological systems, sulfur species, such as hydrogen sulfide, disulfides, hydropersulfides, dialkyltrisulfides and thiols, are all in dynamic equilibrium [83]. Hydropersulfide, not H2S, has been proposed as a new product of interest in signaling research; in many cases, H2S could be a marker of its presence [84].
2.1.13. 반응성 황 종
황은 자연계와 인체에 매우 풍부하며, 생명 기원과 연관성이 제기되어 왔다[68]. 황의 유기 유도체는 티올(-2), 이황화물(-1), 설펜산 또는 설폭사이드(0), 설핀산(+2), 설폰산(+4)을 형성할 수 있다. ROS 및 RNS와 유사하게, 이러한 화합물들은 반응성 황 종(RSS)으로 분류된다[16]. 티올은 자유 라디칼을 생성할 수 있다. 미량의 전이 금속 이온이 존재할 경우, 티올 화합물은 티일 라디칼 (RS•) 및 활성산소종으로 산화된다. 촉진산화 작용은 Fe3+와 같은 전이 금속을 Fe2+로 환원시켜 티일 라디칼을 형성하고 과산화물 라디칼 음이온을 생성함으로써 발생한다. 티올, 황화수소(H₂S) 및 그 황화수소 유도체의 생화학은 단백질 구조/접힘, 세포 산화환원 평형, 신호전달, 금속 결합, 세포 보호, 효소학, 대사 및 미토콘드리아 기능에 기여한다[69]. 인간과 동물은 지속적으로 다양한 외인성 티올 및 관련 이황화물(disulfide)에 노출된다. 티올 화합물은 식품, 오염물질 및 황 함유 물질이 분해되는 제품에서 발견된다.
황화수소(H2S)는 산화 상태가 가장 낮은(-2) 수소화 황 화합물이다. 약간의 소수성을 가지며 지질 막에 용해되어 빠르게 막을 통과하여 구획 간에 확산됩니다. H2S는 잠재적인 건강상의 이점을 가진 여러 생리학적 활동을 발휘합니다 [68]. 주로 효소적으로 합성되지만 포유류 조직에서는 비효소적으로도 생성되며[70], 미토콘드리아[71], 신장 및 뇌[72]에서 서로 다른 경로를 통해 생산됩니다. 황화수소는 시토크롬 c 산화효소에 대한 억제 효과로 인해 산화적 인산화 과정을 방해한다는 점에서 전통적으로 포유류에 독성 물질로 간주되어 왔습니다[73] 일산화질소(NO)와 일산화탄소(CO)가 가스전달물질로 확인된 이후, H2S는 세 번째 가스전달물질로 인정받게 되었다[69]. NO 및 CO와 유사하게, H2S는 다양한 생리적 및 병리적 과정을 조절하는 것으로 여겨졌다.
최근 황화수소의 생물학적 작용과 신호전달[68]에 대한 연구가 활발해지면서, H2S 관련 종 및/또는 H2S에서 유래된 잠재적 매개체/생물학적 효과자에 대한 관심이 높아졌다. H2S가 매개하는 생물학적 효과는 주로 단백질의 과황화 작용에 기인하는 것으로 알려져 있으며, 이는 ATP-민감성 K+ 채널 활성화에 의한 혈관 이완 효과[74]에서 확인할 수 있다. H2S는 또한 p66Shc 과황화 유도[75]를 통해 미토콘드리아 ROS 생성을 차단하고, 수용체 과황화를 통해 당화 최종 생성물의 고급 독성을 감소시킵니다 [76]. H2S는 염증 과정[77], 백혈구 부착 억제[78], 발암 과정[79]에도 관여한다. 폴리설파이드(Polysulfides)는 Keap1/Nrf2(Kelch-like ECH associated protein 1/transcription nuclear factor erythroid 2-related factor 2) 시스템 활성화를 통해 뉴런을 산화 스트레스로부터 보호하며, 신경돌기 성장도 유도한다[80]. H2S는 동맥경화증 발생과 혈소판 응집을 억제하는 것으로 보이며[81], 미토콘드리아 기능 보존을 통해 허혈-재관류 손상으로부터 보호하는 것으로 입증되었다[82]. 생물학적 시스템에서 황화수소, 이황화물, 하이드로퍼설파이드, 디알킬트리설파이드, 티올과 같은 황 화합물들은 모두 역동적 평형 상태에 있다는 점이 강조된다[83]. 신호 전달 연구에서 관심의 새로운 생성물로 H2S가 아닌 하이드로퍼설파이드가 제안되었으며, 많은 경우 H2S는 그 존재의 지표가 될 수 있다 [84].
2.2. Generation of Free Radicals
Radicals can be formed by mechanisms other than the addition of a single electron to a non-radical. They can form by homolytic fission, when a covalent bond (C–C, C–H or C–O) is broken and one electron from the bonding pair remains on each atom. These covalent bonds are difficult to break; others are more easily broken, such as disrupted disulfide bonds that generate sulfur radicals [85], whereas the O–O bond in H2O2 is divided by exposing it to ultraviolet light, generating •OH. Sources of free radicals may be endogenous or exogenous (Figure 1). Endogenous sources, generated during normal metabolism, include different cell organelles, such as mitochondria, peroxisomes and endoplasmic reticulum, many enzyme activities, fatty acid metabolism and phagocytic cells [86]. Exogenous sources include radiation X-rays, γ-rays, ultraviolet A, visible light in the presence of a sensitizer, chemical reagents such as heavy or transition metals (e.g., Cd, Hg, Pb, As, metal ions such as Fe2+ and Cu+), HONOO, ozone, N2O2, deoxyosones, ketamine, H2O2, HOCl and HOBr, cooking (smoked meat, used cooking oil), high temperatures, environmental pollutants (aromatic hydrocarbons, pesticides, polychlorinated biphenyls, dioxins and many others), microbial infections, drugs and their metabolites [9,28,87].
2.2. 자유 라디칼 생성
라디칼은 비라디칼에 단일 전자가 첨가되는 메커니즘 외에도 생성될 수 있다. 공유 결합(C–C, C–H 또는 C–O)이 끊어지고 결합 쌍의 전자가 각 원자에 하나씩 남는 동해성 분열을 통해 형성될 수 있다. 이러한 공유 결합은 끊기 어렵지만, 다른 결합은 더 쉽게 끊어집니다. 예를 들어, 이황화 결합이 끊어지면 황 라디칼이 생성됩니다[85]. 반면 H2O2의 O–O 결합은 자외선에 노출되어 분해되며, 이 과정에서 •OH가 생성됩니다. 자유 라디칼의 발생원은 내인성 또는 외인성일 수 있다(그림 1). 정상 대사 과정에서 생성되는 내인성 발생원에는 미토콘드리아, 퍼옥시좀, 소포체 등 다양한 세포 소기관, 다수의 효소 활성, 지방산 대사, 식세포성 세포 등이 포함된다 [86]. 외인성 원천에는 방사선(X선, γ선, 자외선 A), 감광제 존재 하의 가시광선, 중금속 또는 전이 금속(예: Cd, Hg, Pb, As, Fe2+ 및 Cu+와 같은 금속 이온)과 같은 화학 시약, HONOO, 오존, N2O2, 데옥시오손, 케타민, H2O2, HOCl 및 HOBr, 조리 과정(훈제육, 사용된 조리유), 고온, 환경 오염물질(방향족 탄화수소, 농약, 폴리염화비페닐, 다이옥신 등 다수), 미생물 감염, 약물 및 그 대사산물 등이 있다[9,28,87].
Figure 1. Source of free radicals generation. Either endogenous or exogenous sources generate ROS (O2•−, superoxide anion; •OH, hydroxyl; HO2•, hydroperoxyl; H2O2, hydrogen peroxide; RO2, peroxyl; HOCl, hypochlorous acid); RNS (NO•, nitric oxide; NO2•, nitrogen dioxide; ONOO−, peroxynitrite; HNO2, nitrous acid; RONOO, alkylperoxynitrates; N2O3, dinitrogen trioxide). Endogenous free radicals are produced by the activation of immune cells (eosinophils, neutrophils, etc.) to fight bacteria and other invaders, by the mitochondrial respiratory chain, by enzymatic activity (xanthin oxidase, NADPH oxidase, lipo-oxygenase, NO synthase, etc.) and by various pathological disorders and diseases. Exogenous free radicals arise from air and water pollution, cigarette smoke, heavy metals or transition, drugs, industrial solvents, radiation and high temperatures.
그림 1. 자유 라디칼 생성원. 내인성 또는 외인성 원천은 ROS(O2•−, 과산화수소 음이온; •OH, 하이드록실; HO2•, 하이드로퍼옥실; H2O2, 과산화수소; RO2, 퍼옥실; HOCl, 차아염소산)를 생성합니다; 반응성 질소 종(RNS: NO•, 일산화질소; NO2•, 이산화질소; ONOO−, 과산화질소; HNO2, 아질산; RONOO, 알킬과산화질소; N2O3, 삼산화이질소)). 내인성 자유 라디칼은 세균 및 기타 침입자와 싸우기 위한 면역 세포(호산구, 호중구 등)의 활성화, 미토콘드리아 호흡 사슬, 효소 활성(잔틴 산화효소, NADPH 산화효소, 리포옥시게나제, NO 합성효소 등) 및 다양한 병리학적 장애와 질병에 의해 생성됩니다. 외인성 자유 라디칼은 대기 및 수질 오염, 담배 연기, 중금속 또는 전이 금속, 약물, 산업용 용제, 방사선 및 고온에서 발생합니다.

2.2.1. Mitochondria
All the cells of the human body rely on adenosine triphosphate (ATP) to store and transport chemical energy. The body uses molecular oxygen to produce energy via oxidative phosphorylation in mitochondria. Mitochondria generate more than 90% of ATP by oxidative phosphorylation [88], consuming about 85% of the oxygen requirements of the cell to do so. Most of the oxygen is reduced to water, and a small proportion is converted to free radicals. The phosphorylation unit combines oxygen and hydrogen to produce H2O and ATP molecules. The oxidative unit consists mainly of a series of protein complexes in the inner mitochondrial membrane (IMM), known as the respiratory or electron transfer chain (ETC). Hydrogen atoms are known as reducing equivalents. The passage of hydrogen atoms along the respiratory chain is equivalent to the passage of electrons through sequential redox reactions along protein complexes I-IV of the ETC [89], where O2 is reduced to H2O. The production of ATP by oxidative phosphorylation associated with the ETC has an energy loss in the form of electrons [90], which determines the production of free radicals. In eukaryotic organisms, over 90% of ROS are produced by the mitochondrial ETC as a by-product of respiration [91]. A quantity of ROS are also produced by the ETC in the plasma [92], nuclear [93] and endoplasmic reticulum [94] membranes.
Reactive oxygen species generated as by-products of mitochondrial electron transfer mainly include the superoxide radical anion and hydrogen peroxide. A multielectron reduction of O2 is carried out by protein complexes in the ETC. By virtue of its electron configuration (two unpaired electrons in the outer shell), the oxygen molecule is not very reactive [41] and consequently tends to accept electrons one at a time. If O2 accepts a single electron, the electron must enter an antibonding orbital, producing the superoxide radical O2•−. A two-electron reduction of O2, with the addition of 2H+, generates hydrogen peroxide (H2O2). A one-electron reduction of H2O2 forms a hydroxyl radical (HO•) and a hydroxyl anion HO−. Water is formed after the electron and proton addition to HO•. Although the ETC is a highly efficient system, the redox reactions predispose electron vectors to reactions with molecular oxygen. Thus, up to 2% of electrons leak along the ETC and react directly with oxygen in a one-electron reduction to produce a superoxide (radical anion) instead of a water molecule [95]. About 5% of the oxygen consumed by living organisms can be converted to O2•− by mitochondria under physiological conditions [87]. The production of O2•− in mitochondria is estimated to be approximately 2 to 3 nmol/min per mg of protein [20], confirming its importance as the main source of this radical in living organisms.
Mitochondria are the most significant intracellular source of O2•−. An O2•− concentration 5 to 10 times greater has been estimated in mitochondria than in the nuclear space or the cytosol [91]. Ubiquinone links complex I with III and II with III and is regarded as a major player in the formation of O2•−. The oxidation of ubiquinone proceeds in a set of reactions known as the Q-cycle, and the unstable semiquinone is responsible for O2•− formation [44]. The transfer of electrons from complex I or II dehydrogenase to coenzyme Q or ubiquinone (Q) leads to the formation of a reduced form of coenzyme Q (QH2) that regenerates coenzyme Q via an unstable intermediate semiquinone anion Q•−. The latter transfers electrons to molecular oxygen, leading to the formation of superoxide radical [44]. Since the generation of superoxide is not enzymic, most ROS production will be linked to the higher metabolic rate.
Additionally, mitochondrial superoxide is generated by electron-transfer during fatty acid oxidation, by glycerol-3-phosphate dehydrogenase and other IMM-associated oxidoreductases [96]. The superoxide anion (O2•−) serves as a ROS precursor. Most O2•− is readily metabolized to non-radical H2O2 by superoxide dismutase (SOD) or non-enzyme mechanisms [97]. The subsequent Haber–Weiss reaction of H2O2 and O2•− [98], or Fe2+- (or Cu2+)-driven Fenton cleavage of H2O2 [99], may generate the highly reactive hydroxyl radical (•OH).
The H2O2 produced is in its optimum state for respiration, characterized by a high degree of reduction of the electron carriers and a limiting supply of adenosine diphosphate (ADP) [100]. An additional source of H2O2, not related to breathing, is situated on the external mitochondrial membrane [101], where the oxidative deamination of biogenic amines by monoamine oxidases is associated with the direct two-electron reduction of O2 to H2O2. The hydrogen peroxide produced during the oxidative deamination of catecholamines may be involved in neurodegenerative disorders such as Parkinson’s and Alzheimer’s diseases, presumably through oxidative damage to the mitochondrial membrane [102]. The factors that control the ETC generation of ROS in vivo are not fully understood. Antioxidant enzymes can eliminate ROS. SODs convert O2•− to H2O2, and many enzymes, such as catalase, glutathione peroxidase and peroxiredoxin 3, remove H2O2 [19]. Moreover, the signaling capacity of ROS may be altered by mitochondrial localization. Since ROS are molecules of short duration, the location of their production or signaling site can increase their efficiency.
Conventionally, complex I and complex III, including complex II, are considered the major contributors to ROS production [103]. However, the relative contribution of each site to the total production of O2•− and H2O2 varies from one organ to another and depends on respiration rate and redox state [19,44]. The different sites of ROS production have distinct signaling roles and presumably change under different physiological conditions [103]. It is therefore difficult to pinpoint the specific site of ROS production [104]. Up to eleven distinct mitochondrial sites of production of superoxide and/or hydrogen peroxide linked to substrate catabolism, electron transport and oxidative phosphorylation were recently identified in mammalian mitochondria [19,104]. Sites I [105] and III [44] are considered to generate predominantly or exclusively superoxide. Site II may generate both superoxide and hydrogen peroxide [103]. These sites may also act as sources of mitochondrial redox signal. H2O2 is the primary form of ROS utilized for intracellular signaling. Individual sites of ROS production are implicated in specific pathologies. Parkinson’s disease and longevity are linked to superoxide production from the flavin- and ubiquinone (Q)-binding sites of respiratory complex I [106], ROS from the complex II flavin is linked to Huntington’s disease and cancer [107,108] and ROS from complexes I, II and III and from mitochondrial glycerol phosphate dehydrogenase and matrix dehydrogenases are all invoked in ischemia/reperfusion injury [109,110].
Since most ATP is produced by mitochondria, impaired mitochondrial function is implicated in a variety of health chronic conditions and degenerative diseases [111], many of which can be attributed to excessive mitochondrial production of ROS. However, modest levels of ROS stimulate essential biological processes, such as proliferation, differentiation and immunity [112]. Furthermore, mitohormesis [113], a decrease in the net basal metabolism production of ROS, which increases resistance to oxidative stress [112], may be a way to improve mitochondrial function and resistance to chronic and degenerative diseases. Mitohormesis, a defense mechanism, can therefore promote health and increase longevity through the prevention or delay of diseases [113,114].
2.2.1. 미토콘드리아
인체의 모든 세포는 화학 에너지를 저장하고 운반하기 위해 아데노신 삼인산(ATP)에 의존합니다. 신체는 미토콘드리아에서 산화적 인산화 과정을 통해 분자 산소를 이용해 에너지를 생산합니다. 미토콘드리아는 산화적 인산화 작용을 통해 ATP의 90% 이상을 생성하며[88], 이를 위해 세포 산소 요구량의 약 85%를 소비합니다. 대부분의 산소는 물로 환원되고, 소량은 자유 라디칼로 전환됩니다. 인산화 단위는 산소와 수소를 결합하여 H2O와 ATP 분자를 생성합니다. 산화 단위는 주로 미토콘드리아 내막(IMM)에 위치한 일련의 단백질 복합체로 구성되며, 호흡 사슬 또는 전자 전달 사슬(ETC)로 알려져 있습니다. 수소 원자는 환원 등가체로 알려져 있습니다. 호흡 사슬을 따라 수소 원자가 이동하는 것은 ETC의 단백질 복합체 I-IV를 따라 연속적인 산화 환원 반응을 통해 전자가 이동하는 것과 동일합니다[89], 여기서 O2는 H2O로 환원됩니다. ETC와 연관된 산화적 인산화 작용에 의한 ATP 생산은 전자의 형태로 에너지 손실을 동반하며[90], 이는 자유 라디칼 생성을 결정한다. 진핵생물에서 ROS의 90% 이상은 호흡의 부산물로 미토콘드리아 ETC에 의해 생성된다[91]. 일부 ROS는 혈장[92], 핵[93], 소포체[94] 막의 ETC에서도 생성된다.
미토콘드리아 전자 전달의 부산물로 생성되는 활성산소는 주로 슈퍼옥사이드 라디칼 음이온과 과산화수소를 포함한다. O2의 다전자 환원은 ETC 내 단백질 복합체에 의해 수행된다. 산소 분자는 전자 구성(외각 껍질에 두 개의 짝을 이루지 않은 전자)으로 인해 반응성이 높지 않아[41] 일반적으로 전자를 하나씩 받아들이는 경향이 있다. O2가 단일 전자를 받아들이면, 전자는 반결합 궤도에 들어가야 하며, 이로 인해 슈퍼옥사이드 라디칼 O2•−이 생성된다. 2H+의 첨가와 함께 O2의 2전자 환원 반응은 과산화수소(H2O2)를 생성한다. H2O2의 1전자 환원 반응은 하이드록실 라디칼(HO•)과 하이드록실 음이온 HO−을 형성한다. HO•에 전자와 양성자가 첨가된 후 물이 생성된다. ETC는 매우 효율적인 시스템이지만, 산화환원 반응은 전자 전달체들이 분자 산소와 반응하도록 유도한다. 따라서 최대 2%의 전자가 ETC를 따라 누출되어 산소와 직접 반응하여 1전자 환원 과정을 거쳐 물 분자가 아닌 과산화물(라디칼 음이온)을 생성한다 [95]. 생물체가 소비하는 산소의 약 5%는 생리적 조건에서 미토콘드리아에 의해 O2•−로 전환될 수 있다[87]. 미토콘드리아 내 O2•− 생성량은 단백질 1mg당 분당 약 2~3 nmol로 추정되며[20], 이는 생물체 내 이 라디칼의 주요 공급원으로서 그 중요성을 입증한다.
미토콘드리아는 세포 내 O2•−의 가장 중요한 공급원이다. 미토콘드리아 내 O2•− 농도는 핵 공간이나 세포질보다 5~10배 높은 것으로 추정된다[91]. 유비퀴논은 복합체 I과 III, II와 III를 연결하며 O2•− 형성의 주요 매개체로 간주된다. 유비퀴논의 산화는 Q-사이클로 알려진 일련의 반응을 통해 진행되며, 불안정한 세미퀴논이 O2•− 형성에 관여한다 [44]. 복합체 I 또는 II 탈수소효소에서 코엔자임 Q 또는 유비퀴논(Q)으로의 전자 전달은 환원형 코엔자임 Q(QH2)의 생성을 초래하며, 이는 불안정한 중간체 세미퀴논 음이온 Q•−를 통해 코엔자임 Q를 재생성한다. 후자는 분자 산소로 전자를 전달하여 슈퍼옥사이드 라디칼의 생성을 유발한다 [44]. 과산화수소 생성은 비효소적 과정이므로, 대부분의 활성산소종(ROS) 생산은 높은 대사율과 연관된다.
또한 미토콘드리아 과산화수소는 지방산 산화 과정 중 전자 전달, 글리세롤-3-인산 탈수소효소 및 기타 내막 관련 산화환원효소에 의해 생성된다 [96]. 슈퍼옥사이드 음이온(O2•−)은 ROS 전구체 역할을 한다. 대부분의 O2•−는 슈퍼옥사이드 디스뮤타제(SOD) 또는 비효소적 기전에 의해 비라디칼인 H2O2로 쉽게 대사된다 [97]. 이후 H2O2와 O2•− 사이의 하버-바이스 반응[98], 또는 Fe2+(또는 Cu2+)에 의해 촉진되는 H2O2의 펜튼 분해[99]를 통해 고반응성 하이드록실 라디칼(•OH)이 생성될 수 있다 .
생성된 H2O2는 호흡에 최적화된 상태로, 전자 운반체의 높은 환원도와 아데노신 이인산(ADP)의 제한적 공급이 특징이다[100]. 호흡과 무관한 추가적인 H2O2 공급원은 미토콘드리아 외막에 위치한다[101]. 여기서 모노아민 산화효소에 의한 생체 아민의 산화적 탈아미노화는 O2의 직접적인 2전자 환원을 통해 H2O2로 전환된다. 카테콜아민의 산화적 탈아미노화 과정에서 생성된 과산화수소는 미토콘드리아 막에 대한 산화적 손상을 통해 파킨슨병 및 알츠하이머병과 같은 신경퇴행성 질환에 관여할 수 있다[102]. 생체 내에서 전자전달계(ETC)에 의한 활성산소종(ROS) 생성을 조절하는 요인들은 완전히 이해되지 않았다. 항산화 효소들은 ROS를 제거할 수 있다. SOD는 O2•−를 H2O2로 전환하며, 카탈라제, 글루타티온 퍼옥시다제, 퍼옥시레독신 3과 같은 여러 효소가 H2O2를 제거한다[19]. 또한 ROS의 신호 전달 능력은 미토콘드리아 국소화에 의해 변화될 수 있다. ROS는 수명이 짧은 분자이므로, 생성 위치나 신호 전달 부위가 효율성을 높일 수 있다.
전통적으로 복합체 I과 복합체 III(복합체 II 포함)이 ROS 생성의 주요 기여자로 간주된다[103]. 그러나 O2•− 및 H2O2 총생성에 대한 각 부위의 상대적 기여도는 장기마다 다르며 호흡 속도와 산화환원 상태에 따라 달라진다[19,44]. ROS 생성 부위마다 신호 전달 역할이 다르며, 다양한 생리학적 조건에 따라 변화할 것으로 추정됩니다[103]. 따라서 ROS 생성의 특정 부위를 정확히 규명하기는 어렵습니다[104]. 최근 포유류 미토콘드리아에서 기질 분해, 전자 전달, 산화적 인산화와 연관된 11개 이상의 상이한 미토콘드리아 슈퍼옥사이드 및/또는 과산화수소 생성 부위가 확인되었습니다[19,104]. 사이트 I [105]과 III [44]은 주로 또는 독점적으로 슈퍼옥사이드를 생성하는 것으로 간주됩니다. 사이트 II는 슈퍼옥사이드와 과산화수소 모두를 생성할 수 있습니다 [103]. 이러한 사이트들은 미토콘드리아 산화환원 신호의 원천으로도 작용할 수 있습니다. H2O2는 세포 내 신호 전달에 활용되는 주요 ROS 형태입니다. 개별 ROS 생성 사이트들은 특정 병리학적 상태와 연관되어 있습니다. 파킨슨병과 장수는 호흡 복합체 I의 플라빈 및 유비퀴논(Q) 결합 부위에서 발생하는 슈퍼옥사이드 생성과 연관되어 있다[106]. 복합체 II 플라빈에서 발생하는 ROS는 헌팅턴병 및 암과 연관되어 있다[107,108]. 복합체 I, II, III 및 미토콘드리아 글리세롤 인산 탈수소효소와 매트릭스 탈수소효소에서 발생하는 ROS는 모두 허혈/재관류 손상과 관련이 있다 [109,110].
대부분의 ATP가 미토콘드리아에서 생성되므로, 미토콘드리아 기능 장애는 다양한 만성 건강 상태 및 퇴행성 질환[111]과 연관되며, 이 중 상당수는 미토콘드리아의 과도한 ROS 생산에 기인할 수 있습니다. 그러나 적정 수준의 ROS는 증식, 분화, 면역과 같은 필수 생물학적 과정을 자극합니다[112]. 또한 미토호르메시스[113]는 기초 대사 과정에서 생성되는 ROS의 순 생산량을 감소시켜 산화 스트레스에 대한 저항성을 높이는 현상[112]으로, 미토콘드리아 기능과 만성 및 퇴행성 질환에 대한 저항성을 향상시키는 방법이 될 수 있다. 따라서 방어 기제인 미토호르메시스는 질병의 예방 또는 지연을 통해 건강 증진과 수명 연장을 촉진할 수 있다[113,114].
2.2.2. Peroxisomes
In peroxisomes, the respiratory pathway involves the transfer of electrons from various metabolites to oxygen, leading to the formation of H2O2 with the release of free energy in the form of heat [115]. It is not coupled to the production of ATP by oxidative phosphorylation [116]. Other free radicals produced in peroxisomes include O2•−, •OH and NO•. β-oxidation of fatty acids is the main metabolic process producing H2O2 in peroxisomes. However, different peroxisomal enzymes, such as acyl CoA oxidase, d-amino acid oxidase, L-a-hydroxy oxidase, urate oxidase, xanthine oxidase and D-aspartate oxidase, have been shown to produce different ROS [117]. Peroxisome and β-oxidation alterations are involved in many conditions and diseases, such as neurological disorders, and in the development of cancer [118].
2.2.3. Endoplasmic Reticulum
The electron transport chain of the endoplasmic reticulum is the second greatest source of ROS [94]. Catabolism of cell and foreign chemicals by cytochrome P450 includes redox steps and is responsible for the production of ROS in the endoplasmic reticulum. The enzymes of the endoplasmic reticulum that contribute to the formation of ROS include cytochrome P450, b5 enzymes and diamine oxidase [119]. Another important thiol oxidase, Erop1p, catalyzes the transfer of electrons from dithiols to molecular oxygen, resulting in the formation of H2O2 [120]. Other endogenous sources of ROS include the auto-oxidation of adrenalin, reduced riboflavin, inflammation, mental stress, over-exertion, infection, cancer, aging and ischemia [119].
2.2.2. 퍼옥시좀
퍼옥시좀에서 호흡 경로는 다양한 대사 산물로부터 산소로의 전자 전달을 포함하며, 이는 열 형태의 자유 에너지 방출과 함께 H2O2의 생성을 초래한다[115]. 이는 산화적 인산화(oxidation phosphorylation)에 의한 ATP 생산과 결합되지 않는다[116]. 퍼옥시좀에서 생성되는 다른 자유 라디칼로는 O2•−, •OH 및 NO•가 있다. 지방산의 β-산화는 퍼옥시좀에서 H2O2를 생성하는 주요 대사 과정이다. 그러나 아실 CoA 산화효소, d-아미노산 산화효소, L-α-하이드록시 산화효소, 요산 산화효소, 크산틴 산화효소, D-아스파르트산 산화효소와 같은 다양한 과산화소체 효소들이 서로 다른 활성산소종(ROS)을 생성하는 것으로 밝혀졌다[117]. 과산화소체 및 β-산화 과정의 이상은 신경계 장애와 같은 다양한 상태 및 질환과 암 발생에 관여한다[118].
2.2.3. 소포체
소포체의 전자 전달계는 두 번째로 큰 ROS 발생원이다[94]. 시토크롬 P450에 의한 세포 및 외부 화학물질의 이화작용은 산화환원 단계를 포함하며, 소포체 내 ROS 생성의 원인이 된다. ROS 형성에 기여하는 소포체 효소로는 시토크롬 P450, b5 효소 및 디아민 산화효소가 있다[119]. 또 다른 중요한 티올 산화효소인 Erop1p는 디티올에서 분자 산소로의 전자 전달을 촉매하여 H2O2를 생성한다[120]. ROS의 다른 내인성 원천으로는 아드레날린의 자가산화, 환원 리보플라빈, 염증, 정신적 스트레스, 과도한 운동, 감염, 암, 노화 및 허혈 등이 있다[119].
2.2.4. Role of the Enzyme System
A variety of oxidative enzymes that occur in cells can produce free radicals. Those catalyzing ROS generation include nitric oxide synthases, NADPH oxidase, prostaglandin synthase, xanthine oxidase, lipoxygenases, ribonucleotide reductase, glucose oxidase, myeloperoxidase, cyclooxygenases and cytochrome P450 [28]. A certain quantity of ROS is produced by various oxidases. For example, xanthine oxidase and cytochrome P450 reductase mainly produce the superoxide anion radical, while oxidases of amino acids and glucose mainly generate hydrogen peroxide [121]. In particular, under normal physiologic conditions, xanthine oxidase acts as a dehydrogenase, removing hydrogen from xanthine or hypoxanthine and binding it to nicotinamide adenine dinucleotide (NAD), thus generating the NADH.
Lipoxygenase generates free radicals; it can convert PUFA to hydroperoxides once Fe2+ has been oxidized to Fe3+ [122]. The three major mammalian lipoxygenases are 5-, 12-, and 15-lipoxygenase; they can oxidize arachidonic acid, abundant in the central nervous system, to hydroperoxyeicosatetraenoic acid. In addition, 15-lipoxygenase has been identified in atherosclerotic lesions, suggesting that the enzyme may be involved in the formation of oxidized lipids in vivo [24].
High ROS levels are also generated by immune cells (lymphocytes, granulocytes and phagocytes) which defend the body against invading microorganisms [123]. Macrophages and neutrophils contain NADPH oxidase complex, which, when activated, generates superoxide radicals and hydrogen peroxide. The latter then interacts with intracellular chloride ions to produce hypochlorite, which destroys the pathogen. Patients with chronic granulomatous disease, in which ROS production is drastically reduced by NADPH oxidase complex, are highly sensitive to infections and usually die at an early age [124]. The main enzyme expressed by neutrophils is myeloperoxidase. With heme as a cofactor, it produces hypochlorous acid from hydrogen peroxide and chloride anion [125]. It also oxidizes tyrosine to the tyrosine radical. Hypochlorous acid and the tyrosine radical are both cytotoxic and are used by neutrophils to kill pathogenic organisms [126].
Cytochrome P450 molecules use O2 in their biochemical reactions and generate small amounts of ROS. The amount of ROS produced varies depending on the compound degraded and the cytochrome P450 molecule involved. A molecule particularly active in the production of ROS is cytochrome P450 2E1 [127].
2.2.4. 효소 시스템의 역할
세포 내 다양한 산화 효소들은 자유 라디칼을 생성할 수 있다. ROS 생성을 촉매하는 효소로는 일산화질소 합성효소, NADPH 산화효소, 프로스타글란딘 합성효소, 크산틴 산화효소, 리폭시게나제, 리보뉴클레오티드 환원효소, 포도당 산화효소, 골수과산화효소, 사이클로옥시게나제 및 시토크롬 P450 등이 있다[28] . 다양한 산화효소에 의해 일정량의 ROS가 생성된다. 예를 들어, 크산틴 산화효소와 시토크롬 P450 환원효소는 주로 슈퍼옥사이드 음이온 라디칼을 생성하는 반면, 아미노산 및 포도당의 산화효소는 주로 과산화수소를 생성한다 [121]. 특히 정상 생리 조건에서 크산틴 산화효소는 탈수소효소 역할을 하여 크산틴 또는 하이포크산틴으로부터 수소를 제거하고 이를 니코틴아미드 아데닌 디뉴클레오타이드(NAD)에 결합시켜 NADH를 생성한다.
리폭시게나제는 자유 라디칼을 생성하며, 철(II)이온(Fe2+)이 철(III)이온(Fe3+)으로 산화되면 다불포화지방산(PUFA)을 과산화수소로 전환시킬 수 있다[122]. 포유류의 주요 리폭시게나제 3종은 5-, 12-, 15-리폭시게나제이며, 이들은 중추신경계에 풍부한 아라키돈산을 과산화 에이코사테트라엔산으로 산화시킬 수 있다. 또한 15-리폭시게나제는 죽상경화성 병변에서 확인되어, 이 효소가 생체 내 산화 지질 형성에 관여할 수 있음을 시사한다 [24].
침입 미생물로부터 신체를 방어하는 면역 세포(림프구, 과립구 및 식세포)에서도 높은 수준의 활성산소가 생성된다[123]. 대식세포와 호중구는 NADPH 산화효소 복합체를 포함하며, 활성화 시 슈퍼옥사이드 라디칼과 과산화수소를 생성한다. 후자는 세포 내 염화물 이온과 반응하여 병원체를 파괴하는 차아염소산을 생성한다. 만성 육아종성 질환 환자는 NADPH 산화효소 복합체에 의해 ROS 생성이 극적으로 감소되어 감염에 매우 취약하며 대개 조기에 사망한다 [124]. 호중구가 주로 발현하는 효소는 골수과산화효소이다. 이 효소는 헤모를 보조인자로 사용하여 과산화수소와 염화물 음이온으로부터 차아염소산을 생성한다 [125]. 또한 티로신을 티로신 라디칼로 산화시킵니다. 차아염소산과 티로신 라디칼은 모두 세포독성이 있으며, 호중구가 병원성 유기체를 사멸시키는 데 사용됩니다 [126].
시토크롬 P450 분자는 생화학적 반응에서 O2를 사용하며 소량의 ROS를 생성한다. 생성되는 ROS의 양은 분해되는 화합물과 관련된 시토크롬 P450 분자에 따라 달라진다. ROS 생성에서 특히 활발한 분자는 시토크롬 P450 2E1이다 [127].
2.2.5. Role of Metals
The production of free radicals through reactions mediated by transition metals is well established [10,27]. Almost all transition metal ions have the ability to function in various oxidation states. In the active redox state, these ions may act as catalysts in the autoxidation of many biomolecules. In most cases, the oxidation of biomolecules is initiated by the hydroxyl radical (HO•) generated in Fenton and Fenton-like reactions between redox-active transition metal ions and hydrogen peroxide [128]. In biological systems, a two-step reaction may occur in the presence of metal ions, especially free iron, more important because of its abundance in biological material, or copper, leading to the production of hydroxyl radicals. Hydrogen peroxide can produce the hydroxyl radical by removing an electron from the participating metal ion [10]. In the second step, the superoxide radical is involved in regenerating the original metal ions, making them newly available for the reaction with hydrogen peroxide. The two chemical reactions support the role of metals such as iron and copper in creating oxidative stress and cell injury by ROS. Again, the redox state of the transition metal is more important for pro-oxidant activity than its concentration. The ferrous ion (Fe2+) is a stronger pro-oxidant than the ferric ion (Fe3+), which only shows pro-oxidant activity in the presence of a reducing agent, such as ascorbic acid [10]. The pro-oxidant activity of transition metals includes the decomposition of lipid hydroperoxides into free radicals capable of initiating or propagating lipid peroxidation [129]. The metals can decompose hydroperoxides to peroxyl and alkoxyl radicals and greatly accelerate lipid oxidation [66]. The ferric and ferrous ions can both be catalysts in the degradation of lipid hydroperoxides to hydroperoxide-derived free radicals, but the catalytic activity of the ferrous ion is superior to that of the ferric ion. Moreover, the alkoxy radical is more reactive in the abstraction of a labile hydrogen atom than the peroxyl radical [27]. Because of the fundamental contribution of iron to the formation of hydroxyl radicals, any increase in cell concentration of free iron promotes the generation of ROS and oxidative stress [130].
2.2.5. 금속의 역할
전이 금속이 매개하는 반응을 통한 자유 라디칼 생성은 잘 알려져 있다 [10,27]. 거의 모든 전이 금속 이온은 다양한 산화 상태에서 기능할 수 있다. 활성 산화환원 상태에서 이러한 이온들은 많은 생체 분자의 자동 산화 반응에서 촉매 역할을 할 수 있다. 대부분의 경우 생체 분자의 산화는 산화환원 활성 전이 금속 이온과 과산화수소 사이의 펜튼 및 펜튼 유사 반응에서 생성되는 하이드록실 라디칼(HO•)에 의해 시작된다 [128]. 생물학적 시스템에서는 금속 이온, 특히 생물학적 물질에 풍부하게 존재하는 자유 철 또는 구리가 존재할 때 2단계 반응이 발생할 수 있으며, 이는 하이드록실 라디칼 생성을 초래한다. 과산화수소는 참여 금속 이온으로부터 전자를 제거함으로써 하이드록실 라디칼을 생성할 수 있다 [10]. 두 번째 단계에서는 슈퍼옥사이드 라디칼이 원래 금속 이온을 재생하는 데 관여하여, 이들이 과산화수소와의 반응에 다시 활용될 수 있게 합니다. 이 두 화학 반응은 철과 구리 같은 금속이 ROS에 의한 산화 스트레스 및 세포 손상 생성에서 역할을 한다는 점을 뒷받침합니다. 다시 말해, 전이 금속의 산화환원 상태는 그 농도보다 산화 촉진 활성에 더 중요합니다. 2가 철 이온(Fe2+)은 3가 철 이온(Fe3+)보다 강력한 산화 촉진제이며, 3가 철 이온은 아스코르브산과 같은 환원제가 존재할 때만 산화 촉진 활성을 나타낸다[10]. 전이 금속의 산화 촉진 활성에는 지질 과산화물을 분해하여 지질 과산화 반응을 시작하거나 진행시킬 수 있는 자유 라디칼을 생성하는 과정이 포함된다[129]. 금속은 하이드로퍼옥사이드를 퍼옥실 및 알콕실 라디칼로 분해하여 지질 산화를 크게 촉진할 수 있다 [66]. 철(III) 이온과 철(II) 이온 모두 지질 과산화물을 과산화물 유래 자유 라디칼로 분해하는 촉매 역할을 할 수 있으나, 철(II) 이온의 촉매 활성은 철(III) 이온보다 우수하다. 또한 알콕실 라디칼은 과산화 라디칼보다 불안정한 수소 원자 추출 반응에서 더 반응성이 높다 [27]. 철이 하이드록실 라디칼 형성에 근본적으로 기여하기 때문에, 세포 내 자유 철 농도의 증가는 ROS 생성 및 산화 스트레스를 촉진한다 [130].
2.3. Detection of ROS and RNS
The formation of ROS and RNS can be monitored by a variety of procedures, including fluorometric and spectrophotometric methods, chemiluminescence and electron paramagnetic resonance [44]. Many of these methods are based on the redox properties of specific ROS or RNS and are therefore subject to artifacts caused by species of similar reactivity or by reactive intermediates produced by the probe itself [131]. Electron paramagnetic resonance (EPR) spectroscopy has been studied to measure ROS, RNS and their secondary products [132]. The method is very suitable for the direct detection of free radicals at concentrations up to 1 μM. Due to its low sensitivity, EPR can measure ROS directly in vivo. It differs from other methods by virtue of its unique ability to detect free radicals with short and long half-lives, and it can provide information on oxygen/nitrogen radicals and related processes. Since NO is a free diatomic radical, it can be detected directly by EPR, even in tumors [133].
2.3. ROS 및 RNS 검출
ROS 및 RNS의 형성은 형광측정법, 분광광도법, 화학발광법, 전자상자성공명법 등 다양한 방법으로 모니터링할 수 있다 [44]. 이러한 방법 중 상당수는 특정 ROS 또는 RNS의 산화환원 특성에 기반하므로, 유사 반응성을 가진 종이나 시약 자체에서 생성된 반응성 중간체에 의한 인공적 영향에 취약하다[131]. 전자상자성공명(EPR) 분광법은 ROS, RNS 및 그 2차 생성물 측정을 위해 연구되어 왔다[132]. 이 방법은 최대 1μM 농도까지 자유 라디칼을 직접 검출하는 데 매우 적합하다. 낮은 감도에도 불구하고, EPR은 생체 내에서 ROS를 직접 측정할 수 있다. 이 방법은 반감기가 짧은 자유 라디칼과 긴 자유 라디칼을 모두 감지할 수 있는 독특한 능력으로 다른 방법과 차별화되며, 산소/질소 라디칼 및 관련 과정에 대한 정보를 제공할 수 있다. NO는 자유 이원자 라디칼이므로, 종양 내에서도 EPR로 직접 검출될 수 있다[133].
2.4. Molecular Targets of Free Radicals
The term reactive is not always appropriate for radical species; hydrogen peroxide (H2O2), nitric oxide (NO•) and superoxide (O2•−) react promptly with some molecules, while the hydroxyl radical (•OH) reacts promptly with almost everything. Species such as peroxyl radicals (RO2•), nitrate radicals (NO3•), alkoxyl radicals (RO•), hypochlorous acid (HOCl), hypobromous acid (HOBr), carbonate (CO3•−), carbon dioxide radicals (CO2•−), nitrogen dioxide (NO2•−), peroxynitrite (ONOO−), nitrogen dioxide (NO2•) and ozone (O3) have intermediate reactivities [10]. Free radicals have several types of reactions and targets. Oxidative processes are chemical/biochemical reactions involving the transfer of one or more electrons from an electron donor (reducing agent) to an electron acceptor (oxidizing agent). In biological systems, most molecules are non-radicals. Thus, when a free radical reacts with a non-radical, it creates a new radical and can trigger a chain reaction. When two free radicals meet, their unpaired electrons can unite to form a covalent bond. For example, NO• and O2•− react rapidly to form ONOO− [67], a non-radical product that rapidly protonates to peroxynitrous acid (ONOOH), a powerful oxidizing and nitrating agent that can directly damage proteins, lipids and DNA. Systems that produce NO• and O2•− can therefore cause biological damage, linked to different human diseases [10,67]. Free radicals exist in low concentrations (10−4 to 10−9 M), and their effects are observed locally where they are generated. Free radical reactions can chemically modify surrounding compounds, promoting the loss of physiological function in living organisms. Imbalance between the production of free radicals (ROS/RNS) and antioxidant defenses increases their concentrations, damaging important classes of biological molecules, such as nucleic acids, proteins, lipids and sugars (Figure 2), resulting in cell and tissue lesions with pathological implications [11,86].
2.4. 자유 라디칼의 분자 표적
'반응성'이라는 용어가 라디칼 종에 항상 적합한 것은 아니다. 과산화수소(H2O2), 일산화질소(NO•), 과산화수소 라디칼(O2•−)은 일부 분자와 신속히 반응하는 반면, 하이드록실 라디칼(•OH)은 거의 모든 것과 신속히 반응한다. 과산화 라디칼(RO2•), 질산 라디칼(NO3•), 알콕실 라디칼(RO•), 차염소산(HOCl), 차브롬산(HOBr), 탄산염(CO3•−), 이산화탄소 라디칼(CO2•−), 이산화질소(NO2•−), 과산화질산염(ONOO−), 이산화질소(NO2•), 오존(O3) 등은 중간 정도의 반응성을 보인다 [10]. 자유 라디칼은 여러 유형의 반응과 표적을 가집니다. 산화 과정은 전자 공여체(환원제)로부터 전자 수락체(산화제)로 하나 이상의 전자가 이동하는 화학적/생화학적 반응입니다. 생물학적 시스템에서 대부분의 분자는 비라디칼입니다. 따라서 자유 라디칼이 비라디칼과 반응하면 새로운 라디칼이 생성되어 연쇄 반응을 유발할 수 있습니다. 두 자유 라디칼이 만나면, 그들의 짝을 이루지 않은 전자가 결합하여 공유 결합을 형성할 수 있다. 예를 들어, NO•와 O2•−는 빠르게 반응하여 ONOO− [67]를 형성하는데, 이는 비라디칼 생성물로 빠르게 양성자화되어 과산화질소산(ONOOH)이 된다. 이는 강력한 산화제 및 질화제로 단백질, 지질 및 DNA를 직접 손상시킬 수 있다. 따라서 NO•와 O2•−를 생성하는 시스템은 다양한 인간 질환과 연관된 생물학적 손상을 유발할 수 있다[10,67]. 자유 라디칼은 낮은 농도(10⁻⁴~10⁻⁹ M)로 존재하며, 생성된 부위에서 국소적으로 그 효과가 관찰된다. 자유 라디칼 반응은 주변 화합물을 화학적으로 변형시켜 생물체의 생리적 기능 상실을 촉진할 수 있다. 자유 라디칼(ROS/RNS) 생성량과 항산화 방어 체계 간의 불균형은 그 농도를 증가시켜 핵산, 단백질, 지질, 당류(그림 2)와 같은 중요한 생물학적 분자 군을 손상시키며, 이는 병리학적 의미를 지닌 세포 및 조직 손상으로 이어집니다[11,86].
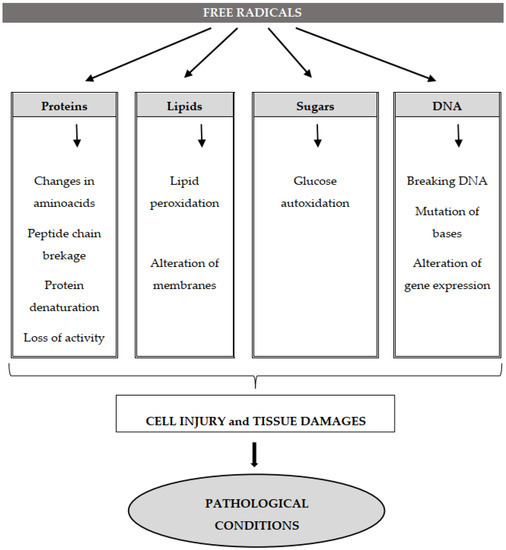
Figure 2. The molecular target of free radicals and oxidative damages. An excessive production of ROS and/or RNS can affect the main cell molecules and result in the oxidation of proteins, with alterations of amino acids, breakdown of the peptide chain, enzymatic inactivation, denaturation of proteins and loss of their activity; lipid peroxidation and alteration of membrane functions; autooxidation of glucose; fragmentation of DNA filament, base mutation and alteration of gene expression. All this leads to cell injuries, tissue damage and subsequent pathological disorders.
그림 2. 자유 라디칼 및 산화 손상의 분자 표적. 과도한 ROS 및/또는 RNS 생성은 주요 세포 분자에 영향을 미쳐 단백질 산화를 유발할 수 있으며, 이는 아미노산 변형, 펩타이드 사슬 분해, 효소 비활성화, 단백질 변성 및 활성 상실을 초래합니다. 또한 지질 과산화 및 막 기능 변화, 포도당의 자동 산화, DNA 필라멘트 단편화, 염기 돌연변이 및 유전자 발현 변화를 일으킵니다. 이 모든 과정은 세포 손상, 조직 손상 및 후속 병리학적 장애로 이어진다.
2.4.1. Deoxyribonucleic (DNA) and Ribonucleic (RNA) Acids
Both ROS and RNS can damage nucleic acids. The former damage DNA, inducing base modifications, deletions, strand breakage, chromosomal rearrangements, hyper- and hypo-methylation and gene expression modulation [31,134]. Mitochondrial DNA is more vulnerable to ROS attack than nuclear DNA because it is near where ROS are generated. A cell produces around 50 hydroxyl radicals per second; in a day, all the cells of a human would generate four million hydroxyl radicals, which can attack biomolecules [25]. The •OH radical reacts directly with all components of DNA, such as purine and pyrimidine bases and the deoxyribose sugar backbone [10,31], causing alterations, including breakages to single and double strands. It abstracts hydrogen atoms, modifying purine and giving rise to pyrimidine derivatives and DNA protein cross-linking [31]. It oxidizes guanosine and thymine in 8-hydroxyl-2-deoxyguanosine and thymine glycol, respectively, modifying DNA and triggering mutagenesis and carcinogenesis. In addition, 8-Hydroxy deoxyguanosine (8-OHdG) is considered a biomarker of DNA oxidative damage and has been used as a biomarker of oxidative stress [135]. It is also involved in mutagenesis, carcinogenesis and aging. Levels of 8- OHdG are higher in mitochondrial than nuclear DNA [10]. Reactive nitrogen species, especially peroxynitrite, interact with guanine to produce nitrative and oxidative DNA lesions such as 8-nitroguanine and 8-oxodeoxyguanosine, respectively [136]. The resulting 8-nitroguanine is unstable and can be spontaneously removed, giving rise to an apurinic site; conversely, adenine can couple with 8-nitroguanine during DNA synthesis, resulting in G-T transversions. Therefore, 8-Nitroguanine is a mutagenic DNA lesion involved in carcinogenesis [135].
Reactive oxygen species can attack different RNAs produced in the body. RNA is more susceptible to oxidative damage than DNA, due to its single strand, lack of an active repair mechanism when oxidized and less protection by proteins. These cytoplasmic RNAs are located near mitochondria where ROS are abundantly produced [137]. Levels of 7,8-dihydro-8-oxo-guanosine (8-oxoG), the most studied product of RNA damage, are elevated in pathological conditions such as Alzheimer’s disease [138], Parkinson’s disease [139], atherosclerosis [140], hemochromatosis [141] and myopathies [142].
2.4.1. 데옥시리보핵산(DNA) 및 리보핵산(RNA)
ROS와 RNS 모두 핵산을 손상시킬 수 있다. 전자는 DNA를 손상시켜 염기 변형, 삭제, 가닥 파열, 염색체 재배열, 과메틸화 및 저메틸화, 유전자 발현 조절을 유발한다[31,134]. 미토콘드리아 DNA는 핵 DNA보다 ROS 공격에 더 취약한데, 이는 미토콘드리아가 ROS가 생성되는 부근에 위치하기 때문이다. 세포는 초당 약 50개의 하이드록실 라디칼을 생성하며, 하루 동안 인간의 모든 세포는 생체 분자를 공격할 수 있는 4백만 개의 하이드록실 라디칼을 생성한다[25]. •OH 라디칼은 퓨린 및 피리미딘 염기, 데옥시리보스 당 골격 등 DNA의 모든 구성 요소와 직접 반응하여[10,31] 단일 가닥 및 이중 가닥 파손을 포함한 변형을 유발합니다. 이는 수소 원자를 추출하여 퓨린을 변형시키고 피리미딘 유도체를 생성하며 DNA-단백질 가교를 일으킵니다[31]. 또한 구아노신과 티민을 각각 8-하이드록시-2-데옥시구아노신과 티민 글리콜로 산화시켜 DNA를 변형시키고 돌연변이 유발 및 발암을 촉발합니다. 더불어 8-하이드록시 데옥시구아노신(8-OHdG)은 DNA 산화 손상의 생체지표로 간주되며 산화 스트레스의 생체지표로 활용되어 왔습니다[135]. 또한 돌연변이 유발, 발암 및 노화 과정에도 관여합니다. 8-OHdG 수준은 핵 DNA보다 미토콘드리아 DNA에서 더 높습니다 [10]. 반응성 질소 종, 특히 퍼옥시나이트라이트는 구아닌과 상호작용하여 각각 8-니트로구아닌 및 8-옥소데옥시구아노신과 같은 질산화 및 산화성 DNA 손상을 생성합니다 [136]. 생성된 8-니트로구아닌은 불안정하여 자발적으로 제거되어 아퓨린 결손 부위를 유발할 수 있다. 반대로, DNA 합성 과정에서 아데닌이 8-니트로구아닌과 결합하여 G-T 전위(transversion)를 일으킬 수 있다. 따라서 8-니트로구아닌은 발암 과정에 관여하는 돌연변이 유발성 DNA 손상이다 [135].
활성산소는 체내에서 생성되는 다양한 RNA를 공격할 수 있다. RNA는 단일 가닥 구조, 산화 시 능동적 복구 메커니즘 부재, 단백질에 의한 보호 기능 부족으로 인해 DNA보다 산화 손상에 더 취약하다. 이러한 세포질 RNA는 ROS가 풍부하게 생성되는 미토콘드리아 근처에 위치한다[137]. RNA 손상의 가장 많이 연구된 생성물인 7,8-디하이드로-8-옥소구아노신(8-oxoG)의 농도는 알츠하이머병[138], 파킨슨병 [139], 죽상경화증 [140], 혈색소증 [141], 근병증 [142]과 같은 병리학적 상태에서 증가한다.
2.4.2. Lipid Oxidation
Lipid peroxidation is a physiological process that takes place in all aerobic cells. It is estimated to involve about 1% of all the oxygen taken up by cells, organs and bodies. The main targets of oxidation are polyunsaturated fatty acids (PUFAs) and phospholipids [143]. Free fatty acids have a carbonyl oxygen (C=O), deficient in electrons, and unsaturated fatty acids are deficient in electrons at their unsaturated carbon–carbon bonds (C=C); these regions of electron deficiency make fatty acids susceptible to attack by a variety of oxidizing agents [144]. Thus, lipid peroxidation takes place where there are high concentrations of polyunsaturated fatty acids. Triglycerides contain linear-chain fatty acids, mainly with 16- to 18-carbon atoms and minimal amounts of unsaturated fatty acids, while phospholipids in the tissue membranes contain up to 15 times the amount of unsaturated fatty acids (C18:4, C20:4, C20:5, C22:5 and C22:6) of triglycerides and are much more susceptible to oxidation due to the greater number of unsaturated carbon–carbon bonds (C=C) [145]. Polyunsaturated fatty acid residues in cell membranes are the main target of oxidation by free radicals.
A reactive radical (e.g., •OH or NO2•) may abstract a hydrogen atom from a C–H bond in a hydrocarbon side chain of a polyunsaturated fatty acid (PUFA) residue in a membrane. The resulting carbon-centered radicals (C•) react rapidly with O2 to generate peroxyl radicals (C–OO•) that can attack side chains adjacent to PUFAs, triggering a chain reaction that forms lipid hydroperoxide. Hence, lipid peroxidation is initiated when any free radical attacks and abstracts hydrogen from a methylene group (CH2) in a fatty acid (L:H), resulting in a carbon centered lipid radical (L•), which in turn reacts with molecular oxygen to form a lipid peroxyl radical (LOO•). The resulting lipid peroxide radical (LOO•) undergoes rearrangement through a cyclization reaction to form endoperoxides, which, in the end, form malondialdehyde (MDA) and 4-hydroxyl-nonenal (4-HNA) [12,142,146], recognized as markers of lipid oxidative decay. In particular, the cellular non-enzymic peroxidation of lipids, similar to all radical reactions, can be divided into three steps: initiation, propagation and termination. It proceeds as a chain reaction mediated by carbon- and oxygen-centered radicals [64]. The initiator of lipid peroxidation (usually an iron-oxygen complex) first produces a carbon-centered radical that reacts with oxygen. After the addition of oxygen, the lipid hydroperoxyl radical formed starts the propagation phase. The major mechanism of initiation is the abstraction of hydrogen by a lipid alkoxy radical, in turn produced by the breakdown of the O–O bond of a lipid hydroperoxide (LOOH). The players crucial for initiation are therefore a transition metal and a preexisting LOOH. In cells, this is achieved with a transition metal iron, which reacts by “Fenton chemistry” with hydrogen peroxide or superoxide produced endogenously to form oxygen-centered radicals [64]. In Fenton chemistry, ferrous iron disproportionates hydrogen peroxide, and the oxidant, ferric iron, generates an anion hydroxide and a highly reactive hydroxyl radical. If another equivalent of hydrogen peroxide is available, ferric iron can be reduced to its ferrous state and generate a peroxyl radical. Once the initial step is completed, lipid peroxidation proceeds to the propagation step. Iron and copper can accelerate lipid peroxidation [10]. They convert H2O2 to •OH by dividing the O–O bond (by Fenton reaction, in the case of Fe2+). In a similar reaction, lipid hydroperoxides can be divided, giving radical alkoxyl (LO•) and more peroxyl (LOO•) to maintain the chain reaction. The free radical chain reaction propagates until two free radicals conjugate and terminate the chain. Enzymic lipid peroxidation by lipoxygenase, cyclooxygenase or cytochrome P450 occurs via regulated mechanisms to produce regio-, stereo- and enantio-specific products [147].
2.4.2. 지질 산화
지질 과산화는 모든 호기성 세포에서 일어나는 생리적 과정이다. 이는 세포, 장기 및 신체에 의해 흡수되는 전체 산소의 약 1%를 차지하는 것으로 추정된다. 산화의 주요 표적은 다중불포화 지방산(PUFAs)과 인지질이다[143]. 자유 지방산은 전자 결핍 상태의 카르보닐 산소(C=O)를 가지며, 불포화 지방산은 불포화 탄소-탄소 결합(C=C) 부위에서 전자 결핍 상태이다. 이러한 전자 결핍 영역으로 인해 지방산은 다양한 산화제의 공격에 취약해진다[144]. 따라서 지질 과산화는 다중 불포화 지방산이 고농도로 존재하는 곳에서 발생한다. 트리글리세라이드는 주로 16~18개의 탄소 원자를 가진 직쇄 지방산을 포함하며 불포화 지방산 함량은 극소량이다. 반면 조직 막 내 인산지질은 트리글리세라이드에 비해 최대 15배에 달하는 불포화 지방산(C18:4, C20:4, C20: 5, C22:5 및 C22:6)을 함유하며 불포화 탄소-탄소 결합(C=C) 수가 더 많아 산화에 훨씬 취약하다[145]. 세포막 내 다불포화 지방산 잔기는 자유 라디칼에 의한 산화의 주요 표적이다.
반응성 라디칼(예: •OH 또는 NO2•)는 막 내 다중불포화지방산(PUFA) 잔기의 탄화수소 측쇄 내 C–H 결합으로부터 수소 원자를 추출할 수 있다. 생성된 탄소 중심 라디칼(C•)은 O2와 신속히 반응하여 퍼옥실 라디칼(C–OO•)을 생성하며, 이는 PUFA에 인접한 측쇄를 공격하여 지질 과산화물을 형성하는 연쇄 반응을 유발한다. 따라서 지질 과산화는 어떤 자유 라디칼이 지방산(L:H)의 메틸렌기(CH2)를 공격하여 수소를 추출할 때 시작되며, 이로 인해 탄소 중심 지질 라디칼(L•)이 생성됩니다. 이 라디칼은 다시 분자 산소와 반응하여 지질 퍼옥실 라디칼(LOO•)을 형성합니다 . 생성된 지질 과산화 라디칼(LOO•)은 고리화 반응을 통한 재배열을 거쳐 내과산화물을 형성하며, 이는 결국 지질 산화 분해의 지표로 인정되는 말론디알데히드(MDA)와 4-하이드록실-노네날(4-HNA)을 생성한다[12,142,146]. 특히 세포 내 비효소적 지질 과산화는 모든 라디칼 반응과 유사하게 개시, 전파, 종결의 세 단계로 구분될 수 있다. 이는 탄소 및 산소 중심 라디칼에 의해 매개되는 연쇄 반응으로 진행된다[64] . 지질 과산화의 개시체(일반적으로 철-산소 복합체)는 먼저 산소와 반응하는 탄소 중심 라디칼을 생성합니다. 산소 첨가 후 형성된 지질 하이드로퍼옥실 라디칼이 전파 단계를 시작합니다. 개시의 주요 메커니즘은 지질 하이드로퍼옥사이드(LOOH)의 O–O 결합 분해로 생성된 지질 알콕시 라디칼에 의한 수소 추출입니다 . 따라서 개시에 중요한 역할을 하는 요소는 전이 금속과 기존 LOOH이다. 세포 내에서 이는 전이 금속 철을 통해 이루어지며, 철은 “펜톤 화학”을 통해 내생적으로 생성된 과산화수소 또는 슈퍼옥사이드와 반응하여 산소 중심 라디칼을 형성한다[64]. 펜톤 화학에서 2가 철은 과산화수소를 불균형 분해하고, 산화제인 3가 철은 하이드록사이드 음이온과 고반응성 하이드록실 라디칼을 생성한다. 추가 과산화수소가 존재할 경우, 철(III) 이온은 철(II) 상태로 환원되어 퍼옥실 라디칼을 생성할 수 있다. 초기 단계가 완료되면 지질 과산화는 증폭 단계로 진행된다. 철과 구리는 지질 과산화를 촉진할 수 있다[10]. 이들은 O–O 결합을 분해하여 H2O2를 •OH로 전환한다(Fe2+의 경우 펜톤 반응에 의해). 유사한 반응으로 지질 과산화물은 분해되어 라디칼 알콕실(LO•)과 더 많은 퍼옥실(LOO•)을 생성하여 연쇄 반응을 유지합니다. 자유 라디칼 연쇄 반응은 두 개의 자유 라디칼이 결합하여 사슬을 종결할 때까지 진행됩니다. 리폭시게나제, 사이클로옥시게나제 또는 시토크롬 P450에 의한 효소적 지질 과산화는 조절된 기전을 통해 위치특이적, 입체특이적 및 거울상특이적 생성물을 생성한다[147].
Cholesterol Oxidation
Cholesterol, (3β)-cholest-5-en-3-ol, is a lipid produced endogenously but can also be acquired from dietary sources. It plays important biological roles. The cholesterol content of membranes of eukaryotic cells has been estimated to range from 20% to 50% [148]. It is crucial for maintaining the stability, fluidity and permeability of cell membranes, but being a polycyclic monounsaturated alcohol, it is susceptible to oxidation, and its products are known as oxysterols. Oxysterols are 27-carbon derivatives of cholesterol created by enzymic or radical oxidation [149]. Several enzymes of the cytochrome P450 family oxidize cholesterol to specific hydroxyl cholesterols (OHCh), such as 7α- and 7β-hydroperoxycholesterol (7α- and 7β-OOHCh), 7α-OHCh, 7β-OHCh, 5α,6α-epoxycholesterol, 5b,6β-epoxycholesterol and 7-ketocholesterol (7-KCh) [150]. The oxysterols occur in vivo in different forms, namely esterified, sulfated, conjugated and free [149]. In very low concentrations, oxysterols mediate many physiological functions; they participate in the regulation of cholesterol metabolism, biosynthesis of bile acids and various signaling pathways [150,151]. Oxysterols can affect membrane fluidity, membrane permeability to cations, albumin and glucose and membrane-bound protein kinase c activity [151]. The accumulation of cholesterol oxidation products is mainly due to the overconsumption of cholesterol-rich foods, such as meat, eggs and dairy products [152], and has been associated with the onset and development of diseases, such as atherosclerosis, diabetes, Alzheimer’s and Parkinson’s disease [153], carcinogenesis and cancer progression [154].
콜레스테롤 산화
콜레스테롤(3β)-콜레스테-5-엔-3-올)은 체내에서 생성되지만 식이 공급원으로도 획득될 수 있는 지질이다. 이는 중요한 생물학적 역할을 수행한다. 진핵세포 막의 콜레스테롤 함량은 20%에서 50% 사이로 추정된다[148]. 이는 세포막의 안정성, 유동성 및 투과성 유지에 필수적이지만, 다환 단일불포화 알코올로서 산화에 취약하며, 그 생성물은 옥시스테롤로 알려져 있다. 옥시스테롤은 효소적 또는 라디칼 산화에 의해 생성되는 콜레스테롤의 27탄소 유도체이다[149]. 시토크롬 P450 계열의 여러 효소들은 콜레스테롤을 특정 하이드록실 콜레스테롤(OHCh)로 산화시키는데, 예를 들어 7α- 및 7β-하이드로퍼옥시콜레스테롤(7α- 및 7β-OOHCh), 7α-OHCh, 7β-OHCh, 5α,6α-에폭시콜레스테롤, 5β,6β-에폭시콜레스테롤 및 7-케토콜레스테롤(7-KCh) 등이 있습니다[150]. 옥시스테롤은 생체 내에서 에스테르화, 황산화, 공액화 및 유리 형태 등 다양한 형태로 존재합니다[149]. 매우 낮은 농도에서 옥시스테롤은 많은 생리적 기능을 매개합니다. 이들은 콜레스테롤 대사 조절, 담즙산 생합성 및 다양한 신호 전달 경로에 관여합니다 [150,151]. 옥시스테롤은 막 유동성, 양이온, 알부민 및 포도당에 대한 막 투과성, 그리고 막 결합 단백질 키나제 c 활성에 영향을 미칠 수 있습니다 [151]. 콜레스테롤 산화 생성물의 축적은 주로 육류, 계란, 유제품과 같은 콜레스테롤이 풍부한 식품의 과다 섭취로 인해 발생하며[152], 동맥경화증, 당뇨병, 알츠하이머병 및 파킨슨병[153], 발암 및 암 진행[154]과 같은 질병의 발병 및 진행과 연관되어 있다.
Lipid Peroxides in Disease and Death
Lipid peroxidation is important because of its involvement in various pathological conditions. It affects cell membrane integrity (rupture of vacuolar or central lysosomal membranes), increases loss of membrane sealing against substances (K+ and Ca2+) that normally do not cross it except through specific channels and damages membrane protein inactivating receptors, enzymes and ion channels [155]. Lipid peroxidation involves the production of a variety of breakdown products, including alcohols, ketones, alkanes, aldehydes and ethers. About 32 aldehydes have been identified as products of lipid peroxidation, 4-hydroxynonenal (4-HNE) and malondialdehyde (MDA) being the best described and used as markers of lipid oxidation [156]. HNE is the major decomposition product of hydroperoxides of n-6 fatty acids. MDA and 4-HNE damage DNA, causing mutagenic lesions [143] and proteins. Both bind avidly to membrane proteins, inactivating enzymes and receptors. Changes in proteins from aldehyde products contribute to neurodegenerative diseases, the activation of kinases and the inhibition of nuclear transcription factors [157].
The toxicity of lipid peroxidation products in mammals generally involves hepatotoxicity, neurotoxicity and nephrotoxicity [64]; increases in products of lipid oxidation occur in liver diseases, diabetes, inflammation, atherosclerosis, cancer, apoplexy and aging. PUFAs and cholesterol molecules are a major part of the low-density lipoproteins (LDLs), and the oxidative modification of LDLs is reported to be involved in the development of atherosclerosis and cardiovascular disease. Lipid peroxides have long been considered important in the progression and regulation of inflammation [158]. Lipid peroxidation also has a role in neurodegenerative diseases [159], ischemia-reperfusion injury, diabetes [160] and mutagenic and carcinogenic activity [161].
Lipid peroxidation also plays a role in regulated cell death. The product 4-HNE has been shown to induce apoptosis in specific contexts [162], and lipid peroxidation is also the primary driver of ferroptosis, a type of regulated necrotic cell death [163]. However, it has been reported that many products of lipid peroxidation may have opposite effects, such as cytotoxic and cytoprotective, pro- and anti-inflammatory, pro and anti-atherogenic and pro and anti-apoptotic [164].
The assay of malondialdehyde (MDA) levels is one of the main methods of assessing the effects of ROS on biological systems. One rather non-specific method is based on the reaction of MDA with thiobarbituric acid (TBA) to form thiobarbituric acid reactive substances (TBARS), whereas an HPLC method is preferred if possible [165]. Lipid peroxides can be measured with different techniques, including the quite suitable iron/xylenol method [166]. Products such as MDA and 4-hydroxy-nonenal (4-HNE), which conjugate with proteins, can be measured by immune assay [167].
질병과 사망에서의 지질 과산화물
지질 과산화는 다양한 병리적 상태에 관여하기 때문에 중요합니다. 이는 세포막 무결성(소포체 또는 중앙 리소좀 막 파열)에 영향을 미치고, 특정 채널을 통해서만 통과하는 물질(K+ 및 Ca2+)에 대한 막 밀봉 손실을 증가시키며, 수용체, 효소 및 이온 채널을 비활성화하는 막 단백질을 손상시킵니다 [155]. 지질 과산화는 알코올, 케톤, 알칸, 알데히드, 에테르 등 다양한 분해 생성물의 생성을 수반한다. 지질 과산화 생성물로 확인된 약 32종의 알데히드 중 4-하이드록시노넨알(4-HNE)과 말론디알데히드(MDA)가 가장 잘 연구되었으며 지질 산화의 지표로 사용된다 [156]. HNE는 n-6 지방산의 하이드로퍼옥사이드의 주요 분해 생성물이다. MDA와 4-HNE는 DNA를 손상시켜 돌연변이 유발 병변[143]과 단백질을 손상시킨다. 둘 다 막 단백질에 강하게 결합하여 효소와 수용체를 비활성화한다. 알데히드 생성물에 의한 단백질 변화는 신경퇴행성 질환, 키나아제 활성화 및 핵 전사 인자 억제에 기여한다[157].
포유류에서 지질 과산화 생성물의 독성은 일반적으로 간독성, 신경독성 및 신독성과 관련이 있다[64]; 지질 산화 생성물의 증가는 간 질환, 당뇨병, 염증, 죽상경화증, 암, 뇌졸중 및 노화에서 발생한다. 다불포화지방산(PUFAs)과 콜레스테롤 분자는 저밀도 지단백질(LDL)의 주요 구성 요소이며, LDL의 산화 변형은 동맥경화증 및 심혈관 질환 발병과 관련이 있다고 보고된다. 지질 과산화물은 오랫동안 염증의 진행과 조절에 중요한 역할을 하는 것으로 여겨져 왔다[158]. 지질 과산화는 또한 신경퇴행성 질환[159], 허혈-재관류 손상, 당뇨병[160], 돌연변이 유발 및 발암 활성[161]에도 관여한다.
지질 과산화는 조절된 세포 사멸에도 역할을 한다. 생성물인 4-HNE는 특정 상황에서 세포 사멸을 유도하는 것으로 밝혀졌다[162], 또한 지질 과산화는 조절된 괴사성 세포 사멸의 일종인 철사멸(ferroptosis)의 주요 원동력이다[163]. 그러나 지질 과산화 생성물 다수가 세포독성과 세포보호, 염증 촉진 및 억제, 동맥경화 촉진 및 억제, 세포사멸 촉진 및 억제 등 상반된 효과를 가질 수 있다는 보고가 있다[164].
말론디알데하이드(MDA) 수준 분석은 생물학적 시스템에 대한 ROS의 영향을 평가하는 주요 방법 중 하나입니다. 비교적 비특이적인 방법으로는 MDA가 티오바르비투르산(TBA)과 반응하여 티오바르비투르산 반응성 물질(TBARS)을 형성하는 원리에 기반한 것이 있으며, 가능하다면 HPLC 방법이 선호됩니다[165]. 지질 과산화물은 철/자일렌올법[166]과 같은 다양한 기법으로 측정할 수 있다. 단백질과 결합하는 MDA 및 4-하이드록시-노네날(4-HNE)과 같은 생성물은 면역 분석법[167]으로 측정 가능하다.
2.4.3. Protein Oxidation
Protein oxidation can be induced by radical species such as superoxide, hydroxyl, peroxyl, alkoxyl and hydroperoxyl or non-radical species such as hydrogen peroxide, ozone, hypochlorous acid, singlet oxygen and peroxynitrite anion [168]. Reactive oxygen species may attack proteins and produce carbonyls and other amino acid derivatives. The availability of oxygen, superoxide anion and its protonated form (HO2−) determines the process of protein oxidation. The induction of 3-chlorotyrosine from tyrosine by hypochlorous acid, the oxidization of histidine to 2-oxohistidine at the site of the metal binding of proteins, the oxidation of thiol groups and the generation of carbonyl derivatives of amino acids are some examples of protein modifications [57]. Reactive oxygen species cause oxidative damage to amino acid residues such as lysine, proline, threonine and arginine, producing carbonyl derivatives. The oxidation of different amino acids denatures proteins and causes loss of function, be it enzyme activity, receptor function or transport function [169]. Carbonyl groups on proteins were considered markers of oxidation proteins mediated by free radicals [170]. Specific markers of protein oxidation are O-tyrosine (a marker of the hydroxyl radical) and 3-nitrotyrosine (a marker of RNS). An increase in serum concentration of protein carbonyls is observed in various pathological conditions such as Parkinson’s disease [171], muscle dystrophies [172], rheumatoid arthritis [173], progeria, atherosclerosis, Werner’s syndrome [57] and aging [174]. Levine and Stadtman postulated an increase in protein carbonylation levels as a function of age [175]. A recent protein database lists over 180 proteins that are carbonylated during aging and in age-related disorders [176].
2.4.3. 단백질 산화
단백질 산화는 슈퍼옥사이드, 하이드록실, 페록실, 알콕실, 하이드로퍼옥실과 같은 라디칼 종 또는 과산화수소, 오존, 차아염소산, 일중항 산소, 퍼옥시나이트라이트 음이온과 같은 비라디칼 종에 의해 유도될 수 있다[168]. 활성산소종은 단백질을 공격하여 카르보닐 및 기타 아미노산 유도체를 생성할 수 있다. 산소, 슈퍼옥사이드 음이온 및 그 양성자화 형태(HO2−)의 가용성은 단백질 산화 과정을 결정한다. 차아염소산에 의한 티로신으로부터 3-클로로티로신의 유도, 단백질의 금속 결합 부위에서 히스티딘의 2-옥소히스티딘으로의 산화, 티올 그룹의 산화 및 아미노산의 카르보닐 유도체 생성은 단백질 변형의 몇 가지 예이다 [57]. 활성산소는 라이신, 프롤린, 트레오닌, 아르기닌과 같은 아미노산 잔기에 산화적 손상을 일으켜 카르보닐 유도체를 생성합니다. 다양한 아미노산의 산화는 단백질을 변성시키고 효소 활성, 수용체 기능 또는 수송 기능과 같은 기능 상실을 초래합니다 [169]. 단백질의 카르보닐기는 자유 라디칼에 의해 매개되는 산화 단백질의 표지로 간주되었다[170]. 단백질 산화의 특이적 표지자는 O-티로신(하이드록실 라디칼의 표지자)과 3-니트로티로신(반응성 질소 종의 표지자)이다. 혈청 내 단백질 카르보닐 농도 증가는 파킨슨병[171], 근이영양증[172], 류마티스 관절염[173], 조로증, 동맥경화증, 베르너 증후군[57], 노화[174] 등 다양한 병리적 상태에서 관찰됩니다. Levine과 Stadtman은 연령에 따른 단백질 카르보닐화 수준 증가를 가설로 제시하였다[175]. 최근 단백질 데이터베이스에는 노화 및 노화 관련 질환 과정에서 카르보닐화되는 180개 이상의 단백질이 등재되어 있다[176].
2.5. Free Radicals and Diseases
The implications of free radical processes concern the fields of biology and medicine. Free radicals accumulate due to an imbalance between antioxidants and oxidants that damage macromolecules, such as nucleic acids, proteins and lipids, causing abnormal gene expression, disturbance of receptor activity, cell proliferation, immune perturbation, mutagenesis, tissue damage and various disease conditions [87,177]. Many clinical disorders have been linked to free radicals (Figure 3), including diabetes mellitus [178], inflammatory diseases [179], neurodegenerative diseases (Alzheimer’s [180], Parkinson’s [181] and Huntington’s disease [182]), lateral amyotrophic [183] and multiple sclerosis [184], cancer (colorectal [185], breast [186], prostate [187] and lung [188]), cardiovascular disease [189] (atherosclerosis [190] and hypertension [191]), cataract [192,193], rheumatoid arthritis [194], asthma [195] and aging [174].
2.5. 자유 라디칼과 질환
자유 라디칼 과정의 영향은 생물학과 의학 분야에 걸쳐 있습니다. 자유 라디칼은 항산화제와 산화제 사이의 불균형으로 축적되며, 이는 핵산, 단백질, 지질과 같은 거대분자를 손상시켜 비정상적인 유전자 발현, 수용체 활동 장애, 세포 증식, 면역 교란, 돌연변이 유발, 조직 손상 및 다양한 질환 상태를 유발합니다 [87,177] . 당뇨병 [178], 염증성 질환 [179], 신경퇴행성 질환(알츠하이머병 [180], 파킨슨병 [181], 헌팅턴병 [182]), 측삭경화증 [183], 다발성 경화증 [184], 암 (대장암[185], 유방암[186], 전립선암[187], 폐암[188]), 심혈관 질환[189] (동맥경화증[190], 고혈압[191]), 백내장[192,193], 류마티스 관절염[194], 천식[195], 노화 [174].
그림 3. 자유 라디칼과 질병. 병리학적 조건에서 과도한 자유 라디칼 생성은 단백질 산화, 지질 과산화, DNA 손상, 신호 전달 및 유전자 발현 변화, 그리고 여러 질병을 유발할 수 있습니다.
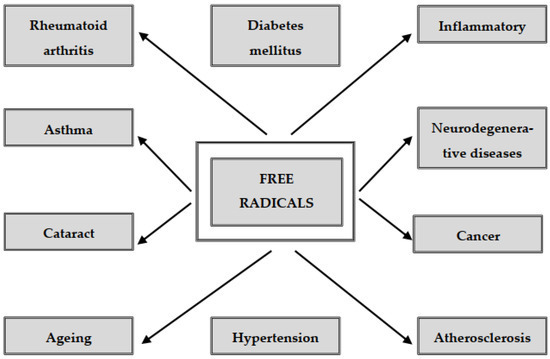
Figure 3. Free radicals and diseases. Under pathological conditions, an excess amount of free radical generation can cause protein oxidation, lipid peroxidation, DNA damage, changes in signal transduction and gene expression and several diseases.
3. Antioxidants
The deleterious effects of excess free radicals, or oxidative stress, have been reported to eventually lead to cell death. The overproduction of reactive oxygen and nitrogen species has been implicated in the development of various chronic and degenerative diseases [177]. The body has natural antioxidant defenses against free radicals. Antioxidants inhibit the oxidation process, even at relatively low concentrations, and can protect cells against free-radical damage by delaying or preventing the oxidation of proteins, carbohydrates, lipids and DNA [196]. Antioxidants have the ability to donate electrons. Antioxidants that break the chain reaction are strong electron donors and react with free radicals before major molecules are damaged. The antioxidants are therefore oxidized and must be regenerated or replaced. Antioxidant enzymes catalyze the degradation of species of free radicals, generally in the cell. Transition metal binding proteins prevent the interaction of transition metals, such as iron and copper, with hydrogen peroxide and superoxide and hence the production of highly reactive hydroxyl radicals.
Antioxidants can be endogenous or exogenous (Figure 4). The former may be enzymes, such as superoxide dismutase (SOD), catalase (CAT), glutathione peroxidase (GPx) and glutathione reductase (GRx), or non-enzymes such as metabolic antioxidants, such as lipoic acid, glutathione, L-arginine, uric acid, bilirubin and antioxidant nutrients [11]. Some exogenous antioxidant nutrients cannot be produced by the body and must be obtained from food; they include vitamin E, vitamin C, trace elements (Se, Cu, Zn, Mn) and phytochemicals such as isoflavones, polyphenols and flavonoids [197]. Endogenous and exogenous antioxidants are effective scavengers of free radicals; by giving electrons to ROS, they neutralize the negative effects of the latter, reducing oxidative stress and the oxidation of cell molecules [196]. The active interaction of endogenous and exogenous antioxidants has also been demonstrated; indeed, vitamin E administered orally to humans induces a significant increase in red blood cell glutathione levels. These findings may be explained by an increase in glutathione synthesis by stimulation of glutathione synthetase activity. An alternative possibility is the reduced utilization of glutathione for the detoxification of free radicals. These two mechanisms could be effective in counteracting glutathione feedback of its own synthesis [198].
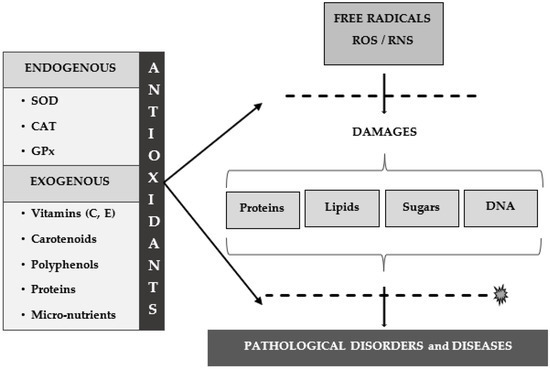
Figure 4. Antioxidant defense against free radicals. Antioxidants can be endogenous or exogenous. The antioxidants that break the chain are strong electron donors and react with free radicals before the major molecules are damaged. The first line of defense against free radicals includes the enzymes superoxide dismutase (SOD), catalase (CAT), glutathione peroxidase (GPx) and glutathione reductase (GRx). Exogenous antioxidants are compounds provided through foods or supplements, such as vitamin E, vitamin C, carotenoids, trace metals and polyphenols. These compounds represent the second line of defense against free radicals and consequent pathological disorders and diseases, acting with a scavenging effect, a stimulatory effect on endogenous antioxidant enzymes or both.
In recent years, the attention to diet as an essential source of exogenous antioxidants has increased. The demand for natural antioxidants has reduced the use of synthetic antioxidants due to their toxicity, carcinogenicity or hepatotoxicity in the human body [66]. The dietary antioxidants naturally present in food have aroused considerable interest because of their safety and potential nutritional and therapeutic effects on health [199]. Natural antioxidants can be found in all parts of plants such as fruit, vegetables, nuts, seeds, leaves, roots and bark [200], and people receive antioxidant supplements directly from fresh fruit and vegetables. It should be noted that, if antioxidant supplements are consumed in large doses, they can act as pro-oxidants [201]. Compared to supplements, the dietary intake of antioxidants from natural fruit and vegetables may be a safe way to avoid overdosing.
Foods rich in micronutrients such as α-tocopherol (vitamin E) and minerals have been considered useful to alleviate ROS-related damage. For example, selenium and zinc interact with GPx and SOD, respectively, to combat oxidative stress. The combination of selenium and vitamin E has shown protective effects against oxidative damage in the colon of rats with ulcerative colitis [202]. Although dietary antioxidants are essential in supplying endogenous antioxidants for the neutralization of oxidative stress, inappropriate use may be detrimental for the physiological scavenging of ROS [203]. In fact, malnutrition and antioxidant deficiency have been related to diseases such as chronic obstructive pulmonary disease (COPD) and Crohn’s disease [204,205]. The lack of antioxidants induced by malnutrition can increase the risk of disease and negative treatment outcomes [206]. Decreased intake or availability of dietary antioxidants such as vitamins C and E, carotenoids and polyphenols can reduce the efficiency of the antioxidant system and aggravate disease progression [204,207]. A diet rich in fruit, vegetables, fish and whole grains has been associated with better lung function and reduced risk of COPD [208]. Experimental evidence has suggested an association between nutrition and lens opacities.
A dietary deficiency of antioxidants and reactive oxygen scavengers may be involved in the pathogenesis of so-called “idiopathic” human senile cataract, as demonstrated in experimental cataracts. Indeed, the results of a pooled analysis showed a protective effect of antioxidants on the cataract, supporting the hypothesis of a nutritional deficiency in the human senile cataract, but not all studies reached statistical significance. Vitamin C, beta-carotene, lutein and zeaxanthin exert a protective effect, whereas the effect of vitamin E, vitamin A and alpha-carotene is not completely demonstrated [209].
The consumption of fruit and vegetables increases the blood concentration of antioxidants such as carotene and vitamin C and depresses the oxidation of cholesterol [210], and it has been inversely correlated with mortality due to CVD [211].
Epidemiological studies have detected a significantly reduced risk of CVD in relation to higher polyphenol intake [212]. Polyphenols are the most abundant antioxidants in the human diet (~1 g/d) and are common in fruit and vegetables, coffee, tea and cereals [213]. Their protective effects not only ensue from their antioxidant properties but also from their anti-inflammatory and vasodilatory effects on endothelial cells [214].
Clinical evidence indicates that deterioration in neurodegenerative diseases can be improved by the correct use of natural antioxidants [215]. It has been suggested that inadequate serum concentrations in vitamin D are highly associated with the loss of dopaminergic neurons in the brains of Parkinson’s disease patients and with an increased risk of the disease [216]. Neurological impairment has also manifested in subjects with vitamin B deficiency. Multiple vitamin B deficiencies (B1, B3 and folate) are involved in the pathology of neurodegenerative diseases such as Parkinson’s and Alzheimer’s diseases [217]. In addition to vitamins, phytochemicals found in fruit and vegetables show high antioxidant capacity with potential neuroprotective effects against Parkinson’s disease [218].
The aging population is at higher risk of malnutrition due to a general decline in body function, including reduced metabolic activity, digestive ability and absorption, as well as cognitive decline [219]. The elderly are therefore more likely to suffer from diseases associated with inadequate nutrition. Dietary antioxidants seem to play an anti-aging role due to their ability to suppress the generation of free radicals [220]. It has been found that women who consume more green leafy vegetables and crucifers have less cognitive decline [219]. A higher intake of green and yellow vegetables was also correlated with a slower rate of skin aging in Japanese women [221]. The supplementation of fruit and vegetable extracts significantly improves many parameters of immune function in elderly subjects [222].
The intestinal inflammation associated with oxidative stress plays an important role in various gastrointestinal diseases, such as inflammatory bowel disease [223,224]. Low levels of enzyme antioxidants and vitamins due to malnutrition were observed in subjects with inflammatory bowel syndrome [205]. Antioxidant use has been shown to restore redox balance, thereby mitigating intestinal damage and maintaining a healthy gastro-intestinal tract [223].
Fruit and vegetables, which are rich in antioxidants, exert a protective effect against several different types of cancer [225]. About 35% of cancers can be prevented by dietary modifications [226]. It has been demonstrated that plant foods containing polyphenols have anti-cancer activity that is effective against cancer of the lung, breast, tongue, stomach, larynx, colon and prostate [227,228]. Fruit with high phenolic content has stronger antioxidant properties that induce the replacement of the hydroxyl group in the aromatic rings of phenol compounds [229].
It should be emphasized that many dietary polyphenols are valid in cell experiments but are ineffective in animals and humans. For example, every year there are many reports of the anti-cancer activity of polyphenols on different tumor cell lines under controlled conditions [230]. However, few polyphenols are considered to be antitumor agents for clinical use [231]. In the typical cytotoxicity or proliferation assay with dietary polyphenols and cancer cell lines, the single polyphenol or extract rich in polyphenols is only incubated with the cells for 24–72 h [232,233,234]. Again, quercetin, considered the most bioactive compound, has been claimed to inhibit cell growth and induce apoptosis, necrosis and autophagy in different cancer cell lines (A549 cells [235], HeLa cells [216], HT29 and HCT15 cells [236] and PATU-8988 cells [237]); however, quercetin is relatively insoluble in water and unstable in physiological systems, which leads to very low bioavailability [238,239]. There are no clinical studies demonstrating the efficacy of quercetin [240].
The lack of randomized trials on the relationship between diet and cancer is due to the difficulty of whole diet intervention for ethical reasons [241]. Thus, in order to reduce the risk of cancer, the general recommendations are a diet rich in fruit, vegetables and grains, a low intake of red meat and alcohol and a healthy lifestyle [241].
Thus, in regards to the use of antioxidants in the prevention and treatment of diseases, many problems still remain elusive. Some results indicate that antioxidants do not exert favorable effects on the control of the diseases. The precise roles of ROS in the pathogenesis of various diseases remain to be clarified. Most exogenously administrated antioxidants are not selective or uniformly distributed in the various parts of cells or tissues [242,243]. The intake level (threshold level) of antioxidant nutrients needed for optimal nutrition is still unclear, and there is little information on antioxidant bioavailability in vivo in humans [244,245]. The lack of specificity of antioxidants and their possible interactions [245,246] may explain their ineffectiveness in the treatment of diseases related to oxidative stress. It is therefore suggested to concentrate on the development of innovative targeted antioxidants to focus their precise therapeutic effects [243,247].
3. 항산화제
과잉 자유 라디칼 또는 산화 스트레스의 유해한 영향은 결국 세포 사멸로 이어진다고 보고되었습니다. 반응성 산소 및 질소 종의 과잉 생산은 다양한 만성 및 퇴행성 질환의 발병과 관련이 있는 것으로 밝혀졌다[177]. 인체는 자유 라디칼에 대항하는 자연적인 항산화 방어 체계를 갖추고 있다. 항산화제는 비교적 낮은 농도에서도 산화 과정을 억제하며, 단백질, 탄수화물, 지질 및 DNA의 산화를 지연시키거나 방지함으로써 자유 라디칼 손상으로부터 세포를 보호할 수 있다[196]. 항산화제는 전자를 기증하는 능력을 지닌다. 연쇄 반응을 차단하는 항산화제는 강력한 전자 공여체로, 주요 분자가 손상되기 전에 자유 라디칼과 반응합니다. 따라서 항산화제는 산화되어 재생되거나 대체되어야 합니다. 항산화 효소는 일반적으로 세포 내에서 자유 라디칼 종의 분해를 촉매합니다. 전이 금속 결합 단백질은 철과 구리 같은 전이 금속이 과산화수소 및 슈퍼옥사이드와 상호작용하는 것을 방지하여 고반응성 하이드록실 라디칼의 생성을 억제합니다.
항산화제는 내인성 또는 외인성일 수 있다(그림 4). 전자는 슈퍼옥사이드 디스뮤타제(SOD), 카탈라제(CAT), 글루타티온 퍼옥시다제(GPx), 글루타티온 환원효소(GRx)와 같은 효소이거나, 리포산, 글루타티온, L-아르기닌, 요산, 빌리루빈 및 항산화 영양소 등이 있습니다[11]. 일부 외인성 항산화 영양소는 체내에서 생성되지 않아 식품을 통해 섭취해야 합니다. 여기에는 비타민 E, 비타민 C, 미량 원소(셀레늄, 구리, 아연, 망간) 및 이소플라본, 폴리페놀, 플라보노이드와 같은 식물성 화합물이 포함됩니다[197]. 내인성 및 외인성 항산화제는 자유 라디칼의 효과적인 소거제 역할을 합니다. 활성산소종(ROS)에 전자를 제공함으로써 후자의 부정적 영향을 중화시켜 산화 스트레스와 세포 분자의 산화를 감소시킵니다[196]. 내인성 및 외인성 항산화제의 능동적 상호작용도 입증되었습니다. 실제로 인간에게 경구 투여된 비타민 E는 적혈구 글루타티온 수치를 현저히 증가시킵니다. 이러한 결과는 글루타티온 합성효소 활성 자극에 의한 글루타티온 합성 증가로 설명될 수 있다. 다른 가능성은 자유 라디칼 해독을 위한 글루타티온 이용 감소이다. 이 두 메커니즘은 글루타티온 자체 합성에 대한 피드백을 효과적으로 억제할 수 있다 [198].
그림 4. 자유 라디칼에 대한 항산화 방어. 항산화제는 내인성 또는 외인성일 수 있다. 사슬을 끊는 항산화제는 강력한 전자 공여체로서 주요 분자가 손상되기 전에 자유 라디칼과 반응한다. 자유 라디칼에 대한 첫 번째 방어선에는 슈퍼옥사이드 디스뮤타제(SOD), 카탈라제(CAT), 글루타티온 퍼옥시다제(GPx), 글루타티온 환원효소(GRx) 등의 효소가 포함된다. 외인성 항산화제는 비타민 E, 비타민 C, 카로티노이드, 미량 금속, 폴리페놀 등 식품이나 보충제를 통해 공급되는 화합물이다. 이러한 화합물은 자유 라디칼 및 그에 따른 병리적 장애와 질병에 대한 2차 방어선을 구성하며, 소거 효과, 내인성 항산화 효소에 대한 자극 효과 또는 둘 다를 통해 작용한다.
최근 외인성 항산화제의 필수 공급원으로서 식단에 대한 관심이 증가하고 있다. 천연 항산화제에 대한 수요는 인체 내 독성, 발암성 또는 간독성으로 인해 합성 항산화제 사용을 감소시켰다[66]. 식품에 자연적으로 존재하는 식이 항산화제는 안전성과 건강에 대한 잠재적 영양 및 치료 효과로 인해 상당한 관심을 불러일으키고 있다[199]. 천연 항산화제는 과일, 채소, 견과류, 씨앗, 잎, 뿌리, 나무껍질 등 식물의 모든 부분에서 발견될 수 있다[200]. 사람들은 신선한 과일과 채소를 통해 항산화제를 직접 섭취한다. 항산화제 보충제를 과다 복용할 경우 오히려 산화 촉진제로 작용할 수 있다는 점에 유의해야 한다[201]. 보충제 대비 천연 과일과 채소를 통한 항산화제 식이 섭취는 과다 복용을 피할 수 있는 안전한 방법일 수 있다.
α-토코페롤(비타민 E) 및 미네랄과 같은 미량영양소가 풍부한 식품은 ROS 관련 손상을 완화하는 데 유용한 것으로 간주되어 왔다. 예를 들어, 셀레늄과 아연은 각각 글루타치온 과산화효소(GPx) 및 슈퍼옥사이드 디스뮤타제(SOD)와 상호작용하여 산화 스트레스에 대항한다. 셀레늄과 비타민 E의 조합은 궤양성 대장염을 가진 쥐의 대장에서 산화 손상에 대한 보호 효과를 나타냈다[202]. 식이 항산화제는 산화 스트레스 중화를 위한 내인성 항산화제 공급에 필수적이지만, 부적절한 사용은 ROS의 생리적 제거에 해로울 수 있다[203]. 실제로 영양실조와 항산화제 결핍은 만성 폐쇄성 폐질환(COPD) 및 크론병과 같은 질환과 관련이 있다[204,205]. 영양실조에 의한 항산화제 부족은 질병 위험과 부정적인 치료 결과를 증가시킬 수 있다 [206]. 비타민 C와 E, 카로티노이드, 폴리페놀과 같은 식이 항산화제의 섭취량 감소 또는 이용 가능성 저하는 항산화 시스템의 효율성을 떨어뜨리고 질병 진행을 악화시킬 수 있다 [204,207]. 과일, 채소, 생선, 통곡물이 풍부한 식단은 폐 기능 개선 및 COPD 위험 감소와 연관성이 있는 것으로 나타났다 [208]. 실험적 증거는 영양과 수정체 혼탁 사이의 연관성을 시사한다.
실험적 백내장에서 입증된 바와 같이, 항산화제 및 활성산소 제거제의 식이 결핍은 소위 “특발성” 노인성 백내장의 발병 기전에 관여할 수 있다. 실제로 통합 분석 결과 항산화제가 백내장에 대한 보호 효과를 보였으며, 이는 노인성 백내장의 영양 결핍 가설을 뒷받침하지만 모든 연구에서 통계적 유의성을 달성한 것은 아니다. 비타민 C, 베타카로틴, 루테인 및 제아잔틴은 보호 효과를 발휘하는 반면, 비타민 E, 비타민 A 및 알파카로틴의 효과는 완전히 입증되지 않았다 [209].
과일과 채소 섭취는 카로틴 및 비타민 C와 같은 항산화제의 혈중 농도를 증가시키고 콜레스테롤의 산화를 억제한다[210], 그리고 이는 심혈관 질환(CVD)으로 인한 사망률과 역상관 관계가 있다[211].
역학 연구들은 폴리페놀 섭취량이 높을수록 심혈관 질환(CVD) 위험이 현저히 감소한다는 사실을 발견했다[212]. 폴리페놀은 인간 식단에서 가장 풍부한 항산화제(~1g/일)로 과일과 채소, 커피, 차, 곡류에 널리 분포한다[213]. 그 보호 효과는 항산화 특성뿐만 아니라 내피 세포에 대한 항염증 및 혈관 확장 효과에서도 비롯된다[214].
임상 증거에 따르면 신경퇴행성 질환의 악화는 천연 항산화제의 적절한 사용으로 개선될 수 있다[215]. 비타민 D 혈청 농도 부족은 파킨슨병 환자의 뇌에서 도파민성 뉴런 손실 및 질병 발병 위험 증가와 높은 연관성이 있는 것으로 제안되었다[216]. 비타민 B 결핍 환자에서도 신경학적 장애가 나타났습니다. 다중 비타민 B 결핍(B1, B3 및 엽산)은 파킨슨병 및 알츠하이머병과 같은 신경퇴행성 질환의 병리에 관여합니다[217]. 비타민 외에도 과일과 채소에 함유된 식물성 화학물질은 높은 항산화 능력을 보여주며 파킨슨병에 대한 잠재적 신경보호 효과를 가질 수 있습니다[218].
노인 인구는 대사 활동 감소, 소화 능력 및 흡수력 저하, 인지 기능 감퇴 등 전반적인 신체 기능 저하로 인해 영양실조 위험이 더 높습니다[219]. 따라서 노인은 영양 불균형과 관련된 질환에 걸릴 가능성이 더 큽니다. 식이 항산화제는 자유 라디칼 생성을 억제하는 능력으로 인해 노화 방지 역할을 하는 것으로 보입니다[220]. 녹색 잎채소와 십자화과 채소를 더 많이 섭취하는 여성은 인지 기능 저하가 덜한 것으로 밝혀졌다[219]. 녹색 및 노란색 채소 섭취량이 높은 것은 일본 여성의 피부 노화 속도 둔화와도 연관성이 있었다[221]. 과일 및 채소 추출물 보충은 노인 대상자의 면역 기능 여러 지표를 유의미하게 개선한다[222].
산화 스트레스와 연관된 장 염증은 염증성 장 질환 등 다양한 위장관 질환에서 중요한 역할을 한다[223,224]. 염증성 장 증후군 환자에서는 영양실조로 인한 효소 항산화제 및 비타민 수치 저하가 관찰되었다[205]. 항산화제 사용은 산화환원 균형을 회복시켜 장 손상을 완화하고 건강한 위장관을 유지하는 것으로 나타났다[223].
항산화제가 풍부한 과일과 채소는 여러 유형의 암에 대해 보호 효과를 발휘한다[225]. 약 35%의 암은 식이 조절을 통해 예방 가능하다[226]. 폴리페놀을 함유한 식물성 식품은 폐암, 유방암, 설암, 위암, 후두암, 대장암 및 전립선암에 효과적인 항암 활성을 지닌다는 것이 입증되었다[227,228]. 페놀 함량이 높은 과일은 페놀 화합물의 방향족 고리 내 하이드록실 그룹을 치환시키는 강력한 항산화 특성을 지닌다[229].
단, 많은 식이성 폴리페놀은 세포 실험에서는 유효하나 동물 및 인간에서는 효과가 없다는 점을 강조해야 한다. 예를 들어 매년 통제된 조건 하에서 다양한 종양 세포주에 대한 폴리페놀의 항암 활성 보고가 다수 발표된다[230]. 그러나 임상적으로 항종양제로 인정받는 폴리페놀은 극소수에 불과하다[231]. 식이성 폴리페놀과 암세포주를 대상으로 한 전형적인 세포독성 또는 증식 실험에서는 단일 폴리페놀 또는 폴리페놀이 풍부한 추출물을 세포와 24~72시간 동안만 배양한다[232,233,234]. 다시 말해, 가장 생물학적 활성이 높은 화합물로 여겨지는 케르세틴은 다양한 암 세포주(A549 세포 [235], HeLa 세포 [216], HT29 및 HCT15 세포 [236], PATU-8988 세포 [237])에서 세포 성장 억제 및 세포 사멸(아포토시스), 괴사, 자가포식(autophagy)을 유도한다고 주장되어 왔습니다. 그러나 케르세틴은 물에 상대적으로 불용성이며 생리적 시스템에서 불안정하여 생체 이용률이 매우 낮습니다 [238,239]. 케르세틴의 효능을 입증하는 임상 연구는 존재하지 않습니다 [240].
식이와 암의 관계에 대한 무작위 대조 시험이 부족한 것은 윤리적 이유로 전체 식이 개입이 어렵기 때문입니다 [241]. 따라서 암 위험을 줄이기 위한 일반적인 권고 사항은 과일, 채소, 곡물이 풍부한 식단, 적색육과 알코올 섭취 감소, 건강한 생활습관이다[241].
따라서 질병 예방 및 치료에 항산화제를 사용하는 것과 관련하여 여전히 많은 문제가 해결되지 않은 상태이다. 일부 연구 결과는 항산화제가 질병 통제에 유리한 효과를 발휘하지 못함을 시사한다. 다양한 질병의 발병 기전에서 ROS의 정확한 역할은 아직 명확히 밝혀지지 않았다. 외인성으로 투여된 대부분의 항산화제는 선택적이지 않거나 세포나 조직의 다양한 부위에 균일하게 분포되지 않는다[242,243]. 최적의 영양을 위해 필요한 항산화 영양소의 섭취 수준(역치 수준)은 여전히 불분명하며, 인체 내 항산화제의 생체 이용률에 대한 정보도 거의 없다[244,245]. 항산화제의 비특이성과 가능한 상호작용[245,246]은 산화 스트레스 관련 질환 치료에서 그 효과가 미미한 이유를 설명할 수 있다. 따라서 정확한 치료 효과를 집중시키기 위해 혁신적인 표적 항산화제 개발에 주력할 것을 제안한다[243,247].
4. Conclusions
Free radicals are produced by various normal endogenous and exogenous cell processes. Mitochondria are the main source of endogenous cellular ROS, which, in high concentrations, may damage macromolecules such as DNA, proteins and lipids. Such damage has been implicated in the development of various pathological disorders, including cancer and inflammatory, respiratory, cardiovascular, neurodegenerative and digestive-tract diseases. The body has innate antioxidant defenses against free radicals. Recent nutritional recommendations include a diet rich in fruit, vegetables and grains. Dietary antioxidants are considered useful in the prevention and treatment of disease, although some studies indicate that they are not particularly effective in the control of disease. Many questions regarding antioxidant supplementation and disease prevention remain unanswered. Further research is needed before antioxidant supplements can be recommended as adjuvant therapy.
4. 결론
자유 라디칼은 다양한 정상적인 내인성 및 외인성 세포 과정에서 생성됩니다. 미토콘드리아는 내인성 세포 ROS의 주요 공급원으로, 고농도에서는 DNA, 단백질, 지질과 같은 거대분자를 손상시킬 수 있습니다. 이러한 손상은 암, 염증성 질환, 호흡기 질환, 심혈관 질환, 신경퇴행성 질환, 소화관 질환 등 다양한 병리적 장애의 발병과 연관되어 있습니다. 인체는 자유 라디칼에 대한 선천적 항산화 방어 체계를 갖추고 있다. 최근 영양 권장사항에는 과일, 채소, 곡물이 풍부한 식단이 포함된다. 식이 항산화제는 질병 예방 및 치료에 유용한 것으로 간주되나, 일부 연구에서는 질병 통제에 특별히 효과적이지 않다고 지적한다. 항산화제 보충과 질병 예방에 관한 많은 의문점은 아직 해결되지 않았다. 항산화제 보충제를 보조 요법으로 권장하기 전에 추가 연구가 필요하다.
Author Contributions
Conceptualization, writing and review of draft, G.M.; critical revision of manuscript, C.C.; literature review, writing of some paragraphs and editing, M.M., L.D. and P.N.; conceptualization, supervision, review and funding acquisition, A.G.D. All authors have read and agreed to the published version of the manuscript.
Funding
This study was funded by the Innovation and Competitiveness Cooperation Programme Interreg V/A Greece-Italy (EL-IT) 2014–2020 co-financed by the European Regional Development Fund (ERDF)—INNO.TRITION (Mis. Code: 5003778).
Conflicts of Interest
The authors declare no conflict of interest.
References
- Michaelis, L. Free radicals as intermediate steps of oxidation- reduction. Cold Spring Harb. Symp. Quant. Biol. 1939, 7, 33–49. [Google Scholar] [CrossRef]
- Gerschman, R.; Gilbert, D.L.; Nye, S.W.; Dwyer, P.; Fenn, W.O. Oxygen poisoning and X-irradiation: A mechanism in common. Science 1954, 119, 62362–62366. [Google Scholar] [CrossRef] [PubMed]
- McCord, J.M.; Fridovich, I. Superoxide dismutase, an enzymic function for erythrocuprein (hemocuprein). J. Biol. Chem. 1969, 244, 6049–6055. [Google Scholar] [CrossRef]
- Loschen, G.; Flohe, L.; Chance, B. Respiratory chain linked H2O2 production in pigeon heart mitochondria. FEBS Lett. 1971, 18, 261–264. [Google Scholar] [CrossRef]
- Halliwell, B.; Gutteridge, J.M. Role of free radicals and catalytic metal ions in human disease: An overview. Methods Enzymol. 1990, 186, 1–85. [Google Scholar] [CrossRef]
- Palmer, R.M.; Rees, D.D.; Ashton, D.S.; Moncada, S. L-arginine is the physiological precursor for the formation of nitric oxide in endothelium-dependent relaxation. Biochem. Biophys. Res. Commun. 1988, 153, 1251–1256. [Google Scholar] [CrossRef]
- Ferrari, C.K.; Souto, P.C.; França, E.L.; Honorio-França, A.C. Oxidative and nitrosative stress on phagocytes’ function: From effective defense to immunity evasion mechanisms. Arch. Immunol. Ther. Exp. 2011, 59, 441–448. [Google Scholar] [CrossRef]
- Stone, J.R.; Yang, S. Hydrogen peroxide: A signaling messenger. Antioxid. Redox Signal. 2006, 243–270. [Google Scholar] [CrossRef]
- Pham-Huy, L.A.; He, H.; Pham-Huy, C. Free radicals, antioxidants in disease and health. Int. J. Biomed. Sci. 2008, 4, 89–96. [Google Scholar]
- Halliwell, B.; Gutteridge, J.M.C. Free Radicals in Biology and Medicine, 4th ed.; Halliwell, B., Gutteridge, J.M.C., Eds.; Oxford University Press: New York, NY, USA, 2007. [Google Scholar]
- Kohen, R.; Nyska, A. Oxidation of biological systems: Oxidative stress and antioxidants. Toxicol. Pathol. 2002, 30, 620–630. [Google Scholar] [CrossRef]
- Halliwell, B. Reactive species and antioxidants. Redox biology is a fundamental theme of aerobic life. Plant Physiol. 2006, 141, 312–322. [Google Scholar] [CrossRef] [PubMed]
- Glasauer, A.; Chandel, N.S. ROS. Curr. Biol. 2013, 23, R100–R102. [Google Scholar] [CrossRef] [PubMed]