chemical barrier
- 보체시스템의 탐구!!
- 보체 시스템이 문제가 되어 면역 불균형을 야기하는 지점이 어디인가? 간경화!!

Liver Cirrhosis: The Immunocompromised State
by
Elda Victoria Rodríguez-Negrete
1,2,
Marisol Gálvez-Martínez
1,
Karina Sánchez-Reyes
3,
Carlos Fernando Fajardo-Felix
1,
Karla Erika Pérez-Reséndiz
1,
Eduardo Osiris Madrigal-Santillán
2
1
Servicio de Gastroenterología, Hospital de Especialidades, Centro Médico Nacional Siglo XXI, Ciudad de México 06720, Mexico
2
Laboratorio de Medicina de Conservación, Escuela Superior de Medicina, Instituto Politécnico Nacional, Mexico City 11340, Mexico
3
Servicio de Cirugía General, Hospital de Especialidades, Centro Médico Nacional Siglo XXI, Ciudad de México 06720, Mexico
4
Escuela Superior de Cómputo, Instituto Politécnico Nacional, Unidad Profesional “A. López Mateos”, Ciudad de México 07738, Mexico
*
Author to whom correspondence should be addressed.
J. Clin. Med. 2024, 13(18), 5582; https://doi.org/10.3390/jcm13185582
Submission received: 26 July 2024 / Revised: 11 September 2024 / Accepted: 17 September 2024 / Published: 20 September 2024
(This article belongs to the Section Gastroenterology & Hepatopancreatobiliary Medicine)
Downloadkeyboard_arrow_down
Abstract
Systemic inflammation and immunodeficiency are important components of cirrhosis-associated immune dysfunction (CAID), the severity of which is dynamic, progressive, and associated with the greater deterioration of liver function. Two inflammation phenotypes have been described: low-grade and high-grade systemic inflammation. Both of these phenotypes are related to liver cirrhosis function; thus, high-grade inflammation is correlated with the severity of hepatic insufficiency, bacterial translocation, and organic insufficiency, with which the risk of infections increases and the prognosis worsens. Bacterial translocation (BT) plays a relevant role in persistent systemic inflammation in patients with cirrhosis, and the prophylactic employment of antibiotics is useful for reducing events of infection and mortality.
초록
전신성 염증과 면역결핍은
간경변증 관련 면역기능장애(CAID)의 중요한 구성 요소이며,
그 중증도는 동적이며 진행성이고
간 기능의 더 큰 악화와 연관되어 있다.
두 가지 염증 표현형이 기술되어 있다:
저등급 및 고등급 전신성 염증.
이 두 표현형 모두 간경변증 기능과 관련이 있으며,
고등급 염증은 간부전, 세균 이동, 장기부전과 상관관계를 보이며,
이로 인해 감염 위험이 증가하고 예후가 악화된다.
세균 이동(BT)은
간경변증 환자의 지속적 전신 염증에 중요한 역할을 하며,
항생제의 예방적 사용은 감염 발생률과 사망률을 감소시키는 데 유용하다.
Keywords:
liver cirrhosis; cirrhosis-associated immune dysfunction; systemic inflammation; bacterial translocation
1. Introduction
Liver cirrhosis is a chronic disease (because it generates complications such as portal hypertension and the development of hepatocellular carcinoma), and it is associated with frequent hospitalizations and high mortality; it represents 1.2 million deaths annually worldwide and is the 14th leading cause of death worldwide [1].
Cirrhosis is classified into two stages: compensated cirrhosis and decompensated cirrhosis. Acute decompensation (AD) involves the development of an acute complication (e.g., ascites, variceal hemorrhage, hepatic encephalopathy), and the first event of AD marks the transition from compensated to decompensated cirrhosis. The evolution of decompensated cirrhosis is characterized by repeated episodes of AD in which patients are prone to developing bacterial infections [2]. Finally, Acute-on-Chronic Liver Failure (ACLF) is the presence of insufficiency of an organic system or multiple organic systems, with high short-term mortality, and always occurs within the context of AD. Systemic inflammation (SI) is a well-recognized characteristic of decompensated cirrhosis [2]. Cirrhosis affects various organs and systems, including the immune system [3], is considered an immunocompromised state that increases the risk of infections, and has an approximate mortality of 30% [4]. The term cirrhosis-associated immune dysfunction (CAID) is characterized by two important components: immunodeficiency due to an altered response to pathogens and systemic inflammation as a consequence of a persistent and inadequate stimulation of the immune system. CAID should be considered a complication of cirrhosis of any etiology [5], a multifactorial state that diminishes the patient’s capacity to eliminate bacteria, cytokines, and endotoxins from the circulation [6].
1. 서론
간경변증은
만성 질환(문맥 고혈압 및 간세포암 발생과 같은 합병증을 유발하기 때문)으로,
빈번한 입원과 높은 사망률과 연관되어 있으며,
전 세계적으로 연간 120만 명의 사망을 초래하여 전 세계 사망 원인 14위를 차지합니다 [1].
간경변은 두 단계로 분류됩니다:
보상성 간경변증과
비보상성 간경변증이다.
compensated cirrhosis and
decompensated cirrhosis.
https://pmc.ncbi.nlm.nih.gov/articles/PMC10523240/

급성 비보상(AD)은
급성 합병증(예: 복수, 정맥류 출혈, 간성 뇌병증)의 발생을 수반하며,
첫 AD 사건은 보상성 간경변증에서 비보상성 간경변증으로의 전환을 의미한다.
비보상성 간경변증의 진행은
반복적인 AD 에피소드로 특징지어지며,
이 과정에서 환자는 세균 감염에 취약해진다 [2].
마지막으로,
만성 간부전 위상에서 발생한 급성 간부전(ACLF)은
단기 사망률이 높은 장기 시스템 또는 다중 장기 시스템의 기능 부전을 의미하며,
항상 AD의 맥락에서 발생합니다.
전신성 염증(SI)은
비보상성 간경변의 잘 알려진 특징이다[2].
간경변은
면역계를 포함한 다양한 장기 및 시스템에 영향을 미치며[3],
감염 위험을 증가시키는 면역결핍 상태로 간주되며,
약 30%의 사망률을 보인다[4].
간경변증 관련 면역 기능 장애(CAID)라는 용어는
두 가지 중요한 구성 요소로 특징지어집니다:
병원체에 대한 반응 변화로 인한 면역 결핍과
면역계의 지속적이고 부적절한 자극의 결과로서의 전신성 염증입니다.
CAID는
모든 원인에 의한 간경변증의 합병증으로 간주되어야 합니다[5],
이는 환자의 순환계에서
박테리아, 사이토카인 및 내독소를 제거하는 능력을 저하시키는 다인성 상태입니다[6].
1.1. Immunological Role of Resident Cells in the Liver
The liver is a component of the innate immunological system, which contains 90% of the body’s reticuloendothelial (RE) cells [7,8]. Within the liver, antigen-presenting cells (APCs); T and B cells; natural killer (NK) cells; and finally monocytes control the local and systemic inflammatory response and, thus, are fundamental for the elimination of bacteria. Hepatocytes serve as APCs because they show major histocompatibility complex (MHC) type I and II [9]. In a sterile injury, the release of DAMPs from necrotic cells triggers the recruitment of innate immune cells [8,10]. In healthy patients, during an acute phase or systemic inflammatory response, a variety of pro-inflammatory cytokines (IL-6, IL-1, TNF, and IFN-γ) can stimulate hepatocytes to produce high levels of complements and PRRs (recognition receptors of patterns); however, this is altered in patients with liver cirrhosis [8,11].
Progressive damage to liver tissue (parenchymal and non-parenchymal cells) decreases the activity of the mononuclear phagocytic system, leading to an increased risk of infections and mortality [3,12]. Furthermore, intrahepatic shunts through vascularized septa prevent systemic and portal bacteria from being filtered and eliminated by Kupffer cells [13]. Associated with this is the loss of hepatocytes, which diminishes the synthesis of proteins (albumin and acute phase protein) and immune receptors (complement components, soluble PRRs) [14]. The serum concentrations of C3 and C4, as well as the hemolytic activity of the complement, are reduced in patients with decompensated cirrhosis compared to controls; these alterations predispose to infectious processes and confer higher mortality in patients with alcoholic cirrhosis [15].
1.1. 간 내 상주 세포의 면역학적 역할
간은 선천성 면역 체계의 구성 요소로,
신체 내 망상내피계(RE) 세포의 90%를 포함한다[7,8].
The liver is a component of the innate immunological system,
which contains 90% of the body’s reticuloendothelial (RE) cells
간 내에서는 항원제시세포(APC);
T 및 B 세포; 자연살해(NK) 세포; 그리고 마지막으로
단핵구가 국소 및 전신 염증 반응을 조절하며,
따라서 세균 제거에 근본적인 역할을 한다.
간세포는
주요조직적합성복합체(MHC) I형 및 II형을 발현하므로
항원제시세포로 기능한다[9].
무균성 손상 시 괴사 세포로부터의 손상유래분자(DAMPs) 방출은
건강한 환자의 급성기 또는 전신성 염증 반응 시
다양한 전염증성 사이토카인(IL-6, IL-1, TNF, IFN-γ)이
간세포를 자극하여 높은 수준의 보체 및 패턴 인식 수용체(PRR)를 생성하게 하지만,
간 조직(실질 세포 및 비실질 세포)의 진행성 손상은
단핵 식세포계의 활성을 감소시켜 감염 및 사망 위험을 증가시킵니다[3,12].
또한 혈관화된 격막을 통한 간내 단락은
전신 및 문맥 세균이 쿠퍼 세포에 의해 여과 및 제거되는 것을 방해합니다[13].
이와 함께 간세포의 손실은
단백질(알부민 및 급성기 단백질)과 면역 수용체(보체 성분, 용해성 PRR)의 합성을
감소시킵니다 [14].
보체 C3 및 C4의 혈청 농도와 용혈 활성은 대조군에 비해
비보상성 간경변증 환자에서 감소하며,
이러한 변화는 감염 과정에 취약하게 하고
알코올성 간경변증 환자에게 더 높은 사망률을 초래합니다 [15].
https://pmc.ncbi.nlm.nih.gov/articles/PMC8560502/

1.2. Systemic Inflammation in Cirrhosis
Pathogen-associated molecular patterns (PAMPs) are molecules derived from bacteria, such as lipopolysaccharides (LPSs) from Gram-negative bacteria, lipoteichoic acid from Gram-positive bacteria, and DNA regions, as well as viruses. Danger-associated molecular patterns (DAMPs) are molecules found inside cells and released by damaged cells [3,8]. Inflammation is a physiological response that restores homeostasis after multiple aggressions, for example, bacterial infections or tissue lesions; similarly, it may originate from recognizing distinctive bacteria-derived molecules (LPSs), described as PAMPs [3,16]. PAMPs and DAMPs bind with PRRs (pattern-recognition receptors) that are expressed in epithelial and peripheral innate immune cells. PRRs can be localized on the cellular surface (the type-4 Toll-like [TLR4]), the endolysosome (TLR9), or the cytosol (Nucleotide Oligomerization Dominion [NOD] 1) [3,17]. Once DAMPs and PAMPs reach the liver, they are recognized by PRRs, and pro-inflammatory signaling pathways are activated that aim to restore homeostasis through the release of pro-inflammatory cytokines (TNF; IL-1 β; IL-6; IFN-γ; IL-17; monocyte chemotactic protein type 1; macrophage inflammatory protein beta; the activation of neutrophils; monocytes; T lymphocytes; and the activation of endothelial molecules such as cell-adhesion molecule type 1 (ICAM-1), vascular adhesion type 1 (VCAM 1), endothelial growth factor (VEGF), Von Willebrand factor (vWF), and nitrates) and C-Reactive Protein (CRP) [3,18]. PAMPs in the intestinal lumen are recognized by PRRs in gut-associated lymphoid tissue (GALT) and mesenteric lymph nodes. The latter leads to gene expression through activating immune cells to produce molecules responsible for intestinal inflammation and finally extends to the systemic circulation and the peripheral organs [19]. The PAMP-induced inflammatory response is indispensable for combating invasive bacteria; however, an excessive or chronic response can cause collateral tissue damage (immunopathology) and provoke a marked compensatory anti-inflammatory response that, in the latter instance, leads to immune suppression and a greater risk of secondary infections and, with that, greater mortality [20] (Figure 1).
1.2. 간경변증에서의 전신성 염증
병원체 관련 분자 패턴(PAMPs)은
그람 음성균의 지질다당류(LPS),
그람 양성균의 리포테이코산,
DNA 영역 및 바이러스와 같은 세균에서 유래한 분자들이다.
손상 관련 분자 패턴(DAMPs)은
세포 내부에 존재하며
염증은
세균 감염이나 조직 손상과 같은 다양한 공격 후 항상성을 회복하는 생리적 반응이다.
마찬가지로,
PAMPs로 설명되는 세균 유래 분자(LPS)의 인식에서 비롯될 수도 있다[3,16].
PAMPs와 DAMPs는
상피 및 말초 선천성 면역 세포에 발현되는
PRRs(패턴 인식 수용체)와 결합합니다.
PRRs는
세포 표면(4형 Toll-like [TLR4]), 내소체(TLR9),
또는 세포질(뉴클레오티드 올리고머화 도메인 [NOD] 1)에 위치할 수 있습니다[3,17].
DAMPs와 PAMPs가
간에 도달하면 PRR에 의해 인식되어,
다음과 같은 염증성 사이토카인
(TNF; IL-1β; IL-6; IFN-γ; IL-17;
단핵구 화학유인인자 1형; 대식세포 염증 단백질 베타; 호중구 활성화;
단핵구; T 림프구; 그리고 세포접착분자 1형(ICAM-1), 혈관접착분자 1형(VCAM-1),
내피성장인자(VEGF),
폰 빌레브란트 인자(vWF),
질산염 등의 내피 분자 활성화) 및
C-반응성 단백질(CRP)의 분비를 통해 항상성을 회복시키려는 목적으로 활성화됩니다 [3,18].
장 내강 내 PAMP는
장 관련 림프 조직(GALT) 및 장간막 림프절의 PRR에 의해 인식된다.
후자는
면역 세포를 활성화하여 장 염증을 유발하는 분자를 생성하도록 하여
유전자 발현을 유도하며,
결국 전신 순환계와 말초 기관으로 확산된다 [19].
PAMP에 의한 염증 반응은
침습성 세균 퇴치에 필수적이지만,
과도하거나 만성적인 반응은 부수적 조직 손상(면역병리학)을 유발하고
현저한 보상성 항염증 반응을 촉발할 수 있다.
후자의 경우 면역 억제를 초래하여
이차 감염 위험 증가와 함께 사망률 상승으로 이어진다[20] (그림 1).
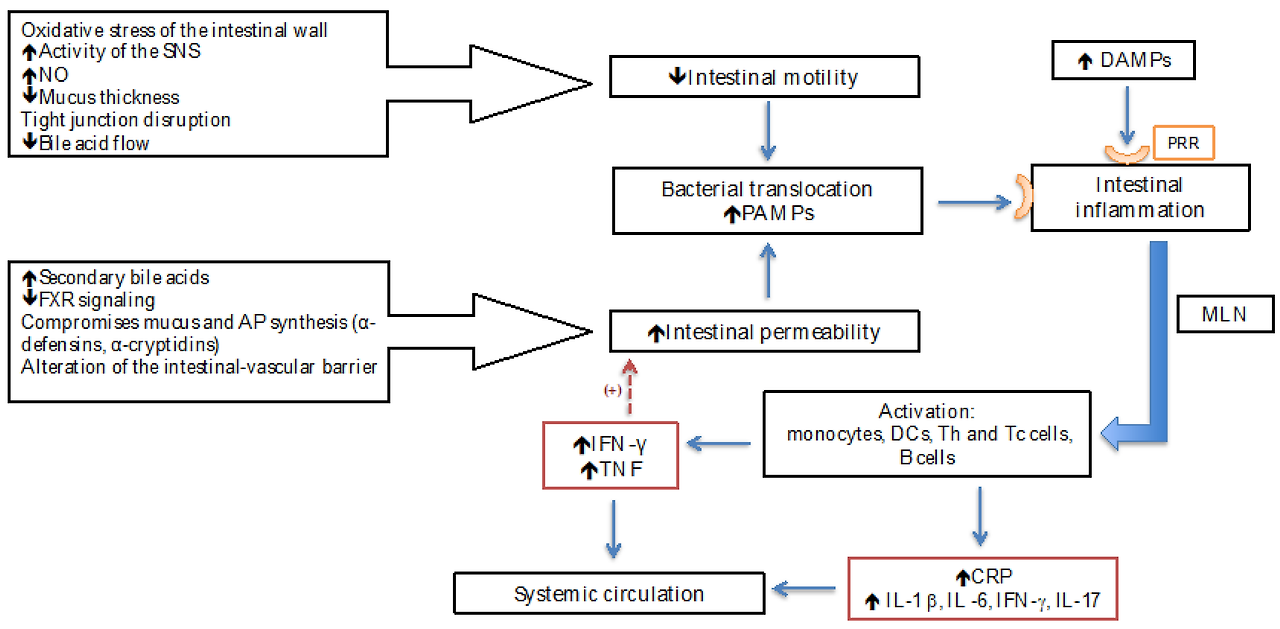
Figure 1. Changes in intestinal motility and permeability in liver cirrhosis contribute to the promotion of bacterial translocation and increased presence of PAMPs. Concurrently, DAMPs are released from necrotic cells, and both PAMPs and DAMPs are recognized by PRRs, triggering intestinal inflammation and subsequently leading to systemic inflammation due to the release of pro-inflammatory cytokines and acute phase proteins. PAMPs: pathogen-associated molecular patterns; DAMPs: danger-associated molecular patterns; PRRs: pattern-recognition receptors; SNS: Sympathetic Nervous System; FXR: farnesoid X receptor; APs: antimicrobial peptides; DCs: dendritic cells; MLNs: mesenteric lymph nodes; CRP: C-Reactive Protein; NO: nitric oxide.
그림 1. 간경변증에서 장 운동성과 투과성의 변화는 세균 전위 촉진 및 PAMP 증가에 기여한다.
동시에 괴사 세포로부터 DAMP가 방출되며,
PAMP와 DAMP 모두 PRR에 의해 인식되어 장 염증을 유발하고,
이후 전신 염증으로 이어진다.
이는 전염증성 사이토카인과 급성기 단백질의 방출로 인해 발생한다.
PAMPs: 병원체 관련 분자 패턴; DAMPs: 위험 관련 분자 패턴; PRRs: 패턴 인식 수용체; SNS: 교감 신경계; FXR: 파네소이드 X 수용체; APs: 항균 펩타이드; DCs: 수지상 세포; MLNs: 장간막 림프절; CRP: C-반응성 단백질; NO: 산화질소.
1.3. Evidence of Systemic Inflammation
Cirrhosis is associated with SI, as evidenced by increased white blood cell count, neutrophils, activated circulating monocytes, plasma CRP, pro-inflammatory cytokines, macrophage activation markers, and systemic oxidative stress [17].
As liver function deteriorates, systemic inflammation increases; this is characteristic of CAID [3]. Short-term mortality (3 months) in ACLF has been associated with the activation of mediators of leukocyte adhesion and migration (VCAM1, ICAM1, granulocyte, and macrophage colony-stimulating factor [GM-CSF]) [21].
1.3. 전신성 염증의 증거
간경변증은
백혈구 수, 호중구, 활성화된 순환 단핵구, 혈장 CRP, 전염증성 사이토카인,
대식세포 활성화 마커 및 전신성 산화 스트레스의 증가로 입증되듯이
전신성 염증(SI)과 관련이 있습니다[17].
간 기능이 악화됨에 따라 전신 염증이 증가하며,
이는 CAID의 특징이다 [3].
ACLF의 단기 사망률(3개월)은
백혈구 부착 및 이동 매개체(VCAM1, ICAM1,
과립구 및 대식세포 군집 자극 인자[GM-CSF])의 활성화와 관련이 있다 [21].
1.3.1. Low-Grade Systemic Inflammation
BT is defined as the passage of viable bacteria or bacterial subproducts through the intestinal mucosa to the systemic circulation [2]. In cirrhosis, intestinal permeability increases due to the modification of the mucosal lining, the intercellular binding proteins, the loss of epithelial tight junction proteins through TNF receptor-I-mediated activation of myosin light-chain kinase, and the endothelial cells. In addition, the excessive growth of bacteria and dysbiosis favors the arrival of bacteria and their products into the systemic and portal circulation [22,23].
In healthy patients, gut bacteria reside in a symbiotic state along with the host; dysbiosis is the quantitative and/or qualitative change in the microbiota and occurs due to the modification of intestinal homeostasis [17]. Liver cirrhosis is associated with both an overgrowth of intestinal bacteria and dysbiosis, in the sense that native bacteria decrease and potentially pathogenic bacteria increase; for example, there are fewer Bacteroidetes but more Proteobacteria and Fusobacteria [24]. Another common intestinal characteristic of cirrhosis is an altered intestinal barrier, which leads to pathological BT [25]. Hypergammaglobulinemia, which is common in decompensated cirrhosis, is a sign of escape of intestinal antigens into the systemic circulation and correlates with clinical outcomes [2]. BT and SI are continually present in patients who are non-infected with decompensated cirrhosis [2,26].
Infections increase mortality by four times among patients with cirrhosis; 30% of cases occur within the first month after the infectious process, and 63% of patients die within 1 year. The Odds Ratio (OR) for dying in infected vs. non-infected patients is 3.75 (95% Confidence Interval [CI]: 2.12–4.23) [27]. Patients with cirrhosis who are hospitalized exhibit a greater risk of becoming infected, particularly those with gastrointestinal (GI) bleeding. A 2001 study identified 34% (n = 150) of bacterial infections in patients admitted with cirrhosis (89 were community-acquired, and 61 were hospital-acquired), where the urinary tract was the most frequent site of infection (41%); 60% of cases at the time of admission already had an infectious process, and 40% occurred during hospitalization, where the prevalence of bacterial peritonitis was 12%. However, it is noteworthy that 51% of bacterial peritonitis was found in asymptomatic patients; the main bacteria found were Gram-negative [28].
Since 1996, the effectiveness of antibiotic treatment has been evaluated in preventing bacterial infections after hemorrhage in patients with cirrhosis. In one study, three groups were assigned: group 1 included patients with Child–Pugh A or B without bleeding (without antibiotic prophylaxis); group 2 included patients with Child–Pugh A or B and bleeding events, as well as patients with Child–Pugh C with hemorrhage without antibiotic prophylaxis; and group 3 included patients with Child–Pugh C with hemorrhage and antibiotic prophylaxis for 10 days. The incidence of bacterial infection was significantly higher in patients in group 2 than in those of group 1, and infections were more severe in group 2; however, when comparing mortality between groups 2 (23.5%) and 3 (13.3%) during the first 4 weeks, there was no significant difference [29].
In the PREDICT study, 1071 patients with AD were included; three groups of patients were identified, with a differential white blood cell count and CRP levels (as markers of inflammation); patients with pre-ACLF (n = 218) and who developed ACLF during the first hospitalization (20%) had a mortality rate of 53.7% at 3 months and 67.4% at 1 year. Patients with unstable decompensated cirrhosis (n= 233) and who required hospitalizations on several occasions without developing ACLF had lower mortality rates at 3 months (21%) and at 1 year (35.6%). Patients with stable decompensated cirrhosis (n = 620) who did not require hospitalization or develop ACLF had a 1-year mortality rate of 9.5% [30].
1.3.1. 저등급 전신성 염증
BT는 생존 가능한 세균 또는 세균 부산물이 장 점막을 통과하여 전신 순환계로 유입되는 현상으로 정의된다[2]. 간경변에서는 점막 내피, 세포간 결합 단백질의 변화, TNF 수용체-I 매개 마이오신 경쇄 키나아제 활성화에 의한 상피 세포 간 밀착 연결 단백질의 손실, 그리고 내피 세포의 변화로 인해 장 투과성이 증가한다. 또한 세균의 과도한 증식과 장내 미생물 불균형은 세균 및 그 대사 산물이 전신 및 문맥 순환계로 유입되는 것을 촉진한다 [22,23].
건강한 환자의 경우 장내 세균은 숙주와 공생 상태를 유지한다; 장내 미생물 불균형은 미생물 군집의 양적 및/또는 질적 변화를 의미하며, 장내 항상성 변화로 인해 발생한다 [17]. 간경변증은 장내 세균의 과잉 증식과 장내 미생물 불균형 모두와 연관되어 있으며, 이는 토착 세균이 감소하고 잠재적 병원성 세균이 증가한다는 의미에서 나타납니다. 예를 들어, 박테로이데테스(Bacteroidetes)는 감소하지만 프로테오박테리아(Proteobacteria)와 푸소박테리아(Fusobacteria)는 증가합니다[24]. 간경변증의 또 다른 흔한 장 특성은 장 장벽 기능 변화로, 이는 병리학적 장-혈관 누출(BT)로 이어진다[25]. 비보상성 간경변증에서 흔히 관찰되는 고감마글로불린혈증은 장 항원이 전신 순환계로 유출된 징후이며 임상적 결과와 상관관계가 있다[2]. 비감염성 비보상성 간경변증 환자에서는 장-혈관 누출(BT)과 장-혈관 누출 증후군(SI)이 지속적으로 관찰된다[2,26].
간경변증 환자에서 감염은 사망률을 4배 증가시키며, 감염 발생 후 첫 달 내 30%의 사례가 발생하고 63%의 환자가 1년 이내에 사망한다. 감염 환자 대비 비감염 환자의 사망 오즈비(OR)는 3.75(95% 신뢰구간 [CI]: 2.12–4.23)이다 [27]. 입원한 간경변 환자는 감염 위험이 더 높으며, 특히 위장관(GI) 출혈이 있는 환자가 그렇다. 2001년 연구에 따르면 간경변으로 입원한 환자에서 세균 감염이 34%(n = 150) 확인되었으며(89건은 지역사회 감염, 61건은 병원 감염), 요로가 가장 흔한 감염 부위(41%)였다 . 입원 시점의 60% 사례는 이미 감염 과정이 진행 중이었으며, 40%는 입원 중 발생했다. 이 중 세균성 복막염 유병률은 12%였다. 그러나 주목할 점은 세균성 복막염의 51%가 무증상 환자에서 발견되었다는 것이다. 주요 병원균은 그람 음성균이었다 [28].
1996년 이후 간경변 환자의 출혈 후 세균 감염 예방을 위한 항생제 치료 효과가 평가되어 왔다. 한 연구에서는 세 그룹으로 분류했다: 그룹 1은 출혈이 없는 Child–Pugh A 또는 B 단계 환자(항생제 예방요법 미적용); 그룹 2는 Child–Pugh A 또는 B 등급의 출혈 환자 및 항생제 예방적 투여를 받지 않은 Child–Pugh C 등급 출혈 환자; 그룹 3은 항생제 예방적 투여를 10일간 받은 Child–Pugh C 등급 출혈 환자였다. 그룹 2 환자의 세균 감염 발생률은 그룹 1보다 유의하게 높았으며, 감염의 중증도 또한 그룹 2에서 더 심했다; 그러나 첫 4주 동안 그룹 2(23.5%)와 그룹 3(13.3%)의 사망률을 비교했을 때 유의미한 차이는 없었다 [29].
PREDICT 연구에서는 1071명의 AD 환자가 포함되었으며; 백혈구 수치와 CRP 수치(염증 지표)에 따라 세 그룹으로 분류되었으며, ACLF 전 단계 환자(n=218) 중 첫 입원 중 ACLF가 발생한 환자(20%)의 3개월 사망률은 53.7%, 1년 사망률은 67.4%였다. 불안정성 비보상성 간경변증 환자(n=233)는 ACLF를 발병하지 않은 상태에서 여러 차례 입원이 필요했으나, 3개월(21%) 및 1년(35.6%) 사망률이 더 낮았다 . 입원이 필요하지 않거나 ACLF를 발병하지 않은 안정된 비보상성 간경변 환자(n = 620)의 1년 사망률은 9.5%였다 [30].
1.3.2. High-Grade Systemic Inflammation
Bacterial infections are the most common trigger of ACLF [6]. The chronic consumption of alcohol alters the intestinal barrier, promoting dysbiosis, altering the tight junctions, decreasing the mucous thickness, reducing intestinal farnesoid X receptor (FXR), and diminishing the production of antimicrobial peptides (which play a crucial role in the innate immunity of the host against a broad range of microorganisms). In ACLF, there is an increase in BT [31,32]. Alcohol alters innate and adaptive responses; similarly, dietary factors (fructose, saturated fats, trans fats, and cholesterol) trigger inflammation via lipotoxic effects, alterations in mitochondrial function, and oxidative and endoplasmic reticulum stress [33].
1.3.2. 고도 전신성 염증
세균 감염은
ACLF의 가장 흔한 유발 요인이다 [6].
만성적인 알코올 섭취는 장벽 기능을 변화시켜 장내 미생물 불균형을 촉진하고,
단단한 접합부를 변화시키며,
점액 두께를 감소시키고,
장 내 파네소이드 X 수용체(FXR)를 감소시키며,
항균 펩타이드(광범위한 미생물에 대한 숙주의 선천적 면역에서 중요한 역할을 함)의 생산을
감소시킵니다.
알코올은 선천적 및 후천적 반응을 변화시킵니다.
마찬가지로,
식이 인자(과당, 포화 지방, 트랜스 지방, 콜레스테롤)는
지질 독성 효과, 미토콘드리아 기능 변화, 산화 및 소포체 스트레스를 통해 염증을 유발합니다 [33].
1.4. Consequences of Systemic Inflammation
Impaired peripheral, portal, and systemic vasodilatation is caused by SI and the endothelial production of nitric oxide (NO) and reactive oxygen species (ROS). Cardiac dysfunction is related to the severity of systemic circulatory dysfunction, as well as markers of SI and BT [3,34,35]. Patients with AD present persistent low-grade inflammation, with the deterioration of portal pressure and, in turn, increased 1-year mortality (35%); those with pre-ACLF exhibit a high-grade inflammation, which gives them a mortality of 67.4% [3]; with the progression of liver disease, the biomarkers of systemic inflammation increase. High-grade SI is manifested by organ failure due to tissue damage (immunopathology) or an energy imbalance (immunometabolism). In ACLF, the risk of acute renal failure increases due to microthrombosis, capillary leukocyte infiltration, and mitochondrial injury, leading to the development of ischemic acute renal tubular necrosis [3,36,37].
The degree of inflammation parallels the presence of hepatic encephalopathy and the severity of hepatic, circulatory, and renal dysfunction [6,19,38].
1.4. 전신성 염증의 결과
SI 및 내피세포의 산화질소(NO)와 활성산소종(ROS) 생성은 말초, 문맥 및 전신 혈관 확장 장애를 유발합니다. 심장 기능 장애는 전신 순환 기능 장애의 중증도뿐만 아니라 SI 및 BT의 지표와도 관련이 있습니다[3,34,35].AD 환자는 지속적인 저등급 염증을 보이며, 문맥압 악화로 인해 1년 사망률이 증가합니다(35%); 전-ACLF 환자는 고등급 염증을 나타내며, 이로 인해 사망률이 67.4%에 달합니다[3]; 간 질환이 진행됨에 따라 전신 염증 생체표지자가 증가합니다. 고등급 SI는 조직 손상(면역병리학) 또는 에너지 불균형(면역대사)으로 인한 장기 부전으로 나타난다. ACLF에서는 미세혈전증, 모세혈관 백혈구 침윤 및 미토콘드리아 손상으로 인해 급성 신부전 위험이 증가하여 허혈성 급성 신세관 괴사가 발생한다[3,36,37].
염증의 정도는 간성 뇌증의 존재와 간, 순환기 및 신장 기능 장애의 중증도와 비례한다 [6,19,38].
1.5. Immunodeficiency and Cirrhosis
The abnormalities of immune system cells compromise their effector function and cause immune paralysis (cellular immune depression), including functional defects (production of TNF-α and a diminished HLA-DR expression on monocytes), the expansion of immune inhibitors, and/or the reduced expression of costimulatory molecules (IFNγ and TNF) [39]. Immunodeficiency is a feature of CAID, present in compensated cirrhosis, but is further altered in decompensated cirrhosis, reaching its maximal point in ACLF [40].
1.5. 면역결핍과 간경변
면역계 세포의 이상은 효과기 기능을 저해하여 면역 마비(세포성 면역 억제)를 유발하며, 여기에는 기능적 결함(TNF-α 생성 및 단핵구에서의 HLA-DR 발현 감소), 면역 억제제 확장 및/또는 공자극 분자(IFNγ 및 TNF) 발현 감소가 포함됩니다 [39]. 면역결핍은 보상성 간경변에서 관찰되는 CAID의 특징이지만, 비보상성 간경변에서는 더욱 악화되어 ACLF에서 최고조에 달한다 [40].
1.6. Progressive Loss of Tolerance in Cirrhosis
A progressive deterioration of tolerance to antigen recognition in cirrhosis allows an increase in the pro-inflammatory response and contributes to chronic inflammation. In patients with compensated cirrhosis, monocytes increase their expression of HLA-DR and increase the spontaneous production of TNF (due to the alteration in the inducible suppressor of TNF) and IL-10; however, when the disease progresses—for example, patients with ACLF and acute decompensation of cirrhosis had increased numbers of MER receptor tyrosine kynase (MERKT)-expressing monocytes and macrophages—this results in a decrease in the activation of TLR and pro-inflammatory cytokines and an increase in anti-inflammatory cytokines (IL-10). MERKT negatively controls the innate immune response. In ACLF, MERKT expression was correlated with the severity of hepatic and extrahepatic disease and the systemic inflammatory response [13,41].
1.6. 간경변에서의 점진적 내성 상실
간경변에서 항원 인식에 대한 내성의 점진적 악화는 전염증 반응을 증가시키고 만성 염증에 기여한다. 보상성 간경변 환자에서는 단핵구가 HLA-DR 발현을 증가시키고 TNF(TNF 유도성 억제 인자의 변화로 인해) 및 IL-10의 자발적 생산을 증가시킨다; 그러나 질병이 진행되면(예: ACLF 및 간경변 급성 비보상 환자의 경우) MER 수용체 티로신 키나제(MERKT) 발현 단핵구 및 대식세포 수가 증가하여, 이는 TLR 활성화 및 전염증성 사이토카인 감소와 항염증성 사이토카인(IL-10) 증가로 이어진다. MERKT는 선천성 면역 반응을 음성 조절한다. ACLF에서 MERKT 발현은 간내 및 간외 질환의 중증도와 전신성 염증 반응과 상관관계를 보였다 [13,41].
1.7. Damage to Circulating Immune Cells
Immune dysfunction in cirrhosis affects the innate and adaptive immune cells, showing cellular hyperactivation and altered effector response [3] (Table 1).
1.7. 순환 면역 세포 손상
간경변증에서의 면역 기능 장애는 선천성 및 적응성 면역 세포에 영향을 미치며, 세포 과활성화 및 효과기 반응 변화를 보인다 [3] (표 1).
Table 1. Damage to the immune cells in cirrhosis [3].
Immunodeficiency is manifested by alterations in APCs (i.e., monocytes and neutrophils) and reduced phagocytic capacity; however, it is more pronounced in patients with a greater deterioration of liver function. Immunodeficiency in ACLF is due to a diminished HLA-DR expression and damage to TNF production as a consequence of LPS by monocytes and elevated levels of MERKT (receptor tyrosine kinase-expressing monocytes and macrophages), which produce IL-10 [42].
표 1. 간경변증에서의 면역 세포 손상 [3].
면역결핍은 항원제시세포(APC, 단핵구 및 호중구)의 변화와 식균능 감소로 나타납니다. 그러나 간 기능 악화가 심한 환자에서 더 두드러집니다. ACLF에서의 면역결핍은 단핵구에 의한 LPS의 결과로 HLA-DR 발현 감소 및 TNF 생산 손상과, IL-10을 생성하는 MERKT(수용체 티로신 키나아제 발현 단핵구 및 대식세포) 수치 상승으로 인해 발생한다[42].
1.8. Compensatory Anti-Inflammatory Response Syndrome (CARS)
Decreased effector activity by lymphocytes against an antigen, a decrease in cytokine production, HLA expression after monocytes stimulation, and an upregulation of anti-inflammatory cytokines define compensatory anti-inflammatory response syndrome (CARS) [43]. In a cohort of 51 patients with a diagnosis of ACLF and decompensated cirrhosis, the degree of SI (levels of IL-10, IL-6, and TNF-α) determines the outcome. In patients with ACLF, IL-10 levels are higher and correlated with a poor prognosis. In addition to IL-10, another finding is that together with the International Normalized Ratio (INR) (OR 1.7), at the moment of admission, they predict unfavorable clinical outcomes [44]. IL-10 constitutes an important part of CARS, which is closely related to the functional deactivation of monocytes, immunoparesis, and predisposition to recurrent and opportunistic infections [45].
1.8. 보상성 항염증 반응 증후군(CARS)
항원에 대한 림프구의 효과기 활성 감소, 사이토카인 생산 감소, 단핵구 자극 후 HLA 발현 감소, 항염증성 사이토카인의 상향 조절이 보상성 항염증 반응 증후군(CARS)을 정의한다 [43]. ACLF 및 비보상성 간경변증으로 진단된 51명의 환자 코호트에서, SI의 정도(IL-10, IL-6 및 TNF-α 수준)가 예후를 결정한다. ACLF 환자에서 IL-10 수준은 더 높으며 불량한 예후와 상관관계가 있다. IL-10 외에도, 입원 시점의 국제표준화비(INR) (OR 1.7)와 함께 불리한 임상 결과를 예측한다는 점이 추가로 확인되었다 [44]. IL-10은 단핵구 기능 비활성화, 면역저하, 재발성 및 기회감염에 대한 취약성과 밀접하게 연관된 CARS의 중요한 구성 요소이다 [45].
1.9. Intestinal–Liver Axis and the Intestinal Immune System
The intestinal–liver axis plays an important role in the development of CAID [3]. To maintain tolerance to harmless stimuli, interactions of the vascular barrier, intestinal epithelium, microbiota, liver, and immune system are important. Cirrhosis presents dysbiosis and increased intestinal permeability that promote BT, notably contributing to SI [3,46].
Intestinal macrophages kill the translocated bacteria; intestinal dendritic cells (DCs) transport them alive to mesenteric lymph nodes to stimulate the adaptive T-cell response; 94% of CD4 T cells are found in the GALT. Intraepithelial lymphocytes, particularly the γδ subpopulation, maintain a close relationship with intestinal epithelial cells, acting as essential mediators that balance host microbial homeostasis [4,46,47].
Intestinal motility is decreased in patients with cirrhosis, which favors overgrowth within the intestine. This, together with the portosystemic shunt, allows the perpetuation of the bacteria and can cause bacteremia [48]. This, in turn, causes greater oxidative damage due to the increase in endotoxins, pro-inflammatory cytokines, and NO [49]. Peptidoglycans, or LPSs, bind to Toll-like receptors, initiating the cellular signaling cascade and releasing cytokines (TNF-α, IL-6, and IL-1). In systemic inflammatory response syndrome (SIRS), anti-inflammatory cytokines (IL-10, IL-4, IL-13, and PGE2) balance pro-inflammatory cytokines, a process known as the “cytokine storm”, leading to excessive inflammation [50]. The development of SIRS is determined by the severity of the liver disease; this, in turn, favors the presence of variceal hemorrhage and hepatic encephalopathy and negatively affects survival [51].
In experimental models of cirrhosis, intestinal CD103+ DCs are activated when the decompensation of liver function (ascites) occurs, and there is an expansion of pro-inflammatory CD4+ DCs, which favors the increase in the production of TNF and the increase in phagocytosis and migration capacity [52]. When ascites develop, T helper cells switch to TH1, thus increasing TNF and IFNγ production in the lamina propria, with a concomitant TH17 depletion and an increase in IL-1 and IL-18 in ascites but not in serum [35,53].
In spontaneous bacterial peritonitis (SBP), there is a difference between the low microbial load in ascites and the intensity of the inflammatory response in the peritoneum, which shows a correlation between SI and prognosis [54]. During SBP, CD206 levels in ascites, but not in serum, correlate with SI, peritoneal inflammation, and mortality; the massive release of pro-inflammatory cytokines during bacterial infection contributes to SI and organ failure [55].
The use of non-absorbable antibiotics decreases NO production, inflammation, and hemodynamic alterations [56,57] and reduces endotoxemia and the severity of liver disease [3].
1.9. 장-간 축과 장 면역계
장-간 축은 CAID 발병에 중요한 역할을 한다[3]. 무해한 자극에 대한 내성을 유지하기 위해서는 혈관 장벽, 장 상피, 미생물군집, 간, 면역계의 상호작용이 중요하다. 간경변은 장내 미생물 불균형과 장 투과성 증가를 초래하여 세균의 장내 침투(BT)를 촉진하며, 특히 장내 감염(SI)에 기여한다[3,46] .
장 대식세포는 장벽을 통과한 세균을 사멸시키며, 장 수지상세포(DC)는 이들을 생체 상태로 장간막 림프절로 운반하여 적응성 T세포 반응을 자극한다. CD4 T세포의 94%가 GALT(장 관련 림프조직)에서 발견된다. 상피내 림프구, 특히 γδ 하위집단은 장 상피세포와 긴밀한 관계를 유지하며, 숙주 미생물 균형 유지의 핵심 매개체 역할을 한다 [4,46,47].
간경변증 환자에게서 장 운동성이 감소하여 장내 과증식을 촉진한다. 이는 문맥체순환단락과 함께 세균의 지속적 존재를 가능하게 하여 균혈증을 유발할 수 있다[48]. 이는 다시 내독소, 전염증성 사이토카인 및 NO의 증가로 인해 더 큰 산화적 손상을 초래한다[49]. 펩티도글리칸 또는 LPS는 Toll-유사 수용체에 결합하여 세포 신호 전달 계통을 시작하고 사이토카인(TNF-α, IL-6 및 IL-1)을 방출합니다 . 전신성 염증 반응 증후군(SIRS)에서는 항염증성 사이토카인(IL-10, IL-4, IL-13, PGE2)이 염증 유발성 사이토카인과 균형을 이루며, 이는 “사이토카인 폭풍”으로 알려진 과정으로 과도한 염증을 유발합니다 [50]. SIRS의 발생은 간 질환의 중증도에 의해 결정되며, 이는 다시 정맥류 출혈과 간성 뇌병증의 발생을 촉진하고 생존율에 부정적인 영향을 미칩니다 [51].
간경변증 실험 모델에서 간 기능 불균형(복수) 발생 시 장내 CD103+ DC가 활성화되며, 친염증성 CD4+ DC가 증식하여 TNF 생산 증가와 식작용 및 이동 능력 향상을 촉진한다[52]. 복수가 발생하면 T 헬퍼 세포가 TH1으로 전환되어 점막하층에서 TNF 및 IFNγ 생산이 증가하며, 동시에 TH17이 고갈되고 혈청이 아닌 복수에서 IL-1 및 IL-18이 증가한다[35,53].
자연 발생성 세균성 복막염(SBP)에서는 복수의 낮은 미생물 부하와 복막의 염증 반응 강도 사이에 차이가 있으며, 이는 SI와 예후 사이의 상관관계를 보여줍니다 [54]. SBP 동안, 혈청이 아닌 복수 내 CD206 수치는 SI, 복막 염증 및 사망률과 상관관계를 보입니다; 세균 감염 시 대량으로 분비되는 전염증성 사이토카인은 SI 및 장기 부전에 기여합니다 [55].
비흡수성 항생제 사용은 NO 생성, 염증 및 혈역학적 변화를 감소시키고 [56,57], 내독소혈증과 간 질환의 중증도를 완화시킵니다 [3].
1.10. Humoral Factors in Circulation
Norepinephrine acts on the microbiome, has harmful effects on enterocytes, increases intestinal permeability, and facilitates the perpetuation of intestinal inflammation. In ACLF, norepinephrine levels are three times higher in AD and strongly correlate with the severity of the systemic inflammatory response [58,59].
The adaptive immune response is induced and regulated by T helper (Th) cells. Patients with cirrhosis frequently present with Th cell lymphopenia due to splenic sequestration, as well as a reduction in the naïve Th cell compartment [60]. Lario et al. examined circulating lymphocytes, determining their number and distribution; compared with controls, they showed a drastic reduction in the number of Th and cytotoxic T (Tc) cells. The number of naive T cells was reduced 2.7-fold, while the number of memory Th cells was reduced 1.5-fold in patients with cirrhosis. The reduction in naïve Th cells favors the state of lymphopenia in cirrhosis, characterized by an increase in memory Th cells, increased apoptosis, and the accumulation of splanchnic Th cells [61].
In cirrhosis, endothelial activation and hemodynamic changes are related in part to elevated levels of TNF-α [62]. The plasma levels of LBP increase in response to LPSs. Its function is to transport LPSs to effector immune cells, and the decontamination of the intestine with norfloxacin decreases the risk of bacterial infections, decreases circulating levels of TNF-α and LBP, and improves the hemodynamic status of patients with advanced cirrhosis [63].
A prospective study included 25 healthy subjects and 60 patients with alcoholic cirrhosis with at least 1 year of abstinence from alcohol; the patients were aged between 25 and 70 years, and ascites were detected in 28/60 patients (46%). Serum LBP levels were above the threshold level of healthy controls in 11 of the 28 patients with ascites; peripheral blood had a significant increase in the total number of monocytes in patients with ascites compared to patients without ascites, in healthy patients, in patients with ascites with normal LBP or without ascites, and healthy controls. The levels of LPS, LBP, sCD14, TNF-α, sTNFα-RI, and IL-6 were increased; it was evident that the behavior of T cells was depleted and that enteric bacteria play a relevant role in these abnormalities of cellular immunity [35].
The subtype of patients with cirrhosis and ascites revealed a higher number of monocytes and a higher expression of HLA-DR on the cell surface and, in particular, of sCD14 and CD80 molecules due to LPS signaling [64].
There was reduced expression of HLA-DR antigen-presenting molecules in patients with AD, resulting in decreased monocyte activation and, in turn, cytokine secretion. In addition to the dysfunction of the RE system, patients with cirrhosis demonstrate a diminution of neutrophil mobilization and phagocytic activity, a phenomenon that correlates with the severity of liver disease [65]. Immunoglobin levels (IgM, IgG, and IgA) are decreased in the ascites of patients with cirrhosis, and the concentrations of C3, C4, and CH50 are significantly lower in serum as well as in ascites [66].
Most bacteria that cause serious infections must be phagocyted and eliminated by phagocytic cells. This process requires that the surface of the bacterial cell be first opsonized with IgG and/or with the third component of this process that requires complement (C3), with the fixation of the complement to the surface of the bacteria being the most important step in opsonization. Complement deficiencies are known to predispose individuals to bacterial infections [67,68]. Bruce et al. determined how opsonization activity in ascites correlates with the content of total protein (CH100) and complement (C3 and C4) in ascites; CH100 was measured in both ascites as well as in serum, observing that ascites caused by cirrhosis present less opsonic activity than in ascites of other etiologies [66].
1.10. 순환계 내 체액성 인자
노르에피네프린은 미생물군집에 작용하며, 장상피세포에 유해한 영향을 미치고 장 투과성을 증가시켜 장 염증의 지속을 촉진한다. ACLF에서 노르에피네프린 수치는 AD에서 3배 높으며 전신성 염증 반응의 중증도와 강한 상관관계를 보인다[58,59].
적응 면역 반응은 T 헬퍼(Th) 세포에 의해 유도 및 조절된다. 간경변 환자는 비장 격리 및 미경험 Th 세포 구획 감소로 인해 Th 세포 림프구 감소증을 흔히 보인다[60]. Lario 등은 순환 림프구의 수와 분포를 조사한 결과, 대조군에 비해 Th 및 세포독성 T(Tc) 세포 수가 급격히 감소했음을 확인했다. 미경험 T 세포 수는 2.7배 감소한 반면, 기억 Th 세포 수는 감소했다. 대조군과 비교했을 때 간경변증 환자군에서 Th 세포와 세포독성 T(Tc) 세포 수가 급격히 감소한 것으로 나타났다. 순수 T 세포 수는 2.7배 감소한 반면, 기억 Th 세포 수는 1.5배 감소했다. 순수 Th 세포의 감소는 간경변에서 나타나는 림프구 감소 상태를 촉진하며, 이는 기억 Th 세포 증가, 세포 사멸 증가, 내장 Th 세포 축적 등의 특징을 보인다[61].
간경변에서 내피 세포 활성화와 혈역학적 변화는 부분적으로 TNF-α 수치 상승과 관련이 있다[62]. LBP 혈장 농도는 LPS에 반응하여 증가한다. LBP의 기능은 LPS를 효과기 면역세포로 수송하는 것이며, 노플록사신으로 장을 소독하면 세균 감염 위험이 감소하고 순환하는 TNF-α 및 LBP 수치가 낮아지며, 진행성 간경변증 환자의 혈역학적 상태가 개선된다[63].
전향적 연구에는 건강한 피험자 25명과 최소 1년간 금주한 알코올성 간경변증 환자 60명이 포함되었다; 환자 연령은 25~70세였으며, 60명 중 28명(46%)에서 복수가 확인되었다. 복수 환자 28명 중 11명에서 혈청 LBP 수치가 건강한 대조군의 기준치를 초과했으며, 복수 환자의 말초혈액에서는 복수가 없는 환자, 건강한 대조군에 비해 단핵구 총 수가 유의하게 증가했다. 정상 LBP를 보인 복수 환자군, 복수가 없는 환자군, 그리고 건강한 대조군과 비교했을 때도 마찬가지였다. LPS, LBP, sCD14, TNF-α, sTNFα-RI, IL-6 수치가 증가했으며, T 세포 기능이 저하되었고 장내 세균이 이러한 세포 면역 이상에 중요한 역할을 한다는 것이 명백히 드러났다[35].
간경변 및 복수 환자 하위군에서는 단핵구 수가 더 많았고, 세포 표면의 HLA-DR 발현이 더 높았으며, 특히 LPS 신호 전달로 인해 sCD14 및 CD80 분자의 발현이 더 높았습니다 [64].
AD 환자에서는 HLA-DR 항원제시 분자의 발현이 감소하여 단핵구 활성화가 저하되고, 결과적으로 사이토카인 분비가 감소하였다. 간수지(RE) 시스템의 기능 장애 외에도, 간경변 환자는 호중구 동원 및 식균 활성의 감소를 보이며, 이는 간 질환의 중증도와 상관관계가 있다[65]. 간경변증 환자의 복수에서는 면역글로불린(IgM, IgG, IgA) 수치가 감소하며, 혈청 및 복수 내 C3, C4, CH50 농도 역시 현저히 낮다[66].
There is a correlation between the presence of liver failure and elevated circulating levels of endotoxins, and plasma levels of endotoxins and serum bilirubin are important factors for predicting short-term survival [69]. In cirrhosis, there is a reduction in anti-inflammatory and antiapoptotic factors, high-density lipoproteins, and Protein C, but NO is increased; NO contributes to oxidative stress and causes greater alteration in vasodilation because endotoxemia improves the expression of iNOS [70].
Patients with cirrhosis present alterations in immune function that mainly involve components of the innate immune system. This system represents the first line of defense against pathogens [71]. B cells are part of the humoral immune system, and they are responsible for protection against pathogens and contribute to immune regulation and the maintenance of self-tolerance [71]. B cells are activated as a consequence of the activation of T cells; they migrate to the germinal center where they proliferate and differentiate into memory B cells and antibody-secreting cells; there is an increase in the secretion of immunoglobulins, which forms immune complexes and further activates the immune response leading to liver injury; B lymphocytes are cells that produce pro- or anti-inflammatory cytokines and regulate the immune response [5].
Between 60 and 70% of circulating B lymphocytes are naïve B cells, which express immunoglobulins D and M [72]; when naïve B cells recognize antigens within the germinal centers, memory B cells (MBCs) develop, which return to the peripheral blood. Approximately 96% of MBCs are CD27+ and are B cells that have been exposed to protein antigens. Plasmablasts represent 3% of circulating B cells and are the last stage of differentiation. They are a product of MBCs, and in the bone marrow, they complete their maturation and finally become plasma cells [72,73].
Alcohol consumption damages hepatocytes and leukocytes due to the formation of ROS and the production of acetaldehyde (a breakdown product of alcohol), which destroys cell membranes [71]. Patients with alcohol liver disease (ALD) have an altered B cell compartment, manifested by a significant reduction in memory and naïve B cells (which is associated with increased susceptibility to infection and poor response to vaccination) [74,75], while the percentage of plasma cells is elevated. This increase in plasma cells may be responsible for high levels of IgA, IgG, and IgM in ALD. In Cardoso’s study, it was shown that these cells have a greater increase in acute decompensation than in stable disease [76].
중증 감염을 유발하는 대부분의 세균은 식세포에 의해 포식 및 제거되어야 한다. 이 과정은 먼저 세균 세포 표면이 IgG 및/또는 보체(C3)를 필요로 하는 이 과정의 세 번째 구성 요소로 오포니제이션되어야 하며, 보체가 세균 표면에 고정되는 것이 오포니제이션의 가장 중요한 단계이다. 보체 결핍은 개인이 세균 감염에 취약하게 만든다는 것이 알려져 있다[67,68]. Bruce 등은 복수 내 포식 활성이 총 단백질(CH100) 및 보체(C3와 C4) 함량과 어떻게 상관관계를 보이는지 규명하였다; CH100은 복수와 혈청 모두에서 측정되었으며, 간경변으로 인한 복수는 다른 원인에 의한 복수보다 포식 활성이 낮다는 점을 관찰하였다 [66].
간부전 발생과 순환 내 엔도톡신 수치 상승 사이에는 상관관계가 있으며, 혈장 내 엔도톡신 수치와 혈청 빌리루빈은 단기 생존을 예측하는 중요한 요소이다 [69]. 간경변에서는 항염증 및 항세포사멸 인자, 고밀도 지단백질, 프로틴 C가 감소하는 반면, NO는 증가한다; NO는 산화 스트레스에 기여하며, 내독소혈증이 iNOS 발현을 증가시키므로 혈관확장 기능에 더 큰 변화를 초래한다 [70].
간경변 환자는 주로 선천성 면역 체계 구성 요소를 포함한 면역 기능 변화를 보입니다. 이 체계는 병원체에 대한 첫 번째 방어선 역할을 합니다[71]. B 세포는 체액성 면역 체계의 일부로, 병원체로부터의 보호를 담당하며 면역 조절과 자가 내성 유지에 기여합니다[71]. B 세포는 T 세포 활성화의 결과로 활성화되며, 생식소로 이동하여 증식하고 기억 B 세포 및 항체 분비 세포로 분화한다. 면역글로불린 분비가 증가하여 면역 복합체를 형성하고, 이는 간 손상을 초래하는 면역 반응을 더욱 활성화시킨다. B 림프구는 전염증성 또는 항염증성 사이토카인을 생성하고 면역 반응을 조절하는 세포이다[5].
순환 B 림프구의 60~70%는 면역글로불린 D와 M을 발현하는 미경험 B 세포이다[72]. 미경험 B 세포가 생식소 내에서 항원을 인식하면 기억 B 세포(MBC)가 발달하여 말초 혈액으로 회귀한다. MBC의 약 96%는 CD27+이며 단백질 항원에 노출된 B 세포이다. 혈액 내 순환하는 B 세포의 3%를 차지하는 플라스마블라스트는 분화의 최종 단계입니다. 이들은 MBC의 산물로, 골수에서 성숙을 완료한 후 최종적으로 플라스마 세포가 됩니다 [72,73].
알코올 섭취는 활성산소종(ROS)의 형성과 알코올 분해산물인 아세트알데히드의 생성으로 인해 간세포와 백혈구를 손상시킵니다. 이는 세포막을 파괴합니다 [71]. 알코올성 간질환(ALD) 환자는 B 세포 구획이 변화하여 기억 B 세포와 미경험 B 세포가 현저히 감소하는 것으로 나타납니다(이는 감염에 대한 취약성 증가 및 백신 접종에 대한 반응 저하와 관련됨) [74,75], 반면 형질세포 비율은 증가합니다. 이러한 형질세포 증가는 ALD에서 높은 수준의 IgA, IgG 및 IgM을 유발할 수 있습니다. 카르도소(Cardoso)의 연구에서는 이러한 세포들이 안정된 질환보다 급성 불균형 상태에서 더 크게 증가하는 것으로 나타났다[76].
1.11. Infections in Cirrhosis
GI bleeding confers a higher risk of infection; about 17% to 45% of patients develop SBP or bacteremia [70]. The development of infection increases the risk of early bleeding; therefore, the preferred prophylactic strategies are third-generation cephalosporins, both for Gram-negative and Gram-positive bacteria. It has been shown that intravenous treatment with 1 g of ceftriaxone for 7 days after the bleeding event is more effective in preventing bacterial infections than oral antibiotics in patients with advanced cirrhosis [77]. Prokinetic agents can reduce dysmotility and BT; prophylaxis with antibiotics and prokinetic agents reduces the risk of SBP compared with antibiotics alone [78].
The prevalence of SBP in hospitalized patients with cirrhosis and ascites ranges from 10% to 30%, with approximately half of the cases occurring at the time of hospitalization and the other half of cases occurring during hospitalization [79]. The hospital mortality rate due to SBP is approximately 32%; renal failure develops in approximately one-third of all patients with SBP and is a strong predictor of mortality during hospitalization [80]. The activation of the cytokine cascade and the production of NO in cirrhosis and SBP negatively impacts kidney function; therefore, the use of intravenous albumin (1.5 g/kg within 6 h of SBP followed by 1 g/kg on day 3) in conjunction with cefotaxime reduces the incidence of kidney failure from 33% to 10% and the incidence of mortality from 29% to 10%. The mean arterial volume improves with albumin, as it binds to TNF-α and NO to compensate for the inflammatory state due to the infectious process, eliminating toxins from the circulation [81].
In patients without antibiotic prophylaxis, the SBP recurrence rate was 43% at 6 months, 69% at 1 year, and 74% at 2 years after the initial episode. Ginés et al. determined that 400 mg of norfloxacin orally per day reduced the recurrence of SBP from 68% to 20% [82].
It has been shown that in-hospital mortality is similar between patients with severe sepsis (32%) and ACLF (30%). The determination of CRP and procalcitonin (PCT) is higher in the sepsis group compared with patients with ACLF; the serum concentrations of IL-6 and IL-10 are higher in severe sepsis and different from those in subjects with ACLF or with stable cirrhosis. In contrast, CRP, PCT, and the average levels of IL-6 and IL-10 are higher in ACLF than in patients with decompensated cirrhosis [39].
As previously described, SI occurs in a setting attributable to the translocation of pro-inflammatory signals from the intestinal lumen to the systemic circulation and/or the release of DAMPs that trigger pro-inflammatory mediators [16,83]. The direct deleterious effects of these pro-inflammatory mediators on organ microcirculation and the homeostasis of cellular physiology can lead to organ failure [10]. At any stage of cirrhosis, patients can develop AD, but patients will only develop ACLF when systemic inflammation is widely activated [84].
1.11. 간경변증에서의 감염
위장관 출혈은 감염 위험을 높이며, 약 17%에서 45%의 환자가 문맥혈류감염(SBP) 또는 균혈증을 발생시킨다[70]. 감염 발생은 조기 출혈 위험을 증가시키므로, 그람음성균과 그람양성균 모두에 대해 3세대 세팔로스포린계 항생제를 우선적으로 예방적으로 투여하는 전략이 선호된다. 진행성 간경변증 환자에서 출혈 사건 후 7일간 세프트리악손 1g을 정맥 투여하는 것이 경구 항생제보다 세균 감염 예방에 더 효과적임이 입증되었다[77] . 운동촉진제는 운동장애와 위체류(BT)를 감소시킬 수 있으며, 항생제 단독 투여 대비 항생제와 운동촉진제 병용 예방요법이 SBP 위험을 낮춘다[78].
간경변증 및 복수 환자의 입원 중 SBP 유병률은 10~30%로, 약 절반은 입원 시점에 발생하고 나머지 절반은 입원 중 발생한다[79] . SBP로 인한 입원 중 사망률은 약 32%이며, SBP 환자의 약 1/3에서 신부전이 발생하며 이는 입원 중 사망의 강력한 예측인자이다 [80]. 간경변증 및 SBP에서 사이토카인 캐스케이드 활성화와 NO 생성은 신기능에 부정적 영향을 미치므로, 세포탁심과 병용하여 정맥 내 알부민(SBP 발생 후 6시간 이내 1.5g/kg, 이후 3일차에 1g/kg)을 투여하면 신부전 발생률을 33%에서 10%로, 사망률을 29% 10%로 감소시킵니다. 알부민은 TNF-α 및 NO와 결합하여 감염 과정으로 인한 염증 상태를 보상하고 순환계에서 독소를 제거함으로써 평균 동맥 혈량을 개선합니다 [81].
항생제 예방요법을 받지 않은 환자에서 SBP 재발률은 초기 발병 후 6개월 시점 43%, 1년 시점 69%, 2년 시점 74%였다. Ginés 등은 노플록사신 400mg 경구 투여가 SBP 재발률을 68%에서 20%로 감소시킨다고 보고하였다 [82].
중증 패혈증 환자(32%)와 ACLF 환자(30%) 간 입원 중 사망률은 유사한 것으로 나타났다. CRP 및 프로칼시토닌(PCT) 수치는 ACLF 환자군에 비해 패혈증 환자군에서 더 높게 측정되며, IL-6 및 IL-10 혈청 농도는 중증 패혈증에서 더 높고 ACLF 또는 안정성 간경변증 환자군과 차이가 있다. 반면, CRP, PCT 및 IL-6, IL-10의 평균 수치는 비보상성 간경변 환자보다 ACLF에서 더 높다[39].
앞서 설명한 바와 같이, SI는 장 내강에서 전신 순환계로의 전염성 신호 전달 및/또는 전염성 매개체를 유발하는 DAMPs의 방출로 인한 환경에서 발생한다[16,83]. 이러한 전염증성 매개체들이 장기 미세순환 및 세포 생리학적 항상성에 미치는 직접적인 유해 효과는 장기 부전으로 이어질 수 있다[10]. 간경변증의 어느 단계에서든 환자는 급성 간부전(AD)을 발병할 수 있으나, 전신 염증이 광범위하게 활성화된 경우에만 ACLF가 발생한다[84].
The triggers of ACLF are not fully understood; the SI may be increased and allow the development of ACLF without an external trigger [85].
Monteiro et al. evaluated inflammasome activation, estimated by the pro-inflammatory cytokines IL-1α and IL-1β of compensated and recompensated patients, and its role in developing fatal ACLF. The hypothesis of this study was that SI is a prerequisite and necessary for the development of ACLF in patients with compensated and recompensated states. In total, 88 (35%) patients died; the most common cause of death was ACLF in 52 (58.5%) patients. In 63.5% of cases, the trigger of ACLF was not identified. The recompensated patients had significantly higher rates of fatal ACLF and overall mortality compared to those with compensated patients. IL-1β levels were higher and detectable in patients with ACLF compared to those without ACLF (69% vs. 34%); patients with ACLF demonstrated significantly higher rates of IL-10 and IL-1β compared to patients without ACLF [86].
In the observations by Rolando et al., patients with acute hepatic failure (n = 887) were included; 56% of them presented SI regardless of whether or not they had bacterial infections. The prevalence of infections in patients with gastrointestinal hemorrhage is less than 2%. SI favors the development of ascites and kidney damage; in 30% of hospitalized patients with AD, bacterial infections and ascites coincide. SI can increase portal hypertension, and its severity correlates with the severity of portal hypertension in patients with cirrhosis. SI activates TLR on HSCs, causing them to become activated and increasing the production of pro-inflammatory cytokines and ROS; however, SI can generate an imbalance within the liver between vasoconstrictor and vasodilator mechanisms, resulting in increased vascular resistance [87].
ACLF의 유발 요인은 완전히 밝혀지지 않았으며, SI가 증가하면 외부 유발 요인 없이도 ACLF가 발생할 수 있다[85].
Monteiro 등은 보상기 및 재보상기 환자의 염증성 사이토카인 IL-1α 및 IL-1β를 통해 평가한 인플라마좀 활성화와 치명적 ACLF 발병에서의 그 역할을 평가하였다. 본 연구의 가설은 보상기 및 재보상기 환자에서 ACLF 발생에 SI가 선행 조건이자 필수 요소라는 것이었다. 총 88명(35%)의 환자가 사망했으며, 가장 흔한 사망 원인은 52명(58.5%)에서 ACLF였다. 63.5%의 사례에서 ACLF 유발 인자는 확인되지 않았다. 재보상 상태 환자는 보상 상태 환자 대비 치명적 ACLF 발생률 및 전체 사망률이 유의하게 높았다. ACLF 환자군에서 IL-1β 수치가 비ACLF 환자군 대비 유의하게 높고 검출 가능했다(69% vs. 34%); ACLF 환자군은 비ACLF 환자군 대비 IL-10 및 IL-1β 수치가 유의하게 높았다 [86].
Rolando 등의 관찰 연구에서는 급성 간부전 환자(n=887)가 포함되었으며, 이 중 56%가 세균 감염 유무와 관계없이 SI를 나타냈다. 위장관 출혈 환자의 감염 유병률은 2% 미만이다. SI는 복수 및 신장 손상 발생을 촉진하며, 입원 중인 AD 환자의 30%에서 세균 감염과 복수가 동시에 발생한다. SI는 문맥 고혈압을 증가시킬 수 있으며, 그 중증도는 간경변 환자의 문맥 고혈압 중증도와 상관관계가 있습니다. SI는 HSC(간성상세포)의 TLR(Toll-like 수용체)을 활성화시켜, 이들이 활성화되고 전염증성 사이토카인과 ROS(활성산소종)의 생산을 증가시킵니다. 그러나 SI는 간 내에서 혈관수축기 및 혈관확장기 메커니즘 간의 불균형을 초래하여 혈관 저항을 증가시킬 수 있습니다 [87].
1.12. SI Generates Complications and Organ Failure in AD
Two studies, CANONIC and PREDICT, described ACLF at hospital admission (CANONIC study) and critical periods before and within 3 months after admission in AD non-ACLF (PREDICT study). Mortality rates increased progressively and in parallel with the severity of AD at 3 months and 1 year after admission [6,30,88].
“Sterile” inflammation can derive from acute hepatic inflammatory processes [89]. The preactivation of the innate immune system has been observed to be induced by an exaggerated inflammatory response to bacterial infections and other pro-inflammatory stimuli; the inflammasome is highly active in ascites in patients with cirrhosis without the presence of infection, explaining the exacerbated inflammatory response in the inflammasomes that is associated with a higher degree of liver disease [53].
IL-6 is a sensitive marker of SI; among the 1211 patients with AD, the plasma level of IL-6 was normal upon admission in 3.3% (n = 40) of patients; 37 of them exhibited elevated plasma levels of other SI markers (TNF-α, IL-8, IL-10, IL-1RA, and CRP). Of the patients with compensated cirrhosis without a history of AD (n = 97), 48 (49.4%) showed normal plasma levels of IL-24 and IL-6. The SI is a prognostic marker in AD and correlates with the number of decompensations [18,30].
Patients with any precipitating factor represent 44% of patients with AD non-ACLF and 70% of AD-ACLF patients [2]. BT is probably the precipitant of SI and AD in 30% of patients with ACLF-AD. The number of precipitants influences the severity of SI [88].
Traditionally, it has been thought that SI causes organ failure due to two different mechanisms that can occur at the same time; SI stimulates the production of NO, causing greater damage to the systemic circulation, which results in increased inflammation, decreased effective arterial blood volume, and the overactivation of endogenous vasoconstrictor systems, resulting in organ hypoperfusion and the subsequent impairment of organ function. SI activates immune cells, resulting in tissue injury and organ damage [17]. It has been suggested to involve metabolic alterations associated with SI, which condition the development of organic dysfunction in cirrhosis [90].
1.12. SI는 AD에서 합병증 및 장기 부전을 유발한다
CANONIC 및 PREDICT 연구는 입원 시점의 ACLF(CANONIC 연구)와 입원 전 및 입원 후 3개월 이내의 중환기(PREDICT 연구)를 기술하였다. 사망률은 입원 후 3개월 및 1년 시점에서 AD 중증도와 병행하여 점진적으로 증가하였다[6,30,88].
“무균성” 염증은 급성 간 염증 과정으로부터 기인할 수 있다[89]. 선천성 면역 체계의 사전 활성화는 세균 감염 및 기타 염증 유발 자극에 대한 과도한 염증 반응에 의해 유도되는 것으로 관찰되었다; 간경변 환자에서 감염 없이도 복수 내 염증체(inflammasome)가 매우 활발하게 작용하며, 이는 간 질환의 중증도와 연관된 염증체의 악화된 염증 반응을 설명한다[53].
IL-6는 SI의 민감한 지표이다; AD 환자 1211명 중 입원 시 IL-6 혈장 수치가 정상인 환자는 3.3%(n=40)였으며, 이 중 37명은 다른 SI 지표(TNF-α, IL-8, IL-10, IL-1RA, CRP)의 혈장 수치가 상승되어 있었다. AD 병력이 없는 보상성 간경변 환자(n = 97) 중 48명(49.4%)은 IL-24 및 IL-6 혈장 수치가 정상이었다. SI는 AD의 예후 지표이며, 탈보상 횟수와 상관관계가 있다[18,30].
어떤 유발 인자를 가진 환자는 AD 비-ACLF 환자의 44%, AD-ACLF 환자의 70%를 차지한다[2]. BT는 ACLF-AD 환자의 30%에서 SI 및 AD의 유발 인자로 추정된다. 유발 인자의 수는 SI의 중증도에 영향을 미친다[88].
전통적으로 SI는 동시에 발생할 수 있는 두 가지 다른 기전으로 장기 부전을 유발한다고 여겨져 왔다: SI는 NO 생성을 자극하여 전신 순환에 더 큰 손상을 초래하고, 이는 염증 증가, 유효 동맥혈량 감소, 내인성 혈관수축 시스템의 과활성화를 유발하여 장기 저관류 및 후속적인 장기 기능 장애를 초래한다. SI는 면역 세포를 활성화시켜 조직 손상과 장기 손상을 초래한다[17]. 이는 SI와 관련된 대사 변화가 간경변에서 장기 기능 장애 발생을 유발하는 조건을 조성한다는 점이 제안되었다[90].
1.13. Immunoparesis
Immunoparesis is a mechanism that alters the response of the immune system and thus increases the risk of patients acquiring infections; this term was initially used in patients with sepsis [91]. In a study by J. Fernández et al., 407 patients with ACLF were included, as well as 235 patients with AD. A total of 152 patients (37%) had a bacterial infection at the diagnosis of ACLF; 117 patients (46%) of the remaining 255 patients with ACLF developed a bacterial infection during the 4-week follow-up. Serious infections (SBP, pneumonia, severe sepsis/shock, and nosocomial infections) were more frequent in ACLF. Patients with ACLF and bacterial infections (either at diagnosis or during follow-up) showed a higher degree of SI at diagnosis, a worse prognosis, and decreased 90-day survival compared to patients with ACLF without infection. It is more common to develop fungal infections during the ACLF event than in AD, and this infection gives patients a high 90-day mortality (71%) [92]. In the PREDICT study, the reported incidence of infections in patients with AD non-ACLF was 53% [88,93]. In decompensated cirrhosis, neutrophils show alterations in migration, bacterial identification, and phagocytosis, as well as an increase in ROS production [94,95].
1.13. 면역감소증
면역감소증은 면역 체계의 반응을 변화시켜 환자의 감염 획득 위험을 증가시키는 기전으로, 이 용어는 초기 패혈증 환자에서 사용되었다[91]. J. Fernández 등의 연구에서는 ACLF 환자 407명과 AD 환자 235명이 포함되었다. 총 152명(37%)의 환자가 ACLF 진단 시 세균 감염을 보였으며, 나머지 255명의 ACLF 환자 중 117명(46%)이 4주 추적 관찰 기간 동안 세균 감염을 발생시켰다. 중증 감염(혈류감염, 폐렴, 중증 패혈증/쇼크, 병원감염)은 ACLF에서 더 빈번하게 발생했다. ACLF 및 세균성 감염(진단 시 또는 추적 관찰 중)이 있는 환자는 감염이 없는 ACLF 환자에 비해 진단 시 SI 정도가 더 높고, 예후가 더 나쁘며, 90일 생존율이 낮았다. ACLF 발생 중에는 AD보다 진균 감염이 더 흔하게 발생하며, 이 감염은 환자에게 높은 90일 사망률(71%)을 초래한다[92]. PREDICT 연구에서 AD 비-ACLF 환자의 감염 발생률은 53%로 보고되었다[88,93]. 비보상성 간경변에서는 호중구가 이동, 세균 식별, 식작용에 변화를 보이며 활성산소종(ROS) 생산이 증가한다[94,95].
1.14. Dysfunction of Immune Cells Due to Metabolic Anomalies of Cirrhosis
In healthy individuals, albumin can bind to pro-inflammatory molecules in the serum and immunosuppressive mediators (PGE), whose serum concentrations are elevated in cirrhosis. In addition to presenting low albumin concentrations, it alters their immune function [96]. Low serum albumin levels (<30 mg/dL) are one of the causes of immunosuppression in acute decompensation and end-stage liver disease. They present elevated concentrations of circulating PGE2 secondary to increased production, which, in combination with hypoalbuminemia, drives innate immune dysfunction, resulting in vulnerability to infection. Human albumin infusion reduces the circulating levels of PGE2 and attenuates the suppressed secretion of pro-inflammatory cytokines from macrophages [58].
1.14. 간경변의 대사 이상에 의한 면역 세포 기능 장애
건강한 개인에서는 알부민이 혈청 내 전염증성 분자 및 면역억제 매개체(PGE)와 결합할 수 있으나, 간경변에서는 이들 혈청 농도가 상승합니다. 알부민 농도 저하 외에도 면역 기능을 변화시킵니다 [96]. 저혈청 알부민 수치(<30 mg/dL)는 급성 불균형 및 말기 간 질환에서 면역억제의 원인 중 하나이다. 이들은 생산 증가에 따른 순환 PGE2 농도 상승을 보이며, 이는 저알부민혈증과 결합하여 선천성 면역 기능 장애를 유발하여 감염에 취약하게 만든다. 인간 알부민 주입은 순환 PGE2 수준을 감소시키고 대식세포의 프로염증성 사이토카인 분비 억제를 완화시킵니다 [58].
1.15. Sarcopenia in Cirrhosis
The progressive and widespread loss of skeletal muscle, strength, and function is defined as sarcopenia, which is observed in up to 70% of patients with cirrhosis. It is relevant as it leads to physical disability and functional impairment, low quality of life, poor prognosis, and increased mortality before and after liver transplantation [97,98]. Its prevalence is high in patients with cirrhosis and low left ventricle mass due to decreased (Neuregulin/Epidermal growth factor) NRG/ERB signaling; this causes a decrease in myogenesis and myoblast differentiation [99]. Skeletal muscle releases myokines upon contraction and degradation. This is relevant because these processes have multiple beneficial physiological functions, including immunoregulation, which facilitate energy metabolism and the remodeling of cardiac architecture, playing a role in improving insulin resistance and reducing systemic inflammation. Due to all these functions, sarcopenia has a systemic impact (Figure 2). Myostatin is a myokine that inhibits protein synthesis and regeneration; sarcopenia results from an imbalance between protein synthesis and catabolism [100].
1.15. 간경변증에서의 근감소증
골격근, 근력 및 기능의 진행성 광범위 손실을 근감소증이라 정의하며, 간경변증 환자의 최대 70%에서 관찰됩니다. 이는 신체 장애 및 기능 저하, 낮은 삶의 질, 불량한 예후, 간 이식 전후 사망률 증가로 이어지므로 관련성이 높습니다 [97,98]. 간경변증 환자와 좌심실 질량이 낮은 환자에서 사르코페니아 유병률이 높은 것은 (뉴레굴린/상피성장인자) NRG/ERB 신호전달 감소로 인한 것으로, 이는 근육생성 및 근모세포 분화 감소를 유발한다 [99]. 골격근은 수축 및 분해 시 마이오카인을 분비한다. 이러한 과정들은 에너지 대사 촉진, 심장 구조 재형성, 인슐린 저항성 개선, 전신 염증 감소 등에 기여하는 면역 조절을 포함한 다양한 유익한 생리적 기능을 수행하므로 중요합니다. 이러한 모든 기능으로 인해 사르코페니아는 전신적 영향을 미칩니다(그림 2). 마이오스타틴은 단백질 합성과 재생을 억제하는 마이오카인입니다; 사르코페니아는 단백질 합성과 분해 사이의 불균형으로 발생합니다[100].
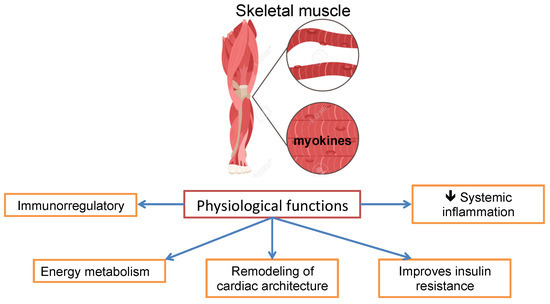
Figure 2. Physiological functions of skeletal muscle.
Hyperammonemia plays a critical role in the development of sarcopenia, regulates the rise of myostatin levels, and activates autophagia; elevated ammonia levels lead to the impairment of the mTOR pathway through increased mitochondrial dysfunction and ROS production. Similarly, hyperammonemia affects muscle contractility and increases fatigue, contributing to muscle dysfunction [101].
Sarcopenia conditions a sedentary lifestyle as a consequence of physical limitation and functional deterioration. Patients change their lifestyle, which, together with the decrease in energy expenditure, favors an increase in adipose tissue and obesity, leading to sarcopenic obesity; this increase in adipose tissue observed in sarcopenia activates SI [102] (Figure 3).
그림 2. 골격근의 생리적 기능.
고암모니아혈증은 사르코페니아 발병에 핵심적 역할을 하며, 마이오스타틴 수치 상승을 조절하고 자가포식을 활성화합니다. 상승된 암모니아 수치는 미토콘드리아 기능 장애 및 활성산소(ROS) 생성을 증가시켜 mTOR 경로의 손상을 초래합니다. 마찬가지로 고암모니아혈증은 근육 수축성을 저하시키고 피로를 증가시켜 근육 기능 장애에 기여합니다[101].
근감소증은 신체적 제한과 기능 저하로 인해 좌식 생활 방식을 초래한다. 환자들은 생활 방식을 변경하게 되며, 이는 에너지 소비 감소와 함께 지방 조직 증가 및 비만을 촉진하여 근감소성 비만으로 이어진다; 근감소증에서 관찰되는 이러한 지방 조직 증가는 SI를 활성화한다 [102] (그림 3).
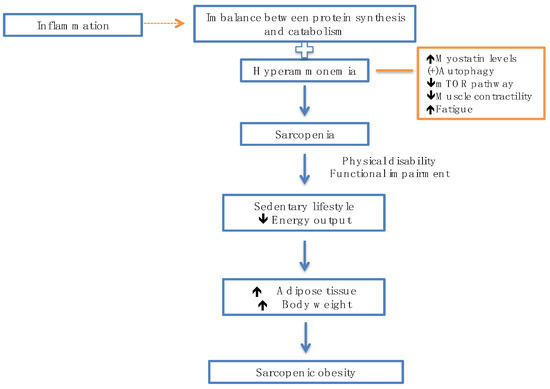
Figure 3. Inflammation and hyperammonemia predispose to the development of sarcopenia.
Patients are at risk of decompensation of liver function through the development of sarcopenia; this is associated with higher mortality, where the risk is five times higher. Meanwhile, the risk of developing cancer is also doubled, with a higher risk of infection [103].
그림 3. 염증과 고암모니아혈증은 사르코페니아 발병을 촉진한다.
환자는 사르코페니아 발병을 통해 간 기능 불균형 위험에 처하며, 이는 사망률 증가(위험도 5배)와 연관된다. 한편 암 발병 위험도 두 배로 증가하며 감염 위험도 높아진다[103].
2. Conclusions
Patients with liver cirrhosis present alterations mainly in the response of the innate immune system; however, the humoral immune system is also affected, which conditions an altered response to the recognition of pathogens. The liver is of great importance, as APCs are responsible for the immune response at local and systemic levels and as hepatocytes are responsible for PAMP and DAMP surveillance. The evolution of decompensated liver cirrhosis is characterized by repetitive episodes of acute decompensation events, which favor the presence of ACLF. It has been shown that patients with liver cirrhosis present alterations in the activation of the immune system. Following the recognition of PAMPs and DAMPs by PRRs, the pro-inflammatory pathway is activated to restore homeostasis through releasing CRP and pro-inflammatory cytokines. Patients with cirrhosis present an increase in intestinal permeability and a decrease in intestinal motility; both situations favor bacterial translocation, and these bacteria will also enter the systemic circulation. This explanation has been given to explain why patients with cirrhosis present constant immune system activation (low-grade inflammation). It is well known that bacterial infections are the triggers of ACLF. These types of patients have a higher risk of infection, which increases mortality at 3 months and 1 year. Furthermore, those who present with gastrointestinal bleeding have an increased risk of developing an infection. For this reason, there is an indication for the use of prophylactic antibiotics in patients with cirrhosis who are hospitalized for gastrointestinal bleeding. The use of antibiotics modifies the microbiota, thereby reducing the activation of immune cells in the mucosa which, in turn, reduces intestinal permeability and bacterial transfer. The presence of SBP confers a high rate of mortality and kidney damage. Hence, administering treatment based on intravenous albumin and antibiotics improves survival and reduces the risk of kidney damage. Within the group of patients with liver cirrhosis, the prognosis is also different: those who develop ACLF have a poor prognosis in the short and medium term, compared to both patients with acute decompensation without developing ACLF and patients with stable decompensated cirrhosis. Pro-inflammatory cytokines stimulate the endothelium to produce nitric oxide and ROS that favor the persistence of peripheral vasodilation, and inflammatory biomarkers change as liver function changes. Patients with ACLF present a high degree of systemic inflammation, evidenced by a decrease in TNF levels and an increase in IL-10. The presence of abnormalities in the cells of the immune system compromises the function of the cells and causes immunological paralysis. Both immunodeficiency and persistent systemic inflammation are characteristic of cirrhosis-associated immune dysfunction (CAID), affecting both innate and adaptive immune cells. Immunodeficiency is marked by an alteration in APCs, a decrease in HLA-DR expression, and an alteration in the phagocytic capacity of the cells. Another factor involved in the risk of developing infections is hypoalbuminemia, as albumin binds to pro-inflammatory cytokines and immunosuppression mediators. GALT is the first defense against pathogens. Moreover, the liver–intestinal axis plays an important role in the pathogenesis of CAID. The presence of SIRS can precipitate the presence of varicella hemorrhage and encephalopathy, worsening the prognosis. The presence of sarcopenia is a frequent complication in liver cirrhosis and negatively affects the health of these patients, deteriorates their quality of life, and worsens their prognosis due to the beneficial physiological effects of skeletal muscle as a regulator of the immune system. The development of hepatic encephalopathy is associated with a poor prognosis. In both HE and sarcopenia, hyperammonemia has a deleterious function, as it can perpetuate the inflammatory state.
2. 결론
간경변증 환자는 선천성 면역 체계 반응에 주로 이상을 보이지만, 체액성 면역 체계도 영향을 받아 병원체 인식에 대한 반응이 변화한다. 간은 항원제시세포(APCs)가 국소 및 전신 수준의 면역 반응을 담당하고, 간세포가 병원체 유사 분자(PAMP) 및 위험 신호 분자(DAMP) 감시를 담당하므로 매우 중요하다. 비보상성 간경변증의 진행은 반복적인 급성 비보상 사건으로 특징지어지며, 이는 급성 간부전(ACLF) 발생을 촉진한다. 간경변증 환자는 면역계 활성화에 이상이 있음을 보여준다. PRR에 의한 PAMP 및 DAMP 인식 후, CRP 및 전염증성 사이토카인 방출을 통해 항상성을 회복하기 위해 전염증 경로가 활성화된다. 간경변 환자는 장 투과성 증가와 장 운동성 감소를 보이며, 두 상황 모두 세균 전위를 촉진하고 이 세균들은 전신 순환계로도 유입됩니다. 이는 간경변 환자가 지속적인 면역계 활성화(저등급 염증)를 보이는 이유를 설명하는 근거로 제시되어 왔습니다. 세균 감염이 급성 간부전(ACLF)의 유발 요인이라는 것은 잘 알려져 있습니다. 이러한 유형의 환자는 감염 위험이 높아 3개월 및 1년 사망률이 증가합니다. 또한 위장관 출혈이 있는 환자는 감염 발생 위험이 더욱 높아집니다. 이러한 이유로 위장관 출혈로 입원한 간경변 환자에게는 예방적 항생제 사용이 권장된다. 항생제 사용은 미생물군집을 변화시켜 점막 내 면역 세포 활성화를 감소시키고, 이는 다시 장 투과성과 세균 이동을 줄인다. SBP(세균성 장벽 손상)의 존재는 높은 사망률과 신장 손상을 초래합니다. 따라서 정맥 내 알부민과 항생제를 기반으로 한 치료를 시행하면 생존율이 향상되고 신장 손상 위험이 감소합니다. 간경변 환자군 내에서도 예후는 다릅니다: ACLF(급성 간부전)를 발병한 환자는 ACLF를 발병하지 않은 급성 간부전 환자 및 안정된 간부전 환자에 비해 단기 및 중기 예후가 불량합니다. 전염증성 사이토카인은 내피세포를 자극하여 일산화질소와 활성산소(ROS)를 생성하게 하여 말초 혈관확장의 지속을 촉진하며, 간 기능 변화에 따라 염증 생체지표도 변화한다. ACLF 환자는 TNF 수치 감소와 IL-10 증가로 입증되는 높은 수준의 전신성 염증을 보인다. 면역계 세포의 이상은 세포 기능을 저해하고 면역학적 마비를 유발한다. 면역결핍과 지속적인 전신 염증은 모두 간경변 관련 면역 기능 장애(CAID)의 특징으로, 선천적 및 적응성 면역 세포 모두에 영향을 미칩니다. 면역결핍은 항원제시세포(APCs)의 변화, HLA-DR 발현 감소, 세포의 식균 능력 변화로 나타납니다. 감염 발생 위험에 관여하는 또 다른 요인은 저알부민혈증으로, 알부민이 전염증성 사이토카인과 면역억제 매개체에 결합하기 때문입니다. GALT(장관내 림프절)는 병원체에 대한 첫 번째 방어선입니다. 또한 간-장 축은 CAID의 병인에서 중요한 역할을 합니다. SIRS(전신성 염증 반응 증후군)의 존재는 수두 출혈 및 뇌병증의 발생을 촉발하여 예후를 악화시킬 수 있습니다. 근감소증은 간경변증에서 흔한 합병증으로, 환자의 건강에 부정적 영향을 미치고 삶의 질을 저하시키며, 면역 체계 조절자로서 골격근의 유익한 생리적 효과로 인해 예후를 악화시킵니다. 간성뇌증의 발생은 불량한 예후와 연관됩니다. 간성뇌증과 근감소증 모두에서 고암모니아혈증은 염증 상태를 지속시킬 수 있어 해로운 기능을 합니다.
Author Contributions
E.V.R.-N. and J.A.M.-G. conceived and designed this study; E.V.R.-N., M.G.-M., K.S.-R., C.F.F.-F., K.E.P.-R., E.O.M.-S. and Á.M.-G. edited and wrote some portions of this paper, compiled the references, and analyzed the data; J.A.M.-G. and E.V.R.-N. wrote this manuscript. All authors have read and agreed to the published version of the manuscript.
Funding
This research received no external funding.
Institutional Review Board Statement
Not applicable.
Informed Consent Statement
Not applicable.
Data Availability Statement
Data are contained within this article.
Conflicts of Interest
The authors declare no conflicts of interest.
References
- Ren, A.; He, W.; Rao, J.; Ye, D.; Cheng, P.; Jian, Q.; Fu, Z.; Zhang, X.; Deng, R.; Gao, Y.; et al. Dysregulation of innate cell types in the hepatic immune microenvironment of alcoholic liver cirrhosis. Front. Immunol. 2023, 14, 1034356. [Google Scholar] [CrossRef] [PubMed]
- Arroyo, V.; Angeli, P.; Moreau, R.; Jalan, R.; Clària, J.; Trebicka, J.; Fernández, J.; Gustot, T.; Caraceni, P.; Bernardi, M. The systemic inflammation hypothesis: Towards a new paradigm of acute decompensation and multiorgan failure in cirrhosis. J. Hepatol. 2021, 74, 670–685. [Google Scholar] [CrossRef] [PubMed]
- Albillos, A.; Martin-Mateos, R.; Van der Merwe, S.; Wiest, R.; Jalan, R.; Álvarez-Mon, M. Cirrhosis-associated immune dysfunction. Nat. Rev. Gastroenterol. Hepatol. 2022, 19, 112–134. [Google Scholar] [CrossRef] [PubMed]
- Bonnel, A.R.; Bunchorntavakul, C.; Reddy, K.R. Immune dysfunction and infections in patients with cirrhosis. Clin. Gastroenterol. Hepatol. 2011, 9, 727–738. [Google Scholar] [CrossRef]
- Albillos, A.; Lario, M.; Álvarez-Mon, M. Cirrhosis-associated immune dysfunction: Distinctive features and clinical relevance. J. Hepatol. 2014, 61, 1385–1396. [Google Scholar] [CrossRef]
- Moreau, R.; Jalan, R.; Gines, P.; Pavesi, M.; Angeli, P.; Cordoba, J.; Durand, F.; Gustot, T.; Saliba, F.; Domenicali, M.; et al. Acute-on-chronic liver failure is a distinct syndrome that develops in patients with acute decompensation of cirrhosis. Gastroenterology 2013, 144, 1426–1437.e9. [Google Scholar] [CrossRef]
- Ghassemi, S.; Garcia-Tsao, G. Prevention and treatment of infections in patients with cirrhosis. Best Pract. Res. Clin. Gastroenterol. 2007, 21, 77–93. [Google Scholar] [CrossRef]
- Gao, B.; Jeong, W.I.; Tian, Z. Liver: An organ with predominant innate immunity. Hepatology 2008, 47, 729–736. [Google Scholar] [CrossRef]
- Franco, A.; Barnaba, V.; Natali, P.; Balsano, C.; Musca, A.; Balsano, F. Expression of class I and class II major histocompatibility complex antigens on human hepatocytes. Hepatology 1988, 8, 449–454. [Google Scholar] [CrossRef]
- Kubes, P.; Mehal, W.Z. Sterile inflammation in the liver. Gastroenterology 2012, 143, 1158–1172. [Google Scholar] [CrossRef]
- Akira, S.; Takeda, K. Toll-like receptor signalling. Nat. Rev. Immunol. 2004, 4, 499–511. [Google Scholar] [CrossRef] [PubMed]
- Rimola, A.; Soto, R.; Bory, F.; Arroyo, V.; Piera, C.; Rodes, J. Reticuloendothelial system phagocytic activity in cirrhosis and its relation to bacterial infections and prognosis. Hepatology 1984, 4, 53–58. [Google Scholar] [CrossRef] [PubMed]