면역반응의 시작!! pattern recognition receptor(Toll-like receptor) 탐구 2021 네이처!
작성자문형철작성시간25.10.05조회수398 목록 댓글 0
Pattern recognition receptors in health and diseases
- Review Article
- Open access
- Published: 04 August 2021
Pattern recognition receptors in health and diseases
Signal Transduction and Targeted Therapy volume 6, Article number: 291 (2021) Cite this article
Abstract
Pattern recognition receptors (PRRs) are a class of receptors that can directly recognize the specific molecular structures on the surface of pathogens, apoptotic host cells, and damaged senescent cells. PRRs bridge nonspecific immunity and specific immunity. Through the recognition and binding of ligands, PRRs can produce nonspecific anti-infection, antitumor, and other immunoprotective effects. Most PRRs in the innate immune system of vertebrates can be classified into the following five types based on protein domain homology: Toll-like receptors (TLRs), nucleotide oligomerization domain (NOD)-like receptors (NLRs), retinoic acid-inducible gene-I (RIG-I)-like receptors (RLRs), C-type lectin receptors (CLRs), and absent in melanoma-2 (AIM2)-like receptors (ALRs). PRRs are basically composed of ligand recognition domains, intermediate domains, and effector domains. PRRs recognize and bind their respective ligands and recruit adaptor molecules with the same structure through their effector domains, initiating downstream signaling pathways to exert effects. In recent years, the increased researches on the recognition and binding of PRRs and their ligands have greatly promoted the understanding of different PRRs signaling pathways and provided ideas for the treatment of immune-related diseases and even tumors. This review describes in detail the history, the structural characteristics, ligand recognition mechanism, the signaling pathway, the related disease, new drugs in clinical trials and clinical therapy of different types of PRRs, and discusses the significance of the research on pattern recognition mechanism for the treatment of PRR-related diseases.
초록
패턴 인식 수용체(PRRs)는
병원체, 세포사멸을 겪은 숙주 세포,
손상된 노화 세포 표면의 특정 분자 구조를 직접 인식할 수 있는 수용체 군이다.
Pattern recognition receptors (PRRs) are
a class of receptors that can directly recognize the specific molecular structures
on the surface of pathogens,
apoptotic host cells, and
damaged senescent cells
PRRs는
비특이적 면역과 특이적 면역을 연결한다.
리간드의 인식 및 결합을 통해 PRRs는
비특이적 항감염, 항종양 및 기타 면역보호 효과를 생성할 수 있다.
척추동물의 선천성 면역계에 존재하는 대부분의 PRR은
단백질 도메인 상동성에 따라
다음과 같은 다섯 가지 유형으로 분류될 수 있다:
Toll-유사 수용체(TLRs),
뉴클레오티드 올리고머화 도메인(NOD)-유사 수용체(NLRs),
레티노산 유도 유전자-I(RIG-I)-유사 수용체(RLRs),
C형 렉틴 수용체(CLRs),
흑색종 결핍 단백질-2(AIM2) 유사 수용체(ALRs)로 분류됩니다.
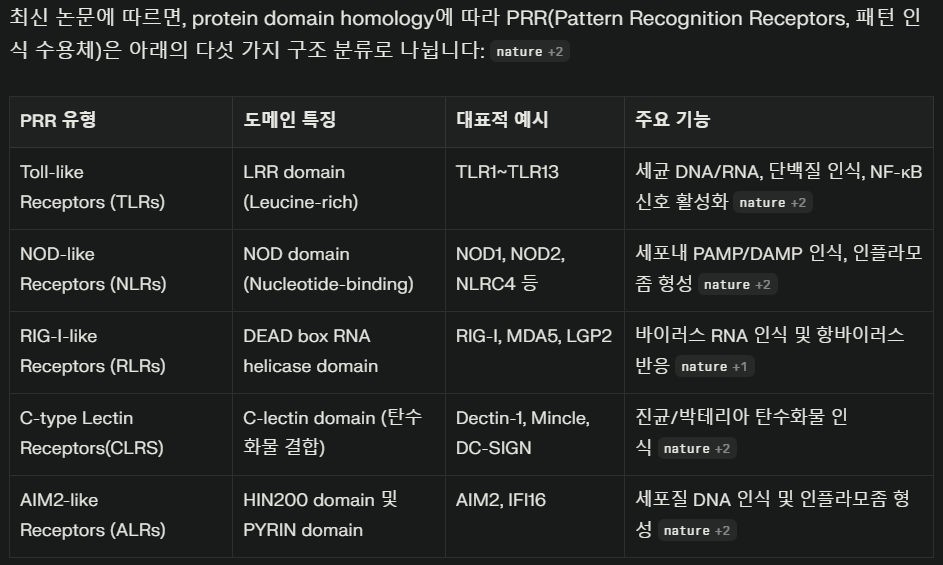
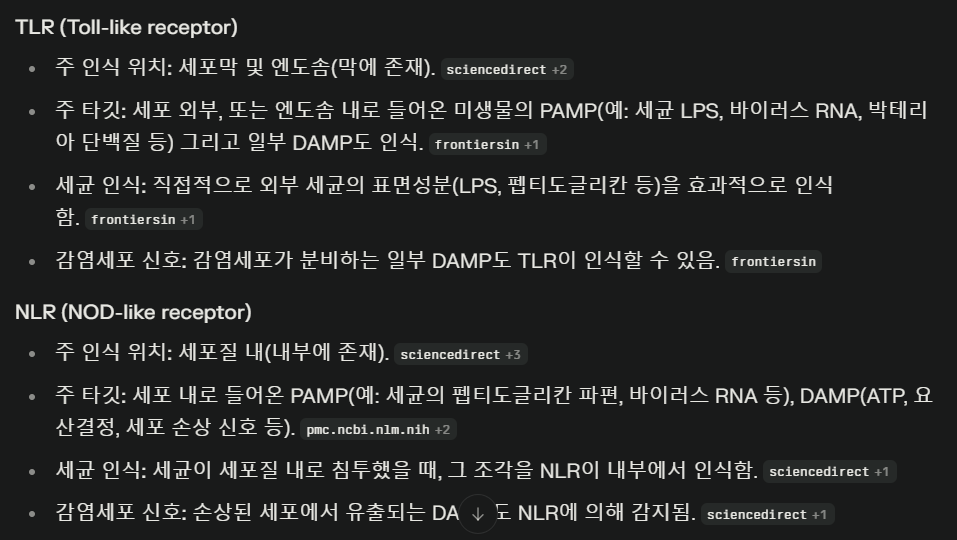
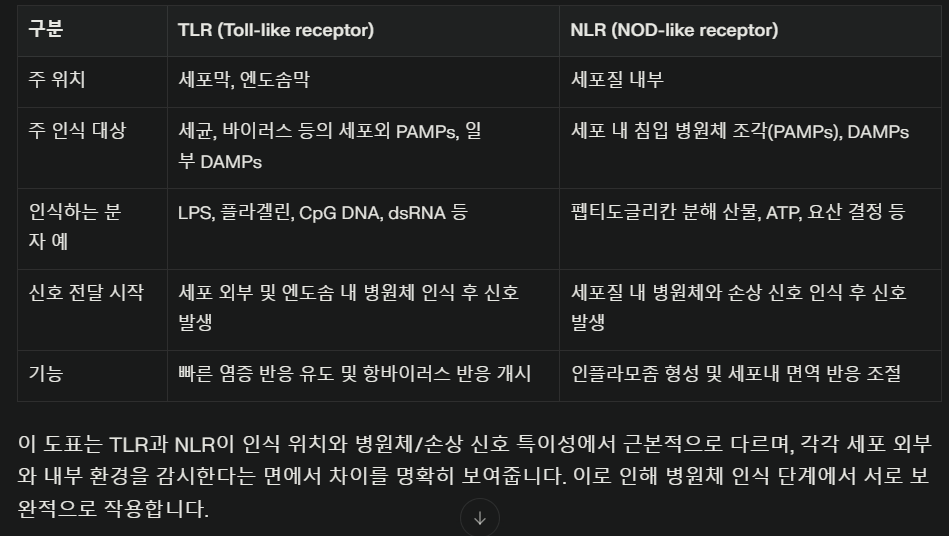
PRR은 기본적으로
리간드 인식 도메인, 중간 도메인, 효과기 도메인으로 구성됩니다.
PRRs are basically composed of ligand recognition domains,
intermediate domains, and
effector domains.

PRR은
각자의 리간드를 인식 및 결합하고
효과기 도메인을 통해 동일한 구조의 어댑터 분자를 모집하여
하류 신호전달 경로를 활성화시켜 효과를 발휘합니다.
최근 몇 년간 PRR과 그 리간드의 인식 및 결합에 대한 연구가 증가하면서
다양한 PRR 신호전달 경로에 대한 이해가 크게 진전되었으며,
이는 면역 관련 질환 및 종양 치료에 대한 아이디어를 제공하였다.
본 리뷰는
다양한 유형의 PRR에 대한 역사, 구조적 특성,
리간드 인식 메커니즘, 신호전달 경로, 관련 질환,
임상시험 중인 신약 및 임상 치료법을 상세히 기술하고,
PRR 관련 질환 치료를 위한 패턴 인식 메커니즘 연구의 중요성을 논의한다.
Similar content being viewed by others
Pattern recognition receptors: function, regulation and therapeutic potential
Article Open access11 July 2025
NOD-like receptors in autoimmune diseases
Article 15 February 2021

Article Open access03 May 2024
Introduction
The first line of defense against pathogens that gradually evolved in organisms is innate immunity,1 which is divided into two levels: first, the skin, mucosal tissue, blood–brain barrier, and chemical barrier (e.g. fatty acid, pH, enzyme, and complement system) of the host can effectively resist the invasion of general pathogenic microorganisms;2,3,4 second, the innate immune system of vertebrates protects the organism through nonspecific immune defense and surveillance by innate immune cells. Innate immune cells mainly include monocytes, neutrophils, macrophages, dendritic cells, natural killer (NK) cells, mast cells, eosinophils, and basophils.5,6 Unlike T cells and B cells, which have high specificity, innate immune cells do not express specific antigen recognition receptors. Through the recognition and binding of some common molecules on the surface of pathogens, apoptotic host cells, and damaged senescent cells, pattern recognition receptors (PRRs) induce immunoprotective effects, such as anti-infection and antitumor effects, and participate in the initiation and effect process of specific immune response.7,8,9
서론
생물체 내에서 점진적으로 진화한 병원체에 대한 첫 번째 방어선은
선천성 면역으로,1 이는 두 단계로 구분됩니다:
첫째,
숙주의 피부, 점막 조직, 혈뇌 장벽 및
화학적 장벽(예: 지방산, pH, 효소, 보체 시스템)은
일반 병원성 미생물의 침입을 효과적으로 저항할 수 있습니다; 2,3,4
chemical barrier
(e.g. fatty acid, pH, enzyme, and complement system)
| A chemical barrier uses a range of substances and systems to inhibit the growth of or destroy invading pathogens as part of the innate immune system. These defenses exist on external surfaces, like the skin, and at openings and internal linings, including the digestive and respiratory tracts. Examples of chemical barriers Fatty acids Location: Found on the skin, secreted in sebum by the sebaceous glands. Mechanism: Fatty acids, such as sapienic acid, help to lower the skin's surface pH to a range of 3–5, creating an "acid mantle" that is hostile to many microorganisms. These lipids can also have direct antimicrobial properties that control the skin's microbiota. Role: Maintains the integrity of the skin's physical and microbiological barriers by creating an environment where many pathogens cannot thrive. pH Location: Strategic locations throughout the body maintain an acidic pH to prevent microbial growth. Mechanisms: Stomach acid: The highly acidic environment created by hydrochloric acid in the stomach kills most ingested pathogens. Vaginal secretions: The acidic pH of the vagina inhibits the growth of many pathogens. Urine: The slightly acidic nature of urine helps prevent bacterial growth in the urinary tract. Enzymes Location: Found in various bodily fluids, including saliva, tears, mucus, and breast milk. Mechanism: These proteins break down the structure of invading pathogens. Lysozyme: This enzyme attacks the peptidoglycan cell walls of bacteria, causing them to break apart. Proteases: Digestive enzymes in the stomach and intestines break down the proteins of microorganisms. Role: Provides a frontline chemical defense at exposed body openings where pathogens are likely to enter. Complement system Location: A complex system of over 60 proteins that circulate in the blood and other extracellular fluids in an inactive state. Mechanism: The system is activated in a cascade sequence upon contact with microbes. It defends against infection in three main ways: Opsonization: It coats the surface of a pathogen with complement proteins, marking it for destruction by phagocytes (a process called opsonization). Inflammation: Small fragments of complement proteins act as signals (chemoattractants) to recruit more immune cells to the infection site. Cell lysis: The terminal proteins of the cascade can form a membrane attack complex (MAC) that creates pores in the cell membranes of certain pathogens, causing them to burst. Role: Acts as a major effector of the innate immune system, directly killing pathogens and assisting other immune responses. 화학적 장벽은 선천성 면역 체계의 일환으로 침입한 병원체의 증식을 억제하거나 파괴하기 위해 다양한 물질과 시스템을 활용합니다. 이러한 방어 기전은 피부와 같은 외부 표면과 소화관 및 호흡기를 포함한 개구부 및 내부 점막에 존재합니다. 화학적 장벽의 예시 지방산 위치: 피부에 존재하며 피지선에서 피지로 분비됩니다. 작용 기전: 사피엔산과 같은 지방산은 피부 표면 pH를 3~5 범위로 낮추어 많은 미생물에 불리한 “산성 보호막”을 형성합니다. 이러한 지질은 피부 미생물군을 조절하는 직접적인 항균 특성도 가질 수 있습니다. 역할: 많은 병원체가 번식할 수 없는 환경을 조성하여 피부의 물리적 및 미생물학적 장벽의 무결성을 유지합니다. pH 위치: 신체의 전략적 위치에서 산성 pH를 유지하여 미생물 증식을 방지합니다. 기전: 위산: 위의 염산에 의해 생성된 고산성 환경은 섭취된 대부분의 병원체를 사멸시킵니다. 질 분비물: 질의 산성 pH는 많은 병원체의 성장을 억제합니다. 소변: 소변의 약산성 특성은 요로 내 세균 증식을 방지하는 데 도움이 됩니다. 효소 위치: 타액, 눈물, 점액, 모유 등 다양한 체액에서 발견됩니다. 기전: 이 단백질들은 침입한 병원체의 구조를 분해합니다. 리소자임: 이 효소는 박테리아의 펩티도글리칸 세포벽을 공격하여 분해시킵니다. 프로테아제: 위와 장의 소화 효소는 미생물의 단백질을 분해합니다. 역할: 병원체가 침입할 가능성이 높은 노출된 신체 개구부에서 최전선 화학적 방어 기능을 제공합니다. 보체 시스템 위치: 60개 이상의 단백질로 구성된 복잡한 시스템으로, 비활성 상태로 혈액 및 기타 세포외액에서 순환합니다. 작용 기전: 미생물과 접촉 시 연쇄 반응으로 활성화됩니다. 감염 방어는 크게 세 가지 방식으로 이루어집니다: 오포소니제이션: 병원체 표면을 보체 단백질로 코팅하여 식세포에 의해 파괴되도록 표지합니다(오포소니제이션 과정). 염증: 보체 단백질의 작은 조각들이 신호(화학유인물질) 역할을 하여 감염 부위로 더 많은 면역 세포를 모집합니다. 세포 용해: 연쇄 반응의 최종 단백질들은 막 공격 복합체(MAC)를 형성하여 특정 병원체의 세포막에 구멍을 만들어 터지게 합니다. 역할: 선천성 면역 체계의 주요 효과기 역할을 하여 병원체를 직접 죽이고 다른 면역 반응을 보조합니다. |
둘째,
척추동물의 선천성 면역계는
비특이적 면역 방어와 선천성 면역 세포에 의한 감시를 통해 유기체를 보호한다.
선천성 면역 세포는
주로 단핵구, 호중구, 대식세포, 수지상 세포, 자연살해(NK) 세포,
높은 특이성을 지닌 T 세포 및 B 세포와 달리,
선천성 면역 세포는 특이적인 항원 인식 수용체를 발현하지 않는다.
병원체,
사멸한 숙주 세포,
손상된 노화 세포 표면의 공통 분자를 인식하고 결합함으로써,
패턴 인식 수용체(PRRs)는
항감염 및 항종양 효과와 같은 면역 보호 효과를 유도하며
특이적 면역 반응의 개시 및 효과 과정에 참여한다.7,8,9
In the 1990s, the hypothesis of pathogen-associated molecular patterns (PAMPs) and PRRs that recognize PAMPs was proposed by Janeway, which was of epoch-making significance and changed research on innate immunity.10 The main point of this hypothesis is the connection between the innate immune signal and the initiation of the adaptive immune response. Some unique and conserved components of pathogenic microorganisms can induce the second signal required to activate T cells, so as to control the adaptive immunity from being activated under normal conditions.11,12 In addition, there are a class of receptors in the host that can recognize pathogenic microorganisms and activate the second signal in time, which are independent of gene rearrangement. In vertebrates, innate immunity recognizes pathogenic microorganisms and assists in the activation and expression of second signals that activate the adaptive immunity.13
1990년대에 Janeway는
병원체 관련 분자 패턴(PAMPs)과 이를 인식하는 PRRs에 대한 가설을 제안했는데,
이는 획기적인 의미를 지니며 선천성 면역 연구를 변화시켰습니다.10
이 가설의 핵심은
선천성 면역 신호와 적응성 면역 반응의 개시 사이의 연관성입니다.
innate immune signal and the initiation of the adaptive immune response.
병원성 미생물의 일부 독특하고 보존된 구성 요소는
T 세포 활성화를 위해 필요한 제2 신호를 유도하여
정상 조건에서 적응 면역이 활성화되는 것을 제어할 수 있다.11, 12
또한
숙주에는 병원성 미생물을 인식하고
제2 신호를 적시에 활성화할 수 있는 수용체 군이 존재하며,
이는 유전자 재조합과 무관하다.
척추동물에서 선천 면역은
병원성 미생물을 인식하고 적응 면역을 활성화하는
제2 신호의 활성화 및 발현을 보조한다.13
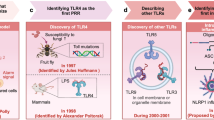
Toll-like receptors (TLRs) are one of the earliest PRRs discovered in the innate immune system, which plays an important role in inflammatory responses.14,15 Therefore, here is a brief description of the development history of PRRs with TLRs as a representative. TLRs were first found in Drosophila in the form of genes in 1994. Studies have shown that the function of this gene is related to the formation of the dorsal–ventral axis during the embryonic development of Drosophila.16 In 1988, Hashimoto et al. discovered that the Toll gene encodes a transmembrane protein and clarified the structure of the Toll protein.17 In 1991, Gay et al. found that Toll protein had structural homology with interleukin-1 (IL-1), a natural immune molecule in mammals, suggesting that the function of Toll may be related to immunity.18 In 1996, Hoffmann team found that Toll plays a role in the resistance of Drosophila to fungal infection. Toll-activated mutants persistently express antifungal peptides, while Toll-deletion mutants, on the contrary, lose their ability to arrest fungal infection. It has been found that Toll can recognize spatzle (an important protein in the development of the dorsal and abdomen of Drosophila) and initiate a series of signal transduction to activate the expression of antifungal peptide.19 In 1997, Janeway et al. cloned human TLR4. TLR4 can induce the activation of nuclear factor (NF)-κB and the expression of the co-stimulatory molecule CD80. This proves that innate immunity recognizes pathogenic microorganisms and activates the expression of the second signal, which is indispensable for the activation of adaptive immunity.20 Since the discovery of TLR4, many PRRs and their corresponding ligands have been discovered. PRRs can be divided into the following five types based on protein domain homology: TLRs, nucleotide oligomerization domain (NOD)-like receptors (NLRs), retinoic acid-inducible gene-I (RIG-I)-like receptors (RLRs), C-type lectin receptors (CLRs), and absent in melanoma-2 (AIM2)-like receptors (ALRs) (Table 1).21 PRRs are representative of immune receptors in innate immunity and exist in various forms. PRRs are not only expressed on the cell membrane but also widely distributed in intracellular compartment membranes and the cytoplasm.22 Membrane-bound PRRs and PRRs in the cytoplasm are basically composed of ligand recognition domains, intermediate domains, and effector domains.23,24 PRRs activate downstream signaling pathways through recognition of their ligands. The activation of downstream signaling pathways can produce many effects: recruiting and releasing cytokines, chemokines, hormones, and growth factors; inducing chronic inflammation; forming an inflammatory microenvironment; initiating innate immune killing and subsequent acquired immune response,9 maintaining the balance of host microecology; and eliminating dead or mutated cells.
톨 유사 수용체(TLRs)는
선천 면역 체계에서 발견된 최초의 PRR 중 하나로,
따라서
여기서는 TLRs를 대표로 하여
PRRs의 발전 역사를 간략히 설명한다.
TLRs는 1994년 초파리에서 유전자 형태로 처음 발견되었다. 연구에 따르면 이 유전자의 기능은 초파리 배아 발생 중 등배축 형성과 관련이 있는 것으로 나타났다.16 1988년 하시모토 등은 Toll 유전자가 막 관통 단백질을 암호화함을 발견하고 Toll 단백질의 구조를 규명하였다. 17
1991년 Gay 등은
Toll 단백질이 포유류의 자연 면역 분자인
인터루킨-1(IL-1)과 구조적 상동성을 가지고 있음을 발견하여
Toll의 기능이 면역과 관련될 수 있음을 시사했습니다. 18
1996년, 호프만(Hoffmann) 팀은
Toll이 초파리의 곰팡이 감염 저항성에 역할을 한다는 것을 발견했습니다.
Toll이 활성화된 돌연변이체는
지속적으로 항진균 펩타이드를 발현하는 반면,
Toll이 결손된 돌연변이체는 반대로 곰팡이 감염을 저지하는 능력을 상실합니다.
Toll은 스파츨레(spatzle, 초파리 등쪽과 복부 발달에 중요한 단백질)를 인식하여 일련의 신호 전달을 시작하여 항진균 펩타이드의 발현을 활성화할 수 있는 것으로 밝혀졌다.19
1997년, Janeway 등은
인간 TLR4를 복제했다.
TLR4는
핵 인자(NF)-κB의 활성화와 공동 자극 분자 CD80의 발현을 유도할 수 있다.

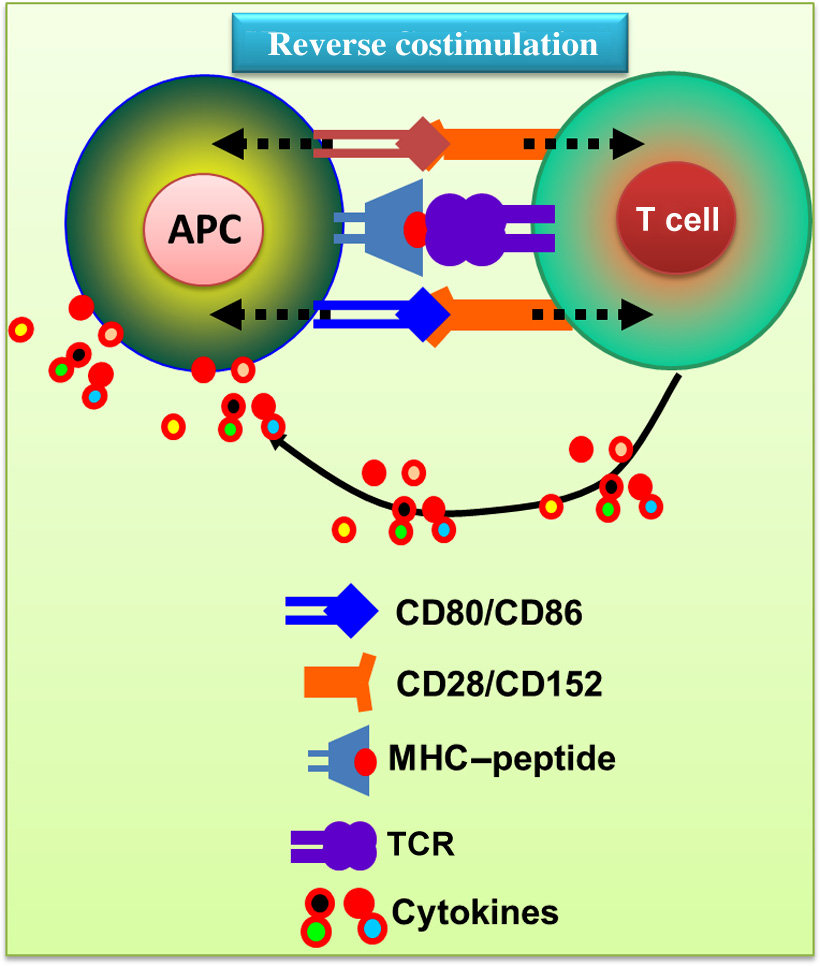
이는 선천성 면역이
병원성 미생물을 인식하고
적응성 면역 활성화에 필수적인 제2 신호 전달의 발현을 활성화함을 증명한다.20
TLR4 발견 이후,
다수의 PRR과 그에 대응하는 리간드가 발견되었다.
PRR은 단백질 도메인 상동성에 따라
다음과 같은 다섯 가지 유형으로 나눌 수 있습니다:
TLR, 뉴클레오티드 올리고머화 도메인(NOD)-유사 수용체(NLR),
레티노산 유도 유전자-I(RIG-I)-유사 수용체(RLR),
C형 렉틴 수용체(CLR),
흑색종에서 결핍된-2(AIM2)-유사 수용체 (ALRs)로 분류할 수 있다(표 1).21
PRR은
선천성 면역에서 대표적인 면역 수용체로 다양한 형태로 존재한다.
PRR은 세포막뿐만 아니라
세포 내 소기관 막과 세포질에도 광범위하게 분포합니다.22
막 결합형 PRR과 세포질 내 PRR은
기본적으로 리간드 인식 도메인, 중간 도메인, 효과기 도메인으로 구성됩니다.23,24
PRR은
리간드 인식을 통해 하류 신호 전달 경로를 활성화합니다.
하류 신호 전달 경로의 활성화는
다양한 효과를 유발할 수 있습니다:
사이토카인, 케모카인, 호르몬 및 성장 인자의 모집 및 방출;
만성 염증 유도;
염증성 미세환경 형성;
선천성 면역 살상 및 후속 후천성 면역 반응 개시,9
숙주 미생물 생태계의 균형 유지;
그리고 사멸 또는 돌연변이된 세포 제거.
recruiting and releasing cytokines, chemokines, hormones, and growth factors;
inducing chronic inflammation;
forming an inflammatory microenvironment;
initiating innate immune killing and subsequent acquired immune response,9
maintaining the balance of host microecology; and
eliminating dead or mutated cells.
Table 1 Common PRRs in innate immunity
ItemsPRRDomainsCellular distributionPAMPSourcesSignaling pathways
| Toll-like receptors (TLRs) | TLR1 (TLR1–TLR2) | LRR domain–transmembrane domain–TIR domain (extracellular to intracellular) | Mo, DC, Ma, Eo, Ba | Triacyl lipopeptide | Bacteria | Most TLRs: MyD88-dependent pathways; TLR3: TRIF-dependent pathways; TLR4: MyD88-dependent pathways and TRIF-dependent pathways |
| TLR2 (TLR1–TLR2, TLR2–TLR6) | Mo, DC, Ma, Eo, Ba | Lipoteichoic acid | Bacteria | |||
| Arabinomannan | Mycobacterium | |||||
| Peptidoglycan | Bacteria | |||||
| Zymosan | Fungi | |||||
| Lipoprotein | Mycoplasma | |||||
| Pore protein | Neisseria | |||||
| TLR3 | Mφ, DC, IEC | dsRNA | Virus | |||
| TLR4 (MD-2/CD14) | Mφ, DC, Ma, Eo | Lipopolysaccharides | Bacteria | |||
| Heat-shock proteins | Host | |||||
| TLR5 | IEC | Flagellin | Bacteria | |||
| TLR6 (TLR2–TLR6) | Mo, DC, Ma, Eo, Ba | Lipoteichoic acid | Bacteria | |||
| Peptidoglycan | Bacteria | |||||
| TLR7 | pDC, Mφ, Eo | ssRNA | Virus | |||
| Imidazoquinoline | Artificially synthesized | |||||
| TLR8 | Mφ, N | ssRNA | Virus | |||
| TLR9 | pDC, Eo, Ba | Non-methylated CpG DNA | Bacteria, Virus | |||
| TLR10 (human) | pDC, Eo, Ba | dsRNA | Virus | |||
| TLR11 (mouse) | Mφ, DC | Profilin and related proteins | Toxoplasma gondii | |||
| TLR12 (mouse) | DC | Profilin and related proteins | Toxoplasma gondii | |||
| TLR13 (mouse) | Unknown | 23s ribosomal RNA | Bacteria | |||
| Nucleotide-binding oligomerization domain-like receptors (NLRs) | NOD1 | LRR domain–NBD–effector domains | IEC, cytosol of Mφ | iE-DAP | Gram negative bacteria | RIP2-TAK1-NF-κB pathways |
| NOD2 | MDP | Gram-negative bacteria, Gram-positive bacteria | ||||
| RIG-I-like receptors (RLRs) | RIG-I | (RD)-CTD-DexD/H helicase domain–CARD | Cytosol | 5’-triphosphorylated RNA, short-chain dsRNA | Virus | MAVS-TRAF6-NF-κB/TBK1 pathways |
| MDA5 | poly IC, long-chain dsRNA | Virus | ||||
| LGP2 | dsRNA | Virus | ||||
| C-type lectin receptors (CLRs) | Dectin-1 | CTLD–ITAM | DC, Mφ | β-Glucan | Fungus | Tyrosine kinase-dependent and non-tyrosine kinase-dependent pathways |
| Dectin-2 | α-Mannan | Fungus | ||||
| Absent in melanoma-2-like receptors (ALRs) | ALRs | HIN-200-PYD | Cytosol | dsDNA | Bacteria | Inflammasome–pyroptosis |
- LRR leucine-rich repeat, TIR Toll/IL-1R domain, NBD nucleotide-binding domain, RD repressor domain, CTD C-terminal domain, CARD caspase activation and recruitment domain, CTLD C-type lectin-like domains, ITAM immunoreceptor tyrosine-based activation motif, PYD pyrin domain, Mo monocyte, DC dendritic cell, Ma mastocyte, Eo eosinophils, Ba basophils, pDC plasmacytoid dendritic cell, IEC intestinal epithelial cell, N neutrophil, dsRNA double-stranded RNA, ssRNA single-stranded RNA, iE-DAP γ-D-glu-meso-diaminopimelic acid, MDP muramyl dipeptide, MyD88 myeloid differentiation factor 88, TRIF TIR domain-containing adaptor protein-inducing interferon β, RIP2 receptor-interacting serine–threonine protein 2, TAK1 transforming growth factor-β-activated kinase 1, NF-κB nuclear factor κB, MAVS mitochondrial antiviral signaling protein, TRAF6 tumor necrosis factor receptor-associated factor, TBK1 TANK-binding kinase 1
PAMPs are the specific and highly conserved molecular structures shared by the same kind of pathogenic microorganisms,25,26 including lipids, proteins, and nucleic acids, such as lipopolysaccharides (LPS), lipoteichoic acid (LTA), and bacterial DNA.27,28 PAMPs are essential for pathogen survival and usually have unique molecular or subcellular characteristics that are not found in host cells. Therefore, innate immune cells can recognize PAMPs via PRRs, distinguish “self” and “non-self,”29 and respond to pathogens and their products. However, the host will produce some proteins and metabolites after being stimulated by its own tissue damage, cell necrosis, and other factors.30 These molecules are called damage-associated molecular pattern (DAMP).31 PRRs can also recognize such molecules, activate natural immunity, and cause inflammation.32
PAMPs는
동일한 종류의 병원성 미생물이 공유하는
지질, 단백질, 핵산(예: 리포폴리사카라이드(LPS), 리포테이코산(LTA), 박테리아 DNA) 등이
PAMPs are the specific and highly conserved molecular structures shared by
the same kind of pathogenic microorganisms,25,26 i
ncluding lipids, proteins, and nucleic acids,
such as lipopolysaccharides (LPS), lipoteichoic acid (LTA), and bacterial DNA
https://www.nature.com/articles/s41598-019-42502-5

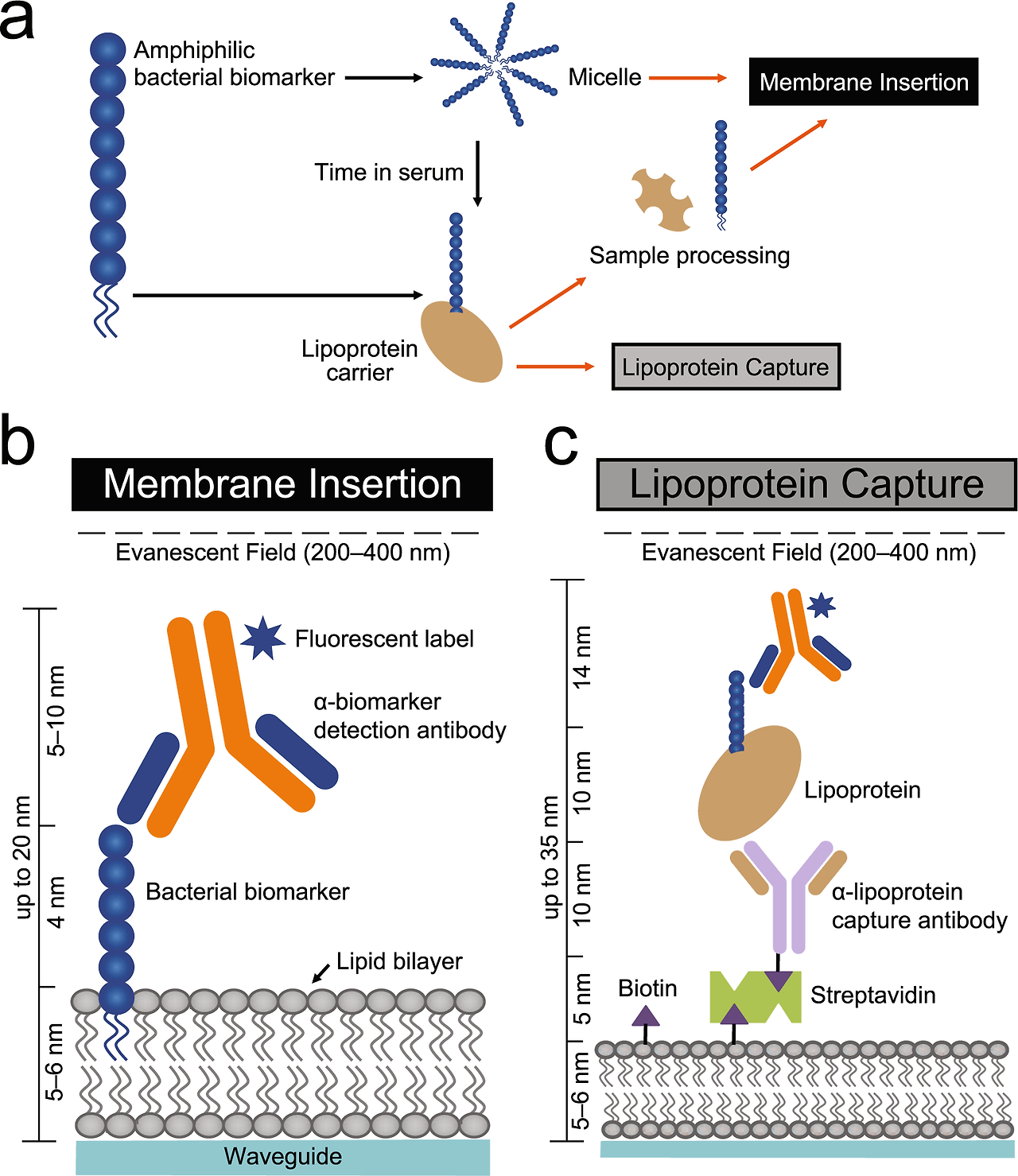
병원체관련 분자패턴(PAMPs)는
병원체의 생존에 필수적이며
일반적으로 숙주 세포에서는 발견되지 않는
독특한 분자적 또는 세포 내 특성을 지닙니다.
따라서
선천성 면역 세포는
PRR을 통해 PAMP를 인식하고, “자신”과 “비자신”을 구별하며,29
병원체와 그 산물에 반응할 수 있습니다.
그러나
숙주는 자신의 조직 손상, 세포 괴사 및 기타 요인에 의해 자극을 받은 후
일부 단백질과 대사 산물을 생성합니다.30
이러한 분자를
손상 관련 분자 패턴(DAMP)이라고 합니다. 31
PRR은 이러한 분자들도 인식하여
선천 면역을 활성화시키고 염증을 유발할 수 있습니다.32
With advances in research on PRRs structure and distribution at different levels, the role of PRRs in the innate immune regulatory network has become clearer. The recognition and binding of PRRs to their ligands is critical in initiating the innate immune response. Therefore, the study of PRR-mediated pattern recognition mechanisms will help to elucidate the signaling pathways and mechanisms of disease and provide new targets and methods for the treatment of diseases. In this review, we describe the structural characteristics, ligand recognition mechanism, the signaling pathway, the related disease, new drugs in clinical trials, and clinical therapy of different types of PRRs in detail. We focus on the different domains and ligand recognition mechanisms between PRRs, which can not only provide new ideas for the definition, role, and clinical application of PRRs but also promote the study of the role of the innate immune system in related diseases and even tumors.
PRR의 구조와 다양한 수준에서의 분포에 대한 연구가 진전됨에 따라
선천 면역 조절 네트워크에서 PRR의 역할이 더욱 명확해졌습니다.
PRR과 그 리간드의 인식 및 결합은
선천 면역 반응을 시작하는 데 매우 중요합니다.
The recognition and binding of PRRs to their ligands
is critical in initiating the innate immune response.
따라서
PRR 매개 패턴 인식 메커니즘 연구는
질병의 신호 전달 경로와 기전을 규명하고
질병 치료를 위한 새로운 표적과 방법을 제공하는 데 도움이 될 것입니다.
본 리뷰에서는 다양한 유형의 PRR에 대한 구조적 특성
, 리간드 인식 메커니즘, 신호 전달 경로, 관련 질환,
임상 시험 중인 신약 및 임상 치료법을 상세히 기술한다.
특히 PRR 간 서로 다른 도메인과 리간드 인식 메커니즘에 초점을 맞추어, PRR의 정의, 역할 및 임상 적용에 대한 새로운 아이디어를 제공할 뿐만 아니라 선천성 면역 체계가 관련 질환 및 종양에서 수행하는 역할 연구를 촉진할 수 있다.
PRRs and ligand-recognition mechanisms
Toll-like receptors
TLRs are membrane-bound signal receptors and are important PRRs in the innate immune system of vertebrates.15,33 Such receptor molecules usually have two functions, one is to bind specifically to the ligand, and the other is to transmit signals. The corresponding signal transduction will amplify the effect of anti-pathogen infection, so that the immune cells active in the inflammatory response can be activated through the transcription of genes, and produce and secrete a variety of pro-inflammatory and antiviral factors.34,35,36 Up to now, 10 functional TLRs (TLR1–10) have been found in humans and 12 (TLR1–9 and TLR11–13) in mice.37,38,39,40,41 TLR10 in mice is not functional due to the insertion of reverse transcriptase.42 TLRs recognize PAMPs in different subcellular structures. The cellular localization of TLRs determines the types of ligands and the recognition mechanism. Some TLRs (TLR1, 2, 4, 5, 6, 10) are expressed on the surface of immune cells in the form of heterodimers or homodimers, mainly recognizing the membrane components of pathogenic microorganisms, such as lipids, lipoproteins, and proteins; others (TLR3, 7, 8, 9) are expressed in the form of homodimers, which mainly recognize the nucleic acids of microorganisms (Fig. 1).43
PRR과 리간드 인식 메커니즘톨 유사 수용체(TLR)
TLR은
막 결합형 신호 수용체로,
척추동물의 선천성 면역 체계에서 중요한 PRR이다.15,33
TLRs are membrane-bound signal receptors
and are important PRRs in the innate immune system of vertebrates
이러한 수용체 분자는
일반적으로 두 가지 기능을 가지는데,
하나는 리간드에 특이적으로 결합하는 것이고,
다른 하나는 신호를 전달하는 것이다.
해당 신호 전달은 병원체 감염에 대한 방어 효과를 증폭시켜,
염증 반응에 관여하는 면역 세포가 유전자 전사를 통해 활성화되어
다양한 염증 촉진 및 항바이러스 인자를 생성·분비할 수 있게 한다.34,35, 36
지금까지 인간에서는 10개의 기능성 TLR(TLR1–10)이, 쥐에서는 12개(TLR1–9 및 TLR11–13)가 발견되었다.37,38,39,40,41 쥐의 TLR10은 역전사효소 삽입으로 인해 기능하지 않는다.42 TLR은 서로 다른 세포 내 구조에서 PAMP를 인식한다. TLR의 세포 내 국소화는 리간드 유형과 인식 메커니즘을 결정한다. 일부 TLR(TLR1, 2, 4, 5, 6, 10)은 이종 이량체 또는 동종 이량체 형태로 면역 세포 표면에 발현되며, 주로 지질, 지단백질, 단백질과 같은 병원성 미생물의 막 구성 성분을 인식한다. 다른 TLR(TLR3, 7, 8, 9)는 주로 미생물의 핵산을 인식하는 동종 이량체 형태로 발현됩니다(그림 1).43
Fig. 1
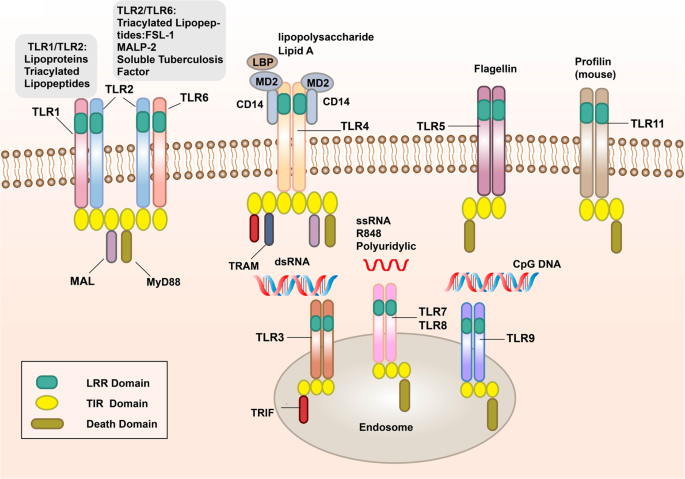
| 해당 이미지는 여러 종류의 Toll-like receptor (TLR) 단백질이 세포막 또는 엔도솜에 위치해 병원체의 다양한 분자를 인식하는 구조와 신호전달 도메인을 보여줍니다. 도식의 주요 설명 세포막 표면의 TLR TLR1/TLR2, TLR2/TLR6: Lipoprotein(지질단백질), Triacylated lipopeptides(3중 지방산 펩타이드) 등과 결합. TLR4: Lipopolysaccharide(LPS)와 결합. 이 과정에 LBP, MD2, CD14 보조분자가 관여. TLR5: 플라젤린(Flagellin, 세균 편모 단백질)을 인식. TLR11: Profilin(주로 마우스에서 확인). 엔도솜(내부 소기관)의 TLR TLR3: dsRNA(이중가닥 RNA, 바이러스 유래)를 인식, TRIF 어댑터를 사용. TLR7/TLR8: ssRNA(단일가닥 RNA), Polyuridylic acid 등 바이러스 유래 RNA 인식. TLR9: CpG DNA(무메틸화 CpG 모티프, 주로 세균/바이러스 DNA)를 인식. 도메인 구조 LRR Domain (연녹색): Leucine-rich repeat 도메인으로, 병원체 리간드 인식에 관여. TIR Domain (노란색): Toll/IL-1 receptor 도메인, 신호전달 단백질들과 결합해 신호를 전달함. Death Domain (진한 회색): 일부 TLR 경로에서 세포사멸 신호와 연관. 신호전달 어댑터 MAL, MyD88, TRAM, TRIF 등은 TIR 도메인과 상호작용해 하위 신호를 전달. 전체 해석 TLR은 각각 특정 병원체 분자(PAMPs)를 인식하는 데 특화되어 있고, 리간드를 인식하면 세포 내부 쪽 TIR 도메인을 매개로 신호전달 단백질이 결합하여, NF-κB 등의 전사인자 활성화를 비롯한 선천면역 반응을 유발합니다. 각 TLR마다 인식 분자가 다르며, 세포막 혹은 엔도솜 등 위치 역시 각각 다르게 분포함으로써 포괄적인 면역 감시체계를 형성합니다. |
The signal transduction pathways and structure of TLR-binding ligand complex.
TLRs can recognize one or more PAMPs through LRR domain. They usually dimerize themselves and recruit adaptor molecules with the same TIR domain to transmit signals
TLR-결합 리간드 복합체의 구조 및 신호 전달 경로.
TLR은
LRR 도메인을 통해 하나 이상의 PAMP를 인식할 수 있습니다.
이들은 일반적으로 자체적으로 이량체화하고 동일한 TIR 도메인을 가진 어댑터 분자를 모집하여 신호를 전달합니다.
TLRs are type I transmembrane glycoproteins and are composed of an extracellular region, a transmembrane region, and an intracellular region.44 The extracellular region contains leucine-rich repeats (LRRs), which are responsible for the recognition of specific ligands and perform extracellular pattern recognition. The intracellular domain contains the same Toll/IL-1R (TIR) domain as IL-1R, which plays a role in signal transduction. The extracellular region of TLRs contains LRRs, which mediate the pattern recognition of TLRs (Fig. 1).45 In 2007, researchers used X-ray crystal diffraction to analyze and determine the structure of the TLR–ligand complex,46 which provided a deeper understanding of the LRR domain. The LRR domain is shaped like a horseshoe, and each module consists of a conserved leucine motif and a variable region. The “LxxLxLxxN (L leucine, x any amino acid, N asparagine)” motif is composed of 20–30 amino acids and is on the concave surface of the horseshoe-like structure.47,48,49,50 The horseshoe-shaped N-terminus and C-terminus contain disulfide bridges formed by cysteine clusters51,52 to protect the hydrophobic core. After TLRs recognize and bind the corresponding PAMPs and endogenous ligands, the TIR domains conduct signals by binding to different receptor adaptor proteins in the cytoplasmic region.53,54 The TIR domain has three conserved amino acid sequences, which are called 1,2,3 cassettes. Depending on the different adaptor proteins, TLRs signaling can be divided into myeloid differentiation factor 88 (MyD88)-dependent and MyD88-independent pathways (Fig. 1).55,56
TLR은
제1종 막횡단 당단백질로, 세포외 영역, 막횡단 영역, 세포내 영역으로 구성된다.44
세포외 영역에는
특정 리간드 인식과 세포외 패턴 인식을 담당하는
류신 풍부 반복 구조(LRRs)가 포함된다.
세포내 도메인에는 신호전달 역할을 하는 IL-1R과 동일한 Toll/IL-1R(TIR) 도메인이 포함된다.
TLR의 세포외 영역은 TLR의 패턴 인식을 매개하는 LRR을 포함한다(그림 1).45 2007년 연구진은 X선 결정 회절을 이용해 TLR-리간드 복합체의 구조를 분석 및 규명했으며,46 이는 LRR 도메인에 대한 심층적 이해를 제공했다. LRR 도메인은 말굽 모양을 띠며, 각 모듈은 보존된 류신 모티프와 가변 영역으로 구성된다. "LxxLxLxxN (L: 류신, x: 임의의 아미노산, N: 아스파라긴)" 모티프는 20~30개의 아미노산으로 구성되며 말굽 모양 구조의 오목한 표면에 위치한다.47,48,49,50 말굽 모양의 N-말단과 C-말단에는 소수성 코어를 보호하기 위해 시스테인 클러스터로 형성된 이황화 결합이 존재한다.51,52 TLR이 해당 PAMP 및 내인성 리간드를 인식하고 결합한 후, TIR 도메인은 세포질 영역에서 다양한 수용체 어댑터 단백질에 결합하여 신호를 전달합니다.53,54 TIR 도메인에는 1,2,3 카세트라고 불리는 세 가지 보존된 아미노산 서열이 있습니다. 어댑터 단백질에 따라 TLR 신호전달은 골수분화인자 88(MyD88) 의존 경로와 MyD88 비의존 경로로 구분된다(그림 1).55,56
Exploring the pattern recognition mechanisms of TLRs is very valuable for understanding innate immunity and some tumorigenesis mechanisms. Therefore, researchers used X-ray crystal diffraction to determine the crystallographic structure of the extracellular domain of TLRs and the ligand complex. Although the ligand complexes have different structures, all these complexes have similar M-type crystal structures (Fig. 2).50,51 TLR1 or TLR6 can form TLR1/TLR2 and TLR6/TLR2 heterodimers with TLR2 to recognize tri-acylated lipopeptide and di-acylated lipopeptide,57 respectively. After recognizing the appropriate ligands, TLR2 can form an M-type structure with the extracellular region of TLR1 and TLR6, and the pocket structure formed binds to the ligand.58,59,60,61 The crystal structure of TLR1–TLR2–tri-acylated lipopeptide complex is similar to that of TLR2–TLR6–di-acylated lipopeptide complex, but there are important structural differences between TLR1 and TLR6 in the ligand-binding site and dimerization surface. The ligand-binding pocket of TLR1–TLR2 is located in the interface between the central and C-terminal domain, and TLR1–TLR2–tri-acylated lipopeptide is stabilized by non-covalent bonds such as hydrogen bonds, hydrophobic interactions, and ionic interactions near the ligand-binding pocket.62 In TLR6, the side chains of amino acid residues block the ligand-binding pocket, resulting in a pocket less than half the length of TLR1. In addition, the TLR2–TLR6 heterodimer is mainly regulated by the surface exposed residues of the LRR11–14 module (Fig. 2a, b).63 Researches on the structure of ligand complexes can significantly promote the discovery of small molecule agonists/antagonists targeting PRRs. A recent study revealed the activation mechanism of atypical agonists for TLR1–TLR2. Diprovocim is a recently found small molecule activator for TLR1–TLR2, but it has no structural similarity with the tri-acylated lipopeptide complex. It also interacts with TLR1–TLR2 in the same binding pocket as typical lipopeptide ligand.64 Crystal structure analysis revealed that double-stranded RNA (dsRNA) binds to the LRR domains of the N-terminus and C-terminus of TLR3.65,66 Different from the way that other TLRs directly recognize ligands,67,68,69 TLR4 specifically recognizes LPS in combination with two auxiliary molecules, myeloid differentiation factor 2 (MD2) and the LRR structural protein CD14. LPS is transported by LPS-binding protein to CD14 on the cell membrane of monocytes and macrophages to form a complex and then interacts with TLR4/MD2.70 After LPS binds with the TLR4/MD2 complex, the hydrophobic pocket of MD2 is used to bridge the two TLR4–MD2–LPS complexes to form a spatially symmetrical M-type TLR4–MD2–LPS dimer,71 and then conformational changes affect their respective functional domains and transmit signals (Fig. 2c). In addition to binding to LPS, TLR4 is also involved in the recognition of natural products (carnosic acid, paclitaxel) and pneumolysin.72,73,74 TLR5 is the most conserved and important PRR, which is usually stimulated by bacterial flagellin. In the form of homodimer, TLR5 plays a major role in the primary defense of invasive pathogens and immune homeostasis regulation.75 Although the heterodimeric structure of TLR5a–TLR5b in zebrafish and the crystallographic structure of TLR5–flagellin complex has been clearly reported, the lack of biochemical and structural information of fish TLR hinders the understanding of flagellin-based therapies. In the future, experimental TLR5–flagellin complex structure modeling and computational simulation should be used to study flagellin-mediated interactions between various pathogens and host immune receptors (Fig. 2d).76 It has been reported that TLR1–6 each exist as monomers in solution, and dimerization occurs only when the ligand is bound; in contrast, TLR8 and TLR9 exist as preformed dimers, and the binding of ligands induces conformational changes in preformed dimers (Fig. 1).49,77,78 Lee revealed that TLR10 binds dsRNA in vitro at endosomal pH, indicating that dsRNA is a ligand of TLR10. The recognition of dsRNA by TLR10 recruits MyD88, thereby transducing signals and inhibiting interferon regulatory factor 7 (IRF7)-dependent type I interferon (IFN) production.79 In mice, TLR11 and TLR12 are the main effector molecules to recognize Toxoplasma gondii. The recognition of T. gondii profilin by TLR11 depends on the parasite-specific, surface-exposed motif in TgPRF consisting of an acidic loop and a β-hairpin.80,81,82
TLR의 패턴 인식 메커니즘을 탐구하는 것은 선천성 면역과 일부 종양 발생 메커니즘을 이해하는 데 매우 가치 있습니다. 따라서 연구자들은 X선 결정 회절을 사용하여 TLR의 세포외 도메인과 리간드 복합체의 결정 구조를 규명했습니다. 리간드 복합체는 서로 다른 구조를 가지지만, 이들 복합체는 모두 유사한 M형 결정 구조를 가진다(그림 2).50,51 TLR1 또는 TLR6은 TLR2와 TLR1/TLR2 및 TLR6/TLR2 이종 이합체를 형성하여 각각 트리아실화 지질펩타이드와 디아실화 지질펩타이드를 인식한다.57 적절한 리간드를 인식한 후, TLR2는 TLR1 및 TLR6의 세포외 영역과 M형 구조를 형성하며, 형성된 포켓 구조가 리간드에 결합한다.58,59,60, 61 TLR1–TLR2–삼아실화 지질펩타이드 복합체의 결정 구조는 TLR2–TLR6–이아실화 지질펩타이드 복합체와 유사하지만, 리간드 결합 부위와 이량체화 표면에서 TLR1과 TLR6 사이에 중요한 구조적 차이가 존재한다. TLR1–TLR2의 리간드 결합 포켓은 중앙 도메인과 C-말단 도메인 사이의 경계면에 위치하며, TLR1–TLR2–삼아실화 리포펩타이드 복합체는 리간드 결합 포켓 근처에서 수소 결합, 소수성 상호작용, 이온성 상호작용과 같은 비공유 결합에 의해 안정화됩니다. 62 TLR6에서는 아미노산 잔기의 측쇄가 리간드 결합 포켓을 막아 포켓 길이가 TLR1의 절반 미만으로 줄어듭니다. 또한 TLR2-TLR6 이종 이합체는 주로 LRR11-14 모듈의 표면 노출 잔기들에 의해 조절됩니다(그림 2a, b).63 리간드 복합체의 구조 연구는 PRR을 표적으로 하는 소분자 작용제/길항제 발견을 크게 촉진할 수 있습니다. 최근 연구에서 TLR1-TLR2에 대한 비전형적 작용제의 활성화 메커니즘이 밝혀졌습니다. 디프로보심(Diprovocim)은 최근 발견된 TLR1–TLR2 소분자 활성화제이지만, 삼중 아실화 지질펩타이드 복합체와 구조적 유사성이 없습니다. 또한 전형적인 지질펩타이드 리간드와 동일한 결합 포켓에서 TLR1–TLR2와 상호작용합니다.64 결정 구조 분석 결과, 이중가닥 RNA (dsRNA)가 TLR3의 N-말단 및 C-말단 LRR 도메인에 결합함을 보여주었다.65,66 다른 TLR들이 리간드를 직접 인식하는 방식과 달리,67,68,69 TLR4는 두 보조 분자인 골수분화인자 2 (MD2) 및 LRR 구조 단백질 CD14와 결합하여 특이적으로 인식한다. LPS는 LPS 결합 단백질에 의해 단핵구 및 대식세포의 세포막 상 CD14로 수송되어 복합체를 형성한 후 TLR4/MD2와 상호작용한다.70 LPS가 TLR4/ MD2 복합체와 결합한 후, MD2의 소수성 포켓은 두 개의 TLR4–MD2–LPS 복합체를 연결하여 공간적으로 대칭적인 M형 TLR4–MD2–LPS 이량체를 형성하는 데 사용됩니다.71 그런 다음 구조적 변화가 각각의 기능 도메인에 영향을 미치고 신호를 전달합니다(그림 2c). LPS 결합 외에도 TLR4는 천연물(카르노산, 파클리탁셀) 및 폐렴균독소(pneumolysin) 인식에도 관여한다.72,73,74 TLR5는 가장 보존적이고 중요한 PRR로, 일반적으로 세균성 편모단백질(flagellin)에 의해 자극된다. 동형 이량체 형태로 존재하는 TLR5는 침습성 병원체에 대한 1차 방어 및 면역 항상성 조절에서 주요 역할을 수행한다.75 제브라피쉬의 TLR5a–TLR5b 이종 이량체 구조와 TLR5–편모단백질 복합체의 결정 구조는 명확히 보고되었으나, 어류 TLR의 생화학적 및 구조적 정보 부족으로 인해 편모단백질 기반 치료법 이해가 제한된다. 향후 실험적 TLR5-편모단백질 복합체 구조 모델링과 계산 시뮬레이션을 활용하여 다양한 병원체와 숙주 면역 수용체 간 편모단백질 매개 상호작용을 연구해야 한다(그림 2d).76 보고에 따르면 TLR1-6은 용액 내에서 각각 단량체로 존재하며, 리간드 결합 시에만 이량체화가 발생한다; 반면 TLR8과 TLR9는 미리 형성된 이량체 형태로 존재하며, 리간드 결합은 미리 형성된 이량체의 구조적 변화를 유도한다(그림 1).49,77,78 Lee는 TLR10이 체외에서 엔도좀 pH 조건에서 dsRNA에 결합함을 밝혀, dsRNA가 TLR10의 리간드임을 시사한다. TLR10에 의한 dsRNA 인식은 MyD88을 모집하여 신호를 전달하고 인터페론 조절 인자 7(IRF7) 의존성 제1형 인터페론(IFN) 생성을 억제한다.79 생쥐에서 TLR11과 TLR12는 Toxoplasma gondii를 인식하는 주요 효과기 분자이다. TLR11에 의한 T. gondii 프로필린 인식은 TgPRF 내 산성 루프와 β-헤어핀으로 구성된 기생충 특이적 표면 노출 모티프에 의존한다.80,81,82
Fig. 2
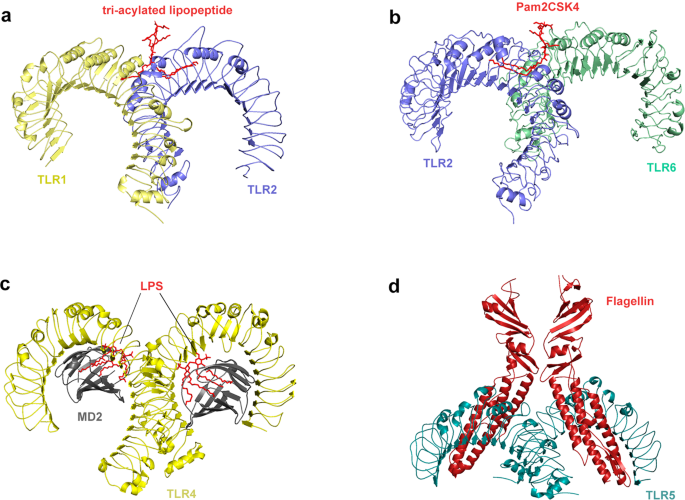
Crystal structure of TLRs with ligands. a Crystal structure of the TLR1–TLR2 heterodimer induced by binding of a tri-acylated lipopeptide (PDB 2Z7X). TLR2 initiates immune responses by recognizing di-acylated and tri-acylated lipopeptides. The ligand specificity of TLR2 is controlled by whether it heterodimerizes with TLR1 or TLR6. Binding of the tri-acylated lipopeptide (red) induced the formation of M-type crystal structures of the TLR1 (pale yellow) and TLR2 (slate) ectodomains. b Crystal structure of TLR2–TLR6–Pam2CSK4 complex (PDB 3A79). Binding of the di-acylated lipopeptide, Pam2CSK4 (red), induced the formation of M-type crystal structures of the TLR2 (slate) and TLR6 (pale green) ectodomains. c Crystal structure of mouse TLR4/MD2/LPS complex (PDB 3VQ2). After LPS (red) binds with the TLR4 (yellow)/MD2 (gray) complex, the hydrophobic pocket of MD2 is used to bridge the two TLR4–MD2–LPS complexes to form a spatially symmetrical M-type structure. Mouse TLR4/MD2/LPS exhibited an complex similar to the human TLR4/MD2/LPS complex. d Crystal structure of the N-terminal fragment of zebrafish TLR5 in complex with Salmonella flagellin (PDB 3V47). Two TLR5 (cyan)–flagellin (firebrick) 1:1 heterodimers assemble into a 2:2 tail-to-tail signaling complex to function
그림 2
리간드와 결합한 TLR의 결정 구조.
a 트리아실화 리포펩타이드 결합에 의해 유도된 TLR1-TLR2 이합체 결정 구조(PDB 2Z7X). TLR2는 디아실화 및 트리아실화 리포펩타이드를 인식하여 면역 반응을 시작한다. TLR2의 리간드 특이성은 TLR1 또는 TLR6과의 이종이량체화 여부에 의해 조절된다. 트라이아실화 리포펩타이드(빨간색)의 결합은 TLR1(옅은 노란색) 및 TLR2(슬레이트색) 외막 도메인의 M형 결정 구조 형성을 유도했다.
b TLR2–TLR6–Pam2CSK4 복합체 결정 구조(PDB 3A79). 이아실화 리포펩타이드 Pam2CSK4(빨간색)의 결합은 TLR2(슬레이트색) 및 TLR6(연두색) 외막 도메인의 M형 결정 구조 형성을 유도했다.
c 마우스 TLR4/MD2/LPS 복합체 결정 구조 (PDB 3VQ2). LPS(빨간색)가 TLR4(노란색)/MD2(회색) 복합체와 결합한 후, MD2의 소수성 포켓이 두 개의 TLR4–MD2–LPS 복합체를 연결하여 공간적으로 대칭적인 M형 구조를 형성한다. 마우스 TLR4/MD2/LPS는 인간 TLR4/MD2/LPS 복합체와 유사한 복합체를 나타냈다.
d 제브라피시 TLR5의 N-말단 단편과 살모넬라 플라젤린의 복합체 결정 구조 (PDB 3V47). 두 개의 TLR5(청록색)–편모단백질(적갈색) 1:1 이종 이량체는 꼬리-꼬리 신호 전달 복합체로 조립되어 기능한다
NOD-like receptors
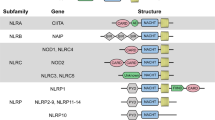
The growth cycle of some pathogenic microorganisms involves infection of the cytoplasm. For example, viral genes are often transcribed and translated in the cytoplasm, and virus particles are assembled. In addition, some bacteria and parasites have a series of escape mechanisms, such as making holes in the phagosome membrane and entering the cytoplasm. Therefore, pathogens and their components, as well as other components produced by infection and injury, will appear in the cytoplasm,83 which requires the recognition of PRRs in the body. NLRs are intracellular PRRs, composed of three domains:84,85 one is the central nucleotide-binding domain (NBD), also known as the NACHT domain (synthesized by the abbreviations of the following four kinds of NLR members: NAIP, CIITA, HETE, TP1), which is shared by the NLR family and is very important for nucleic acid binding and oligomerization of NLRs (Fig. 3); LRRs at the C-terminus, which are used to identify ligands; and the N-terminal effector domain, which is the protein interaction domain, such as the caspase activation and recruitment domain (CARD) or the pyrin domain (PYD).86,87,88,89 According to the different N-terminal effector domains, the NLRs family can be divided into five subfamilies: the NLRC subfamily, which contain CARDs; the NLRP subfamily, which contain PYDs; the NLRB subfamily, which contain baculovirus inhibitor of apoptosis protein repeats; the NLRA subfamily, which contain acidic activation domains; and the NLRX subfamily containing other NLR effector domains.85
NOD 유사 수용체
일부 병원성 미생물의 생장 주기에는
세포질 감염이 포함됩니다.
예를 들어,
바이러스 유전자는 종종 세포질에서 전사 및 번역되며, 바이러스 입자가 조립됩니다.
또한 일부 박테리아와 기생충은
식세포체 막에 구멍을 내고 세포질로 침투하는 등
일련의 회피 기전을 가지고 있습니다.
따라서
병원체와 그 구성 요소, 그리고 감염 및 손상으로 생성된 다른 구성 요소들은
세포질에 나타나게 되며,83
이는 체내 PRR의 인식이 필요합니다.
NLR은 세포 내 PRR로, 세 가지 도메인으로 구성됩니다:84,85
하나는 중심적인 뉴클레오티드 결합 도메인(NBD)으로, NACHT 도메인으로도 알려져 있으며 (다음 네 종류의 NLR 구성원 NAIP, CIITA, HETE, TP1의 약어를 합성한 것)로, NLR 계열이 공유하며 NLR의 핵산 결합 및 올리고머화에 매우 중요합니다(그림 3); C-말단에 위치한 LRR(리거드 인식 도메인)은 리간드 식별에 사용되며; N-말단 효과기 도메인은 단백질 상호작용 도메인으로, 카스파제 활성화 및 모집 도메인(CARD)이나 피린 도메인(PYD) 등이 해당됩니다. 86,87,88,89 서로 다른 N-말단 효과기 도메인에 따라 NLR 가족은 다섯 개의 아가족으로 나뉩니다: CARD를 포함하는 NLRC 아가족; PYD를 포함하는 NLRP 아가족; 바쿨로바이러스 사멸 억제 단백질 반복 구조를 포함하는 NLRB 아가족; 산성 활성화 도메인을 포함하는 NLRA 아가족; 그리고 기타 NLR 효과기 도메인을 포함하는 NLRX 아가족.85
Fig. 3
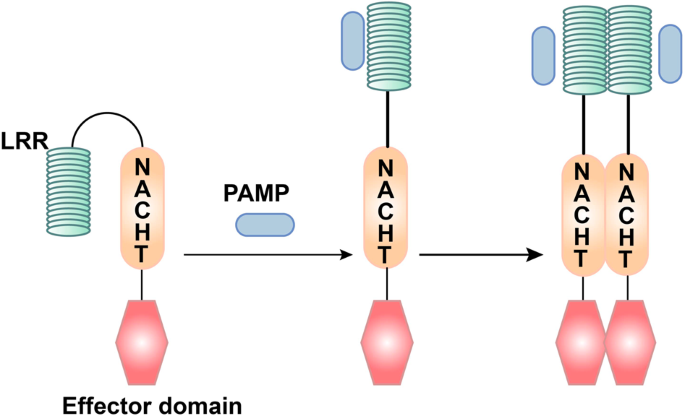
The ligand recognition mechanism of NLRs. The combination of PAMP and LRR changes the conformation of NLRs from self-inhibition to activation
NLR의 리간드 인식 메커니즘.
PAMP와 LRR의 결합은 NLR의 구조를
자가 억제 상태에서 활성화 상태로 변화시킵니다.
Among the NLRs family, the most in-depth study has focused on NOD1 and NOD2 proteins. NOD1 mainly recognizes the diaminopimelic acid (γ-D-glu-meso-diaminopimelic acid (iE-DAP)) of the cell wall of Gram-negative bacteria.90,91 In addition to recognizing muramyl dipeptide (MDP) in all bacterial cell walls, NOD2 can also recognize single-stranded RNA (ssRNA) of the virus, but it must be a complete viral ssRNA.92 The basic process of NOD2 activation and signal transduction is as follows: after pathogenic bacteria are phagocytosed by macrophages, they first form phagosomes, and then fuse with lysosomes to become phagolysosomes. Under the action of lysosomal enzymes, bacterial cell wall components are decomposed into peptidoglycan, which can be degraded into a cell wall peptide with immunomodulatory activity and enter the cytosol, thereby activating NOD2.93 In general, the LRR domain of the NLR molecule folds to form a U-shaped configuration with the central NACHT domain, which inhibits its multimerization and makes the NLRs inactive.94 Once PAMPs directly or indirectly bind to the LRRs, the NLR molecule change their conformation, exposing the NACHT oligomerization domain, which triggers oligomerization, and the NLR molecule is activated.95 At the same time, the N-terminal effector domain is exposed, and through homotypic interactions, downstream adaptor molecules and signaling proteins with the same structure are recruited to initiate the corresponding signal transduction (Fig. 3).96 Although NOD1 and NOD2 do not have transmembrane domains, studies have shown that they are recruited into the plasma membrane and endosomal membrane, which is necessary for signal transduction.97 In this process, palmitoylation plays a vital role. The modification of NOD1/2 protein under the action of palmitoyltransferase ZDHHC5, which makes NOD1/2, possess the characteristics of rapid and reversible localization changes, which is necessary for membrane recruitment and inflammatory signal transduction.98 This study gives us a good enlightenment that the modification of PRRs may play a key role in the regulation of host innate immune signal.
NLR 가족 중 가장 심층적인 연구는
NOD1 및 NOD2 단백질에 집중되어 있다.
NOD1은
주로 그람 음성균 세포벽의 디아미노피멜산(γ-D-글루-메소-디아미노피멜산(iE-DAP))을 인식한다.90, 91
NOD2는
모든 세균 세포벽의 무라밀 디펩타이드(MDP)를 인식할 뿐만 아니라,
바이러스의 단일 가닥 RNA(ssRNA)도 인식할 수 있으나,
이는 완전한 바이러스 ssRNA여야 합니다.92
NOD2 활성화 및 신호 전달의 기본 과정은 다음과 같습니다:
병원성 세균이 대식세포에 의해 식균된 후,
먼저 식포체를 형성하고,
이후 리소좀과 융합하여 식리소좀이 된다.
리소좀 효소의 작용 하에 세균 세포벽 성분은
펩티도글리칸으로 분해되며,
이는 면역조절 활성을 지닌 세포벽 펩타이드로 분해되어
세포질 내로 유입된다.
이를 통해 NOD2를 활성화시킵니다.93
Under the action of lysosomal enzymes,
bacterial cell wall components are decomposed into peptidoglycan,
which can be degraded into a cell wall peptide with immunomodulatory activity and
enter the cytosol, thereby activating NOD2.
일반적으로 NLR 분자의 LRR 도메인은 중앙 NACHT 도메인과 함께 U자형 구조를 형성하며, 이는 다량체화를 억제하여 NLR을 비활성화 상태로 유지합니다.94 PAMPs가 LRR에 직접 또는 간접적으로 결합하면 NLR 분자는 구조를 변경하여 NACHT 올리고머화 도메인을 노출시키고, 이는 올리고머화를 유발하여 NLR 분자를 활성화시킵니다.95 동시에 N-말단 효과기 도메인이 노출되며, 동형 상호작용을 통해 동일한 구조를 가진 하류 어댑터 분자 및 신호 전달 단백질이 모집되어 해당 신호 전달을 시작합니다(그림 3). 96 NOD1과 NOD2는 막횡단 도메인을 가지지 않지만, 연구에 따르면 신호전달에 필수적인 세포막 및 소포체막으로 모집되는 것으로 나타났습니다.97 이 과정에서 팔미토일화는 중요한 역할을 합니다. 팔미토일전달효소 ZDHHC5의 작용 하에 NOD1/2 단백질이 변형되면, NOD1/2는 신속하고 가역적인 국소화 변화 특성을 가지게 되며, 이는 막 모집 및 염증 신호 전달에 필수적이다.98 이 연구는 PRR의 변형이 숙주 선천 면역 신호 조절에 핵심적인 역할을 할 수 있음을 잘 보여준다.
RIG-I-like receptors
RLRs are also intracellular PRRs. In innate antiviral immunity, in addition to the recognition of viral nucleic acids by TLR7 and TLR9, most other types of cells recognize viral nucleic acids through RLRs to induce antiviral immune responses.99,100 The currently discovered RLR family members mainly include three: RIG-I, melanoma differentiation-associated gene 5 (MDA5), and laboratory of genetics and physiology 2 (LGP2) (Fig. 4).101
RIG-I-like 수용체
RLRs 또한 세포 내 PRR입니다.
선천성 항바이러스 면역에서,
TLR7 및 TLR9에 의한 바이러스 핵산 인식 외에도,
대부분의 다른 유형의 세포는 RLRs를 통해 바이러스 핵산을 인식하여
현재 발견된 RLR 가족 구성원은 주로 세 가지로 포함됩니다:
RIG-I, 흑색종 분화 관련 유전자 5(MDA5), 유전학 및 생리학 연구소 2(LGP2)이다(그림 4).101
Fig. 4
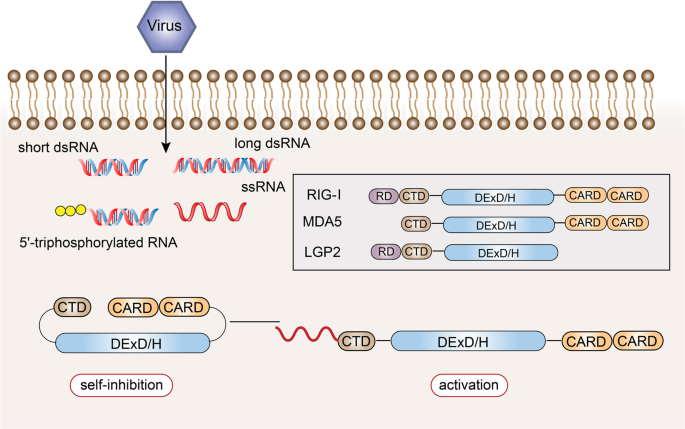
Structural features and ligand recognition mechanism of RLRs. The structure and functions of MDA5 are similar to those of RIG-I. However, MDA5 lacks the repressor domain, so it does not have self-inhibitory functions. LGP2 does not have CARD, and so it cannot transmit signals. The combination of viral RNA and CTD changes the conformation of RLRs
RLR의 구조적 특징 및 리간드 인식 메커니즘.
MDA5의 구조와 기능은 RIG-I와 유사합니다.
그러나 MDA5는 억제 도메인이 없어 자가 억제 기능을 가지지 않습니다.
LGP2는 CARD를 가지지 않아 신호를 전달할 수 없습니다.
바이러스 RNA와 CTD의 결합은 RLR의 구조를 변화시킵니다.
RIG-I was first discovered in acute promyelocytic leukemia cells induced by retinoic acid. In 2004, it was found that RIG-I could induce the expression of a reporter gene in the IFN-β promoter region, which confirmed its antiviral activity.102 The structure of the RIG-I protein consists of three parts.103,104,105 The middle part is the DexD/H helicase domain, which is the common domain of the RLR family, and has ATPase and helicase activities.106,107,108 The N-terminus of the RIG-I protein is composed of two caspase activation and recruitment domains in series,109 which are responsible for transmitting signals downstream.110 The C-terminus is composed of the repressor domain (RD) and the C-terminal domain (CTD), which can regulate its own state.106,111 The former can inhibit the activation of the receptor, and the latter is responsible for the recognition of viral RNA.112,113 In the resting state, CARD, CTD, and the helicase domain are folded, and RIG-I is in a self-inhibited state. During viral infection, the CTD of RIG-I recognizes viral RNA and undergoes a conformational change.114 RIG-I uses ATP hydrolase activity to expose and activate the CARD and multimerize, thereby recruiting downstream signaling linker molecules (Fig. 4).115,116,117
The structure and functions of MDA5 are similar to those of RIG-I, with the DexD/H helicase domain in the middle, two CARD at the N-terminus, and a CTD at the C-terminus; however, MDA5 lacks the RD, and so it does not have self-inhibitory functions. In contrast to other RLRs, LGP2 does not have CARD,118,119 and so it cannot recruit molecules of the same structure to transmit signals, but it can regulate the recognition of viral nucleic acids by RIG-I and MDA5, thereby preventing RLR-mediated resistance.120,121,122,123 LGP2 can negatively regulate RIG-I-mediated recognition of viral dsRNA, reduce the production of IFNs and inflammatory factors, and ultimately inhibit the antiviral innate immune response.124 LGP2 is also critical in the antiviral response mediated by MDA5.125 LGP2 exhibits a concentration-dependent conversion between MDA5-specific enhancement and interference.126 The latest research revealed a mechanistic basis for LGP2-mediated regulation of MDA5 antiviral innate immune responses. LGP2 facilitates MDA5 fiber assembly and is incorporated into the fibers, forming hetero-oligomers with MDA5.127 In addition, LGP2 can significantly induce the exposure of the CARD domain of MDA5.128 Under bacterial infection of the Indian major carp Labeo rohita, LGP2 gene expression was significantly increased after dsRNA and various PAMPs were stimulated, indicating that LGP2 can act as an antiviral and antibacterial cytoplasmic receptor.129
Although the RLR family members have similar structures, they recognize the RNA of different viruses through ligand-recognition domains.130 Both RIG-I and MDA5 can recognize viral dsRNA, but their recognition depends on the length of the dsRNA.131 RIG-I mainly recognizes viruses with relatively short dsRNA (<1000 bp), while MDA5 tends to recognize long-chain dsRNA (>1000 bp).132 Additionally, RIG-I mediates the antiviral response by recognizing the 5’-triphosphate RNA of viruses.133 The 5’-terminal triphosphate group can be recognized by RIG-I as a non-self component, but after posttranslational modification, this molecule cannot be recognized by RIG-I.134 Because host cell RNA needs to undergo different degrees of processing and modification after synthesis in the nucleus, these results indicate that RIG-I can distinguish viral dsRNA from endogenous RNA. In the cell, RIG-I mainly recognizes influenza virus,135 vesicular stomatitis virus,136 Sendai virus, and Japanese encephalitis virus,137,138 while MDA5 mainly recognizes small RNA viruses, such as poliovirus.139,140 MDA5 also participates in the synthesis of the dsRNA analog polycytidylic acid (poly I:C). Previous studies have shown that filamentous fibers are formed during the recognition of ligands by RIG-I and MDA5, and signaling pathways are initiated from the tail and inside of the viral dsRNA, respectively.141
Although it is mentioned in the “Toll-like receptors” section that TLR3, TLR7, TLR8, and TLR9 specifically recognize virus-derived nucleic acid molecules and bacterial nuclear components, they mainly appear in the endosomal membrane. RLRs can not only be expressed in cells infected by various viruses but also can directly recognize and perceive the virus products and virus particles that exist in the cytosol. Its antiviral significance cannot be ignored.142
RIG-I는 레티노산에 의해 유도된 급성 전골수구 백혈병 세포에서 최초로 발견되었습니다. 2004년 RIG-I가 IFN-β 프로모터 영역에서 리포터 유전자 발현을 유도할 수 있다는 사실이 확인되어 항바이러스 활성이 입증되었습니다.102 RIG-I 단백질 구조는 세 부분으로 구성됩니다.103,104,105 중간 부분은 RLR 가족의 공통 도메인인 DexD/H 헬리카제 도메인으로, ATPase 및 헬리카제 활성을 지닌다.106,107,108 RIG-I 단백질의 N-말단은 두 개의 카스파제 활성화 및 모집 도메인이 연속적으로 구성되어 있으며,109 이는 하류 신호 전달을 담당한다.110 C-말단은 억제자 도메인(RD)과 C-말단 도메인(CTD)으로 구성되어 자체 상태를 조절할 수 있다. 106,111 전자는 수용체 활성화를 억제할 수 있으며, 후자는 바이러스 RNA 인식을 담당한다.112,113 휴지 상태에서 CARD, CTD 및 헬리카제 도메인은 접혀 있으며, RIG-I는 자가 억제 상태에 있다. 바이러스 감염 시 RIG-I의 CTD는 바이러스 RNA를 인식하고 구조적 변화를 겪습니다.114 RIG-I는 ATP 가수분해 활성을 이용해 CARD를 노출 및 활성화하고 다량체화하여 하류 신호 전달 연결 분자를 모집합니다(그림 4).115,116,117
MDA5의 구조와 기능은 RIG-I와 유사하며, 중간에 DexD/H 헬리카제 도메인, N-말단에 두 개의 CARD, C-말단에 CTD를 가지고 있습니다. 그러나 MDA5는 RD를 결여하여 자가억제 기능을 가지지 않습니다. 다른 RLR과 달리 LGP2는 CARD를 가지지 않아,118,119 동일한 구조의 분자를 모집하여 신호를 전달할 수 없지만, RIG-I와 MDA5에 의한 바이러스 핵산 인식을 조절하여 RLR 매개 저항성을 방지할 수 있습니다.120,121,122,123 LGP2는 RIG-I 매개 바이러스 dsRNA 인식을 음성 조절하여 인터페론(IFN) 및 염증 인자의 생산을 감소시키고, 궁극적으로 항바이러스 선천 면역 반응을 억제한다.124 LGP2는 또한 MDA5에 의해 매개되는 항바이러스 반응에서 핵심적인 역할을 한다.125 LGP2는 MDA5 특이적 증강과 간섭 사이에서 농도 의존적 전환을 나타낸다.126 최신 연구는 LGP2가 MDA5 항바이러스 선천 면역 반응을 조절하는 기전적 근거를 밝혀냈다. LGP2는 MDA5 섬유 조립을 촉진하며 섬유에 통합되어 MDA5와 이종 올리고머를 형성한다.127 또한, LGP2는 MDA5의 CARD 도메인 노출을 현저히 유도할 수 있다.128 인도 주요 잉어 Labeo rohita의 세균 감염 시, LGP2 유전자 발현은 dsRNA 및 다양한 PAMPs 자극 후 현저히 증가하여 LGP2가 항바이러스 및 항균성 세포질 수용체로 작용할 수 있음을 시사한다.129
RLR 가족 구성원들은 유사한 구조를 지니지만, 리간드 인식 도메인을 통해 서로 다른 바이러스의 RNA를 인식한다.130 RIG-I와 MDA5 모두 바이러스 dsRNA를 인식할 수 있으나, 그 인식은 dsRNA의 길이에 의존한다.131 RIG-I는 주로 상대적으로 짧은 dsRNA(<1000 bp)를 가진 바이러스를 인식하는 반면, MDA5는 긴 사슬 dsRNA (>1000 bp)를 인식하는 경향이 있습니다.132 또한 RIG-I는 바이러스의 5'-트리포스페이트 RNA를 인식하여 항바이러스 반응을 매개합니다.133 5'-말단 트리포스페이트 그룹은 RIG-I에 의해 비자신 성분으로 인식될 수 있지만, 번역 후 변형을 거친 후에는 이 분자는 RIG-I에 의해 인식될 수 없습니다.134 숙주 세포 RNA는 핵에서 합성된 후 다양한 정도의 처리 및 변형을 거쳐야 하기 때문에, 이러한 결과는 RIG-I가 바이러스성 dsRNA와 내인성 RNA를 구별할 수 있음을 시사합니다. 세포 내에서 RIG-I는 주로 인플루엔자 바이러스,135 수포성 구내염 바이러스,136 센다이 바이러스, 일본 뇌염 바이러스,137,138 등을 인식하는 반면, MDA5는 주로 소아마비 바이러스와 같은 소형 RNA 바이러스를 인식한다.139,140 또한 MDA5는 이중가닥 RNA 유사체인 폴리시티딜산(poly I:C)의 합성에도 관여한다. 기존 연구에 따르면, RIG-I와 MDA5가 리간드를 인식하는 과정에서 필라멘트 섬유가 형성되며, 신호 전달 경로는 각각 바이러스 dsRNA의 꼬리 부분과 내부에서 시작됩니다.141
“톨 유사 수용체” 섹션에서 TLR3, TLR7, TLR8, TLR9가 바이러스 유래 핵산 분자와 세균 핵 성분을 특이적으로 인식한다고 언급되었지만, 이들은 주로 내소체 막에 존재한다. RLR은 다양한 바이러스에 감염된 세포에서 발현될 뿐만 아니라 세포질 내에 존재하는 바이러스 생성물 및 바이러스 입자를 직접 인식하고 감지할 수 있다. 그 항바이러스적 중요성은 무시할 수 없다.142
C-type lectin receptors
CLRs, which belong to phagocytic PRRs, are also a popular type of receptor under study.143 The function of phagocytic receptor is different from the receptor that activates cells by signal transduction. It recognizes and binds to PAMPs through PRRs and places pathogens in cytoplasmic vesicles for direct digestion and elimination to control infection.144 CLRs are a class of receptors that recognize carbohydrates on the surface of pathogenic microorganisms with the participation of Ca+.145 It is expressed on macrophages, dendritic cells (DCs), and certain tissue cells. The ability of CLRs to recognize carbohydrates existing on self and non-self structures is mediated by carbohydrate recognition domain (CRD).146 The CRD of CLRs is a compact spherical structure, and this region is called C-type lectin-like domain (CTLD).147,148 Depending on the location of the protein on the cell membrane, CLRs are divided into transmembrane receptors and secretory receptors.146,149,150 The main representative of secretory receptors is collagen lectin family (under the “Extracellular pattern recognition molecules”).151 Transmembrane receptors can be divided into type I and type II according to their topological structure.152,153 The N-terminal of type I receptors points to extracellular and contains multiple CRDs, while the N-terminal of type II receptors points to intracellular and contains only one CRD.154,155 It has been shown that the vast majority of CLRs are involved in the presentation of antigens as active membrane-associated receptors, and CLRs are mainly expressed on antigen-presenting cells such as DCs and macrophages.145 CLRs are circular structures connected by two disulfide bonds.156 CLRs contain at least one CTLD outside the cell, while the intracellular domain is different.
Mannose receptors (MRs) belong to membrane CLRs, which are single-chain transmembrane molecules.157,158,159 The extracellular segment of MR consists of two parts: one is the proximal membrane end with eight consecutive CTLDs, which is responsible for the endocytosis and transport of the ligand; the other is the distal membrane end of the cysteine-rich lectin domain, which recognizes sulfation of carbohydrate conjugates.160 The endogenous ligands of MR are lysosomal hydrolase and myeloperoxidase, as well as the mannan-rich structure expressed by pathogens.161,162
Dendritic cell-associated C-type lectin (Dectin)-1 and Dectin-2 are typical representatives of the CLR family.163,164 Dectin-1 is a type II transmembrane protein expressed in DCs, macrophages, neutrophils, and monocytes.165 The extracellular region is a CTLD. The intracellular tail is connected to an immunoreceptor tyrosine-based activation motif (ITAM),166 indicating that the receptor also has a signal transduction function. Dectin-1 can identify a variety of fungi,167 including yeast,168 Candida albicans,169,170 Pneumocystis carinii,171,172 Cryptococcus,173,174 and Aspergillus.175,176 The ligand of Dectin-1 is β-1,3-glucan, which can activate downstream signals through tyrosine kinase-dependent and tyrosine kinase-independent pathways after recognition and binding of the ligand.177,178 Glycosylation is an important modification of the posttranslational modification of proteins (including antibodies),179 which can significantly change the structure and function of proteins or antibodies, so it is also a key mechanism for the immune system to regulate biological activity.180 Abnormal glycosylation is usually associated with malignant tumors.179 Therefore, the identification of molecules that bind glycosylated glycans can provide a new way for the treatment of human infectious and malignant diseases. Studies have found that Dectin-1 can recognize aromatic amino acids adjacent to the N-terminal asparagine at the glycosylation site as well as the core fucose on IgG antibodies, which do not compete for the same protein binding site for β-glucan, so Dectin-1 can regulate the immune response induced by IgG by combining with core fucose.181
Dectin-2, which is different from Dectin-1, does not contain the ITAM sequence and has no signal transduction function.182 Dectin-2 mainly recognizes α-mannan in the fungal cell wall and recognizes the Schistosoma mansoni egg antigen.183,184 The molecular mechanism by which Dectin-2 recognizes the binding ligand has always been the focus of research. Decout et al.185 found that the stimulation of Dectin-2 by purified Mycobacterium tuberculosis mannose-capped lipoarabinomannan requires the (α1 → 2)-linked mannosides forming the cap. Besides, Dectin-2 can also recognize lipoglycans from other bacterial species.185,186 From the perspective of the relationship between the structure and function of the above two ligands, dimannoside caps and multivalent interaction are necessary for Dectin-2 to recognize binding ligands and conduct signals.187
C형 렉틴 수용체
포식성 PRR에 속하는 CLR 역시
연구 중인 인기 있는 수용체 유형이다.143
포식성 수용체의 기능은 신호 전달을 통해 세포를 활성화하는 수용체와 다르다.
이들은 PRR을 통해 PAMP를 인식하고 결합하여 병원체를 세포질 소포 내에 위치시켜
직접 소화 및 제거함으로써 감염을 제어합니다.144
CLR은
Ca+의 참여 하에
병원성 미생물 표면의 탄수화물을 인식하는 수용체 계열입니다.145
이는 대식세포, 수지상 세포(DC), 및 특정 조직 세포에 발현됩니다.
CLR이 자가 및 비자가 구조에 존재하는 탄수화물을 인식하는 능력은
탄수화물 인식 도메인(CRD)에 의해 매개됩니다.146
CLR의 CRD는 조밀한 구형 구조이며, 이 영역은 C형 렉틴 유사 도메인(CTLD)이라고 불립니다.147,148 단백질이 세포막에서 위치한 위치에 따라, CLR은 막횡단 수용체와 분비형 수용체로 구분됩니다.146,149,150 분비형 수용체의 주요 대표자는 콜라겐 렉틴 패밀리입니다(“세포외 패턴 인식 분자” 하위 분류).151 막횡단 수용체는 토폴로지 구조에 따라 I형과 II형으로 나뉩니다. 152,153 제1형 수용체의 N-말단은 세포외를 향하며 다수의 CRD를 포함하는 반면, 제2형 수용체의 N-말단은 세포내를 향하며 단 하나의 CRD만을 포함한다.154,155 대다수의 CLR은 활성 막 관련 수용체로서 항원 제시 과정에 관여하는 것으로 밝혀졌으며, CLR은 주로 DC 및 대식세포와 같은 항원제시세포에 발현된다.145 CLR은 두 개의 이황화 결합으로 연결된 고리형 구조이다.156 CLR은 세포 외부에서 적어도 하나의 CTLD를 포함하며, 세포 내 도메인은 서로 다르다.
만노스 수용체(MRs)는 단일 사슬 막 관통 분자인 막 CLR에 속한다.157,158,159 MR의 세포외 부위는 두 부분으로 구성된다: 하나는 8개의 연속적인 CTLD를 가진 근접 막 말단으로, 리간드의 내포 및 수송을 담당한다; 다른 부분은 시스테인 풍부 렉틴 도메인의 원위막 말단으로, 탄수화물 접합체의 설포화를 인식한다.160 MR의 내인성 리간드는 리소좀 가수분해효소와 골수과산화효소, 그리고 병원체가 발현하는 만난 풍부 구조이다.161,162
수지상 세포 관련 C형 렉틴(Dectin)-1과 Dectin-2는 CLR 가족의 대표적인 구성원이다.163,164 Dectin-1은 수지상 세포, 대식세포, 호중구, 단핵구에서 발현되는 II형 막 관통 단백질이다.165 세포외 영역은 CTLD이다. 세포 내 꼬리는 면역 수용체 티로신 기반 활성화 모티프(ITAM)에 연결되어 있어,166 이 수용체가 신호 전달 기능도 가지고 있음을 나타냅니다. Dectin-1은 효모,168 Candida albicans,169,170 Pneumocystis carinii,171,172 Cryptococcus,173,174 및 Aspergillus를 포함한 다양한 곰팡이를 식별할 수 있습니다. 175,176 Dectin-1의 리간드는 β-1,3-글루칸으로, 리간드의 인식 및 결합 후 티로신 키나아제 의존적 및 티로신 키나아제 비의존적 경로를 통해 하류 신호를 활성화할 수 있다.177,178 당화(glycosylation)는 단백질의 번역 후 변형(포스트트랜슬레이션 변형)의 중요한 변형이다 (항체 포함)의 중요한 변형 과정으로,179 단백질 또는 항체의 구조와 기능을 크게 변화시킬 수 있으므로 면역 체계가 생물학적 활성을 조절하는 핵심 메커니즘이기도 하다.180 비정상적인 당화 작용은 일반적으로 악성 종양과 관련이 있다.179 따라서 당화된 당질에 결합하는 분자를 확인하는 것은 인간 감염성 및 악성 질환 치료를 위한 새로운 방법을 제공할 수 있다. 연구에 따르면 Dectin-1은 IgG 항체의 당화 부위에서 N-말단 아스파라긴에 인접한 방향족 아미노산과 코어 푸코스를 인식할 수 있으며, 이는 β-글루칸과 동일한 단백질 결합 부위를 경쟁하지 않으므로 Dectin-1은 코어 푸코스와 결합하여 IgG에 의해 유도된 면역 반응을 조절할 수 있다.181
Dectin-1과 다른 Dectin-2는 ITAM 서열을 포함하지 않으며 신호 전달 기능이 없습니다.182 Dectin-2는 주로 곰팡이 세포벽의 α-만난을 인식하며 Schistosoma mansoni 알 항원을 인식합니다.183,184 Dectin-2가 결합 리간드를 인식하는 분자적 메커니즘은 항상 연구의 초점이 되어 왔습니다. Decout 등185은 정제된 Mycobacterium tuberculosis 만노스 캡핑 리포아라비노만난에 의한 Dectin-2의 자극에는 캡을 형성하는 (α1→2)-결합 만노사이드가 필요하다는 것을 발견했습니다. 또한 Dectin-2는 다른 세균 종의 지질당류도 인식할 수 있다.185,186 위 두 리간드의 구조와 기능 간 관계 관점에서, Dectin-2가 결합 리간드를 인식하고 신호를 전달하기 위해서는 디만노사이드 캡과 다가 상호작용이 필수적이다.187
AIM2-like receptors
ALRs are a new type of PRRs that can recognize intracellular DNA.188,189 The C-terminus is the DNA-binding domain HIN-200, and the N-terminus is the PYD.189,190,191,192 The HIN-200 domain recognizes double-stranded DNA and binds to it. The N-terminal PYD binds to the PYD of apoptosis-associated speck-like protein containing CARD (ASC),193,194 thereby promoting the formation of inflammasomes and the maturation and release of IL-1β and IL-18.195 Both the DNA-binding affinity of AIM2 and the activity of its inflammasome depend on dsDNA, and it can assemble into filamentous structures along dsDNA. However, without dsDNA, it can also form filaments at high protein concentrations.196,197,198 ALRs can not only participate in the innate immune response but also regulate apoptosis, which is related to the occurrence and development of tumors.199
AIM2-유사 수용체
ALR은
세포 내 DNA를 인식할 수 있는 새로운 유형의 PRR이다.188,189
C-말단은 DNA 결합 도메인 HIN-200이며,
HIN-200 도메인은 이중 가닥 DNA를 인식하고 결합한다. N-말단 PYD는 CARD를 포함하는 세포사멸 관련 스펙클 유사 단백질(ASC)의 PYD에 결합하여 (ASC)의 PYD에 결합하여 염증체 형성과 IL-1β 및 IL-18의 성숙 및 방출을 촉진합니다.195 AIM2의 DNA 결합 친화도와 염증체 활성은 모두 이중가닥 DNA에 의존하며, 이중가닥 DNA를 따라 필라멘트 구조로 조립될 수 있습니다. 그러나 dsDNA가 없어도 높은 단백질 농도에서 필라멘트를 형성할 수 있습니다.196,197,198 ALR은 선천성 면역 반응에 참여할 뿐만 아니라 종양의 발생 및 진행과 관련된 세포 사멸을 조절할 수도 있습니다.199
Extracellular soluble pattern recognition molecules
The initiation of the innate immune response depends on the recognition of PAMPs by pattern recognition molecules (PRMs), including cell PRRs and extracellular soluble PRMs. They are a class of free receptors that can play an antibacterial effect in serum.200 Although the pattern recognition of innate immunity does not have the antigen specificity of the adaptive immune response, some PRMs produced by the body after infection by pathogenic microorganisms will exist in the serum. Once the new pathogens invade, they can also bind to the pathogen like an antibacterial molecule and play an effective function. Unlike cell-related PRRs, extracellular soluble PRMs are an important part of non-specific humoral immunity.201 Extracellular soluble PRMs are composed of different molecular families, mainly including pentraxin,202 collectin, and ficolin.203 They generally function in two ways: one is that they recognize various pathogenic factors and eliminate them through complement activation,204,205 opsonization,206 aggregation, and neutralization of inflammatory regulation; the other is that they interact with cell-related PRRs and regulate their functions to jointly regulate innate immune response.207
Pentraxin is characterized by the aggregation of five molecules and is highly conserved in evolution, including two families of short molecules and long molecules.208,209,210,211 The family of short molecules is called acute phase proteins, which is represented by C-reactive protein (CRP)212,213,214 and serum amyloid P component215,216 in humans and mice, respectively. These molecules are mainly produced by the liver under the stimulation of inflammatory signals and interleukins. They are non-specific proteins that reflect the systemic inflammatory response. Serum levels increase rapidly after the body is infected or injured. CRP generally binds to phosphocholine expressed on the surface of pathogenic microorganisms in a Ca+-dependent manner.217 SAA can bind to the outer membrane protein A of bacteria and interact with TLRs.218,219 In clinic, SAA and CRP are usually used as auxiliary diagnostic indicators for infectious diseases, but studies have shown that they also have diagnostic value in non-infectious diseases and can be used as disease classification markers.220,221 The representative of the pentraxin long molecule family is PTX3,222 which is unique in that it has a long N-terminal domain. PTX3 is produced by dendritic cells, monocyte macrophages, epithelial cells, smooth muscle cells (SMCs), and endothelial cells under the regulation of a variety of inflammatory factors.223 PTX3 is involved in the defense of selected pathogens and the regulation of inflammation.224,225,226 Due to its expression increases sharply under the conditions of inflammatory stimulation, PTX3 can become a biomarker of general acute inflammation and a variety of tumors.227 In coronavirus disease 2019 (COVID-19) patients, circulating and lung bone marrow monocytes and endothelial cells express high levels of PTX3, and PTX3 plasma concentration can serve as an independent strong prognostic indicator of short-term mortality in COVID-19.228,229
Collectin mainly includes mannose-binding lectin (MBL) and surfactant protein (SP).151,230 MBL is formed by connecting multiple homotrimers. Each component of the trimer includes a CRD, an alpha helix, and a main stem formed by spirals of collagen.231,232 The main stem of collagen gathers each trimer into bundles. MBL is composed of six CRDs.151 The end of CRD can identify the sugar structure on the surface of various pathogens, such as mannose, fucose, glucose, etc.233,234,235 The pathogens involved include yeast, parasites, Gram bacteria, and so on.236,237,238,239,240 When the distance of each CRD between the same trimer or adjacent trimers is 45 Å, it is most conducive to ligand binding.241 The other family members include A and D,242 which exist on the surface of the alveoli and are important innate immune defense molecules in the lungs. Both of them are composed of N-terminal region, CRD, neck region, collagen-like region, and other parts.243 CRD recognizes and binds glycosyl groups. The biological significance is that they can selectively identify microbial carbohydrate structures that are harmful to themselves.244,245
The domain of ficolin is similar to collectin, but it recognizes a variety of bacteria with a fibrinogen-type carbohydrate recognition structure.246,247 Its ligands are N-acetylglucosamine and LTA, a cell wall component of Gram-positive bacteria.248,249
세포외 수용성 패턴 인식 분자
선천성 면역 반응의 개시는
세포 PRR 및 세포외 가용성 PRM을 포함한
패턴 인식 분자(PRM)에 의한 PAMP의 인식에 달려 있습니다.
이들은 혈청에서
항균 효과를 발휘할 수 있는 자유 수용체 계열입니다.200
선천성 면역의 패턴 인식은
적응성 면역 반응의 항원 특이성을 가지지는 않지만,
병원성 미생물에 감염된 후 체내에서 생성된 일부 PRM은 혈청에 존재합니다.
새로운 병원체가 침입하면 항균 분자처럼 병원체에 결합하여 효과적인 기능을 발휘할 수 있다. 세포 관련 PRR과 달리 세포외 용해성 PRM은 비특이적 체액성 면역의 중요한 부분이다.201 세포외 용해성 PRM은 다양한 분자 군으로 구성되며, 주로 펜트락신,202 콜렉틴, 피콜린을 포함한다.203 이들은 일반적으로 두 가지 방식으로 기능한다: 하나는 다양한 병원성 인자를 인식하여 보체 활성화,204,205 포식작용,206 응집 및 염증 조절 중화 등을 통해 제거하는 방식이다; 다른 하나는 세포 관련 PRR과 상호작용하여 그 기능을 조절함으로써 선천성 면역 반응을 공동으로 조절하는 방식이다.207
펜트락신은 다섯 분자의 응집을 특징으로 하며 진화적으로 고도로 보존되어 있으며, 짧은 분자와 긴 분자 두 가지 계열을 포함한다.208,209,210,211 짧은 분자 계열은 급성기 단백질이라 불리며, 인간과 쥐에서 각각 C-반응성 단백질(CRP)212,213,214 및 혈청 아밀로이드 P 성분215,216으로 대표된다. 이들 분자는 주로 염증 신호와 인터루킨의 자극 하에 간에서 생성됩니다. 이들은 전신 염증 반응을 반영하는 비특이적 단백질입니다. 신체가 감염되거나 손상된 후 혈청 농도가 급격히 증가한다. CRP는 일반적으로 병원성 미생물 표면에 발현된 포스포콜린에 Ca+ 의존적 방식으로 결합한다.217 SAA는 세균의 외막 단백질 A에 결합할 수 있으며 TLRs와 상호작용한다.218,219 임상에서는 SAA와 CRP는 일반적으로 감염성 질환의 보조 진단 지표로 사용되지만, 연구에 따르면 비감염성 질환에서도 진단적 가치가 있으며 질병 분류 마커로 활용될 수 있다.220,221 펜트락신 장분자 계열의 대표적 분자는 PTX3로,222 긴 N-말단 도메인을 가진 독특한 구조를 지닌다. PTX3는 다양한 염증 인자의 조절 하에 수지상 세포, 단핵구 대식세포, 상피 세포, 평활근 세포(SMCs), 내피 세포에 의해 생성됩니다.223 PTX3는 선택된 병원체에 대한 방어 및 염증 조절에 관여합니다.224,225,226 염증 자극 조건 하에서 발현이 급격히 증가하기 때문에, PTX3는 일반적인 급성 염증 및 다양한 종양의 바이오마커가 될 수 있습니다.227 코로나바이러스 감염증-2019(COVID-19) 환자에서 순환 및 폐 골수 단핵구와 내피 세포는 높은 수준의 PTX3를 발현하며, PTX3 혈장 농도는 COVID-19의 단기 사망률에 대한 독립적인 강력한 예후 지표 역할을 할 수 있습니다.228,229
콜렉틴은 주로 만노스 결합 렉틴(MBL)과 계면활성 단백질(SP)을 포함한다.151,230 MBL은 여러 동종 삼량체(homotrimer)가 연결되어 형성된다. 삼량체의 각 구성 요소는 CRD, 알파 나선, 그리고 콜라겐 나선으로 형성된 주간(主幹)을 포함한다.231,232 콜라겐 주간은 각 삼량체를 다발로 모은다. MBL은 여섯 개의 CRD로 구성된다.151 CRD의 말단은 만노스, 푸코스, 포도당 등233,234,235 관련 병원체에는 효모, 기생충, 그람 음성균 등이 포함됩니다.236,237,238,239,240 동일 트리머 또는 인접 트리머 간 각 CRD의 거리가 45Å일 때 리간드 결합에 가장 유리합니다.241 다른 패밀리 구성원으로는 A와 D가 있으며,242 이들은 폐포 표면에 존재하며 폐의 중요한 선천성 면역 방어 분자입니다. 이들 모두 N-말단 영역, CRD, 목 영역, 콜라겐 유사 영역 등으로 구성된다.243 CRD는 당기(glycosyl group)를 인식하고 결합한다. 생물학적 중요성은 이들이 자신에게 유해한 미생물 탄수화물 구조를 선택적으로 식별할 수 있다는 점이다.244,245
피콜린 도메인은 콜렉틴과 유사하지만, 피브리노겐형 탄수화물 인식 구조를 가진 다양한 세균을 인식한다.246,247 그 리간드는 N-아세틸글루코사민과 그람양성균 세포벽 성분인 LTA이다.248,249
Signaling pathways of PRRs
There are three main types of molecules involved in signal transduction: protein kinases, adaptor proteins, and transcription factors. Although PRRs are activated by their respective ligands in different subcellular structures with different mechanisms, the three main types of molecules involved in signal transduction have similar structures and functions, and the signals they transmit are cross-talking, which can converge into several common signaling pathways.
PRR의 신호전달 경로
신호 전달에 관여하는 분자는 크게 세 가지 유형이 있습니다:
단백질 키나제,
어댑터 단백질,
전사 인자입니다.
protein kinases, adaptor proteins, and transcription factors.
PRR은 각기 다른 세포 내 구조에서 서로 다른 기전으로 해당 리간드에 의해 활성화되지만, 신호 전달에 관여하는 이 세 가지 주요 분자 유형은 유사한 구조와 기능을 가지며, 전달하는 신호는 교차 소통하여 여러 공통 신호 전달 경로로 수렴될 수 있습니다.
The NF-κB signaling
The transcription factor NF-κB is named after it was first discovered to be involved in the transcription of B cell κ chain genes.250 NF-κB is a heterodimer composed of two molecules, p50 and p65, and is inactive due to binding to the inhibitory protein IκB under normal conditions. NF-κB plays a key role in the process of cellular inflammation and immune response,251,252 and its mediated signal pathways are commonly seen in the activation of various immune cells, including signal transduction initiated by PRRs in innate immunity (Fig. 5).253
NF-κB 신호전달
전사인자 NF-κB는 처음 발견 당시 B세포 κ 사슬 유전자 전사에 관여하는 것으로 밝혀져 명명되었다.250 NF-κB는 p50과 p65 두 분자로 구성된 이종 이량체이며, 정상 상태에서는 억제 단백질 IκB에 결합하여 비활성 상태를 유지한다. NF-κB는 세포 염증 및 면역 반응 과정에서 핵심적인 역할을 수행하며,251,252 선천성 면역에서 PRR에 의해 시작되는 신호 전달을 포함하여 다양한 면역 세포의 활성화에서 그 매개 신호 경로가 흔히 관찰됩니다(그림 5).253
Fig. 5
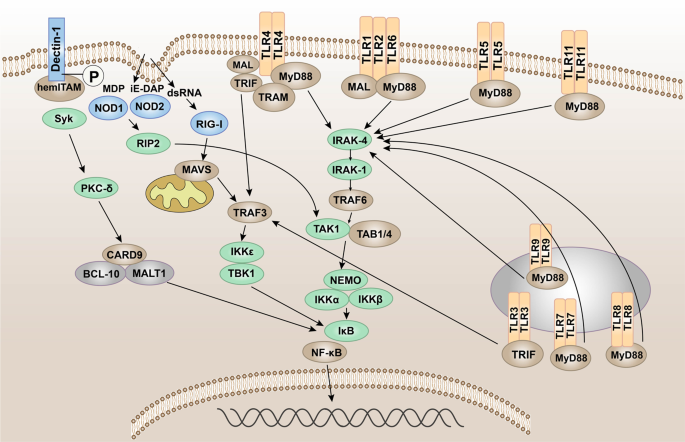
Pattern recognition receptor-mediated NF-κB signaling. The NF-κB protein can regulate gene expression and affect various biological processes, including innate and adaptive immunity, inflammation, stress response, B cell development, and lymphoid organ formation. TLRs, NLRs, RLRs, and CLRs can generally phosphorylate IκB protein, which inhibits the activation of NF-κB protein, thereby promoting the transcription and activation of inflammatory genes
그림 5
패턴 인식 수용체 매개 NF-κB 신호 전달. NF-κB 단백질은 유전자 발현을 조절하여 선천적 및 적응성 면역, 염증, 스트레스 반응, B 세포 발달, 림프 기관 형성과 같은 다양한 생물학적 과정에 영향을 미칠 수 있습니다. 일반적으로 TLRs, NLRs, RLRs 및 CLRs는 NF-κB 단백질의 활성화를 억제하는 IκB 단백질을 인산화하여 염증 유전자의 전사와 활성화를 촉진합니다.
In the signal transduction initiated by TLRs,45 after TLRs recognize and bind the corresponding PAMPs and DAMPs, the TIR domains conduct signals by binding to different receptor adaptor proteins in the cytoplasmic region.254,255 Depending on the different adaptor proteins, TLR signaling can be divided into MyD88-dependent and MyD88-independent pathways.256 MyD88 has a TIR domain at the C-terminus and a death domain at the N-terminus and is the linker molecule in most TLR signal transduction pathways.257 The current research indicated that, in the MyD88-dependent pathway, MyD88 signaling mainly leads to the production of pro-inflammatory cytokines, such as tumor necrosis factor (TNF), IL-6, IL-1, and chemokines.258,259,260 The C-terminus of MyD88 binds to the intracellular TIR domain of TLRs, and the N-terminus of MyD88 recruits IL-1R-related kinase 4 (IRAK4)261 and activates IRAK1 and IRAK2 through autophosphorylation of its central kinase domain. Then ubiquitin ligase TNF receptor-associated factor 6 (TRAF6) is recruited to form a complex with transforming growth factor (TGF)-β-activated kinase 1 (TAK1) and two TAK-binding proteins (TAB1 and TAB4). TRAF6 is degraded due to its own ubiquitination.262,263 The TAK1–TAB1–TAB4 complex activates the IκB kinase (IKK) complex through phosphorylation. The latter phosphorylates IκB and degrades itself by ubiquitination. NF-κB is released and translocated to the nucleus, thereby regulating the transcription of inflammatory genes.264,265
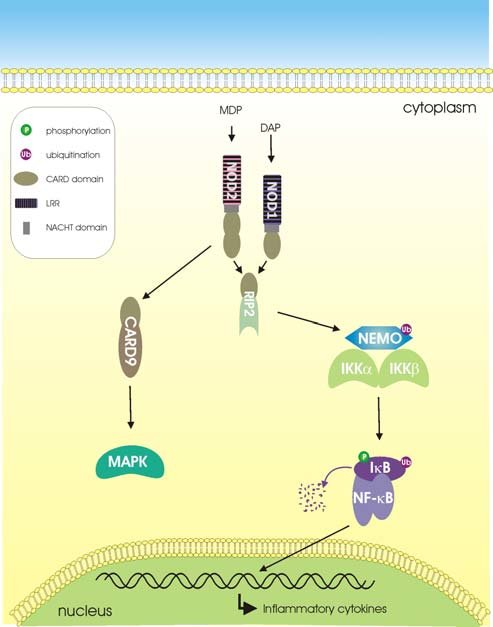
In the signal pathway mediated by NLRs, when the bacterial component invades the cell, NOD1 and NOD2 recognize the bacterial iE-DAP and MDP, respectively.266,267 And then NOD-like receptors are activated, self-dimerize, and recruit downstream receptor-interacting serine–threonine protein 2 (RIP2) through its CARD.268 Activated RIP2 gathers downstream TAK1, TAK1-binding protein 1, and the NF-κB essential modulator/IKKα/IKKβ complex, and the former activates IKKα/IKKβ,269 thereby activating the transcription of NF-κB and promoting the release of pro-inflammatory factors.
When virus invades cells, RIG-I and MDA5 recognize the corresponding viral RNA through the CTD and undergo conformation changes.270 Activated RIG-I and MDA-5 induce downstream signal transduction by binding with mitochondrial antiviral signaling protein (MAVS). MAVS is an important adaptor protein for downstream signal transduction. The N-terminus contains a CARD-like domain, which binds to RIG-I and MDA-5 through the CARD–CARD interaction.271,272 The proline-enriched domain in MAVS can interact with a series of downstream signaling molecules, such as TRAF3 and 6,273 and activate the protein kinase IKK, which causes phosphorylation of IκB,265 and then IκB is ubiquitinated and degraded by proteases, activating the NF-κB pathway.274
Different from other typical PRR-mediated signaling pathways, spleen tyrosine kinase (Syk) can be activated by associating with the phosphorylated ITAM motif of CLRs.275 In the Dectin-1/Syk pathway, Syk activates protein kinase C-δ, which mediates the phosphorylation of CARD9.276 This allows CARD9 to bind to B cell lymphoma 10277 and para-aspase mucosa-associated lymphoid tissue lymphoma translocation protein 1, forming a three molecular structure that can typically activate NF-κB.278
TLR에 의해 시작되는 신호 전달에서,45 TLR이 해당 PAMP 및 DAMP를 인식하고 결합한 후, TIR 도메인은 세포질 영역에서 서로 다른 수용체 어댑터 단백질에 결합하여 신호를 전달한다.254,255 서로 다른 어댑터 단백질에 따라, TLR 신호전달은 MyD88 의존적 경로와 MyD88 비의존적 경로로 구분됩니다.256 MyD88은 C-말단에 TIR 도메인을, N-말단에 데스 도메인을 가지며 대부분의 TLR 신호전달 경로에서 연결 분자 역할을 합니다.257 현재 연구에 따르면, MyD88 의존적 경로에서 MyD88 신호전달은 주로 종양괴사인자(TNF), IL-6, IL-1 및 케모카인과 같은 전염증성 사이토카인의 생성을 유도한다.258,259,260 MyD88의 C-말단은 TLR의 세포내 TIR 도메인에 결합하며, MyD88의 N-말단은 IL-1R 관련 키나아제 4 (IRAK4)를 모집하고, 그 중심 키나아제 도메인의 자가인산화를 통해 IRAK1 및 IRAK2를 활성화합니다. 그런 다음 유비퀴틴 리가아제 TNF 수용체 관련 인자 6(TRAF6)이 모집되어 변형 성장 인자(TGF)-β 활성화 키나아제 1(TAK1) 및 두 개의 TAK 결합 단백질(TAB1 및 TAB4)과 복합체를 형성합니다. TRAF6는 자체 유비퀴틴화 때문에 분해된다.262,263 TAK1–TAB1–TAB4 복합체는 인산화를 통해 IκB 키나아제(IKK) 복합체를 활성화한다. 후자는 IκB를 인산화하고 자체 유비퀴틴화를 통해 분해된다. NF-κB가 방출되어 핵으로 이동함으로써 염증 유전자 전사를 조절한다.264,265
NLR 매개 신호 경로에서 세균 성분이 세포를 침입하면 NOD1과 NOD2가 각각 세균성 iE-DAP 및 MDP를 인식한다.266,267 이후 NOD 유사 수용체가 활성화되어 자가 이량체화하고, CARD를 통해 하류 수용체 상호작용 세린-트레오닌 단백질 2(RIP2)를 모집한다. 268 활성화된 RIP2는 하류의 TAK1, TAK1 결합 단백질 1 및 NF-κB 필수 조절자/IKKα/IKKβ 복합체를 모으고, 전자는 IKKα/IKKβ를 활성화하여269 NF-κB의 전사를 활성화하고 전염증 인자의 방출을 촉진합니다.
바이러스가 세포를 침입하면 RIG-I와 MDA5는 CTD를 통해 해당 바이러스 RNA를 인식하고 구조적 변화를 겪습니다.270 활성화된 RIG-I와 MDA-5는 미토콘드리아 항바이러스 신호 전달 단백질(MAVS)과 결합하여 하류 신호 전달을 유도합니다. MAVS는 하류 신호 전달을 위한 중요한 어댑터 단백질입니다. N-말단에는 CARD-like 도메인이 포함되어 있으며, CARD-CARD 상호 작용을 통해 RIG-I 및 MDA-5에 결합합니다. 271,272 MAVS의 프롤린 풍부 도메인은 TRAF3 및 6과 같은 일련의 하류 신호 분자와 상호작용할 수 있으며,273 단백질 키나아제 IKK를 활성화하여 IκB의 인산화를 유발합니다.265 이후 IκB는 유비퀴틴화되어 프로테아제에 의해 분해되며, 이는 NF-κB 경로를 활성화시킵니다.274
다른 전형적인 PRR 매개 신호전달 경로와 달리, 비장 티로신 키나제(Syk)는 CLR의 인산화된 ITAM 모티프와 결합함으로써 활성화될 수 있다.275 Dectin-1/Syk 경로에서, Syk는 단백질 키나제 C-δ를 활성화하여 CARD9의 인산화를 매개한다.276 이를 통해 CARD9는 B 세포 림프종 10277 및 파라아스파제 점막 관련 림프 조직 림프종 전위 단백질 1과 결합하여 전형적으로 NF-κB를 활성화할 수 있는 삼분자 구조를 형성한다.278
The mitogen-activated protein kinase (MAPK) signaling
MAPK is a group of serine–threonine protein kinases that can be activated by different extracellular stimuli,279 such as cytokines, neurotransmitters, hormones, cell stress, and cell adhesion. The MAPK pathway is one of the common intersections of signal transduction pathways, such as cell proliferation, stress, inflammation, differentiation, functional synchronization, transformation, and apoptosis.280,281 It is an important transmitter of signals from the cell surface to the inside of the nucleus.
In the MyD88-dependent pathway of TLRs, IRAK-1 is activated by phosphorylation and interacts with TRAF6. In addition to activating the IKK complex, it can also cause the activation of MAPKs (c-Jun N-terminal kinase (JNK), p38 MAPK).282 In addition, when bacterial components invade cells, NLRs are activated, recruiting downstream CARD9, thereby activating p38, JNK, and finally activating the MAPK pathway283 to promote the release of pro-inflammatory factors.
미토겐 활성화 단백질 키나아제(MAPK) 신호 전달
MAPK는 사이토카인, 신경전달물질, 호르몬, 세포 스트레스, 세포 접착 등 다양한 세포외 자극에 의해 활성화될 수 있는 세린-트레오닌 단백질 키나아제 그룹이다. MAPK 경로는 세포 증식, 스트레스, 염증, 분화, 기능적 동기화, 변형 및 세포 사멸과 같은 신호 전달 경로의 공통 교차점 중 하나입니다.280,281 이는 세포 표면에서 핵 내부로 신호를 전달하는 중요한 매개체입니다.
TLR의 MyD88 의존 경로에서 IRAK-1은 인산화에 의해 활성화되어 TRAF6과 상호작용합니다. IKK 복합체를 활성화하는 것 외에도 MAPK(c-Jun N-말단 키나아제(JNK), p38 MAPK)의 활성화도 유발할 수 있습니다.282 또한 세균 성분이 세포에 침입하면 NLR이 활성화되어 하류 CARD9를 모집함으로써 p38, JNK를 활성화하고, 최종적으로 MAPK 경로를 활성화하여283 전염증 인자의 방출을 촉진합니다.
The TBK1–IRF-3 signaling
IRF-3 is a key transcription factor that promotes the synthesis of type I IFN and plays an important role in the antiviral innate immune response.284 IRF-3 can be activated through two innate immune antiviral signal pathways, TLR3/TLR4-TIR domain-containing adaptor protein-inducing interferon β (TRIF) and RIG-I-MAVS,285 and then dimerize and merge into the nucleus to work (Fig. 6).286
TBK1–IRF-3 신호전달
IRF-3은 제1형 인터페론(IFN) 합성을 촉진하는 핵심 전사인자로, 항바이러스 선천면역 반응에서 중요한 역할을 합니다.284 IRF-3은 두 가지 선천면역 항바이러스 신호 경로, TLR3/TLR4-TIR 도메인 함유 적응 단백질-인터페론 β 유도체(TRIF) 및 RIG-I-MAVS 경로를 통해 활성화되며,285 이후 이량체화되어 핵으로 이동하여 작용합니다(그림 6).286
Fig. 6
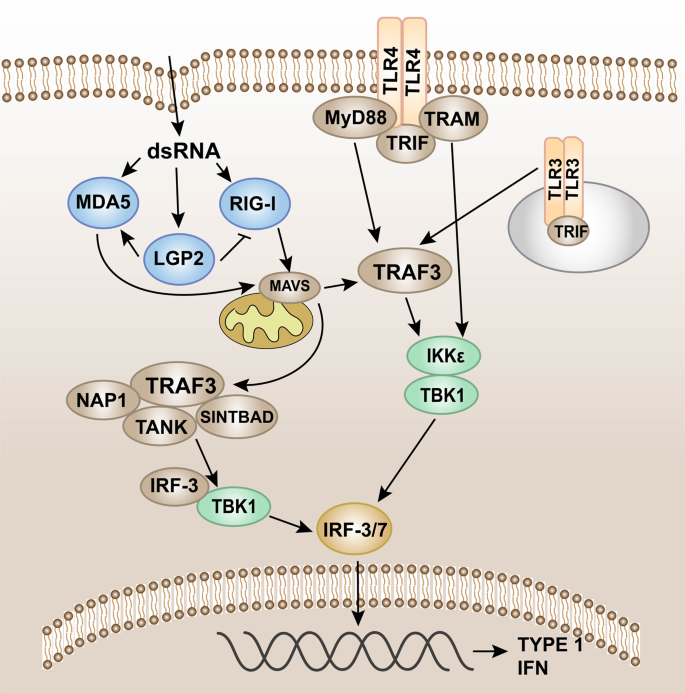
Pattern recognition receptor-mediated TBK1-IRF-3 signaling. Intracellular induction of pathogens is carried out through the detection of foreign molecular components (including cytoplasmic viral and bacterial nucleic acids). Once detected, the innate immune system induces type I interferon (IFN) production through the TANK-binding kinase 1 (TBK1)-interferon regulatory factor-3/7 (IRF-3/7) pathway. IRF-3/7 can be activated through two innate immune antiviral signal pathways, TLR3/TLR4-TIR domain-containing adaptor protein-inducing interferon β (TRIF) and RIG-I-MAVS, and then dimerize and merge into the nucleus to work
그림 6
패턴 인식 수용체 매개 TBK1-IRF-3 신호전달. 병원체의 세포 내 유도는 외래 분자 구성 요소(세포질 내 바이러스 및 세균 핵산 포함)의 검출을 통해 이루어진다. 검출 시 선천 면역 체계는 TANK 결합 키나아제 1(TBK1)-인터페론 조절 인자-3/7(IRF-3/7) 경로를 통해 제1형 인터페론(IFN) 생산을 유도한다. IRF-3/7은 두 가지 선천성 면역 항바이러스 신호 경로, TLR3/TLR4-TIR 도메인 함유 어댑터 단백질-인터페론 β 유도체(TRIF) 및 RIG-I-MAVS를 통해 활성화될 수 있으며, 이후 이량체화되어 핵으로 이동하여 작용한다.
The adaptor protein in the MyD88-independent pathway is TRIF. The TRIF axis mainly induces the expression of type I IFNs.287 After the receptor is recognized and combined with the ligand, the pathway is activated by TRIF and TRAF3, leading to the recruitment of IKKε/TANK-binding kinase 1 (TBK1),288 phosphorylation of IRF3, and the activation of type I IFN genes, which promotes the expression of IFN-α and IFN-β, and exerts antiviral effects (Fig. 6).289,290,291
RLRs such as RIG-I and MDA5 can detect viral nucleic acid. MDA5 and RIG-I will interact with the shared caspase recruitment domain to induce MAVS to dimerize and bind to TRAF3.134,140,292 In turn, TRAF3 recruits the adaptor proteins TANK, NAP1, and SINTBAD. TANK connects upstream RLR signal transduction to TBK1, which induces phosphorylation of IRF-3. IRF-3 phosphorylation and subsequent dimerization induce IRF-3 nuclear translocation, leading to type I IFN gene expression (Fig. 6).192,293,294
MyD88 독립 경로의 어댑터 단백질은 TRIF이다. TRIF 축은 주로 제1형 인터페론(IFN)의 발현을 유도한다.287 수용체가 인식되어 리간드와 결합한 후, TRIF와 TRAF3에 의해 경로가 활성화되어 IKKε/TANK 결합 키나아제 1(TBK1)의 모집, (TBK1)의 활성화, IRF3의 인산화, 제1형 인터페론 유전자 활성화를 유발하여 IFN-α 및 IFN-β 발현을 촉진하고 항바이러스 효과를 발휘한다(그림 6).289,290,291
RIG-I 및 MDA5와 같은 RLR은 바이러스 핵산을 감지할 수 있습니다. MDA5와 RIG-I는 공유 카스파제 모집 도메인과 상호작용하여 MAVS의 이량체화를 유도하고 TRAF3에 결합합니다.134,140,292 차례로 TRAF3는 어댑터 단백질 TANK, NAP1 및 SINTBAD를 모집합니다. TANK는 상류 RLR 신호전달을 TBK1에 연결하여 IRF-3의 인산화를 유도한다. IRF-3 인산화와 후속 이량체화는 IRF-3의 핵 내 이동을 유발하여 제1형 인터페론 유전자 발현으로 이어진다(그림 6).192,293,294
The inflammasome signaling
Inflammasome is the multi-protein complex assembled by PRRs in the cytoplasm and is an important part of the innate immune system.295 The inflammasome can recognize PAMPs or DAMPs and recruit and activate Caspase-1. The activated Caspase-1 spliced proIL-1β/proIL-18 into the corresponding mature cytokine.193,296 There are five main types of inflammasomes that have been discovered, namely, NLRP1 inflammasome,297 NLRP3 inflammasome,298 NLRC4 inflammasome,299,300 IPAF inflammasome, and AIM2 inflammasome.301 Known inflammasomes generally contain ASC, caspase protease, and a protein of the NLR family (e.g., NLRP3) or HIN-200 family protein (e.g., AIM2). Taking NLRP3 as an example,302 the dimerization of NLRP3 under the action of intracellular PAMPs or DAMPs makes the two PYDs to polymerize. With the help of homotype interaction, NLRP3 binds and activates the ASC complex with both PYD and CARD domains, which reactivates the effector complex composed of CARD and caspase-1. In this way, NLRP3 (LRR + NACHT + PYD), ASC (PYD + CARD), and the effector complex (CARD + Caspase-1) together constitute the inflammasome, which produces important pro-inflammatory factors.303,304,305 After AIM2 recognizes cytoplasmic dsDNA, it also uses inflammasomes to produce IL-1β and IL-18. After AIM2 recognizes cytoplasmic dsDNA, it also produces IL-1β and IL-18 through the inflammasome pathway (Fig. 7).306
인플라마좀 신호전달
인플라마좀은 세포질 내 PRR에 의해 조립되는 다중 단백질 복합체로 선천성 면역 체계의 중요한 구성 요소이다.295 인플라마좀은 PAMP 또는 DAMP를 인식하여 카스파제-1을 모집 및 활성화한다. 활성화된 카스파제-1은 프로IL-1β/프로IL-18을 각각 성숙 사이토카인으로 절단한다.193,296 현재까지 발견된 주요 인플라마좀 유형은 NLRP1 인플라마좀,297 NLRP3 인플라마좀,298 NLRC4 인플라마좀,299,300 IPAF 인플라마좀, AIM2 인플라마좀 등 다섯 가지이다. 301 알려진 인플람소좀은 일반적으로 ASC, 카스파제 프로테아제, 그리고 NLR 계열 단백질(예: NLRP3) 또는 HIN-200 계열 단백질(예: AIM2)을 포함합니다. NLRP3를 예로 들면,302 세포 내 PAMP 또는 DAMP의 작용 하에서 NLRP3의 이량체화는 두 개의 PYD를 중합하게 합니다. 동형 상호작용의 도움으로, NLRP3는 PYD 및 CARD 도메인을 모두 가진 ASC 복합체에 결합하고 이를 활성화하여 CARD 및 카스파제-1로 구성된 효과기 복합체를 재활성화합니다. 이러한 방식으로 NLRP3(LRR+NACHT+PYD), ASC(PYD+CARD) 및 효과기 복합체(CARD+Caspase-1)가 함께 인플람소좀을 구성하여 중요한 전염증 인자를 생성합니다. 303,304,305 AIM2가 세포질 이중가닥 DNA(dsDNA)를 인식한 후에도 염증체(inflammasome)를 이용해 IL-1β와 IL-18을 생성합니다. AIM2가 세포질 dsDNA를 인식한 후 염증체 경로를 통해 IL-1β와 IL-18을 생성합니다(그림 7).306
Fig. 7
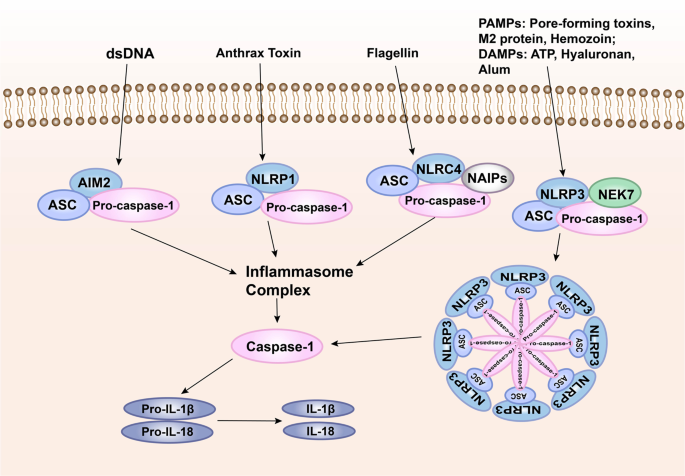
Pattern recognition receptor-mediated inflammasome signaling. One way for pathogenic microorganisms to induce inflammation is by activating inflammasomes, which are multi-protein complexes assembled by PRRs in the cytoplasm and activate caspase-1 and subsequent activation of pro-inflammatory cytokines IL-1β and IL-18. The inflammasome complex usually contains cytoplasmic PRRs, adaptor protein (ASC), and pro-caspase-1. Many different inflammasome complexes have been detected, each with unique PRRs and activation triggers
그림 7
패턴 인식 수용체 매개 인플라마좀 신호전달. 병원성 미생물이 염증을 유도하는 한 가지 방법은 세포질 내 PRR에 의해 조립된 다중 단백질 복합체인 인플라마좀을 활성화하여 카스파제-1을 활성화하고, 이후 염증 유발 사이토카인인 IL-1β 및 IL-18의 활성화를 유도하는 것이다. 인플라마좀 복합체는 일반적으로 세포질 PRR, 어댑터 단백질(ASC), 프로카스파제-1을 포함한다. 각각 고유한 PRR과 활성화 유발 인자를 가진 다양한 인플라마좀 복합체가 발견되었다.
Innate immunity not only plays a role in controlling the infection and spread of pathogens in the early stage of infection but also plays an important role in initiating and regulating adaptive immunity.12,307 Innate immune cells produce different types of cytokines through signal transduction initiated after PRRs recognize PAMPs, which directly affect the differentiation of T helper type 1 (Th1), Th2, Th17, and other subgroups in adaptive immunity.15 For example, pathogenic microorganisms activate macrophages to secrete IL-6, TGF-β, IL-23, and other cytokines, which promote Th17 response, leading to excessive immune-inflammatory effects and tissue damage, or activate NK cells to secrete IFN-γ, and then activate macrophages to secrete IL-12, promote the differentiation of Th0 into Th1, promote cellular immune response, and effectively eliminate viral infections.13,308 Therefore, the immune system is a system of mutual influence. Any anti-infection process is completed by mutually activating or inhibiting of different components. These components are as small as each cytokine and as large as the immune system.
선천성 면역은 감염 초기 단계에서 병원체의 감염 및 확산을 제어하는 역할을 할 뿐만 아니라, 적응성 면역의 개시 및 조절에도 중요한 역할을 합니다.12,307 선천성 면역 세포는 PRR이 PAMP를 인식한 후 시작되는 신호 전달을 통해 다양한 유형의 사이토카인을 생성하며, 이는 적응성 면역에서 T 헬퍼 1형(Th1), Th2, Th17 및 기타 하위 집단의 분화에 직접적인 영향을 미칩니다.15 예를 들어, 병원성 미생물은 대식세포를 활성화시켜 Th17 반응을 촉진하는 IL-6, TGF-β, IL-23 및 기타 사이토카인을 분비하게 하여 Th17 반응을 촉진함으로써 과도한 면역-염증 효과와 조직 손상을 초래하거나, NK 세포를 활성화하여 IFN-γ를 분비하게 한 후 대식세포를 활성화하여 IL-12를 분비하게 하여 Th0의 Th1 분화를 촉진하고 세포성 면역 반응을 증진시켜 바이러스 감염을 효과적으로 제거합니다.13,308 따라서 면역 체계는 상호 영향을 미치는 시스템입니다. 모든 항감염 과정은 서로 다른 구성 요소들의 상호 활성화 또는 억제를 통해 완성됩니다. 이러한 구성 요소들은 각 사이토카인처럼 작을 수도 있고 면역 체계처럼 클 수도 있습니다.
PRR-related diseases
PRRs and cancers
The inflammatory microenvironment of tumor constitutes the barrier for tumor growth, which is conducive to tumor formation and development.309 PRRs are widely expressed in a variety of tumor tissues, such as colon cancer, lung cancer, breast cancer, gastric cancer, melanoma, and so on.310,311 The activation of PRRs on the surface of tumor cells can induce the expression of a large number of cytokines, chemokines, hormones, and vascular-promoting factors, which is one of the important factors to induce the formation of tumor inflammatory microenvironment and promote the development of tumor.312,313 At the same time, the activation of PRRs on immune cells can induce antigen-presenting cells including DCs, tumor-associated macrophages, and B cells to activate tumor-specific T cell responses or enhance the antitumor effects of phagocytes. These also indicate that the role of PRRs in immunotherapy against tumors is very important and might represent a new strategy for patients with tumors.314,315
We can see from the data in GEPIA316 (http://gepia.cancer-pku.cn/) that TLR level is significantly increased in tumors, including glioblastoma multiforme, brain lower-grade glioma, kidney renal clear cell carcinoma, acute myeloid leukemia (AML), and pancreatic adenocarcinoma (PAAD). NOD1/2 are highly expressed in AML and PAAD, while RLRs are highly expressed in AML, PAAD, diffuse large B cell lymphoma, head and neck squamous cell carcinoma, and thymoma.
PRR 관련 질환
PRR과 암
종양의 염증성 미세환경은 종양 성장에 대한 장벽을 구성하며, 이는 종양의 형성과 발달에 유리합니다.309 PRR은 대장암, 폐암, 유방암, 위암, 흑색종 등 다양한 종양 조직에서 광범위하게 발현됩니다.310,311 종양 세포 표면의 PRR 활성화는 다량의 사이토카인, 케모카인, 호르몬 및 혈관 촉진 인자의 발현을 유도할 수 있으며, 이는 종양 염증성 미세환경 형성을 유도하고 종양 발달을 촉진하는 중요한 요인 중 하나이다.312,313 동시에, 면역 세포 상의 PRR 활성화는 DC, 종양 연관 대식세포 및 B 세포를 포함한 항원제시세포가 종양 특이적 T 세포 반응을 활성화하거나 식세포의 항종양 효과를 강화하도록 유도할 수 있다. 이러한 점들은 PRR이 종양 면역치료에서 매우 중요한 역할을 하며, 종양 환자를 위한 새로운 전략이 될 수 있음을 시사한다.314,315
GEPIA316 (http://gepia.cancer-pku.cn/)의 데이터에서 볼 수 있듯이, 다형성 교모세포종, 뇌 저등급 신경교종, 신장 투명세포암종, 급성 골수성 백혈병(AML), 췌장 선암종(PAAD)을 포함한 종양에서 TLR 수준이 현저히 증가합니다 . NOD1/2는 AML과 PAAD에서, RLRs는 AML, PAAD, 미만성 거대 B세포 림프종, 두경부 편평세포암종, 흉선종에서 높은 발현을 보인다.
Colorectal cancer (CRC)
CRC, including colon cancer and rectal cancer, is one of the most common gastrointestinal malignancies in clinical practice, and it is also one of the cancers that seriously endanger human health.317,318 Intestinal mucosal epithelial cells and immune cells recognize intestinal microorganisms and their products through TLRs.319,320,321,322 TLR2 can recognize peptidoglycans and lipopeptides that infect intestinal epithelial bacteria and produce anti-infection and other immune-protective effects.323 Studies have shown that the expression level of TLR2 protein in colon cancer is significantly upregulated compared with normal epithelial tissues,324 and the use of TLR2 agonists significantly enhances the proliferation, migration, and invasion capabilities of colon cancer cells.325 TLR4 is highly expressed on the surface of colon cancer cells. After stimulation and activation, it can induce a variety of immunosuppressive factors, thus promoting the proliferation and immune escape of colon cancer cells.326 First, TLR4 can produce trophic factors and vascular growth factors through the TLR4/MyD88/NF-κB signaling pathway, thereby promoting tumor cell invasion.327,328 Second, TLR4 can promote tumor proliferation through TLR4/Cyclooxygenase 2 (COX2)/prostaglandin E2 (PGE2). PGE2 is an important cell growth and regulatory factor. After binding to specific receptors, it plays a key role in mediating a series of cell activities, such as cell proliferation, differentiation, and apoptosis, and has immunosuppressive and anti-inflammatory effects. COX2 is the rate-limiting enzyme of prostaglandin synthesis, and it is also highly expressed in inflammation, tumor, and other pathological states.329 Hsu et al.330 found that knocking out the mouse TLR4 gene significantly reduced the expression of COX2 and PGE2 in the intestinal mucosa; after administration of PGE2, the expression of COX2 in the intestinal mucosa increased significantly and promoted the occurrence of intestinal tumors. After administration of PGE2, the expression of COX2 in the intestinal mucosa increased significantly and promoted the occurrence of intestinal tumors. At the same time, it has also been found to promote the expression of amphiregulin and epidermal growth factor receptor (EGFR) in the intestinal mucosa. Finally, the study showed that the abnormal expression of TLR4 in CRC caused by chronic inflammation of the intestine can significantly enhance the expression of PGE2, the upregulation of COX2, and the phosphorylation of EGFR in intestinal mucosal cells, thereby positive feedback promotes the proliferation of tumor cells. TLR5 also plays an important role in tumor immunotherapy.331 In mouse xenograft models of human colon cancer, flagellin around the tumor activates TLR5 to inhibit tumor growth and promote tumor apoptosis.332 In addition, TLR9 is expressed on the surface of the mesentery, which maintains intestinal homeostasis and repairs intestinal damage by generating an immune response.333 TLR9 relies on the MyD88 pathway to induce downstream signals to recruit many inflammatory factors, such as IL-8, TGF-β, PGE2, and other immunosuppressive molecules,334 leading to the continuous development of inflammation, resulting in immune escape, and promoting the unlimited proliferation of tumor cells. After TLR9 recognizes the exogenous ligand, it upregulates the expression of NF-κB signaling factor. Once this pathway is opened, it may induce the secretion of matrix metalloproteinase-13 (MMP-13) and the activation of intercellular adhesion molecule-1, thus promoting the metastasis of tumor cells.335,336 At the same time, the metastatic tumor cells are better adapted and combined with the cell matrix at the metastasis, and the stability of tumor cell metastasis is enhanced. Although TLRs have been shown to enhance colon cancer metastasis, inhibiting these receptors cannot completely hinder tumor progression. Surprisingly, NOD1 is highly expressed in human CRC and its cell lines. After being activated by C12-iE-DAP, it mainly enhances the adhesion, migration, and metastasis of CRC cells through the p38 MAPK pathway.337
대장암(CRC)
대장암(CRC)은 대장암과 직장암을 포함하며, 임상에서 가장 흔한 위장관 악성 종양 중 하나이며, 또한 인체 건강을 심각하게 위협하는 암 중 하나입니다.317,318 장 점막 상피 세포와 면역 세포는 TLR을 통해 장내 미생물과 그 생성물을 인식합니다. 319,320,321,322 TLR2는 장 상피 세균을 감염시키는 펩티도글리칸 및 지질펩타이드를 인식하여 항감염 및 기타 면역 보호 효과를 생성할 수 있다.323 연구에 따르면 대장암에서 TLR2 단백질의 발현 수준은 정상 상피 조직에 비해 현저히 상향 조절되며,324 TLR2 작용제를 사용하면 대장암 세포의 증식, 이동 및 침습 능력을 현저히 증진시킵니다.325 TLR4는 대장암 세포 표면에 고도로 발현됩니다. 자극 및 활성화 후 다양한 면역억제 인자를 유도하여 대장암 세포의 증식과 면역 회피를 촉진한다.326 첫째, TLR4는 TLR4/MyD88/NF-κB 신호전달 경로를 통해 영양 인자와 혈관 성장 인자를 생성하여 종양 세포 침습을 촉진한다.327,328 둘째, TLR4는 TLR4/사이클로옥시게나제 2(COX2)/프로스타글란딘 E2(PGE2) 경로를 통해 종양 증식을 촉진할 수 있다. PGE2는 중요한 세포 성장 및 조절 인자이다. 특정 수용체에 결합한 후, 세포 증식, 분화, 세포 사멸과 같은 일련의 세포 활동을 매개하는 데 핵심적인 역할을 하며, 면역억제 및 항염증 효과를 가진다. COX2는 프로스타글란딘 합성의 속도 제한 효소이며, 염증, 종양 및 기타 병리학적 상태에서도 고도로 발현된다.329 Hsu 등330은 마우스 TLR4 유전자를 녹아웃하면 장 점막에서 COX2와 PGE2의 발현이 현저히 감소함을 발견했다. PGE2 투여 후 장 점막의 COX2 발현이 현저히 증가하여 장 종양 발생을 촉진했다. PGE2 투여 후 장 점막에서 COX2 발현이 현저히 증가하여 장 종양 발생을 촉진했습니다. 동시에 장 점막에서 암피레굴린(amphiregulin)과 표피 성장 인자 수용체(EGFR)의 발현을 촉진하는 것으로도 밝혀졌습니다. 마지막으로, 연구에 따르면 장의 만성 염증으로 인한 CRC에서 TLR4의 비정상적인 발현은 장 점막 세포에서 PGE2 발현, COX2의 상향 조절 및 EGFR의 인산화를 현저히 증가시켜 양의 피드백을 통해 종양 세포의 증식을 촉진하는 것으로 나타났습니다. TLR5 또한 종양 면역 치료에서 중요한 역할을 합니다.331 인간 대장암 마우스 이종이식 모델에서 종양 주변의 플라젤린은 TLR5를 활성화하여 종양 성장을 억제하고 종양 세포 사멸을 촉진합니다.332 또한, TLR9는 장간막 표면에 발현되어 면역 반응을 생성함으로써 장의 항상성을 유지하고 장 손상을 복구합니다.333 TLR9는 MyD88 경로를 통해 하류 신호를 유도하여 IL-8, TGF-β, PGE2 및 기타 면역억제 분자 등을 유도하여334 염증이 지속적으로 발전하게 하여 면역 회피를 초래하고 종양 세포의 무제한 증식을 촉진합니다. TLR9가 외인성 리간드를 인식한 후에는 NF-κB 신호 인자의 발현을 상향 조절합니다. 이 경로가 활성화되면, 매트릭스 메탈로프로테이나제-13(MMP-13)의 분비와 세포간 접착 분자-1(ICAM-1)의 활성화를 유도하여 종양 세포의 전이를 촉진할 수 있다.335,336 동시에 전이된 종양 세포는 전이 부위에서 세포 기질과 더 잘 적응하고 결합하여 종양 세포 전이의 안정성이 강화된다. TLR이 대장암 전이를 촉진하는 것으로 밝혀졌지만, 이러한 수용체를 억제한다고 해서 종양 진행을 완전히 막을 수는 없습니다. 놀랍게도 NOD1은 인간 대장암(CRC) 및 그 세포주에서 고도로 발현됩니다. C12-iE-DAP에 의해 활성화된 후, 주로 p38 MAPK 경로를 통해 CRC 세포의 접착, 이동 및 전이를 촉진합니다.337
Hepatocellular carcinoma (HCC)
HCC is the most common type of primary liver cancer. Among its many influencing factors, inflammation is one of the main reasons that induce liver cancer.338 The expression of TLR2 in liver cancer tissues is significantly higher than that in normal liver tissues, and the expression of TLR2 protein is related to some mutant genes that lead to the occurrence of HCC, such as p53, PIK3CA, and β-catenin.339,340,341,342 In addition, Chew et al. revealed that the expression of TLR3 has independent effects on tumor parenchyma and infiltrating NK cells, and the expression of these two parts is related to inhibiting tumor cell proliferation, promoting tumor cell death, and prolonging the survival rate of patients.343 This indicates that TLR3 may directly act on tumor parenchymal cells, promote the recruitment and activation of NK cells, and exert antitumor effects. More and more evidences show that LPS plays a role in the development of HCC. Zhou et al.344 found that LPS activates the TLR4–AKT–SOX2 signaling pathway of liver cancer cell lines to improve the ability of cancer stem cells; Lin et al.345 found that there is a positive feedback loop of COX-2/PGE2/signal transducer and activator of transcription factor 3 (STAT3) activated by LPS in liver cancer cells, which regulates the expression of genes related to tumor proliferation, differentiation, and apoptosis. In the latest research on the treatment of liver cancer, it is found that the antitumor effect of TLR9 agonist combined with anti-PD-1 antibody or anti-PD-L1 is significantly better than single-agent therapy.346 The activation of TLR9 inherent in liver cancer cells regulates the autoarylation and ubiquitination of poly(ADP-ribose) polymerase-1 and the phosphorylation of STAT3, which together upregulate the expression of PD-L1 and eventually induce immune escape. Although TLRs have been reported to be associated with chronic inflammation of the liver, whether they promote the development of HCC remains uncertain. Song et al.347 found that the deficiency of TLR4, TLR9, and their downstream molecule MyD88 in a mouse model characterized by hepatic deletion of TAK1 could block the liver inflammation–fibrosis–cancer axis and reduce liver injury and tumor growth. For TLR3, the downregulation of TLR3 in HCC patients leads to poor prognosis (e.g., defective immune cell recruitment and lack of killing of transformed hepatocytes), leading to protection of transformed hepatocytes from apoptosis, thereby promoting the occurrence of liver cancer.348 Therefore, the expression of TLR3 may become a useful clinical treatment monitoring marker.
In addition to the above reasons, there is now more and more evidence that the imbalance of the gut–hepatic axis may also play a role in the occurrence of HCC.349 Zhou et al.350 discovered that NOD2 acts as a bacterial sensor, linking gut-derived microorganisms to the occurrence of HCC through a known mechanism and a newly discovered mechanism. The known mechanism is that NOD2 activates NF-κB, JAK2/STAT3, and MAPK pathways in a RIP2-dependent manner, leading to liver inflammation.351 It is worth noting that activated NOD2 can also act as the initiator of the nuclear autophagy pathway that does not depend on RIP2, thereby promoting the degradation of the nuclear component lamin A/C, leading to damage to DNA damage repair mechanisms and increased genomic instability, which eventually leads to the occurrence of HCC.350 Meanwhile, the study found that the expression of ALRs was negatively correlated with tumor volume, stage, and metastasis of HCC patients. The researchers proposed that overexpression of ALRs in HCC cells could increase the expression of caspase-1 and IL-1a, and the release of lactate dehydrogenase was also observed,352 which was a marker of the initiation of apoptosis. Thus, ALRs may play an antitumor role by promoting tumor cell apoptosis.
간세포암(HCC)
HCC는 가장 흔한 원발성 간암 유형입니다. 여러 영향 요인 중 염증은 간암을 유발하는 주요 원인 중 하나이다.338 간암 조직에서 TLR2 발현은 정상 간 조직보다 현저히 높으며, TLR2 단백질 발현은 p53, PIK3CA, β-catenin 등 HCC 발생을 유도하는 일부 돌연변이 유전자와 관련이 있다.339,340,341, 342 또한 Chew 등은 TLR3 발현이 종양 실질 세포와 침윤성 NK 세포에 독립적인 영향을 미치며, 이 두 부분의 발현은 종양 세포 증식 억제, 종양 세포 사멸 촉진, 환자 생존율 연장 등과 관련이 있음을 밝혀냈다.343 이는 TLR3가 종양 실질 세포에 직접 작용하여 NK 세포의 모집 및 활성화를 촉진하고 항종양 효과를 발휘할 수 있음을 시사한다. 점점 더 많은 증거가 LPS가 간세포암(HCC) 발생에 역할을 한다는 것을 보여주고 있다. Zhou 등344은 LPS가 간암 세포주의 TLR4-AKT-SOX2 신호전달 경로를 활성화하여 암 줄기세포의 능력을 향상시킨다는 것을 발견했다; Lin 등345은 간암 세포에서 LPS에 의해 활성화된 COX-2/PGE2/전사 인자 3의 신호 전달 및 활성화 인자(STAT3)의 양의 피드백 루프가 존재하며, 이는 종양 증식, 분화 및 세포 사멸과 관련된 유전자 발현을 조절한다는 사실을 발견했습니다. 간암 치료에 관한 최신 연구에서, TLR9 작용제와 항-PD-1 항체 또는 항-PD-L1을 병용한 항종양 효과가 단일 요법보다 현저히 우수하다는 것이 밝혀졌다. 346 간암 세포에 내재된 TLR9의 활성화는 폴리(ADP-리보스) 중합효소-1의 자가아릴화 및 유비퀴틴화와 STAT3의 인산화를 조절하며, 이들이 함께 PD-L1 발현을 상향 조절하여 결국 면역 회피를 유도한다. TLR이 간 만성 염증과 연관된다는 보고는 있으나, 간세포암(HCC) 발병을 촉진하는지는 불확실하다. 송 등347은 TAK1이 간에서 결손된 마우스 모델에서 TLR4, TLR9 및 그 하류 분자인 MyD88의 결핍이 간 염증-섬유증-암 축을 차단하고 간 손상 및 종양 성장을 감소시킬 수 있음을 발견했습니다. TLR3의 경우, 간세포암 환자에서 TLR3의 하향 조절은 불량한 예후(예: 결함 있는 면역 세포 모집 및 변형 간세포 사멸 부족)로 이어져 변형 간세포를 세포 사멸로부터 보호함으로써 간암 발생을 촉진한다.348 따라서 TLR3의 발현은 유용한 임상 치료 모니터링 지표가 될 수 있다.
위와 같은 이유 외에도, 장-간 축의 불균형이 간세포암 발생에 관여할 수 있다는 증거가 점점 더 많아지고 있다.349 Zhou 등350은 NOD2가 박테리아 센서 역할을 하여, 알려진 기전과 새로 발견된 기전을 통해 장 유래 미생물과 간세포암 발생을 연결한다는 사실을 발견했다. 알려진 기전은 NOD2가 RIP2 의존적 방식으로 NF-κB, JAK2/STAT3 및 MAPK 경로를 활성화하여 간 염증을 유발한다는 것이다.351 주목할 점은 활성화된 NOD2가 RIP2에 의존하지 않는 핵 오토파지 경로의 개시자 역할도 하여 이를 통해 핵 구성 요소인 라민 A/C의 분해를 촉진하여 DNA 손상 복구 기전의 손상과 유전체 불안정성 증가를 초래하며, 결국 간세포암 발생으로 이어진다.350 한편, 연구진은 ALR 발현이 간세포암 환자의 종양 부피, 병기 및 전이와 음의 상관관계를 보인다는 사실을 발견했다. 연구진은 간세포암 세포에서 ALRs의 과발현이 카스파제-1과 IL-1a의 발현을 증가시키고, 유산탈수소효소(LDH)의 방출도 관찰되었다고 제안했다.352 이는 세포사멸(아포토시스)의 시작을 나타내는 지표이다. 따라서 ALRs는 종양 세포의 세포사멸을 촉진함으로써 항종양 역할을 할 수 있다.
Breast cancer
Breast cancer is one of the most common malignant tumors in the female population. It has a strong ability to invade and metastasize.353 It can metastasize to the liver, lung, brain, bone, and other organs, forming complications and increasing the difficulty of treatment. Studies have shown that the promotion of the TLR2 signaling pathway on the metastasis and invasion ability of human breast cancer cells is achieved by upregulating the secretion of inflammatory cytokines.354 LTA, a TLR2 specific ligand, can significantly promote the secretion of tumor metastasis-related factors IL-6, TGF-β, and vascular endothelial growth factor (VEGF) in breast cancer cells,355 thereby promoting the proliferation and metastatic invasion of breast cancer cells, and this promotion is related to the level of TLR2 expression.356,357 In addition, the activation of TLR4 can increase the secretion of IL-6 and IL-10 of cancer cells and induce the production of more MMP-2, MMP-9, and VEGF,358,359 which can significantly enhance the invasion ability of breast cancer. It has been reported that activation of TLR4 on metastatic breast cancer cells can regulate the expression of integrin, which can promote its adhesion and invasion.360
유방암
유방암은 여성 인구에서 가장 흔한 악성 종양 중 하나입니다. 침습 및 전이 능력이 매우 강합니다.353 간, 폐, 뇌, 뼈 및 기타 장기로 전이되어 합병증을 유발하고 치료 난이도를 높일 수 있습니다. 연구에 따르면, 인간 유방암 세포의 전이 및 침습 능력에 대한 TLR2 신호 전달 경로의 촉진은 염증성 사이토카인의 분비를 상향 조절함으로써 달성된다.354 TLR2 특이적 리간드인 LTA는 종양 전이 관련 인자인 IL-6, TGF-β 및 혈관 내피 성장 인자(VEGF)의 분비를 현저히 촉진하여355 유방암 세포의 증식과 전이 침습을 촉진하며, 이러한 촉진은 TLR2 발현 수준과 관련이 있다.356,357 또한 TLR4의 활성화는 암세포의 IL-6 및 IL-10 분비를 증가시키고 더 많은 MMP-2, MMP-9 및 VEGF의 생성을 유도할 수 있으며,358,359 이는 유방암의 침습 능력을 현저히 향상시킬 수 있습니다. 전이성 유방암 세포에서 TLR4의 활성화는 인테그린의 발현을 조절하여 그 부착 및 침습을 촉진할 수 있다고 보고되었습니다.360
Head and neck squamous cell carcinoma
Squamous cell carcinoma, also known as epidermal carcinoma, is a malignant tumor occurring in the epidermis or adnexal cells.361,362 It is more common in the parts covered by squamous epithelium, such as skin, mouth, lip, esophagus, cervix, vagina, etc.363,364 TLR2, TLR4, and TLR9 are expressed in primary tumors, neck metastases, and recurrent tumors of oral tongue squamous cell carcinoma (OTSCC), and their expression varies from the tumor surface to the invasive front, which may be one of the important factors to promote the invasion of OTSCC.365,366 NOD1 and NOD2 genes are expressed in the human oral squamous cell carcinoma (OSCC) cell line YD-10B, and they may trigger immune responses through the MAPK pathway. Surprisingly, the study revealed that stimulation by the NOD2 agonist MDP can inhibit cell growth by inducing apoptosis. These findings provide the potential value of MDP as a new candidate for OSCC antitumor drugs.367
두경부 편평세포암
편평세포암(표피암)은 표피 또는 부속기 세포에서 발생하는 악성 종양이다.361,362 편평상피로 덮인 피부, 구강, 입술, 식도, 자궁경부, 질, 등에서 더 흔하게 발생한다.363,364 구강 혀 편평세포암종(OTSCC)의 원발성 종양, 경부 전이 및 재발성 종양에서 TLR2, TLR4 및 TLR9가 발현되며, 그 발현은 종양 표면에서 침습 전선까지 다양하며, 이는 OTSCC의 침습을 촉진하는 중요한 요인 중 하나일 수 있다.365,366 NOD1 및 NOD2 유전자는 인간 구강 편평세포암종(OSCC) 세포주 YD-10B에서 발현되며, 이들은 MAPK 경로를 통해 면역 반응을 유발할 수 있다. 놀랍게도, 연구 결과 NOD2 작용제 MDP에 의한 자극이 세포 사멸을 유도하여 세포 성장을 억제할 수 있음을 밝혀냈다. 이러한 발견은 MDP가 OSCC 항종양 약물의 새로운 후보 물질로서 잠재적 가치를 지닌다는 점을 시사한다.367
Respiratory diseases
Aspergillus fumigatus is a fungus widely distributed in nature. It can easily invade the respiratory tract and cause bronchitis and pneumonia in patients.368,369 For the allergic lung inflammation caused by Aspergillus, the recognition of PAMPs by the body’s dendritic cells is mainly negatively regulated through the TLR2-MyD88 pathway. The results showed that PAMPs recognized by TLR2 upregulated IL-10 and decreased the recruitment of pulmonary eosinophils, thus downregulating Th2 response.370,371 In allergic asthma, TLR9–IL-2 affects the Th2 response by regulating the expression of IL-17A, so small molecule inhibitors targeting TLR9 may become a new treatment strategy.372
Nervous diseases
The connection between innate immunity and nervous system is becoming more and more complex and close.373,374,375 Studies have shown that NOD1/NOD2 may be a new target for the treatment of stress-related gut–brain diseases.376 The gut–brain axis is a biochemical signal of the digestive tract and central nervous system, which affects all events from brain development to the progression of neurological diseases. The hypothalamic–pituitary–adrenal axis (HPA) is one of the main pathways of gut–brain axis signal transmission.377 It has been reported that the immune system plays a key role in brain function and stress response. NLRs are PRRs expressed in the gut and brain. The lack of NOD1 and NOD2 affects the serotonergic signaling of gut and brain, the proliferation of hippocampal cells, and the maturation of neurons, which makes the mice lacking both of them vulnerable to HPA overactivation under stimulation, thus showing anxiety, cognitive impairment, and depression.378,379,380 TLR4 is very important in the process of neuropathic pain caused by infection and sterile neuronal injury. TLR4 exerts its effects through the activation and nuclear localization of NF-κB and the production of pro-inflammatory cytokines, which can activate pain receptors to cause neuropathic pain.381,382 Relevant studies have revealed for the first time that lysozyme acts as an endogenous ligand for activating TLR4 in sterile nerve injury, thereby promoting neuronal excitement and neuropathic pain.383 The identification of lysozyme as DAMPs has improved our understanding of neuroinflammation and opened up prospects for the treatment of neuropathic pain.
Digestive diseases
Newborns with chronic obstructive jaundice make their livers prone to cholestatic liver disease, and biliary atresia (BA) accounts for half of the cases.384 Viruses have always been considered as the causative pathogen of this disease, and the role of TLRs in the pathogenesis and progression of BA has been determined.385 Subsequent studies have shown that activation of TLR7 can induce type 1 IFN signal transduction, apoptosis, and dysplasia of the neonatal liver and biliary system. This new discovery reveals the pathogenesis of neonatal cholestatic liver disease.386
The expression of TLR5 is closely related to various infectious diseases caused by bacteria.387,388 The lack of TLR5 can cause changes in the intestinal flora and cause colitis.389 The protein–protein interaction between TLR5 and flagellin plays an important role in pathogen defense, immune diseases, and tumors. 4-((4-benzyl-5-(pyridin4yl)-4H-1,2,4-triazol-3-yl)thio)pyrido[3’,2’:4,5]thieno[3,2-d] Pyrimidine (TH1020) is a small molecule inhibitor identified through high-throughput screening, which can disrupt the association between TLR5 and flagellin, and provides a lead compound for new therapies against TLR5.390,391
Alcoholic liver disease is a liver disease caused by long-term heavy drinking. The initial stage usually manifests as fatty liver, which can then develop into alcoholic hepatitis, liver fibrosis, and cirrhosis.392,393 Patients with advanced alcoholic cirrhosis are more susceptible to infection.394 This phenomenon is related to multiple organ failure and immunodeficiency and is usually manifested as insufficient antibacterial activity of neutrophils.395 The neutrophil function to resist microbial infections needs to generate reactive oxygen species through NADPH oxidase 2. Rolas et al. found that, in patients with alcoholic liver cirrhosis, the lack of catalytic core flavocytochrome b558 (gp91phox, p22phox) and p47phox of the NADPH enzyme may be a new factor that patients are susceptible to infection. What is surprising is that the activation of TLR7/8 can reverse the expression and activity of the deficient gp91phox, which provides a direction for restoring the antibacterial response of immunodeficiency patients.396,397
Cardiovascular diseases
Atherosclerosis is a chronic inflammatory disease caused by plaques composed of lipids, cholesterol, calcium, and other substances in blood vessels.398,399 It has been reported that TLRs are extensively and deeply involved in the process of atherosclerosis.400,401 TLR7 has been identified as a good prognosis marker for patients with severe atherosclerosis. TLR7 in the plaque produced in atherosclerotic lesions will secrete IL-10 and TNF-α after being stimulated by ligand. Studies have found that TLR7 may regulate inflammation in atherosclerosis by inhibiting the effects of pro-inflammatory cytokines.402 In addition to the production of plaque, cell-free DNA (cfDNA) is also released in atherosclerotic lesions. TLR9 recognizes cfDNA and plays a key role in the development of vascular inflammation and atherosclerosis by promoting the pro-inflammatory activation of macrophages.403 The formation of initial atherosclerotic plaques is caused by the interaction of macrophages and endothelial cells, macrophage infiltration, and other factors that lead to an increase in neointima.404,405 It is worth noting that studies have shown that TLR5-mediated activation of NADPH oxidase 4 (Nox4) can regulate the migration of SMCs and promote the expression of pro-inflammatory cytokines, which may contribute to the formation of atherosclerotic plaques. This indicates that the flagellin–TLR5–Nox4 cascade is of great significance in atherosclerotic intimal hyperplasia.406,407 In addition, TLR2 activates p38 and extracellular signal-regulated kinase 1/2 signals, thereby upregulating IL-6-mediated receptor activator of NF-κB ligand and downregulating osteoprotegerin. These will make the cartilage formation of vascular SMC transdifferentiate, leading to vascular calcification.408 The expression of TLR3 is reduced in the lung tissue and endothelial cells of patients with pulmonary hypertension, and its deficiency increases the susceptibility to apoptosis and pulmonary hypertension.409 In addition to TLRs, the lack of NOD1 and NOD2 can lead to lipid deposition of atherosclerotic plaques and the reduction of inflammatory cell infiltration, so it has been identified as pre-disease factors.410
Human brain pericytes (HBPs) are an important component of the microvascular wall and contribute to the integrity of the blood–brain barrier (BBB).411 It has been found that TLR4 and NOD1 are expressed in HBP, which also reveals that HBP has the ability to sense systemic infection or blood-borne PAMPs. HBP can perceive Gram-negative bacteria to protect BBB through different pathways mediated by TLR4 and NOD1, or it can trigger paracrine signaling pathways by releasing chemokines and cytokines, leading to the destruction of BBB.412,413 These are all new insights that PRRs are involved in the body’s inflammatory response and may have an impact on the treatment of diseases.
Endocrine diseases
In order to adapt to the constantly changing internal and external environment and maintain the relative stability of the internal environment, the human body must rely on the cooperation and regulation of the nervous, endocrine, and immune systems,414,415 so that the activities of various organs and systems are coordinated, and jointly shoulder all the life phenomena of the body. The immune system is not only regulated by the other two systems but also affects them through chemical information molecules and receptors.416,417
In patients with autoimmune thyroid disease, the expression and activation of TLR2, 3, and 9 are significantly increased.418,419 In addition, it has been reported that TLR9 negatively regulates pancreatic islet development and β cell differentiation, providing new directions for diabetes prevention and treatment strategies.420 In diet-induced obesity, TLR2 and TLR4 inhibit the replication of β cells and affect the nuclear abundance of the cell cycle regulators cyclin D2 and Cdk4. Therefore, targeting TLR2–TLR4 may alleviate the failure of β cells in diabetic patients.421
One of the most common complications of diabetes is diabetic foot ulcers, and the reason why it is not easy to get better is the inflammation of the wound.422,423 Singh et al. believe that changes in the expression level of intracellular TLRs may be one of the reasons for the continuous inflammation of chronic wounds, such as diabetic foot ulcers, and may hinder wound healing in patients with type 2 diabetes mellitus (T2DM).424 The basis of these pro-inflammatory effects is that intracellular TLRs activate dendritic cells and B cells to produce IFN I and III, aggravating the inflammatory response.425,426,427 The inflammatory phase of the wound healing cascade is the decisive stage of wound development, and studies have found that certain members of innate immunity play an important role in the pathogenesis of chronic wound healing abnormalities.428,429 The signaling pathway of intracellular TLRs is shown to be involved in some chronic inflammatory diseases, such as systemic lupus erythematosus (SLE), multiple sclerosis, hepatitis, and T2DM.430
Skeletal diseases
The expression level of NOD2 in human osteoarthritis (OA) cartilage is significantly higher than that of normal cartilage, and its combined action with TLR2 contributes to the pro-catabolic gene expression induced by 29-kDa amino terminal (matrix degradation product in synovial fluid of patients with OA) in human chondrocytes.431,432 This indicates that the NOD2 and TLR2 cross-regulatory pathway may be a target to prevent the development of arthritis. More and more evidences indicate that the interaction between different signal pathways may be a new way for the occurrence and development of diseases. The latest research combines three biological processes in skeletal muscle during exercise, innate immune response, autophagy protein homeostasis, and adenosine monophosphate-activated protein kinase (AMPK) activation, revealing that TLR9 can regulate the energy metabolism of skeletal muscle during exercise, and TLR9 regulates exercise-induced skeletal muscle AMPK activation by interacting with the core autophagy protein beclin1.433,434
호흡기 질환
Aspergillus fumigatus는 자연계에 널리 분포하는 곰팡이이다. 이는 호흡기로 쉽게 침입하여 환자에게 기관지염과 폐렴을 유발할 수 있다.368,369 아스페르길루스에 의한 알레르기성 폐염의 경우, 체내 수지상 세포에 의한 PAMP 인식은 주로 TLR2-MyD88 경로를 통해 음성 조절된다. 결과에 따르면 TLR2가 인식한 PAMPs는 IL-10 발현을 상향 조절하고 폐 호산구 유입을 감소시켜 Th2 반응을 하향 조절한다.370,371 알레르기성 천식에서 TLR9-IL-2는 IL-17A 발현 조절을 통해 Th2 반응에 영향을 미치므로, TLR9를 표적으로 하는 소분자 억제제가 새로운 치료 전략이 될 수 있다.372
신경계 질환
선천성 면역과 신경계의 연결은 점점 더 복잡하고 밀접해지고 있다.373,374,375 연구에 따르면 NOD1/NOD2는 스트레스 관련 장-뇌 질환 치료의 새로운 표적이 될 수 있다.376 장-뇌 축은 소화관과 중추신경계의 생화학적 신호로, 뇌 발달부터 신경계 질환 진행에 이르기까지 모든 과정에 영향을 미친다. 시상하부-뇌하수체-부신 축(HPA)은 장-뇌 축 신호 전달의 주요 경로 중 하나이다.377 면역 체계가 뇌 기능과 스트레스 반응에 핵심적인 역할을 한다는 보고가 있다. NLRs는 장과 뇌에서 발현되는 PRRs이다. NOD1과 NOD2의 결핍은 장과 뇌의 세로토닌 신호 전달, 해마 세포 증식, 신경 세포 성숙에 영향을 미치며, 이 두 가지가 모두 결핍된 마우스는 자극 하에서 HPA 과활성화에 취약해져 불안, 인지 장애, 우울증을 나타낸다.378,379,380 TLR4는 감염 및 무균성 신경 손상으로 인한 신경병성 통증 과정에서 매우 중요하다. TLR4는 NF-κB의 활성화 및 핵 국소화와 전염증성 사이토카인 생성을 통해 그 효과를 발휘하며, 이는 통증 수용체를 활성화하여 신경병성 통증을 유발할 수 있습니다.381,382 관련 연구를 통해 리소자임이 무균성 신경 손상에서 TLR4를 활성화하는 내인성 리간드 역할을 하여 이를 통해 신경 세포 흥분과 신경병성 통증을 촉진한다.383 리소자임을 DAMP로 규명한 것은 신경염증에 대한 이해를 높였으며 신경병성 통증 치료의 전망을 열었다.
소화기 질환
만성 폐쇄성 황달을 보이는 신생아는 간이 담즙 정체성 간 질환에 취약하며, 담도 폐쇄증(BA)이 그 절반을 차지한다.384 바이러스는 항상 이 질환의 원인 병원체로 여겨져 왔으며, 그리고 TLR이 담도폐쇄증의 병인 및 진행에 미치는 역할이 확인되었다.385 후속 연구에서 TLR7 활성화가 신생아 간 및 담도계의 제1형 인터페론 신호전달, 세포사멸 및 이형성증을 유발할 수 있음이 밝혀졌다. 이 새로운 발견은 신생아 담즙정체성 간질환의 병인을 규명한다.386
TLR5의 발현은 세균에 의한 다양한 감염성 질환과 밀접한 관련이 있다.387,388 TLR5의 결핍은 장내 미생물 군집 변화를 초래하여 대장염을 유발할 수 있다.389 TLR5와 플라젤린 간의 단백질-단백질 상호작용은 병원체 방어, 면역 질환 및 종양에서 중요한 역할을 한다. 4-((4-벤질-5-(피리딘-4-일)-4H-1,2,4-트리아졸-3-일)티오)피리도[3',2':4,5]티에노[3,2-d] 피리미딘(TH1020)은 고효율 스크리닝을 통해 확인된 소분자 억제제로, TLR5와 플래겔린 간의 결합을 방해하여 TLR5를 표적으로 하는 새로운 치료법의 선도 화합물을 제공한다.390,391
알코올성 간질환은 장기간의 과음으로 인해 발생하는 간 질환이다. 초기 단계에서는 일반적으로 지방간으로 나타나며, 이후 알코올성 간염, 간 섬유증, 간경변으로 진행될 수 있다.392,393 진행성 알코올성 간경변 환자는 감염에 더 취약하다.394 이 현상은 다기관 기능 부전 및 면역 결핍과 관련이 있으며, 일반적으로 호중구의 항균 활성 부족으로 나타난다.395 미생물 감염에 저항하는 호중구 기능은 NADPH 산화효소 2를 통해 활성산소를 생성해야 한다. Rolas 등은 알코올성 간경변 환자에서 NADPH 효소의 촉매 핵심 플라보시토크롬 b558(gp91phox, p22phox) 및 p47phox 결핍이 환자의 감염 취약성에 대한 새로운 요인일 수 있음을 발견했다. 놀라운 점은 TLR7/8의 활성화가 결핍된 gp91phox의 발현과 활성을 역전시킬 수 있다는 것으로, 이는 면역결핍 환자의 항균 반응을 회복시키는 방향을 제시한다.396,397
심혈관 질환
동맥경화는 혈관 내 지질, 콜레스테롤, 칼슘 등 물질로 구성된 플라크에 의해 유발되는 만성 염증성 질환이다.398,399 TLR이 동맥경화 과정에 광범위하고 깊게 관여한다는 보고가 있다.400,401 TLR7은 중증 동맥경화 환자의 예후 지표로 확인되었다. 동맥경화 병변에서 생성된 플라크 내 TLR7은 리간드 자극 후 IL-10과 TNF-α를 분비한다. 연구에 따르면 TLR7은 전염증성 사이토카인의 효과를 억제함으로써 동맥경화에서의 염증을 조절할 수 있다.402 플라크 생성 외에도, 동맥경화 병변에서는 세포외 DNA(cfDNA)도 방출된다. TLR9는 cfDNA를 인식하며 대식세포의 친염증 활성화를 촉진함으로써 혈관 염증 및 동맥경화증 발병에 핵심적인 역할을 합니다.403 초기 동맥경화성 플라크 형성은 대식세포와 내피세포의 상호작용, 대식세포 침윤 및 기타 요인에 의해 유발되며, 이는 신내막의 증가로 이어진다.404,405 주목할 점은 연구에 따르면 TLR5 매개 NADPH 산화효소 4(Nox4)의 활성화가 평활근세포(SMCs)의 이동을 조절하고 염증성 사이토카인의 발현을 촉진하여 동맥경화성 플라크 형성에 기여할 수 있다는 것이다. 이는 플라젤린-TLR5-Nox4 연쇄 반응이 죽상경화성 내막 증식에 매우 중요함을 시사한다.406,407 또한, TLR2는 p38 및 세포외 신호 조절 키나아제 1/2 신호를 활성화하여 IL-6 매개 NF-κB 리간드 수용체 활성화 인자를 상향 조절하고 오스테오프로테제린을 하향 조절한다. 이러한 작용은 혈관 평활근세포(SMC)의 연골 형성 전분화를 유발하여 혈관 석회화로 이어집니다.408 폐고혈압 환자의 폐 조직 및 내피세포에서 TLR3 발현이 감소하며, 그 결핍은 세포사멸 및 폐고혈압에 대한 감수성을 증가시킵니다.409 TLR 외에도, NOD1 및 NOD2 결핍은 죽상경화성 플라크의 지질 침착과 염증 세포 침윤 감소를 유발할 수 있어, 이는 전병인성 인자로 확인되었다.410
인간 뇌 주위 세포(HBP)는 미세혈관벽의 중요한 구성 요소이며 혈액-뇌 장벽(BBB)의 완전성에 기여한다.411 HBP에서 TLR4와 NOD1이 발현되는 것으로 밝혀졌으며, 이는 HBP가 전신 감염 또는 혈액을 통한 PAMP를 감지할 수 있는 능력을 가지고 있음을 보여준다. HBP는 그람 음성균을 인지하여 TLR4 및 NOD1이 매개하는 다양한 경로를 통해 BBB를 보호하거나, 케모카인과 사이토카인을 방출하여 파라크라인 신호 전달 경로를 유발하여 BBB를 파괴할 수 있습니다.412,413 이는 PRR이 신체의 염증 반응에 관여하며 질병 치료에 영향을 미칠 수 있다는 새로운 통찰력입니다.
내분비 질환
끊임없이 변화하는 내외부 환경에 적응하고 내부 환경의 상대적 안정성을 유지하기 위해 인체는 신경계, 내분비계, 면역계의 협력과 조절에 의존해야 합니다.414,415 이를 통해 다양한 기관과 시스템의 활동이 조화를 이루고, 신체의 모든 생명 현상을 공동으로 담당합니다. 면역계는 다른 두 계통에 의해 조절될 뿐만 아니라 화학 정보 분자와 수용체를 통해 이들에 영향을 미칩니다.416,417
자가면역 갑상선 질환 환자에서는 TLR2, 3, 및 9의 발현과 활성화가 현저히 증가한다.418,419 또한 TLR9이 췌장 섬 발달과 β 세포 분화를 부정적으로 조절하여 당뇨병 예방 및 치료 전략에 새로운 방향을 제시한다는 보고가 있다.420 식이 유발 비만에서는 TLR2와 TLR4가 β 세포 복제를 억제하고 세포 주기 조절인자인 사이클린 D2와 Cdk4의 핵 내 풍부도에 영향을 미친다. 따라서 TLR2–TLR4 표적화는 당뇨병 환자의 β 세포 기능 부전을 완화시킬 수 있다.421
당뇨병의 가장 흔한 합병증 중 하나는 당뇨병성 족부 궤양이며, 이 궤양이 쉽게 낫지 않는 이유는 상처의 염증 때문입니다.422,423 Singh 등은 세포 내 TLR 발현 수준의 변화가 당뇨병성 족부 궤양과 같은 만성 상처의 지속적인 염증 원인 중 하나일 수 있으며, 제2형 당뇨병(T2DM) 환자의 상처 치유를 방해할 수 있다고 생각합니다. (T2DM).424 이러한 염증 촉진 효과의 근거는 세포 내 TLR이 수지상 세포와 B 세포를 활성화하여 IFN I 및 III를 생성함으로써 염증 반응을 악화시키기 때문이다.425,426,427 상처 치유 과정의 염증 단계는 상처 발달의 결정적 단계이며, 선천성 면역의 특정 구성원들이 만성 상처 치유 이상 병리에서 중요한 역할을 한다는 연구 결과가 있다. 428,429 세포 내 TLR의 신호 전달 경로는 전신성 홍반성 루푸스(SLE), 다발성 경화증, 간염 및 T2DM과 같은 일부 만성 염증성 질환에 관여하는 것으로 나타났습니다.430
골격계 질환
인간 골관절염(OA) 연골에서 NOD2의 발현 수준은 정상 연골보다 현저히 높으며, TLR2와의 복합 작용은 인간 연골 세포에서 29-kDa 아미노 말단(OA 환자의 활액 내 매트릭스 분해 산물)에 의해 유도된 분해 촉진 유전자 발현에 기여한다. 431,432 이는 NOD2와 TLR2의 교차 조절 경로가 관절염 발병을 예방하는 표적이 될 수 있음을 시사한다. 서로 다른 신호 경로 간의 상호작용이 질병의 발생 및 진행에 대한 새로운 메커니즘일 수 있다는 증거가 점점 더 많아지고 있다. 최신 연구는 운동 중 골격근에서 발생하는 세 가지 생물학적 과정(선천성 면역 반응, 자가포식 단백질 항상성, 아데노신 모노포스페이트 활성화 단백질 키나아제(AMPK) 활성화)을 결합하여, TLR9가 운동 중 골격근의 에너지 대사를 조절할 수 있으며, TLR9가 핵심 자가포식 단백질 베클린1(beclin1)과 상호작용함으로써 운동 유발 골격근 AMPK 활성화를 조절함을 밝혀냈다.433,434
Clinical therapy of PRRs
Based on the important role that PRRs play in innate immunity, they have received extensive attention in the fields of immunology and drug research.310,435 There are many types of PRRs and a wide range of ligands. They can be used as drug targets for tumor, inflammation, autoimmune disease, pathogenic microbial infection, and other diseases, which are important entry points for immunotherapy.314 The activation of PRRs brings double-sided effects: on the one hand, it stimulates innate immunity and adaptive immunity to resist pathogenic microorganisms; on the other hand, it promotes the expression of a large number of cytokines, forms an inflammatory microenvironment, and causes tissue damage.29,436 Therefore, the treatment strategy targeting PRRs is mainly to use ligand analogs to activate PRRs,435 use antagonists to inhibit their activation, or use antibodies and small molecules to inhibit PRR signaling pathways.437 It is reported that most of the agonists and antagonists of TLRs are only in the clinical development stage, which are studied comprehensively in PRRs (Table 2). In addition, microRNA (miRNA), exosomes, and combination therapy also have certain potential in this field.438,439
PRR의 임상 치료
선천성 면역에서 PRR이 수행하는 중요한 역할을 바탕으로, PRR은 면역학 및 약물 연구 분야에서 광범위한 관심을 받아 왔습니다.310,435 PRR에는 여러 유형이 있으며 리간드의 범위가 넓습니다. 이들은 종양, 염증, 자가면역질환, 병원성 미생물 감염 등 다양한 질환의 치료 표적으로 활용될 수 있으며, 이는 면역치료의 중요한 진입점이다.314 PRR의 활성화는 양면적인 효과를 가져온다: 한편으로는 선천성 면역과 적응성 면역을 자극하여 병원성 미생물에 저항하게 하며, 다른 한편으로는 다량의 사이토카인 발현을 촉진하여 염증성 미세환경을 형성하고 조직 손상을 유발한다. 29,436 따라서 PRR을 표적으로 하는 치료 전략은 주로 리간드 유사체를 사용하여 PRR을 활성화하거나,435 길항제를 사용하여 그 활성화를 억제하거나, 항체 및 소분자를 사용하여 PRR 신호 전달 경로를 억제하는 것입니다.437 TLR의 대부분의 작용제 및 길항제는 임상 개발 단계에 불과한 것으로 보고되며, PRR에서 종합적으로 연구되고 있습니다(표 2). 또한, 마이크로RNA(miRNA), 엑소좀 및 병용 요법도 이 분야에서 일정한 잠재력을 가지고 있다.438,439
Table 2 Clinical trials investigating the use of TLR agonists and antagonists in diseases
PRR agonists for therapy
Imiquimod is the first targeted drug for TLRs. It is a specific agonist of the TLR7 receptor. It can induce the production of IFN-α, IL-6, and TNF-α to achieve the purpose of regulating immunity and treating tumors.440 Selgantolimod, a novel TLR8 agonist, can activate TLR8 and elicit cytokine responses in patients with chronic hepatitis B infection.441,442 Further studies with longer durations of selgantolimod treatment are required to evaluate efficacy. The ligand of TLR9 is unmethylated DNA, and CpG oligodinucleotide (CpG ODN) that mimics this structure has good antitumor potential (e.g., IMO-2055, MGN-1703, MGN-1704).443 The research of MGN-1703 on the treatment of advanced CRC is in phase III. MGN-1703 can induce a potent type I IFN response in the intestine, which is related to the subtle changes of intestinal flora.444 Clinically, PRR agonists can be potentially used not only as therapeutic agents to treat but also as adjuvants in conjunction with other immunotherapies.445,446 Due to the instability and drug resistance of existing drugs, some adjuvants targeting PRRs emerge as the times require. A TLR3-specific adjuvant, ARNAX, can enhance DC priming and CTL proliferation without cytokine toxicity.447 And the conjugated STING and TLR1/2 agonist Pam3CSK4-CDGSF can be used as an effective adjuvant for constructing vaccines to enhance antitumor immunotherapy.448 NLR agonists can promote the processing and secretion of IL-1β, which is very important for activating many immune cells.449,450 Therefore, NLR agonists can be served as effective components of vaccines and immune stimulants.
The class II major histocompatibility complex transactivator (CIITA) is a single member of the NLRA subfamily.451 As the main regulator of major histocompatibility complex II, its own modification is very important in the occurrence and development of tumors. Both the deacetylation of histones and the demethylation of DNA will downregulate the transcription of CIITA.452 Decitabine (5-aza-2’-deoxycytidine), Entinostat (MS-275), and Trichostatin A target CIITA to promote its expression recovery in tumors. In addition, andrographolide, arglabin, formononetin, mangiferin, and other botanicals can be used to treat tumors by inhibiting NLRP3 inflammasome.453,454,455,456,457 Representative NLR agonists like Mifamurtide have been approved for clinical trials of non-metastatic sarcoma.
RLRs are involved in the recognition of viral infection by the innate immune system, and their agonists include poly I:C.99 Studies have revealed the link between energy metabolism and innate immunity, indicating that lactate may act as a natural inhibitor of RLR signal transduction by targeting the adaptor protein MAVS.458 The latest research shows that activating RIG-I before diffusing alpha-emitting radiation therapy for metastatic and low immunogenic tumors is a more effective combination therapy technique that can inhibit tumor growth and metastasis.459
PRR antagonists for therapy
PRR antagonists belong to immunosuppressants, which are mainly used to inhibit the function of receptors and block the connection between receptors and ligands.460 They can be used to treat diseases with abnormal activation of the immune system. The abnormal activation of TLR7, 8, and 9 contributes to the onset and maintenance of inflammatory diseases.461,462 The inhibitors IMO-3100 and IMO-8400 targeting them can significantly reduce the expression of IL-17A induced by IL-23, which has a potential role in the inflammatory cascade.463,464 In addition, inhibition of TLR7 and TLR9 with IRS-954 or chloroquine may be a new treatment for HCC.465 In addition to the immune inhibitory oligonucleotides that can be used as TLR inhibitors, CPG-52364, a derivative of the small molecular weight chemical compound quinazoline, can also block ligand-induced activation of TLR7, 8, and 9.462 FP7 is a synthetic glycolipid, which can be used as TLR4 inhibitor to treat septic shock.466 Studies have found that inhibitory ODN-containing phosphorothioate modifications of the backbone have potential therapeutic effects for SLE and rheumatoid arthritis. ODN1411 directly binds to the extracellular domain of TLR8 and competitively inhibits its signal transduction.467
In the NLR family, the NLRP3 inflammasome is closely related to the pathophysiology of a variety of inflammatory diseases, so it is usually used as an inhibitor target.298,304,305 MCC950 is a specific NLRP3 antagonist, which can prevent its activation or maintain its activation state.468 β-Carotene has been shown to directly bind to the PYD of NLRP3, thereby blocking the association between NLRP3 and its adaptor protein and ultimately inhibiting the activation of NLRP3 inflammasomes.469 This result further complements the new pharmacological strategy to prevent NLRP3 inflammasome-driven gouty arthritis. The development of small molecule inhibitors for NLRP3 has been in full swing.470,471 Dai et al. reported a series of tetrahydroquinoline inhibitors. In further studies in vitro, it was found that compound 6 directly binds to the NACHT domain of NLRP3 but not to the PYD or LRR domains, which inhibits the assembly and activation of NLRP3 inflammasomes. In vivo, compound 6 can significantly inhibit the expression of IL-1β and alleviate the symptoms of colitis.472 Agarwal et al. identified alkenyl sulfonylurea derivatives as a novel, oral, and biologically effective NLRP3 inhibitor. Compound 7 of alkenyl sulfonylurea derivatives has good pharmacokinetic characteristics and high oral bioavailability.473
Other potential therapies via PRRs
Emerging evidence suggests that the interaction between miRNA and PRR pathway and immunoregulation are intimately interwoven.438 The interaction between the two is particularly significant in the pathogenesis of rheumatoid arthritis (RA).474,475 RA is a common autoimmune disease, which is characterized by synovial hyperplasia and irreversible bone destruction caused by chronic synovitis. Rheumatoid arthritis synovial fibroblast (RASF) plays a central role in this process.476,477,478 The expression of miR-146a and miR-155 is upregulated in RASF. miR-146a inhibits the expression of TRAF-6 and IRAK-1 in the TLR signaling pathway, thereby inhibiting the production of key adaptor molecules downstream of TLRs in RA.479 And miR-155 negatively regulates the activation of TLRs/IL-1R inflammatory pathway. Both of them will eventually reduce RA inflammation.480 In addition, miR19a/b, miR-20a, and miR-10a are downregulated in RASF. Downregulated miR19a/b directly targets TLR2 to increase its expression481; miR-20a inhibits the expression of ASK1, a key component of the TLR4 pathway482; miR-10a targets IRAK4 and TAK1 to accelerate IκB degradation and NF-κB activation.483 These effects promote the inflammatory response of RA. All these evidences indicate that miRNAs can surpass their conventional functions and act as physiological ligands for TLRs, thereby regulating the expression of cytokines in the inflammatory response. miRNA can also target other PRRs. miR-485 can target RIG-I mRNA for degradation, leading to enhancement of virus replication and inhibition of antiviral response.484 miRNA-155 can aggravate the brain tissue inflammation in neonatal rats with hypoxia and ischemia by regulating the NOD1/NF-κB signaling pathway, thereby causing hypoxia and ischemic brain damage in neonatal rats.485,486
In addition, exosomes are also involved in the complex immune regulatory network of miRNA and PRRs.487 Exosomes are small membrane vesicles containing complex RNA and protein. A variety of cells can secrete exosomes under normal and pathological conditions.488,489 There is evidence that exosomes can regulate innate immunity by combining with TLRs, which provides a new method for the body to resist pathogens and treat diseases.487 Brain exosomes are rich in amyloid-beta (Aβ), the main component of neuritic plaques, which can activate TLR2, TLR4, and TLR9 signaling, thus alleviating the early symptoms of Alzheimer’s disease.490 It was found that the expression of miR-216a-5p in the plasma of patients with syphilis is negatively correlated with the expression of inflammatory cytokines. Exosomes containing miR-216a-5p inhibit the inflammatory response induced by recombinant Tp17 by targeting the TLR4–MyD88 pathway.491 Melphalan, a genotoxic agent, can enhance the ability of multiple myeloma (MM) cells to release exosomes in MM. Hsp70 on the surface of MM-derived exosomes activates TLR2 in NK cells, thereby inducing the production of INFγ.492 This enlightens us that exosomes with significant exposure to DAMPs can link chemotherapy with antitumor innate immune response.
However, whether they are therapeutic agents, adjuvants, or others, it still needs a long time to further improve the research in vitro and in vivo before clinical application in tumor treatment.493
Conclusions and future perspectives
The innate immune system has multiple recognition mechanisms in different cell types with different subcellular structures. Recently, great progress has been made in the study of the interaction between PRRs and ligands. A preliminary understanding of the crystal structure of some PRRs and the commonalities and differences in the structural composition of different types of PRRs has been made. We understand the existing forms of PRRs alone in solution and after binding to ligands, as well as the molecules involved in the process of PRR identification and ligand binding. As the initiation step of the innate immune response and antiviral response, PRR recognition and binding of ligands is critical. PRRs recognize targets through their respective ligand-recognition domains: LRRs, CTDs, CTLDs, and a variety of DNA- or RNA-binding domains. Ligand binding induces activation and transmission of the signal, which is transmitted through cascade amplification by their respective domains—TIR domain, protein interaction domain, CARD, ITAM, and PYD. In some cases, one kind of PRRs can recognize multiple PAMPs, and one kind of PAMPs can also be recognized by different PRRs, which can induce an inflammatory response and adaptive immune response in a synergistic manner.494
PRRs that are difficult to find and identify and complex ligand-recognition mechanisms have hindered the study of the role of the innate immune system in related diseases and even tumors. In previous studies, computational modeling and mutational analysis of human TLR10 showed that the structure of TLR10 was modeled with the explicit inclusion of TLR2 and lipopeptide structures.495 Recently, RRGPredictor, a tool mainly based on text mining and set theory to predict new plant PRRs, makes the identification of PRRs more effective, specific, and sensitive than other available tools.496 And a random forest-based method was proposed to identify PRRs, which is superior to other machine learning methods for PRRs. This method constructs a benchmark database, uses the amino acid composition and the composition transition distribution to formulate the sequences in the dataset, and then uses the maximum relevance maximum distance to select the best features. However, due to the small amount of data and the low sensitivity of the method, the identification results for PRRs are still unsatisfactory.497 Therefore, the ability to develop a vertebrate PRR predictor based on protein domain similarity and homology modeling is becoming an important part of this story. In addition, the future studies on the how membrane PRRs are secreted into body fluids and act as soluble PRRs will undoubtedly further our understandings of their roles in antimicrobial immune defense and autoimmune and autoinflammatory disorders. Therefore, the study of PRR-mediated pattern recognition mechanisms will help to elucidate the signaling pathways and mechanisms of disease, provide new targets and methods for the treatment of diseases, and promote the development of immunology and oncology research and improvements in their theoretical systems.
치료용 PRR 작용제
이미퀴모드는 TLR을 표적으로 하는 최초의 약물이다. 이는 TLR7 수용체의 특이적 작용제이다. 이 약물은 IFN-α, IL-6 및 TNF-α의 생성을 유도하여 면역 조절 및 종양 치료 목적을 달성할 수 있습니다.440 새로운 TLR8 작용제인 셀간톨리모드(selgantolimod)는 만성 B형 간염 감염 환자에서 TLR8을 활성화하고 사이토카인 반응을 유발할 수 있습니다.441,442 효능 평가를 위해서는 셀간톨리모드 치료 기간을 연장한 추가 연구가 필요합니다. TLR9의 리간드는 비메틸화 DNA이며, 이 구조를 모방한 CpG 올리고디뉴클레오티드(CpG ODN)는 우수한 항종양 잠재력을 지닙니다(예: IMO-2055, MGN-1703, MGN-1704).443 MGN-1703의 진행성 대장직장암 치료 연구는 3상 단계에 있습니다. MGN-1703은 장내 미생물 군집의 미묘한 변화와 관련된 장에서 강력한 제1형 인터페론 반응을 유도할 수 있다.444 임상적으로, PRR 작용제는 치료제로서뿐만 아니라 다른 면역요법과 병용하는 보조제로서도 잠재적으로 활용될 수 있다.445,446 기존 약물의 불안정성과 내성 문제로 인해, 시대적 요구에 부응하는 PRR 표적 보조제가 등장하고 있다. TLR3 특이적 보조제인 ARNAX는 사이토카인 독성 없이 DC 프라이밍과 CTL 증식을 향상시킬 수 있다.447 또한 STING 및 TLR1/2 작용제인 Pam3CSK4와 결합된 -CDGSF는 항종양 면역치료를 강화하는 백신 구축을 위한 효과적인 보조제 역할을 할 수 있다.448 NLR 작용제는 많은 면역세포 활성화에 매우 중요한 IL-1β의 처리 및 분비를 촉진할 수 있다.449,450 따라서 NLR 작용제는 백신 및 면역 자극제의 효과적인 구성 요소로 활용될 수 있다.
II형 주요 조직적합성 복합체 전사활성제(CIITA)는 NLRA 아가족의 유일한 구성원이다.451 주요 조직적합성 복합체 II의 주요 조절자로서, 그 자체의 변형은 종양의 발생과 진행에 매우 중요하다. 히스톤의 탈아세틸화와 DNA의 탈메틸화는 모두 CIITA의 전사를 하향 조절합니다.452 데시타빈(5-aza-2'-deoxycytidine), 엔티노스타트(MS-275), 트리코스타틴 A는 CIITA를 표적으로 하여 종양에서 그 발현 회복을 촉진합니다. 또한, 안드로그라폴리드, 아글라빈, 포르모노네틴, 망기페린 및 기타 식물성 물질은 NLRP3 인플람소좀을 억제하여 종양 치료에 사용될 수 있습니다.453,454,455,456,457 미파무르타이드와 같은 대표적인 NLR 작용제는 비전이성 육종에 대한 임상 시험 승인을 받았습니다.
RLR은 선천성 면역 체계에 의한 바이러스 감염 인식에 관여하며, 그 작용제에는 폴리 I: C.99 연구에 따르면 에너지 대사와 선천성 면역 간의 연관성이 밝혀졌으며, 젖산이 어댑터 단백질 MAVS를 표적으로 하여 RLR 신호 전달의 자연적 억제제로 작용할 수 있음을 시사합니다.458 최신 연구에 따르면 전이성 및 낮은 면역원성 종양에 대해 알파선 방사선 치료를 시행하기 전에 RIG-I를 활성화하는 것이 종양 성장과 전이를 억제할 수 있는 보다 효과적인 병용 치료 기법입니다.459
치료용 PRR 길항제
PRR 길항제는 면역억제제에 속하며, 주로 수용체 기능을 억제하고 수용체와 리간드 간의 연결을 차단하는 데 사용됩니다.460 이는 면역 체계의 비정상적 활성화로 인한 질환 치료에 활용될 수 있습니다. TLR7, 8, 9의 비정상적 활성화는 염증성 질환의 발병 및 유지에 기여한다.461,462 이를 표적으로 하는 억제제 IMO-3100 및 IMO-8400은 염증성 연쇄 반응에서 잠재적 역할을 하는 IL-23에 의해 유도된 IL-17A의 발현을 현저히 감소시킬 수 있다. 463,464 또한 IRS-954 또는 클로로퀸을 통한 TLR7 및 TLR9 억제는 간세포암(HCC)의 새로운 치료법이 될 수 있습니다.465 TLR 억제제로 사용 가능한 면역 억제 올리고뉴클레오티드 외에도, 저분자량 화합물 퀴나졸린 유도체인 CPG-52364 역시 리간드에 의한 TLR7, 8, 9의 리간드 유도 활성화를 차단할 수 있다.462 FP7은 합성 당지질로, 패혈성 쇼크 치료를 위한 TLR4 억제제로 사용될 수 있다.466 연구에 따르면, 억제성 ODN의 백본에 포스포로티오에이트 변형을 도입하면 SLE 및 류마티스 관절염에 대한 잠재적 치료 효과가 있는 것으로 나타났다. ODN1411은 TLR8의 세포외 도메인에 직접 결합하여 신호 전달을 경쟁적으로 억제한다.467
NLR 가족에서 NLRP3 인플라마좀은 다양한 염증성 질환의 병리생리학과 밀접한 관련이 있으므로 일반적으로 억제제 표적으로 사용됩니다.298,304,305 MCC950은 특정 NLRP3 길항제로, 그 활성화를 방지하거나 활성화 상태를 유지할 수 있습니다.468 β-카로틴은 NLRP3의 PYD에 직접 결합하여 이를 통해 NLRP3와 그 어댑터 단백질 간의 결합을 차단하고 궁극적으로 NLRP3 인플라마좀의 활성화를 억제한다.469 이 결과는 NLRP3 인플라마좀에 의해 유발되는 통풍성 관절염을 예방하기 위한 새로운 약리학적 전략을 더욱 보완한다. NLRP3를 표적으로 하는 소분자 억제제의 개발은 활발히 진행 중이다.470,471 Dai 등은 일련의 테트라하이드로퀴놀린 억제제를 보고했다. 추가적인 시험관 내 연구에서, 화합물 6은 PYD 또는 LRR 도메인이 아닌 NLRP3의 NACHT 도메인에 직접 결합하여 NLRP3 인플람소좀의 조립 및 활성화를 억제하는 것으로 밝혀졌습니다. 생체 내에서는 화합물 6이 IL-1β 발현을 현저히 억제하고 대장염 증상을 완화시킬 수 있다.472 Agarwal 등은 알켄일 설포닐우레아 유도체를 새로운 경구용 생물학적 활성 NLRP3 억제제로 확인하였다. 알켄일 설포닐우레아 유도체인 화합물 7은 우수한 약동학적 특성과 높은 경구 생체이용률을 보인다.473
PRR을 통한 기타 잠재적 치료법
새로운 증거에 따르면 miRNA와 PRR 경로 간의 상호작용 및 면역 조절은 밀접하게 연관되어 있다.438 이 둘의 상호작용은 특히 류마티스 관절염(RA)의 병인에서 중요하다.474,475 RA는 만성 활막염으로 인한 활막 증식과 비가역적 골 파괴가 특징인 흔한 자가면역 질환이다. 류마티스 관절염 활막 섬유아세포(RASF)는 이 과정에서 핵심적인 역할을 합니다.476,477,478 RASF에서는 miR-146a 및 miR-155의 발현이 상향 조절됩니다. miR-146a는 TLR 신호 전달 경로에서 TRAF-6 및 IRAK-1의 발현을 억제하여 RA에서 TLR의 하류에 있는 주요 어댑터 분자의 생성을 억제합니다.479 그리고 miR-155는 TLR/IL-1R 염증 경로의 활성화를 부정적으로 조절합니다. 이 둘 모두 궁극적으로 RA 염증을 감소시킵니다.480 또한, miR-19a/b, miR-20a 및 miR-10a는 RASF에서 하향 조절됩니다. 하향 조절된 miR-19a/b는 TLR2를 직접 표적하여 그 발현을 증가시킵니다.481; miR-20a는 TLR4 경로의 핵심 구성 요소인 ASK1의 발현을 억제한다482; miR-10a는 IRAK4와 TAK1을 표적하여 IκB 분해를 가속화하고 NF-κB 활성화를 촉진한다.483 이러한 효과들은 RA의 염증 반응을 촉진한다. 이 모든 증거들은 miRNA가 기존의 기능을 넘어 TLR의 생리적 리간드 역할을 하여 염증 반응에서 사이토카인 발현을 조절할 수 있음을 시사한다. miRNA는 다른 PRR도 표적할 수 있다. miR-485는 RIG-I mRNA를 표적하여 분해시킴으로써 바이러스 복제를 증강시키고 항바이러스 반응을 억제한다.484 miRNA-155는 NOD1/NF-κB 신호전달 경로를 조절함으로써 신생아 쥐의 저산소증 및 허혈성 뇌조직 염증을 악화시켜 신생아 쥐의 저산소증 및 허혈성 뇌손상을 유발한다.485,486
또한 엑소좀은 miRNA와 PRR의 복잡한 면역 조절 네트워크에도 관여합니다.487 엑소좀은 복잡한 RNA와 단백질을 포함하는 작은 막 소포입니다. 정상 및 병리학적 조건에서 다양한 세포가 엑소좀을 분비할 수 있다.488,489 엑소좀이 TLR과 결합하여 선천성 면역을 조절할 수 있다는 증거가 있으며, 이는 신체가 병원체에 저항하고 질병을 치료하는 새로운 방법을 제공한다.487 뇌 엑소좀은 신경원성 플라크의 주요 구성 성분인 아밀로이드 베타(Aβ)가 풍부하며, 이는 TLR2, TLR4 및 및 TLR9 신호전달을 활성화하여 알츠하이머병 초기 증상을 완화시킵니다.490 매독 환자의 혈장 내 miR-216a-5p 발현은 염증성 사이토카인 발현과 음의 상관관계가 있는 것으로 확인되었습니다. miR-216a-5p를 함유한 엑소좀은 TLR4-MyD88 경로를 표적으로 하여 재조합 Tp17에 의해 유발된 염증 반응을 억제한다.491 유전독성 물질인 멜팔란은 다발성 골수종(MM) 세포가 MM에서 엑소좀을 방출하는 능력을 향상시킬 수 있다. 다발성 골수종 유래 엑소좀 표면의 Hsp70은 NK 세포에서 TLR2를 활성화하여 INFγ 생성을 유도한다.492 이는 DAMPs에 상당한 노출을 보이는 엑소좀이 항암 화학요법과 항종양 선천성 면역 반응을 연결할 수 있음을 시사한다.
그러나 치료제, 보조제 또는 기타 용도 여부와 관계없이 종양 치료에 임상 적용하기 전 체외 및 생체 내 연구를 더욱 개선하기 위해서는 여전히 오랜 시간이 필요하다.493
결론 및 향후 전망
선천성 면역 체계는 다양한 세포 유형과 세포 내 구조에 따라 다중 인식 기전을 가진다. 최근 PRR과 리간드 간 상호작용 연구에서 큰 진전이 이루어졌다. 일부 PRR의 결정 구조와 다양한 유형의 PRR 구조 구성 요소 간 공통점 및 차이점에 대한 기초적 이해가 이루어졌다. 용액 내 단독 상태 및 리간드 결합 후 PRR의 존재 형태와 PRR 식별 및 리간드 결합 과정에 관여하는 분자들을 이해하게 되었다. 선천성 면역 반응과 항바이러스 반응의 개시 단계로서 PRR의 리간드 인식 및 결합은 매우 중요하다. PRR은 각각의 리간드 인식 도메인(LRR, CTD, CTLD 및 다양한 DNA/RNA 결합 도메인)을 통해 표적을 인식한다. 리간드 결합은 신호 활성화 및 전달을 유도하며, 이는 TIR 도메인, 단백질 상호작용 도메인, CARD, ITAM, PYD 등 각 도메인을 통한 연쇄적 증폭으로 전달된다. 경우에 따라 한 종류의 PRR이 여러 PAMP를 인식할 수 있으며, 한 종류의 PAMP도 서로 다른 PRR에 의해 인식될 수 있어 시너지 효과를 통해 염증 반응과 적응 면역 반응을 유도할 수 있다.494
발견 및 동정이 어려운 PRR과 복잡한 리간드 인식 메커니즘은 선천성 면역 체계가 관련 질환 및 종양에서 수행하는 역할 연구를 방해해 왔습니다. 기존 연구에서 인간 TLR10의 컴퓨터 모델링 및 돌연변이 분석을 통해 TLR10 구조는 TLR2 및 지질펩타이드 구조를 명시적으로 포함하여 모델링되었습니다.495 최근, 텍스트 마이닝과 집합론을 기반으로 새로운 식물 PRR을 예측하는 도구인 RRGPredictor는 기존 도구들보다 PRR 식별을 더 효과적이고 특이적이며 민감하게 만듭니다.496 또한 PRR 식별을 위한 랜덤 포레스트 기반 방법이 제안되었으며, 이는 PRR에 대한 다른 기계 학습 방법들보다 우수합니다. 이 방법은 벤치마크 데이터베이스를 구축하고, 아미노산 구성과 구성 전환 분포를 사용하여 데이터 세트의 서열을 공식화한 다음, 최대 관련성 최대 거리를 사용하여 최상의 특징을 선택합니다. 그러나 데이터의 양이 적고 방법의 민감도가 낮기 때문에 PRR에 대한 식별 결과는 여전히 만족스럽지 못합니다.497 따라서 단백질 도메인 유사성과 상동 모델링을 기반으로 척추동물 PRR 예측기를 개발하는 능력이 이 이야기의 중요한 부분이 되고 있습니다. 또한, 막 PRR이 체액으로 분비되어 가용성 PRR로 작용하는 방식에 대한 향후 연구는 항균 면역 방어 및 자가면역 및 자가염증성 장애에서 PRR의 역할에 대한 이해를 더욱 심화시킬 것입니다. 따라서 PRR 매개 패턴 인식 메커니즘 연구는 신호 전달 경로와 질병 기전을 규명하고, 질병 치료를 위한 새로운 표적과 방법을 제공하며, 면역학 및 종양학 연구의 발전과 이론 체계 개선을 촉진하는 데 기여할 것이다.
References