Cell Rep Med
. 2022 Jul 19;3(7):100696. doi: 10.1016/j.xcrm.2022.100696
Manipulation of the inflammatory reflex as a therapeutic strategy
Mark J Kelly 1,2, Caitríona Breathnach 2, Kevin J Tracey 3, Seamas C Donnelly 1,2,∗
- Author information
- Article notes
- Copyright and License information
PMCID: PMC9381415 PMID: 35858588
Summary
The cholinergic anti-inflammatory pathway is the efferent arm of the inflammatory reflex, a neural circuit through which the CNS can modulate peripheral immune responses. Signals communicated via the vagus and splenic nerves use acetylcholine, produced by Choline acetyltransferase (ChAT)+ T cells, to downregulate the inflammatory actions of macrophages expressing α7 nicotinic receptors. Pre-clinical studies using transgenic animals, cholinergic agonists, vagotomy, and vagus nerve stimulation have demonstrated this pathway’s role and therapeutic potential in numerous inflammatory diseases. In this review, we summarize what is understood about the inflammatory reflex. We also demonstrate how pre-clinical findings are being translated into promising clinical trials, and we draw particular attention to innovative bioelectronic methods of harnessing the cholinergic anti-inflammatory pathway for clinical use.
요약
콜린성 항염증 경로는
염증 반사의 원심성 경로로,
중추신경계(CNS)가 말초 면역 반응을 조절할 수 있는 신경 회로이다.
미주신경과 비장신경을 통해 전달되는 신호는
콜린 아세틸트랜스퍼라제(ChAT)+ T 세포가 생성한 아세틸콜린을 사용하여
α7 니코틴성 수용체를 발현하는 대식세포의 염증 작용을 억제한다.
형질전환 동물, 콜린성 작용제, 미주신경절제술 및 미주신경 자극을 이용한 전임상 연구를 통해
이 경로의 역할과 다양한 염증성 질환에서의 치료 가능성이 입증되었다.
본 리뷰에서는
염증 반사에 대해 현재까지 알려진 내용을 요약한다.
We also demonstrate how pre-clinical findings are being translated into promising clinical trials,
and we draw particular attention to innovative bioelectronic methods of harnessing
the cholinergic anti-inflammatory pathway for clinical use.
또한 전임상 연구 결과가 어떻게 유망한 임상 시험으로 전환되고 있는지 설명하며,
특히 콜린성 항염증 경로를 임상적으로 활용하기 위한
혁신적인 생체전자학적 방법에 주목한다.
Keywords: inflammatory reflex, cholinergic anti-inflammatory pathway, inflammatory disease, α7 nicotinic acetylcholine receptor, vagus nerve stimulation
Graphical abstract
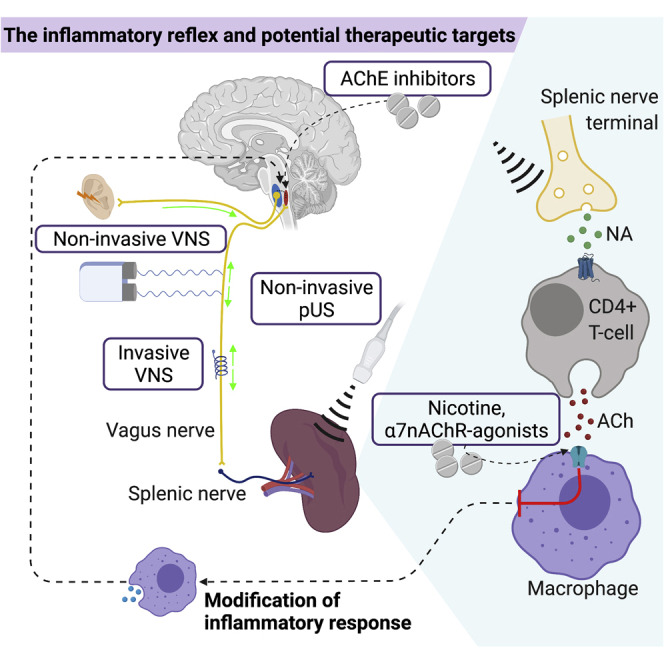
Increasing evidence has revealed the significant anti-inflammatory activity of the cholinergic pathway. Kelly and colleagues review the current knowledge of the neural inflammatory reflex and highlight recent work harnessing the cholinergic anti-inflammatory pathway as a therapeutic strategy targeting disease.
Introduction
By the end of the 20th century, the key influence of the central nervous system (CNS) on modulating our systemic inflammatory response was well recognized. Cytokines released by immune cells in response to pathogens have the capacity to transmit signals across the blood-brain barrier (BBB) through a variety of mechanisms, including stimulation of the afferent (sensory) vagus nerve.1,2 This stimulates a reciprocal response via the hypothalamic-pituitary-adrenal (HPA) axis.1
Building on these initial observations, researchers found that the CNS transmits efferent signals more directly via neural circuits, specifically the efferent vagus nerve of the parasympathetic nervous system, to exert a systemic anti-inflammatory effect.3 They termed this the cholinergic anti-inflammatory pathway (CAP) after the acetylcholine-mediated effects of the vagus nerve. The combination of the afferent and efferent arms of this vagal-immune interaction is termed the “inflammatory reflex.”4 These seminal observations led to the proposed concept of harnessing the systemic anti-inflammatory activity of the efferent arm of the vagus nerve as a therapeutic platform targeting chronic inflammatory diseases.5,6
The aim of this review is to highlight the historical evidence that supports the concept of harnessing the potential of the parasympathetic nervous system as a complementary anti-inflammatory therapy. In addition, we will describe more recent work translating these observations into the clinical trials arena. In particular, we will highlight the exciting advances in the realm of bioelectronics as potential non-pharmacological therapies.
서론
20세기 말까지,
중추신경계(CNS)가 전신 염증 반응 조절에 미치는 핵심적 영향은 잘 알려져 있었다.
병원체에 대한 반응으로 면역 세포가 분비하는 사이토카인은
감각성 미주신경 자극을 포함한 다양한 기전을 통해
혈뇌장벽(BBB)을 가로질러 신호를 전달할 수 있다.1,2
이는 시상하부-뇌하수체-부신(HPA) 축을 통한
상호 반응을 자극한다.1
이러한 초기 관찰을 바탕으로 연구자들은
중추신경계가 신경 회로,
특히 부교감신경계의 원심성 미주신경을 통해
더 직접적으로 원심성 신호를 전달하여 전
신적 항염증 효과를 발휘한다는 사실을 발견했습니다.3
그들은
미주신경의 아세틸콜린 매개 효과를 바탕으로
이를 콜린성 항염증 경로(CAP)라고 명명했습니다.
이 미주신경-면역 상호작용의 구심성 및 원심성 경로를 결합한 것을
“염증 반사”라고 명명하였다.4

이러한 획기적인 관찰 결과는
미주신경 원심성 경로의 전신적 항염증 활성을 만성 염증성 질환을 표적으로 하는
치료 플랫폼으로 활용하는 개념을 제안하는 계기가 되었다.5,6
본 리뷰의 목적은
부교감신경계의 잠재력을 보완적 항염증 치료법으로 활용한다는 개념을 뒷받침하는
역사적 근거를 강조하는 데 있다.
또한 이러한 관찰 결과를
임상시험 분야로 전환하는 최근 연구를 설명할 것이다.
특히 비약물적 치료법으로서
생체전자공학 분야의 흥미로운 진전을 부각할 예정이다.
The inflammatory reflex
Kevin Tracey and colleagues made the seminal observation that acetylcholine (ACh) and nicotine attenuated pro-inflammatory actions of macrophages. ACh is the key parasympathetic system neurotransmitter. This led to the hypothesis that these ACh-mediated anti-inflammatory effects were mediated via peripheral nicotinic (rather than muscarinic) receptors (nAChR).3 The cholinergic vagus nerve is the mediator of the parasympathetic nervous system. In vivo, transection of this nerve (vagotomy) in rats subjected to LPS-induced endotoxemia led to a more aggressive systemic inflammatory response, characterized by earlier onset of shock and higher serum and liver levels of the pro-inflammatory cytokine tumor necrosis factor alpha (TNF-α), typically released from macrophages.3 Electrical stimulation of the distal arm of the transected vagus attenuated this response.3,7 These findings revealed that the vagus nerve, previously thought only to be activated in response to peripheral inflammation,1 was also capable of modulating the inflammatory response through its efferent projections, the now-called cholinergic anti-inflammatory pathway (CAP).4
염증 반사
케빈 트레이시(Kevin Tracey)와 동료들은 아세틸콜린(ACh)과 니코틴이 대식세포의 염증 촉진 작용을 약화시킨다는 획기적인 관찰을 했다. ACh는 부교감 신경계의 핵심 신경전달물질이다. 이로 인해 ACh 매개 항염증 효과는 말초 니코틴성(무스카린성 대신) 수용체(nAChR)를 통해 매개된다는 가설이 제기되었다.3 콜린성 미주신경은 부교감 신경계의 매개체이다. 생체 내에서, LPS로 유발된 내독소혈증 상태의 쥐에서 이 신경(미주신경)을 절단(미주신경절제술)하면 더 공격적인 전신 염증 반응이 나타났으며, 이는 쇼크의 조기 발현과 대식세포에서 주로 분비되는 전염증성 사이토카인인 종양괴사인자 알파(TNF-α)의 혈청 및 간 수치 상승으로 특징지어졌다.3 절단된 미주신경의 말단 부위를 전기 자극하면 이러한 반응이 약화되었다. 3,7 이러한 결과는 이전에 말초 염증에 대한 반응으로만 활성화되는 것으로 여겨졌던 미주 신경이,1 그 원심성 투사(현재 콜린성 항염증 경로(CAP)로 불리는)를 통해 염증 반응을 조절할 수도 있음을 보여주었다.4
While these initial observations were important, they did not explain the full story. Further animal studies found that splenectomy and transection of the splenic nerve abolished the effects of vagus nerve stimulation (VNS) on systemic TNF-α released in response to endotoxemia and polymicrobial sepsis8, 9, 10 In other words, the vagus nerve modulated the TNF-α response of nAChR-positive splenic macrophages through signals transmitted via the splenic nerve. Specifically, the α7nAChR subtype was responsible for the anti-inflammatory effects of ACh, as demonstrated in α7nAChR knockout (KO) mice.8,9,11 The splenic nerve is believed to synapse not with macrophages directly (splenic neurons are catecholaminergic, not cholinergic12), but instead with choline acetyltransferase-positive (ChAT+), β2-adrenergic-receptor-positive (β2AR+) T cells, which release non-neuronal ACh in response to noradrenaline signaling. Nude mice, devoid of functional lymphocytes, are insensitive to the anti-inflammatory effects of VNS. ChAT+ T cells have been identified at synapses with splenic nerve terminals and are necessary for VNS inhibition of endotoxin-induced TNF-α release.13 Furthermore, a series of experiments by Vida and colleagues confirmed β2AR-expressing lymphocytes to be crucial for VNS-induced anti-inflammatory activity.14 Nude mice and β2AR KO mice were insensitive to VNS, but the effect was restored by the transferring of β2AR+ T cells into these animal models. The transfer of β2AR KO lymphocytes into nude mice did not restore the effect of VNS. The findings of Rosas-Ballina13 and Vida14 in combination identify β2AR+, ChAT+ lymphocytes as an essential mediating step between the splenic nerve and macrophages, completing Tracey’s model of the CAP as it is understood today (see Figure 1).15
이러한 초기 관찰은 중요했지만 전체적인 메커니즘을 설명하지는 못했다. 추가 동물 연구에서 비장 적출 및 비장 신경 절단이 내독소혈증과 다균성 패혈증에 반응하여 방출되는 전신적 TNF-α에 대한 미주신경 자극(VNS)의 효과를 소멸시킨다는 사실이 밝혀졌다.8, 9, 10 즉, 미주신경은 비신경을 통해 전달되는 신호를 통해 nAChR 양성 비장 대식세포의 TNF-α 반응을 조절했다. 특히 α7nAChR 하위형이 아세틸콜린(ACh)의 항염증 효과를 담당한다는 사실은 α7nAChR 녹아웃(KO) 마우스에서 입증되었다.8,9, 11 비장 신경은 대식세포와 직접 시냅스를 형성하지 않는 것으로 알려져 있다(비장 신경세포는 콜린성(cholinergic)이 아닌 카테콜아민성(catecholaminergic)이다12). 대신 콜린 아세틸트랜스퍼라제 양성(ChAT+), β2-아드레날린 수용체 양성(β2AR+) T 세포와 시냅스를 형성하며, 이 세포들은 노르아드레날린 신호에 반응하여 비신경성 아세틸콜린(ACh)을 방출한다. 기능성 림프구가 결여된 누드 마우스는 VNS의 항염증 효과에 반응하지 않는다. ChAT+ T 세포는 비장 신경 말단과의 시냅스에서 확인되었으며, 내독소 유발 TNF-α 방출을 VNS가 억제하는 데 필수적이다. 13 또한 Vida와 동료들의 일련의 실험은 β2AR 발현 림프구가 VNS 유도 항염증 활성에 결정적임을 확인했다.14 누드 마우스와 β2AR KO 마우스는 VNS에 반응하지 않았으나, 이 동물 모델에 β2AR+ T 세포를 이식함으로써 효과가 회복되었다. β2AR KO 림프구를 누드 마우스에 이식해도 VNS의 효과는 회복되지 않았다. Rosas-Ballina13과 Vida14의 연구 결과를 종합하면, β2AR+, ChAT+ 림프구가 비장 신경과 대식세포 사이의 필수 매개 단계임을 확인하며, 이는 오늘날 이해되는 CAP(비장-대식세포-비장 신경) 모델을 완성한다(그림 1 참조).15
Figure 1.
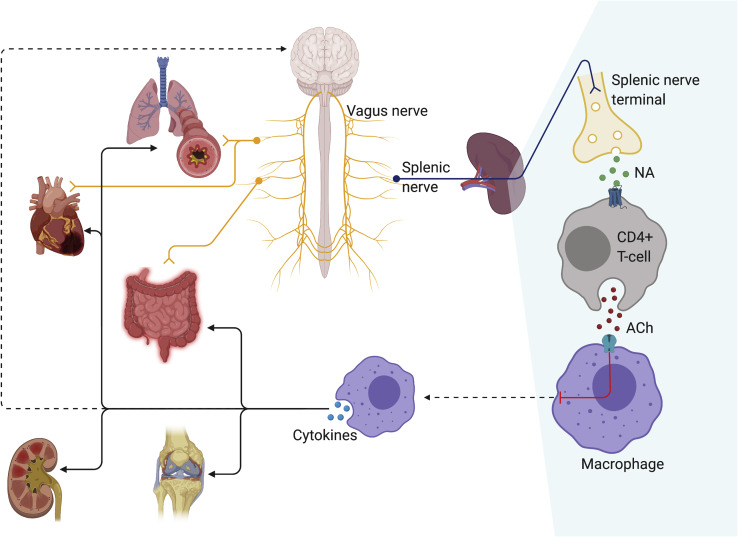
The cholinergic anti-inflammatory pathway
Through the inhibition of splenic macrophages, the vagus nerve attenuates inflammatory responses in multiple bodily systems, including the lungs, GIT, myocardium, synovia, and kidneys. The vagus nerve may also mediate some of its effects directly through innervation of viscera (e.g., lungs, heart, GIT). Suppression of the systemic inflammatory response can likewise influence neuroinflammation.
콜린성 항염증 경로
미주신경은 비장 대식세포를 억제함으로써 폐, 위장관, 심근, 활막, 신장 등 여러 신체 시스템의 염증 반응을 완화합니다. 미주신경은 또한 내장 기관(예: 폐, 심장, 위장관)에 직접 분포하여 일부 효과를 매개할 수 있습니다. 전신 염증 반응의 억제는 신경염증에도 영향을 미칠 수 있습니다.
ACH, 아세틸콜린; NA, 노르아드레날린.
ACH, acetylcholine; NA, noradrenaline.
It should be noted that alternative theories to the CAP have been proposed. The concept of a di-synaptic connection between the vagus and splenic nerve has been questioned.16 This was based on the observation that VNS did not induce detectable action potentials in the splenic nerves of rats, and an anatomical connection could not be identified at a synaptic level.17 This led to an alternative concept that the efferent arm of the inflammatory reflex is not the CAP, but rather the sympathetic nervous system.17 Subsequent research demonstrated that action potentials were transmitted via the sympathetic chain and splanchnic nerves, in turn innervating the splenic nerve and ultimately inhibiting cytokine release.16, 17, 18 Another group found that the anti-inflammatory effects of stress and activation of autonomic C1 neurons in the brainstem were not attenuated by subdiaphragmatic vagotomy.19 It was similarly found that vagotomy did not exacerbate the effects of endotoxemia, whereas splanchnic neurotomy did.18 However, a substantive body of work including Borovikova and colleagues3,20, 21, 22 has supported the importance of the CAP mediated via the splenic nerve and β2AR-expressing lymphocytes. Martelli and colleagues attributed this discrepancy to an interruption of the HPA axis. However, this failed to explain why stimulation of the distal vagus nerve (which was transected proximally and therefore incapable of transmitting an afferent signal to the hypothalamus) would result in suppression of splenic TNF release without any alteration of corticosterone levels.3 Furthermore, the corticosterone antagonist mifepristone did not block the effects of the CAP.19 Abe and colleagues showed that VNS could activate the CAP regardless of whether it was applied to the distal or proximal limb of the vagus,23 while the contralateral vagus nerve was blocked with lignocaine, potentially suggesting the existence of a second efferent arm to the CAP that could be stimulated via the afferent vagus nerve.
Vida and colleagues9 reported that suppression of serum TNF levels in a mouse model of systemic sepsis could also be achieved by splenic nerve stimulation (SNS), and while VNS was dependent on the α7nAChR, SNS was effective in α7nAChR KO mice. Their findings suggested that, although the α7nAChR is an essential component of the CAP at the level of vagus-to-splenic nerve signaling, splenic nerve-to-macrophage signaling may be possible through alternate, α7nAChR-independent mechanisms, though such a mechanism has yet to be identified. Further supporting these findings is the recent finding that while T cells certainly appear capable of forming synapse-like structures with splenic neurons,24 and ChAT+ lymphocytes in the spleen are primarily concentrated in the white pulp where sympathetic are situated,13 a synaptic connection with ChAT+ lymphocytes could not be identified on confocal microscopy.25
CAP에 대한 대안 이론들이 제안된 점에 유의해야 한다. 미주신경과 비장신경 사이의 이시냅스 연결 개념은 의문을 제기받았다.16 이는 쥐의 비장신경에서 VNS가 감지 가능한 활동 전위를 유도하지 않았으며, 시냅스 수준에서 해부학적 연결을 확인할 수 없었다는 관찰에 근거한다.17 이로 인해 염증 반사의 원심성 경로는 CAP가 아닌 교감신경계라는 대안적 개념이 제시되었다. 17 후속 연구에서는 교감 신경 사슬과 내장 신경을 통해 활동 전위가 전달되어 비장 신경을 다시 분포시키고 궁극적으로 사이토카인 방출을 억제한다는 것이 입증되었다.16, 17, 18 다른 연구 그룹은 스트레스의 항염증 효과와 뇌간 자율 신경 C1 뉴런의 활성화가 횡격막하 미주신경 절제술로도 약화되지 않는다는 사실을 발견했다. 19 마찬가지로, 미주절제술은 내독소혈증의 효과를 악화시키지 않는 반면, 내장신경절제술은 악화시킨다는 사실이 밝혀졌다.18 그러나 Borovikova와 동료들3,20, 21, 22를 포함한 상당한 양의 연구는 비장신경과 β2AR 발현 림프구를 매개로 하는 CAP의 중요성을 지지해왔다. 마르텔리(Martelli)와 동료들은 이러한 불일치를 HPA 축의 차단으로 설명하였다. 그러나 이는 원위 미주신경 자극(근위부 절단으로 시상하부에 구심성 신호를 전달할 수 없는 상태)이 코르티코스테론 수치 변화 없이 비장 TNF 방출을 억제하는 이유를 설명하지 못했다.3 또한, 코르티코스테론 길항제인 미페프리스톤은 CAP의 효과를 차단하지 못했다.19 Abe와 동료들은23 미주신경의 원위부 또는 근위부에 적용되었는지 여부와 관계없이 VNS가 CAP를 활성화할 수 있음을 보여주었으며, 이 과정에서 대측 미주신경은 리도카인으로 차단되어, 미주신경의 구심성 경로를 통해 자극될 수 있는 CAP로의 두 번째 원심성 경로의 존재 가능성을 시사했다.
Vida와 동료들9은 전신성 패혈증 마우스 모델에서 혈청 TNF 수치 억제가 비장 신경 자극(SNS)을 통해서도 달성될 수 있다고 보고했으며, VNS는 α7nAChR에 의존하는 반면 SNS는 α7nAChR KO 마우스에서도 효과적이었다. 이들의 연구 결과는 미주신경-비장신경 신호 전달 수준에서 α7nAChR이 CAP의 필수 구성 요소임에도 불구하고, 비장신경-대식세포 신호 전달은 α7nAChR과 무관한 대체 기전을 통해 가능할 수 있음을 시사한다. 다만 그러한 기전은 아직 규명되지 않았다. 이러한 결과를 뒷받침하는 최근 연구에 따르면, T 세포가 비장 신경세포와 시냅스 유사 구조를 형성할 수 있는 것으로 보이지만,24 비장의 ChAT+ 림프구는 주로 교감신경이 위치한 백색 펄프에 집중되어 있음에도 불구하고,13 공초점 현미경 관찰에서 ChAT+ 림프구와의 시냅스 연결은 확인되지 않았다.25
These findings suggest that the CAP model may be one of the additional pathways by which our nervous system modulated the systemic inflammatory response. For example, Murray and colleagues have proposed that splenic neurons may communicate with ChAT+ lymphocytes via neurotransmitter diffusion or chemotaxis through the CXCL13 chemokine,25 which is upregulated by sympathetic activity, rather than through synaptic transmission. Detailed characterization of alternative or additional pathways within the inflammatory reflex will be essential to developing the therapeutic potential of this field, particularly if these pathways present additional therapeutic targets or help to explain treatment failure in a sub-group of patients. Nevertheless, it is our opinion that there is a convincing and growing wealth of evidence for targeting the vagus nerve and the α7nACh receptor as anti-inflammatory therapies.
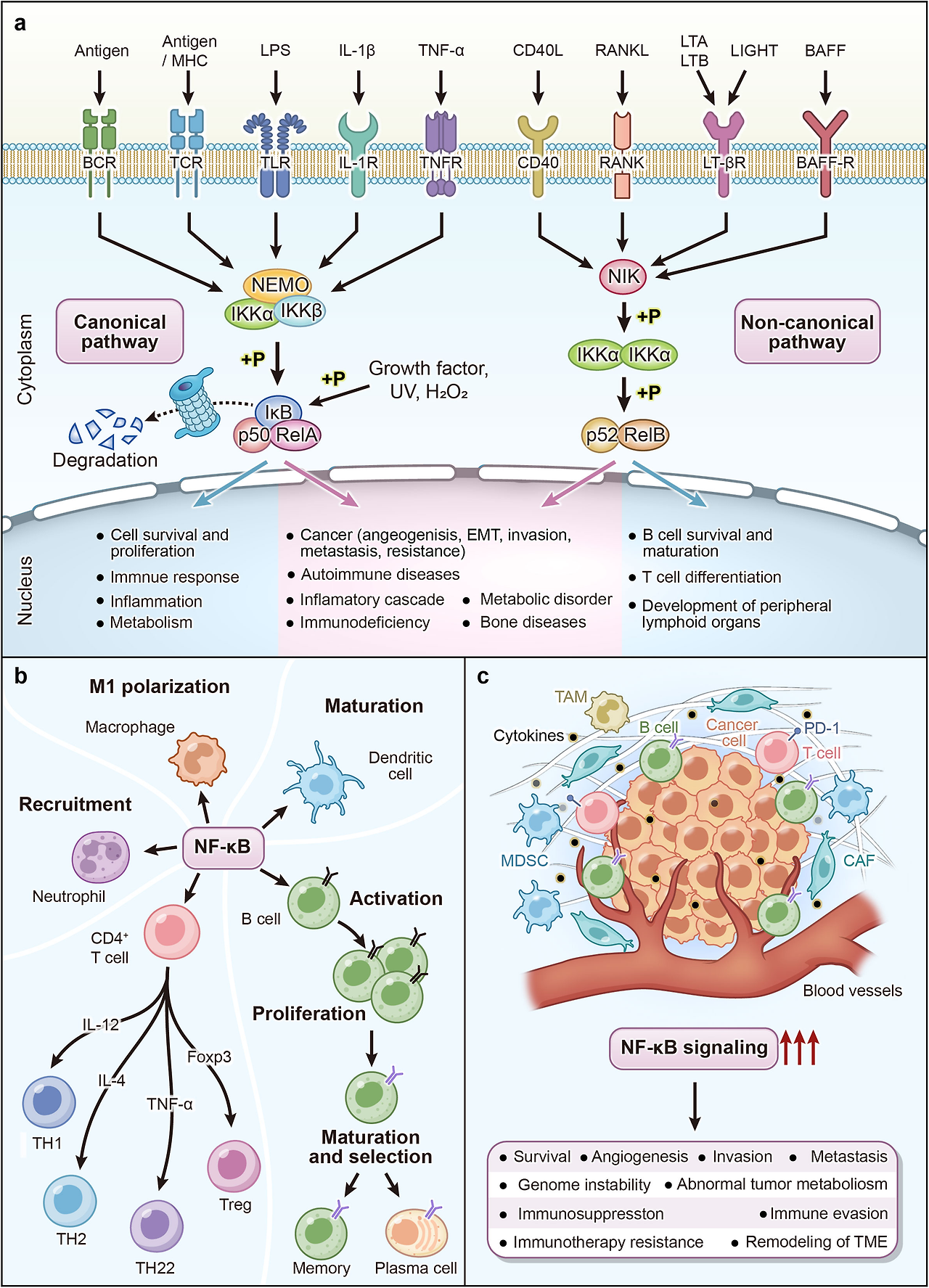
As discussed above, the α7nAChR has been identified as the extracellular target of the CAP through KO studies.8,9,11 The intracellular effects of α7nAChR activation, however, are numerous and not mutually exclusive. In non-neuronal cells, intracellular-signaling cascades are activated via ligand binding of intracellular molecules and tyrosine kinase-mediated increases in intracellular calcium, rather than by ion-channel opening, as seen in neurons.26 In macrophages and monocytes, anti-inflammatory effects of VNS are mediated by the recruitment of the tyrosine kinase JAK2 to the α7nAChR and subsequent phosphorylation of STAT3, which blocks cytokine transcription by NF-κB.27
이러한 결과는 CAP 모델이 우리 신경계가 전신 염증 반응을 조절하는 추가 경로 중 하나일 수 있음을 시사한다. 예를 들어 Murray와 동료들은 비장 신경세포가 시냅스 전달보다는 교감 신경 활동에 의해 상향 조절되는 CXCL13 케모카인을 통한 신경전달물질 확산 또는 화학유인 작용을 통해 ChAT+ 림프구와 소통할 수 있다고 제안했다. 염증 반사 내 대체 또는 추가 경로의 상세한 규명은 이 분야의 치료적 잠재력 개발에 필수적이며, 특히 이러한 경로가 추가 치료 표적을 제시하거나 일부 환자군에서 치료 실패를 설명하는 데 도움이 될 경우 더욱 그러하다. 그럼에도 불구하고, 미주신경과 α7nACh 수용체를 표적으로 하는 항염증 치료법에 대한 설득력 있고 증가하는 증거가 존재한다는 것이 우리의 견해이다.
앞서 논의한 바와 같이, α7nAChR은 KO 연구를 통해 CAP의 세포외 표적으로 확인되었다.8,9,11 그러나 α7nAChR 활성화의 세포내 효과는 다양하며 상호 배타적이지 않다. 비신경 세포에서는, 신경세포에서 관찰되는 이온 채널 개방보다는 세포내 분자의 리간드 결합 및 티로신 키나아제 매개 세포내 칼슘 증가를 통해 세포내 신호 전달 계통이 활성화된다. 26 대식세포와 단핵구에서 VNS의 항염증 효과는 티로신 키나제 JAK2가 α7nAChR에 모집되고, 이후 STAT3의 인산화가 일어나 NF-κB에 의한 사이토카인 전사를 차단함으로써 매개됩니다.27
The JAK2/STAT3 pathway is not the only one implicated in intracellular signaling of the α7nAChR (see Figure 2). Other molecules have been implicated and may interact with STAT3 or act independently (see Figure 2). These include inhibition of mitogen-activated protein kinase (MAPK) pathways such as ERK1/2,28 the activation of adenylyl cyclase (AC) 6, which in turn activates the cAMP-CREB-cFOS pathway,29 signaling via heme-oxygenase 130,31 and heat shock protein (HSP)-70,32 and the suppressed phosphorylation of IκB.33 Through other pathways, α7nAChR may downregulate cell surface expression of NF-κB-inducing receptors CD14 and Toll-like receptor (TLR)-434,35 and enhance autophagic activity,36, 37, 38 further contributing to the anti-inflammatory phenotype. ACh, which enters the cytoplasm during states of inflammation, can also act on mitochondrial α7nAChR, preventing the release of mtDNA and the activation of the NLRP3 inflammasome complex responsible for release of cytokines IL-1β and HMGB1.39 α7nAChR activation promotes the expression of microRNA-124, which inhibits IL-6 and TNF-α release.40 The proposed mechanisms of action of microRNA-124 include targeting of IκB and inhibition of TNF-α-converting enzyme (TACE), but also the suppression of STAT3, which was paradoxically found to be an essential mediator of IL-6 production.40 Conflicting results of this type demonstrate that elements of this signaling cascade are still poorly understood and that there may be multiple intracellular pathways through which the α7nAChR can act. While the majority of “CAP-targeted” therapies to date are directed toward extracellular components such as the vagus nerve and α7nAChR, further investigation of downstream pathways will help to clarify the mechanism underlying the CAP and may present new therapeutic targets.
JAK2/STAT3 경로는 α7nAChR의 세포 내 신호 전달에 관여하는 유일한 경로는 아닙니다(그림 2 참조). 다른 분자들도 관여하며 STAT3와 상호작용하거나 독립적으로 작용할 수 있습니다(그림 2 참조). 여기에는 ERK1/2와 같은 미토겐 활성화 단백질 키나제(MAPK) 경로의 억제,28 아데닐산 시클라제(AC)의 활성화 6(이는 차례로 cAMP-CREB-cFOS 경로를 활성화함),29 헤모글로빈 산화효소 130,31 및 열 충격 단백질(HSP) -70,32 및 IκB 인산화 억제33 등이 있다. 다른 경로를 통해 α7nAChR은 NF-κB 유도 수용체인 CD14 및 Toll-like receptor (TLR)-4의 세포 표면 발현을 하향 조절하고34,35 자가포식 활성을 증진시켜36, 37, 38 항염증 표현형에 추가적으로 기여할 수 있다. 염증 상태에서 세포질로 유입되는 ACh는 미토콘드리아 α7nAChR에도 작용하여 mtDNA 방출과 사이토카인 IL-1β 및 HMGB1 방출을 담당하는 NLRP3 인플라마좀 복합체의 활성화를 방지할 수 있다.39 α7nAChR 활성화는 IL-6 및 TNF-α 방출을 억제하는 microRNA-124의 발현을 촉진한다. 40 microRNA-124의 제안된 작용 기전에는 IκB 표적화와 TNF-α 전환 효소(TACE) 억제가 포함되지만, 역설적으로 IL-6 생산의 필수 매개체로 밝혀진 STAT3의 억제도 포함됩니다. 40 이러한 상반된 결과들은 이 신호 전달 계통의 요소들이 아직 제대로 이해되지 않았으며, α7nAChR이 작용할 수 있는 세포 내 경로가 여러 개 존재할 수 있음을 보여준다. 현재까지 대부분의 “CAP 표적” 치료법은 미주신경 및 α7nAChR과 같은 세포 외 성분을 대상으로 하지만, 하류 경로에 대한 추가 연구는 CAP의 기저 메커니즘을 명확히 하는 데 도움이 될 것이며 새로운 치료 표적을 제시할 수 있을 것이다.
Figure 2.
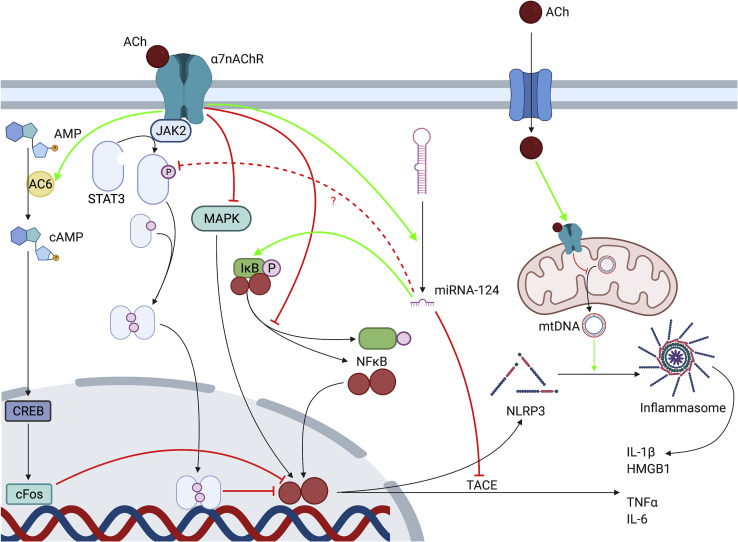
| α7nAChR의 세포 내 메커니즘: Cholinergic Anti-Inflammatory Pathway (CAP)의 분자적 기반 제공된 다이어그램은 " **α7 nicotinic acetylcholine receptor (α7nAChR)의 제안된 세포 내 메커니즘(proposed intracellular mechanisms)**을 시각화한 것. 이 다이어그램은 자율신경계(특히 미주신경(vagus nerve)과 비장신경(splenic nerve), 그리고 대안적으로 splanchnic nerves)를 통해 매개되는 **cholinergic anti-inflammatory pathway (CAP, 콜린성 항염증 경로)**의 efferent(운동성) arm을 중점적으로 다룹니다. CAP는 중추신경계(CNS)가 말초 면역 반응을 조절하는 신경 회로로, 아세틸콜린(ACh)이 α7nAChR을 통해 대식세포(macrophages)의 염증 작용을 억제. 논문은 이 경로가 만성 염증 질환(예: 췌장염, 류마티스 관절염) 치료에 잠재력을 강조하며, 전임상 연구(예: vagus nerve stimulation, VNS)와 임상 시험을 통해 검증된 바를 요약. 논문의 Figure 2는 ACh가 α7nAChR에 결합한 후 여러 비배타적(non-exclusive) 신호 전달 경로를 통해 NF-κB, NLRP3 inflammasome 등의 염증 매개체를 억제하는 과정. 이는 splanchnic nerves(내장신경, 이전 PDF 논문에서 thoracic/lumbar/sacral로 설명된 교감성 신경)와 연결되는데, 논문에서 대안 이론으로 sympathetic chain과 splanchnic nerves가 비장신경을 통해 CAP를 매개할 수 있다고 제안. (예: splanchnic neurotomy가 endotoxemia를 악화시킴.) 이는 이전 PDF("Clinical Anatomy of the Splanchnic Nerves", Haroun 2018)에서 splanchnic nerves가 vagus가 아닌 efferent motor limb으로 염증 억제에 관여한다고 언급한 바와 일치. 아래에서 다이어그램을 단계적으로 설명하겠습니다. 1. 수용체 활성화: ACh 결합과 초기 신호 주요 요소: ACh (빨간 원)가 α7nAChR (파란 채널 구조, 비신경세포如 macrophages에서 발현)에 결합. 논문에 따르면, α7nAChR은 이온 채널 개방 외에 t yrosine kinase-mediated calcium 증가를 통해 신호를 시작. 메커니즘: 리간드 결합(ligand binding)이 JAK2 (Janus kinase 2, 황색 원)를 모집(recruitment)해 STAT3 (signal transducer and activator of transcription 3, 파란 원)의 인산화(phosphorylation, P 표시)를 유발. 이는 NF-κB의 사이토카인 전사(cytokine transcription)를 차단. 항염증 효과: STAT3가 대식세포 활성화를 약화시켜 TNF-α 같은 프로염증 사이토카인 생산을 억제. 논문: "JAK2/STAT3 activation attenuates macrophage activation and cytokine production." 2. 주요 신호 전달 경로: 증폭과 억제 다이어그램은 여러 병렬 경로를 녹색(활성화)과 빨간(억제) 화살표로 표시합니다. 논문은 이들이 비배타적이며, α7nAChR 활성화가 HO-1(heme-oxygenase 1), HSP-70(heat shock protein 70), autophagy(자噬) 강화와 함께 작용한다고 설명합니다. 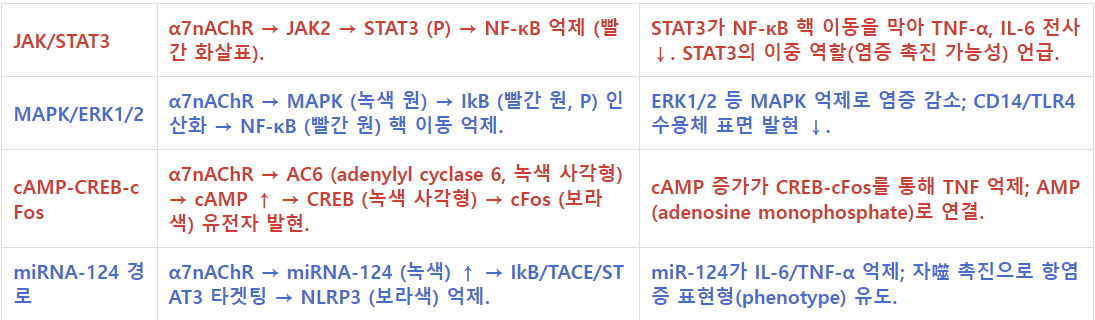 3. 최종 억제: Inflammasome과 사이토카인 방출 차단 주요 요소: NF-κB 경로: IkB 안정화 → NF-κB 핵 이동 ↓ → TACE (TNF-α converting enzyme) 억제 → TNF-α (회색) ↓. NLRP3 Inflammasome: miR-124 → NLRP3 억제 → mtDNA (mitochondrial DNA, 미토콘드리아 DNA) 방출 ↓ → IL-1β (회색) 생성 ↓. HMGB1 (빨간 원) 방출 억제 → IL-6 ↓. 미토콘드리아 α7nAChR: 세포 내 ACh가 mtDNA 방출을 막아 inflammasome 조립(assembly) 차단. 메커니즘: 논문: "Intracellular ACh acts on mitochondrial α7nAChR to prevent mtDNA release and NLRP3 inflammasome activation, inhibiting IL-1β and HMGB1 release." 이는 caspase-1 활성화를 막아 프로-IL-1β 프로세싱을 억제합니다. splanchnic nerves 연결: 논문에서 CAP의 대안 efferent arm으로 splanchnic nerves(교감성)가 제안되며, splenic nerve 자극이 α7nAChR 독립적으로 TNF 억제. 이전 PDF와 연계: thoracic splanchnic nerves (GSN 등)가 celiac ganglion을 통해 상복부 염증(췌장염 등) 억제. 4. 전체적 함의와 치료 잠재력 논문은 CAP가 비장 대식세포 억제를 통해 폐, GIT(위장관), 심근, 관절낭, 신장 등 다중 시스템 염증을 완화한다고 강조합니다. VNS나 cholinergic agonists(예: nicotine)가 전임상에서 TNF-α/IL-1β/IL-6를 줄였으나, STAT3의 이중성 등 미해결 과제 지적. 임상적으로 bioelectronic medicine(생체전자 의학, 예: implantable VNS device)이 sepsis/RA 치료에 유망. splanchnic nerves의 역할은 vagotomy 모델에서 확인되며, PDF처럼 splanchnicectomy가 통증 관리에 사용되지만, 과도 절제 시 면역 저하 위험. 이 메커니즘은 자율신경계(미주/비장/splanchnic nerves)가 면역을 '하드와이어'로 조절하는 증거로, 논문의 Figure 2 legend: "AC6, adenylyl cyclase 6; Ach, acetylcholine; ... STAT3, signal transducer and activator of transcription 3." |
<!--br {mso-data-placement:same-cell;}-->
경로주요 구성요소 및 흐름항염증 효과 (논문 기반)
| JAK/STAT3 | α7nAChR → JAK2 → STAT3 (P) → NF-κB 억제 (빨간 화살표). | STAT3가 NF-κB 핵 이동을 막아 TNF-α, IL-6 전사 ↓. STAT3의 이중 역할(염증 촉진 가능성) 언급. |
| MAPK/ERK1/2 | α7nAChR → MAPK (녹색 원) → IkB (빨간 원, P) 인산화 → NF-κB (빨간 원) 핵 이동 억제. | ERK1/2 등 MAPK 억제로 염증 감소; CD14/TLR4 수용체 표면 발현 ↓. |
| cAMP-CREB-cFos | α7nAChR → AC6 (adenylyl cyclase 6, 녹색 사각형) → cAMP ↑ → CREB (녹색 사각형) → cFos (보라색) 유전자 발현. | cAMP 증가가 CREB-cFos를 통해 TNF 억제; AMP (adenosine monophosphate)로 연결. |
| miRNA-124 경로 | α7nAChR → miRNA-124 (녹색) ↑ → IkB/TACE/STAT3 타겟팅 → NLRP3 (보라색) 억제. | miR-124가 IL-6/TNF-α 억제; 자噬 촉진으로 항염증 표현형(phenotype) 유도. |

| 미주신경은 대식세포 표면의 α7-니코틴성 아세틸콜린 수용체(α7nAChR)를 매개로 하는 '콜린성 항염증 경로'를 통해 염증 반응을 조절할 수 있다. 그러나 α7nAChR 활성화와 염증성 사이토카인 생산을 연결하는 세포 내 기전은 아직 명확히 규명되지 않았다. 본 연구에서 우리는 LPS에 노출된 세포 및 생쥐에서 콜린성 작용제에 의해 miR-124가 상향 조절됨을 발견했습니다. miR-124 모방체 및 siRNA 노크다운을 활용하여, miR-124가 콜린성 항염증 작용의 핵심 매개체임을 입증했습니다. 또한, 우리의 데이터는 miR-124가 신호전달 및 전사활성인자 3(STAT3)을 표적하여 IL-6 생산을 감소시키고, TNF-α 전환 효소(TACE)를 표적하여 TNF-α 방출을 감소시킴으로써 LPS에 의해 유도된 사이토카인 생산을 조절함을 시사한다. 이러한 결과는 또한 miR-124가 염증성 질환 치료를 위한 잠재적 치료 표적임을 시사한다. |
https://www.nature.com/articles/s41392-024-01757-9

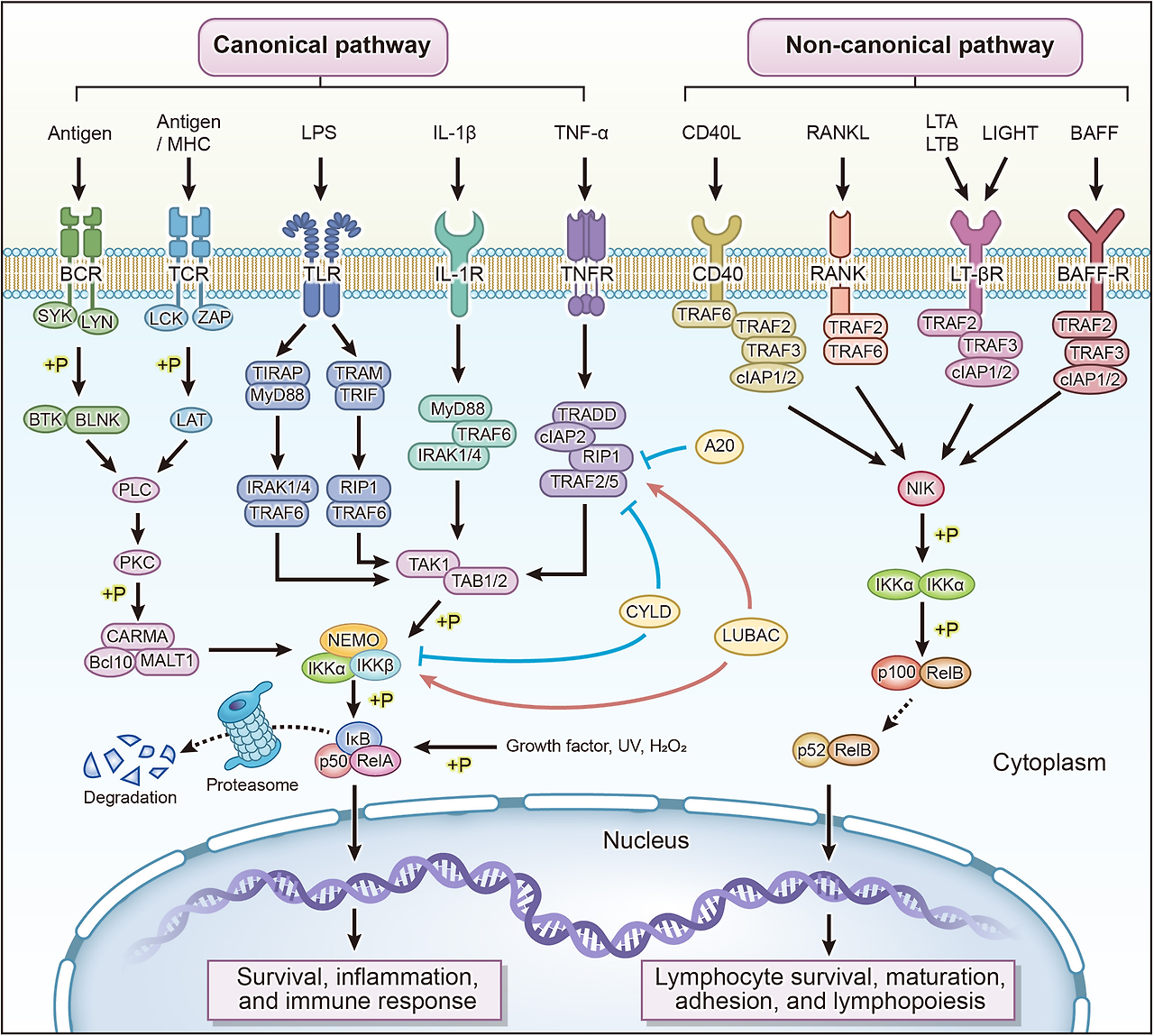
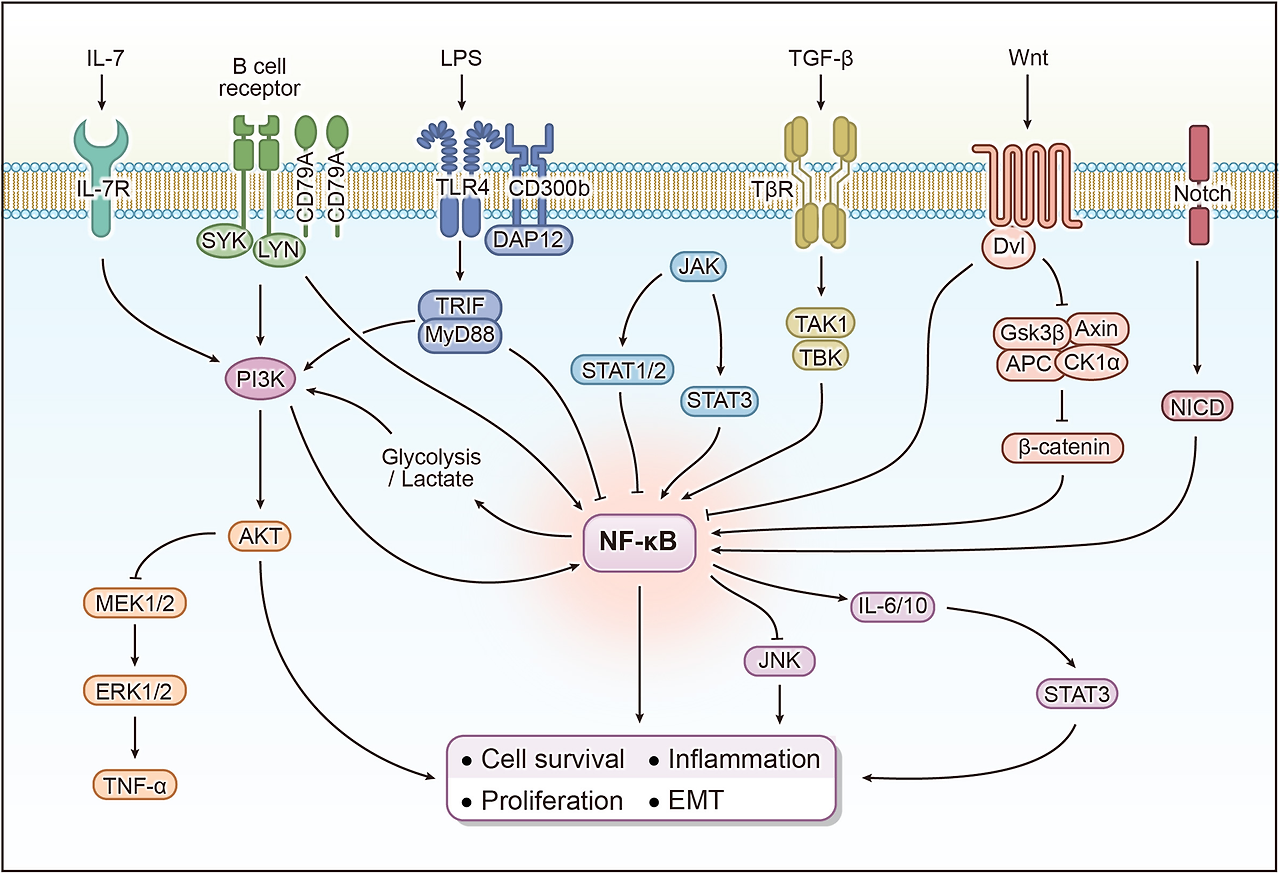
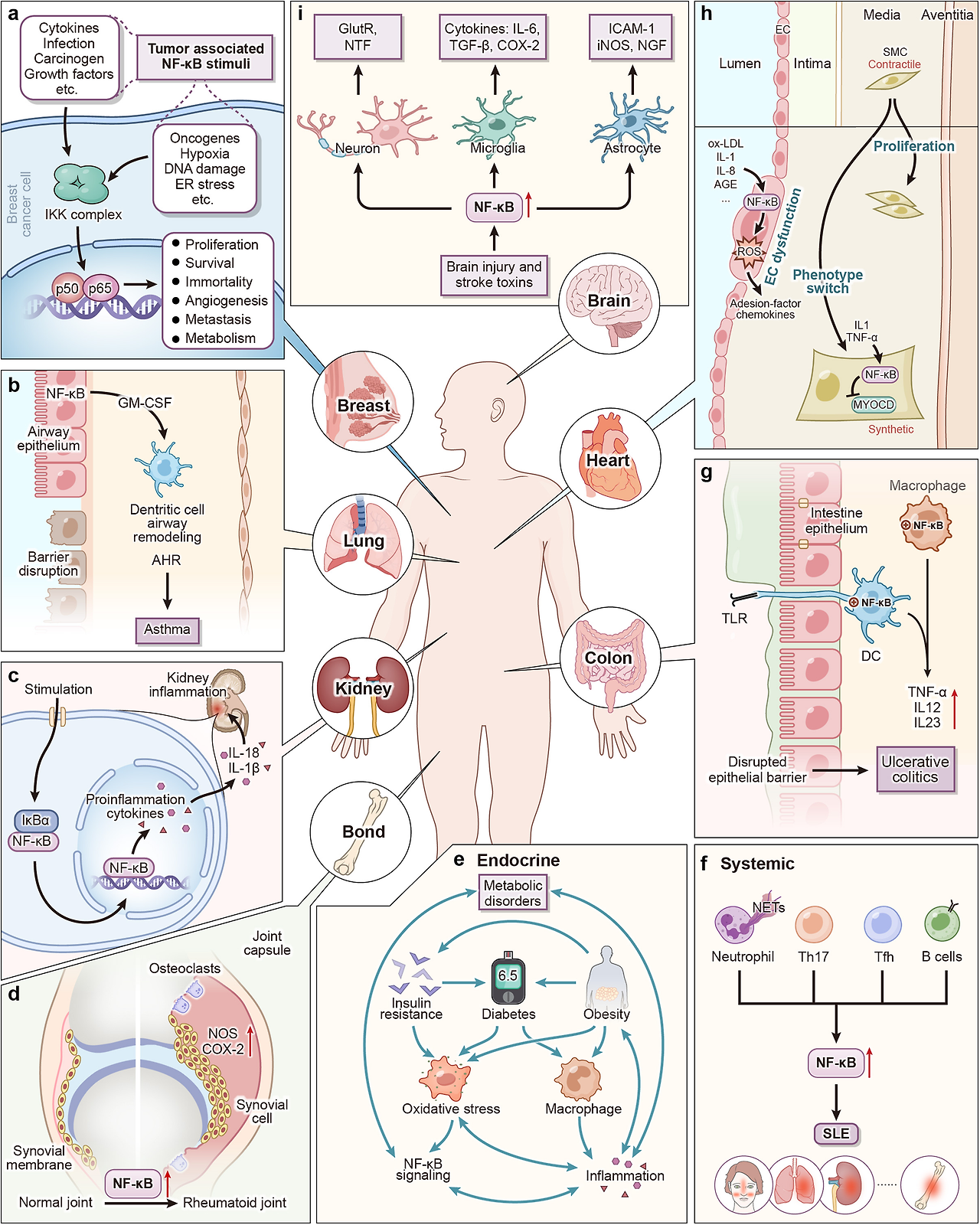
Proposed intracellular mechanisms of the α7nAChR
AC6, adenylyl cyclase 6; Ach, acetylcholine; AMP, adenosine monophosphate; cAMP, cyclic adenosine monophosphate; CREB, cAMP response element-binding protein; JAK2, Janus kinase 2; MAPK, mitogen-activated protein kinase; miRNA, microRNA; NF-κB, nuclear factor κ-B; NLRP3, NOD-, LRR-, and pyrin domain-containing protein; STAT3, signal transducer and activator of transcription 3.
그림 2.
α7nAChR의 제안된 세포 내 기전
AC6, 아데닐릴 시클레이스 6; Ach, 아세틸콜린; AMP, 아데노신 모노포스페이트; cAMP, 사이클릭 아데노신 모노포스페이트; CREB, cAMP 반응 요소 결합 단백질; JAK2, 자누스 키나제 2; MAPK, 미토겐 활성화 단백질 키나제; miRNA, 마이크로RNA; NF-κB, 핵인자 κ-B; NLRP3, NOD-, LRR-, 및 피린 도메인 함유 단백질; STAT3, 신호 전달 및 전사 활성화 인자 3.
The inflammatory reflex in disease
Inflammation is implicated in the pathogenesis of a broad range of human diseases. The demonstration of the significant systemic anti-inflammatory properties of the inflammatory neural reflex makes the CAP an attractive therapeutic target. This could potentially be harnessed pharmaceutically by targeting the α7nAChR or bioelectronically via both VNS and other methods such as splenic ultrasound (see Figure 3). Here, we review evidence on the role of the CAP and its therapeutic potential in inflammatory diseases.
질병에서의 염증 반사
염증은 광범위한 인간 질환의 병인에 관여합니다. 염증성 신경 반사의 중요한 전신적 항염증 특성이 입증됨에 따라 CAP는 매력적인 치료 표적이 되었습니다. 이는 α7nAChR을 표적으로 하는 약리학적 접근이나 VNS 및 비장 초음파(그림 3 참조)와 같은 생체전자학적 방법을 통해 잠재적으로 활용될 수 있다. 본고에서는 염증성 질환에서 CAP의 역할과 치료적 잠재력에 관한 증거를 검토한다.
Figure 3.
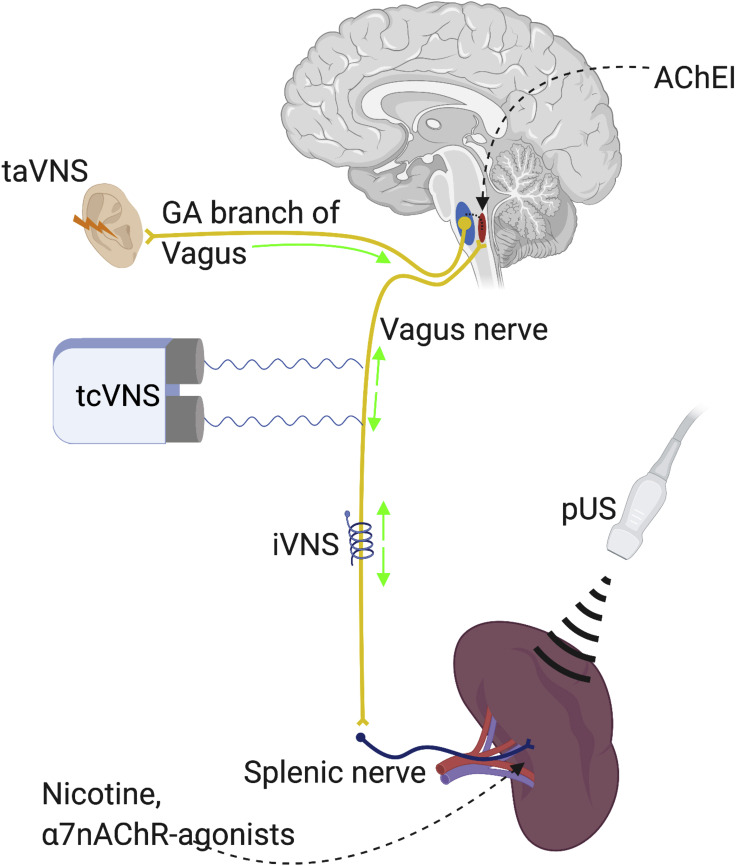
Stimulation of the CAP
The CAP can be stimulated pharmacologically through centrally acting acetylcholinesterase inhibitors (AChEI) and peripherally acting nicotine or α7nAChR agnoists. Non-pharmacological stimulation is achieved through invasive and non-invasive VNS or pUS. iVNS, invasive vagus nerve stimulation; taVNS, transauricular vagus nerve stimulation; tcVNS, transcervical Vagus nerve stimulation.
그림 3.
CAP 자극
CAP는 중추 작용 아세틸콜린에스테라제 억제제(AChEI) 및 말초 작용 니코틴 또는 α7nAChR 애그노이스트를 통해 약리학적으로 자극될 수 있다. 비약리학적 자극은 침습적 및 비침습적 VNS 또는 pUS를 통해 달성된다. iVNS: 침습적 미주신경 자극; taVNS: 경이적 미주신경 자극; tcVNS: 경경추적 미주신경 자극.
Rheumatological disease
Rheumatoid arthritis (RA), a chronic inflammatory condition of synovial membranes, and related connective tissue disorders are the most studied with regard to the potential of exploiting the inflammatory reflex therapeutically. Extensive pre-clinical research over the past twenty years has led to more recent exploratory early clinical trials, resulting in an expanding body of work supporting this therapeutic strategy in connective tissue disorders.
Administration of nicotine,41 selective α7nAChR-agonist AR-R17779,42 and partial agonist GTS-2143,44 mitigate joint swelling42, 43, 44 and reduce both radiological42,44 and histological41 measures of bony erosion in animal models of collagen-induced arthritis (CIA). α7nAChR-selective antagonist methyllycaconitine (MLA) attenuated the effect of GTS-21.43 These clinical and radiological findings are associated with a significant fall in systemic pro-inflammatory cytokines findings (e.g., TNF-α,41, 42, 43, 44 IL-6,41, 42, 43 and IL-1β44). Analysis of synovial fluid reveals a parallel fall in pro-inflammatory cytokines with a consequent reduction in joint inflammatory cells42 and osteoclasts.44
류마티스 질환
활막의 만성 염증성 질환인 류마티스 관절염(RA) 및 관련 결합 조직 장애는 염증 반사를 치료적으로 활용할 가능성과 관련해 가장 많이 연구된 분야이다. 지난 20년간의 광범위한 전임상 연구는 최근 탐색적 초기 임상 시험으로 이어졌으며, 그 결과 결합 조직 장애에서 이 치료 전략을 뒷받침하는 연구 성과가 확대되고 있다.
니코틴,41 선택적 α7nAChR 작용제 AR-R17779,42 및 부분 작용제 GTS-2143,44의 투여는 콜라겐 유발 관절염(CIA) 동물 모델에서 관절 부종42, 43, 44를 완화시키고 방사선학적42,44 및 조직학적41 측정 기준에 따른 골 침식 정도를 모두 감소시킨다. α7nAChR 선택적 길항제 메틸리카코니틴(MLA)은 GTS-2143의 효과를 약화시켰다.43 이러한 임상적 및 방사선학적 소견은 전신성 프로염증성 사이토카인(예: TNF-α,41, 42, 43, 44 IL-6,41, 42, 43 및 IL-1β44)의 현저한 감소와 연관되어 있습니다. 활액 분석 결과, 전염증성 사이토카인의 병행적 감소와 함께 관절 염증 세포42 및 파골세포의 감소가 관찰되었습니다.44
The synovia of CIA mice treated with GTS-21 has significantly reduced expression of CD11c, a relatively specific marker of dendritic cells (DCs), known to be pathogenic in RA.43 One potential mechanism for this is that GTS-21 inhibited the differentiation of bone marrow-derived DCs from progenitor cells in vitro, and this differentiation was inhibited by MLA.43
Nicotine treatment results in lower levels of synovial Th17 cells, a subset of CD4+ lymphocytes believed to promote inflammation in RA through secretion of IL-17a.45 α7nAChR KO exacerbates CIA with greater levels of joint destruction, higher serum levels of TNF-α and chemokine MCP-1, and a shift to a higher ratio of inflammatory cytokine-producing Th1 cells to IL-10-producing Th2 cells.46
Overall, these studies demonstrate that the α7nAChR has anti-inflammatory and potentially disease-modifying effects on RA. A range of cells including macrophages, fibroblasts, T cells, and B cells expressing these receptors can be found in the synovia of patients with RA.47 Though it remains to be determined whether infiltration of these cells is actually stimulated directly by ACh or by α7nAChR-independent mechanisms downstream of macrophage activation and cytokine release, or whether α7nAChR expression is purely a secondary marker of inflammatory cell activation.
The vagus nerve has been implicated in RA. Vagotomy was associated with greater levels of synovial neutrophil infiltration and hyperalgesia in a mouse model of antigen-induced arthritis.21 Two studies demonstrated that the disease-exacerbating effects of vagotomy were attenuated by α7nAChR stimulation.42,48 While these effects only trended toward statistical significance, the studies used unilateral vagotomy solely, which may, because of compensation from the contralateral nerve, have more modest effects than that of bilateral vagotomy seen in other disease models.20 Furthermore, VNS has demonstrated efficacy in the treatment of CIA in at least two studies, one using electrical stimulation49 and the other mechanical.50 Together, these studies reveal that VNS inhibits joint inflammation and destruction49,50 and release of inflammatory cytokines.50 These studies led to a clinical trial of VNS in RA patients.51 Eighteen RA patients were implanted with VNS and experienced a rapid improvement in disease severity as measured by the internationally validated disease activity score-28 (DAS28). This DAS is derived from the assessment of 28 specific joints by a healthcare professional combined with both a patient self-reported score for health and well-being and input of blood systemic inflammatory markers (e.g., ESR or CRP). In addition, a corresponding reduction in TNF-α release on lipopolysaccharide (LPS)-whole blood culture was observed, a measure of the systemic pro-inflammatory state, in which blood samples from participants are exposed to an inflammatory trigger ex vivo. When VNS was suspended for two weeks, symptoms relapsed but were once again attenuated on reactivation of the stimulator. Recently a sham-controlled pilot study assessed the safety of an implantable VNS device in RA patients but was underpowered to assess clinical efficacy. However, it is worth noting that 5 of 10 patients (seven blinded, three unblinded) in the treatment arm demonstrated a clinically significant change in disease severity score, versus zero out of four sham controls.52 Neither of these trials reported serious adverse events, though a high proportion (89% in the former,51 57% in the latter;52 60% of in the treatment arm and 50% of controls) reported mild to moderate side effects. Many adverse events are attributable to procedural complications (i.e., secondary to the surgery itself), but cough and hoarseness are well recognized adverse effects of device activation. In epilepsy, these effects are generally well tolerated by patients and do not limit treatment compliance.53 Large-scale placebo-controlled trials are now required to definitively address the therapeutic efficacy of this treatment strategy.
GTS-21로 치료한 CIA 마우스의 활막에서는 류마티스 관절염(RA)에서 병인성으로 알려진 상대적으로 특이적인 수지상 세포(DC) 표지자인 CD11c의 발현이 현저히 감소하였다.43 이에 대한 한 가지 가능한 기전은 GTS-21이 in vitro에서 조상 세포로부터 골수 유래 DC의 분화를 억제했으며, 이 분화는 MLA에 의해 억제되었다는 점이다.43
니코틴 처리는 활막 내 Th17 세포 수치를 낮추는데, 이는 CD4+ 림프구 하위 집합으로 IL-17a 분비를 통해 RA에서 염증을 촉진하는 것으로 여겨진다.45 α7nAChR KO는 관절 파괴 증가, 혈청 내 TNF-α 및 케모카인 MCP-1 수치 증가, 그리고 염증성 사이토카인 생성 Th1 세포 대 IL-10 생성 Th2 세포 비율의 상승으로 이어진다.46
종합하면, 이러한 연구들은 α7nAChR이 RA에 대해 항염증 및 잠재적 질병 수정 효과를 지닌다는 것을 입증한다. 이러한 수용체를 발현하는 대식세포, 섬유아세포, T 세포, B 세포 등 다양한 세포들이 RA 환자의 활막에서 발견된다.47 다만 이러한 세포의 침윤이 실제로 아세틸콜린(ACh)에 의해 직접 자극되는지, 아니면 대식세포 활성화 및 사이토카인 방출 하류의 α7nAChR 독립적 기전에 의해 유발되는지, 또는 α7nAChR 발현이 순수하게 염증 세포 활성화의 이차적 표지자인지는 아직 규명되지 않았다.
미주신경은 RA와 관련이 있는 것으로 알려져 있다. 항원유발 관절염 마우스 모델에서 미주신경절제술은 활막 내 호중구 침윤 증가 및 통각과민과 연관되었다.21 두 연구에서 미주신경절제술의 질병 악화 효과가 α7nAChR 자극에 의해 완화된다는 것이 입증되었다.42, 48 이러한 효과는 통계적 유의성에 근접하는 경향만을 보였으나, 해당 연구들은 일측성 미주신경절제술만을 사용했기 때문에, 반대측 신경의 보상 작용으로 인해 다른 질환 모델에서 관찰된 양측성 미주신경절제술보다 효과가 더 미미할 수 있다.20 또한, VNS는 최소 두 건의 연구에서 CIA 치료에 효능을 입증했는데, 하나는 전기 자극을49, 다른 하나는 기계적 자극을 사용한 연구였다. 50 종합하면, 이 연구들은 VNS가 관절 염증 및 파괴49,50과 염증성 사이토카인 방출을 억제함을 보여준다.50 이러한 연구 결과는 RA 환자를 대상으로 한 VNS 임상 시험으로 이어졌다.51 18명의 RA 환자에게 VNS를 이식한 결과, 국제적으로 검증된 질병 활동 점수-28(DAS28)로 측정했을 때 질병 중증도가 급속히 개선되었다. 이 DAS는 의료 전문가가 28개의 특정 관절을 평가하고, 환자가 직접 보고한 건강 및 웰빙 점수와 혈액 전신 염증 마커(예: ESR 또는 CRP)의 입력값을 결합하여 도출됩니다. 또한, 전신성 염증 상태를 측정하는 지표인 리포폴리사카라이드(LPS) 전혈 배양에서 TNF-α 방출의 상응하는 감소가 관찰되었는데, 이는 참가자의 혈액 샘플을 ex vivo에서 염증 유발 물질에 노출시킨 결과입니다. VNS를 2주간 중단했을 때 증상이 재발했지만, 자극기를 재가동하자 다시 한번 증상이 완화되었습니다. 최근 위약 대조 파일럿 연구에서 류마티스 관절염 환자를 대상으로 이식형 VNS 장치의 안전성을 평가했으나 임상적 효능을 평가하기에는 통계적 검정력이 부족했습니다. 그러나 치료군 10명 중 5명(맹검 7명, 비맹검 3명)이 위약군 4명 중 0명 대비 임상적으로 유의미한 질환 중증도 점수 변화를 보였다는 점은 주목할 만하다.52 두 연구 모두 중대한 이상반응은 보고되지 않았으나, 높은 비율(전자의 경우 89%,51 후자의 경우 57%; 52 치료군 60%, 대조군 50%)가 경증에서 중등도의 부작용을 보고했다. 많은 부작용은 시술 관련 합병증(즉, 수술 자체에 기인)에 기인하지만, 기기 활성화 시 발생하는 기침과 쉰 목소리는 잘 알려진 부작용이다. 간질 환자의 경우 이러한 부작용은 일반적으로 잘 견디며 치료 순응도를 제한하지 않습니다.53 이 치료 전략의 치료 효능을 명확히 입증하기 위해서는 대규모 위약 대조 임상시험이 필요합니다.
Gastrointestinal disease
Inflammatory bowel disease (IBD) encompasses ulcerative colitis (UC) and Crohn’s disease (CD), disorders characterized by inflammation of the gastrointestinal tract (GIT). This inflammation is largely mediated by the activation of macrophages and cytokine pathways including TNF-α. The emergence of anti-TNF biologic therapies has transformed the treatment of IBD, particularly CD,54 but neither are without risk nor universally effective. Heart-rate variability (HRV) is reduced in IBD,55,56 implying a disruption of vagal tone, which, as discussed in the introduction, can be associated with greater inflammatory activity and represents an attractive target for new therapies.
Evidence for the importance of the inflammatory reflex in IBD comes from in vivo studies. α7nAChR KO mice demonstrate more severe responses to dextran sulfate sodium (DSS)-induced colitis, with more severe symptoms, higher disease activity scores, higher tissue and serum levels of cytokines (IL-1β, IL-6, IL-18, and TNF-α), and higher mortality rates,38,57 though not all studies confirm this finding.58 α7nAChR-selective agonist PNU28298759 and partial agonist encenicline60 (the effects of which are significantly attenuated by MLA) inhibit the development of DSS-induced colitis, reflected by less histological damage,59,60 less macrophage infiltration,59,60 and lower tissue levels of cytokines.59 Of note, other studies have found α7nAChR activation to be ineffective once DSS-induced colitis is established (i.e., if agonists are administered three days after DSS).60,61 Similar benefits to α7nAChR agonism have been demonstrated in 2,4,6-trinitrobenzene sulfonic acid (TNBS)-induced colitis, a model considered more representative of CD than UC.60,62 However, an earlier study found two agonists (AR-R17779 and GSK1345038A) to be ineffective in TNBS- and DSS-colitis; low doses were paradoxically harmful whereas high doses were protective.63 The authors theorized that higher agonist doses might have α7nAChR-independent effects. This hypothesis requires replication and further investigation.
Vagotomy was found to be associated with a 50% greater risk of IBD in a recent epidemiological study including over 15,000 vagotomized patients and more than 600,000 age-matched controls.64 A series of comprehensive experiments by one research group further demonstrated this phenomenon. Galantamine, an acetylcholinesterase inhibitor (AChEI), has demonstrated promising results in preventing the induction of TNBS-65 and DSS-induced colitis,66 an effect mediated by central muscarinic (mAChR) activation of the CAP65 and dependent on the vagus nerve and α7nAChR. Vagotomy leads to an increase in colitis severity and tissue cytokine levels in mouse models of DSS- and dinitrobenzene sulfonic acid (DNBS)-induced colitis.22 Similar effects were seen following splenic denervation and splenectomy.66 However, VNS, which has demonstrated efficacy in models of IBD,67 has also been shown to reduce bowel inflammation independently of splenic innervation, and instead via cholinergic stimulation of α7nAChR-expressing resident macrophages in the gut.68 This pathway has recently been termed the “enteric-CAP.”69 Thus, the vagus nerve once again appears key to the α7nAChR-mediated effects in IBD. Further research has suggested that the vagus nerve is capable of inducing α7nAChR-independent anti-colitic effects, such as by the recruitment of regulatory T cells (Tregs).58
To date, there have been few published clinical trials of cholinergic agonists in IBD. Studies have shown that transdermal nicotine provides clinically meaningful benefits as an adjuvant therapy in active UC.1 These trials were based on the hypothesis that nicotine is the causative agent behind the inverse relationship between smoking and UC risk and predate discovery of the CAP. The effect of nicotine on UC remains unexplained, and while it is tempting to imagine a mechanistic role for the α7nAChR between nicotine and UC, such a hypothesis would require further and more specific investigation. It is also important to note that smoking has the opposite relationship with CD, and some have even proposed that nicotine may be responsible for this effect via immunomodulatory mechanisms, though this lacks convincing evidence.70 Semapimod (a.k.a. CNI-1493), a small molecule that centrally activates the CAP,7 failed to reduce severity in CD patients over placebo after three doses. It did demonstrate intra-patient improvements after repeated dosing in an open-label continuation trial, but a high rate of infusion site reactions limited its tolerability.71 Large-scale trials are required to more accurately define responders while limiting systemic side effects in this patient population.
Because such off-site effects may prevent the delivery of α7nAChR agonists at the doses required for clinical benefit, efforts have therefore been made to target the CAP more directly using VNS. Two small open-label trials,72 one published in abstract form only,73 have trialed VNS in a total of 23 CD patients, reporting clinically meaningful improvements in clinical and endoscopic disease scores. However, a relatively high number (9–11) of cases experienced worsening of disease. Again, more substantive clinical trial data is required to evaluate the efficacy and safety of VNS in IBD.
위장관 질환
염증성 장질환(IBD)은 궤양성 대장염(UC)과 크론병(CD)을 포함하며, 위장관(GIT)의 염증이 특징인 질환이다. 이 염증은 주로 대식세포와 TNF-α를 포함한 사이토카인 경로의 활성화에 의해 매개된다. 항-TNF 생물학적 치료제의 출현은 IBD, 특히 CD의 치료를 변화시켰으나,54 어느 것도 위험이 없거나 보편적으로 효과적인 것은 아니다. IBD에서는 심박 변이도(HRV)가 감소하며,55,56 이는 미주신경 긴장도의 교란을 시사한다. 이는 서론에서 논의된 바와 같이 더 큰 염증 활동과 연관될 수 있으며, 새로운 치료법의 매력적인 표적이 된다.
IBD에서 염증 반사의 중요성에 대한 증거는 생체 내 연구에서 비롯된다. α7nAChR KO 마우스는 황산덱스트란 나트륨(DSS) 유발 대장염에 대해 더 심각한 반응을 보이며, 더 심한 증상, 더 높은 질병 활동 점수, 더 높은 조직 및 혈청 사이토카인 수치(IL-1β, IL-6, IL-18 및 TNF-α), 그리고 더 높은 사망률을 나타낸다.38,57 비록 모든 연구가 이 결과를 확인하는 것은 아니다.58 α7nAChR 선택적 작용제 PNU28298759 및 부분 작용제 엔세니클린60(MLA에 의해 그 효과가 현저히 약화됨)은 조직학적 손상 감소,59,60 대식세포 침윤 감소,59,60 및 사이토카인 조직 농도 저하로 반영되는 DSS 유발 대장염의 발병을 억제한다. 59 주목할 점은, 다른 연구들에서는 DSS 유발성 대장염이 일단 확립된 후(즉, DSS 투여 3일 후에 작용제를 투여하는 경우) α7nAChR 활성화가 효과가 없음을 발견했다.60,61 α7nAChR 작용과 유사한 이점은 2,4,6-트리니트로벤젠 설폰산(TNBS) 유발성 대장염에서도 입증되었으며, UC보다 CD를 더 대표적으로 반영하는 모델로 간주됩니다.60,62 그러나 이전 연구에서는 두 가지 작용제(AR-R17779 및 GSK1345038A)가 TNBS 및 DSS 대장염에서 효과가 없음을 발견했습니다. 저용량은 역설적으로 해로운 반면 고용량은 보호 효과가 있었습니다.63 저자들은 더 높은 작용제 용량이 α7nAChR 독립적 효과를 가질 수 있다고 이론화했습니다. 이 가설은 재현 및 추가 연구가 필요하다.
최근 15,000명 이상의 미주신경절제술 환자와 600,000명 이상의 연령대별 대조군을 포함한 역학 연구에서 미주신경절제술이 IBD 발병 위험을 50% 증가시키는 것으로 나타났다.64 한 연구 그룹의 일련의 포괄적 실험에서도 이 현상이 추가로 입증되었다. 아세틸콜린에스테라제 억제제(AChEI)인 갈란타민은 TNBS65 및 DSS 유발 대장염 예방에 유망한 결과를 보였으며,66 이 효과는 중추성 무스카린성 아세틸콜린 수용체(mAChR)에 의한 CAP65 활성화에 의해 매개되며, 미주신경과 α7nAChR에 의존한다. 미주신경절제술은 DSS 및 디니트로벤젠설폰산(DNBS) 유발 대장염 마우스 모델에서 대장염 중증도와 조직 사이토카인 수치를 증가시켰다.22 비장 신경절제술 및 비장 적출 후에도 유사한 효과가 관찰되었다.66 그러나 IBD 모델에서 효능이 입증된 VNS는67 비장 신경 분포와 무관하게 장 염증을 감소시키는 것으로 나타났으며, 대신 장 내 α7nAChR 발현 상주 대식세포에 대한 콜린성 자극을 통해 작용한다.68 이 경로는 최근 “장-CAP(enteric-CAP)”로 명명되었다. 69 따라서 미주신경은 IBD에서 α7nAChR 매개 효과의 핵심으로 다시 한번 부각된다. 추가 연구에 따르면 미주신경은 조절 T 세포(Tregs)의 동원과 같은 α7nAChR 독립적 항대장염 효과를 유도할 수 있다.58
현재까지 IBD에서 콜린성 작용제에 대한 임상 시험은 거의 발표되지 않았다. 연구에 따르면 경피적 니코틴은 활동성 UC의 보조 치료제로 임상적으로 의미 있는 이점을 제공한다.1 이러한 시험은 니코틴이 흡연과 UC 위험 사이의 역관계의 원인 물질이라는 가설에 기반했으며, CAP 발견 이전에 수행되었다. 니코틴이 UC에 미치는 효과는 아직 설명되지 않았으며, 니코틴과 UC 사이에서 α7nAChR의 기전적 역할을 상상하기 쉽지만, 이러한 가설은 더 구체적인 추가 연구가 필요하다. 또한 흡연은 크론병(CD)과는 반대 관계를 보이며, 일부에서는 니코틴이 면역조절 기전을 통해 이러한 효과를 유발할 수 있다고 제안하기도 했으나, 이를 뒷받침할 만한 설득력 있는 증거는 부족하다.70 중추적으로 CAP를 활성화하는 소분자인 세마피모드(Semapimod, 일명 CNI-1493)는7 위약 대비 크론병 환자의 중증도 감소에 실패했다. 개방형 지속 시험에서 반복 투여 후 환자 내 개선은 확인되었으나, 높은 주입 부위 반응률로 내약성이 제한되었다.71 이 환자 집단에서 전신 부작용을 제한하면서 반응자를 더 정확히 정의하기 위해서는 대규모 시험이 필요하다.
이러한 비표적 효과로 인해 임상적 이점에 필요한 용량의 α7nAChR 작용제 전달이 방해될 수 있으므로, VNS를 통해 CAP를 보다 직접적으로 표적화하려는 노력이 이루어져 왔다. 두 건의 소규모 공개 시험(72, 하나는 초록 형태로만 발표됨73)에서 총 23명의 크론병 환자를 대상으로 VNS를 시험한 결과, 임상 및 내시경적 질환 점수에서 임상적으로 의미 있는 개선이 보고되었다. 그러나 상대적으로 많은 수(9~11건)의 사례에서 질환 악화가 관찰되었다. 다시 한번, IBD에서 VNS의 효능과 안전성을 평가하기 위해서는 보다 실질적인 임상 시험 데이터가 필요하다.
Lung disease
In a mouse model of acid-induced acute lung injury,74 markers of inflammation, including excess lung water, lung vascular permeability, and bronchoalveolar lavage levels of leukocytes, were significantly reduced by the administration of nicotine, choline, and α7nAChR-selective agonist PNU-282987. These acid-induced effects were enhanced in α7nAChR KO mice. Leukocytes expressed higher cytoplasmic levels of NF-κB, and this effect was abrogated by treatment with nicotine. Vagotomy exacerbates the inflammatory response in animal models of ventilator-induced lung injury (VILI).20 Stimulation of the inflammatory reflex using α7nAChR agonists20,74,75 or VNS20,75 mitigated these inflammatory responses. α7nAChR agonist GTS-21 proved effective in reducing both organ injury and inflammatory markers in radiation-induced lung injury.76 Recently, neostigmine, an AChEI, demonstrated efficacy in a model of allergic asthma. This effect was associated with an increased expression of α7nAChR in the lungs.77
These studies present a strong case for the role of the CAP in lung inflammation and justify further study of the vagus nerve and its effects in the lungs. However, the relationship between the vagus nerve and the lungs may be more complex than that seen in inflammatory diseases of other organs. Activation of mAChR has bronchoconstrictive and possibly pro-inflammatory effects in the lungs.78 The use of beta-adrenergic agonism and muscarinic antagonism in the symptomatic treatment of COPD and asthma is based on this very concept. On the other hand, activation of other α7nAChR+ airway mucosa cells (e.g., type 2 innate lymphoid cells [ILC2s] and pulmonary neuroendocrine cells [PNECs]) downregulates the production of pro-inflammatory cytokines.79 It is possible that vagal release of ACh, which is capable of activating not only the α7nAChR but also other ACh receptors, in the airway mucosa could activate both pro- and anti-inflammatory processes. There are therefore two important clinical questions: how do these two pathways behave together in vivo, and does the balance tip toward a pro- or anti-inflammatory endpoint when there is an increase in vagal tone?
One study found that VNS inhibited LPS-induced TNF production in cardiac and hepatic tissues, but not in the lungs.80 However, other studies20,75 have found VNS to be protective against VILI and to impair anti-inflammatory processes in the lungs including IL-6 release.20 So, while evidence is variable, there is an increasing body of work supporting the hypothesis that vagus nerve activity mitigates inflammation in the lungs as it does in other organs, though whether this effect results solely from the spleen-mediated CAP or is also influenced by direct parasympathetic innervation of the airways warrants further investigation.
α7nAChR are expressed by various cells within lung mucosa.81 The downstream effects of α7nAChR activation in lung tissue are heterogeneous, complex, and remain to be fully elucidated but are important to consider when targeting the α7nAChR for therapeutic purposes. It has been postulated on the basis of in vitro studies and some animal models that α7nAChR activation may increase the metastatic potential of lung cancers81 and fibrogenesis in pulmonary fibrosis.80,82 However, these hypotheses lack clinical evidence to date. In fact, vagotomy has associated with a higher risk of lung and other cancers in pre-clinical and human epidemiological studies.79 Therefore, the CAP may actually have anti-cancer properties.
While there are some conflicting studies and unanswered questions, the trend of available evidence indicates that the CAP has therapeutic potential in lung disease, warranting further pre-clinical and clinical study. Other inflammatory lung diseases such as sarcoidosis, in which TNF-α-release from macrophages is central to the pathogenesis,83 also present tempting targets for future interventions.
폐 질환
산 유발 급성 폐 손상 마우스 모델에서,74 니코틴, 콜린 및 α7nAChR 선택적 작용제 PNU-282987 투여 시 과다 폐수, 폐 혈관 투과성, 기관지폐포 세척액 백혈구 수치 등 염증 지표가 유의하게 감소하였다. 이러한 산 유발 효과는 α7nAChR KO 마우스에서 증폭되었다. 백혈구는 세포질 내 NF-κB 발현 수준이 증가했으며, 이 효과는 니코틴 치료로 소멸되었다. 미주신경절제술은 인공호흡기 유발 폐 손상(VILI) 동물 모델에서 염증 반응을 악화시킨다.20 α7nAChR 작용제20,74,75 또는 VNS20,75를 이용한 염증 반사 자극은 이러한 염증 반응을 완화시켰다. α7nAChR 작용제 GTS-21은 방사선 유발 폐 손상에서 장기 손상과 염증 표지자 모두를 감소시키는 데 효과적임이 입증되었다.76 최근, AChEI인 네오스티그민이 알레르기성 천식 모델에서 효능을 보였다. 이 효과는 폐에서 α7nAChR 발현 증가와 연관되었다.77
이러한 연구들은 폐 염증에서 CAP의 역할을 강력히 입증하며, 미주신경과 그 폐 내 효과에 대한 추가 연구의 필요성을 정당화한다. 그러나 미주신경과 폐의 관계는 다른 장기 염증 질환에서 관찰되는 것보다 더 복잡할 수 있다. mAChR 활성화는 폐에서 기관지 수축 및 잠재적 염증 촉진 효과를 나타낸다.78 COPD 및 천식의 증상 치료에 베타-아드레날린성 작용제와 무스카린성 길항제를 사용하는 것은 바로 이 개념에 기반한다. 반면, 다른 α7nAChR+ 기도 점막 세포(예: 제2형 선천성 림프구[ILC2] 및 폐 신경내분비 세포[PNEC])의 활성화는 염증 촉진성 사이토카인의 생성을 하향 조절한다. 79 기도 점막에서 α7nAChR뿐만 아니라 다른 아세틸콜린 수용체도 활성화할 수 있는 미주신경의 아세틸콜린(ACh) 방출은 염증 촉진 및 억제 과정 모두를 활성화할 가능성이 있습니다. 따라서 두 가지 중요한 임상적 질문이 제기됩니다: 이 두 경로는 생체 내에서 어떻게 함께 작용하는가? 그리고 미주신경 긴장도가 증가할 때 균형이 염증 촉진 또는 억제 결과로 기울어지는가?
한 연구에서는 VNS가 심장 및 간 조직에서 LPS 유발 TNF 생성을 억제했지만 폐에서는 그렇지 않다는 사실을 발견했습니다.80 그러나 다른 연구들20,75에서는 VNS가 VILI에 대해 보호 효과가 있으며 IL-6 방출을 포함한 폐의 항염증 과정을 저해한다는 사실을 발견했습니다.20 따라서 증거가 다양하지만, 미주신경 활동이 다른 장기에서와 마찬가지로 폐의 염증을 완화한다는 가설을 지지하는 연구가 점차 늘어나고 있다. 다만 이 효과가 비장 매개 CAP(항염증성 조절 경로)에서만 비롯되는지, 아니면 기도 직접 부교감 신경 분포의 영향도 받는지는 추가 연구가 필요하다.
α7nAChR은 폐 점막 내 다양한 세포에 발현된다.81 폐 조직에서 α7nAChR 활성화의 하류 효과는 이질적이고 복잡하며 완전히 규명되지는 않았으나, 치료 목적으로 α7nAChR을 표적할 때 고려해야 할 중요한 요소이다. 체외 연구 및 일부 동물 모델을 바탕으로 α7nAChR 활성화가 폐암의 전이 가능성81 및 폐섬유증에서의 섬유생성을 증가시킬 수 있다는 가설이 제기되었다.80,82 그러나 이러한 가설들은 현재까지 임상적 증거가 부족하다. 실제로, 전임상 및 인간 역학 연구에서 미주신경절제술은 폐암 및 기타 암의 위험 증가와 연관되었다.79 따라서 CAP는 실제로 항암 특성을 가질 수 있다.
일부 상충되는 연구와 미해결 질문이 존재하지만, 현재 이용 가능한 증거의 추세는 CAP가 폐 질환 치료에 잠재력을 지니며 추가적인 전임상 및 임상 연구가 필요함을 시사한다. 대식세포에서 TNF-α 방출이 병인에 핵심적인 역할을 하는 사르코이드증과 같은 다른 염증성 폐 질환들83 역시 향후 치료 개입을 위한 유망한 표적이 될 수 있다.
CNS disease
Underlying inflammation forms the basis for the pathogenesis of many CNS diseases. These include not only the classic “inflammatory” disorders such as encephalitis and multiple sclerosis (MS), but also degenerative diseases such as Alzheimer’s disease (AD) and Parkinson’s disease (PD) and psychiatric disorders including depression and schizophrenia. The CNS immune system, which was once considered immune-privileged, operates somewhat independently, but not totally isolated, from the peripheral system. The BBB, under normal physiological conditions, limits the influence of peripheral immune cells on the CNS. A specialized subset of macrophages known as microglia govern innate immunity.84 The α7nAChR appears to play an important role in modulating the neuroinflammatory response in CNS diseases; the clinical use of VNS in epilepsy and depression are therapeutic examples of this. However, as we will demonstrate, the intricacies of the CNS immune system add an extra layer of complexity to its relationship with the CAP.
ACh is a ubiquitous and multifunctional neurotransmitter of the CNS, and α7nAChR are expressed abundantly on neuronal and non-neuronal cells, including microglia, astrocytes (CNS glial cells), BBB endothelial cells, and oligodendrocyte precursors (responsible for myelin production).85 Microglia mediate inflammatory processes through the release of TNF-α, amongst other mechanisms, and are sensitive to the anti-inflammatory effects of α7nAChR activation,85 presenting a suitable target for the CAP.
The risk of AD correlates with genetic variation in the α7nAChR.86 α7nAChR KO mice exhibit enhanced depression-type behaviors,87 and in a transgenic model of AD, experience fewer deficits and less neurodegeneration.88 In an ischemic stroke model, α7nAChR KO confers smaller infarct size with corresponding preservation of neurological function.89 One study found that α7nAChR KO was protective against experimental autoimmune encephalomyelitis (EAE),90 the gold-standard rodent model of MS. Two other studies found that KO did not alter the EAE phenotype.91,92 Though all three found that nicotine was protective against EAE, α7nAChR KO attenuated this protection.90, 91, 92 The reason proposed for this discrepancy was that α7nAChR activation not only mediates the migration and activation of pathogenic Th1 and Th17 cells in EAE, but also the actions of antigen-presenting cells (APCs) within the CNS, which are necessary to trigger EAE.90 Other research suggests that nicotine confers some of its anti-inflammatory effects through other nicotinic-receptor subtypes,91 including α9nAChR.90,93 Nevertheless, PNU-282987 has demonstrated clinical efficacy in EAE, improving clinical severity scores, reducing leukocyte infiltration into the CNS, and reducing mRNA expression of IL-6, IL-1β, IL-18, and TNF-α while also inducing autophagy by microglia and splenic macrophages. Thus, while α7nAChR may have a number of heterogeneous and possibly opposing functions, therapeutic strategies targeting the receptor are likely to be neuroprotective in EAE based on current evidence.
Pharmacological α7nAChR activation has also demonstrated therapeutic potential in models of other CNS disorders including AD,94 PD,95 schizophrenia,96 ischemic stroke,97 intracerebral haemorrhage,98 LPS-induced anxiety and depression,99 traumatic brain injury (TBI),100 and cardiopulmonary bypass-induced brain injury.101 AChEIs are licensed for use in improving cognition in AD. Historically, clinical efficacy of AChEIs was thought to be mediated via increasing synaptic concentrations of ACh and thus compensating for the loss of cholinergic neurons. However, it now appears likely that at least some of the clinical benefit is conferred through its anti-inflammatory effect.102 That being said, at least three α7nAChR-selective agonists have been studied in clinical trials of human AD patients, but none have progressed past stage two, either because of adverse effects, insufficient clinical benefit, or without explanation.103
The only diseases in which VNS is currently licensed for clinical use are epilepsy, depression, and headache, fundamentally CNS disorders. There is emerging clinical evidence for efficacy in other CNS disorders including AD53 and stroke.104 VNS has proven to be very efficacious in reducing seizure frequency in treatment-refractory epilepsy,105 though its mechanism of action is not understood. It was first used in epilepsy over 30 years ago, long predating characterization of the CAP, and was thought to directly inhibit the electrical activity of partial seizures. Soon thereafter, research showed that chronic intermittent stimulation induced long-term neural network changes, reducing seizure frequency.106
VNS demonstrates disease-modifying effects in pre-clinical models of schizophrenia by restoring normal neuronal activity and by reversing the hypersensitive amphetamine psychomotor response.107 It has been shown to enhance the rate of recovery after established ischaemic108 and haemorrhagic109 stroke. These effects might be seen as neuroplastic rather than neuroprotective. Cholinergic circuits and microglia are believed to have important neuroplastic properties.110 It is not clear from these studies that VNS exerts its effect through anti-inflammatory mechanisms or via the α7nAChR. One might expect that CNS inflammation would activate intrinsic cholinergic circuits and directly modulate inflammation without the unnecessary steps of involving the vagus nerve and spleen. Certainly, microglia appear susceptible to intrinsic cholinergic circuits with anti-inflammatory and neuroprotective effects.109 However, there is evidence to support a role for VNS in neuroinflammation and that CAP suppression of systemic inflammation could mediate this.
VNS reduces CNS levels of inflammatory cytokines and other biomarkers in models of systemic endotoxaemia.110,111 In the context of addressing was that this observed VNS anti-inflammatory activity a peripheral response, investigators have shown that this anti-inflammatory CNS effect is inhibited in vagotomized mice, supporting the role of the efferent vagus mediating these effects on neuroinflammation.112 Supporting this hypothesis, splenectomy impaired the anti-inflammatory effects of α7nAChR-agonism in TBI.100 Again, this may not be the most suitable model for organ-specific neuroinflammation, as TBI is accompanied by a systemic inflammatory response and translocation of peripheral immune cells across the disrupted BBB.100 Systemic inflammation is associated with deleterious effects in most neurodegenerative disorders.112 So, it is plausible that VNS would have neuroprotective effects mediated via the efferent nerve.
중추신경계 질환
기저 염증은 많은 중추신경계 질환의 병인학적 기초를 형성합니다. 여기에는 뇌염 및 다발성 경화증(MS)과 같은 고전적인 “염증성” 장애뿐만 아니라 알츠하이머병(AD) 및 파킨슨병(PD)과 같은 퇴행성 질환, 그리고 우울증 및 정신분열증을 포함한 정신 질환도 포함됩니다. 한때 면역 특권 영역으로 여겨졌던 중추신경계 면역 체계는 말초 시스템과 완전히 격리되지는 않았지만 어느 정도 독립적으로 작동한다. 정상 생리 조건에서 혈뇌 장벽(BBB)은 말초 면역 세포가 중추신경계에 미치는 영향을 제한한다. 미세아교세포로 알려진 대식세포의 특수 하위 집합이 선천성 면역을 관장한다.84 α7nAChR은 중추신경계 질환에서 신경염증 반응 조절에 중요한 역할을 하는 것으로 보인다; 간질 및 우울증에 대한 VNS의 임상적 사용이 이에 대한 치료적 사례이다. 그러나 우리가 보여줄 것처럼, 중추신경계 면역계의 복잡성은 CAP와의 관계에 추가적인 복잡성을 더한다.
아세틸콜린(ACh)은 중추신경계의 보편적이며 다기능적인 신경전달물질이며, α7nAChR은 미세아교세포, 성상세포(중추신경계 신경교세포), 혈뇌장벽 내피세포, 그리고 (미엘린 생성을 담당).85 미세아교세포는 TNF-α 방출 등 다양한 기전을 통해 염증 과정을 매개하며, α7nAChR 활성화의 항염증 효과에 민감하게 반응하여85 CAP의 적합한 표적이 됩니다.
알츠하이머병(AD)의 발병 위험은 α7nAChR의 유전적 변이와 상관관계가 있습니다.86 α7nAChR KO 마우스는 우울증 유형 행동이 증가하는 것으로 나타났으며,87 AD 트랜스제닉 모델에서는 기능 저하와 신경퇴행이 덜 발생하는 것으로 관찰되었습니다. 88 허혈성 뇌졸중 모델에서 α7nAChR KO는 신경학적 기능 보존과 함께 더 작은 경색 크기를 나타냈다.89 한 연구는 α7nAChR KO가 다발성 경화증(MS)의 표준 실험 모델인 실험적 자가면역 뇌척수염(EAE)에 대해 보호 효과를 보인다는 것을 발견했다.90 다른 두 연구에서는 KO가 EAE 표현형을 변화시키지 않는다는 것을 발견했습니다.91,92 세 연구 모두 니코틴이 EAE에 대해 보호 효과가 있다는 것을 발견했지만, α7nAChR KO는 이러한 보호 효과를 약화시켰습니다.90, 91, 92 이러한 불일치에 대해 제안된 이유는 α7nAChR 활성화가 EAE에서 병원성 Th1 및 Th17 세포의 이동과 활성화를 매개할 뿐만 아니라 EAE 유발에 필수적인 중추신경계(CNS) 내 항원제시세포(APCs)의 작용도 조절하기 때문이라고 제안되었다.90 다른 연구에서는 니코틴이 α9nAChR을 포함한 다른 니코틴성 수용체 서브타입들을 통해 일부 항염증 효과를 발휘한다고 제안한다.91,90,93 그럼에도 불구하고, PNU-282987은 EAE에서 임상적 효능을 입증하여 임상 중증도 점수를 개선하고, 중추신경계로의 백혈구 침윤을 감소시키며, IL-6, IL-1β, IL-18 및 TNF-α의 mRNA 발현을 감소시키는 동시에 미세아교세포와 비장 대식세포에 의한 자가포식을 유도한다. 따라서 α7nAChR이 여러 가지 이질적이고 아마도 상반되는 기능을 가질 수 있지만, 현재 증거에 따르면 이 수용체를 표적으로 하는 치료 전략은 EAE에서 신경 보호 효과가 있을 가능성이 높습니다.
약리학적 α7nAChR 활성화는 또한 AD,94 PD,95 정신분열증,96 허혈성 뇌졸중,97 뇌내출혈,98 LPS 유발 불안 및 우울증,99 외상성 뇌손상(TBI),100 및 심폐 우회술 유발 뇌손상 등 다른 중추신경계 장애 모델에서도 치료 가능성을 입증했습니다. 101 아세틸콜린에스테라제 억제제(AChEIs)는 알츠하이머병(AD)에서 인지 기능 개선을 위해 사용이 허가되었습니다. 역사적으로 AChEIs의 임상적 효능은 아세틸콜린(ACh)의 시냅스 농도를 증가시켜 콜린성 신경세포 손실을 보상함으로써 매개되는 것으로 여겨졌습니다. 그러나 현재는 적어도 일부 임상적 이점이 항염증 효과를 통해 부여되는 것으로 보입니다.102 그럼에도 불구하고, 인간 AD 환자를 대상으로 한 임상 시험에서 적어도 세 가지의 α7nAChR 선택적 작용제가 연구되었으나, 부작용, 불충분한 임상적 이점 또는 설명되지 않은 이유로 인해 어느 것도 2상 이후로 진행되지 못했습니다.103
현재 VNS가 임상 사용 허가를 받은 유일한 질환은 간질, 우울증, 두통으로, 근본적으로 중추신경계(CNS) 장애입니다. AD53 및 뇌졸중을 포함한 다른 CNS 장애에 대한 효능에 대한 임상적 증거가 점차 나타나고 있습니다.104 VNS는 치료 저항성 간질에서 발작 빈도를 감소시키는 데 매우 효과적인 것으로 입증되었으나,105 그 작용 기전은 아직 명확히 이해되지 않았습니다. VNS는 30년 이상 전, CAP(경련성 발작의 특성)가 규명되기 훨씬 이전에 간질 치료에 처음 사용되었으며, 부분 발작의 전기적 활동을 직접 억제하는 것으로 여겨졌다. 이후 연구에서 만성 간헐적 자극이 장기적인 신경망 변화를 유도하여 발작 빈도를 감소시킨다는 사실이 밝혀졌다.106
VNS는 정상적인 신경 세포 활동을 회복시키고 과민한 암페타민 정신운동 반응을 역전시킴으로써 정신분열증의 전임상 모델에서 질병 수정 효과를 나타낸다.107 또한, 이미 발생한 허혈성108 및 출혈성109 뇌졸중 후 회복 속도를 향상시키는 것으로 나타났다. 이러한 효과는 신경보호적이라기보다는 신경가소성으로 볼 수 있다. 콜린성 회로와 미세아교세포는 중요한 신경가소성 특성을 지닌 것으로 여겨진다.110 이러한 연구들로부터 VNS가 항염증 기전을 통해 또는 α7nAChR을 경유하여 효과를 발휘하는지는 명확하지 않다. 중추신경계 염증이 미주신경과 비장을 거치는 불필요한 단계를 거치지 않고 내재적 콜린성 회로를 활성화하여 염증을 직접 조절할 것이라고 예상할 수 있다. 확실히, 미세아교세포는 항염증 및 신경보호 효과를 지닌 내재적 콜린성 회로의 영향을 받는 것으로 보인다.109 그러나 VNS가 신경염증에서 역할을 한다는 증거가 있으며, 전신 염증의 CAP 억제가 이를 매개할 수 있다는 증거도 있다.
VNS는 전신성 내독소혈증 모델에서 중추신경계의 염증성 사이토카인 및 기타 바이오마커 수치를 감소시킵니다.110, 111 이 관찰된 VNS 항염증 활성이 말초 반응인지에 대한 논의에서, 연구자들은 이 항염증 중추신경계 효과가 미주신경 절제 마우스에서 억제됨을 보여주어, 신경염증에 대한 이러한 효과를 매개하는 미주신경 원심성 신경의 역할을 뒷받침하였습니다.112 이 가설을 지지하듯, 비장 절제술은 TBI에서 α7nAChR 작용제의 항염증 효과를 손상시켰습니다.100 다시 말해, 이는 장기 특이적 신경염증에 가장 적합한 모델이 아닐 수 있다. TBI는 전신성 염증 반응과 손상된 혈뇌장벽(BBB)을 통한 말초 면역 세포의 이동을 동반하기 때문이다.100 전신성 염증은 대부분의 신경퇴행성 질환에서 유해한 효과와 연관된다.112 따라서 VNS가 원심성 신경을 매개로 신경보호 효과를 가질 가능성이 있다.
Other systems
The cholinergic system, which is found in both neuronal and non-neuronal cells, mediates complex functions in all organs of the body. Therefore, it is plausible that manipulation of the CAP would have therapeutic potential in chronic inflammatory end-organ injury. In a comprehensive set of experiments, Inoue and colleagues23 illustrated the capabilities of the CAP in protecting the kidney from renal ischemia-reperfusion injury (IRI). VNS, when applied 24 or 48 h before ischemia, attenuated cytokine response and acute kidney injury. This effect was not seen in α7nAChR KO or splenectomized mice. The efferent vagus nerve does not innervate the kidney,113 and blocking of the sympathetic renal nerve actually prevented renal IRI,23 so VNS appears to exert its reno-protective effect indirectly through the spleen.
Deletion of the α7nAChR results in larger infarct size and greater inflammatory response in mice subjected to myocardial infarction.36 α7nAChR agonists114 and VNS115 have the opposite effect. A non-invasive form of transcutaneous VNS, discussed below and in Table 1, has demonstrated cardioprotective effects during acute myocardial infarction in a human randomized control trial (RCT).116 Unlike the kidney, the heart receives extensive parasympathetic input from the vagus nerve, though whether the cardioprotective effects of VNS are mediated via direct myocardial innervation, the splenic CAP, or both has not been investigated.
기타 시스템
콜린성 시스템은 신경 세포와 비신경 세포 모두에 존재하며, 신체 모든 장기의 복잡한 기능을 매개한다. 따라서 CAP(교감신경계) 조작이 만성 염증성 말초 장기 손상에 치료적 잠재력을 가질 수 있다는 가설은 타당하다. 포괄적인 실험 시리즈에서 이노우에와 동료들23은 신장 허혈-재관류 손상(IRI)으로부터 신장을 보호하는 CAP의 능력을 입증했다. 허혈 24시간 또는 48시간 전에 시행한 VNS는 사이토카인 반응과 급성 신장 손상을 완화시켰다. 이 효과는 α7nAChR KO 마우스나 비장 적출 마우스에서는 관찰되지 않았다. 원심성 미주신경은 신장을 신경 분포하지 않으며,113 교감 신장 신경 차단이 실제로 신장 IRI를 예방했기 때문에,23 VNS는 비장을 통해 간접적으로 신장 보호 효과를 발휘하는 것으로 보인다.
α7nAChR 결손은 심근경색을 유발한 쥐에서 더 큰 경색 크기와 더 강한 염증 반응을 초래한다.36 반면 α7nAChR 작용제114와 VNS115는 반대 효과를 보인다. 비침습적 경피적 VNS(아래 및 표 1 참조)는 인간 무작위 대조 시험(RCT)에서 급성 심근경색 시 심장 보호 효과를 입증하였다. (RCT).116 신장과 달리 심장은 미주신경으로부터 광범위한 부교감신경 입력을 받지만, VNS의 심장보호 효과가 직접적인 심근 신경 분포, 비장 CAP, 또는 둘 다를 통해 매개되는지는 아직 연구되지 않았다.
Table 1.
Clinical trials using electrical stimulation of the CAP
TreatmentPopulationReferenceFindings
| iVNS | rheumatoid arthritis | Koopman et al., 201652 | n = 18 RA patients were implanted with VNS and stimulated up to four times daily. Stimulation was associated with a reduction in disease activity (DAS28) and impaired TNF release on LPS-whole blood culture. These measures relapsed when stimulation was suspended for 14 days but improved again after reactivation. Clinical improvement was maintained at 84 days post-implantation. |
| Crohn’s disease | Sinniger et al.,74 2020 | n = 9 patients with active CD receiving azathioprine or no treatment were implanted with VNS. Over twelve months, five experienced improvement in symptomatic (CDAI) and six in endoscopic (CDEIS) measures of severity. Two experienced worsening of disease and were removed from the study. | |
| rheumatoid arthritis | Genovese et al., 202053 | n = 14 treatment-refractory RA patients. 3 received treatment in an open label pilot study. The remaining 10 were randomized to receive 1 min of stimulation daily (n = 3), four times daily (n = 4), or sham procedure (n = 4) using a novel design of VNS device. 5 of 10 actively treated subjects demonstrated clinical improvement versus no controls. There was a significant reduction in cytokine (IL-1β, IL-6, and TNF) response to LPS-whole blood culture in the treatment group. MRI features of RA did not improve. One case of transient Horner’s syndrome and another of transient vocal cord paralysis, amongst other adverse effects, were reported. | |
| TcVNS | healthy participants | Lerman et al., 2016117 | n = 20 (10 tcVNS and 10 sham controls, randomized). 3 courses of tcVNS over one day (2 min to each Vagus nerve per course) significantly reduced cytokine (TNF-α, IL-1β) and chemokine (MIP-1α, MCP-1, IL-8) response to LPS-whole blood culture compared to baseline and to controls. |
| healthy participants | Brock et al., 2016118 | n = 20 (internal controls). A single course of 120 s of tcVNS to each vagus nerve was sufficient to induce a small but significant reduction in circulating TNF-α levels, but no other cytokines, after 24 h. Blood samples were not challenged with LPS. | |
| Sjögren’s syndrome | Tarn et al., 2018119 | n = 15 female participants (internal controls). 3 weeks of twice daily tcVNS was associated with (1) improvement in fatigue score (n = 12/15), (2) reduced cytokines (TNF-α, IL-6, IL-1β, IP-10) and chemokine (MIP1α) response to LPS-whole blood culture, and (3) a transient rise in circulating T cells, NK cells, and NKT cells after first administration only. | |
| rheumatoid arthritis | Drewes et al., 2020120 | n = 36, 16 with active RA and 20 with low activity RA. 120 s of tVNS three times daily for four days was associated with a significant reduction in DAS28-CRP and IFN-γ in non-stimulated blood (but not other cytokines) in the active group only. There was also a statistically significant reduction in blood pressure in this group, possibly indicative of vagus nerve activity. Surprisingly, the low activity group actually experienced a reduction in cardiac vagal tone and in serum levels of IL-10. | |
| TaVNS | impaired glucose tolerance | Huang et al., 2014121 | n = 35 who received 12 weeks of taVNS experienced a reduction in fasting plasma glucose, 2-h plasma glucose, and Hba1c compared with n = 30 receiving no treatment in a parallel non-randomized observational study. However, a sham-placebo group (n = 35) experienced a similar reduction in 2-h plasma glucose and Hba1c. |
| acute STEMI and MIRI post-PCI | Yu et al., 2016122 | n = 95 (47 taVNS, 48 sham-controls, randomized). TaVNS was applied before and throughout percutaneous coronary intervention (PCI). Intervention group demonstrated (1) fewer arrhythmias, (2) more favorable echocardiographic features, and (3) lower levels of serum cardiac enzymes and cytokines (TNF-α, IL-6, IL-1β, HMGB-1). | |
| rheumatoid arthritis and healthy participants | Addorisio et al., 2019123 | Two days of twice-daily taVNS was associated with lower cytokine levels on LPS-whole blood assay in two separate studies (n = 9, TNF-α assay. n = 19 TNF, IL-1β, and IL-6 assays). n = 9 patients with RA experienced a significant reduction in disease activity (DAS28), sustained for at least one week after treatment. | |
| systemic lupus erythematosus | Aranow et al., 2021124 | n = 18 (12 taVNS and 6 controls) received 5 min of taVNS or sham procedure daily for four days in a double-blinded RCT. One subject was excluded and replaced due to a respiratory tract infection. 83.3% of taVNS participants experienced a meaningful reduction in subjective measurements of pain and fatigue at 12 days versus 16.7 and 0% of controls, respectively. However, improvements in objective measures by blinded physicians of disease activity were not statistically significant, nor were inflammatory markers or cytokine levels. |
iVNS, invasive VNS; taVNS, transauricular VNS; tcVNS, transcervical VNS; SLE, systemic lupus erythematosus.
Vagotomy has an exacerbating effect on models of pancreatitis.125 Stimulation of the CAP with α7nAChR agonists125 or centrally acting agents122 attenuates the disease process.
CAP의 전기적 자극을 이용한 임상 시험
치료 대상 인구 참고문헌 결과
iVNS 류마티스 관절염 Koopman et al., 201652 n = 18명의 RA 환자에게 VNS를 이식하고 하루 최대 4회 자극을 가했습니다. 자극은 질병 활동도(DAS28) 감소 및 LPS 전혈 배양 시 TNF 분비 저하와 연관되었다. 자극 중단 14일 후 이러한 지표들은 재발했으나 재개 후 다시 개선되었다. 임상적 개선은 이식 후 84일까지 유지되었다.
크론병 Sinniger et al.,74 2020 n = 9 아자티오프린 치료 또는 무치료를 받는 활동성 크론병 환자에게 VNS를 이식했다. 12개월 동안 5명은 증상(CDAI)이, 6명은 내시경적 중증도(CDEIS)가 개선되었다. 중증도 지표에서 개선을 보였다. 2명은 질환 악화를 경험하여 연구에서 제외되었다.
류마티스 관절염 Genovese 등,, 202053 치료 불응성 RA 환자 n = 14. 3명은 공개 라벨 파일럿 연구에서 치료를 받았다. 나머지 10명은 새로운 설계의 VNS 장치를 사용하여 매일 1분 자극(n = 3), 매일 4회 자극(n = 4), 또는 위장 시술(n = 4)을 받도록 무작위 배정되었다. 적극적으로 치료받은 10명 중 5명은 대조군 대비 임상적 개선을 보였다. 치료군에서 LPS 전혈 배양에 대한 사이토카인(IL-1β, IL-6, TNF) 반응이 유의하게 감소했다. 류마티스 관절염의 MRI 소견은 개선되지 않았다. 일시적 호너 증후군 1건과 일시적 성대 마비 1건을 포함한 기타 부작용이 보고되었다.
TcVNS 건강한 참가자 Lerman et al., 2016117 n = 20 (10 tcVNS 및 10 위약 대조군, 무작위 배정) . 하루 동안 3회 과정의 tcVNS(각 과정당 미주신경당 2분)는 대조군 및 기준치 대비 LPS 전혈 배양에 대한 사이토카인(TNF-α, IL-1β) 및 케모카인(MIP-1α, MCP-1, IL-8) 반응을 유의미하게 감소시켰다.
건강한 참가자 Brock et al., 2016118 n = 20 (내부 대조군). 각 미주신경에 120초 동안 tcVNS를 단일 과정으로 시행한 것만으로도 24시간 후 순환하는 TNF-α 수치를 작지만 유의미하게 감소시키는 데 충분했으나, 다른 사이토카인에는 영향을 미치지 않았다. 혈액 샘플은 LPS에 노출되지 않았다.
쇼그렌 증후군 Tarn et al., 2018119 n = 15명의 여성 참가자(내부 대조군). 3주간 하루 두 번 시행한 tcVNS는 (1) 피로 점수 개선(n = 12/15), (2) LPS 전혈 배양에 대한 사이토카인(TNF-α, IL-6, IL-1β, IP-10) 및 케모카인(MIP1α) 반응 감소, (3) 첫 번째 투여 후 일시적인 순환 T 세포, NK 세포 및 NKT 세포 증가와 연관되었다.
류마티스 관절염 Drewes et al., 2020120 명, 활동성 RA 16명, 저활동성 RA 20명. 4일간 하루 3회 120초 tVNS는 DAS28-CRP 및 비자극 혈액 내 IFN-γ의 유의한 감소를 동반함 (다른 사이토카인은 제외). 또한 이 그룹에서 혈압이 통계적으로 유의미하게 감소했으며, 이는 미주신경 활동의 가능성을 시사함. 놀랍게도, 저활동성 그룹은 실제로 심장 미주신경 긴장도와 혈청 IL-10 수치가 감소함.
TaVNS는 포도당 내성을 저하시켰다 Huang et al., 2014121명의 참가자가 12주 동안 taVNS를 받은 결과, 병행 비무작위 관찰 연구에서 치료를 받지 않은 30명의 참가자에 비해 공복 혈장 포도당, 2시간 혈장 포도당 및 Hba1c가 감소한 것으로 나타났습니다. 그러나 위약 대조군(n = 35)에서도 2시간 혈장 포도당과 HbA1c 수치가 유사하게 감소했습니다.
급성 STEMI 및 PCI 후 MIRI Yu et al., 2016122 n = 95 (47명 taVNS, 48명 위약 대조군, 무작위 배정). TaVNS는 경피적 관상동맥 중재술(PCI) 전과 중 적용되었습니다. 중재군은 (1) 부정맥 발생 감소, (2) 더 유리한 심초음파 소견, (3) 혈청 심장 효소 및 사이토카인(TNF-α, IL-6, IL-1β, HMGB-1) 수치 저하를 보였습니다.
류마티스 관절염 및 건강한 참가자 Addorisio et al., 2019123 두 건의 별도 연구에서, 2일 동안 하루 두 번 taVNS를 시행한 결과, LPS 전혈 검사에서 사이토카인 수치가 낮아진 것으로 나타났습니다 (n = 9, TNF-α 검사. n = 19 TNF, IL-1β 및 IL-6 검사). 류마티스 관절염 환자 n = 9명은 치료 후 최소 1주일 동안 지속된 질병 활동도(DAS28)의 유의미한 감소를 경험했습니다.
전신성 홍반성 루푸스 Aranow et al., 2021124 n = 18명(taVNS 12명, 대조군 6명)이 이중 맹검 RCT에서 4일 동안 매일 5분간의 taVNS 또는 위약 시술을 받았습니다. 호흡기 감염으로 인해 1명의 피험자가 제외되고 대체되었습니다. taVNS 참가자의 83.3%가 12일째 주관적 통증 및 피로 측정에서 의미 있는 감소를 경험한 반면, 대조군은 각각 16.7%와 0%였습니다. 그러나 맹검 의사가 평가한 객관적 질병 활동 지표의 개선은 통계적으로 유의하지 않았으며, 염증 표지자나 사이토카인 수치도 마찬가지였습니다.
iVNS, 침습적 VNS; taVNS, 경이적 VNS; tcVNS, 경경부 VNS; SLE, 전신성 홍반성 루푸스.
미주신경절제술은 췌장염 모델에서 악화 효과를 나타낸다.125 α7nAChR 작용제125 또는 중추 작용제122로 CAP를 자극하면 질병 진행이 완화된다.
Clinical applications and future directions
As the therapeutic potential of the CAP becomes increasingly realized in pre-clinical studies, efforts have begun to translate this work into new clinical therapies (see Figure 3).
Attempts at pharmacological stimulation of the CAP have had mixed success. As discussed above, an RCT of Semapimod in CD failed to meet its primary endpoint, and the medication was poorly tolerated.73 A pilot study of GTS-21 in 14 healthy volunteers failed to attenuate the inflammatory response in LPS-induced endotoxemia in vivo. The pharmacokinetics of GTS-21 were found to vary greatly between participants in this study. It is possible that insufficient doses were used and it is likely that the study was underpowered.126 On the other hand, an RCT of galantamine successfully reduced serum levels of TNF-α, increased levels of IL-10, and improved insulin resistance in patients with metabolic syndrome.127 α7nAChR and other AChR have extensive non-immune actions on other cell types. These actions could be responsible for some of these agents’ adverse effects, limiting their clinical use.
Bioelectronic therapies, which target the CAP more specifically, such as VNS, offer an attractive alternative to drug-based therapies modulating cellular α7nAChR expression. Pilot studies of invasive VNS (iVNS), which have shown promise in RA51,52 and IBD,72 are described above and in Table 1. As already discussed, VNS implantation is generally well tolerated but is not without adverse effects. Patients may be reluctant, or even physically unsuitable, to undergo implantation. Implantation may be impractical and unjustified in acute or monophasic illnesses which require urgent, but not long-term, intervention and therefore would be more suited to a temporary form of immunomodulation. In recognition of these limitations, but staying cognizant of the significant burden of chronic inflammatory diseases, the industry has expressed significant interest in developing non-invasive bioelectronic devices for these diseases.
The vagus nerve can be stimulated transcutaneously (tVNS) by placing an electrode over the cervical vagus nerve in the neck (transcervical VNS, tcVNS) or the auricular branch in the cymba concha of the external ear (transauricular VNS, taVNS). A device for the former is FDA approved for use in migraine, though efficacy was only demonstrated in a sub-group analysis of patients adherent to treatment,128 so patient concordance may limit the efficacy of such a treatment in practice. More recently, the FDA fast-tracked approval for tVNS use in treating respiratory symptoms of COVID-19.129 Stimulation of the afferent vagus nerve with taVNS activates vagal brainstem nuclei (see Figure 3).130,131 It is proposed that signals in these nuclei are, in turn, relayed to the efferent vagus nerve based on the observation that taVNS can have systemic autonomic effects. Certainly, both tcVNS and taVNS have demonstrated anti-inflammatory effects in an animal model of endotoxaemia.132 These effects were eliminated by both vagotomy and an α7nAChR antagonist, suggesting involvement of the CAP. TaVNS has also demonstrated anti-inflammatory and disease-modifying effects in models of post-operative ileus.130 Neuroprotective effects have been demonstrated in PD,133 post-operative cognitive dysfunction,134 and ischemic stroke.131 In more recent studies, such effects were associated with a reduction in intracerebral cytokine release and an upregulation of α7nAChR expression.133,134 Intracerebral upregulation of the α7nAChr has also been observed in response to PNU-282987 with apparent anxiolytic and anti-depressant effects.135
Table 1 summarizes the findings of human clinical trials aimed at harnessing the CAP using iVNS and tVNS. Several other tVNS trials not listed in Table 1 have been conducted,136 for example in conditions for which iVNS has already been approved (epilepsy and migraine) and in patients with other neurological conditions (e.g., depression and PD) where symptomatic improvement has been demonstrated. However, unlike the conditions listed in Table 1, the anti-inflammatory role of VNS in these neurological disorders remains less well defined and is not typically measured in trial outcomes, so the effects of tVNS may or may not be anti-inflammatory. One short, double-blinded pilot study in systemic lupus erythematosus (SLE) showed improvement in only subjective markers of disease but not in objective measures or inflammatory markers.137 However, the overall evidence from these studies, though small in size and number, supports a potential therapeutic benefit for both iVNS and tVNS across a range of inflammatory disorders, warranting larger RCTs.
Recently, an innovative method of stimulating the CAP using non-invasive pulsed ultrasound (pUS) was proposed.138 Administration of abdominal ultrasound was found to attenuate subsequent renal IRI in rats. This effect was dependent on functional CD4+ T cells139 and was not observed following splenectomy, KO or inhibition of the α7nAChR, or splenic denervation.124 Prevention of acute kidney injury (AKI) was associated with impaired inflammatory potential of splenic leukocytes and reduced levels of serum and renal cytokines including TNF-α and IL-6.124 It is believed that the pUS stimulates the CAP downstream of the vagus nerve in the spleen. Focusing pUS waves at the site of splenic nerve terminals stimulates the release of noradrenaline and ACh in a process dependent on ChAT+ CD4+ T cells and the α7nAChR.138 Splenic138,140,141 or abdominal142 pUS has proven effective in preventing the effects of endotoxaemia,138 prolonging survival in sepsis141 and reversing the effects of established inflammatory arthritis140 and DSS-colitis.142 pUS applied to the spleen or neck reduces infarct size 3-fold in myocardial ischemia-reperfusion injury exacerbated by hyperglycaemia.143 Focused pUS may also have anti-inflammatory uses at other sites. The afferent fibers of the vagus nerve be stimulated at the porta hepatis in the liver, modulating hypothalamic insulin sensitivity resulting in attenuation of hyperglycaemia138 with associated reduction in weight gain and an overall down-regulation of hepatic inflammation.69 Together, these results present a potential therapeutic role in modulating the CAP across a range of organ systems.
In addition to being non-invasive and apparently safe, a theoretical advantage to splenic pUS is that it avoids the non-CAP effects on other organs in which the vagus has been implicated, such as in the lungs.79,82 By the same token, however, limiting the CAP effects to those mediated by splenic macrophages could be less efficacious in conditions such as IBD, where vagal innervation of the GIT might play a role.68 The effects of pUS on DSS-colitis, administered non-specifically throughout the abdomen, were almost absent in splenectomized mice, aside from a mild improvement in bloody stool frequency and evidence of AChR+ cell recruitment in the mesenteric lymph node.142 Recently, however, pUS was shown to be effective in DSS-colitis by stimulating the CAP at the level of the celiac ganglion.144 Human clinical trials of pUS in inflammatory disease are now warranted to assess its therapeutic potential and answer these questions.
임상 적용 및 향후 방향
전임상 연구에서 CAP의 치료 잠재력이 점차 확인됨에 따라, 이 연구를 새로운 임상 치료법으로 전환하려는 노력이 시작되었다(그림 3 참조).
CAP의 약리학적 자극 시도는 혼합된 결과를 보였다. 앞서 논의된 바와 같이, CD에서 세마피모드(Semapimod)의 무작위 대조 시험(RCT)은 주요 평가 변수를 충족하지 못했으며, 약물 내약성이 좋지 않았다.73 14명의 건강한 지원자를 대상으로 한 GTS-21의 파일럿 연구는 생체 내(in vivo) LPS 유발 내독소혈증에서 염증 반응을 완화시키지 못했다. 이 연구에서 GTS-21의 약동학은 참가자 간에 크게 차이가 나는 것으로 나타났다. 충분하지 않은 용량이 사용되었을 가능성이 있으며, 연구의 검정력이 부족했을 가능성이 있다.126 반면, 갈란타민의 무작위 대조 시험(RCT)은 대사 증후군 환자에서 혈청 TNF-α 수치를 성공적으로 감소시키고, IL-10 수치를 증가시키며, 인슐린 저항성을 개선했습니다.127 α7nAChR 및 기타 AChR은 다른 세포 유형에 대해 광범위한 비면역 작용을 합니다. 이러한 작용은 일부 약제의 부작용을 유발하여 임상적 사용을 제한할 수 있습니다.
VNS와 같이 CAP를 보다 특이적으로 표적하는 생체전자 치료법은 세포 내 α7nAChR 발현을 조절하는 약물 기반 치료법에 대한 매력적인 대안을 제시한다. RA51,52 및 IBD72에서 유망한 결과를 보인 침습적 VNS(iVNS)의 파일럿 연구는 위와 표 1에 설명되어 있다. 앞서 논의한 바와 같이, VNS 이식은 일반적으로 내약성이 우수하나 부작용이 전혀 없는 것은 아니다. 환자는 이식 시술을 꺼리거나 신체적으로 적합하지 않을 수 있다. 시급한 개입이 필요하지만 장기적 치료가 필요하지 않은 급성 또는 단상성 질환의 경우 이식은 비실용적이며 정당화되기 어려우므로, 일시적인 형태의 면역조절이 더 적합할 수 있다. 이러한 한계를 인지하면서도 만성 염증성 질환의 중대한 부담을 고려하여, 업계는 이러한 질환을 위한 비침습적 생체전자 장치 개발에 상당한 관심을 표명해 왔다.
미주신경은 경부 미주신경(경부 미주신경자극, tcVNS)이나 외이도 귓바퀴의 귀지개(귀지개 미주신경, taVNS)에 전극을 부착하여 경피적으로 자극할 수 있습니다(경피적 미주신경자극, tVNS). 전자의 경우 편두통 치료용으로 FDA 승인을 받은 장치가 있지만, 그 효능은 치료를 준수한 환자 하위 그룹 분석에서만 입증되었으므로128, 실제 치료에서는 환자의 순응도가 치료 효능을 제한할 수 있다. 최근 FDA는 COVID-19의 호흡기 증상 치료에 tVNS 사용을 신속 승인했습니다.129 taVNS를 통한 구심성 미주 신경 자극은 미주 뇌간 핵을 활성화합니다(그림 3 참조). 130,131 taVNS가 전신 자율 신경계에 영향을 미칠 수 있다는 관찰을 바탕으로, 이러한 핵의 신호가 다시 운동성 미주 신경으로 전달된다는 가설이 제시되었습니다. 확실히, tcVNS와 taVNS 모두 내독소혈증 동물 모델에서 항염증 효과를 입증했습니다.132 이러한 효과는 미주신경절제술과 α7nAChR 길항제 모두에 의해 제거되어 CAP의 관여를 시사합니다. TaVNS는 또한 수술 후 장폐색 모델에서 항염증 및 질병 수정 효과를 입증하였다.130 파킨슨병(PD),133 수술 후 인지 기능 장애,134 및 허혈성 뇌졸중에서 신경 보호 효과가 입증되었다.131 최근 연구에서는 이러한 효과가 뇌내 사이토카인 방출 감소 및 α7nAChR 발현 증가와 연관되었다.133, 134 PNU-282987 투여 시 명백한 항불안 및 항우울 효과를 동반한 α7nAChr의 뇌내 상향 조절도 관찰되었다.135
표 1은 iVNS 및 tVNS를 이용한 CAP 활용을 목표로 한 인간 임상시험 결과를 요약한다. 표 1에 기재되지 않은 다른 여러 tVNS 임상시험이 수행되었으며,136 예를 들어 iVNS가 이미 승인된 질환(간질 및 편두통)과 다른 신경학적 질환(예: 우울증 및 파킨슨병) 환자에서 증상 개선이 입증된 사례가 있습니다. 그러나 표 1에 나열된 질환들과 달리, 이러한 신경학적 장애에서 VNS의 항염증 역할은 아직 명확히 규명되지 않았으며 일반적으로 시험 결과에서 측정되지 않으므로, tVNS의 효과가 항염증성일 수도 있고 아닐 수도 있습니다. 전신성 홍반성 루푸스(SLE)를 대상으로 한 한 건의 짧은 이중맹검 예비 연구에서는 질병의 주관적 지표만 개선되었을 뿐 객관적 측정값이나 염증 지표에는 변화가 없었습니다.137 그러나 규모와 수가 작음에도 불구하고, 이러한 연구들의 종합적 증거는 다양한 염증성 질환에 걸쳐 iVNS와 tVNS 모두의 잠재적 치료적 이점을 뒷받침하며, 더 큰 규모의 무작위 대조 시험(RCT)이 필요함을 시사합니다.
최근 비침습적 펄스 초음파(pUS)를 이용한 CAP 자극의 혁신적 방법이 제안되었다.138 쥐에서 복부 초음파 투여가 후속 신장 IRI를 완화시키는 것으로 확인되었다. 이 효과는 기능적 CD4+ T 세포에 의존적이었으며139 비장 적출, KO 또는 α7nAChR 억제, 비장 신경 절제 후에는 관찰되지 않았다.124 급성 신장 손상(AKI) 예방은 비장 백혈구의 염증 잠재력 저하 및 TNF-α와 IL-6를 포함한 혈청 및 신장 사이토카인 수치 감소와 연관되었다.124 pUS가 비장 내 미주신경 하류의 CAP를 자극하는 것으로 여겨진다. 비장 신경 말단 부위에 초점화된 pUS 파동은 ChAT+ CD4+ T 세포와 α7nAChR에 의존하는 과정으로 노르아드레날린과 ACh의 방출을 자극한다.138 비장138,140,141 또는 복부142 pUS는 내독소혈증의 효과 예방, 138 패혈증 생존율 향상141 및 확립된 염증성 관절염140 및 DSS-대장염142의 효과 역전에 효과적임이 입증됨. 고혈당으로 악화된 심근 허혈-재관류 손상 시 비장 또는 경부에 적용된 pUS는 경색 크기를 3배 감소시킴.143 집중된 pUS는 다른 부위에서도 항염증 용도로 활용 가능할 수 있음. 미주 신경의 구심성 섬유는 간문의 문맥에서 자극되어 시상하부 인슐린 감수성을 조절함으로써 고혈당증138을 완화시키고, 이에 따른 체중 증가 감소 및 간 염증의 전반적인 하향 조절을 초래한다.69 이러한 결과들은 종합적으로 다양한 장기 시스템 전반에 걸쳐 CAP를 조절하는 잠재적 치료적 역할을 제시한다.
비침습적이고 명백히 안전하다는 점 외에도, 비장 pUS의 이론적 이점은 미주 신경이 관여하는 다른 장기(예: 폐)에 대한 비-CAP 효과를 회피한다는 것이다.79,82 그러나 마찬가지로, CAP 효과를 비장 대식세포에 의해 매개되는 것으로 제한하는 것은 IBD와 같은 상태에서는 효과가 떨어질 수 있다. 위장관(GIT)의 미주신경 분포가 역할을 할 수 있는 경우입니다.68 복부 전체에 비특이적으로 투여된 pUS가 DSS 대장염에 미치는 효과는, 혈변 빈도의 경미한 개선과 장간막 림프절에서의 AChR+ 세포 모집 증거를 제외하면 비장 적출 마우스에서는 거의 관찰되지 않았습니다.142 그러나 최근, 비장절 신경절 수준에서 CAP를 자극함으로써 pUS가 DSS 대장염에 효과적임이 입증되었다.144 염증성 질환에 대한 pUS의 치료 가능성을 평가하고 이러한 의문점에 답하기 위해 인간 임상 시험이 시급히 필요하다.
Conclusion
The inflammatory reflex is a pervasive homeostatic mechanism that can influence inflammatory diseases across all bodily systems. The nature of certain interactions between the CAP and individual organs remains unclear, as with the CAP’s downstream cellular mechanisms. Nevertheless, evidence to date presents the CAP as an enticing therapeutic target for a wide range of diseases. Findings of pre-clinical experiments are now being translated into small but promising clinical trials. Pharmacological manipulation of the CAP remains somewhat elusive but warrants further study. Bioelectronic techniques capable of harnessing the CAP through invasive and non-invasive methods such as VNS and splenic pUS have shown promising results and may present an innovative form of anti-inflammatory therapy.
결론
염증 반사는 모든 신체 시스템에 걸쳐 염증성 질환에 영향을 미칠 수 있는 광범위한 항상성 조절 기전이다. CAP와 개별 장기 간의 특정 상호작용의 본질은 CAP의 하류 세포 기전과 마찬가지로 여전히 불분명하다. 그럼에도 불구하고 현재까지의 증거는 CAP를 다양한 질환에 대한 매력적인 치료 표적으로 제시한다. 전임상 실험 결과는 현재 소규모이지만 유망한 임상 시험으로 전환되고 있다. CAP의 약리학적 조작은 다소 불분명하지만 추가 연구가 필요합니다. VNS 및 비장 pUS와 같은 침습적 및 비침습적 방법을 통해 CAP를 활용할 수 있는 생체전자 기술은 유망한 결과를 보였으며, 혁신적인 형태의 항염증 치료법을 제시할 수 있습니다.
Acknowledgments
S.C.D., C.B., and M.J.K. gratefully acknowledge the support of Science Foundation Ireland (SFI) and the Health Research Board (HRB) of Ireland.
Author contributions
M.J.K. and S.C.D. searched the literature and wrote the first draft of the manuscript. C.B. and K.T. critically revised each version of the manuscript.
Declaration of interests
All authors declare no competing interests.
References
- 1.Sternberg E.M. Neural-immune interactions in health and disease. J. Clin. Invest. 1997;100:2641–2647. doi: 10.1172/JCI119807. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 2.Watkins L.R., Maier S.F., Goehler L.E. Cytokine-to-brain communication: A review and analysis of alternative mechanisms. Life Sci. 1995;57:1011–1026. doi: 10.1016/0024-3205(95)02047-m. [DOI] [PubMed] [Google Scholar]
- 3.Borovikova L.V., Ivanova S., Zhang M., Yang H., Botchkina G.I., Watkins L.R., Wang H., Abumrad N., Eaton J.W., Tracey K.J. Vagus nerve stimulation attenuates the systemic inflammatory response to endotoxin. Nature. 2000;405:458–462. doi: 10.1038/35013070. [DOI] [PubMed] [Google Scholar]
- 4.Tracey K.J. The inflammatory reflex. Nature. 2002;420:853–859. doi: 10.1038/nature01321. [DOI] [PubMed] [Google Scholar]
- 5.Chavan S.S., Pavlov V.A., Tracey K.J. Mechanisms and therapeutic relevance of neuro-immune communication. Immunity. 2017;46:927–942. doi: 10.1016/j.immuni.2017.06.008. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 6.Tracey K.J. Hacking the inflammatory refelex. Lancet Neurol. 2021;3:E237–E239. doi: 10.1016/s2665-9913(20)30448-3. [DOI] [PubMed] [Google Scholar]
- 7.Borovikova L.V., Ivanova S., Nardi D., Zhang M., Yang H., Ombrellino M., Tracey K.J. Role of vagus nerve signaling in CNI-1493-mediated suppression of acute inflammation. Auton. Neurosci. 2000;85:141–147. doi: 10.1016/s1566-0702(00)00233-2. [DOI] [PubMed] [Google Scholar]
- 8.Huston J.M., Ochani M., Rosas-Ballina M., Liao H., Ochani K., Pavlov V.A., Gallowitsch-Puerta M., Ashok M., Czura C.J., Foxwell B., et al. Splenectomy inactivates the cholinergic antiinflammatory pathway during lethal endotoxemia and polymicrobial sepsis. J. Exp. Med. 2006;203:1623–1628. doi: 10.1084/jem.20052362. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 9.Vida G., Peña G., Deitch E.A., Ulloa L. α7-cholinergic receptor mediates vagal induction of splenic norepinephrine. J. Immunol. 2011;186:4340–4346. doi: 10.4049/jimmunol.1003722. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 10.Rosas-Ballina M., Ochani M., Parrish W.R., Ochani K., Harris Y.T., Huston J.M., Chavan S., Tracey K.J. Splenic nerve is required for cholinergic antiinflammatory pathway control of TNF in endotoxemia. Proc. Natl. Acad. Sci. U S A. 2008;105:11008–11013. doi: 10.1073/pnas.0803237105. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 11.Wang H., Yu M., Ochani M., Amella C.A., Tanovic M., Susarla S., Li J.H., Wang H., Yang H., Ulloa L., et al. Nicotinic acetylcholine receptor α7 subunit is an essential regulator of inflammation. Nature. 2003;421:384–388. doi: 10.1038/nature01339. [DOI] [PubMed] [Google Scholar]
- 12.Bellinger D.L., Felten S.Y., Lorton D., Felten D.L. Origin of noradrenergic innervation of the spleen in rats. Brain Behav. Immun. 1989;3:291–311. doi: 10.1016/0889-1591(89)90029-9. [DOI] [PubMed] [Google Scholar]
- 13.Rosas-Ballina M., Olofsson P.S., Ochani M., Valdés-Ferrer S.I., Levine Y.A., Reardon C., Tusche M.W., Pavlov V.A., Andersson U., Chavan S., et al. Acetylcholine-synthesizing T cells relay neural signals in a vagus nerve circuit. Science. 2011;334:98–101. doi: 10.1126/science.1209985. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 14.Vida G., Peña G., Kanashiro A., Thompson-Bonilla M. d R., Palange D., Deitch E.A., Ulloa L. β2-Adrenoreceptors of regulatory lymphocytes are essential for vagal neuromodulation of the innate immune system. FASEB J. 2011;25:4476–4485. doi: 10.1096/fj.11-191007. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 15.Pavlov V.A., Tracey K.J. Neural circuitry and immunity. Immunol. Res. 2015;63:38–57. doi: 10.1007/s12026-015-8718-1. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 16.Martelli D., McKinley M.J., McAllen R.M. The cholinergic anti-inflammatory pathway: a critical review. Auton. Neurosci. 2014;182:65–69. doi: 10.1016/j.autneu.2013.12.007. [DOI] [PubMed] [Google Scholar]
- 17.Martelli D., Farmer D.G.S., Yao S.T. The splanchnic anti-inflammatory pathway: could it be the efferent arm of the inflammatory reflex? Exp. Physiol. 2016;101:1245–1252. doi: 10.1113/EP085559. [DOI] [PubMed] [Google Scholar]