Review Article
Ann Hematol Oncol. 2021; 8(7): 1353.
Concise Review: How are Red Blood Cells Born, How do they Live and Die?
Vives Corrons J-L¹*, Casafont LB² and Frasnedo EF³
1Emeritus Professor, Red Blood Cell Pathology and Hematopoietic Disorders (Rare Anaemias Unit), Josep Carreras Leukaemia Research Institute, Badalona, Barcelona, Spain
2Professor (ret.), Polytechnic University of Catalonia, Barcelona, Spain
3Emeritus Professor, Josep Carreras International Leukaemia Foundation, Barcelona, Spain
*Corresponding author: Joan-Lluis Vives Corrons, Institute for Leukaemia Research, Josep Carreras Ctra de Can Ruti, Camí de les Escoles s/n 08916 Badalona, Barcelona, Spain
Received: April 05, 2021; Accepted: May 20, 2021; Published: May 27, 2021
Abstract
The average life cycle of a human RBC is approximately 120 days. Generally, by this point, the cell is worn out and damaged. RBCs pass through both the spleen and liver, where specialized immune cells called macrophages are found. Macrophages recognize when an RBC is spent, and undergo a process called phagocytosis where they digest the cell. In this process, the iron in hemoglobin is recycled for use in new blood cells and the hem molecule is degraded, conjugated to bilirubin, and eliminated from the body. All the other cellular proteins are either recycled or eliminated. Historically, this process was thought to occur exclusively in the spleen, but recent studies have shown that it occurs in the bone marrow .The RBC has been analyzed from many perspectives: cytological, hematological, and immunological, as well as from the focus of molecular biology, biophysics, and mathematics. Here we analyze how are red blood cells born and how they live and die in a brief overview of the whole process with special mention of the morphological aspects from bone marrow and spleen provided by Transmission and Scanning Electron Microscopy.
간 적혈구(RBC)의 평균 수명 주기는 약 120일이다.
일반적으로 이 시점에 이르면 세포는 마모되고 손상된다.
RBC는
비장과 간을 통과하며,
여기에는 대식세포라고 불리는 특수 면역 세포가 존재한다.
대식세포는 RBC가 소모되었음을 인식하고,
세포를 소화하는 식작용(phagocytosis) 과정을 거친다.
이 과정에서 헤모글로빈의 철은 새로운 혈구 생성에 재활용되고,
헴 분자는 빌리루빈으로 분해되어 결합된 후 체내에서 배출된다.
다른 모든 세포 단백질은 재활용되거나 제거된다.
역사적으로 이 과정은
비장에서만 발생한다고 여겨졌으나,
최근 연구에 따르면 골수에서도 발생한다.
RBC는
세포학적, 혈액학적, 면역학적 관점뿐만 아니라 분자생물학, 생물물리학, 수학적 관점에서도 분석되어 왔다.
여기서는 적혈구가 어떻게 태어나고, 어떻게 살고 죽는지에 대한 전체 과정의 간략한 개요를 제시하며,
특히 골수와 비장에서의 형태학적 측면을
투과전자현미경(TEM)과 주사전자현미경(SEM)이 제공하는 관점을 특별히 언급한다.
키워드: 적혈구; 노화; 변형성; 유변학; 전자현미경
Keywords: Erythrocytes; Aging; Deformability; Rheology; Electron microscopy
Introduction
The blood and its components are one of the best investigated biological fluids due to its accessibility. Blood is the internal fluid that delivers oxygen and various metabolic substances to the cells of organs and systems in the human body, while collecting products from the cellular metabolism, and particularly carbon dioxide. It also serves as a communication fluid providing defense against outside incomes on our organism. Blood is formed by plasma and cells: the Red Blood Cells (RBCs) or erythrocytes; the White Blood Cells (WBCs) or leukocytes and the platelets or thrombocytes (Figure 1a). Humans have about 4.5 to 5 liters [1] of blood in their circulatory system, and the normal concentrations of blood cells are RBCs: 4.5 to 5.9x1012/l, WBCs: 4 to 11x109/l, and platelets: 150-350x109/l. The Red Blood Cell (RBC) has been analyzed from many different perspectives: cytological and morphological (optical microscopy and or without phase contrast, transmission and scanning electronic microscopy, immunological analysis, molecular and genetic analysis, rheological and physicochemical studies, and mathematics. The combination of all these perspectives, with holistic visions, always represents an advance in the amalgamation of a unique reality as seen from diverse facets.
혈액과 그 구성 요소는 접근성이 높아 가장 잘 연구된 생물학적 체액 중 하나이다.
혈액은 인간 체내에서 산소와 다양한 대사 물질을 장기와 시스템의 세포로 전달하는 내부 체액이며,
세포 대사의 산물, 특히 이산화탄소를 수집한다.
또한 외부 침입에 대한 방어를 제공하는
통신 체액으로 작용한다.
혈액은 혈장과 세포로 구성되며:
적혈구(RBCs) 또는 적혈구; 백혈구(WBCs) 또는 백혈구; 혈소판 또는 혈소판(그림 1a).
인간은 순환계에 약 4.5~5리터[1]의 혈액을 가지고 있으며,
정상 혈구 농도는 RBCs: 4.5~5.9×10¹²/l, WBCs: 4~11×10⁹/l, 혈소판: 150~350×10⁹/l이다.
적혈구(RBC)는
세포학적·형태학적(광학현미경 및 위상차, 투과 및 주사 전자현미경),
면역학적 분석,
분자 및 유전 분석,
유변학 및 물리화학 연구,
수학적 관점 등 다양한 관점에서 분석되어 왔다.
이러한 모든 관점을 홀리스틱한 시각으로 결합하는 것은
항상 독특한 현실을 다양한 측면에서 본 통합의 진보를 나타낸다.
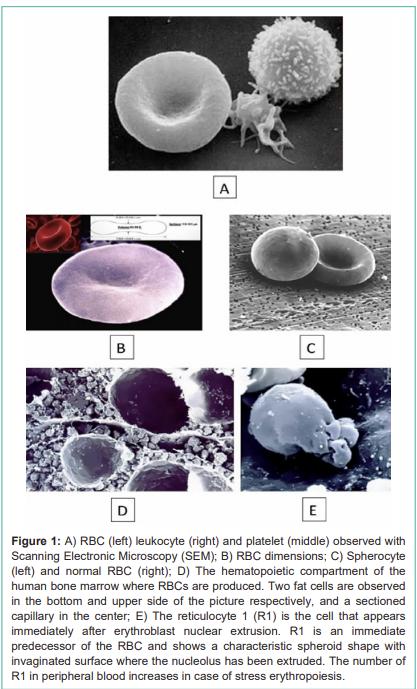
Figure 1:
A) RBC (left) leukocyte (right) and platelet (middle) observed with Scanning Electronic Microscopy (SEM);
B) RBC dimensions;
C) Spherocyte (left) and normal RBC (right);
D) The hematopoietic compartment of the human bone marrow where RBCs are produced. Two fat cells are observed in the bottom and upper side of the picture respectively, and a sectioned capillary in the center;
E) The reticulocyte 1 (R1) is the cell that appears immediately after erythroblast nuclear extrusion. R1 is an immediate predecessor of the RBC and shows a characteristic spheroid shape with invaginated surface where the nucleolus has been extruded. The number of R1 in peripheral blood increases in case of stress erythropoiesis.
그림 1:
A) 주사전자현미경(SEM)으로 관찰된 RBC(왼쪽), 백혈구(오른쪽), 혈소판(가운데);
B) RBC 치수;
C) 구상적혈구(왼쪽)와 정상 RBC(오른쪽);
D) RBC가 생성되는 인간 골수의 조혈 구획. 그림 아래쪽과 위쪽에 각각 지방 세포 두 개가 관찰되며, 중앙에 절단된 모세혈관;
E) 적아구 핵 압출 직후 나타나는 세포인 망상적혈구 1(R1). R1은 RBC의 직계 전구체로, 핵이 압출된 부분에 특징적인 구상 형태와 함입된 표면을 보인다. 말초 혈액에서 R1 수는 스트레스 적혈구생성 시 증가한다.
The RBCs are performing a key role in the whole blood function that is, the oxygen transport from lungs to tissues for cell respiration. In hematology, different parameters are used to characterize the RBCs:
a) their quantity or the number of cells per liter of blood;
b) their size, or Mean Cellular Volume (MCV), and
c) their hemoglobin content or Mean Cellular Hemoglobin (MCH) and Mean Cellular Concentration of Hemoglobin (MCCH).
MCV, MCH and MCCH are known as RBC indexes and are pivotal for the morphological classification of the anemias into microcytic (low MCV), macrocytic (high MCV), and normocytic (normal MCV). However, to understand the physiopathology of Hereditary Hemolytic Anemias (HHA) due to RBC defects, the most important RBC parameter is the morphology characterized by its unique biconcave discoid shape [1]. Each discocyte has a diameter of about 7.5μm, a maximum thickness of 2.0- 2.5 μm, a diameter/thickness ratio of ~3.4, a volume, referred to as MCV of 83 to 98 fl, and a surface of about 140μm² (Figure 1b).
RBC는 전혈 기능의 핵심 역할,
즉 폐에서 조직으로 산소를 운반하여 세포 호흡을 수행한다.
혈액학에서 RBC를 특징짓는 다양한 매개변수가 사용된다:
a) 혈액 리터당 세포 수 또는 양;
b) 크기, 즉 평균 세포 용적(MCV);
c) 헤모글로빈 함량 또는 평균 세포 헤모글로빈(MCH) 및 평균 세포 헤모글로빈 농도(MCCH).
MCV, MCH, MCCH는 RBC 지수로 알려져 있으며,
빈혈의 형태학적 분류(저용적성: 낮은 MCV, 고용적성: 높은 MCV, 정상용적성: 정상 MCV)에 중요하다.
그러나 RBC 결함으로 인한 유전성 용혈성 빈혈(HHA)의 병태생리를 이해하기 위해 가장 중요한 RBC 매개변수는 독특한 양오목 원반형(biconcave discoid shape)으로 특징지어지는 형태이다[1].
각 원반세포(discocyte)는 직경 약 7.5μm, 최대 두께 2.0~2.5μm, 직경/두께 비율 ~3.4, MCV로 불리는 용적 83~98fl, 표면적 약 140μm²이다(그림 1b).
This is not a static situation, and the shape of circulating RBCs changes permanently in normal conditions and different pathologies, facilitating the diagnosis. For many years, Scanning Electronic Microscopy (SEM) has been a useful complementary tool for exploring RBC shape because a three-dimensional image has allowed the reinterpretation of the conventional morphology observation of RBCs by MGG stained blood smears, where are seen as squashed or flattened cells on extension [2]. Due to this, SEM has allowed evaluating the real RBC shape in different pathological conditions as can be demonstrated in Hereditary Spherocytosis (HS) where RBCs are spherical (Figure 1c). This very distinctive shape of RBCs is the best demonstration that, as in many other life situations, form and function are here, inseparable elements. In the human organism, cells have perfectly adapted their shapes to perform their function in the most efficient and optimum way. Due to its discoid shape RBCs are an example of this tight relationship, and it explains how a large surface area, when compared to the volume, can allow the cell to perform its function, the interchange of oxygen (O2) , carbon dioxide (CO2) and metabolites between plasma and cells, most efficiently.
이것은 정적인 상황이 아니며,
순환 중인 RBC의 형태는 정상 조건과 다양한 병리 상태에서 지속적으로 변화하며,
진단을 용이하게 한다.
오랫동안 주사전자현미경(SEM)은
RBC 형태를 탐색하는 유용한 보완 도구였으며,
3차원 이미지가
MGG 염색 혈액 도말에서 관찰되는 평평하거나 납작한 세포로 보이는 전통적인 형태 관찰을 재해석할 수 있게 했다[2].
이로 인해 SEM은
유전성 구상적혈구증(HS)에서 RBC가 구형인 것처럼 다양한 병리 상태에서
실제 RBC 형태를 평가할 수 있게 했다(그림 1c).
RBC의 이 매우 독특한 형태는
많은 다른 생명 상황에서처럼 형태와 기능이 분리될 수 없는 요소임을 가장 잘 보여준다.
인간 유기체에서 세포는 기능을 가장 효율적이고 최적으로 수행하기 위해 형태를 완벽하게 적응시켰다.
원반형으로 인해 RBC는 이 긴밀한 관계의 예이며,
용적에 비해 큰 표면적이 세포가 산소(O₂), 이산화탄소(CO₂), 대사물의 교환을 가장 효율적으로 수행할 수 있게 설명한다.
How do Red Blood Cells Born?
The RBC production, or erythropoiesis, takes place in the bone marrow hematopoietic compartment. Continuous production of RBCs unfolds within a complex three-dimensional tissue scaffold established by highly organized stromal cell networks of mesenchymal, neural, and vascular origin inside Bone Marrow (BM) cavities (Figure 1d). Here it is frequently seen the first stage of RBC maturation after erythroblast enucleation and is known as reticulocyte type 1 (R1). Accordingly, the R1 is a very young reticulocyte with a high MCV that still contains all the machinery necessary for the synthesis of Hb, until its final conversion into a mature RBC. It has a sheroidal globulous shape with the surface strongly invigilated and with the roughness created by the nuclear extrusion (Figure 1e).
적혈구는 어떻게 태어나는가?
RBC 생성 또는 적혈구생성(erythropoiesis)은
골수 조혈 구획에서 일어난다.
RBC의 지속적인 생성은
골수(BM) 공동 내 중간엽, 신경, 혈관 기원의 고도로 조직화된 기질 세포 네트워크가 구축한
복잡한 3차원 조직 스캐폴드 내에서 펼쳐진다(그림 1d).
여기서
적아구 핵 제거 후 RBC 성숙의 첫 단계가 자주 관찰되며,
망상적혈구 1형(R1)으로 알려져 있다.
따라서 R1은 매우 젊은 망상적혈구로 높은 MCV를 가지며,
최종 성숙 RBC로 전환될 때까지
Hb 합성에 필요한 모든 기계를 여전히 포함한다.
그것은 핵 압출로 인해 표면이 강하게 함입되고
거칠어진 구상 형태를 가진다(그림 1e).
Collectively, stromal cells have been shown to serve two principal roles; first as primary participants of bone remodeling and metabolism, and second, as master regulators of different stages of blood cell development and production. RBC precursors are called erythroblasts; a group of cells generated from proliferating and differentiating of earlier, more immature, cells termed erythroid progenitors. Erythroid progenitors are detectable functionally only by their ability to form in vitro colonies. The development of tissue culture techniques for cloning hematopoietic progenitor cells in semisolid culture media in vitro has led to the recognition and assay in the human and murine bone marrow of at least two erythroid progenitors, the Colony-Forming Unit Erythroid (CFU-E) and the Burst-Forming Unit-Erythroid (BFU-E). Under the influence of Epo, these progenitors can grow in semisolid culture media and give rise to colonies of well-hemoglobinised erythroblasts (Figure 2). Maintenance of erythropoiesis occurs primarily through the action of Erythropoietin (Epo) promoting both progenitor proliferation and accelerating terminal maturation. A well-balanced erythropoietic mechanism is necessary for maintaining the response to a variety of normal and abnormal situations. Epo is synthesized in the kidney under the stimulus of hypoxia. Accordingly, a change of blood Hemoglobin concentration (Hb), leads to a change in kidney tissue oxygen, and in response to hypoxia, the kidney secretes Epo, which induces differentiation of erythroid progenitor cells, expansion of the erythroid marrow, and increased red cell production. This, in turn, leads to a compensatory increase in tissue oxygen levels [3].
기질 세포 stromal cells 는 골격 재형성 및 대사의 주요 참여자로서,
그리고 혈구 발달 및 생성의 다양한 단계의 마스터 조절자로서
두 가지 주요 역할을 수행하는 것으로 나타났다.
RBC 전구체는 적혈구 전구세포라고 불리며,
더 미성숙한 세포인 적혈구 조혈모세포의 증식과 분화로 생성된 세포 군이다.
적혈구 조혈모세포는
기능적으로만 반고체 배지에서 in vitro 콜로니 형성 능력으로 검출된다.
반고체 배지에서 조혈 전구세포를 클로닝하는 조직 배양 기술의 개발은
인간과 쥐 골수에서 적혈구 전구세포인
콜로니 형성 단위 적혈구(CFU-E)와 버스트 형성 단위 적혈구(BFU-E)를 인식하고 분석하게 했다.
Colony-Forming Unit Erythroid (CFU-E) and the
Burst-Forming Unit-Erythroid (BFU-E).
Epo의 영향으로 이 전구세포는 반고체 배지에서 성장하여
잘 헤모글로빈화된 적아구 콜로니를 형성한다(그림 2).
적혈구생성의 유지'는
주로 Epo의 작용으로 전구세포 증식과 말기 성숙 가속을 촉진한다.
다양한 정상 및 비정상 상황에 대한 반응을 유지하기 위해
잘 균형 잡힌 적혈구생성 메커니즘이 필요하다.
Epo는
저산소증 자극 하에 신장에서 합성된다.
따라서
혈액 헤모글로빈 농도(Hb) 변화는
신장 조직 산소 변화로 이어지며,
저산소증에 반응하여
신장이 Epo를 분비하고,
이는 적혈구 전구세포 분화, 적혈구 골수 확장, 적혈구 생성 증가를 유도한다.
이는 조직 산소 수준의 보상적 증가로 이어진다[3].

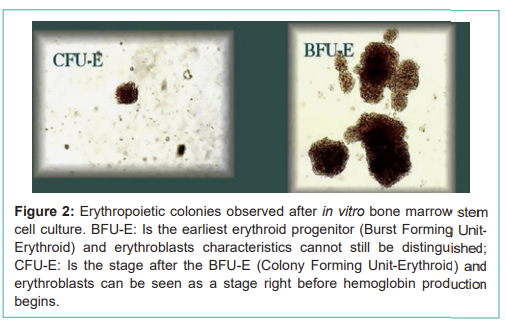
Figure 2: Erythropoietic colonies observed after in vitro bone marrow stem cell culture. BFU-E: Is the earliest erythroid progenitor (Burst Forming Unit- Erythroid) and erythroblasts characteristics cannot still be distinguished; CFU-E: Is the stage after the BFU-E (Colony Forming Unit-Erythroid) and erythroblasts can be seen as a stage right before hemoglobin production begins.
그림 2: in vitro 골수 줄기세포 배양 후 관찰된 적혈구생성 콜로니. BFU-E: 가장 초기 적혈구 전구세포(Burst Forming Unit-Erythroid)로 적아구 특성이 아직 구분되지 않음; CFU-E: BFU-E 이후 단계(Colony Forming Unit-Erythroid)로 헤모글로빈 생성 직전 단계에서 적아구가 보임.
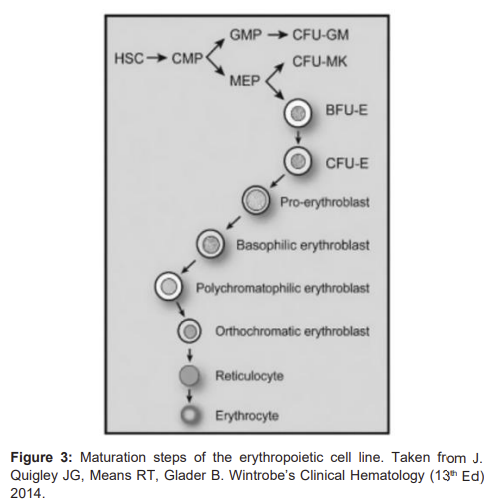
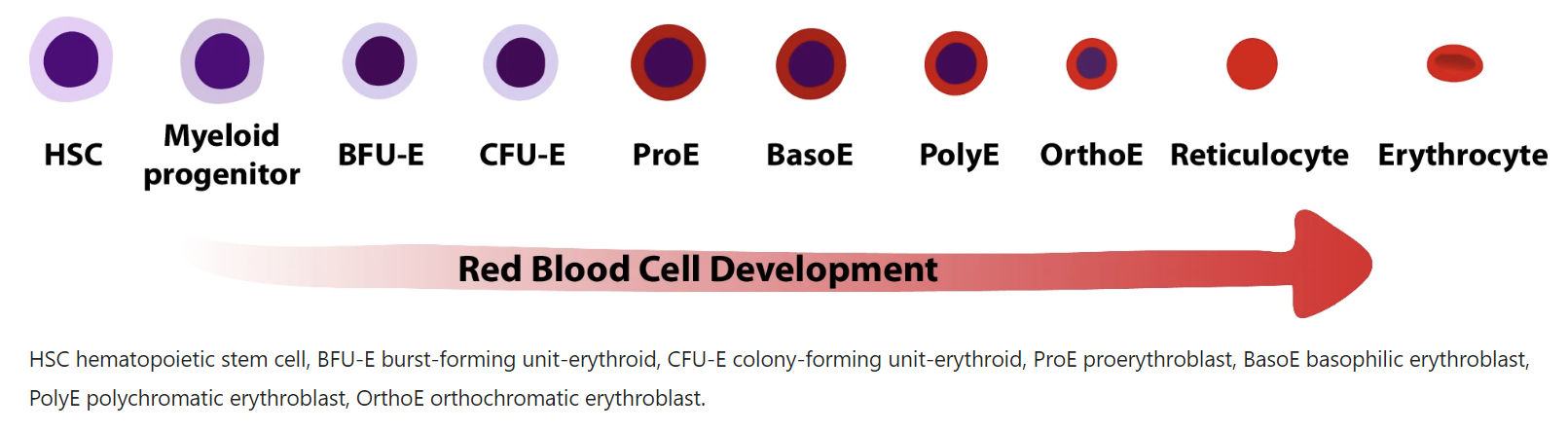
The least mature recognizable erythrocyte precursor cell is known as the proerythroblast, and the various stages of maturation, in order of increasing maturity, are basophilic erythroblasts, polychromatophilic erythroblasts, and orthochromatic erythroblasts (Figure 3). Cytoplasm maturation is assessed by the change in staining characteristics, as the deep blue color derived from the high RNA content of immature cells, gives rise to the red color characteristic of hemoglobin. Nuclear maturation is evaluated by the disappearance of nucleoli and the condensation of chromatin as nuclear activity decreases. Besides, there is a gradual decrease in cell size and Epo Receptors (EpoR) expression and terminally exit from the cell cycle. Orthochromatic erythroblasts are the smallest of the nucleated erythrocyte precursors (8 to 12 μm in diameter) and at this stage, the nucleus undergoes pyknotic degeneration, the chromatin becomes greatly condensed, and the nucleus shrinks and, in the end, it is removed from the cell by extrusion. Erythroblasts nuclear extrusion, or enucleation, occurs in orthochromatic erythroblasts producing two kinds of cells: the reticulocyte type 1 or R1 and the pyrenocyte. As mentioned before, the R1 is a very young reticulocyte R1 matures to normal reticulocyte, until its final conversion into a RBC, with its classical discocyte shape. Pyrenocytes are nucleus surrounded by a thin layer of cytoplasm and the plasma membrane and are rapidly eliminated by the macrophages of the erythroblastic island, where RBC membrane phosphatidylserine exposure acts as an “eat me” signal [4]. In this process, the factor of proliferation is 24, which means that each erythroblast produces about 8 to 32 reticulocytes in approximately one week.
가장 미성숙한 인식 가능한 적혈구 전구세포는
원적아구(proerythroblast)로 알려져 있으며,
성숙도 증가 순서로 basophilic erythroblasts, polychromatophilic erythroblasts, orthochromatic erythroblasts이다(그림 3).
세포질 성숙은 염색 특성 변화로 평가되며,
미성숙 세포의 높은 RNA 함량에서 유래한 짙은 청색이 헤모글로빈의 특징적인 적색으로 변한다.
핵 성숙은
핵소체 소실과 핵 활동 감소에 따른 염색질 응축으로 평가된다.
또한 세포 크기 점진적 감소, Epo 수용체(EpoR) 발현, 세포 주기 말기 종료가 있다.
orthochromatic erythroblasts는
핵을 가진 적혈구 전구세포 중 가장 작으며(직경 8~12μm),
이 단계에서 핵은 pyknotic 변성을 겪고 염색질이 크게 응축되며 핵이 축소되어 결국 압출된다.
적아구 핵 압출 또는 핵 제거(enucleation)는 orthochromatic erythroblasts에서 발생하여
두 종류의 세포: 망상적혈구 1형(R1)과 pyrenocyte를 생성한다.
앞서 언급한 바와 같이
R1은 매우 젊은 망상적혈구로 정상 망상적혈구로 성숙하여
최종적으로 고전적인 원반세포 형태의 RBC로 전환된다.
Pyrenocyte는
얇은 세포질 층과 혈장막으로 둘러싸인 핵으로,
적아구 섬의 대식세포에 의해 빠르게 제거되며,
여기서 RBC 막 포스파티딜세린 노출이 “먹어라” 신호로 작용한다[4].
이 과정에서 증식 인자는 24로,
각 적아구가 약 일주일 동안 8~32개의 망상적혈구를 생성한다.
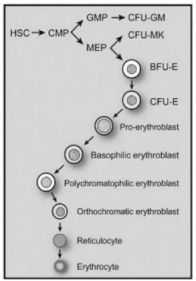
Figure 3: Maturation steps of the erythropoietic cell line. Taken from J. Quigley JG, Means RT, Glader B. Wintrobe’s Clinical Hematology (13th Ed) 2014.
Cytoskeletal elements play an important role in erythroblast enucleation, acting similarly to cytokinesis but in an asymmetric way. Specifically, as observed by electron and immunofluorescence microscopy, actin filaments (F-actin) condensate behind the extruding nucleus to form the Contractile Actin Rings (CAR). Unfortunately, we are still at the beginning of understanding the mechanism and the players involved in the enucleation process.
Two events may decrease the theoretic yield of cells, one of these is the death of erythrocytes before or shortly after release from the marrow (ineffective erythropoiesis) and the second is a skipped cell division, a phenomenon that may occur with increased Epo stimulation and that results in a large hemoglobin-poor cell. These events occur only to a limited extent in normal subjects but occur much more frequently under pathologic circumstances [5].
세포골격 요소는
적아구 핵 제거에 중요한 역할을 하며,
비대칭 방식으로 세포분열과 유사하게 작용한다.
특히 전자 및 면역형광 현미경으로 관찰된 바와 같이,
액틴 필라멘트(F-actin)가 압출되는 핵 뒤에서 응축되어 수축성 액틴 고리(Contractile Actin Rings, CAR)를 형성한다.
불행히도
우리는 핵 제거 과정의 메커니즘과 관련 플레이어를 이해하는 초기 단계에 있다.
세포의 이론적 수율을 감소시키는 두 가지 사건이 있으며,
하나는 골수에서 또는 방출 직후 적혈구의 사멸(비효과적 적혈구생성)이고,
다른 하나는 Epo 자극 증가 시 발생할 수 있는 건너뛰기 세포 분열로, 헤모글로빈이 부족한 큰 세포를 초래한다.
이러한 사건은
정상 피험자에서 제한적으로 발생하지만
병리 상황에서 훨씬 더 자주 발생한다[5].
The mechanism of RBCs egress from the bone marrow to the bloodstream is still not yet well understood, but it seems to be determined by the so-called “bone marrow restraining barrier” that separates the hematopoietic compartment from the sinusoids. This barrier is formed by a thin layer (0.2 - 0.4 μm) of very flat endothelial cells that completely cover the sinuses and have overlapping interdigitate and sliding joints (Figure 4). Electron microscopy has resealed that marrow sinusoids are trilaminar structures containing adventitial cells towards marrow cord, a middle basement membrane, and endothelial cells lining toward sinusoid, containing pores [6]. The adventitial cell provides an area for deformed mature RBCs, but only the pores of endothelial cells allow their egress to the bloodstream. The pores of endothelial cells are thin slots with a diameter of 1 to 5 μm, which is smaller than that of the RBCs, and under normal conditions, this bone marrow barrier ensures that the RBCs, released into the bloodstream have the required standard of quality [7]. The cellular movement through the barrier is very intense with some 200,000 million red blood cells, 10,000 million, granulocytes, and 400,000 million platelets passing on average each day. Several studies indicate that only mature RBCs can cross the pores of barrier membrane as compared to immature cells due to their deformability and denucleation, and it has been demonstrated that certain humoral factors may also increase this permeability by increasing pore size [8].
RBC가 골수에서 혈류로 빠져나가는 메커니즘은 아직 잘 이해되지 않았으나,
조혈 구획과 정현동을 분리하는 “골수 억제 장벽”에 의해 결정되는 것으로 보인다.
이 장벽은 정현동을 완전히 덮는 매우 평평한 내피 세포의 얇은 층(0.2~0.4μm)으로 형성되며, 겹치고 서로 맞물린 미끄러지는 접합을 가진다(그림 4).
전자현미경으로 골수 정현동이 삼층 구조로 밝혀졌으며, 골수 코드 쪽으로 모세포, 중간 기저막, 정현동 쪽으로 내피 세포를 포함하며 기공이 있다[6]. 모세포는 변형된 성숙 RBC를 위한 영역을 제공하나, 내피 세포의 기공만 혈류로의 빠져나감을 허용한다. 내피 세포의 기공은 직경 1~5μm의 얇은 슬롯으로 RBC보다 작으며, 정상 조건에서 이 골수 장벽은 혈류로 방출된 RBC가 필요한 품질 기준을 갖추었음을 보장한다[7]. 세포 이동은 매우 강렬하며, 매일 평균 2억 개의 적혈구, 1천만 개의 과립구, 4억 개의 혈소판이 통과한다. 여러 연구에 따르면 성숙 RBC만이 변형성과 핵 제거로 인해 장벽 기공을 통과할 수 있으며, 특정 체액 인자가 기공 크기를 증가시켜 투과성을 높일 수 있다[8].
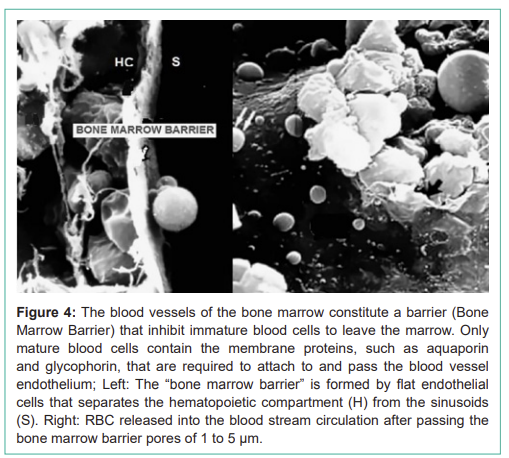
그림 4: 골수의 혈관은 미성숙 혈구가 골수를 떠나는 것을 억제하는 장벽(골수 장벽)을 구성한다. 성숙 혈구만이 아쿠아포린과 글리코포린 같은 막 단백질을 포함하여 혈관 내피에 부착하고 통과하는 데 필요하다;
왼쪽: 평평한 내피 세포로 형성된 “골수 장벽”이 조혈 구획(H)을 정현동(S)에서 분리;
오른쪽: 1~5μm 기공을 통과한 후 혈류 순환으로 방출된 RBC.
Figure 4: The blood vessels of the bone marrow constitute a barrier (Bone Marrow Barrier) that inhibit immature blood cells to leave the marrow. Only mature blood cells contain the membrane proteins, such as aquaporin and glycophorin, that are required to attach to and pass the blood vessel endothelium; Left: The “bone marrow barrier” is formed by flat endothelial cells that separates the hematopoietic compartment (H) from the sinusoids (S). Right: RBC released into the blood stream circulation after passing the bone marrow barrier pores of 1 to 5 μm.
https://pmc.ncbi.nlm.nih.gov/articles/PMC11822345/
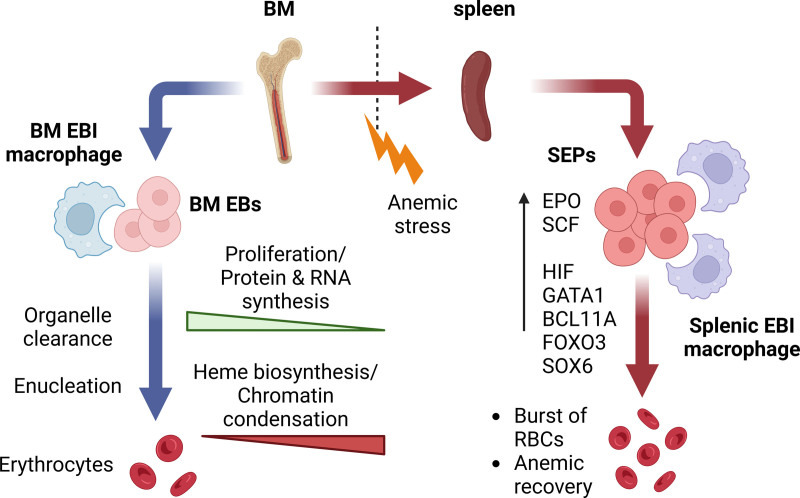
| 정상 상태(steady-state) 및 스트레스(stress) 조혈적 적혈구 생성(erythropoiesis)의 개요. 정상 상태의 적혈구 생성에서는 적혈구 계열의 분화가 골수(BM)에서 이루어진다. 이 과정은 여러 단계의 적아구(EB, erythroblasts)를 거쳐 진행되며, 최종적으로 적아구 섬(EBI, erythroblastic island) 미세환경 내에서 탈핵(enucleation)이 일어나 망상적혈구(reticulocytes)와 성숙 적혈구(RBCs)가 형성된다. 이러한 분화 단계 동안 헴(heme) 생합성, 염색질 응축(chromatin condensation), 그리고 세포소기관 제거(organelle clearance)가 핵심적인 역할을 한다. 빈혈성 스트레스에 반응하여 스트레스 적혈구 생성(stress erythropoiesis)이 활성화되며, 이는 주로 골수 외 조혈 부위인 비장(spleen)에서 일어난다. 이 과정에서는 스트레스 적혈구 전구세포(SEPs, stress erythroid progenitors)의 증식이 일어나며, 에리트로포이에틴(EPO)과 줄기세포 인자(SCF) 등을 포함한 여러 신호 전달 경로에 의해 유도되고, 다양한 전사인자에 의해 조절된다. 이러한 요소들이 함께 작용하여 적혈구의 급속한 대량 생산을 유도함으로써 적혈구계의 회복을 촉진한다. BM = 골수, EB = 적아구, EBI = 적아구 섬, EPO = 에리트로포이에틴, RBC = 적혈구, SEPs = 스트레스 적혈구 전구세포, SCF = 줄기세포 인자. |

How does Red Blood Cell Live?
The RBCs have a lifetime average of about 120 days (4 months) in the bloodstream driven by the pumping force of the heart and travels more than 300km providing oxygen and nutrients to all the tissue cells. A large part of their passage is through the arteries and the arterioles with diameter sizes over 50μm, but also through capillaries with a diameter ranging from 3 to 8 μm (Figure 5a), which is less than its mean cell diameter, of about 7.5μm. For the fluid traffic necessary to reach all the tissues and cells, the RBCs have to adapt to these narrow vascular channels by changing their shape and undergoing a large deformation (Figure 5b). Accordingly, deformability is the key RBC physical property to ensure suitable tissue oxygenation and it is the result of three geometrical and physicochemical characteristics: a) Shape (biconcave discocyte) depending on S/V ratio; b) Viscosity depending on intracellular hemoglobin concentration and its physicochemical state, and c) Viscoelasticity largely determined by the cytoskeleton an actin-spectrin network that underlies the lipid leaflet of the membrane [8]. This structure consists of long twisted strands of alpha and beta spectrin and actin filaments. Spectrin forms the inner shell of the RBC and gives the cell its deformability (Figure 6). Spectrin is bound to the lipid bilayer of the membrane at sites containing the anion exchanger, band 3 via cytoskeletal proteins, ankyrin, and adducin. Some of the transmembrane proteins (such as glycophorin A) are RBC antigens and contribute to the blood group system [9].
적혈구는 어떻게 사는가?
RBC는
혈류에서 평균 약 120일(4개월)의 수명을 가지며,
심장의 펌핑력으로 구동되어 300km 이상을 여행하며
모든 조직 세포에 산소와 영양을 제공한다.
통과의 대부분은 직경 50μm 이상의 동맥과 세동맥이지만,
직경 3~8μm의 모세혈관도 통과한다(그림 5a),
이는 평균 세포 직경 약 7.5μm보다 작다.
모든 조직과 세포에 필요한 유체 교통을 위해 RBC는
이러한 좁은 혈관 채널에 적응하여 형태를 변화시키고 큰 변형을 겪는다(그림 5b).
따라서 변형성은
적절한 조직 산소화를 보장하는 핵심 RBC 물리적 특성으로,
다음 세 가지 기하학적·물리화학적 특성의 결과이다:
a) S/V 비율에 의존하는 형태(양오목 원반세포);
b) 세포내 헤모글로빈 농도와 그 물리화학적 상태에 의존하는 점도;
c) 지질 이중층 아래에 있는 세포골격 액틴-스펙트린 네트워크가 주로 결정하는 점탄성[8].
이 구조는
알파와 베타 스펙트린과 액틴 필라멘트의 긴 꼬인 가닥으로 구성된다.
스펙트린은 RBC의 내부 껍질을 형성하여 세포 변형성을 부여한다(그림 6). 스펙트린은 앙키린과 애듀신 같은 세포골격 단백질을 통해 음이온 교환체인 band 3을 포함하는 부위에서 막 지질 이중층에 결합한다. 일부 막관통 단백질(글리코포린 A 등)은 RBC 항원으로 혈액형 시스템에 기여한다[9].
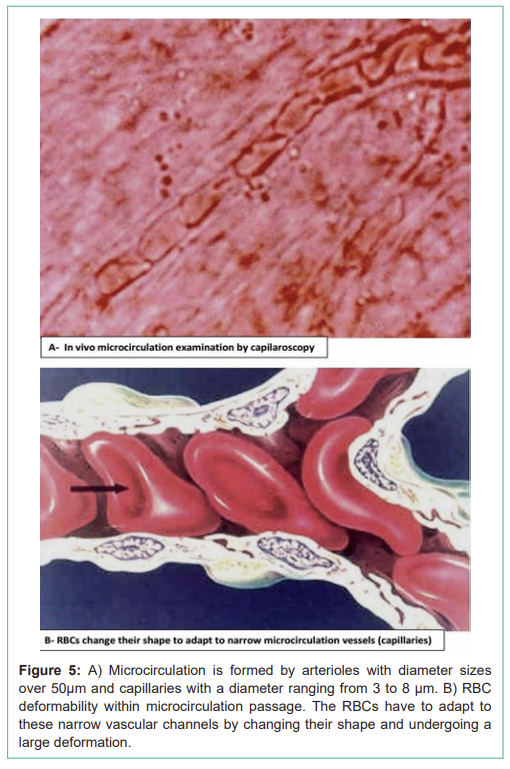
그림 5:
A) 미세순환은 직경 50μm 이상의 세동맥과 3~8μm의 모세혈관으로 구성;
B) 미세순환 통과 시 RBC 변형성. RBC는 좁은 혈관 채널에 적응하여 형태를 변화시키고 큰 변형을 겪는다.
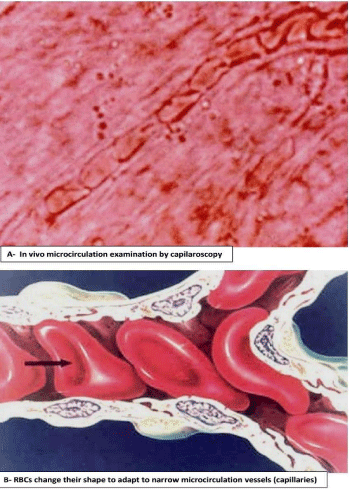
Figure 5: A) Microcirculation is formed by arterioles with diameter sizes over 50μm and capillaries with a diameter ranging from 3 to 8 μm. B) RBC deformability within microcirculation passage. The RBCs have to adapt to these narrow vascular channels by changing their shape and undergoing a large deformation.
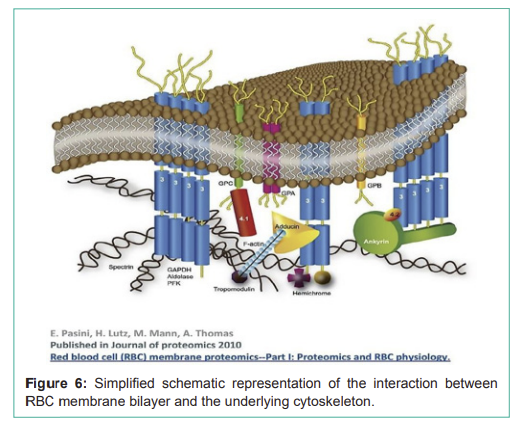
Figure 6: Simplified schematic representation of the interaction between RBC membrane bilayer and the underlying cytoskeleton.
그림 6: RBC 막 이중층과 아래 세포골격 간 상호작용의 간략한 개략도.
In the practice, the cellular shape is quantified by the ratio between the RBC surface (S) and its volume (V) or S/V ratio. Due to their discoid form, normal RBCs have an S/V ratio of about 1.56, indicating an excess of the membrane with regards to the volume. This allows RBCs to change their shape without increasing the surface and subsequently, to undergo highly deformable in the bloodstream. In mechanical terms, this means that RBCs can change their shape under the changes of the capillary diameter and pass through the Inter-Endothelial Slits (IES) in the spleen [10]. The spleen, is a highly vascularised organ, with a blood flow, of about 300ml/min, which represents around 6% of the cardiac flow. In humans, it plays an important role in the immune system by protecting the body from pathogenic microorganisms reaching the bloodstream, through innate phagocytosis or adaptive responses operated by lymphocytes and antibodies. However, due to the IES, the spleen also serves as a filter that can remove RBCs from circulation when alterations in their size, shape, and deformability are detected. The spleen vasculature is composed of a complex network of capillaries, venules, arterioles, but it has a very particular and characteristic structure formed by the endothelial cells of the splenic sinuses, that anastomosed together, cover the sinuses channels without any type of junction (Figure 7). This structure allows the opening of Inter-Endothelial Passage Slots (IES) of about 0.2 to 0.4 μm of diameter, and RBCs are obliged to pass through these IES (Figure 8). This serves as a filter for altered or senescent RBCs because only the cells with normal deformability can overcome this particular splenic barrier. The dynamics of passing through these narrow openings serve not only as a filter for assessing the RBC’s quality but also as a test of their viability. Moreover, through this process, the spleen eliminates the RBC particles such as parasites and inclusions, thereby ensuring that only the full deformable cells may rapidly pass through the barrier posed by the splenic filter [10]. Red Blood Cells (RBCs) can be cleared from circulation when alterations in their size, shape, and deformability are detected. This function is modulated by the spleen-specific structure of the Interendothelial Slit (IES) that selects RBCs for continued circulation based on their geometry, consistent with prior in vivo observations. A companion analysis provides critical bounds relating surface area and volume for healthy RBCs beyond which the RBCs fail the “physical fitness test” to pass through the IES, supporting independent experiments [11]. Accordingly, when the RBC shape is unable to adapt to these stressing circulation conditions, it is easily trapped in the spleen and destroyed (hemolysis).
실제로 세포 형태는
RBC 표면(S)과 용적(V) 비율 또는 S/V 비율로 정량화된다.
원반 형태로 인해 정상 RBC는
S/V 비율 약 1.56을 가지며,
용적에 대한 막의 과잉을 나타낸다.
이는 RBC가 표면을 증가시키지 않고 형태를 변화시켜 혈류에서 고도로 변형될 수 있게 한다.
기계적 용어로 이는 RBC가 모세혈관 직경 변화와 비장의 세포간 내피 슬릿(IES)을 통과할 수 있음을 의미한다[10].
비장은
혈류 약 300ml/min으로 심장 혈류의 약 6%를 차지하는 고도로 혈관화된 장기이다.
인간에서 비장은
혈류에 도달하는 병원성 미생물로부터 신체를 보호하는 면역계에서 중요한 역할을 하며,
선천적 식작용 또는 림프구와 항체에 의한 적응 반응을 통해 작용한다.
The spleen, is a highly vascularised organ, with a blood flow, of about 300ml/min, which represents around 6% of the cardiac flow. In humans, it plays an important role in the immune system by protecting the body from pathogenic microorganisms reaching the bloodstream, through innate phagocytosis or adaptive responses operated by lymphocytes and antibodies.
https://pmc.ncbi.nlm.nih.gov/articles/PMC6495537/
| 이 논문은 비장의 구조-기능적 면역학을 종합적으로 검토하며, 적색질·백색질·경계대역의 조직학적 구획화와 세포 유형별 역할을 강조한다. 비장은 혈액 여과와 병원체 감시를 통해 선천·후천 면역을 연결하며, 특히 MZ 대식세포와 DC가 혈중 항원을 백색질로 전달해 T/B 세포 활성화를 매개한다. 논문 요약Lewis et al. (2019)은 비장의 적색질(RP)이 노화 RBC 제거와 조혈을, 백색질(WP)이 T/B 세포 활성화와 GC 반응을 담당한다고 설명한다. 경계대역(MZ)은 MZB 세포와 대식세포가 항원 포획·전달을 주도하며, 쥐와 인간 간 MZB 세포 기능 차이를 지적한다. 리스테리아 감염 모델에서 cDC1/cDC2의 이동과 FRC 네트워크가 T 세포 프라이밍을 조절하는 메커니즘을 강조하며, 인간 비장 연구의 필요성을 제기한다 |
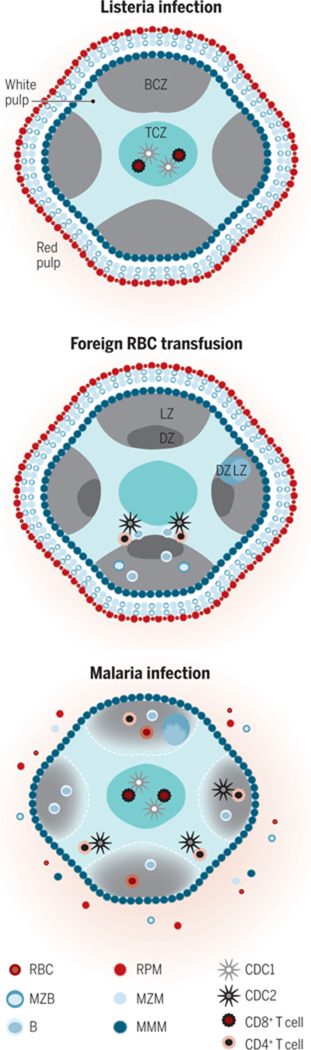

https://pmc.ncbi.nlm.nih.gov/articles/PMC11984396/

그러나 IES로 인해 비장은
크기, 형태, 변형성 변화가 감지될 때
RBC를 순환에서 제거하는 필터로도 작용한다.
비장 혈관은 모세혈관, 정맥, 세동맥의 복잡한 네트워크로 구성되지만,
비장 정현동의 내피 세포가 어떠한 접합 없이 함께 문합되어
정현동 채널을 덮는 매우 특별한 구조를 가진다(그림 7).
이 구조는 직경 약 0.2~0.4μm의 세포간 통과 슬롯(IES)을 열 수 있게 하며,
RBC는 이 IES를 통과해야 한다(그림 8).
이는 변형 또는 노화된 RBC에 대한 필터로 작용하며,
정상 변형성을 가진 세포만 이 특별한 비장 장벽을 극복할 수 있다.
좁은 개구부를 통과하는 역학은
RBC 품질 평가 필터일 뿐만 아니라 생존성 테스트로도 작용한다.
또한 이 과정에서 비장은
기생충과 내포물 같은 RBC 입자를 제거하여
완전히 변형 가능한 세포만 비장 필터 장벽을 빠르게 통과할 수 있게 한다[10].
크기, 형태, 변형성 변화가 감지될 때 RBC는
순환에서 제거될 수 있다.
이 기능은 비장 특유의 세포간 슬릿(IES) 구조에 의해 조절되며,
기하학에 기반한 RBC 순환 지속 선택을 한다.
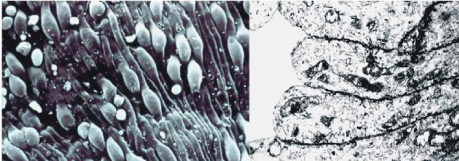
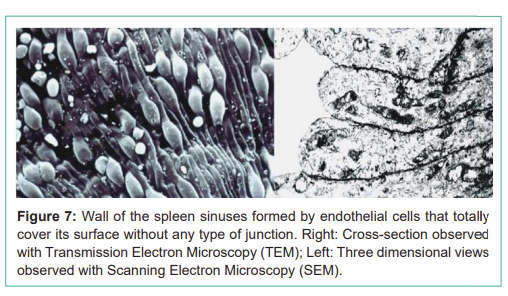
Figure 7: Wall of the spleen sinuses formed by endothelial cells that totally cover its surface without any type of junction. Right: Cross-section observed with Transmission Electron Microscopy (TEM); Left: Three dimensional views observed with Scanning Electron Microscopy (SEM).
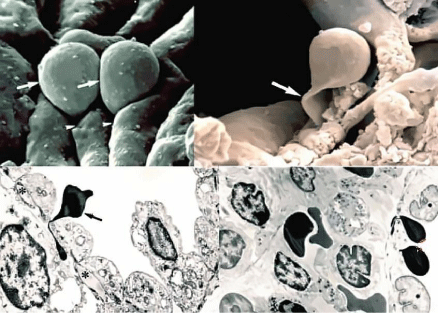
Figure 8: Passage of RBCs through the Inter-Endothelial Slots (IES) of the spleen filter. A marked deformation is appreciated by both three-dimensional view with SEM (above) and cross-section with TEM (below). The arrows indicate the RBCs passing through the narrow IES.
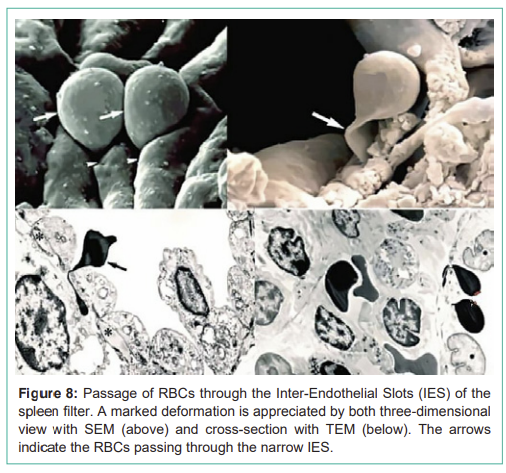
그림 7: 비장 정현동 벽은 어떠한 접합 없이 표면을 완전히 덮는 내피 세포로 형성. 오른쪽: 투과전자현미경(TEM)으로 관찰된 단면; 왼쪽: 주사전자현미경(SEM)으로 관찰된 3차원 뷰.
그림 8: 비장 필터의 세포간 내피 슬롯(IES)을 통과하는 RBC. SEM의 3차원 뷰(위)와 TEM의 단면(아래) 모두에서 뚜렷한 변형이 관찰됨. 화살표는 좁은 IES를 통과하는 RBC를 나타냄.
The archetypical disease where mechanical retention of RBCs in the spleen is the central pathogenic process is Hereditary Spherocytosis (HS), where the RBCs are spherical and, therefore, non-deformable (Figure 3). HS is a genetic disorder resulting in dysfunctional membrane proteins that play a role in transforming the shape of the RBC from a normal discocyte to a sphere. HS occurs at a frequency of 1 in 5,000 births in the Caucasian population and is the most common origin of hereditary intravascular and extravascular hemolysis. In HS, defects in band 3, ankyrin, and spectrin membrane proteins connecting the RBC membrane to the spectrin network can lead to the vesiculation of the unsupported lipid bilayer. Such vesiculation causes a gradual reduction in cell surface area by as much as 20% compared with that of a healthy RBC. This reduction, in turn, can significantly increase the retention rates of RBCs in the spleen because of their increased sphericity [12]. Spheres are forms that have the same surface area for a given volume and, in HS, the spherocytes have a volume of 90fl for a surface of about 97μm², thus giving a minimum value of S/V ratio of about 1.08, making it impossible to change the shape without increasing its surface, and becoming rigid and non-deformable [13]. Severe reduction in RBC deformability, attributable to spherocytosis, results in the obstruction of RBCs flow as they pass through the spleen and consequently, they are phagocytosed by macrophages (Figure 9) causing hemolytic anemia and enlarged spleen (splenomegaly). The fact that surgical removal of the spleen (splenectomy) alleviates anemia to a large extent in patients with severe HS, lends support to the argument that recognition of altered deformability of RBCs is a specific function of the spleen.
비장에서 RBC의 기계적 보유가 중심 병인 과정인 전형적인 질환은
유전성 구상적혈구증(HS)으로,
RBC가 구형이고 따라서 비변형성이다(그림 3).
HS는 RBC를 정상 원반세포에서 구형으로 변화시키는 막 단백질 기능 장애를 초래하는 유전 장애이다.
HS는 백인 인구에서 5,000명당 1명의 빈도로 발생하며, 유전성 혈관내 및 혈관외 용혈의 가장 흔한 원인이다.
HS에서 band 3, 앙키린, 스펙트린 막 단백질 결함은 스펙트린 네트워크에 RBC 막을 연결하며, 지지되지 않은 지질 이중층의 소포화를 초래할 수 있다. 이러한 소포화는 건강한 RBC에 비해 세포 표면적을 최대 20% 점진적으로 감소시킨다. 이는 구형성 증가로 인해 비장에서 RBC 보유율을 크게 증가시킬 수 있다[12]. 구형은 주어진 용적에 대해 동일한 표면적을 가지며, HS에서 구상적혈구는 용적 90fl에 표면 약 97μm²로 S/V 비율 최소값 약 1.08을 주어 표면 증가 없이 형태 변화가 불가능하며, 강직하고 비변형성이 된다[13].
구상적혈구증으로 인한 RBC 변형성의 심각한 감소는
비장을 통과하는 RBC 흐름을 막아 대식세포에 의한 식작용을 초래하며(그림 9),
용혈성 빈혈과 비장 비대를 일으킨다.
중증 HS 환자에서 비장 절제술(splenectomy)이 빈혈을 크게 완화한다는 사실은
변형성 변화된 RBC 인식이 비장의 특정 기능임을 지지한다.
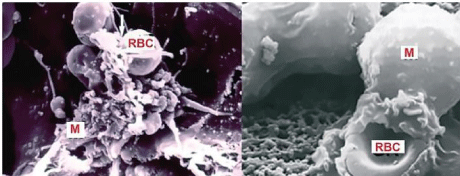
Figure 9: Death of RBCs in the bone marrow phagocytised by Macrophages (M) observed with SEM. RBCs death takes place mainly in the bone marrow, the same place where they have born.
그림 9: 대식세포(M)에 의해 식작용된 골수 내 RBC 사멸, SEM으로 관찰. RBC 사멸은 주로 태어난 동일 장소인 골수에서 발생한다.
How do Red Blood Cells Die?
After their hazardous, day to day, bloodstream circulation, and continuous deformability verification by the spleen, during the approximately 120 days of life the RBCs, begin to age. The whole process of RBC aging is characterized by the expression of death signaling pathways after several progressive biochemical changes mainly due to a reduction of metabolic machinery involving membrane vesiculation hemoglobin modifications and progressive failure of both cellular homeostasis and antioxidant defenses [14]. However, although the RBCs have already been used as a model for aging study, the molecular participants, as well as the signaling pathways involved, are not yet completely clarified. It seems that at the terminal stage of the aging process a cumulative cascade of events appears shortly before RBCs removal by the macrophages [15]. These events include the increase in RBC density, the nonenzymatic glycation of Hb, and the deamidation of protein 4.1b to 4.1a that have been widely used as sensitive RBC age markers. To the current knowledge, the “RBC aging phenotype”, namely the repertoire of age- dependent alterations, can be safely associated with a reported decline in metabolic activity, a progressive cell shape transformation, a membrane remodeling, as well as with oxidative injury, microvesiculation, and exposure of surface removal markers. The only common feature of all these modifications is that, directly or indirectly, triggers erythrophagocytosis through the oxidant stress, common to all cell aging, and its consequence, the decrease of RBC deformability.
The decrease of RBC deformability is mainly due to skeletal architecture and remodeling of the RBC membrane as a consequence of ageing and the current available methods to study such parameter include rotational viscometers [16] and ektacytometry [17]. However, these techniques do not take into consideration the heterogeneity or size differences within the sample population of RBCs. For this reason, flow cytometry has become a very useful tool in the screening of membranopathies and different approaches have been described that are intended to calculate the osmotic fragility of diseased RBCs or to measure Eosin-5'-Maleimide (EMA) binding [18]. The precision of flow cytometry measurements for non- spherical cells such as RBCs is affected by the orientation of cells as they pass through a light source. This is especially true for light scatter measurements, where nearly identically shaped cells can have significantly different scatter signals owing to the variation in the cross section of each individual cell facing a focused laser source. For RBCs this variation is further complicated by secondary light scattering effects arising from their unusual bi-concave disc shape [19]. It is known that distortions of the normal RBC bi-concave disc shape can be the consequence of aging defects in the RBC membrane skeletal architecture and new approaches to light-scattering based on the measurement of RBC orientation have been developed An example is the new generation acustophoretic orientation measurement of RBCs that may become a potentially useful tool for the more precise measurement of the effects of RBC storage and ageing [20].
위험한 일상 혈류 순환과 비장에 의한 지속적인 변형성 검증 후,
약 120일 수명 동안 RBC는 노화되기 시작한다.
RBC 노화 전체 과정은
막 소포화, 헤모글로빈 수정, 세포 항상성 및 항산화 방어 실패를 포함한
여러 점진적 생화학 변화 후 사멸 신호 경로 발현으로 특징지어진다[14].
그러나 RBC가 노화 연구 모델로 사용되었음에도
분자 참여자와 관련 신호 경로가 완전히 밝혀지지 않았다.
노화 과정 말기 단계에서
제거 직전 누적 사건 연쇄가 나타나는 것으로 보인다[15].
이러한 사건에는
RBC 밀도 증가, Hb의 비효소적 당화, 단백질 4.1b에서 4.1a로의 탈아미드화가 포함되며,
이는 민감한 RBC 연령 마커로 널리 사용된다.
현재 지식으로 “RBC 노화 표현형”,
즉 연령 의존적 변화 레퍼토리는
대사 활동 감소, 점진적 세포 형태 변환, 막 재형성, 산화 손상, 미소소포화, 표면 제거 마커 노출과 연관될 수 있다.
이러한 모든 수정의 공통 특징은
직접 또는 간접적으로 산화 스트레스(모든 세포 노화의 공통)와
그 결과인 RBC 변형성 감소를 통해 식작용을 유발한다는 것이다.
RBC 변형성 감소는
주로 노화의 결과인 골격 구조와 막 재형성으로 인해 발생하며,
이를 연구하는 현재 방법에는 회전 점도계[16]와 ektacytometry[17]가 있다.
그러나 이러한 기술은 샘플 내 RBC의 이질성이나 크기 차이를 고려하지 않는다. 이 이유로 흐름세포측정법은 막병증 스크리닝에 매우 유용한 도구가 되었으며, 질병 RBC의 삼투 취약성을 계산하거나 Eosin-5'-Maleimide (EMA) 결합을 측정하는 다양한 접근이 설명되었다[18]. 비구형 세포인 RBC에 대한 흐름세포측정법 측정의 정밀도는 세포가 광원 통과 시 방향에 영향을 받는다. 이는 특히 광산란 측정에서 거의 동일한 형태의 세포가 집중 레이저 소스에 직면한 단면 변이로 인해 산란 신호가 크게 다를 수 있다.
RBC의 경우 이는 이상한 양오목 원반 형태에서 2차 광산란 효과로 더욱 복잡해진다[19]. 정상 RBC 양오목 원반 형태의 왜곡이 RBC 막 골격 구조의 노화 결함 결과일 수 있으며, RBC 방향 측정에 기반한 새로운 광산란 접근이 개발되었다. RBC 방향의 새로운 세대 음향영동 측정이 RBC 보관과 노화 효과의 더 정밀한 측정을 위한 잠재적 유용 도구가 될 수 있다[20].
The “eat me” signal of this event is thought to be the translocation of phosphatidylserine from the inner to the outer membrane leaflet due to activation of the scramblase, while the flippase is inactivated [4] and both processes are triggered by an increased intracellular Ca2+ concentration [21] This aging progress is accompanied by the changes of many RBC surface antigens that facilitate its phagocytosis by the macrophages of the bone marrow (Figure 9). Accordingly, RBCs die in the bone marrow, the same place where they have been born, and its structural components are recycled to produce new RBCs in a splendid form of renovation.
In hereditary Hemolytic Anemias (HHA) due to RBC defects, cell deformability is almost always impaired, and due to the spleen barrier, the majority of abnormal RBCs are retained and destroyed by phagocytosis. As mentioned before, the classical example of this situation is HS, which can be considered an exacerbation of what happens in a normal situation when RBCs are approaching the end of their hazardous 120 days of life. This process is continuously compensated by an active RBC renewal through erythropoiesis, and, for this reason, and on account of its accessibility, blood, and its components, are one of the best biological fluids for investigating the cell aging process in normal and pathological conditions Homeostatic mechanisms must continuously adjust the balance between RBC production and destruction to maintain an appropriate number of circulating RBCs. Whereas, as mentioned before, the control of RBC production by Epo has a well- known mechanism [22], the intrinsic mechanism of underlying changes in the RBCs life span that lead to their destruction, remains largely unknown. It has been postulated that Phosphatidylserine (PS) and CD47 are the key determinants of RBC phagocytosis [23,24] and, more recently, it has been demonstrated that the quantitative aspects of these dynamics are related to oxygen homeostasis [25]. Specifically, it is suggested that PS and CD47 define a molecular algorithm that sets the timing of RBC phagocytosis. Significant changes in RBC lifespan, described in the literature, can be explained as alternative outcomes of this algorithm when it is executed in different conditions of oxygen availability. This theoretical model provides a unified framework to understand a variety of empirical observations regarding RBC biology and highlights the role of RBC lifespan as a key element of RBC homeostasis. Accordingly, this statement is based on two main assumptions. First, that the pattern of PS and CD47 expression changes during the life of the cell, as evidenced by differences between young and aged RBCs, and second, that the conditions that trigger RBC phagocytosis differ in the subsequent behavior they elicit on macrophages. Probably, the combined effects of accelerated PS expression and the lower CD47 expression may induce an immune response against host RBCs with the production of anti-RBC antibodies that would result in a shortened RBC lifespan. Here Epo levels, depending on the levels of oxygen, might continuously adjust the value of the phagocytosis thresholds, thus fine-tuning the lifespan of circulating RBCs. It should be mentioned that the high levels of Oxidative Stress (OS) might also shorten RBC life span by accelerating the rate of PS exposure in the outer membrane of the cell. And that Hypoxia-Induced Factors (HIFs) might be involved in shortening RBC life span in newly young RBCs due to their lower content in catalase activity [26]. All these mechanisms are independent and might be acting simultaneously, and in a coordinated way, to determine the RBC lifespan. However, further research is needed to unveil all the mechanisms underlying RBC lifespan determination.
In future publications of this section, our research group will try to provide a holistic vision of a combination of these procedures for a better understanding of RBC senescence in normal and pathological conditions.
이 사건의 “먹어라” 신호는
스크램블레이스 활성화와 플리페이스 비활성화로 인한 포스파티딜세린의 내부에서 외부 막 잎으로 전위로 여겨지며[4],
둘 다 세포내 Ca²⁺ 농도 증가로 유발된다[21].
이 노화 진행은
골수 대식세포에 의한 식작용을 용이하게 하는 많은 RBC 표면 항원 변화를 동반한다(그림 9).
따라서
RBC는 태어난 동일 장소인 골수에서 사멸하며,
구조 구성 요소는 새로운 RBC 생성을 위해 재활용되어 멋진 재생 형태를 이룬다.
RBC 결함으로 인한 유전성 용혈성 빈혈(HHA)에서 세포 변형성은 거의 항상 손상되며,
비장 장벽으로 인해 대부분의 비정상 RBC가 보유되고 식작용으로 파괴된다.
앞서 언급한 바와 같이 전형적인 예는 HS로,
이는 정상 상황에서 RBC가 위험한 120일 수명 끝에 접근할 때 발생하는 것의 과장이다.
이 과정은 적혈구생성에 의한 활성 RBC 재생으로 지속적으로 보상되며, 이 이유와 접근성으로 인해 혈액과 그 구성 요소는 정상 및 병리 조건에서 세포 노화 과정을 조사하는 최고의 생물학적 체액 중 하나이다. 항상성 메커니즘은 순환 RBC 수를 유지하기 위해 RBC 생성과 파괴 간 균형을 지속적으로 조정해야 한다. 앞서 언급한 바와 같이 Epo에 의한 RBC 생성 제어는 잘 알려진 메커니즘을 가지지만[22], RBC 수명 변화의 근본 메커니즘으로 이어지는 파괴는 대체로 알려지지 않았다. 포스파티딜세린(PS)과 CD47이 RBC 식작용의 핵심 결정자라고 가정되었으며[23,24], 최근에는 이 역학의 정량적 측면이 산소 항상성과 관련됨이 입증되었다[25]. 구체적으로 PS와 CD47이 RBC 식작용 타이밍을 설정하는 분자 알고리즘을 정의한다고 제안된다. 문헌에 설명된 RBC 수명의 유의한 변화는 산소 가용성 조건에서 이 알고리즘이 실행될 때 대안적 결과로 설명될 수 있다. 이 이론 모델은 RBC 생물학에 대한 다양한 경험적 관찰을 이해하는 통합 프레임워크를 제공하며, RBC 수명을 RBC 항상성의 핵심 요소로 강조한다. 따라서 이 진술은 두 가지 주요 가정을 기반으로 한다. 첫째, 젊은과 노화된 RBC 간 차이로 증명된 바와 같이 세포 수명 동안 PS와 CD47 발현 패턴이 변화한다. 둘째, RBC 식작용을 유발하는 조건이 대식세포에 후속 행동을 다르게 유발한다. 가속화된 PS 발현과 낮은 CD47 발현의 결합 효과는 숙주 RBC에 대한 면역 반응을 유발하여 항-RBC 항체 생성으로 RBC 수명 단축을 초래할 수 있다. 여기서 산소 수준에 의존하는 Epo 수준은 식작용 임계값을 지속적으로 조정하여 순환 RBC 수명을 미세 조정할 수 있다. 높은 산화 스트레스(OS) 수준이 외부 막에서 PS 노출 속도를 가속화하여 RBC 수명을 단축할 수 있음도 언급해야 한다. 그리고 저산소 유도 인자(HIFs)가 카탈라아제 활동이 낮은 새로 젊은 RBC에서 RBC 수명을 단축하는 데 관여할 수 있다[26]. 모든 이러한 메커니즘은 독립적이며 동시에 조정된 방식으로 작용하여 RBC 수명을 결정할 수 있다. 그러나 RBC 수명 결정의 모든 근본 메커니즘을 밝히기 위해 추가 연구가 필요하다.
이 섹션의 미래 출판물에서 우리 연구 그룹은 정상 및 병리 조건에서 RBC 노화에 대한 더 나은 이해를 위해 이러한 절차의 홀리스틱 비전을 제공하려고 노력할 것이다.
Disclosure
The authors have no other relevant affiliations or financial involvement with any organization or entity with a financial interest in or financial conflict with the subject matter or materials discussed in the manuscript apart from those disclosed.
Acknowledgement
We are indebted to the European Commission for the Equality Plus (Erasmus+) Grant (Ref. 2019-1-TR01-KA202-076789) and to Mrs. Elena Krishnevskaya for her outstanding collaboration in rare anaemias research and in conditional support for the preparation of this manuscript.
Electron Microscopy Studies were performed in the “Escola Professional d’Hematologia Farreras Valenti” (University of Barcelona) under the leadership of Prof. Ciril Rozman Borstnar (Hemorheology Theoretical Basis and Clinical Applications 1983).
References
- Vives Corrons JL. The Rare Anaemias. Chapter of the Rare Diseases. Intechopen. 2019.
- Berga L, Feliu E, Ferran MJ, Rozman C. Contribution of Scanning Electron Microscopy to the structural study of human bone marrow. Sangre. 1987; 27: 3939.
- Quigley JG, Means RT, Glader B. The Birth, Life, and Death of Red Blood Cells: Erythropoiesis, The Mature Red Blood Cell, and Cell Destruction. In JP Greer, DA Arber, B Glader, AF List, RT Means, Jr., F Paraskevas, and J Foerster (Eds.), Wintrobe’s Clinical Hematology (13th ed. pp.83-124). Philadelphia Philadelphia, PA: Lippincott Williams & Wilkins. 2014.
- Yoshida H, Kawane K, Koike M, Mori Y, Uchiyama Y and Nagata S. Phosphatidylserine-dependent engulfment by macrophages of nuclei from erythroid precursor cells. Nature. 2005; 437: 754.
- Liang R, Ghaffari S. Advances in understanding the mechanisms of erythropoiesis in homeostasis and disease. Br J Haematol. 2016; 174: 661- 673.
- Weiss L. The structure of bone marrow: functional interrelationships of vascular and hemopoietic compartments in experimental hemolytic anemia: an electron microscopic study. J. Morph. 1965; 117: 467.
- DeBrulyin PPHS, Michelson TB, Thomas. The migration of blood cells of the bone marrow through the sinusoidal wall. J Morphol. 1971; 133: 417.
- Berga L, Vives Corrons JL, Feliu E, Woessner S, Rozman C. Hemorheology. Theoretical Basis and Clinical Applications. Salvat Editores (Barcelona). 1983.
- Lux S. Anatomy of the red blood cell membrane skeleton: Unanswered questions. Blood. 2016; 12: 187.
- Mebius RE, Kraal G. Structure and function of the spleen. Nat Rev Immunol. 2005; 5: 606.
- Pivkin IV, Peng Z, Karniadakis GE, Buffet PA, Dao M, and Suresh S. Biomechanics of red blood cells in human spleen and consequences for physiology and disease. Proc Natl Acad Sci USA. 2016; 113: 7804.
- Suresh S. Mechanical response of human red blood cells in health and disease: Some structure-property-function relationships. J Mater Res. 2006; 21: 1871.
- Berga L. Spleen and hemolysis. Medicina Clínica (Barcelona). 1985; 85: 273.
- Brovelli A, Minetti G. Red Cell Ageing. In: Bernhardt I, Ellory JC. (eds) Red Cell Membrane Transport in Health and Disease. Springer, Berlin, Heidelberg. 2003.
- Franco RS. The measurement and importance of red cell survival. Am J Hematol. 2009; 84: 109.
- Groner W, Mohandas N & Bessis M. New optical technique for measuring erythrocyte deformability with the ektacytometer. Clin Chem. 1980; 26: 1435.
- Lazarova E, Gulbis B, Oirschot BV & van Wijk R. Next-generation osmotic gradient ektacytometry for the diagnosis of hereditary spherocytosis: interlaboratory method validation and experience. Clin Chem Lab Med. 2017; 55: 394.
- King MJ, Behrens J, Rogers C, Flynn C, Greenwood D, Chamberset. Rapid flow cytometric test for the diagnosis of membrane cytoskeleton-associated haemolytic anaemia. Br J Haematol. 2000; 111: 924.
- Merola F, Barroso A, Miccio L, Memmolo P, Mugnano M, Ferraro P, et al. Biolens behavior of RBCs under optically-induced mechanical stress. Cytometry A. 2017; 91: 527.
- Rico LG, Juncà J, Ward MD, Bradford JA, Bardina J, Petriz J. Acoustophoretic Orientation of Red Blood Cells for Diagnosis of Red Cell Health and Pathology. Scientific Reports. 2018; 8: 15705.
- Bernhard I, Nguyen DB, Wesseling MC, Kaestner L. Intracellular Ca2+ Concentration and Phosphatidylserine Exposure in Healthy Human Erythrocytes in Dependence on in vivo Cell Age. Front Physiol. 2020; 10; 1629.
- Palis J, Segel GB. Developmental biology of erythropoiesis. Blood Rev. 1998; 12: 106.
- Bosman GJCGM, Lasonder E, Groenen-Döpp YAM, Willekens FLA, Werre JM, Novotý VMJ. Comparative proteomics of erythrocyte aging in vivo and in vitro. J. Proteom. 2010; 73: 396.
- Freikman I, Fibach E. Distribution and shedding of the membrane phosphatidylserine during maturation and aging of erythroid cells. Biochim. Biophys. Acta. 2011; 1808: 2773.

