Cells
. 2022 Feb 14;11(4):663. doi: 10.3390/cells11040663
Subacromial Bursa: A Neglected Tissue Is Gaining More and More Attention in Clinical and Experimental Research
Franka Klatte-Schulz 1,2,*, Kathi Thiele 3, Markus Scheibel 3,4, Georg N Duda 1,2,†, Britt Wildemann 1,5,†
Editor: Gundula Schulze-Tanzil
- Author information
- Article notes
- Copyright and License information
PMCID: PMC8870132 PMID: 35203311
Abstract
The subacromial bursa has long been demolded as friction-reducing tissue, which is often linked to shoulder pain and, therefore, partially removed during shoulder surgery. Currently, the discovery of the stem cell potential of resident bursa-derived cells shed a new light on the subacromial bursa. In the meanwhile, this neglected tissue is gaining more attention as to how it can augment the regenerative properties of adjacent tissues such as rotator cuff tendons. Specifically, the tight fibrovascular network, a high growth factor content, and the large progenitor potential of bursa-derived cells could complement the deficits that a nearby rotator cuff injury might experience due to the fact of its low endogenous regeneration potential. This review deals with the question of whether bursal inflammation is only a pain generator or could also be an initiator of healing. Furthermore, several experimental models highlight potential therapeutic targets to overcome bursal inflammation and, thus, pain. More evidence is needed to fully elucidate a direct interplay between subacromial bursa and rotator cuff tendons. Increasing attention to tendon repair will help to guide future research and answer open questions such that novel treatment strategies could harvest the subacromial bursa’s potential to support healing of nearby rotator cuff injuries.
초록
견봉하낭은
오랫동안 마찰을 줄이는 조직으로 인식되어 왔으며,
이는 종종 어깨 통증과 연관되어 어깨 수술 시 부분적으로 제거되곤 했다.
현재,
상주하는 점액낭 유래 세포의 줄기세포 잠재력 발견은
견봉하 점액낭에 대한 새로운 시각을 제시하고 있다.
the discovery of the stem cell potential of
resident bursa-derived cells shed a new light on
the subacromial bursa.
한편, 이 간과되었던 조직은
회전근개 힘줄과 같은 인접 조직의 재생 능력을 어떻게 증강시킬 수 있는지에 대한
관심으로 주목받고 있다.
특히,
활액낭 유래 세포의 조밀한 섬유혈관 네트워크,
높은 성장 인자 함량,
그리고 큰 전구세포 잠재력은 내인성 재생 능력이 낮은
인근 회전근개 손상이 겪을 수 있는 결핍을 보완할 수 있다.
본 리뷰는
활액낭 염증이 단순히 통증 유발자일 뿐인지,
아니면 치유를 시작하는 촉매 역할도 할 수 있는지에 대한 질문을 다룬다.
또한 여러 실험 모델들은
활액낭 염증과 그에 따른 통증을 극복하기 위한 잠재적 치료 표적들을 제시한다.
견봉하낭과 회전근개 힘줄 간의 직접적 상호작용을 완전히 규명하기 위해서는
더 많은 증거가 필요하다.
힘줄 수복에 대한 관심 증대는 향후 연구 방향을 제시하고 미해결 질문에 답하는 데 도움이 될 것이며, 이를 통해 새로운 치료 전략이 인근 회전근개 손상의 치유를 지원하기 위한 견봉하낭의 잠재력을 활용할 수 있을 것이다.
Keywords: subacromial bursa, bursitis, progenitor cells, inflammation, pain, augmentation
1. Introduction
Bursae are sac-like synovial structures that function as friction-reducing cushions at locations with high mechanical loading experience such as joints [1]. The subacromial respective subdeltoid bursa is the largest bursa in the human body, located at the shoulder laying between the acromion, deltoid, and the rotator cuff tendons (Figure 1). With such anatomical positioning, the bursa is in a clinically relevant location and linked to increasing numbers of musculoskeletal surgeries. Shoulder pain is among the most frequent musculoskeletal complaints, specifically in an aging society but also affects younger individuals such as athletes. Specifically, the subacromial bursitis, an inflammation of the subacromial bursa, is a common cause for shoulder pain [2,3,4]. There are manifold reasons for the development of a subacromial bursitis including recurrent overuse, acute trauma, subacromial impingement, calcific deposits, infection, autoimmune diseases, and inappropriate vaccination agent application (SIRVA, “shoulder injury related to vaccine administration” [5]). The latter being particularly relevant also in the current COVID-19 pandemic [6,7,8,9]. Treatment of bursitis is often performed conservatively using physiotherapy or injection of anti-inflammatory drugs in mild and moderate cases. The removal of parts of the bursa (partial bursectomy) is also a common procedure in severe cases that do not respond to conservative treatments [10]. In the majority of cases, a subacromial decompression is performed as well. If bursitis reaches a chronic stage, it can harm the surrounding structures, such as the supraspinatus (SSP) tendon of the rotator cuff, leading to tendinopathy or even tendon tear. However, it still must be elucidated if subacromial bursitis is the cause or consequence of an SSP tear, as both pathologies often occur simultaneously. An example of the appearance of bursitis in an arthroscopic image compared to a healthy bursa is depicted in Figure 2. Next to its role in the pathogenesis of shoulder pain, recent studies claim the bursa as a healing-promoting structure due to the presence of high proportions of stem cells, vascularization, and growth factors [11,12,13,14].
1. 서론
점액낭은
관절과 같이 기계적 부하가 높은 부위에서
마찰을 줄이는 완충 역할을 하는 주머니 모양의 활막 구조물이다[1].
견봉하점액낭 또는 삼각근하 점액낭은 인체에서 가장 큰 낭으로,
견봉, 삼각근, 회전근개 힘줄 사이에 위치한 어깨에 있다(그림 1).
subacromial respective subdeltoid bursa

이러한 해부학적 위치로 인해 활액낭은
임상적으로 중요한 부위에 위치하며
점점 더 많은 근골격계 수술과 연관되어 있다.
어깨 통증은
특히 고령화 사회에서 가장 흔한 근골격계 증상 중 하나이며,
운동선수와 같은 젊은 층에도 영향을 미친다.
특히 견봉하 활액낭의 염증인 견봉하 활액낭염은
견봉하 활액낭염 발생 원인으로는
반복적 과사용, 급성 외상, 견봉하 충돌 증후군, 석회화 침착, 감염, 자가면역 질환,
부적절한 백신 접종제 투여(SIRVA, “백신 투여 관련 어깨 손상” [5]) 등이 다양하다.
후자의 경우 현재 코로나19 팬데믹 상황에서도 특히 관련성이 높다[6,7,8,9]. 활액낭염 치료는 경증 및 중등도 사례에서 물리치료나 항염증제 주사 등 보존적 방법으로 시행되는 경우가 많습니다. 보존적 치료에 반응하지 않는 중증 사례에서는 활액낭 일부 제거술(부분 활액낭절제술)도 흔히 시행됩니다[10]. 대부분의 경우 견봉하 감압술도 함께 시행됩니다. 활액낭염이 만성 단계에 이르면 회전근개 상근(SSP) 건과 같은 주변 구조물에 손상을 입혀 건병증이나 심지어 건 파열로 이어질 수 있습니다. 그러나 견봉하 활액낭염이 상근 건 파열의 원인인지 결과인지는 아직 명확히 밝혀지지 않았습니다. 두 병변이 동시에 발생하는 경우가 많기 때문입니다. 관절경 영상에서 활액낭염의 모습과 건강한 활액낭의 비교 예는 그림 2에 제시되어 있습니다.
어깨 통증의 병인에서 활액낭의 역할 외에도,
최근 연구들은 활액낭이
높은 비율의 줄기세포, 혈관화, 성장 인자를 함유하고 있어
치유 촉진 구조물이라고 주장합니다 [11,12,13,14].
Figure 1.
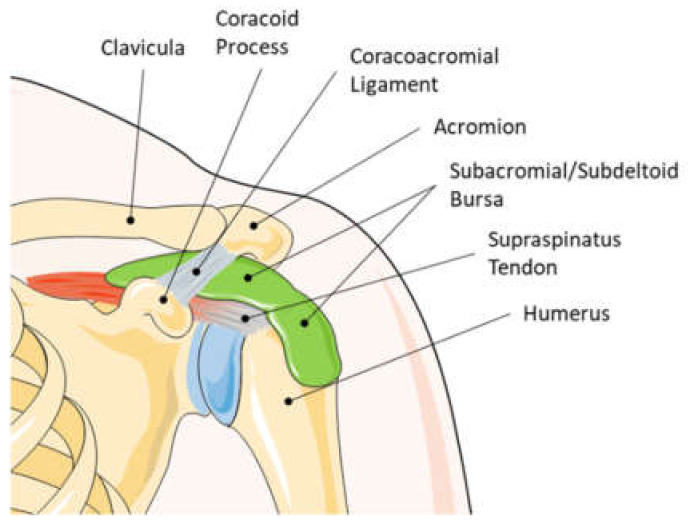
Anatomy of a left human shoulder joint.
The subacromial/subdeltoid bursa lays between the rotator cuff, the deltoid, and the acromion. Due to the close location to the rotator cuff tendons, the contribution of the subacromial bursa in the development or healing of tendon pathologies seems obvious. This graphic was created with an image from Servier Medical Art.
그림 1.
좌측 인간 어깨 관절의 해부학.
견봉하/삼각근하 활액낭은 회전근개, 삼각근, 견봉 사이에 위치한다. 회전근개 힘줄과 인접한 위치로 인해, 견봉하 활액낭이 힘줄 병리의 발생 또는 치유에 기여하는 것은 명백해 보인다. 이 그래픽은 Servier Medical Art의 이미지를 바탕으로 제작되었다.
Figure 2.
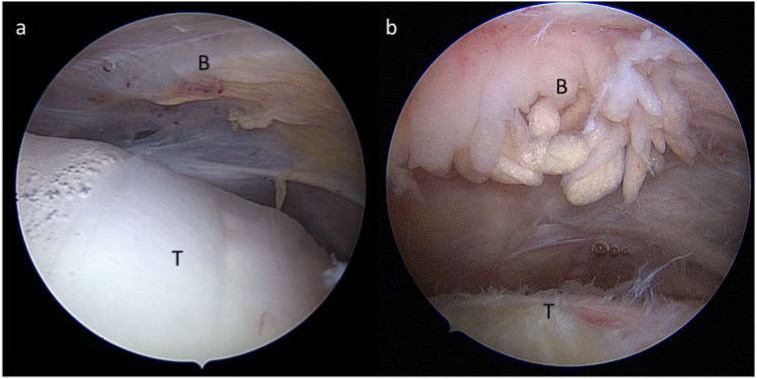
Arthroscopic view from a posterior portal during arthroscopy of a right shoulder showing (a) a normal subacromial/subdeltoid bursa (B) and healthy tendon (T) and (b) a severe hypertrophic subacromial bursitis (B) and fraying of the supraspinatus tendon (T).
그림 2.
우측 어깨 관절경 검사 중 후방 포털을 통한 관절경 소견으로 (a) 정상적인 견봉하/삼각근하낭(B)과 건강한 힘줄(T) 및 (b) 심한 비대성 견봉하낭염(B)과 상근 힘줄(T)의 마모를 보여줍니다.
There still exists a controversy on the role of the subacromial/subdeltoid bursa, whether it leads to the development of shoulder pathologies or is supporting its regeneration [15,16]. In consequence, different surgical strategies are chosen that either lead to no or partial resection of the subacromial bursa, depending on whether the bursa is perceived as a friend or foe of the shoulder pathology. Pre-clinical studies on bursa tissues and its cells arise and provide increasing evidence that the bursa could be an active contributor to improving, specifically, rotator cuff tears in the future [17,18].
견봉하/삼각근하낭의 역할에 대해서는 여전히 논란이 존재하며, 이 구조가 어깨 병리의 발생을 유도하는지 아니면 그 재생을 지원하는지에 대한 의견이 분분하다[15,16]. 결과적으로, 이 낭이 어깨 병리의 '친구'인지 '적'인지에 따라 견봉하낭을 전혀 절제하지 않거나 부분적으로 절제하는 등 서로 다른 수술 전략이 선택된다. 낭 조직 및 그 세포에 대한 전임상 연구가 등장하며, 특히 회전근개 파열의 개선에 낭이 적극적인 기여를 할 수 있다는 증거가 점차 증가하고 있다 [17,18].
2. History of Attention towards the Subacromial Bursa
Already in 1872, the clinical condition of sudden pain and the stiffness of the shoulder was described by Duplay and called “periarthritis humeroscapularis”. In 1934, EA Codman published the book “The Shoulder”, which laid the foundation for a significant understanding of the subacromial bursa and the pathogenesis of bursitis [19], the painful inflammation of the subacromial bursa that leads to swelling and restricted movement of the shoulder joint. Codman was the first to shed light on the role of rotator cuff tendons in the pathogenesis of subacromial bursitis. He described a clear relationships between rotator cuff tears and pathological changes in the subacromial bursa such as calcified particles, villus formation, inflammation, fluid, bursal adhesion, and strap formation [19]. Most of the publications at that time described the subacromial bursa in a clinical context with pain and restricted movement. The studies report on clinical and radiographic observations of painful shoulders, describing the possible pathogenesis of subacromial/subdeltoid bursitis with the appearance of calcified deposits in the tendon and bursa and invasion of immune cells [19,20,21,22,23]. Just recently, these calcific deposits were characterized and identified as being nanometer-sized rod-like crystals, mainly composed of hydroxyapatite. A fragmentation of these crystals as fine needle-like structures has a high potential to induce severe inflammation [24]. It was early recognized that the “floor” of the subacromial bursa, meaning the region that is closely located to the tendons, is the center of pathological changes [19,21]. The choice of treatment was primarily dependent on the severity of symptoms and the presence of calcified deposits in the bursa and the rotator cuff tendons [23]. The surgical excision of the calcified deposits was described as the treatment of choice in acute conditions resulting in immediate and permanent pain relief [21,23]. Other proposed treatment options for acute to chronic shoulder pain resulting from subacromial bursitis in the 1930–1950s included multiple needling and puncture of the bursal fluid [20,25] and injection of local anesthetics such as Novocain, or Procaine [20,26]. Non-invasive therapies used included heat and physical therapies [20], X-ray therapy with medium to high voltage X-rays [20,26,27], and ultrasonic waves [28,29]. The rationale of X-ray therapy and needling was explained by an increase in vascularization, which was hypothesized to reduce the tension and, thus, stiffness of the tissue [20]. Altogether, next to surgical excision, X-ray therapy was described to have the best efficacy at that time [20,30]. Despite the promising results, X-ray therapy disappeared in the 1960s due to the discovery of anti-inflammatory drugs and knowledge about X-ray-induced diseases [31]. From the 1950s on, increasing studies arose on direct treatments of the bursal inflammation with injection of cortisone analogues such as corticotropin [30] or hydrocortisone acetate [29,32]. In most cases, these anti-inflammatory treatments resulted in complete pain relief and return to normal function. In 1972, Neer introduced the term “impingement syndrome”, a painful pinch of soft tissues under the acromion during movement. He proposed a new treatment strategy, anterior acromioplasty, which reduces the subacromial compression by enlargement of the subacromial space [33]. Therefore, in severe cases that failed in healing or providing pain relief after conservative treatment, a subacromial decompression including partial bursectomy was a common scenario [34]. What remains from all the mentioned treatment options today are ultrasound and physiotherapeutic treatment and corticosteroid injections as well as partial bursectomy. In the case of rotator cuff tendinopathy, subacromial injections of platelet-rich plasma (PRP) may also be justified by a possible beneficial effect of the biological components of PRP. PRP’s involvement in pain reduction is likely, but details of its benefits are still under debate [35,36,37,38]. Furthermore, the effectiveness of hyaluronic acid injections, with proposed anti-inflammatory effects [39], were investigated in placebo controlled clinical trials, but could not compete with the effects of corticosteroids in the treatment of subacromial bursitis [40,41]. Nutritional supplementation is gaining popularity as a support in the treatment of tendinopathies [42,43,44], but specific results on its role in subacromial bursitis do not exist so far. Altogether, there is still inconclusive evidence of the efficacy regarding these different conservative and invasive treatment options as summarized in a systemic review [45]. Regarding the value of subacromial decompression, there still exists a controversial debate. Some clinical cohort studies support the value of subacromial decompression for improving clinical outcomes compared to pre-surgical situations and physical therapy alone [46,47]; whereas in a multicenter, randomized, placebo-controlled trial, subacromial decompression resulted in no benefit for the patient regarding pain and function 6 months and 1 year after surgery compared to placebo surgery [48]. Furthermore, in a randomized controlled trial, the long-term outcome for more than 10 years was compared in patients with rotator cuff tendinopathy receiving supervised exercise treatment alone or in combination with subacromial decompression, and no differences were found [49]. Finally, a recent systemic review concluded that subacromial decompression does not beneficially improve clinical outcomes for patients with subacromial pain compared to placebo surgery and physiotherapy only [50]. In Figure 3, the publication records of all PubMed-listed publications around the subacromial bursa from 1934 to 2021 are summarized.
2. 견봉하낭에 대한 관심의 역사
1872년 이미 듀플레이(Duplay)는 갑작스러운 통증과 어깨 경직을 동반한 임상 상태를 기술하며 이를 “상완견갑관절 주위염(periarthritis humeroscapularis)”이라 명명했습니다. 1934년 EA Codman은 “The Shoulder”라는 책을 출간하여 견봉하낭과 활액낭염의 병인에 대한 중요한 이해의 기초를 마련했습니다[19].
견봉하낭의 통증을 동반한 염증인 활액낭염은
견봉하낭의 부종과 어깨 관절의 운동 제한을 초래합니다.
Codman은 견봉하낭염 병인에서 회전근개 힘줄의 역할을 최초로 규명했습니다. 그는 회전근개 파열과 견봉하낭의 병리적 변화(석회화 입자, 융모 형성, 염증, 삼출액, 낭막 유착, 띠 모양 구조 형성 등) 사이의 명확한 연관성을 기술했습니다 [19]. 당시 대부분의 문헌은 통증과 운동 제한이 동반된 임상적 맥락에서 견봉하낭을 기술하였다. 연구들은 통증이 있는 어깨의 임상적 및 방사선학적 관찰을 보고하며, 힘줄과 활액낭 내 석회화 침착물의 출현 및 면역 세포 침입을 동반한 견봉하/삼각근하 활액낭염의 가능한 병인론을 기술하였다[19,20,21,22,23]. 최근에야 이러한 석회화 침착물이 주로 하이드록시아파타이트로 구성된 나노미터 크기의 막대 모양 결정체로 특성화 및 확인되었다. 이러한 결정체가 미세한 바늘 모양 구조로 분해될 경우 심각한 염증을 유발할 가능성이 매우 높습니다[24]. 견봉하낭의 “바닥”, 즉 힘줄에 인접한 부위가 병리학적 변화의 중심부라는 사실은 일찍이 인식되었습니다[19,21]. 치료 선택은 주로 증상의 중증도와 활액낭 및 회전근개 힘줄 내 석회화 침착물의 유무에 따라 결정되었다[23]. 석회화 침착물의 외과적 절제는 급성 상태에서 즉각적이고 영구적인 통증 완화를 가져오는 최선의 치료법으로 기술되었다[21,23]. 1930~1950년대 견봉하 활액낭염으로 인한 급성에서 만성 어깨 통증에 제안된 다른 치료 옵션으로는 활액낭액의 다중 침술 및 천자[20,25], 그리고 노보카인(Novocain)이나 프로카인(Procaine)과 같은 국소 마취제 주사가 포함되었다[20,26]. 사용된 비침습적 치료법으로는 온열 및 물리 치료[20], 중·고전압 X선 치료[20,26,27], 초음파 치료[28,29]가 있었다. X선 치료와 침술의 근거는 혈관 신생 증가로 설명되었으며, 이는 조직의 긴장을 감소시켜 경직을 완화할 것이라는 가설에 기반했다[20]. 종합적으로, 당시에는 수술적 절제술 다음으로 X선 치료가 가장 우수한 효능을 보인다고 기술되었다[20,30]. 유망한 결과에도 불구하고, 항염증제 발견과 X선 유발 질환에 대한 지식으로 인해 X선 치료는 1960년대에 사라졌다[31]. 1950년대부터 코르티코트로핀[30]이나 하이드로코르티손 아세테이트[29,32]와 같은 코르티손 유사체를 주사하여 활액낭 염증을 직접 치료하는 연구가 증가했습니다. 대부분의 경우 이러한 항염증 치료는 통증 완화와 정상 기능 회복을 가져왔다. 1972년 니어(Neer)는 운동 시 견봉 아래 연조직이 압박되어 발생하는 통증을 '충돌 증후군(impingement syndrome)'이라 명명했다. 그는 견봉하 공간을 확대하여 견봉하 압박을 감소시키는 새로운 치료 전략인 전방 견봉 성형술(anterior acromioplasty)을 제안했다[33]. 따라서 보존적 치료 후 치유가 되지 않거나 통증 완화가 이루어지지 않는 중증 사례에서는 부분 활액낭 절제술을 포함한 견봉하 감압술이 흔히 시행되었다[34]. 오늘날 언급된 모든 치료 옵션 중 남아 있는 것은 초음파 및 물리치료, 코르티코스테로이드 주사, 그리고 부분 활액낭 절제술이다. 회전근개 건병증의 경우, 혈소판이 풍부한 혈장(PRP)의 생물학적 성분이 유익한 효과를 발휘할 가능성이 있어 견봉하 PRP 주사가 정당화될 수 있다. PRP가 통증 감소에 관여할 가능성은 높으나, 그 효과의 세부 사항은 여전히 논쟁 중이다[35,36,37,38]. 또한 항염증 효과가 제안된 히알루론산 주사[39]의 효과는 위약 대조 임상 시험에서 조사되었으나, 견봉하 활액낭염 치료에서 코르티코스테로이드의 효과와 경쟁할 수 없었습니다[40,41]. 영양 보충제는 건병증 치료의 보조 수단으로 인기를 얻고 있으나[42,43,44], 견봉하 활액낭염에서의 역할에 대한 구체적인 결과는 아직 존재하지 않는다. 종합적으로, 체계적 문헌고찰[45]에서 요약된 바와 같이 이러한 다양한 보존적 및 침습적 치료 옵션의 효능에 대한 증거는 여전히 결정적이지 않다. 견봉하 감압술의 가치에 관해서는 여전히 논쟁이 존재한다. 일부 임상 코호트 연구는 수술 전 상황 및 물리치료 단독 대비 임상적 결과 개선 측면에서 견갑하 감압술의 가치를 지지한다[46,47]. 반면 다기관 무작위 위약 대조 시험에서는 수술 후 6개월 및 1년 시점에서 통증과 기능 측면에서 위약 수술 대비 견갑하 감압술이 환자에게 유의미한 이점을 제공하지 못했다 [48]. 또한 무작위 대조 시험에서 회전근개 건병증 환자를 대상으로 감독 하 운동 치료 단독 또는 견봉하 감압술 병용 치료를 시행한 후 10년 이상의 장기적 결과를 비교한 결과, 두 군 간 차이는 관찰되지 않았다[49]. 마지막으로, 최근의 체계적 문헌고찰에서는 견봉하 통증 환자에게 시행된 견봉하 감압술이 위약 수술 및 물리치료 단독 대비 임상적 결과를 유의미하게 개선시키지 못한다고 결론지었다 [50]. 그림 3에서는 1934년부터 2021년까지 PubMed에 등재된 견봉하낭 관련 모든 출판 기록을 종합하였다.
Figure 3.
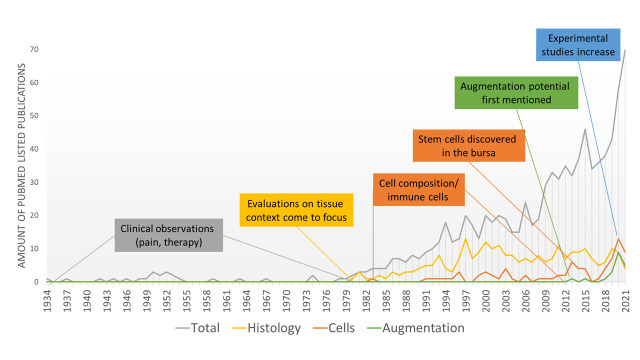
Overview of historical steps towards increased experimental research around the subacromial bursa: number of PubMed listed publications from 1934 to 2021 mentioning subacromial bursa OR subacromial bursitis (total) combined with the search terms “Histology”, “Cells”, and “Augmentation”.
3. Cells Come into Focus
In 1983, the composition of resting cells in the subacromial bursa was mentioned by Sarkar and Uhthoff describing an increase in cells in the bursal wall as well as proliferation of endothelial cells in the vasculature, indicating a proliferating degenerative phenotype of the subacromial bursa in the case of rotator cuff pathology. However, inflammatory leukocyte cell infiltrates were not identified as a common phenomenon [51]; whereas later on, others reported on the presence of T-lymphocytes and monocytes/macrophages in patients with impingement syndrome and pain at rest but not in patients experiencing pain only during movement [52]. Currently, it is not debatable that immune cells are a relevant cell type in subacromial bursa tissue, which is not only the case in pathological conditions but also in healthy bursae to a lesser extent [53]. This seems to indicate that the bursa can serve as a reservoir for relevant immune cell populations. However, to date, it is totally unclear how these cells and their release of inflammatory mediators are affecting adjacent tissue such as rotator cuff tendons.
In 2013, the mesenchymal stem cell (MSC) properties of bursa-derived cells were discovered, indicated by the expression of stromal-cell-associated markers and a multipotent differentiation potential into the adipogenic, osteogenic, and chondrogenic direction [54,55]. Later, others also confirmed the presence of resident MSCs in the human subacromial bursa tissue, which are similar or even better compared to bone marrow MSCs [17,56,57]. Next to the differentiation potential into the adipogenic, osteogenic, and chondrogenic direction, the cells also exhibited a tenogenic differentiation with increased expression of the tendon-associated markers scleraxis, tenomodulin, and tenascin C [18]. This tenogenic differentiation potential makes the subacromial bursa tissue even more interesting for its potential to support healing of the adjacent rotator cuff tendons. Bursa-derived stem cells also exhibited a neurogenic differentiation potential, identifying these cells as a more potent alternative source compared to bone marrow MSCs [58]. The isolation method either using enzymatic digestion or mechanical chopping, in all cases, provided sufficient MSC populations [59], but the age of the donors significantly affected the time to form colonies in culture [60], which is a typical phenomenon also for tenocytes of the rotator cuff [61,62]. Others reported that it was not patient characteristics but the size of the rotator cuff tear that affects the colony forming unit potential [63]. Altogether, the stem cell potential seems to be the most striking reason to preserve the subacromial bursa during shoulder surgery, as it can function as a reservoir for healing-promoting cells. Recently, we were able to show a new property of bursa-derived cells: a mechano-responsiveness. Mechano-transduction pathways, ECM formation, and matrix remodeling processes were activated as a reaction to physiological and/or pathological loading conditions. These hint at a physiological function of mechanical loading in bursa tissue, which should be considered in future studies investigating the role of the bursa in the shoulder joint [57].
3. 세포가 주목받기 시작하다
1983년 Sarkar와 Uhthoff는 견봉하낭의 휴지 상태 세포 구성을 언급하며, 회전근개 병변 시 견봉하낭의 증식성 퇴행성 표현형을 나타내는 낭벽 내 세포 증가 및 혈관 내 내피세포 증식을 기술했다. 그러나 염증성 백혈구 세포 침윤은 흔한 현상으로 확인되지 않았습니다[51]. 반면 이후 연구에서는 압박 증후군 및 휴식 시 통증이 있는 환자에서 T 림프구와 단핵구/대식세포의 존재를 보고했으나, 운동 시에만 통증을 경험하는 환자에서는 발견되지 않았습니다 [52]. 현재 견봉하낭 조직에서 면역 세포가 중요한 세포 유형이라는 점은 논란의 여지가 없으며, 이는 병리적 상태뿐만 아니라 건강한 활액낭에서도 어느 정도 관찰된다[53]. 이는 활액낭이 관련 면역 세포 집단의 저장소 역할을 할 수 있음을 시사한다. 그러나 현재까지 이러한 세포들과 그들이 분비하는 염증 매개체들이 회전근개 힘줄과 같은 인접 조직에 어떻게 영향을 미치는지는 전혀 명확하지 않다.
2013년,
활액낭 유래 세포의 중간엽 줄기세포(MSC) 특성이 발견되었는데,
이는 기질세포 관련 표지자의 발현과 지방형성, 골형성, 연골형성 방향으로의

| 중간엽 줄기세포(MSCs)는 다양한 세포 유형으로 분화할 수 있는 다능성 기질 요소입니다. MSCs는 퇴행성 질환 치료를 위한 우수한 치료 세포 공급원입니다. 이러한 이유로 많은 연구자들이 다른 MSC 공급원을 찾는 데 주력해 왔습니다. 현재 흔히 사용되는 공급원은 골수와 지방 조직이므로, 임상용 MSC를 얻기 위해서는 기증자의 수술이 필요하며 이는 기증자 이환율을 유발할 수 있습니다. 본 연구에서는 수술 후 폐기되는 조직 내 MSC의 존재 여부를 조사하였다. 3명의 부상 환자의 어깨에서 견봉하 활액낭 조직을 채취하였다. 활액낭 조직의 세포는 콜라게나제 처리를 통해 분리하였다. 분리된 세포는 일반 배양 시스템 하에서 연속적인 패싱을 통해 접종 및 증식시켰다. 세포의 MSC 특성을 평가하기 위해 mRNA 및 단백질 발현을 통해 MSC 표지자를 확인하였다. 다능성 능력은 분화 배지와 면역조직화학법을 사용하여 평가했다. 활액낭 유래 세포는 MSC 표지자인 CD29, CD73, CD90, PDGFRB(혈소판 유래 성장 인자 수용체-베타)를 발현했다. 또한 다능성 측면에서 활액낭 세포는 지방세포(지방 세포), 골세포(뼈 세포), 연골세포(연골 세포)로 분화했다. 요약하면, 우리는 수술 후 의료 폐기물인 견봉하낭에서 MSC를 생성할 수 있음을 보여주었다. |
이후 다른 연구에서도 인간 견봉하낭 조직 내 상주 MSC의 존재가 확인되었으며,
이는 골수 유래 MSC와 유사하거나 오히려 더 우수한 특성을 보였습니다[17,56,57].
지방, 골, 연골 분화 능력 외에도,
이 세포들은 건 관련 표지자인
스클레락시스(scleraxis), 테노모둘린(tenomodulin), 테나신 C(tenascin C)의 발현 증가와 함께
건 분화 능력도 나타냈다[18].
이러한 건원성 분화 능력은
견봉하낭 조직이 인접한 회전근개 힘줄의 치유를 지원할 잠재력으로 인해 더욱 주목받게 한다.
또한, 점액낭 유래 줄기세포는
신경원성 분화 능력도 보여주어,
이 세포들이 골수 MSC에 비해 더 강력한 대체 공급원임을 확인시켜 주었다 [58].
효소적 분해 또는 기계적 절단법을 이용한 분리 방법은 모든 경우에 충분한 MSC 군집을 제공했습니다[59]. 그러나 기증자의 연령은 배양에서 콜로니 형성 시간에 상당한 영향을 미쳤습니다[60]. 이는 회전근개 건세포에서도 흔히 관찰되는 현상입니다[61,62]. 다른 연구에서는 환자 특성보다는 회전근개 파열의 크기가 콜로니 형성 단위(CFU) 잠재력에 영향을 미친다고 보고했습니다[63]. 종합하면, 어깨 수술 시 견봉하낭을 보존해야 하는 가장 두드러진 이유는 줄기세포 잠재력으로, 이는 치유 촉진 세포의 저장고 역할을 할 수 있기 때문이다. 최근 우리는 활액낭 유래 세포의 새로운 특성인 기계적 반응성을 입증했다. 기계적 전달 경로, ECM 형성 및 기질 재구성 과정이 생리적 및/또는 병리적 부하 조건에 대한 반응으로 활성화되었다. 이는 활액낭 조직에서 기계적 부하의 생리적 기능을 시사하며, 향후 어깨 관절에서 활액낭의 역할을 연구할 때 고려되어야 한다 [57].
4. Bursitis and Pain: A Clear Correlation
The contribution of inflamed bursa tissue in shoulder pain is well accepted. This is supported by the fact that the subacromial bursa is innervated by several nerves, such as the suprascapular nerve and the lateral pectoral nerves and contains free nerve endings [64,65,66]. Thereby, neural structures are absent in the intima and found primarily in the subintima of the bursa in close proximity to blood vessels [67]. The presence of the neuropeptide substance P was rated as the reason for shoulder pain in patients with rotator cuff disease [68]. In addition, the expression of vascular endothelial growth factor (VEGF) in the subacromial bursa was found to be associated with motion pain in patients with rotator cuff tear or subacromial bursitis [69]. Additionally, it was demonstrated that inflammatory conditions in the synovium of the glenohumeral joint do not contribute to pain in rotator cuff disease but must arise from the bursal side [70]. From a histopathological point of view, it was described in rotator cuff tear patients that bursal inflammation, necrosis, hypertrophy, and oedema correlated with pain, contributing to the role of the subacromial bursa as a pain generator [12]. In summary, the presence of nerves and pain mediators in the subacromial bursa provokes most authors to conclude that a partial bursectomy helps to eliminate pain from the shoulder.
4. 활액낭염과 통증: 명확한 상관관계
염증성 활액낭 조직이
어깨 통증에 기여한다는 점은 널리 인정된다.
이는 견봉하낭이
견갑상신경 및 외측 흉신경 등 여러 신경에 의해 신경 분포를 받고
자유 신경 종말을 포함한다는 사실로 뒷받침된다[64,65,66].
이로 인해 신경 구조는 내막에는 존재하지 않으며 주로 혈관과 인접한 낭의 하내막에서 발견된다[67]. 회전근개 질환 환자의 어깨 통증 원인으로 신경펩타이드 물질 P의 존재가 평가되었다[68]. 또한 견봉하 활액낭에서의 혈관내피성장인자(VEGF) 발현이 회전근개 파열 또는 견봉하 활액낭염 환자의 운동 통증과 연관된 것으로 밝혀졌다[69]. 또한 견관절 활막의 염증 상태는 회전근개 질환의 통증에 기여하지 않으며, 반드시 활액낭 측에서 기인해야 함이 입증되었다[70]. 조직병리학적 관점에서, 회전근개 파열 환자에서 활액낭 염증, 괴사, 비후 및 부종이 통증과 상관관계를 보이며, 견봉하 활액낭이 통증 발생원으로서의 역할을 한다는 점이 기술되었다 [12]. 요약하면, 견봉하낭 내 신경과 통증 매개체의 존재는 대부분의 저자들이 부분적 낭절제술이 어깨 통증 제거에 도움이 된다고 결론 내리게 한다.
5. Bursa as a Friend or Foe for Rotator Cuff Repair
The properties of the subacromial bursa and its scientific interpretation let the subacromial bursa appear either as a friend or a foe for the development of tendon pathologies or its regeneration. The bursa was claimed as a possible reason for tearing due to the presence of active bone morphogenetic proteins (BMPs), such as BMP-2 and BMP-7, which might induce ectopic bone/cartilage formation and promoted tendon tearing. Therefore, the authors postulated the early removal of the subacromial bursa for better healing outcomes [71]. However, recently, no differences in BMP-2 expression were found in bursa tissue of healthy donors compared to different shoulder pathologies including partial and full-thickness SSP tear [53]. The presence of pro-inflammatory cytokines and cells in the bursa tissue often lays the basis for a negative association of the subacromial bursa in rotator cuff repair. It has been described that inflammatory cytokines, such as SDF-1, IL-1β, TNF-α, TGF-β, and IL-6 as well as pain-associated mediators (cyclooxygenase 1 (COX-1) and 2) and proteolytic enzymes (matrix metalloproteases (MMPs)) are increased in subacromial bursae from patients with rotator cuff tear or frozen shoulder compared to healthy controls [14,53,72,73,74,75,76,77,78]. Most authors postulated from this result that a partial bursectomy is necessary during rotator cuff surgery to reduce pain and inflammation and, thus, improve rotator cuff repair. However, only COX-2 expression in the subacromial bursa at the time of surgery was associated with failed rotator cuff healing 6 months post-surgery, whereas several other markers of inflammation, angiogenesis, and remodeling were not linked to healing [79]. Benson et al. investigated the cellular composition of the subacromial bursa of patients with impingement syndrome receiving a subacromial decompression. They found no correlation of histomorphometry regarding cell proliferation, fibroblast cellularity, vascularity, or the appearance of macrophages, leukocytes, mast cells, amyloid, or chondral metaplasia with the outcome after subacromial decompression [80]. Concluding from that, the pure quantity of inflammatory cells and bursa fibroblasts in the subacromial bursa does not influence the healing outcome.
The subacromial bursa is a well vascularized structure [13] with a vessel density of 1.8–3.4%, depending on whether the floor or roof of the bursa is being investigated [67]. Due to the location of the subacromial bursa, its tight fibrovascular network with high proportions of proliferating cells is also covering the tendon in the case of a tendon tear. Uhthoff and Sarkar found more signs of tissue repair rather than markable degeneration or necrosis of the bursa. Therefore, the preservation of the subacromial bursa as an important healing-promoting structure in the shoulder joint was advocated due to the fact of its fibrovascular properties [1]. Similar observations were made by others, supporting the localized bursal reaction at the tendon rupture side as a necessary feature for an optimal tendon repair after surgical reconstruction [11]. Moreover, the presence of fibrosis, the thickening of connective tissue in the bursa, was associated with a better clinical outcome after anterior acromioplasty for impingement syndrome [81]. In contrast to the assumption that inflammation is the driver of rotator cuff pathology, others interpreted the increase in bursal inflammation with the attempt of the bursa to activate rotator cuff repair. More interestingly, a decrease in tendon neo-angiogenesis and inflammation was found with age, but vice versa an increase in neo-angiogenesis, inflammation, and hypertrophy in the bursa was observed. Therefore, it was speculated that the bursa is taking over the reparative processes in the elderly [82]. A further benefit of the bursa for rotator cuff healing might be the presence of resident cells with progenitor potential in the bursa. This has led several authors to conclude that the bursa might be a promising tool in augmentation of rotator cuff repair [17,55].
5. 회전근개 수복에 있어 친구인가 적인가: 견봉하낭
견봉하낭의 특성과 과학적 해석은 힘줄 병리 발생 또는 재생 과정에서 이 낭이 친구가 될 수도, 적이 될 수도 있음을 시사한다. BMP-2 및 BMP-7과 같은 활성 골형성단백질(BMPs)의 존재로 인해 이 낭이 이소성 골/연골 형성을 유발하고 힘줄 파열을 촉진할 수 있다는 점에서 파열의 가능성 있는 원인으로 지목되었다. 따라서 저자들은 더 나은 치유 결과를 위해 견봉하낭의 조기 제거를 제안하였다[71]. 그러나 최근 연구에서는 부분 및 전층 견봉하낭 파열을 포함한 다양한 어깨 병변과 비교했을 때 건강한 기증자의 낭 조직에서 BMP-2 발현 차이를 발견하지 못했다[53]. 낭 조직 내 염증성 사이토카인과 세포의 존재는 회전근개 수복 시 견봉하낭의 부정적 연관성을 뒷받침하는 근거가 된다. SDF-1, IL-1β, TNF-α, TGF-β, IL-6와 같은 염증성 사이토카인과 통증 관련 매개체 (사이클로옥시게나제 1(COX-1) 및 2) 및 단백분해 효소(매트릭스 메탈로프로테아제(MMPs))가 건강한 대조군에 비해 회전근개 파열 또는 동결견 환자의 견봉하 활액낭에서 증가하는 것으로 보고되었다[14,53,72,73,74,75,76,77,78]. 대부분의 저자들은 이 결과로부터 회전근개 수술 시 통증과 염증을 감소시켜 회전근개 수복을 개선하기 위해 부분 활액낭 절제술이 필요하다고 가정했습니다. 그러나 수술 시 견봉하 활액낭의 COX-2 발현만이 수술 6개월 후 회전근개 치유 실패와 연관된 반면, 염증, 혈관신생 및 재형성의 다른 여러 지표들은 치유와 관련이 없었습니다 [79]. Benson 등은 견봉하 감압술을 받은 충돌 증후군 환자의 견봉하낭 세포 구성을 조사했다. 그들은 세포 증식, 섬유모세포 세포밀도, 혈관 분포, 대식세포·백혈구·비만세포·아밀로이드·연골성 변성의 조직형태학적 측정값과 견봉하 감압술 후 결과 간 상관관계를 발견하지 못했다 [80]. 이를 통해 견봉하낭 내 염증 세포 및 낭 섬유아세포의 순수한 양은 치유 결과에 영향을 미치지 않는다고 결론지었다.
견봉하낭은
혈관 분포가 풍부한 구조물[13]로,
낭 바닥 또는 지붕 부위 조사 여부에 따라 혈관 밀도가 1.8~3.4%이다[67].
견봉하낭의 위치 특성상, 이 낭의 조밀한 섬유혈관 네트워크는 건 파열 시에도 건을 덮고 있으며 증식 세포 비율이 높다. Uhthoff와 Sarkar는 낭의 현저한 퇴행이나 괴사보다는 조직 수복 징후가 더 많음을 발견했다. 따라서 견봉하낭이 지닌 섬유혈관적 특성으로 인해, 이 구조가 어깨 관절에서 중요한 치유 촉진 구조로서 보존되어야 한다는 주장이 제기되었다 [1]. 다른 연구자들도 유사한 관찰 결과를 제시하며, 수술적 재건 후 최적의 힘줄 수복을 위해 힘줄 파열 부위에서의 국소적 활액낭 반응이 필수적이라는 점을 지지하였다 [11]. 또한, 활액낭 내 결합 조직의 두꺼워짐인 섬유증의 존재는 충돌 증후군에 대한 전방 견봉 성형술 후 더 나은 임상 결과와 연관되었다[81]. 염증이 회전근개 병리의 주된 원인이라는 가정에 반해, 다른 연구자들은 활액낭 염증의 증가를 활액낭이 회전근개 수리를 활성화하려는 시도로 해석했다. 더 흥미롭게도, 연령이 증가함에 따라 힘줄의 신생혈관형성과 염증은 감소하는 반면, 활액낭에서는 신생혈관형성, 염증 및 비대가 증가하는 것으로 관찰되었다. 따라서 활액낭이 노년층에서 수복 과정을 주도한다는 추측이 제기되었다[82]. 활액낭이 회전근개 치유에 제공하는 추가적 이점은 활액낭 내에 전구세포 잠재력을 지닌 상주 세포가 존재한다는 점일 수 있다. 이로 인해 여러 저자들은 활액낭이 회전근개 수복을 증강시키는 유망한 도구가 될 수 있다고 결론지었습니다 [17,55].
6. Animal Models for Understanding the Role of the Bursa
For pre-clinical assessment and evaluation of therapeutic candidates, animal models are of great importance. They allow us to study the detailed role of the subacromial bursa inflammation and its impact on tendon healing. Recently, the subacromial bursa in the rat was characterized to have similar properties compared to the human bursa having a more fibrous structure beneath the acromion and is fattier in its medial portion [83]. Furthermore, the MSC potential of rat and mice bursa-derived cells is comparable to human bursa-derived cells [83,84], which provides the clinical relevance of such models. The interplay between tendon and bursa was also demonstrated in this model by showing that a bursectomy reduces the inflammatory response in the injured tendon [83]. A study in mice that received an SSP detachment without repair showed the importance of the cells on the bursal side of the SSP tendon in rotator cuff healing. However, the origin of these cells could not be fully identified, whether they come from the paratenon, bursa, or overlying muscle [85]. In rabbit and chicken rotator cuff repair models, the subacromial bursa significantly contributed to the tendon healing process, indicated by high cell proliferation at the bursal side of the tendon [86,87].
Experimental animal models represent the basis for testing strategies to target or better understand the bursa tendon interaction. MicroRNA-29a seems to play a role in the pathogenesis of bursal inflammation and fibrosis in patients with rotator cuff tear with shoulder stiffness. The microRNA-29 family members were described to inhibit the expression of fibrotic markers and extracellular matrix production (He et al., 2013). Therefore, the experimental approach of Ko et al. provided promising evidence of improved rotator cuff integrity and shoulder function in transgenic mice overexpressing microRNA-29a by repressing fibrosis of the subacromial bursa through direct targeting of Col3A1 mRNA [88]. Next to in vitro multipotent differentiation, in vivo implantation in mice of bursa-derived MSCs that were subjected to BMP-12 and seeded onto ceramic scaffolds also formed extensive bone and a tendon-like tissue, which underlines the potential of these cells for tendon repair [18]. Furthermore, in a patella tendon defect model in mice, bursa-derived MSCs that were incorporated into fibrin gels showed superior engraftment into the host tissue and a greater cell survival compared to bone marrow MSCs [89]. Bursa-derived MSCs might therefore be a preferable solution for a cell-assisted tendon repair.
6. 활액낭의 역할을 이해하기 위한 동물 모델
치료 후보 물질의 전임상 평가 및 검증을 위해 동물 모델은 매우 중요합니다. 이를 통해 견봉하 활액낭 염증의 세부적인 역할과 힘줄 치유에 미치는 영향을 연구할 수 있습니다. 최근 연구에서 쥐의 견봉하낭은 인간 낭과 유사한 특성을 보이며, 견봉 아래에는 섬유질 구조가 더 두드러지고 내측 부분은 지방 함량이 더 높다는 점이 밝혀졌다[83]. 또한 쥐와 생쥐의 낭 유래 세포가 가진 중간엽 줄기세포(MSC) 잠재력은 인간 낭 유래 세포와 비교할 수 있을 정도로 유사하다[83,84], 이는 이러한 모델의 임상적 관련성을 입증한다. 이 모델에서는 활액낭 절제술이 손상된 힘줄의 염증 반응을 감소시킨다는 점을 보여줌으로써 힘줄과 활액낭 간의 상호작용도 입증되었다[83]. 수복 없이 SSP(상완골 상완골두) 박리만 시행한 생쥐 연구에서는 회전근개 치유에 있어 SSP 힘줄의 활액낭 측 세포의 중요성을 보여주었다. 그러나 이 세포들의 기원이 파라테논, 활액낭, 또는 상부 근육 중 어디에서 유래하는지 완전히 규명되지는 못했다[85]. 토끼와 닭의 회전근개 수복 모델에서는 견봉하 활액낭이 힘줄 치유 과정에 크게 기여했으며, 이는 힘줄의 활액낭 측에서 높은 세포 증식으로 확인되었다[86,87].
실험 동물 모델은 활액낭-힘줄 상호작용을 표적화하거나 더 잘 이해하기 위한 전략을 시험하는 기초를 제공한다. 마이크로RNA-29a는 어깨 강직을 동반한 회전근개 파열 환자의 활액낭 염증 및 섬유화 병리에서 역할을 하는 것으로 보인다. 마이크로RNA-29 계열은 섬유화 표지자 발현과 세포외 기질 생성을 억제하는 것으로 보고되었다(He et al., 2013). 따라서 Ko 등의 실험적 접근법은 Col3A1 mRNA를 직접 표적화하여 견봉하낭의 섬유화를 억제함으로써 microRNA-29a를 과발현하는 형질전환 마우스에서 회전근개 무결성과 어깨 기능이 개선된다는 유망한 증거를 제시하였다[88]. 체외 다능성 분화 외에도, BMP-12를 처리하고 세라믹 스캐폴드에 접종한 활액낭 유래 MSC를 생쥐에 생체 이식한 결과, 광범위한 뼈와 힘줄과 유사한 조직이 형성되어 이러한 세포의 힘줄 복구 잠재력을 입증하였습니다 [18]. 또한, 생쥐 슬개건 결손 모델에서 피브린 겔에 포함된 활액낭 유래 MSC는 골수 유래 MSC에 비해 숙주 조직 내 우수한 생착률과 더 높은 세포 생존율을 보였다[89]. 따라서 활액낭 유래 MSC는 세포 보조 건 수복을 위한 선호 가능한 해결책이 될 수 있다.
7. Possible Therapeutic Targets
With the knowledge of increased inflammatory mediators in diseased bursa tissue, experimental studies have focused on strategies to target and understand bursal inflammation. The expression of SDF1, a chemokine that stimulates the recruitment of inflammatory cells, decreased in bursa cells by COX-2 inhibitors and steroids, providing a possible therapeutic strategy to treat subacromial bursitis [74]. Furthermore, isolated bursa cells respond to IL-1β stimulation with increased expression of SDF1, which indicates a possible mechanism of these mediators in subacromial bursitis [73]. Using epigallocatechin-3-gallate, a polyphenol in green tea, the IL-1β-induced expression of pain-associated factors and pro-inflammatory cytokines could be reversed in bursa-derived cells, leading to a reduced pro-inflammatory response and expression of pain mediators in tenocytes. This might provide a new strategy to treat pain in rotator cuff tendinopathy [78]. Another option to treat the IL-1β-induced pain mediation in the subacromial bursa could be to target the transforming growth factor (TGF)-β-activated kinase 1 (TAK-1). The TAK-1 inhibitor (5Z)-7-oxozeaenol decreased the expression of the important pain-associated mediators COX-2 and nerve growth factor (NGS) in bursa-derived cells [90]. Furthermore, TNF-α could be a potential target. Here, a lentivirus-mediated RNA interference of TNF-α in a rat rotator cuff disease model provoked a decreased production of the inflammatory mediators NF-κB, MMP-1, MMP-9, COX-1, COX-2, and SDF-1, suggesting this as a potential option to decrease inflammatory-dependent pain in the subacromial bursa [91]. To improve cell migration potential and proliferation, subacromial bursa-derived cells were stimulated with a one-time dosage of insulin or insulin-like growth factor (IGF-1), which might be useful for achieving an improved healing through the provision of a sufficient number of healing-promoting cells at the rotator cuff repair side. However, no significant impact of insulin or IGF-1 on cell proliferation and migration of bursa-derived cells could be detected [92].
7. 가능한 치료 표적
병변 활액낭 조직에서 염증 매개체 증가가 확인됨에 따라, 실험 연구는 활액낭 염증을 표적화하고 이해하는 전략에 집중해 왔다. 염증 세포의 유입을 촉진하는 케모카인인 SDF1의 발현은 COX-2 억제제와 스테로이드에 의해 활액낭 세포에서 감소하여 견봉하 활액낭염 치료를 위한 가능한 치료 전략을 제시한다 [74]. 또한 분리된 활액낭 세포는 IL-1β 자극에 반응하여 SDF1 발현이 증가하는데, 이는 견봉하 활액낭염에서 이러한 매개체들의 가능한 작용 기전을 시사한다[73]. 녹차의 폴리페놀인 에피갈로카테킨-3-갈레이트를 사용하면, IL-1β에 의해 유도된 통증 관련 인자 및 전염증성 사이토카인의 발현을 역전시킬 수 있었으며, 이는 건세포에서 전염증성 반응과 통증 매개체의 발현을 감소시켰습니다. 이는 회전근개 건병증의 통증 치료를 위한 새로운 전략을 제시할 수 있습니다[78]. 견봉하낭에서 IL-1β에 의해 유발되는 통증 매개 작용을 치료하는 또 다른 방법은 변형성장인자(TGF)-β 활성화 키나아제 1(TAK-1)을 표적으로 하는 것이다. TAK-1 억제제 (5Z)-7-옥소제아에놀은 활액낭 유래 세포에서 주요 통증 관련 매개체인 COX-2 및 신경성장인자(NGF)의 발현을 감소시켰다 [90]. 또한 TNF-α도 잠재적 표적이 될 수 있다. 쥐 회전근개 질환 모델에서 렌티바이러스 매개 TNF-α RNA 간섭은 염증 매개체인 NF-κB, MMP-1, MMP-9, COX-1, COX-2 및 SDF-1의 생산 감소를 유발하여, 이는 견봉하낭에서 염증 의존성 통증을 감소시키는 잠재적 옵션임을 시사한다 [91]. 세포 이동 및 증식 잠재력을 향상시키기 위해 견봉하낭 유래 세포를 인슐린 또는 인슐린 유사 성장 인자(IGF-1)의 단일 용량으로 자극했는데, 이는 회전근개 수복 부위에 충분한 수의 치유 촉진 세포를 공급함으로써 치유 개선을 달성하는 데 유용할 수 있다. 그러나 인슐린이나 IGF-1이 활액낭 유래 세포의 증식 및 이동에 미치는 유의미한 영향은 확인되지 않았다[92].
8. Clinical Strategies to Use the Augmentation Potential of the Subacromial Bursa
According to the mentioned promising properties of the subacromial bursa that could be beneficial for the augmentation of rotator cuff repair, some authors already postulated arthroscopic surgical strategies. Freislederer at al. described an easy and reliable surgical technique for bursal augmentation during repair of rotator cuff tears using an arthroscopic double-row suture technique with suturing of the lateral bursa to the tendon footprint. We postulate that the highly vascularized subacromial bursa could serve as a stimulating factor also to re-vascularize the re-attached and strangulated rotator cuff tendons [93]. A similar technique was used by Bhatia, who also prepared a bursa–tendon unit but with suturing of the posterior and posterolateral part of the bursa that covered a larger tendon area, possibly resulting in a more resilient repair [94]. A different approach describes the harvesting of bursa tissue and re-implantation of minced bursa tissue to the repair side. This is a further feasible method for bursa augmentation in rotator cuff repair, which can be used in combination with various surgical repair techniques [95,96]. In a preliminary study, the outcome after a more complex biological augmentation of rotator cuff repair using a stable clotted mixture of concentrated bone marrow, PRP, platelet-poor plasma (PPP), and subacromial bursa tissue was investigated. Using this technique, the patients’ functional outcome after rotator cuff repair significantly increased compared to pre-surgery after a minimum of 1 year follow up with a 93.8% substantial clinical benefit [97]. With the lack of a control group and the mixture of various potentially repair-promoting factors in the clot, it cannot be concluded what impact the subacromial bursa has on this approach. All authors hypothesized that the highly vascularized bursa tissue with significant proportions of repair-promoting stem cells has a strong potential in enhancing rotator cuff healing. In general, more clinical evidence is needed to evaluate the success of these promising techniques for the healing outcome of the patients.
8. 견봉하 활액낭의 증강 잠재력을 활용하는 임상 전략
회전근개 수복 증강에 유익할 수 있는 견봉하 활액낭의 유망한 특성에 따라, 일부 저자들은 이미 관절경 수술 전략을 제안했다. Freislederer 등은 회전근개 파열 수복 시 활액낭 증강을 위한 간단하고 신뢰할 수 있는 수술 기법을 기술했는데, 이는 활액낭을 힘줄 부착부에 봉합하는 관절경적 이중열 봉합 기법을 사용한다. 우리는 혈관 분포가 풍부한 견봉하 활액낭이 재부착되고 압박된 회전근개 힘줄의 재혈관화를 촉진하는 자극 인자로도 작용할 수 있다고 제안한다 [93]. Bhatia 역시 유사한 기법을 사용했는데, 그는 활액낭-힘줄 단위를 준비하되 활액낭의 후방 및 후측부위를 봉합하여 더 넓은 힘줄 영역을 덮도록 하여 더 탄력적인 수복을 가능하게 했다고 보고하였다 [94]. 다른 접근법은 활액낭 조직을 채취하여 잘게 다진 활액낭 조직을 수복 부위에 재이식하는 것을 기술한다. 이는 회전근개 수복 시 활액낭 보강을 위한 또 다른 실행 가능한 방법으로, 다양한 수술적 수복 기법과 병용할 수 있다 [95,96]. 한 예비 연구에서는 농축 골수, PRP, 혈소판 부족 혈장(PPP), 견봉하 활액낭 조직을 혼합한 안정화된 응고 혼합물을 이용한 더 복잡한 회전근개 수복 생물학적 보강술 후 결과를 조사하였다. 이 기법을 사용한 회전근개 수복 후 환자의 기능적 결과는 최소 1년 추적 관찰 후 수술 전 대비 유의미하게 증가하였으며, 93.8%의 상당한 임상적 이점이 관찰되었다 [97]. 대조군이 없었고 응고물 내에 다양한 잠재적 수복 촉진 인자가 혼합되어 있어 견봉하낭이 이 접근법에 미치는 영향을 단정할 수 없다. 모든 저자들은 수복 촉진 줄기세포가 상당 비율로 존재하는 고도로 혈관화된 활액낭 조직이 회전근개 치유를 증진시키는 강력한 잠재력을 지닌다고 가정하였다. 일반적으로, 이러한 유망한 기법들이 환자의 치유 결과에 미치는 성공 여부를 평가하기 위해서는 더 많은 임상적 증거가 필요하다.
9. Future Perspectives
The contribution of immune cells and pro-inflammatory cytokines in bursitis and pain is undeniable. However, it can be speculated that the bursa can serve as reservoir for important inflammatory cells and mediators that are able to initiate and promote tendon tissue repair. Therefore, a major task would be to find strategies to compensate and use inflammatory conditions in the bursa to initiate or promote healing of the nearby rotator cuff tendons. There remains a conflict between pain generation and healing promotion, and it should be carefully considered if there are other options to eliminate pain than removal of the bursa tissue. Some experimental strategies provided promising ideas to dampen pro-inflammatory and pain-generating processes, such as targeting the IL-1β or TNF-α pathways [78,90,91], which might help to overcome pain without a bursectomy in the future. However, the use of anti-inflammatory drugs should be handled with caution, as next to the wanted reduction in pro-inflammatory factors, inflammation-resolving mediators are also suppressed [98]. This is important to consider as processes such as the resolution of inflammation, which is actively mediated by specialized pro-resolving mediators [99], could be an interesting target and has not been studied in the subacromial bursa so far. The contribution of pro-resolving mediators, such as lipoxin, annexins, or resolvins, in the progress of rotator cuff tendinopathy was studied previously [100] and might also be a promising approach to dampen inflammation in bursa tissue in the future. Furthermore, what remains inconclusive from the literature is the direct interplay between the subacromial bursa and the rotator cuff tendons with the core question: is bursal inflammation the cause or consequence of rotator cuff pathologies? In addition, the role of mechanical forces in disease mechanisms remains unclear, even though the bursa serves as the important friction-reducing structure at the shoulder joint. We therefore speculate that mechanical forces are important triggers of inflammatory processes in the bursa and should be investigated in more detail in the future. The enrichment of stem cells, vasculature and growth factors at the tendon rupture site through bursal augmentation seems to be promising and easy and reliable surgical techniques for this augmentation were recently described [93,94,95,96]. However, functional follow-up results of clinical cohort studies comparing conventional rotator cuff repair to bursa-augmented strategies are needed to judge its effectivity.
9. 향후 전망
낭염과 통증에서 면역 세포 및 전염증성 사이토카인의 기여는 부인할 수 없다. 그러나 활액낭이 힘줄 조직 회복을 시작하고 촉진할 수 있는 중요한 염증 세포 및 매개체의 저장소 역할을 할 수 있다고 추측할 수 있다. 따라서 주요 과제는 활액낭 내 염증 상태를 보상하고 활용하여 인접 회전근개 힘줄의 치유를 시작하거나 촉진하는 전략을 찾는 것이다. 통증 유발과 치유 촉진 사이의 상충 관계는 여전히 존재하며, 활액낭 조직 제거 외에 통증을 제거할 다른 방법이 있는지 신중히 고려해야 한다. IL-1β 또는 TNF-α 경로 표적화[78,90,91]와 같은 일부 실험적 전략은 염증 촉진 및 통증 유발 과정을 억제하는 유망한 아이디어를 제공하여, 향후 활액낭 절제술 없이도 통증을 극복하는 데 도움이 될 수 있다. 그러나 항염증제 사용은 염증 촉진 인자의 감소라는 원하는 효과와 함께 염증 해결 매개체도 억제된다는 점에서 주의가 필요합니다[98]. 이는 염증 해결과 같은 과정이 전문적인 염증 해결 매개체에 의해 능동적으로 매개된다는 점[99]을 고려할 때 중요하며, 이는 흥미로운 표적이 될 수 있으나 지금까지 견봉하낭에서는 연구된 바 없습니다. 회전근개 건병증 진행에 대한 리폭신, 아넥신, 레졸빈과 같은 염증해결매개체의 기여도는 이전에 연구된 바 있으며[100], 향후 활액낭 조직의 염증을 완화하는 유망한 접근법이 될 수도 있다. 또한 문헌에서 명확히 규명되지 않은 부분은 견봉하낭과 회전근개 힘줄 간의 직접적 상호작용으로, 핵심 질문은 '낭 염증이 회전근개 병리의 원인인가 결과인가?'이다. 더불어, 낭이 어깨 관절에서 중요한 마찰 감소 구조로 기능함에도 불구하고, 질병 기전에서 기계적 힘의 역할은 여전히 불분명하다. 따라서 우리는 기계적 힘이 활액낭 내 염증 과정의 중요한 유발 요인이라고 추측하며, 향후 더 상세히 연구되어야 한다고 본다. 활액낭 증강술을 통한 힘줄 파열 부위의 줄기세포, 혈관 및 성장인자 농축은 유망해 보이며, 이를 위한 쉽고 신뢰할 수 있는 수술 기법이 최근 보고되었다[93,94,95,96]. 그러나 그 효과를 판단하기 위해서는 기존의 회전근개 봉합술과 활액낭 증강 전략을 비교한 임상 코호트 연구의 기능적 추적 관찰 결과가 필요하다.
10. Summary
In summary, biological evidence of the role of the subacromial bursa has been increasing over the last decades, and the existing knowledge as well as open questions are summarized in Figure 4. Starting as a predominant pain generator, the subacromial bursa has increasingly been considered over the last years as a promising healing-promoting structure in the shoulder joint, particularly because of the strong stem cell potential of the bursa-derived cells and distinct vasculature and growth factor content. A consensus on the role of inflammation has not yet been found, and future strategies should focus on eliminating pain but also on perceiving inflammatory mediators or resolution of inflammation pathways that might initiate or promote tendon healing. In general, further experimental and clinical research is still needed to fully elucidate the contribution of the subacromial bursa in the development and progression of tendon pathologies or its healing-promoting properties in the shoulder joint.
10. 요약
요약하면,
견봉하 활액낭의 역할에 대한 생물학적 증거는 지난 수십 년간 증가해 왔으며,
기존 지식과 미해결 문제는 그림 4에 요약되어 있다.
주된 통증 유발원으로 시작된 견봉하낭은
최근 몇 년간 특히 점액낭 유래 세포의 강력한 줄기세포 잠재력과
뚜렷한 혈관 및 성장인자 함량 덕분에
어깨 관절에서 유망한 치유 촉진 구조물로 점점 더 주목받고 있다.
염증의 역할에 대한 합의는 아직 이루어지지 않았으며,
향후 전략은 통증 제거뿐만 아니라
건 치유를 시작하거나 촉진할 수 있는 염증 매개체나 염증 해소 경로의 감지에도 초점을 맞춰야 한다.
일반적으로 건 병리의 발생 및 진행이나 치유 촉진 특성에 대한 견봉하낭의 기여를 완전히 규명하기 위해서는 추가적인 실험적 및 임상 연구가 여전히 필요하다. 일반적으로 견봉하낭이 힘줄 병리의 발생 및 진행에 기여하는 정도나 어깨 관절에서의 치유 촉진 특성을 완전히 규명하기 위해서는 추가적인 실험적·임상적 연구가 여전히 필요하다.
Figure 4.
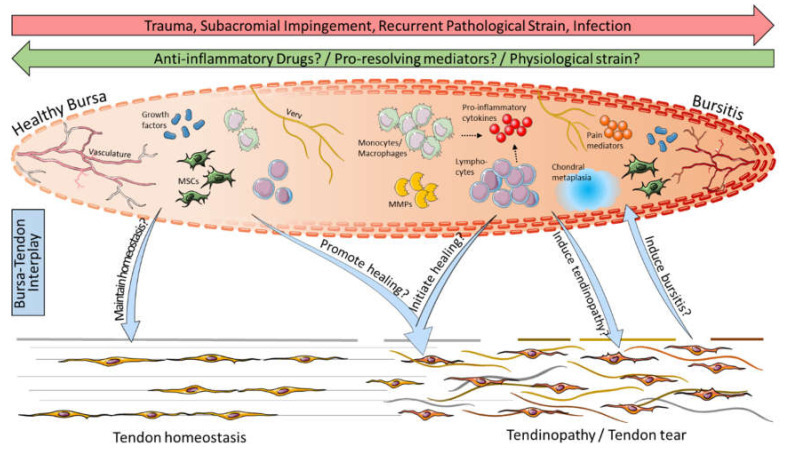
그림 4.
점액낭-건 상호작용 가능성:
외상, 충돌, 반복적 병리적 긴장 또는 감염에 의한 염증은 활액낭염을 유발하는 반면,
항염증제, 염증 해결 촉진 매개체 및/또는 생리적 긴장을 통해 활액낭염이 치유될 수 있다.
활액낭염은
특히 단핵구/대식세포 및 림프구(NK 세포, B 세포, T 세포)와 같은 면역 세포,
프로염증성 사이토카인(예: SDF-1, IL-1β, TNF-α), 매트릭스 메탈로프로테이나제(MMPs),
통증 매개체(예: COX-2, NGF, 서브스턴스 P), 연골성 변성 등이 특징이다.
이에 비해
건강한 활액낭은
면역 세포 수가 적고
성장 인자 및 중간엽 줄기세포(MSCs)가 우세하여
힘줄의 항상성 유지에 기여할 수 있다.
활액낭-힘줄 상호작용에서
활액낭 내 성장 인자와 MSC가 회전근개 파열을 포함한
건병증의 치유를 촉진할 수 있다는 가설이 제기되며,
염증 유발 세포 및 매개체가 힘줄 파열 부위에서 치유 연쇄 반응을 시작하는 데 도움이 될 수 있는지 규명해야 한다.
반대로, 활액낭염이 건의 병리적 상태의 원인인지 결과인지는
여전히 논쟁의 여지가 있습니다. 이 그래픽은 Servier Medical Art의 이미지를 사용하여 제작되었습니다.
Possible bursa–tendon interaction: Inflammation through trauma, impingement, recurrent pathological strain, or infection leads to the development of bursitis, whereas bursitis might be cured by anti-inflammatory drugs, pro-resolving mediators, and/or physiological strain. Bursitis is characterized in particular by the presence of immune cells such as monocytes/macrophages and lymphocytes (NK cells, B cells, and T cells), pro-inflammatory cytokines (e.g., SDF-1, IL-1β, and TNF-α), matrix metalloproteinases (MMPs), pain mediators (e.g., COX-2, NGF, and substance P), and chondral metaplasia. Compared to that, healthy bursae contain lower numbers of immune cells and predominate by growth factors and mesenchymal stem cells (MSCs) and, thus, might maintain tendon homeostasis. In bursa–tendon interplay it is hypothesized that growth factors and MSCs in the bursa can promote the healing of tendinopathies, including rotator cuff tears, and it has to be elucidated if pro-inflammatory cells and mediators might help to initiate healing cascades at the tendon rupture side. Vice versa, it is still debatable if bursitis is the cause or consequence of pathological conditions in the tendon. This graphic was created with images from Servier Medical Art.
Author Contributions
Conceptualization, F.K.-S.; writing—original draft preparation, F.K.-S.; writing—review and editing, K.T., M.S., G.N.D., and B.W.; visualization, F.K.-S. and M.S. All authors have read and agreed to the published version of the manuscript.
Funding
This work was funded by the German Research Foundation (grant number: KL 2983/3-1).
Institutional Review Board Statement
Not applicable.
Informed Consent Statement