Stem Cells Int
. 2019 Jul 24;2019:7513404. doi: 10.1155/2019/7513404
A Review on the Effect of Plant Extract on Mesenchymal Stem Cell Proliferation and Differentiation
Bhuvan Saud 1,2, Rajani Malla 1, Kanti Shrestha 2,✉
- Author information
- Article notes
- Copyright and License information
PMCID: PMC6681598 PMID: 31428160
Abstract
Stem cell has immense potential in regenerative cellular therapy. Mesenchymal stem cells (MSCs) can become a potential attractive candidate for therapy due to its remarkable ability of self-renewal and differentiation into three lineages, i.e., ectoderm, mesoderm, and endoderm. Stem cell holds tremendous promises in the field of tissue regeneration and transplantation for disease treatments. Globally, medicinal plants are being used for the treatment and prevention of a variety of diseases. Phytochemicals like naringin, icariin, genistein, and resveratrol obtained from plants have been extensively used in traditional medicine for centuries. Certain bioactive compounds from plants increase the rate of tissue regeneration, differentiation, and immunomodulation. Several studies show that bioactive compounds from plants have a specific role (bioactive mediator) in regulating the rate of cell division and differentiation through complex signal pathways like BMP2, Runx2, and Wnt. The use of plant bioactive phytochemicals may also become promising in treating diseases like osteoporosis, neurodegenerative disorders, and other tissue degenerative disorders. Thus, the present review article is aimed at highlighting the roles and consequences of plant extracts on MSCs proliferation and desired lineage differentiations.
초록
줄기세포는
재생 세포 치료 분야에서 엄청난 잠재력을 가지고 있습니다.
중간엽 줄기세포(MSCs)는
자체 재생 능력과 상피, 중배엽, 내배엽의 세 가지 계통으로 분화할 수 있는 뛰어난 특성으로 인해
치료법으로 유망한 후보로 주목받고 있습니다.
줄기세포는
질병 치료를 위한 조직 재생 및 이식 분야에서 엄청난 가능성을 보여주고 있습니다.
전 세계적으로 의약용 식물은
다양한 질병의 치료와 예방에 활용되고 있습니다.
식물에서 추출된
나링닌, 이카리인, 제니스틴, 레스베라트롤과 같은 식물 화학 성분은
전통 의학에서 수세기 동안 널리 사용되어 왔습니다.
특정 식물 유래 생물활성 화합물은
조직 재생 속도, 분화, 면역 조절을 촉진합니다.
여러 연구에서 식물 유래 생물활성 화합물이
BMP2, Runx2, Wnt와 같은 복잡한 신호 전달 경로를 통해
세포 분열 및 분화 속도를 조절하는 생물활성 매개체로서 특정 역할을 한다는 것이 밝혀졌습니다.
식물 생물활성 식물화학물질의 사용은
골다공증, 신경퇴행성 질환, 기타 조직 퇴행성 질환 치료에 유망한 가능성이 있습니다.
따라서 본 리뷰 논문은
식물 추출물이 MSC 증식 및 원하는 계통 분화에 미치는 역할과 영향을 강조하는 것을 목적으로 합니다.
1. Background
Stem cells are precursor biological cells that have the ability to self-renew and differentiate into multiple mature cells [1]. Stem cells divide into two major categories, i.e., embryonic stem cells and adult stem cells. Depending upon the differentiation capacity, they can be classified into unipotent, multipotent, pluripotent, or totipotent stem cells. These cells provide the platform to investigate cellular development, maintenance, and differentiation [2]. In 1976, Friedenstein and his coworkers discovered MSCs from mouse bone marrow [3]. MSCs are multipotent stem cells which are nonhematopoietic and possess the ability to differentiate into multilineage cells. The International Society for Cellular Therapy (ISCT) proposes minimal criteria to define human MSC: they are plastic adherent; express CD105, CD73, and CD90; lack expression of CD45, CD34, CD14 or CD11b, CD79a or CD19, and HLA-DR surface molecules; and are capable of differentiating into multilineage cells, i.e., osteoblasts, adipocytes, and chondroblasts in vitro [4]. Human MSCs show morphological subpopulation like rapidly self-renewing cells, spindle-shaped cells, and flattened cells (FC) [5]. Several studies have shown that under standard environmental condition, MSCs can be isolated from different sites including the bone marrow [6, 7], adipose tissue [8, 9], cord and peripheral blood [10, 11], placenta [12], umbilical cord [13, 14], fetal liver [15], fetal lungs [16], dental pulp [17, 18], periodontal ligament [19], trabecular bone [20], compact bone [21], synovial membrane [22], cruciate ligaments [23], amniotic fluid [24, 25], and endometrium [26]. MSCs have been used for several clinical trials for tissue repairing and treating immune-mediated disease including cardiac ischemia, limb ischemia, amyotrophic lateral sclerosis, diabetes, ischemic stroke, osteoarthritis, liver cirrhosis, liver failure, graft versus host disease, Crohn's disease, multiple sclerosis, respiratory distress syndrome, amyloidosis, and rheumatoid arthritis [27–29]. At the National Institute of Health (NIH), USA, several clinical trials are running in different aspects of MSCs used for treatment and regenerative therapy. A total of 945 studies have been found that involve the use of MSCs for different clinical phages among which 264 studies have been completed. Among them, some studies have used dietary supplements including herbal compounds for the trial [30].
1. 배경
줄기세포는
자기 재생 능력과 다양한 성숙한 세포로 분화할 수 있는 전구 생물학적 세포입니다 [1].
줄기세포는
두 가지 주요 범주로 나뉩니다:
배아 줄기세포와 성체 줄기세포.
분화 능력에 따라
단일 분화능, 다분화능, 다능성, 또는 전능성 줄기세포로 분류됩니다.
이 세포들은
세포 발달, 유지, 분화를 연구하는 플랫폼을 제공합니다 [2].
1976년 Friedenstein과 그의 연구진은
쥐의 골수에서 MSC를 발견했습니다 [3].
MSC는 비혈액 생성성 다능성 줄기세포로,
다계열 세포로 분화할 수 있는 능력을 갖추고 있습니다.
국제 세포 치료학회(ISCT)는
인간 MSC를 정의하기 위한 최소 기준을 제안했습니다:
플라스틱에 부착 가능하며;
CD105, CD73, 및 CD90을 발현하며;
CD45, CD34, CD14 또는 CD11b, CD79a 또는 CD19, 및 HLA-DR 표면 분자를 발현하지 않으며;
체외에서 다계열 세포로 분화할 수 있는 능력,
즉 골세포, 지방세포, 및 연골세포로 분화할 수 있는 능력을 갖추고 있습니다 [4].
인간 MSC는
빠르게 자기 재생하는 세포,紡錘형 세포, 평평한 세포(FC)와 같은 형태학적 하위 집단을 보여줍니다 [5].
여러 연구에서 표준 환경 조건 하에서
MSC는
골수 [6, 7], 지방 조직 [8, 9], 탯줄 및 말초 혈액 [10, 11], 태반 [12], 탯줄 [13, 14], 태아 간 [15], 태아 폐 [16],
치아 펄프 [17, 18], 치주 인대 [19], 골격골 [20], 밀집골 [21],
활막 [22], 십자 인대 [23], 양수 [24, 25], 자궁 내막 [26] 등에서
분리될 수 있음을 보여주었습니다.
MSCs는
심근 허혈, 사지 허혈, 근위축성 측삭 경화증, 당뇨병, 허혈성 뇌졸중,
골관절염, 간경변, 간부전, 이식편 대 숙주 질환, 크론병, 다발성 경화증, 호흡 곤란 증후군, 아밀로이드증, 류마티스 관절염 등
조직 재생 및 면역 매개 질환 치료를 위한 여러 임상 시험에 사용되었습니다 [27–29].
미국 국립 보건원(NIH)에서는
MSC를 치료 및 재생 치료에 활용하는 다양한 측면의 임상 시험이 진행 중입니다.
MSC를 다양한 임상 단계에 적용한 연구 총 945건이 확인되었으며,
이 중 264건이 완료되었습니다.
이 중 일부 연구에서는
임상 시험에 식이 보조제 및 허브 성분을 포함했습니다 [30].
From the initial development of human civilization, plants have been used as a medicine for improving growth and development. Medicinal plants are widely acceptable for the treatment of a variety of diseases. The World Health Organization (WHO) declared that the best sources of a variety of drugs are plant derivatives [31]. Globally, around 75% of the population from the developing and developed nations like Britain, Germany, and France use plants and their extracts as a medicine [32]. Out of 150 thousand plants being studied, med-clinically important components have been observed in many of them [33]. Plant derivatives have shown to promote stem cell proliferation and multilineage differentiation. The bioactive compounds obtained from plant extracts could become an alternative, cost effective treatment for bone marrow transplantation and cancer [34]. Most plants have been used both traditionally and therapeutically, but the exact mechanism of action on MSCs of only few plant extracts has been proved. Establishing the differentiation of MSCs into desired lineage-committed progenitors in the presence of a certain plant extract can open a new horizon for regenerative medicine and treatment. Thus, the present review highlights the role of bioactive compounds from plant extracts on MSCs proliferation and differentiation and their use in regenerative therapy and medicine.
인류 문명의 초기 단계부터 식물은
성장과 발달을 개선하기 위한 약물로 사용되어 왔습니다.
약용 식물은
다양한 질병의 치료에 널리 수용되고 있습니다.
세계보건기구(WHO)는
다양한 약물의 최상의 원천이 식물 유래 물질이라고 선언했습니다 [31].
전 세계적으로
영국, 독일, 프랑스 등 개발도상국과 선진국의 약 75% 인구가
식물과 그 추출물을 약물로 사용합니다 [32].
15만 종의 식물 중 많은 종에서
의학적 중요성이 있는 성분이 관찰되었습니다 [33].
식물 유래 물질은
줄기세포 증식과 다계열 분화를 촉진하는 것으로 나타났습니다.
식물 추출물에서 얻은 생물활성 화합물은
골수 이식 및 암 치료를 위한 대체적이고
비용 효율적인 치료법이 될 수 있습니다 [34].
대부분의 식물은
전통적으로 및 치료 목적으로 사용되어 왔지만,
식물 추출물의 MSC에 대한 정확한 작용 메커니즘은 극히 일부에만 입증되었습니다.
특정 식물 추출물의 존재 하에서
MSC가 원하는 분화 경로로 분화되는 것을 확립하는 것은
재생 의학과 치료에 새로운 지평을 열 수 있습니다.
따라서 본 리뷰는
식물 추출물의 생물활성 화합물이
MSC의 증식과 분화에 미치는 역할 및 재생 치료와 의학에서의 활용을 강조합니다.
2. MSCs Proliferation Potential
MSCs are divided by mitosis but are not capable of unlimited cell division in vitro due to senescence, also called irreversible growth arrest phenomenon first described by Hayflick in the 1960s [35]. Increased expression of senescence-associated β-galactosidase (SA-β-Gal) is responsible for stoppage of further division of MSCs [36]. With the increase in SA-β-Gal gene expression and accumulation of excessive reactive oxygen species (ROS) and progressive shortening of the telomeres or modified telomeric structure [35, 37, 38], morphological and biological changes occur and cell undergoes senescence. Morphologically, MSCs change into enlarged and irregular-shaped cells. Different studies reported that single cell-derived colonies of MSCs can expanded up to 30-50 population doublings in about 10-18 weeks [39–41]. In passages 6 and 12, population doubling time (PDT) is the shortest for umbilical cord-derived stem cell (UC-MSC) compared to bone marrow-derived stem cell (BM-MSC) and adipose tissue-derived stem cell (AT-MSC); also, the proliferation rate is the highest from UC-MSCs [42]. The proliferation and persistence rates of stem cells have been influenced by tissue sources, donor's age, and culture conditions [43]. In addition, older donor's cells (>66 years) have lower proliferative ability than younger ones (about <30 years of age) and pediatric donors have the highest proliferation rate in in vitro standard condition [41, 44]. Meanwhile, the absence of irreversible growth arrest could mean neoplastic transformation of MSCs. Furthermore, the culture system also influences homing and differentiation abilities of stem cells. The three-dimensional culture system has more expansion than the two-dimensional culture system [45]. The study has shown that UC-MSCs exhibit a higher proliferation capacity than BM-MSCs [46] and BM-MSCs have greater proliferation capability compared to muscle-derived stem cells (MD-MSCs) and AT-MSCs [47].
2. MSC 증식 잠재력
MSCs는 분열을 통해 증식하지만,
노화(Hayflick이 1960년대 처음 기술한 불가역적 성장 정지 현상)로 인해
체외에서 무제한 세포 분열이 불가능합니다 [35].
노화 관련 β-갈락토시다아제(SA-β-Gal)의 발현 증가가
MSCs의 추가 분열 중단을 유발합니다 [36].
SA-β-Gal 유전자 발현 증가,
과도한 활성산소종(ROS) 축적,
텔로미어의 점진적 단축 또는 텔로미어 구조의 변화[35, 37, 38]와 함께
형태학적 및 생물학적 변화가 발생하며
세포는 노화 과정을 겪습니다.
형태학적으로 MSC는
확대되고 불규칙한 모양의 세포로 변합니다.
다양한 연구에서 단일 세포에서 유래한 MSC 콜로니는
약 10~18주 동안 30~50회 인구 배열까지 확장될 수 있다고 보고되었습니다 [39–41].
6차 및 12차 배양 시,
배양 세포 수 배가 시간(PDT)은
탯줄 유래 줄기세포(UC-MSC)가 골수 유래 줄기세포(BM-MSC) 및 지방 조직 유래 줄기세포(AT-MSC)보다 가장 짧으며,
증식 속도도 UC-MSC에서 가장 높습니다[42].
줄기세포의 증식률과 지속률은
조직 출처, 기증자 연령, 배양 조건에 의해 영향을 받습니다 [43].
또한, 고령 기증자(>66세)의 세포는
젊은 기증자(약 30세 미만)보다 증식 능력이 낮으며,
소아 기증자는 체외 표준 조건에서 가장 높은 증식률을 보입니다 [41, 44].
한편,
불가역적 성장 정지의 부재는
MSC의 종양 변형을 의미할 수 있습니다.
또한 배양 시스템도 줄기세포의 귀환 및 분화 능력에 영향을 미칩니다.
3차원 배양 시스템은
2차원 배양 시스템보다 더 높은 확장성을 보입니다 [45].
연구 결과,
UC-MSCs는 BM-MSCs보다 더 높은 증식 능력을 보였으며 [46],
BM-MSCs는 근육 유래 줄기세포 (MD-MSCs) 및 AT-MSCs보다 더 높은 증식 능력을 나타냈습니다 [47].
3. MSCs Multilineage Differentiation Potential
According to ISCT criteria, MSCs must be able to differentiate into multilineage cells including osteoblasts, adipocytes, and chondroblasts but it depends upon in vitro conditions as well as the cell source [4]. Depending upon the source, UC-MSCs have high potential to differentiate into osteoblast, chondrocyte, adipocyte, skeletal muscle cells, endothelial cells, cardiomyocyte-like cells, and neuronal cells. BM-MSCs differentiate into osteoblast, chondrocyte, adipocyte, tenocyte, and vascular smooth muscle cells. In addition, periosteum MSCs (P-MSCs), synovial MSCs (S-MSCs), adipose tissue MSCs (AT-MSCs), circulating MSCs (C-MSCs), and tendon-derived MSCs (TD-MSCs) also have potential of multilineage differentiation under in vitro standard condition [47].
3. MSCs의 다계열 분화 잠재력
ISCT 기준에 따르면 MSC는 골세포, 지방세포, 연골세포로 분화할 수 있어야 하지만, 이는 체외 조건 및 세포 원천에 따라 달라집니다 [4]. 원천에 따라 UC-MSC는 골세포, 연골세포, 지방세포, 골격근 세포, 내피 세포, 심근 세포 유사 세포, 신경 세포로 분화할 수 있는 높은 잠재력을 가지고 있습니다. 골수 유래 MSCs(BM-MSCs)는 골세포, 연골세포, 지방세포, 힘줄 세포, 혈관 평활근 세포로 분화합니다. 또한 골막 MSCs(P-MSCs), 활막 MSCs(S-MSCs), 지방 조직 MSCs(AT-MSCs), 순환 MSCs(C-MSCs), 힘줄 유래 MSCs(TD-MSCs)도 체외 표준 조건 하에서 다계열 분화 잠재력을 가지고 있습니다[47].
3.1. Adipogenic Differentiation
Adipocyte-specific gene expression, which brings the appearance of intracellular lipids, characterizes phenotypic adipocyte. Sequential action of transcription factors C/EBPβ (CCAAT/enhancer binding protein β), C/EBPα (CCAAT/enhancer binding protein α), and PPARγ (peroxisome proliferator-activated receptor γ) is necessary for 3T3-L1 preadipocyte differentiation [48]. Mitochondrial metabolism is important for adipocytic differentiation by increased expression of UCP-1, UCP-2, and UCP-3 mRNA. The increased level of UCP1 is associated with the brown fat phenotype in newly differentiated adipocytes [49]. In addition, fibroblast growth factor-2 (FGF2) and 17-beta estradiol have induced adipocyte characteristics in cell [50, 51]. Studies show that BM-MSCs [52], S-MSCs [53], and UC-MSCs [54] differentiate into adipocytes. In the presence of dexamethasone and insulin supplement in the medium, UC-MSCs differentiate into adipocytes [54].
3.1. 지방 분화
지방세포 특이적 유전자 발현은
세포 내 지질의 출현을 특징으로 하며,
이는 지방세포의 형질을 결정합니다.
전사 인자 C/EBPβ (CCAAT/enhancer binding protein β), C/EBPα (CCAAT/enhancer binding protein α), 및 PPARγ (peroxisome proliferator-activated receptor γ)의 순차적 작용은 3T3-L1 전지방세포의 분화에 필수적입니다 [48]. 미토콘드리아 대사 과정은 UCP-1, UCP-2, UCP-3 mRNA 발현 증가를 통해 지방세포 분화에 중요합니다. UCP1 수준 증가가 신규 분화된 지방세포의 갈색 지방 세포 형질과 연관되어 있습니다 [49]. 또한 섬유아세포 성장 인자-2 (FGF2)와 17-베타 에스트라디올은 세포 내 지방세포 특성을 유도합니다 [50, 51].
연구 결과,
골수 유래 중간엽 줄기세포(BM-MSCs) [52],
췌장 유래 중간엽 줄기세포(S-MSCs) [53], 및 태반 유래 중간엽 줄기세포(UC-MSCs) [54]가
지방세포로 분화됩니다.
배지 내에 데ksametason과 인슐린을 보충했을 때
UC-MSCs는 지방세포로 분화됩니다 [54].
3.2. Chondrogenic Differentiation
Transforming growth factor-beta (TGF-β) and bone morphogenetic proteins (BMPs) are the most important inducers for chondrogenic differentiation of MSCs [55]. The activation of the Wnt signaling pathway is also involved in chondrogenesis and development of cartilage, and this pathway is activated by glycogen synthase kinase 3 (GSK-3) [56, 57]. Several studies showed that MSCs from different sources differentiated into chondrocytes including BM-MSCs [11, 58], S-MSCs [59], AD-MSCs [60], peripheral blood MSCs (PB-MSCs) [11], and TD-MSCs [61]. Under controlled in vitro condition, supplements such as transforming growth factor-β1, ascorbate-2-phosphate, dexamethasone, and growth and differentiation factor-5 (GDF5) [54, 62, 63] promote chondrogenic differentiation. Formation of shiny cell spheres which express type II collagen in cultures is the evidence for chondrogenic differentiation of MSCs which can be demonstrated by molecular technique and immunohistochemistry.
3.2. 연골 분화
변형 성장 인자-베타 (TGF-β)와 골형성 단백질 (BMPs)은 MSC의 연골 분화에 가장 중요한 유도인자입니다 [55]. Wnt 신호 전달 경로의 활성화도 연골 분화와 연골 발달에 관여하며, 이 경로는 글리코겐 합성 키나제 3 (GSK-3)에 의해 활성화됩니다 [56, 57]. 다양한 연구에서 다양한 출처의 MSC가 연골세포로 분화되었으며, 이는 골수 유래 MSC(BM-MSCs) [11, 58], S-MSCs [59], AD-MSCs [60], 말초 혈액 MSC(PB-MSCs) [11], 및 TD-MSCs [61]를 포함합니다. 통제된 체외 조건에서 변형 성장 인자-β1, 아스코르브산-2-인산, 데카메타손, 성장 및 분화 인자-5(GDF5) [54, 62, 63]와 같은 보조제는 연골 분화를 촉진합니다. 배양에서 유형 II 콜라겐을 발현하는 광택 있는 세포 구의 형성은 MSC의 연골 분화를 증명하며, 분자 기술과 면역조직화학으로 확인할 수 있습니다.
3.3. Osteogenic Differentiation
The two important transcription factors that promote osteoblastic differentiation are runt-related transcription factor 2 (Runx2) and osterix (Osx) [64]. Osterix (Osx) also called Sp7 belonging to the Sp transcription factor family is regulated by Runx2 that specifically binds with the Osx promoter region that regulates osteoblast differentiation in vitro and in vivo [65]. The role of Runx2 in osteogenic regulation is by the formation of heterodimer with cotranscription factor core-binding factor beta (Cbf β) and binding to DNA [66, 67]. In addition, the MSC to osteogenic differentiation increases the expression of early-marker alkaline phosphatase gene and late-marker osteopontin gene [24]. Of the different sources of MSCs differentiating into osteoblast-like BM-MSCs [52], S-MSCs, P-MSCs [59], or AT-MSCs [53], in vitro supplements including dexamethasone, β-glycerophosphate, ascorbic acid, and 1,25-dihydroxy-vitamin D3 help in osteogenic differentiation from MSCs [68–71]. The differentiation can be demonstrated by detection of the Runx2 gene by a molecular method and also von Kossa or alizarin red staining methods.
3.3. 골형성 분화
골형성 분화를 촉진하는 두 가지 중요한 전사 인자는 런트 관련 전사 인자 2(Runx2)와 오스테릭스(Osx)입니다 [64]. 오스테릭스(Osx)는 Sp 전사 인자 가족에 속하는 Sp7로도 알려져 있으며, Runx2에 의해 조절되며, Runx2는 Osx 프로모터 영역에 특이적으로 결합하여 체외 및 체내에서 골형성 분화를 조절합니다 [65]. Runx2의 골형성 조절 역할은 코트랜스크립션 인자 코어 결합 인자 베타(Cbf β)와 이종 이합체를 형성하고 DNA에 결합하는 것을 통해 이루어집니다 [66, 67]. 또한, MSC의 골형성 분화 시 초기 표지자 알칼리 포스파타제 유전자와 후기 표지자 오스테오폰틴 유전자의 발현이 증가합니다 [24]. 다양한 출처의 MSC가 골세포 유사 BM-MSC [52], S-MSC, P-MSC [59], 또는 AT-MSC [53]로 분화될 때, 체외 보조제인 데ksametason, β-글리세로포스페이트, 아스코르브산, 및 1,25-디하이드록시-비타민 D3는 MSC의 골형성 분화에 도움을 줍니다 [68–71]. 분화는 분자적 방법으로 Runx2 유전자의 검출을 통해 또는 von Kossa 또는 알리자린 레드 염색 방법을 통해 확인할 수 있습니다.
3.4. Tendocytic Differentiation
Tendons are tissues of mesodermal origin. MSCs are also considered promising for tendon repair in cell-based therapy. Expression of the transcription factor Scleraxis (Scx) regulates the tendon formation [72]. Mohawk activation is essential for tendon development and to modulate the expression of Scx and tendon-specific extracellular matrix molecules both in vitro and in vivo [73]. Another cytokine called bone morphogenetic protein-12 (BMP-12) [74] also known as growth factor and differentiation factor [75] is superiorly capable of promoting repair of tendon as well as tendon-like tissue formation from MSCs. Studies showed that BM-MSCs [76] and TD-MSCs [77] can differentiate into tendocyte.
3.4. 건세포 분화
건은 중배엽 기원 조직입니다. MSC는 세포 기반 치료에서 건 복원에 유망한 것으로 간주됩니다. 전사 인자 Scleraxis (Scx)의 발현은 건 형성을 조절합니다 [72]. Mohawk 활성화는 인대 발달과 Scx 및 인대 특이적 세포외 기질 분자의 발현 조절에 필수적입니다 [73]. 또 다른 사이토킨인 골형성 단백질-12 (BMP-12) [74]는 성장 인자 및 분화 인자로도 알려져 있으며 [75], MSC에서 인대 및 인대 유사 조직 형성을 촉진하는 데 우수합니다. 연구 결과, BM-MSCs [76]와 TD-MSCs [77]는 건세포로 분화할 수 있습니다.
3.5. Neurogenic Differentiation
In a normal state, MSCs express low levels of neural gene markers, such as nestin, Nurr1, enolase 2, glial fibrillary acidic protein (GFAP), and beta-tubulin III [78]. MSCs also differentiate into NSC-like cells under specific culture conditions that are morphologically and phenotypically similar [79]. This indicates that MSCs have the capability to differentiate into nonmesenchymal-origin cells in the presence of stimuli. In the presence of growth factors, NSCs differentiated into the neural phenotypes: astroglia, oligodendroglia, and neurons [80]. Along with this, increased expression of neuronal markers—neuron-specific enolase (NSE), β-tubulin III, neurofilament-M (NF-M), and microtubule-associated protein 2 (MAP2)—has been observed in vitro [81]. Neuronal cells can be derived from BM-MSCs [78, 79], amniotic fluid MSCs (AF-MSCs) [25], and UC-MSCs [80]. Neurons cells can be detected by using histochemical staining for neuronal Nissl bodies.
3.5. 신경 분화
정상 상태에서 MSCs는 네스틴, Nurr1, 에놀레이스 2, 글리아 섬유산성 단백질(GFAP), 베타-튜불린 III와 같은 신경 유전자 표지자를 낮은 수준으로 발현합니다 [78]. MSCs는 특정 배양 조건 하에서 형태학적 및 표현형적으로 유사한 NSC 유사 세포로 분화됩니다 [79]. 이는 MSCs가 자극 존재 시 비중간엽 기원 세포로 분화할 수 있음을 나타냅니다. 성장 인자 존재 시 NSCs는 신경 표현형인 아스트로글리아, 올리고덴드로글리아, 신경세포로 분화되었습니다 [80]. 이와 함께, 신경 특이적 효소(NSE), β-튜빈 III, 신경 필라멘트-M(NF-M), 미세관 연관 단백질 2(MAP2)와 같은 신경 마커의 발현이 증가한 것이 체외에서 관찰되었습니다 [81]. 신경 세포는 골수 유래 중간엽 줄기세포(BM-MSCs) [78, 79], 양수 유래 중간엽 줄기세포(AF-MSCs) [25], 및 태반 유래 중간엽 줄기세포(UC-MSCs) [80]에서 유래될 수 있습니다. 신경 세포는 신경 Nissl 체에 대한 조직화학 염색을 통해 검출될 수 있습니다.
3.6. Smooth Muscle Differentiation
MSCs differentiation into functional smooth muscle cells (SMCs) requires potential regulators miR-503 and miR-222-5p. Stimulation of transforming growth factor-β1 (TGFβ1) is required for genotypic and phenotypic expression and acts as a strong inducer of myogenic differentiation of MSCs [82]. TGF-β3 also induces MSCs differentiation into SMCs by activating myocardin and myocardin-related transcription factor-A (MRTF-A) [83]. In addition, involvement of sphingosylphosphorylcholine induces contractile SMCs differentiation from human adipose tissue-derived MSCs [84].
3.6. 평활근 분화
MSC가 기능적 평활근 세포(SMCs)로 분화하려면 잠재적 조절인자 miR-503과 miR-222-5p가 필요합니다. 변형 성장 인자-β1(TGFβ1)의 자극은 유전형 및 표현형 발현에 필수적이며, MSC의 근원성 분화를 강력히 유도하는 인자로 작용합니다 [82]. TGF-β3는 마이오카딘과 마이오카딘 관련 전사 인자-A(MRTF-A)를 활성화하여 MSC의 SMC 분화를 유도합니다[83]. 또한 스핑고실포스포릴콜린의 관여는 인간 지방 조직 유래 MSC에서 수축성 SMC 분화를 유도합니다[84].
4. Effect of Medicinal Plant Extracts on MSCs
Globally, plants and their products are used for improving health. Plants have been providing endless sources of medicine throughout history. Their method of production, purpose, and method of use vary. The USA has categorized plants into dietary supplements (intended to supplement the diet and usually consist of vitamins and minerals), drugs (over-the-counter drugs), and botanical drugs (complex extracts used for treatment) [85]. Extracts from different parts of a plant (root, bark, flower, leaf, and seed) may be used for different therapeutic purposes. Ayurveda, South-East and Middle-East Asian, and Chinese traditional medicines are the roots for use of natural products in treating diseases. Plant extracts contain bioactive compounds like polyphenols, flavonoids, and many other compounds and chemical substances which play important roles to treat both communicable and noncommunicable diseases [86]. Due to health benefits, phytochemicals from plants generate a lot of interest, demanding further scientific evaluation [87]. According to the National Institutes of Health, USA database, of the 680 clinical trials on MSCs, 27 have used dietary supplements including herbal compounds [86]. Natural compounds isolated from blueberry, green tea, catechin, carnosine, and vitamin D3 have shown to promote the proliferation of stem cell of bone marrow. Dietary fatty acids (oleic acid and linoleic acid) promote the proliferation of haemopoietic stem cells [34]. Under standard in vitro condition, supplementing plant extract may induce increased rates of MSCs proliferation and multilineage differentiation, as shown in Figure 1. Moreover, studies have shown that extracts also increase pluripotent stem cell proliferation and anticancer potency.
4. 약용 식물 추출물의 MSC에 대한 영향
전 세계적으로 식물과 그 제품은 건강 개선을 위해 사용됩니다.
식물은 역사적으로 무한한 약물의 원천을 제공해 왔습니다.
그들의 생산 방법, 목적, 사용 방법은 다양합니다.
미국은
식물을 식이 보조제(식이 보완을 목적으로 하며 일반적으로 비타민과 미네랄로 구성됨),
약물(일반 의약품), 식물성 약물(치료를 위해 사용되는 복잡한 추출물)로 분류했습니다 [85].
식물의 다양한 부분(뿌리, 껍질, 꽃, 잎, 씨앗)에서 추출된 추출물은
다양한 치료 목적으로 사용될 수 있습니다.
아유르베다, 동남아시아 및 중동 아시아, 중국 전통 의학은 질병 치료에 자연 제품을 사용하는 기반이 되었습니다.
식물 추출물은
폴리페놀, 플라보노이드 등 생물활성 화합물과 다양한 화합물 및 화학 물질을 함유하며,
전염성 및 비전염성 질환 치료에 중요한 역할을 합니다 [86].
건강상의 이점으로 인해
식물에서 유래한 피토케미컬은 많은 관심을 끌고 있으며,
추가적인 과학적 평가가 요구되고 있습니다 [87].
미국 국립 보건원(NIH) 데이터베이스에 따르면,
MSC에 대한 680건의 임상 시험 중 27건이 허브 성분을 포함한 식이 보충제를 사용했습니다 [86].
블루베리, 녹차, 카테킨, 카르노신, 비타민 D3에서 분리된 천연 화합물은
골수 줄기 세포의 증식을 촉진하는 것으로 나타났습니다.
식이 지방산(올레산과 리놀레산)은
혈액 줄기세포의 증식을 촉진합니다 [34].
표준 체외 조건에서 식물 추출물을 보충하면
MSCs의 증식 속도와 다계열 분화율이 증가한다는 것이 그림 1에 표시되어 있습니다.
또한 연구 결과,
추출물이 다능성 줄기세포의 증식과 항암 효과를 증가시킨다는 것이 밝혀졌습니다.
Figure 1.
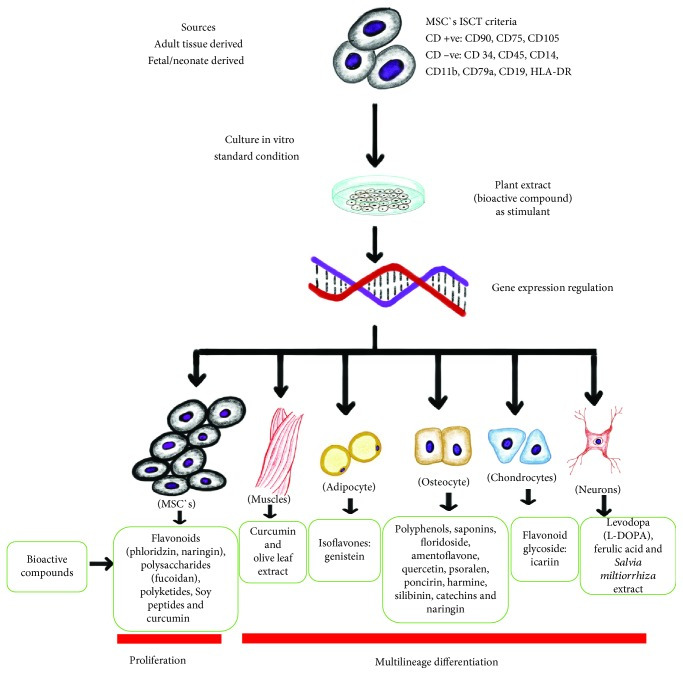
MSCs isolated from different sources derived from adult and fetal tissues. MSCs must be positive for cluster of differentiation CD90, CD75, and CD105 and negative for CD34, CD45, CD14, CD11b, CD79a, CD19, and HLA-DR according to ISCT criteria [4]. Bioactive compound derived from plants regulates MSC gene expression, which may be responsible for the cellular proliferation and multilineage differentiation into osteocyte, muscle cells, nerve cells [86, 88], adipocyte [89], and chondrocyte [90].
5. Proliferation and Differentiation Stimulants
Medicinal plants and herbs have always been valuable in disease treatment. Recently, researchers have investigated and identified those pharmacologically active substances which are responsible for disease prevention and treatment. Recently, medicinal plants have received considerable attention as stimulants for stem cell proliferation in vivo and in vitro [34, 91, 92]. In vitro studies of natural bioactive compounds have suggested that plant-derived substances enhance the adult stem cell proliferation and on the other hand inhibit the proliferation of cancer cells [86]. Several studies have suggested that the proliferation ability of MSCs is influenced by the dose of the stimulant compound, where higher doses of cellular toxicity appear. Using 1-100 μg/ml extract from a citrus increased the human BM-MSCs proliferation and osteogenic differentiation, while using 200 μg/ml concentration decreases BM-MSCs growth [93]. In rat BM-MSCs, naringin 50 μg/ml concentration increased growth of MSCs and a higher concentration at 100 μg/ml suppressed the rate of proliferation [94]. In addition, extracts from brown algae Laminaria japonica (fucoidan) enhance the proliferation of human-derived MSCs when using 0.1–10 μg/ml concentration [95]. Studies have shown MSCs differentiation into osteogenic, neurogenic, and endothelial/vascular progenitor cells in the presence of plant extract supplements. Certain phytochemicals may increase the cellular proliferation and at the same time reduce the time required, as shown in Table 1. The effects of plant extracts on MSCs differentiation and their possible mechanism have been shown in Table 2.
5. 증식 및 분화 촉진제
약용 식물과 허브는 질병 치료에 항상 귀중한 자원으로 활용되어 왔습니다. 최근 연구자들은 질병 예방 및 치료에 책임이 있는 약리학적으로 활성 있는 물질을 조사하고 식별해 왔습니다. 최근 약용 식물은 체내 및 체외에서 줄기세포 증식을 촉진하는 자극제로 주목받고 있습니다 [34, 91, 92]. 체외 연구에서 자연 유래 생물활성 화합물은 식물 유래 물질이 성체 줄기세포의 증식을 촉진하는 반면 암세포의 증식을 억제한다는 것을 제시했습니다 [86]. 여러 연구에서 MSC의 증식 능력은 자극제 화합물의 용량에 영향을 받으며, 용량이 증가할수록 세포 독성이 나타난다는 것이 제안되었습니다. 시트러스 추출물 1-100 μg/ml 농도는 인간 골수 유래 MSCs의 증식과 골형성 분화를 증가시켰으나, 200 μg/ml 농도는 MSCs의 성장을 감소시켰습니다 [93]. 쥐 골수 유래 MSCs에서 나링닌 50 μg/ml 농도는 MSCs의 성장을 증가시켰으며, 100 μg/ml의 높은 농도는 증식 속도를 억제했습니다 [94]. 또한 갈색 해조류 Laminaria japonica (fucoidan) 추출물은 0.1–10 μg/ml 농도에서 인간 유래 MSC의 증식을 촉진했습니다 [95]. 식물 추출물 보충제가 존재할 때 MSC가 골형성, 신경형성, 내피/혈관 전구 세포로 분화되는 것이 연구에서 확인되었습니다. 일부 식물 화합물은 세포 증식을 증가시키며 동시에 필요한 시간을 단축시킬 수 있으며, 이는 표 1에 표시되어 있습니다. 식물 추출물이 MSC 분화에 미치는 영향 및 그 가능성 있는 메커니즘은 표 2에 제시되어 있습니다.
Table 1.
Effect of plant extract on MSC proliferation.
PlantMSC sourceMechanism of actionReferences
| Epimedium pubescens (TCM) | hBMSCs | 20 μg/ml increases significant proliferation | [96] |
| Glycine max var. (vegetable soy peptides) | hAD-MSCs and CB-MSCs | 25% and 20% increase cell proliferation rate, and TGF-β1 plays a crucial role to induce proliferation | [97] |
| Ocimum basilicum | hDP-MSCs and BM-MSC | Induces MSC proliferation and reduces doubling time (DT) at 10 μg/ml concentration | [98] |
| Paullinia cupana (guaraná) | hAD-MSCs | 5 and 10 mg/ml concentrations stimulate proliferation. Increases the catalase (CAT) activity and SOD2, CAT, and GPx gene expression | [99] |
| Glycyrrhiza glabra (licorice root) | hBM-MSC | Increases significant level of proliferation at concentration 10-50 μg/ml | [100] |
| Thymbra spicata var. intricata | h-Dental pulp (DP) and BM-MSCs | Reduces the doubling time (DT) at 10 μg/ml for MSCs and acts as a good proliferation inducer | [101] |
| ZD-I: TCM | Telomerized hMSCs | 0.78–25 μg/ml stimulates the proliferation | [102] |
| Rhizoma drynariae | hBM-MSC | 0–200 μg/ml concentration of the naringin solution enhances the proliferation | [93] |
| Foeniculum vulgare | hBM-MSC | Proliferation activity is seen with a dose of 5 μg/ml | [103] |
| Cissus quadrangularis (Linn.) | Wistar rat BM-MSCs | 300 μg/ml concentration increases the proliferation rate by 2-fold | [91] |
| Apple | h-AD MSCS and CB-MSCs | Proliferation promotes by ERK-dependent cytokine production | [104] |
| Ferula gummosa | hBM-MSCs | 0.5 to 5 μg/ml increases significant cell proliferation | [105] |
| Ginkgo biloba | hBM-MSCs | 25 mg/l increases the cell proliferation by 30% | [106] |
Table 2.
Effect of plant extracts on MSC differentiation.
Plant extractsMSC sourceDifferentiate intoMechanism of actionReferences
| Fructus Ligustri Lucidi (FLL) | — | Osteogenic | Increases ALP activity, expression of osteogenesis-stimulating genes, β-catenin, BMP-2, cyclin D1, MT1MMP (membrane type-1 matrix metalloproteinase), osteoprotegerin, and TBX3 (T-box 3) | [107] |
| Fructus Ligustri Lucidi (FLL) | Rat MSC | Osteogenic | Increases ALP activity, osteoprotegerin- (OPG-) to-receptor activator for nuclear factor-κB ligand (RANKL) mRNA level increase | [108] |
| China Herba epimedii | h BM-MSC | Osteogenic | Increases ALP activity and enhances mRNA expression of BMP-2, Runx2 (runt-related transcription factor 2), and OPN (osteopontin) | [109] |
| Rhizoma drynariae | hBM-MSC | Osteogenic | Increases expression of ALP, collagen I, osteopontin, and osteocalcin genes | [93] |
| Ferula gummosa | hBM-MSC | Osteogenic | Increases alkaline phosphatase activity | [105] |
| TCM: ZD-I | Telomerized hMSCs | Osteogenic | Increases mRNA expression of ALP, Runx2, and osteocalcin | [102] |
| Ginkgo biloba | hBM-MSC | Osteogenic | Increases transcriptional levels of bone morphogenetic protein 4 (BMP4), runt-related transcription factor 2 (Runx2), β-catenin, and cyclin D1 | [106] |
| Berberis aristata | h BM-MSC | Osteogenic | Enhances Runx2, osteocalcin (OCN), and osteopontin (OPN) expression and activation of the canonical Wnt/β-catenin pathway | [110] |
| Mucuna gigantea | hBM-MSC | Neurogenic | Increases expression of mRNA for nestin (a neural precursor marker) and β-tubulin III (an immature neuron marker) | [111] |
| Salvia miltiorrhiza | hUC-WJ MSCs | Neurogenic | Induces expression of nestin, beta-tubulin III, neurofilament (NF), and glial fibrillary acidic protein (GFAP) | [112] |
| Olea europaea leaf | — | Endothelial/vascular genesis | Increases gene expression for vascular endothelial growth factor, platelet-derived growth factor receptor, and vascular endothelial growth factor receptor (VEGFR)-1 | [113] |
| Salvia miltiorrhiza | hMSC | Osteogenic | Increases expression of alkaline phosphatase activity, osteopontin, Runx2, and osterix and promotes osteogenesis by activating the ERK signaling pathway | [114] |
| Angelica sinensis | AD-MSCs | Neurogenic | Increases expression of neuron-specific enolase (a specific marker of neurons) | [115] |
| Epimedium pubescens (TCM) | hM-MSCs | Osteogenic | Increases activity of ALP and the amount of calcified nodules and expression of BMP-2 also increase | [96] |
| Ocimum basilicum | DP-MSCs | Osteogenic | Osteonectin and osteocalcin levels increase | [98] |
| Glycyrrhiza glabra (licorice root) | hBM-MSC | Osteogenic | Osteocalcin, Runx2, BMP2, and ALP gene expression upregulate | [100] |
| Foeniculum vulgare | hBM-MSC | Osteogenic | 17β-Estradiol and ALP activity increase | [103] |
| Thymbra spicata var. intricata | h-DP and BM-MSCs | Osteogenic | Osteocalcin (OCN) (late osteogenic marker) level increases | [101] |
| Cissus quadrangularis (Linn.) | Wistar rat BM-MSCs | Osteogenic | Increases ALP activity | [91] |
5.1. Phytochemical Compounds
5.1.1. Naringin
Naringin (naringenin 7-O-neohesperidose) belongs to the flavonoid group, has an antioxidant effect, is anticancerous, and is used for reducing the cholesterol level. It is also used for the treatment of bone disorders like osteoporosis and osteoarthritis. Naringin has a potential to induce proosteogenic effects which could promote the proliferation of stem cell [116]. In in vitro condition, it has shown to enhance the osteogenic differentiation by increasing the expression of Runx2, OXS, OCN, and Col1 and increase the proliferation by activating the ERK signaling pathway on human BM-MSCs [117]. In rat BMSCs, naringin increases the mRNA levels of osteogenic genes and Notch1 expression [94]. In human amniotic fluid-derived stem cells (hAFSCs), naringin promotes osteogenesis via BMP and Wnt-β-catenin signaling pathways. In addition, it increases the expression of bone morphogenetic protein 4 (BMP4), runt-related transcription factor 2 (Runx2), β-catenin, and cyclin D1 in a dose-dependent manner by 1-100 μg/ml [118]. At 1 μM concentration, it promotes the proliferation and differentiation of human periodontal ligament stem cells (hPDLSCs) both in vitro and in vivo [119]. The proliferation and differentiation are dependent on the dose of naringin in dog-originated BM-MSCs [120]. Rhizoma drynariae is used commonly in the treatment of osteoporosis and bone nonunion in traditional Chinese medicine [93]. The flavanone may become a potential therapeutic candidate to promote the osteogenesis.
5.1. 식물 화학 성분
5.1.1. 나링긴
나링긴(나링게닌 7-O-네오헤스페리도스)은 플라보노이드 그룹에 속하며, 항산화 효과를 가지고 있으며, 항암 작용을 하며, 콜레스테롤 수치를 낮추는 데 사용됩니다. 또한 골다공증과 골관절염과 같은 골격계 질환의 치료에도 사용됩니다.
나링인은
골형성 촉진 효과를 유도할 잠재력을 가지고 있으며,
이는 줄기세포의 증식을 촉진할 수 있습니다 [116].
체외 실험에서 나링인은 Runx2, OXS, OCN, Col1의 발현을 증가시켜 골형성 분화를 촉진하고, 인간 골수 유래 줄기세포(BM-MSCs)에서 ERK 신호전달 경로를 활성화하여 증식을 증가시키는 것으로 나타났습니다 [117].
쥐 골수 유래 줄기세포(BMSCs)에서 나링긴은 골형성 유전자 mRNA 수준과 Notch1 발현을 증가시킵니다 [94].
인간 양수 유래 줄기세포(hAFSCs)에서 나링긴은 BMP 및 Wnt-β-catenin 신호전달 경로를 통해 골형성을 촉진합니다.
또한 1-100 μg/ml 농도에서 골형성 단백질 4(BMP4), 런트 관련 전사 인자 2(Runx2), β-catenin, 및 cyclin D1의 발현을 용량 의존적으로 증가시킵니다 [118]. 1 μM 농도에서 인간 치주 인대 줄기세포(hPDLSCs)의 증식과 분화를 체외 및 체내에서 촉진합니다 [119]. 증식과 분화는 개 유래 골수 줄기세포(BM-MSCs)에서 나링인의 용량에 따라 달라집니다 [120]. Rhizoma drynariae는 전통 중국 의학에서 골다공증과 골유합 부전 치료에 널리 사용됩니다 [93]. 플라바논은 골형성을 촉진하는 잠재적 치료 후보로 작용할 수 있습니다.
5.1.2. Icariin
Icariin (ICA) is the main extract of Herba epimedii which is widely used in traditional Chinese medicine (TCM). Icariin, a natural flavonoid glycoside, possesses anti-inflammatory (through inflammatory cytokines and phosphorylation of p38 and JNK) [121], antiatherosclerosis [122], and anticancer [123] activities and treats type 2 diabetes mellitus [124]. ICA promotes bone formation by stimulating osteogenic differentiation of BMSCs. ICA can promote chondrogenic differentiation by activating the Wnt/β-catenin signaling pathway [90]. In rat BMSCs, proliferation is achieved by activating ERK and p38 MAPK signaling [125]. In Sprague-Dawley (SD) rats, ICA has shown to increase the phosphorylation level of GSK-3β and cyclin D1 protein in BM-MSCs [126]. Icariside II (ICA II) is a kind of metabolite of ICA (loss of the glycosyl moiety at the C-7 position of ICA) [127]. Icariside II (ICS II) is a prenylated active flavonol and has antiosteoporosis, antihypoxia, and anticancer activities. ICS II increases ALP activity and calcium deposition which enhance the osteogenic differentiation of BMSCs at optimal concentration [128] also via enhanced expression of osteogenesis proteins/genes and increases the PI3K/AKT/mTOR/S6K1 signaling pathways [129, 130]. It promotes osteogenesis by upregulating Runx2, ALP, and collagen I and inhibits adipogenesis by downregulating PPARγ, Fabp4, and adipsin gene expression [131].
5.1.2. Icariin
Icariin (ICA)은 전통 중국 의학(TCM)에서 널리 사용되는 Herba epimedii의 주요 추출물입니다.
이카리인은 자연 유래 플라보노이드 글리코사이드로,
염증성 사이토카인과 p38 및 JNK 인산화를 통해 항염증 작용 [121], 항동맥경화 작용 [122], 항암 작용 [123]을 나타내며
제2형 당뇨병 치료에 사용됩니다 [124].
ICA는 BMSC의 골형성 분화를 자극하여 골 형성을 촉진합니다.
ICA는 Wnt/β-catenin 신호전달 경로를 활성화하여 연골 분화를 촉진합니다 [90]. 쥐 BMSC에서 ERK 및 p38 MAPK 신호전달 경로를 활성화하여 증식을 유도합니다 [125]. Sprague-Dawley (SD) 쥐에서 ICA는 골수 유래 중간엽 줄기세포(BM-MSC)에서 GSK-3β 및 cyclin D1 단백질의 인산화 수준을 증가시켰습니다 [126]. Icariside II (ICA II)는 ICA의 대사산물로, ICA의 C-7 위치에서 글리코실 기가 제거된 형태입니다 [127]. Icariside II (ICS II)는 전니화된 활성 플라보놀로, 골다공증 억제, 저산소증 억제, 항암 활성을 나타냅니다. ICS II는 최적 농도에서 BMSCs의 골형성 분화를 촉진하며, 골형성 단백질/유전자 발현을 증가시키고 PI3K/AKT/mTOR/S6K1 신호전달 경로를 활성화합니다 [129, 130]. Runx2, ALP, 콜라겐 I 발현을 증가시켜 골형성을 촉진하고, PPARγ, Fabp4, 아디핀 유전자 발현을 억제하여 지방형성을 억제합니다 [131].
5.1.3. Genistein
Genistein has structural similarity to human estrogen, so it is also called phytoestrogen. It is one of the most abundant isoflavones in soy. Isoflavones belong to the group of flavonoids, and they act as phytoestrogens, antioxidants, and anticancer agents. Genistein when added to medium (10−7 M and 10−8 M) promotes bone formation and also increases the level of alkaline phosphatase activity and DNA content [132]. Genistein promotes the h-BMSCs (human-BMSCs) to osteogenic differentiation through an ER-dependent mechanism. Also, BMP-dependent SMADs and Runx2 signaling play important roles in the process [133]. In addition, it could stimulate differentiation through the p38 MAPK-Cbfa1 pathway [134]. However, studies have shown that it also induces adipogenic differentiation, promotes triglycerides activity in hBMSC, and suppresses osteogenic potential by upregulating the expression of PPAYγ [89]. An in vitro study shows that genistein stimulates hMSC-induced cellular proliferation and survival of cells and enhances antiapoptotic capacity [135].
5.1.3. 제니스틴
제니스틴은 인간 에스트로겐과 구조적 유사성을 가지고 있어 식물성 에스트로겐으로 불립니다. 이는 대두에 가장 풍부하게 존재하는 이소플라본 중 하나입니다. 이소플라본은 플라보노이드 그룹에 속하며, 식물성 에스트로겐, 항산화제, 항암제로 작용합니다. Genistein을 배지(10−7 M 및 10−8 M)에 추가하면 골 형성을 촉진하며 알칼리 포스파타제 활성과 DNA 함량을 증가시킵니다 [132]. 제니스틴은 ER 의존적 메커니즘을 통해 인간 골수 간엽 줄기세포(h-BMSCs)의 골형성 분화를 촉진합니다. 또한 BMP 의존적 SMAD 및 Runx2 신호전달 경로는 이 과정에서 중요한 역할을 합니다[133]. 또한 p38 MAPK-Cbfa1 경로를 통해 분화를 자극할 수 있습니다[134]. 그러나 연구 결과, 이는 지방 분화도 유도하며 hBMSC에서 트리글리세라이드 활성을 촉진하고 PPAYγ 발현을 증가시켜 골형성 잠재력을 억제한다는 것이 밝혀졌습니다 [89]. 체외 연구에서 제니스틴은 hMSC에 의한 세포 증식 및 생존을 촉진하고 항아포토시스 능력을 강화합니다 [135].
5.1.4. Hyaluronic Acid
Hyaluronic acid (HA) as a potential agent for medical use is already documented. HA in combination with BMSCs enhances cartilage regeneration for chondral defects in canines [136]. In addition, an in vivo study done in pigs found that HA with MSCs improves the cartilage healing both histologically and morphologically at 6 and 12 weeks after injection [137]. In humans, HA increases the proliferation which is dose and time dependent. In HA-treated amniotic MSCs, upregulation of the expression of the Wnt/β-catenin pathway has been seen which enhances mRNA expression and protein level of wnt3a, β-catenin, and cyclin D1 [138].
5.1.4. 히알루론산
히알루론산(HA)은 의료용 잠재적 제제로 이미 보고되었습니다. HA와 BMSC의 조합은 개에서 연골 결손에 대한 연골 재생 능력을 향상시킵니다 [136]. 또한 돼지에서 진행된 in vivo 연구에서 HA와 MSC의 조합은 주사 후 6주 및 12주 시점에서 조직학적 및 형태학적 측면에서 연골 치유를 개선했습니다 [137]. 인간에서 HA는 용량 및 시간 의존적으로 증식을 증가시킵니다. 히알루론산 처리된 태반 MSC에서 Wnt/β-catenin 경로의 발현이 증가했으며, 이는 wnt3a, β-catenin, 및 cyclin D1의 mRNA 발현 및 단백질 수준을 향상시켰습니다 [138].
5.1.5. Resveratrol
Resveratrol (RSVL) is a natural type of polyphenolic phytoestrogen. RSVL is mainly found in red grapes, blueberries, peanuts, and other plants [139]. The effect of RSVL on stem cell is well documented. It enhances the hBMSC proliferation and potential to differentiate into osteocyte by activation of extracellular signal-regulated kinase 1/2 (ERK1/2) and p38 mitogen-activated protein kinase (MAPK) signaling through an ER-dependent mechanism [140]. RSVL showed the effect on HMSCs in dose- and time-dependent manners for the self-proliferation and differentiation. 0.1 μM RSVL promotes cell proliferation, but 5 μM or above inhibits cell self-renewal by increasing the senescence rate and cell cycle arrest in S phage. It also helps MSC differentiation into osteogenic cells and suppresses differentiation into the adipogenic lineage [141]. Resveratrol enhances osteogenic differentiation by upregulating HMSC mediated through the SIRT1/FOXO3A. It activates and enhances the proteins SIRT1 and FOXO3A, respectively, in an independent manner. Resveratrol also promotes osteogenesis by upregulating Runx2 gene expression [142].
5.1.5. 레스베라트롤
레스베라트롤(RSVL)은 자연적으로 발생하는 폴리페놀성 식물 에스트로겐입니다. RSVL은 주로 적포도, 블루베리, 땅콩 및 기타 식물에서 발견됩니다 [139]. RSVL의 줄기세포에 대한 효과는 잘 문서화되어 있습니다. 이는 세포외 신호 조절 키나제 1/2 (ERK1/2) 및 p38 미토겐 활성화 단백질 키나제 (MAPK) 신호전달 경로를 통해 ER 의존적 메커니즘을 통해 활성화되어 hBMSC의 증식 및 골세포로 분화 잠재력을 증진시킵니다 [140]. RSVL은 HMSC의 자기 증식과 분화에 용량 및 시간 의존적으로 영향을 미쳤습니다. 0.1 μM RSVL은 세포 증식을 촉진하지만, 5 μM 이상은 세포 노화 속도를 증가시키고 S 상에서 세포 주기 정지를 유발하여 세포 자기 재생 능력을 억제합니다. 또한 MSC의 골세포 분화를 촉진하고 지방세포 분화를 억제합니다 [141]. 레스베라트롤은 SIRT1/FOXO3A를 통해 HMSC의 골형성 분화를 촉진합니다. 이는 각각 SIRT1과 FOXO3A 단백질을 독립적으로 활성화하고 증강시킵니다. 레스베라트롤은 Runx2 유전자 발현을 증가시켜 골형성을 촉진합니다 [142].
6. Future Prospective
Recent advancement in science and technology and advanced research on plant extracts is bringing into light their importance in regenerative and therapeutic medicine. As we know very less about the exact site and mechanism of action and side effect of the use of plant extracts, extensive research on humans will help to replace synthetic pharmaceutical drugs to treat diseases. If protocols for proliferation and differentiation of stem cells into desired lineage cells by use of plant extracts can be established, it will help to treat many untreatable diseases like aplastic anemia, leukemia, bone diseases, and cardiovascular diseases. MSCs have promising roles in regenerative therapy due to their broader differentiation potential [4]. From the last few decades, scientist have been aiming to use MSCs for tissue regeneration in bone injury [143], cartilage injury [144], spinal cord injury [145], graft-versus-host disease [146], Crohn's disease [147], and hematopoietic cell recruitment [148]. Though very less side effects of plant extracts on humans have been noted, they may still show adverse drug effects for certain medical condition which are not well known. With better knowledge of the effects of plant extracts, we may also be able to restrict their undesirable use under certain circumstances. The therapeutic doses can also be well established to have desired effects as well as control toxic effects.
Medicinal plants are being widely accepted and increasingly used by the general public for treatment. They are also used as complementary supplements to reduce the side effects produced by Western medicine [149]. The bioactive compounds derived from plants have shown to be potential candidates to activate stem cells for proliferation and differentiation. Currently, recombinant and synthetic cytokines, growth factors, and other proteins are being produced by using bacterial cell, plants cells, and mammalian cells for stem cell growth supplement. These compounds have significant side effects [150–152] and lead to neoplastic cell transformations [153] with high cost, less stability, and limited application and requiring continuous use making them unaffordable for low-income countries. Certain medicinal plants have always been grown and used as cultural values for primary health benefits. With more knowledge on values of commonly available plants in the community, it will help people to preserve and use them for healthy living and preventive and curative medicine and also restrict undesirable use. This will decrease the health care economic burden for primary health care problems. Thus, plant-derived compounds will be proven as promising agents for stem cell therapy for public health with easy availability and affordability and least or no side effects.
6. 미래 전망
과학 기술의 발전과 식물 추출물에 대한 고급 연구는 재생 의학과 치료 의학에서의 중요성을 밝혀내고 있습니다. 식물 추출물의 정확한 작용 부위, 메커니즘, 부작용에 대해 알려진 바가 매우 적기 때문에, 인간을 대상으로 한 광범위한 연구는 합성 약물을 대체하여 질병을 치료하는 데 기여할 것입니다. 식물 추출물을 사용하여 줄기세포를 원하는 분화 계통으로 증식 및 분화시키는 프로토콜이 확립된다면, 재생불량성 빈혈, 백혈병, 골질환, 심혈관 질환 등 치료가 어려운 질병을 치료하는 데 도움이 될 것입니다. MSCs는 광범위한 분화 잠재력으로 인해 재생 치료에서 유망한 역할을 가지고 있습니다 [4]. 최근 수십 년간 과학자들은 골 손상 [143], 연골 손상 [144], 척수 손상 [145], 이식 대 호스트 질환 [146], 크론병 [147], 혈액 생성 세포 모집 [148] 등에서의 조직 재생에 MSCs를 활용하기 위해 노력해 왔습니다. 식물 추출물의 인간에 대한 부작용은 매우 적게 보고되었지만, 특정 의료 조건에서 알려지지 않은 부작용을 유발할 수 있습니다. 식물 추출물의 효과를 더 잘 이해하면 특정 상황에서 그 사용을 제한할 수 있을 것입니다. 치료 용량을 적절히 설정하여 원하는 효과를 달성하고 독성 효과를 통제할 수 있습니다.
약용 식물은 일반 대중에게 치료 목적으로 널리 수용되고 점점 더 많이 사용되고 있습니다. 이들은 서양 의학의 부작용을 줄이기 위한 보완 보조제로도 사용됩니다 [149]. 식물에서 유래한 생물활성 화합물은 줄기 세포의 증식 및 분화를 활성화하는 잠재적 후보로 밝혀졌습니다. 현재 세균 세포, 식물 세포, 포유류 세포를 사용하여 줄기 세포 성장 보조제로 재조합 및 합성 사이토킨, 성장 인자, 기타 단백질이 생산되고 있습니다. 이러한 화합물은 심각한 부작용[150–152]을 유발하며, 종양 세포 변환[153]을 초래하며, 비용이 높고 안정성이 낮으며 적용 범위가 제한적이며 지속적인 사용이 필요해 저소득 국가에서는 부담스러울 수 있습니다. 특정 약용 식물은 전통적으로 문화적 가치로 재배되어 기본적인 건강 혜택을 위해 사용되어 왔습니다. 지역 사회에서 널리 이용 가능한 식물의 가치를 더 잘 이해하면, 사람들이 이를 건강한 생활과 예방 및 치료 의약품으로 보존하고 활용하며, 부적절한 사용을 제한하는 데 도움이 될 것입니다. 이는 기본 건강 문제에 대한 의료 비용 부담을 줄일 것입니다. 따라서 식물 유래 화합물은 공공 보건을 위한 줄기세포 치료의 유망한 후보로 입증될 것이며, 접근성, 경제성, 최소 또는 없는 부작용을 갖추고 있습니다.
7. Conclusion
MSCs along with medicinal plant extracts have a potential hope in stem cell and regenerative therapy. Plant extracts as stimulants significantly affect proliferation and differentiation into multilineage cells. Bioactive compounds from plants precisely regulate the MSCs through different protein pathways. Medicinal plants/herbs produce less toxic effects, are affordable, and can help to increase disease-treating capability using MSC cell therapy for both noninfectious and infectious diseases. With continued research, by using medicinal plant extracts, improved proliferation and differentiation potential of MSCs will be achieved in the near future and development of cost-effective technology for cellular therapy will be possible.
7. 결론
MSCs와 약용 식물 추출물은 줄기세포 및 재생 치료 분야에서 잠재적인 희망을 가지고 있습니다. 식물 추출물은 자극제로 작용하여 다계열 세포로의 증식과 분화에显著한 영향을 미칩니다. 식물에서 유래한 생물활성 화합물은 다양한 단백질 경로를 통해 MSCs를 정밀하게 조절합니다. 약용 식물/허브는 독성 효과가 적고 비용 효율적이며, MSC 세포 치료를 통해 비감염성 및 감염성 질환의 치료 능력을 향상시키는 데 도움을 줄 수 있습니다. 지속적인 연구를 통해 약용 식물 추출물을 활용하여 MSC의 증식 및 분화 잠재력을 향상시키는 것이 가까운 미래에 달성될 것이며, 세포 치료를 위한 비용 효율적인 기술 개발이 가능할 것입니다.
Acknowledgments
We thank Saroj Adhakari and Suroj Maharjan for their support.
AbbreviationsMSCs:
Mesenchymal stem cells
ISCT:
International Society for Cellular Therapy
PDT:
Population doubling time
UC-MSCs:
Umbilical cord-derived mesenchymal stem cells
BM-MSCs:
Bone marrow-derived mesenchymal stem cells
AT-MSCs:
Adipose tissue-derived mesenchymal stem cells
MD-MSCs:
Muscle-derived mesenchymal stem cells
P-MSCs:
Periosteum-derived mesenchymal stem cells
S-MSCs:
Synovial-derived mesenchymal stem cells
AD-MSCs:
Adipose tissue-derived mesenchymal stem cells
C-MSCs:
Circulating mesenchymal stem cells
TD-MSCs:
Tendon-derived mesenchymal stem cells
Osx:
Osterix
TCM:
Traditional Chinese Medicine
SA-β-Gal:
Senescence-associated β-galactosidase
ALP:
Alkaline phosphatase
Runx2:
Runt-related transcription factor 2
TGF-β:
Transforming growth factor-beta
BMPs:
Bone morphogenetic proteins
TGF-β:
Transforming growth factor-beta
SMC:
Smooth muscle cells
h-UC-WJ:
Human-Umbilical cord Wharton's jelly.
Ethical Approval
Ethical approval was taken from the Nepal Health Research Council, Ramshah Path, Kathmandu, Nepal (registration no. 334/2017).
Conflicts of Interest
There are no conflicts of interest.
Authors' Contributions
Bhuvan Saud and Kanti Shrestha prepared the manuscript. Rajani Malla made critical comments on the manuscript. All the authors finalized and approved the manuscript.
References
- 1.Chagastelles P. C., Nardi N. B. Biology of stem cells: an overview. Kidney International Supplements. 2011;1(3):63–67. doi: 10.1038/kisup.2011.15. [DOI] [PMC free article] [PubMed] [Google Scholar]