Annual Review of Nutrition Volume 40, 2020
Review Article Free
Nutritional Aspects of Spermidine
- Frank Madeo1,2,3, Sebastian J. Hofer1, Tobias Pendl1, Maria A. Bauer1, Tobias Eisenberg1,2,3,4, Didac Carmona-Gutierrez1 and Guido Kroemer5,6,7,8,9
- Vol. 40:135-159 (Volume publication date August 2020) https://doi.org/10.1146/annurev-nutr-120419-015419
- First published as a Review in Advance on July 07, 2020
ABSTRACT
Natural polyamines (spermidine and spermine) are small, positively charged molecules that are ubiquitously found within organisms and cells. They exert numerous (intra)cellular functions and have been implicated to protect against several age-related diseases. Although polyamine levels decline in a complex age-dependent, tissue-, and cell type–specific manner, they are maintained in healthy nonagenarians and centenarians. Increased polyamine levels, including through enhanced dietary intake, have been consistently linked to improved health and reduced overall mortality. In preclinical models, dietary supplementation with spermidine prolongs life span and health span. In this review, we highlight salient aspects of nutritional polyamine intake and summarize the current knowledge of organismal and cellular uptake and distribution of dietary (and gastrointestinal) polyamines and their impact on human health. We further summarize clinical and epidemiological studies of dietary polyamines.
자연적 폴리아민(스퍼미딘과 스퍼민)은
유기체와 세포 내부에 널리 분포된 작은 양이온성 분자입니다.
https://www.mdpi.com/1422-0067/24/22/16469

이들은 다양한 (세포 내) 기능을 수행하며,
여러 노화 관련 질환으로부터 보호하는 역할을 하는 것으로 알려져 있습니다.
폴리아민 수준은
복잡한 연령 의존적, 조직별, 세포 유형별 방식으로 감소하지만,
건강한 90대 및 100대 노인에서는 유지됩니다.
식이 섭취 증가를 포함한 폴리아민 수준의 증가는
건강 개선과 전체 사망률 감소와 일관되게 연관되어 있습니다.
전임상 모델에서 스퍼미딘을
식이 보충제로 섭취하면 수명과 건강 수명이 연장됩니다.
이 리뷰에서는 영양 폴리아민 섭취의 중요한 측면을 강조하고,
식이 (및 위장) 폴리아민의 유기체 및 세포 흡수 및 분포와 인체 건강에 미치는 영향에 대한
현재의 지식을 요약합니다.
또한 식이 폴리아민에 대한
임상 및 역학 연구를 요약합니다.
Keywords
1. INTRODUCTION
The diamine putrescine and the natural polyamines (PAs) spermine and spermidine are aliphatic bioactive amines that carry two or more amino groups [see Figure 1 and the sidebar titled Definition of (Natural) Polyamines]. Due to their polycationic nature (i.e., the amino groups are fully protonated at physiological pH), PAs stabilize negative charges of macromolecules, including DNA, RNA, and proteins (150). PAs are essential for cell growth and proliferation (8) but fulfill many other functions, including promoting antioxidative activities, affecting ion channels, and controlling protein translation, and influence complex processes, such as apoptosis (138), autophagy (34), and immune regulation (55, 122, 136). Although seemingly every type of cell is capable of producing PAs through de novo biosynthesis, a substantial part of PAs comes from external sources, outlining the importance of diet for maintaining PA pools in the body (7, 100, 182). Importantly, external administration of spermidine has general antiaging effects (32, 34, 82, 83, 145, 178), as it confers a variety of positive effects on different organs, including the brain (50–52, 140, 169, 180), the cardiovascular system (1, 23, 32, 76, 174, 179), the skeletal muscles (26, 39, 47), the immune system (122), the liver (178), and the kidney (32, 73, 145), during aging. In line with this, PA levels, including those of spermidine, decline in human serum and whole blood with age (116, 121), which corroborates findings from rodent models showing that age inversely correlates with PA levels in most but not all tissue types (102). Healthy nonagenarians and centenarians display levels of spermine and spermidine comparable to those of 30- to 50-year-old adults (121) and higher than those of 60- to 80-year-olds.
디아민 푸트레스신과 천연 폴리아민(PA)인 스퍼민 및 스퍼미딘은
2개 이상의 아미노기를 가진
지방족 생리 활성 아민입니다(그림 1 및 (천연) 폴리아민의 정의라는 제목의 사이드바 참조).
폴리카티온성 특성(즉, 생리적 pH에서 아미노 그룹이 완전히 프로톤화됨)으로 인해
PAs는 DNA, RNA, 단백질 등 거대분자의 음전하를 안정화시킵니다(150).
PAs stabilize negative charges of macromolecules,
including DNA, RNA, and proteins.
DNA, RNA, 단백질은 거대 분자이며, 음전하를 띠고 있습니다. 폴리케티온은 양전하를 띠고 있기 때문에, 이들과 결합하여 음전하를 중화시키고 구조를 안정화시키는 역할을 합니다. 마치 자석의 N극과 S극처럼 서로 끌어당기는 원리라고 생각하시면 됩니다. 이러한 안정화는 DNA 복제, RNA 전사, 단백질 합성 등 생명 유지에 필수적인 과정에서 중요

스퍼미딘과 키토산은 대표적인 양전하 물질로,
DNA, RNA, 단백질과 같은 음전하를 띤 생체 분자들과 상호작용하여
이들의 구조를 안정화시키는 역할을 합니다.
스퍼미딘은 세포 성장 및 분열, 유전자 발현 조절 등에 관여하며,
키토산은 항균 작용, 지혈 효과, 약물 전달체 등 다양한 용도로 활용
DNA, RNA, 단백질이 음전하를 띠는 이유
DNA, RNA, 단백질은 인산기 또는 카르복실기와 같은 작용기를 가지고 있기 때문입니다.
이러한 작용기는 pH 7.4의 생리적 조건에서 음전하를 띠며,
이로 인해 DNA, RNA, 단백질은 전체적으로 음전하를 띠게 됩니다
인산기, 카르복실기 외에도 황산기(-SO3H)나 설폰산기(-SO3-)와 같은 작용기가
음전하를 띠게 할 수 있습니다.
이러한 작용기들은
pH 7.4의 생리적 조건에서 음전하를 띠며,
생체 분자들의 구조와 기능에 영향을 미칩니다
아민기(-NH2)나 암모늄 이온(-NH4+)과 같은 작용기가 양전하를 띠게 합니다.
이러한 작용기들은 pH 7.4의 생리적 조건에서 양전하를 띠며, 생체 분자들의 구조와 기능에 영향을 미칩니다
전기음성도는 원자가 화학 결합에서 전자를 끌어당기는 힘을 의미합니다. 전기음성도가 큰 원자는 전자를 끌어당겨 음전하를 띠기 쉽고, 전기음성도가 작은 원자는 전자를 잃어 양전하를 띠기 쉽습니다. 예를 들어, 물 분자에서 산소는 전기음성도가 커서 수소 원자의 전자를 끌어당겨 부분적인 음전하를 띠고, 수소 원자는 부분적인 양전하를 띱니다.
polycationic nature
(i.e., the amino groups are fully protonated at physiological pH)
https://pmc.ncbi.nlm.nih.gov/articles/PMC8512059/

키틴과 그 탈아세틸화 유도체인 키토산은 (β1→4) 결합된 N-아세틸-2-아미노-2-데옥시-D-글루코스 (글루코사민, GlcN) 와 2-아미노-2-데옥시-D-글루코스 (N-아세틸-글루코사민, GlcNAc) 잔기로 구성되어 있습니다. 키토산은 수성 산성 매체에서 일차 아민 프로톤화 통해 용해됩니다. 반면 키틴은 아세틸화 잔기의 수가 충분히 많아 수성 산성 매체에서 용해되지 않습니다.
키틴은 갑각류의 외골격, 곤충의 껍질, 해조류 및 곰팡이의 세포벽에서 발견되는 매우 풍부한 생물고분자입니다. 키토산은 자연에서 덜 흔하며 일부 곰팡이 (Mucoraceae)에서 발견됩니다. 역사적으로 상업용 키토산 샘플은 주로 갑각류에서 추출한 키틴의 화학적 아세틸화 제거를 통해 생산되었습니다. 최근에는 식물성 재료에 대한 수요 증가로 인해 곰팡이에서 유래한 키토산이 시장에서 주목받고 있습니다. 또한 이러한 샘플은 낮은 점도 측면에서 더 잘 제어되며 매우 높은 아세틸화 제거도를 나타냅니다 [1]. 곤충의 껍질에서 생산되는 키토산도 단백질 생산에 대한 관심 증가로 인해 주목받고 있습니다.
키틴과 키토산에 대한 관심은 이러한 폴리머가 나타내는 다양한 생물학적 및 기술적 특성(표 1)에 기반을 두고 있습니다. 그러나 이러한 특성은 폴리머의 물리화학적 특성(주로 분자량과 아세틸화 정도)과 밀접하게 연관되어 있습니다[2]. 따라서 키틴과 키토산을 다루는 경우 폴리머의 특성 분석이 필수적입니다. 키틴, 키토산 및 키토올리고사카라이드를 특성 분석하기 위한 여러 방법이 제안되었으나, 이는 본 논문의 목적에서 벗어나므로 관심 있는 독자들은 관련 문헌[3,4]을 참고하시기 바랍니다.
PA는
세포의 성장과 증식에 필수적입니다 (8)
하지만
항산화 활동 촉진, 이온 채널에 영향, 단백질 번역 제어 등
여러 가지 다른 기능도 수행하며,
세포 사멸 (138), 자가포식 (34), 면역 조절 (55, 122, 136) 등 복잡한 과정에도 영향을 미칩니다.
모든 유형의 세포가 신생합성을 통해 PAs를 생성할 수 있지만,
PAs의 상당 부분은 외부에서 유래하며,
이는 신체 내 PA 풀을 유지하는 데 식단의 중요성을 강조합니다(7, 100, 182).
특히,
스페르미딘의 외부 투여는
다양한 장기(뇌(50–52, 140, 169, 180),
심혈관 시스템(1, 23, 32, 76, 174, 179),
면역 시스템(122), 간(178), 신장(32, 73, 145) 등에
긍정적인 영향을 미칩니다.
이와 일치하게,
PA 수준(스페르미딘 포함)은
인간 혈청과 전혈에서 연령과 함께 감소합니다(116, 121),
이는 쥐 모델 연구 결과와 일치하며,
대부분의 조직 유형에서 연령과 PA 수준이 역상관 관계를 보이지만
모든 조직 유형에서 그렇지는 않다는 점을 보여줍니다(102).
건강한 90대 및 100대 노인들은
30~50세 성인과의 스퍼민과 스퍼미딘 수치가 유사하며(121),
60~80세 노인보다 높습니다.
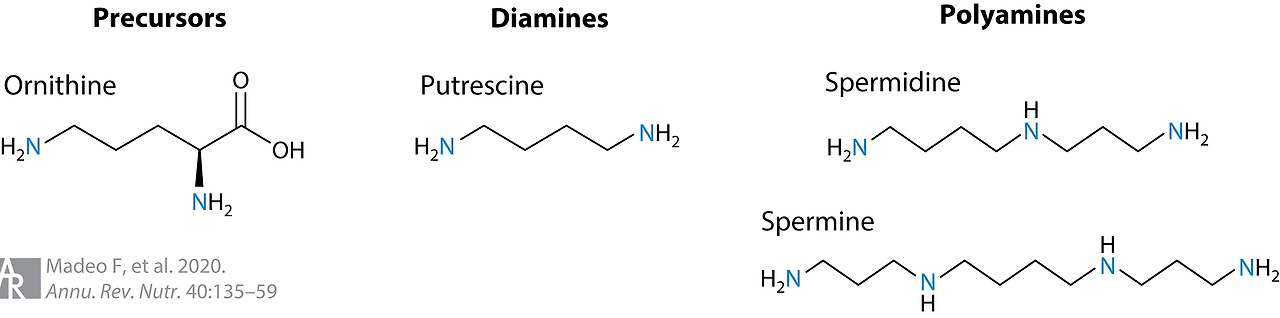
Figure 1 Structural formulas of the polyamine precursor ornithine, the diamine putrescine, and the polyamines spermidine and spermine.
Click to view
| DEFINITION OF (NATURAL) POLYAMINES Polyamines (PAs) are a subclass of bioactive amines that perform a variety of functions in living cells (132). Many of the biogenic (i.e., biologically formed) amines are generated from different amino acids or related metabolites by decarboxylase reactions (142). For example, the diamine putrescine is produced from its precursor ornithine (catalyzed by ODC1) by the ornithine decarboxylase (ODC) reaction. Subsequently, the PAs spermidine and spermine (the only naturally occurring PAs that carry more than two amino groups) originate from their precursor putrescine by distinct metabolic reactions (115, 138). The functions of spermidine and spermine differ from those of diamines and other biogenic amines at the cellular and organismal levels in several respects, particularly regarding their health-promoting effects (32, 61–63, 83). Therefore, we do not consider putrescine, spermidine, and spermine (which are often collectively referred to as natural PAs) to be equivalent. We use distinct terms within this review to differentiate them: Natural polyamine refers to spermidine and spermine, and diamine refers to putrescine. We thus stress the importance of studying separately the functions of the two natural PAs and the diamine putrescine. (자연적) 폴리아민의 정의 폴리아민(PAs)은 생체 세포에서 다양한 기능을 수행하는 생물활성 아민류의 하위 분류입니다(132). 많은 생물학적(즉, 생물학적으로 형성된) 아민은 아미노산이나 관련 대사산물로부터 디카르복실화 반응을 통해 생성됩니다(142). 예를 들어, 다이아민 푸트레신은 전구체 오르니틴(ODC1에 의해 촉매됨)으로부터 오르니틴 탈카복실화 반응(ODC 반응)을 통해 생성됩니다. 이후, PA인 스페르미딘과 스페르민(두 개 이상의 아미노 그룹을 가진 유일한 자연 발생 PA)은 전구체 푸트레신으로부터 서로 다른 대사 반응을 통해 생성됩니다(115, 138). 스페르미딘과 스페르민은 다이아민 및 기타 생물학적 아민과 세포 및 유기체 수준에서 여러 측면에서 기능이 다르며, 특히 건강 증진 효과 측면에서 차이가 있습니다(32, 61–63, 83). 따라서 우리는 푸트레신, 스페르미딘, 스페르민(흔히 자연적 폴리아민으로 통칭됨)을 동일시하지 않습니다. 이 리뷰에서는 이를 구분하기 위해 별도의 용어를 사용합니다: 자연적 폴리아민은 스페르미딘과 스페르민을 지칭하며, 다이아민은 푸트레신을 의미합니다. 우리는 두 자연적 폴리아민과 다이아민인 푸트레신의 기능을 별도로 연구하는 것이 중요함을 강조합니다. |
Whereas its cellular metabolism and basic cellular functions have been studied for a long time, the health-promoting effects of dietary spermidine represent a relatively young field that has just begun to approach clinical translation. This review focuses on the importance of dietary PAs, particularly spermidine, while summarizing the current knowledge of spermidine content in human nutrition, the molecular basis of its uptake and distribution within the body, and its importance for human health.
세포 대사 및 기본 세포 기능에 대한 연구가 오랫동안 진행되어 왔지만, 식이 스퍼미딘의 건강 증진 효과는 임상 적용 단계로 접어들기 시작한 비교적 새로운 분야입니다.
이 리뷰는
식이 폴리아민의 중요성, 특히 스퍼미딘에 초점을 맞추어
인간 영양에서의 스퍼미딘 함량, 체내 흡수 및 분포의 분자적 기반,
그리고 인간 건강에 대한 중요성을 요약합니다.
2. SPERMIDINE CONTENT IN FOOD AND HUMAN NUTRITION
The natural PAs spermidine and spermine are ubiquitously present in living organisms of different phyla, including bacteria, plants, fungi, and animals, and are heat resistant (i.e., they are not destroyed by cooking). As a consequence, PAs are abundant in the daily nutrition of humans (100, 113). However, the PA content of different foods greatly varies ( Figure 2 ). One of the most comprehensive compilations was reported in 2011 by Atiya et al. (7), who summarized the PA content of various types of foods reported in prior reports and databases (9–11, 15, 27, 35, 65–68, 75, 77–79, 97, 101, 102, 105, 106, 108, 130, 143, 164, 181). A more recent summary of the PA content of food categories is also available (100). Moreover, several studies have focused on specialized food types, such as various kinds of cheeses (38, 149).
2. 식품 및 인간 영양에서의 스페르미딘 함량
자연적 PA인 스페르미딘과 스페르민은
박테리아, 식물, 곰팡이, 동물 등 다양한 문에 속하는
생물체에 널리 존재하며 열에 강합니다
(즉, 조리로 파괴되지 않습니다).
이로 인해 PA는
인간의 일상적인 영양에 풍부하게 존재합니다(100, 113).
그러나
다양한 식품의 PA 함량은 크게 다릅니다( Figure 2 ). 가장 포괄적인 집계는 2011년 Atiya 등(7)에 의해 보고되었습니다. 은 이전 보고서와 데이터베이스에 보고된 다양한 식품의 PA 함량을 요약했습니다(9–11, 15, 27, 35, 65–68, 75, 77–79, 97, 101, 102, 105, 106, 108, 130, 143, 164, 181). 식품 카테고리의 PA 함량에 대한 더 최근의 요약도 이용 가능합니다(100). 또한, 다양한 종류의 치즈(38, 149)와 같은 특수 식품 유형에 초점을 맞춘 여러 연구도 진행되었습니다.
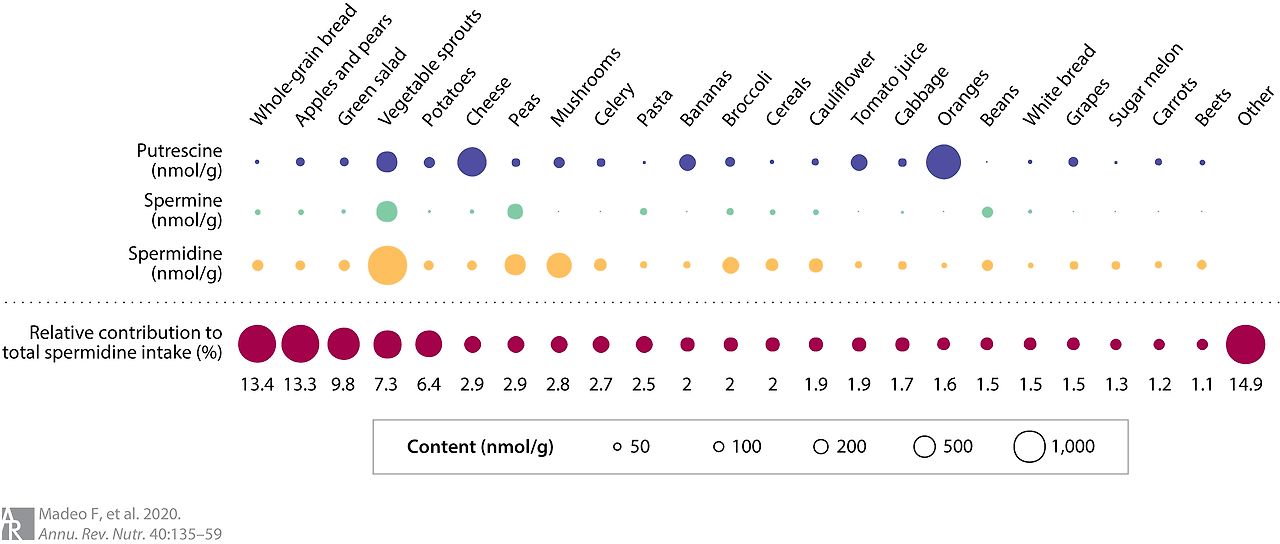
Figure 2 An example of polyamine content and the contribution of food to daily spermidine intake taken from a distinct regional population in South Tyrol, Italy. Data were adapted from polyamine levels and nutritional information previously published in the epidemiological Bruneck Study (71 and references therein) and from personal communication with S. Kiechl. The relative spermidine intake (% of total intake) is depicted (the size of the circles linearly corresponds to the relative intake values) and compared with the absolute mean concentrations of the diamine putrescine and the polyamines spermidine and spermine for indicated food categories. Note that the relative contribution of a given food category to total spermidine intake is calculated from both its spermidine content and the actual amount ingested (not shown). Therefore, both large intake of certain foods (despite moderate spermidine content) and high spermidine content (despite low intake) may result in a high relative contribution to total spermidine intake.
그림 2 이탈리아 남티롤의 특정 지역 인구에서 일일 스페르미딘 섭취량에 대한 폴리아민 함량과 식품의 기여도 예시.
데이터는 역학 연구인 Bruneck Study(71 및 해당 참고문헌)에서 이전에 발표된 폴리아민 수준 및 영양 정보에서 적응되었으며, S. Kiechl과의 개인적 소통을 통해 추가 정보를 얻었습니다. 상대적 스페르미딘 섭취량(총 섭취량의 %)이 표시되어 있으며(원 크기는 상대적 섭취량 값과 선형적으로 대응함) 지정한 식품 카테고리에 대한 다이아민 푸트레신 및 폴리아민 스페르미딘과 스페르민의 절대 평균 농도와 비교되었습니다. 특정 식품군의 총 스페르미딘 섭취량에 대한 상대적 기여도는 해당 식품의 스페르미딘 함량과 실제 섭취량(표시되지 않음)을 모두 고려하여 계산되었습니다. 따라서 특정 식품의 섭취량이 많더라도 스페르미딘 함량이 중간 수준일 경우, 또는 스페르미딘 함량이 높더라도 섭취량이 적을 경우 모두 총 스페르미딘 섭취량에 대한 상대적 기여도가 높을 수 있습니다.
Click to view
One reason for this disparity in PA content is that organismal PA levels vary among different species, cell types, and tissues, and consequently among foods of animal, fungi, or plant origin. Plant- and fungi-derived products represent the most relevant sources for spermidine. Whole-grain products, vegetables, and legumes are among the highest spermidine-containing food categories in common human nutrition. Examples of spermidine-rich foods are wheat germ (0.35 mg/g); soybeans (0.070–0.180 mg/g); select mushrooms (0.060–0.160 mg/g), such as eringi (a.k.a. king trumpet mushroom); and various nuts and seeds, such as pine nuts (0.060 mg/g) (102).
PA 함량의 이 같은 차이는 유기체의 PA 수준이 종, 세포 유형, 조직에 따라 다르며, 따라서 동물, 곰팡이, 식물 기원 식품 간에도 차이가 나기 때문입니다. 식물 및 곰팡이 유래 제품은 스페르미딘의 가장 중요한 원천입니다. 전곡류 제품, 채소, 콩류는 일반적인 인간 영양에서 스페르미딘 함량이 가장 높은 식품 카테고리 중 하나입니다.
스페르미딘이 풍부한 식품의 예시로는
밀 배아(0.35 mg/g); 대두(0.070–0.180 mg/g); 특정 버섯(0.060–0.160 mg/g),
예를 들어 에링이(킹 트럼펫 버섯); 및 다양한 견과류와 씨앗, 예를 들어 소나무 씨앗(0.060 mg/g) (102).

Animal-derived foods generally contain less spermidine than the average plant- or fungi-derived foods. However, they display comparable levels of spermine and therefore have a higher spermine-to-spermidine ratio (7, 100). Among animal tissues, innards such as liver, spleen, and kidney contain the highest amount of spermidine, with average concentrations as high as 0.161 mg/g in cow liver (65), whereas classical meat and meat products range from 0.001 to 0.020 mg/g (7, 66). Note that the published literature reports high variations in spermidine levels for select food items, as exemplified for bovine liver, for which the spermidine level ranges from 0.0068 to 0.390 mg/g (65). Such variation might mirror regional, species-, or food production–related differences, or may even indicate methodological problems with respect to the robustness of PA measurements, and thus clearly requires further investigation. Another relevant source for spermidine from animal-derived products is aged cheese, which contains levels of spermidine as high as 0.073 mg/g (and exceptionally high levels of up to 0.200 mg/g in aged cheddar) (11), although again the levels reported for different kinds of cheeses vary considerably (38, 149). Of note, cheese may contain high concentrations of other biogenic amines, such as putrescine and histamine, among others (38, 149). The high concentration of biogenic amines in aged cheese compared with that in raw milk likely results from microbial activities during the fermentation process (108).
동물성 식품은
일반적으로 식물성 또는 곰팡이 유래 식품보다 스페르미딘 함량이 낮습니다.
그러나
스페르민 함량은 유사하며 따라서
스페르민-스페르미딘 비율이 더 높습니다(7, 100).
동물 조직 중에서는
간, 비장, 신장 등 내장 부위가 가장 높은 스페르미딘 함량을 보이며,
소 간에서는 평균 농도가 0.161 mg/g에 달합니다(65),
반면 전통적인 육류 및 육류 제품은 0.001~0.020 mg/g 사이입니다(7, 66). 참고로, 출판된 문헌에서는 특정 식품의 스페르미딘 함량에 큰 변동이 보고되었으며, 예를 들어 소 간에서는 스페르미딘 함량이 0.0068에서 0.390 mg/g까지 다양합니다(65). 이러한 변동은 지역적, 종별, 또는 식품 생산 관련 차이를 반영할 수 있으며, PA 측정 방법의 신뢰성 문제도 시사할 수 있으므로 추가 연구가 분명히 필요합니다.
동물성 제품에서 스페르미딘의 또 다른 중요한 원천은 숙성 치즈로,
최대 0.073 mg/g (숙성 체다 치즈에서는 예외적으로 높은 0.200 mg/g까지)의 스
페르미딘 함량을 포함합니다 (11).
그러나 다시 한 번, 다양한 종류의 치즈에서 보고된 함량은 크게 다릅니다 (38, 149). 참고로, 치즈는 푸트레신과 히스타민 등 다른 생물학적 아민을 높은 농도로 함유할 수 있습니다(38, 149).
숙성 치즈의 생물학적 아민 농도가
원유보다 높은 것은 발효 과정 중
미생물 활동 때문일 가능성이 높습니다(108).
Importantly, common portion sizes or actual intake amounts should be considered when discussing the relevance of certain foods regarding their contribution to overall spermidine intake. Diverse food items differ in magnitude in their contribution to the dietary intake of spermidine, depending on two combinable variables: (a) the amount of food ingested and (b) the spermidine content of the ingested food ( Figure 2 ). Therefore, food items with moderate levels of spermidine may still contribute to the daily spermidine intake at a similar or even higher degree than spermidine-rich foods if comparably ingested at higher amounts. For instance, whole-grain products, green salad, apples and pears, and potatoes, which are all rather moderately rich in spermidine, were among the top five spermidine-contributing foods ( Figure 2 ) in a food frequency questionnaire (FFQ)-based epidemiological study (32). Another study, also based on FFQ-based data, reported green peas as the main source of spermidine (182).
특히, 특정 식품이 전체 스페르미딘 섭취량에 기여하는 정도를 논의할 때는 일반적인 섭취량이나 실제 섭취량을 고려해야 합니다. 다양한 식품은 섭취량과 섭취한 식품의 스페르미딘 함량이라는 두 가지 결합 가능한 변수에 따라 식이 섭취량에 기여하는 정도가 다릅니다( 그림 2). 따라서 스페르미딘 함량이 중간 수준인 식품도, 스페르미딘이 풍부한 식품과 비교해 유사하거나 더 높은 수준으로 일일 스페르미딘 섭취량에 기여할 수 있습니다. 예를 들어, 스페르미딘 함량이 중간 수준인 전곡류 제품, 녹색 샐러드, 사과와 배, 감자는 식품 빈도 조사(FFQ) 기반 역학 연구(32)에서 스페르미딘 기여도 상위 5개 식품에 포함되었습니다( Figure 2 ). 또 다른 FFQ 기반 연구에서는 녹색 완두콩이 스페르미딘의 주요 원천으로 보고되었습니다(182).
The remarkable differences in the spermidine content of various foods, as well as the regional and cultural variances in human nutrition, have resulted in country-specific estimates of spermidine intake. A positive association between gross domestic product and the total PA per energy content of food for 33 Asian countries was reported (15). Gross domestic product is a representative indicator of socioeconomic status and correlates with health span and life span (15 and references therein), arguing for a potential positive association of PAs in food with healthy diet. However, the cause–effect relationship of this correlation remains elusive and needs to be determined in future intervention trials.
As noted above, the average estimated intake of spermidine differs by country. The daily intake is calculated to be approximately 13 mg for Asian countries (15), 8 mg for the United States, and as low as 5 mg for Turkey (19). For Europe the available data suggest an average intake similar to that of Asian countries, of approximately 13 mg per day (182). However, noticeable variations are present among European countries (summarized in 100): Spermidine intake values range from 10 mg (Sweden) to 12 mg (Italy) to almost 15 mg (Spain) per day. Regional differences are likely present within countries. For instance, the typical Mediterranean diet contains significantly higher levels of spermidine than the average southern European diet, with an estimated intake of up to 26 mg of spermidine per day (7, 9). On the basis of calculations using the recommended composition of a standard healthy diet according to the Swedish Nutrition Recommendations Objectified (SNO), the recommended daily amount of spermidine has been estimated to be approximately 30 mg for males and 25 mg for females (6). As a word of caution, all these estimates rely on calculations from generalized food consumption estimates, which may not always reflect real-life and individual situations.
다양한 식품의 스페르미딘 함량 차이와 지역 및 문화적 영양 차이는 국가별 스페르미딘 섭취량 추정치의 차이를 초래했습니다. 33개 아시아 국가에서 국내총생산(GDP)과 식품 에너지 함량당 총 PA(PA) 사이의 긍정적 연관성이 보고되었습니다(15). 국내총생산은 사회경제적 지위의 대표적 지표로 건강 수명과 수명과 상관관계가 있으며(15 및 해당 참고문헌), 식품 내 PA와 건강한 식습관 간의 잠재적 긍정적 연관성을 시사합니다. 그러나 이 상관관계의 인과관계는 명확하지 않으며, 향후 개입 연구를 통해 확인되어야 합니다.
위에서 언급된 바와 같이, 스페르미딘의 평균 추정 섭취량은 국가별로 다릅니다. 일일 섭취량은 아시아 국가에서 약 13mg(15), 미국에서 8mg, 터키에서는 5mg까지 낮게 추정되었습니다(19). 유럽의 경우 이용 가능한 데이터는 아시아 국가와 유사한 평균 섭취량인 약 13mg/일(182)을 제시합니다. 그러나 유럽 국가 간에는 눈에 띄는 차이가 존재합니다(100에 요약됨):
스퍼미딘 섭취량은
스웨덴 10mg, 이탈리아 12mg, 스페인 15mg에 이릅니다.
국가 내 지역별 차이도 존재할 가능성이 있습니다.
예를 들어,
지중해 식단은 남유럽 평균 식단보다 스퍼미딘 함량이 현저히 높으며,
하루 최대 26mg의 스퍼미딘 섭취량이 추정됩니다(7, 9).
스웨덴 영양 권장 사항 객관화(SNO)에 따른 표준 건강 식단의 권장 구성비를 바탕으로 계산한 결과, 남성의 경우 하루 권장 섭취량은 약 30mg, 여성은 약 25mg으로 추정되었습니다(6). 주의할 점은 모든 추정치가 일반화된 식품 섭취 추정치를 기반으로 한 계산에 의존하며, 실제 생활이나 개인별 상황에 항상 반영되지 않을 수 있다는 점입니다.
An epidemiological study reported similar mean values of spermidine intake based on individual assessments of dietary habits using high-standard food questionnaires assisted by dieticians. A cohort of 829 study participants in Bruneck, a small town in northern Italy, consumed on average approximately 10 mg of spermidine per day (71). However, realistic table values of spermidine have not been determined directly, and present intake estimates are based solely on previously determined PA contents from similar foods. Due to the strong variations in spermidine content, even within specific food items, direct assessments of actual spermidine levels in food samples would be desirable and would allow more rigorous studies of the impact of spermidine intake on human health.
영양사 보조 하에 고품질 식품 설문지를 사용한 개인별 식습관 평가를 기반으로 한 역학 연구에서도 유사한 평균 스페르미딘 섭취량이 보고되었습니다. 이탈리아 북부 작은 마을 브루네크의 829명 연구 참여자는 하루 평균 약 10mg의 스페르미딘을 섭취했습니다(71). 그러나 스페르미딘의 현실적인 표기 값은 직접적으로 결정되지 않았으며, 현재 섭취 추정치는 유사 식품에서 이전에 결정된 PA 함량에 기반합니다. 스페르미딘 함량의 강한 변동성으로 인해, 특정 식품 내 실제 스페르미딘 수준을 직접 평가하는 것이 바람직하며, 이는 스페르미딘 섭취가 인간 건강에 미치는 영향을 더 엄격히 연구하는 데 기여할 것입니다.
3. STABILITY OF SPERMIDINE IN FOODS AND DURING FOOD PROCESSING
Many reports have focused on the actual PA content of select foods, but very little is known about how agricultural and food-processing techniques may influence these levels. Large variations, particularly in animal-derived products such as innards or cheese, suggest that the specific origin and processing of the raw material significantly impact spermidine content. Storage temperature, the stage of ripening, and contact with oxygen may all affect the stability of PAs in stored foods and thus determine the final content of spermidine before consumption (3, 119).
PA stability during storage appears quite diverse. For instance, refrigerated meat displayed stable levels of spermidine over 8 days, however, with a gradual decrease in spermine content and, surprisingly, an increase in putrescine levels (54). In eggplant, spermidine content remained stable over 12 days independent of the storage temperature (3°C versus 20°C), whereas putrescine content increased at low temperature (29). In contrast, spermidine content decreased during a storage period of 12 days when eggplants were subjected to heat (35°C) for 1 h prior to storage, which also prevented an increase in putrescine (29). Such a decrease in spermidine levels, accompanied by an increase in putrescine, in response to chilling injury occurs in other types of fruits, including lemons (89), unripe peaches stored at 1 and 5°C (163), and zucchini squash (139), among others (see 29). In general, these effects may be explained by a metabolic stress response in fruits following storage at low temperatures, leading to the activation of PA biosynthesis, an effect that is avoided by a short-term application of moderate heat. This stress response likely accounts for increased putrescine levels and may even result in the recovery of spermidine, which at first glance seems to be degraded when food is stored. Metabolic adaptations to stress should thus be considered when PA stability in foods is investigated.
Fermentation processes are generally believed to favor the production of several biological amines (142). For instance, fermented fish contains elevated levels of spermidine (177). Yet spermidine appears less affected by fermentation than do other biogenic amines (including putrescine and histamine), implying that not all fermented foods contain increased levels of spermidine. Ripening may potentially impact spermidine levels as well. However, although some variations occurred (a decrease of up to 10–20% depending on the genotype), spermidine content was relatively stable during banana ripening and was barely affected by cooking or frying (17).
In general, spermidine appears to be relatively stable when boiling foods (7, 66). Nevertheless, spermidine and spermine may be significantly lost from foods and released into the cooking broth or water (66, 181). For instance, cowpeas and other common beans cooked in abundant water had 50% less spermidine than their raw, uncooked form (31). However, higher temperatures achieved by baking, grilling, or deep-frying may destroy spermidine (75).
In summary, the effects of food processing, such as various cooking techniques, storage conditions, and local differences in the production process, have been only partially studied. Additional work is needed to understand their impact on the abundance of spermidine in food items.
3. 식품 및 식품 가공 과정에서의 스페르미딘 안정성
많은 연구가 특정 식품의 실제 PA 함량에 초점을 맞췄지만, 농업 및 식품 가공 기술이 이러한 수준에 미치는 영향에 대해 알려진 바는 매우 적습니다. 특히 내장이나 치즈와 같은 동물성 제품에서 큰 변동성은 원료의 특정 원산지와 가공 방법이 스페르미딘 함량에 크게 영향을 미친다는 것을 시사합니다.
저장 온도, 숙성 단계, 산소와의 접촉은
저장된 식품 내 PA의 안정성에 영향을 미칠 수 있으며,
이는 최종 섭취 시 스페르미딘 함량을 결정합니다 (3, 119).
PA의 저장 중 안정성은
매우 다양합니다.
예를 들어,
냉장 보관된 고기는 8일 동안 스페르미딘 함량이 안정적으로 유지되었지만,
스페르민 함량은 점차 감소했으며,
놀랍게도 푸트레신 함량은 증가했습니다 (54).
가지에서는 저장 온도에 관계없이(3°C 대 20°C) 12일 동안 스페르미딘 함량이 안정적으로 유지되었으나, 푸트레신 함량은 저온에서 증가했습니다(29). 반면, 저장 전 1시간 동안 열(35°C)에 노출된 가지는 12일 저장 기간 동안 스페르미딘 함량이 감소했으며, 이는 푸트레신 증가도 방지했습니다(29). 저온 손상에 대한 반응으로 스페르미딘 함량이 감소하고 푸트레신 함량이 증가하는 현상은 레몬(89), 1°C와 5°C에서 보관된 미성숙 복숭아(163), 호박(139) 등 다른 과일에서도 관찰되었습니다(29 참조). 일반적으로 이러한 효과는 저온 저장 후 과일에서 발생하는 대사 스트레스 반응으로 설명될 수 있으며, 이는 PA 생합성 활성화로 이어집니다. 이 효과는 단기적인 중간 온도 적용으로 방지됩니다. 이 스트레스 반응은 푸트레신 수치 증가를 설명할 수 있으며, 심지어 식품 저장 시 처음에는 분해되는 것처럼 보이는 스페르미딘의 회복까지 초래할 수 있습니다. 따라서 식품의 PA 안정성을 조사할 때 스트레스에 대한 대사적 적응을 고려해야 합니다.
발효 과정은
일반적으로 여러 생물학적 아민(142)의 생성을
촉진하는 것으로 알려져 있습니다.
예를 들어
발효된 어류에는
스페르미딘 수치가 높게 나타납니다(177).
그러나
스페르미딘은
다른 생물학적 아민(푸트레신과 히스타민 포함)에 비해 발효에 덜 영향을 받는 것으로 보이며,
이는 모든 발효 식품이 스페르미딘 수치가 증가하지는 않는다는 것을 의미합니다.
숙성도
스페르미딘 수준에 영향을 미칠 수 있습니다.
그러나
유전자형에 따라 최대 10–20% 감소하는 변동이 발생했지만,
바나나 숙성 과정에서 스페르미딘 함량은 상대적으로 안정적이었으며
조리나 튀김에 거의 영향을 받지 않았습니다(17).
일반적으로 스페르미딘은
그러나
스페르미딘과 스페르민은 식품에서 크게 손실되어
조리 국물이나 물로 방출될 수 있습니다(66, 181).
예를 들어,
풍부한 물에서 조리된 콩과 식물은
생식 상태에 비해 스페르미딘 함량이 50% 감소했습니다(31).
그러나
구이, 그릴, 튀김과 같은 고온 조리 방법은
스페르미딘을 파괴할 수 있습니다(75).
요약하면,
양한 조리 기술, 보관 조건, 생산 과정의 지역적 차이 등 식품 가공의 영향은
부분적으로만 연구되었습니다.
식품 내 스페르미딘 함량에 미치는 영향을 이해하기 위해
추가 연구가 필요합니다.
4. SPERMIDINE UPTAKE IN CELLS
4.1. Cellular Spermidine Import in Unicellular Organisms and Plants
Intracellular PA levels are stringently controlled by a triad of synthesis, uptake, and degradation/secretion. The uptake mechanisms of PAs into unicellular organisms have been studied for decades and are well understood, contrasting with the relatively scarce knowledge of PA transport into mammalian cells (59).
In Escherichia coli, two operon-organized adenosine 5′-triphosphate (ATP)-binding cassette (ABC) transport systems are relevant to PA and diamine metabolism: PotABCD for spermidine and PotFGHI for putrescine. Both systems consist of ATPases, channel-forming units, and substrate-binding proteins (e.g., PotD binding spermidine via four acidic residues), in which all partners are essential for metabolite uptake (59).
In yeast cells, multiple factors mediate cellular uptake of spermidine and PAs. AGP2, which was initially misidentified as a PA importer, harbors mainly PA-sensing properties that mediate the expression of other uptake-relevant factors (4, 5). The main membrane-bound PA importers are encoded by DUR3 and SAM3 (159) and GAP1 (158). Another pH-sensitive PA transporter in yeast cells is encoded by TPO1, which catalyzes PA uptake under alkaline conditions and controls export at acidic pH (161). In the unicellular parasites Leishmania major and Trypanosoma cruzi and the bacterium Neisseria gonorrhoeae, transporters bound to the plasma membrane (LmPOT1, TcPOT1.2/TcPAT12, and PotFGHI, respectively) have been identified, and such transporters present potential targets for antibiotics (20, 48, 53).
In plant cells, PA transport systems involve multiple divergent proteins that likely exhibit parallel, redundant, and less-specialized functions compared with proteins in bacterial systems (44). In Arabidopsis thaliana, members of the l-type amino acid transporter (AtLAT) family (especially plasma-membrane-bound RMV1/AtLAT1, a presumed amino acid permease) have been reported to be involved in PA uptake (43, 44). In rice (Oryza sativa), the gene PA uptake transporter 1 (OsPUT1) was identified as a preferred transporter of spermidine (99).
4. 세포 내 스페르미딘 흡수
4.1. 단세포 생물과 식물에서의 세포 내 스페르미딘 흡수
세포 내 PA 수준은
합성, 흡수, 분해/분비라는 삼중 조절 체계에 의해 엄격히 조절됩니다.
단세포 생물에서의 PA 흡수 메커니즘은
수십 년간 연구되어 잘 이해되고 있지만,
포유류 세포로의 PA 운반에 대한 지식은 상대적으로 부족합니다 (59).
Escherichia coli에서는 PA 및 다이아민 대사 관련 두 개의 오페론 조직화된 아데노신 5′-트리포스페이트(ATP) 결합 캐스케이드(ABC) 수송 시스템이 존재합니다: 스페르미딘을 운반하는 PotABCD와 푸트레신(putrescine)을 운반하는 PotFGHI입니다. 두 시스템 모두 ATPase, 채널 형성 단위, 기질 결합 단백질(예: PotD는 네 개의 산성 잔기로 스페르미딘을 결합함)로 구성되며, 모든 구성 요소가 대사체 흡수에 필수적입니다(59).
효모 세포에서, 여러 요인이 스페르미딘과 PA의 세포 흡수를 매개합니다. 처음에는 PA 수입체로 잘못 식별되었던 AGP2는 주로 다른 흡수 관련 인자의 발현을 매개하는 PA 감지 특성을 가지고 있습니다 (4, 5). 주요 막 결합 PA 수입체는 DUR3 및 SAM3 (159)와 GAP1 (158)에 의해 암호화되어 있습니다. 효모 세포에서 또 다른 pH에 민감한 PA 수송체는 TPO1에 의해 암호화되어 알칼리성 조건에서 PA 흡수를 촉매하고 산성 pH에서 수출을 제어합니다 (161). 단세포 기생충 Leishmania major와 Trypanosoma cruzi 및 세균 Neisseria gonorrhoeae에서는 세포막에 결합된 운반체(각각 LmPOT1, TcPOT1.2/TcPAT12, PotFGHI)가 식별되었으며, 이러한 운반체는 항생제의 잠재적 표적이 될 수 있습니다(20, 48, 53).
식물 세포에서 PA 수송 시스템은 세균 시스템의 단백질에 비해 평행적, 중복적, 덜 특화된 기능을 가질 가능성이 높은 다양한 단백질을 포함합니다(44). Arabidopsis thaliana에서 l-형 아미노산 운반체(AtLAT) 가족의 구성원(특히 플라즈마막 결합형 RMV1/AtLAT1, 추정되는 아미노산 투과체)이 PA 흡수(43, 44)에 관여한다는 보고가 있습니다. 쌀(Oryza sativa)에서 PA 흡수 운반체 1(OsPUT1) 유전자가 스퍼미딘의 선호 운반체로 확인되었습니다(99).
4.2. Spermidine Import Mechanisms in Mammals
Intracellular depletion of PAs [e.g., by treatment with difluoromethylornithine (DFMO), an ODC inhibitor] (44), stimulation with growth factors (16), and proliferation (155, 175) all lead to increased uptake of PAs. Enhanced proliferation is indeed linked to elevated uptake of PAs into lung, liver, and cancer cells (44, 137). Several PA analogs, including d-lysine spermine (MQT-1426), N 1-spermyl-l-lysinamide (OR1202), and d-Lys(C16acyl)-spermine (AMXT1501), reduce cellular PA uptake. Preclinical studies have shown that a combination of PA-uptake inhibitors (e.g., AMXT1501) and DFMO drastically reduces intracellular PA levels, thereby exerting a synergistic antiproliferative effect on cancer cells, in vitro and in vivo, in preclinical mouse models (45, 46). However, so far, specific uptake systems in mammalian cells are poorly understood, and single genes/proteins involved in the uptake process have not yet been holistically characterized. The complex picture of the mammalian PA transport system and its regulation has been reviewed elsewhere (2, 120) but likely involves tissue- and cell type–specific factors, suggested by the multiple PA transporter candidates described.
4.2. 포유류에서의 스퍼미딘 수입 메커니즘
PA의 세포 내 고갈[예: ODC 억제제인 디플루오로메틸오르니틴(DFMO) 처리](44), 성장 인자 자극(16), 증식(155, 175)은 모두 PA의 흡수 증가를 유발합니다. 증식 증가가 실제로 폐, 간, 암 세포로의 PA 흡수 증가와 연관되어 있습니다(44, 137). PA 유사체 중 d-라이신 스퍼민 (MQT-1426), N 1-스퍼밀-L-라이신아미드 (OR1202), 및 d-라이스(C16아실)-스퍼민 (AMXT1501)은 세포 내 PA 흡수를 감소시킵니다. 전임상 연구에서 PA 흡수 억제제(예: AMXT1501)와 DFMO의 조합은 세포 내 PA 수준을 급격히 감소시켜 전임상 마우스 모델에서 체외 및 체내에서 암 세포에 대한 시너지 항증식 효과를 발휘합니다(45, 46). 그러나 현재까지 포유류 세포 내 PA 흡수 시스템의 구체적인 메커니즘은 잘 이해되지 않았으며, 흡수 과정에 관여하는 단일 유전자/단백질은 아직 종합적으로 특성화되지 않았습니다. 포유류 PA 운반 시스템과 그 조절 메커니즘의 복잡한 그림은 다른 문헌에서 검토되었으나(2, 120), 조직 및 세포 유형 특이적 요인이 관여할 가능성이 제시되었습니다.
Various transport systems have been suggested to partly mediate PA transport into mammalian cells ( Figure 3 ). These include solute carrier family 7 member 1 (SLC7A1), cation-chloride cotransporter 9 (CCC9), and organic cation transporter 6 (OCT-6), which function as permeases for lysine, arginine, and ornithine; inorganic ions; and cations, anions, and zwitterions, respectively (92, 120). This idea is supported by findings of PA transporters in synaptic vesicles, neurons, and glial cells (85). SLC18B1-encoded vesicular PA transporters may be responsible for storage of vesicular spermidine/spermine in (hippocampal) neurons (56) and are also expressed in mast cells that release PAs (152). More recently, SLC3A2, which forms heterodimers with various partners transporting different molecules, has been identified as a major PA transporter in neuroblastoma. Knockdown of SLC3A2 decreased spermidine uptake, and DFMO-mediated inhibition of synthesis increased SLC3A2 levels (46). SLC3A2 is strongly overexpressed in some cancer cell lines (46). Nonetheless, SLC3A2 has previously been implicated in PA export processes, implying a bidirectional role of intracellular PA regulation (160, 162) and suggesting level-, tissue-, and cell type–specific functions.
포유류 세포로의 PA 수송을 부분적으로 매개하는 다양한 수송 시스템이 제안되었습니다( Figure 3 ). 이에는 라이신, 아르기닌, 오르니틴의 투과체로 기능하는 솔루트 캐리어 가족 7 멤버 1(SLC7A1), 양이온-염화물 공수송체 9(CCC9), 그리고 무기 이온, 양이온, 음이온, 및 양이온-음이온 이온을 수송하는 유기 양이온 수송체 6(OCT-6)가 포함됩니다(92, 120). 이 아이디어는 시냅스 소포, 뉴런 및 신경교 세포에서 PA 수송체가 발견된 사실에 의해 뒷받침됩니다 (85). SLC18B1에 의해 암호화되는 소포 PA 수송체는 (해마) 뉴런에 소포 스퍼미딘/스퍼민을 저장하는 역할을 할 수 있으며 (56), PA를 방출하는 비만 세포에서도 발현됩니다 (152). 최근에는 다양한 파트너와 이종 이합체를 형성하여 다른 분자를 운반하는 SLC3A2가 신경모세포종에서 주요 PA 운반체로 확인되었습니다. SLC3A2의 발현을 억제하면 스페르미딘 흡수량이 감소했으며, DFMO를 통해 합성을 억제하면 SLC3A2 수준이 증가했습니다(46). SLC3A2는 일부 암 세포계에서 강하게 과발현됩니다(46). 그러나 SLC3A2는 이전에 PA 수출 과정에 관여한 것으로 보고되어 세포 내 PA 조절의 양방향 역할을 시사하며(160, 162), 수준, 조직, 세포 유형에 특이적인 기능을 제안합니다.
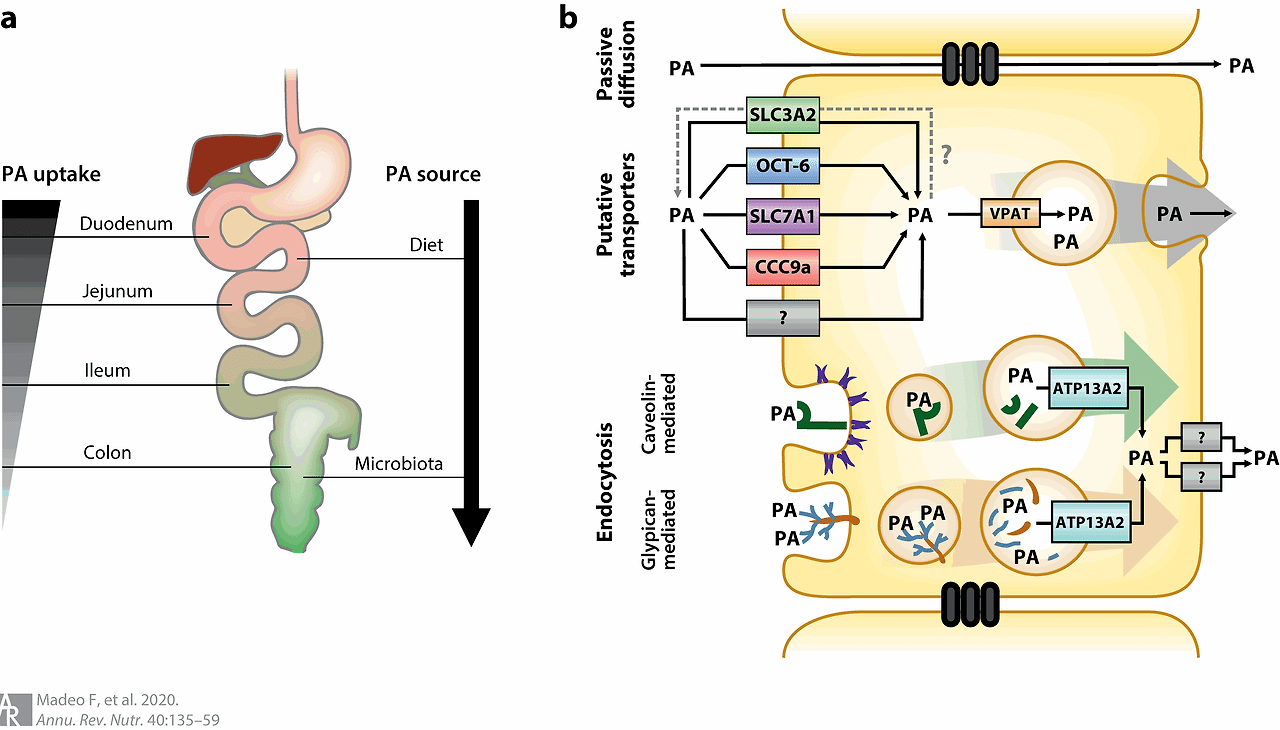
Figure 3 Intestinal uptake and putative cellular transport mechanisms of PAs in mammals. (a) PAs absorbed in the gastrointestinal tract are derived mainly from food and the gut microbiota, with most PAs being resorbed in the upper part of the small intestine from dietary sources. PAs taken up in the lower part of the gastrointestinal tract originate mainly from microbiota. (b) Putative cellular PA import systems in mammals include two distinct modes of endocytosis, several proposed transporters, and paracellular passive diffusion. Depending on the tissue, putative routes of PA export include the release of vesicular PA stores (as suggested for neurons and mast cells) and transport via yet uncharacterized transporters. Abbreviations: ATP13A2, ATPase cation transporting 13A2; CCC9a, cation-chloride cotransporter 9a; OCT-6, organic cation transporter 6; PA, polyamines (spermine, spermidine) and putrescine; SLC3A2, solute carrier family 3 member 2; SLC7A1, solute carrier family 7 member 1; VPAT, vesicular polyamine transporter.
그림 3 포유류에서의 PA 장 흡수 및 추정 세포 내 수송 메커니즘.
(a) 위장관에서 흡수된 PA는 주로 음식과 장 미생물에서 유래하며, 대부분의 PA는 소장 상부에서 식이 원천으로부터 재흡수됩니다. 위장관 하부에서 흡수된 PA는 주로 미생물에서 유래합니다.
(b) 포유류의 PA 세포 내 흡수 시스템에는 두 가지 다른 내포작용 모드, 여러 제안된 운반체, 및 세포 간 수동 확산이 포함됩니다. 조직에 따라 PA 배출 경로는 신경세포와 비만세포에서 제안된 것처럼 소포 내 PA 저장소의 방출 및 아직 특성화되지 않은 운반체를 통한 운반을 포함합니다.
약어: ATP13A2, ATPase 양이온 운반체 13A2; CCC9a, 양이온-염화물 공수송체 9a; OCT-6, 유기 양이온 수송체 6; PA, 폴리아민(스퍼민, 스퍼미딘) 및 푸트레신; SLC3A2, 용질 운반체 가족 3 구성원 2; SLC7A1, 용질 운반체 가족 7 구성원 1; VPAT, 소포체 폴리아민 수송체.
소변으로 70~80%,
대변으로 20~30% 정도 배출
Click to view
In addition to these putative permease-based transport systems, it is believed that the uptake of spermidine and other PAs in mammalian cells may be mediated by endocytosis (12) ( Figure 3 ). In particular, glypican-mediated and caveolin-mediated endocytosis have been suggested to enable PA internalization into mammalian cells (12, 13, 120, 160). The ATPase cation transporting 13A2 (ATP13A2) (also called PARK9) was recently suggested to be a lysosomal PA transporter (favoring spermine and spermidine), facilitating endocytosis-mediated PA uptake (via subsequent export to the cytosol from endolysosomes) (165). Knocking out ATP13A2 results in lowered intracellular PA levels and dysfunctional ATP13A2 impairs lysosomal PA export to the cytosol, resulting in cell death and possibly neurodegeneration (which corroborates its genetic implication in parkinsonisms) (165). ATP13A2 thus emerges as a new and potentially central player in cellular PA homeostasis, regulating both cytosolic and lysosomal PA levels.
Thus, the exact interplay of different uptake mechanisms of spermidine and spermine in mammalian cells and their individual contribution to intracellular PA levels remain to be determined, and the emerging picture will likely involve tissue- and cell type–specific factors.
이들 추정된 퍼미어 기반 운반 시스템 외에도, 포유류 세포에서의 스퍼미딘 및 기타 폴리아민(PA)의 흡수 과정은 엔도사이토시스(12) ( 그림 3 )를 통해 매개될 수 있다고 추정됩니다. 특히, 글리피칸 매개 및 카베올린 매개 엔도사이토시스가 포유류 세포로의 PA 내재화를 가능하게 한다는 제안이 있습니다(12, 13, 120, 160). ATPase 양이온 운반체 13A2 (ATP13A2) (PARK9라고도 함)는 최근 리소좀 PA 운반체(스퍼민과 스퍼미딘을 선호함)로 제안되었으며, 엔도사이토시스 매개 PA 흡수(엔도리소좀에서 세포질로의 후속 수출을 통해)를 촉진합니다(165). ATP13A2를 결손시킨 경우 세포 내 PA 수준이 감소하며, ATP13A2 기능 장애는 리소좀 내 PA의 세포질로의 수출을 방해하여 세포 사멸 및 신경퇴행성 질환(파킨슨증과의 유전적 연관성을 뒷받침함)을 유발합니다(165). 따라서 ATP13A2는 세포 내 PA 항상성을 조절하는 새로운 핵심 요소로 부상하며, 세포질과 리소좀 내 PA 수준을 모두 조절합니다.
따라서 포유류 세포에서 스페르미딘과 스페르민의 다양한 흡수 메커니즘 간의 정확한 상호작용과 각각의 세포 내 PA 수준에 대한 기여도는 아직 명확히 규명되지 않았으며, 이 과정은 조직 및 세포 유형 특이적 요인을 포함할 것으로 예상됩니다
5. UPTAKE, BIOAVAILABILITY, AND TRANSPORT OF DIETARY SPERMIDINE FROM THE GASTROINTESTINAL TRACT
PAs in the gastrointestinal tract originate mainly from food and the intestinal microbiota but also from dying cells and from secretions by the pancreas and gall bladder (100) ( Figure 3 ). Although the exact contribution of the different sources of PAs to the available, gastrointestinal PA pool remains unclear, it has been debated that in humans most PAs in the small intestine are of dietary origin and PA levels in the colon depend more prominently on intestinal microbiota (125). Consequently, PA levels are normally in the low millimolar range (0.5–1 mM) in the intestinal lumen of healthy humans (86) and vary shortly after meals (high PA levels) and upon fasting (low PA levels) (93). The small intestine (particularly the duodenum and proximal jejunum) is the major site of PA absorption (125).
Intestinal epithelial cells are the first barrier between (nutritional) luminal PAs and circulation ( Figure 3 ). Epithelial cells of the intestinal mucosa are also highly proliferative and thus require fair amounts of PAs, which partly result from luminal PA uptake (125). Nevertheless, it is well established that dietary spermidine and other PAs reach the bloodstream and peripheral tissue, with kinetics suggesting rapid uptake and/or elimination from luminal compartments (93, 125, 135). For instance, in rats, 61–76% of labeled PAs administered to the jejunum (performed ex vivo using isolated organ blocks consisting of the small intestine with adjacent blood vessels) were found in the veins after 10 min, suggesting a rapid transition from the intestinal lumen to the bloodstream (157). No significant differences between the uptake of spermidine and that of other PAs were observed (157).
There are two main routes of passage from the intestinal lumen into the bloodstream: (a) uptake in epithelial cells via transporters (as discussed above) in the apical membrane followed by intracellular metabolism or cellular release across the basolateral membrane; and (b) paracellular transport via solute gradients and passive diffusion through the intercellular space between cells, which is likely responsible for most dietary PAs that find their way into the bloodstream (93) ( Figure 3 ). Whereas putrescine seems to be readily metabolized in intestinal epithelial cells, spermidine and spermine appear to be spared from conversion at this site (125).
In blood, spermidine levels tend to be higher than spermine and putrescine levels (137) and are typically in the micromolar range (125). Plasma contains lower PA levels than does whole blood (28). Indeed, most circulating PAs are readily taken up by red blood cells and white blood cells (which exhibit the highest concentrations of PAs). In blood, PAs may be bound by various plasma proteins, mostly by electrostatic interactions (28, 94, 98). However, even in healthy adults, PA levels in blood show a high degree of variability and may be influenced by individual parameters, diseases, and age (22, 144). Thus, several lines of transport distribute dietary or microbially produced PAs to the systemic circulation and then supply peripheral tissues ( Figure 3 ).
5. 식이 스페르미딘의 위장관으로부터의 흡수, 생체 이용률 및 운반
위장관 내 PA는
주로 음식과 장내 미생물에서 유래하지만,
죽은 세포와 췌장 및 담낭의 분비물에서도 발생합니다 (100) ( Figure 3 ).
다양한 PA 원천이 가용성 위장관 PA 풀에 기여하는 정확한 비율은 명확하지 않지만,
인간에서 소장 내 대부분의 PA는 식이 기원이며,
대장 내 PA 수준은 장내 미생물에 더 크게 의존한다는 의견이 제기되었습니다(125).
따라서
건강한 인간의 장 내강에서 PA 수준은
일반적으로 저밀리몰 범위(0.5–1 mM)에 있으며,
식사 후 일시적으로 증가(고 PA 수준)하고 금식 시 감소(저 PA 수준)합니다(93).
소장(특히 십이지장과 근위부 공장)은
PA 흡수 주요 부위입니다(125).
장 상피 세포는
(영양소) 장 내강 PA와 순환계 사이의 첫 번째 장벽입니다( 그림 3 ).
장 점막의 상피 세포는
고도로 증식적이며 따라서 상당량의 PA를 필요로 하며,
이는 부분적으로 장 내강 PA 흡수에서 비롯됩니다(125).
그럼에도 불구하고
식이성 스페르미딘과 다른 PA가 혈류와 주변 조직에 도달한다는 것은 잘 알려져 있으며,
동력학은 장 내강 부위에서의 빠른 흡수 및/또는 배설을 시사합니다(93, 125, 135).
예를 들어, 쥐에서 소장(분리된 장 조직 블록을 사용한 체외 실험)에 투여된 표지된 PA의 61–76%가 10분 후 정맥에서 검출되었으며, 이는 장 내강에서 혈류로의 빠른 전환을 시사합니다(157). 스페르미딘과 다른 PA의 흡수 사이에 유의미한 차이는 관찰되지 않았습니다(157).
장 내강에서 혈류로 이동하는 두 가지 주요 경로는 다음과 같습니다: (a) 상피 세포의 아피칼 막을 통해 운반체에 의해 흡수된 후 세포 내 대사 또는 기저측 막을 통해 세포 외로 방출되는 경로; 및 (b) 세포 간 공간을 통해 용질 농도 차이와 수동 확산에 의해 이루어지는 세포 간 수송 경로로, 이는 혈류로 이동하는 대부분의 식이 PA에 책임이 있을 것으로 추정됩니다(93) ( Figure 3 ). 반면 푸트레신은 장 상피 세포에서 쉽게 대사되지만, 스페르미딘과 스페르민은 이 부위에서 전환되지 않는 것으로 보입니다 (125).
혈액에서는 스페르미딘 농도가 스페르민과 푸트레신보다 높으며 (137), 일반적으로 마이크로몰 범위 내에 있습니다 (125). 혈장에는 전혈보다 PA 농도가 낮습니다 (28). 실제로 순환하는 대부분의 PA는 적혈구와 백혈구(PA 농도가 가장 높은 세포)에 쉽게 흡수됩니다. 혈액에서 PA는 주로 정전기적 상호작용을 통해 다양한 혈장 단백질에 결합됩니다(28, 94, 98). 그러나 건강한 성인에서도 혈중 PA 농도는 높은 변동성을 보이며 개인별 요인, 질환, 연령에 영향을 받을 수 있습니다(22, 144). 따라서, 식이 또는 미생물에서 생성된 PA는 여러 운반 경로를 통해 체내 순환계로 분배된 후 말초 조직에 공급됩니다( Figure 3 ).
6. DISTRIBUTION OF POLYAMINES TO ORGANS AND ITS EFFECTS
Preclinical studies of mice (32, 145) and other model organisms, including S. cerevisiae, worms, and flies (34, 151), show that supplementation with spermidine significantly promotes life span. In mice, this is true for both lifelong feeding (starting at 4 months of age) and late-in-life feeding (starting at 18 months of age) (32).
Upon uptake in the gastrointestinal tract, dietary spermidine becomes available to different organs (11). Accordingly, a PA-enriched diet increases the PA levels in plasma in mice and humans (148). The highest concentrations of PAs in mammalian tissues are found in pancreas (58; F. Madeo, T. Eisenberg, S. Hofer, T. Pendl, M. Poglitsch & C. Magnes, unpublished observations), spleen (F. Madeo, T. Eisenberg, S. Hofer, T. Pendl, M. Poglitsch & C. Magnes, unpublished observations), intestine, thymus, and liver (10, 153), with levels of ∼0.6 mg spermidine/g wet weight tissue in murine pancreas. This value corresponds to a concentration that is three- to sixfold higher than that found in spleen, thymus, liver, and intestine (F. Madeo, T. Eisenberg, S. Hofer, T. Pendl, M. Poglitsch & C. Magnes, unpublished observations). Still, in humans, the impact of dietary and exogenously applied spermidine on specific organs remains largely unexplored, although several reports point toward a systemic and multi-organ effect.
6. 폴리아민의 장기 분포 및 그 효과
쥐(32, 145) 및 S. cerevisiae, 벌레, 파리 등 다른 모델 생물체에 대한 전임상 연구(34, 151)는 스퍼미딘 보충이 수명을 유의미하게 연장함을 보여줍니다. 쥐에서는 평생 급여(4개월령부터 시작)와 노년기 급여(18개월령부터 시작) 모두에서 이 효과가 관찰되었습니다(32).
소화관 흡수 후
식이 스페르미딘은 다양한 장기에 공급됩니다(11).
이에 따라 PA 풍부한 식단은
쥐와 인간에서 혈장 내 PA 농도를 증가시킵니다(148).
포유류 조직에서 PA의 최고 농도는 췌장(58; F. Madeo, T. Eisenberg, S. Hofer, T. Pendl, M. Poglitsch & C. Magnes, 미발표 관찰 결과), 비장(F. Madeo, T. Eisenberg, S. Hofer, T. Pendl, M. Poglitsch & C. Magnes, 미발표 관찰 결과), 장, 흉선, 간(10, 153)에서 발견되며, 쥐의 췌장에서는 조직 습중량 1g당 약 0.6mg의 스페르미딘 농도를 보입니다. 이 값은 비장, 흉선, 간, 장에서 관찰된 농도보다 3~6배 높은 수준입니다(F. Madeo, T. Eisenberg, S. Hofer, T. Pendl, M. Poglitsch & C. Magnes, 미발표 관찰 결과). 그러나 인간에서 식이 및 외부적으로 투여된 스페르미딘이 특정 장기에 미치는 영향은 여전히 대부분 연구되지 않았으며, 몇 가지 보고서는 체계적이고 다기관 효과를 시사합니다.
For instance, increased dietary intake of spermidine has been directly associated with improved cardiovascular health in a prospective, population-based cohort (71). According to preclinical data, cardiovascular improvement by spermidine in rodents might rely on its capability to promote macroautophagy. In mouse cardiomyocytes, spermidine induces mitophagy, a specific form of autophagy that clears dysfunctional mitochondria (32). If damaged, mitochondria can overproduce detrimental reactive oxygen species and ignite cell death pathways, in which case their elimination improves cellular function (33). This is especially important for cells that display a high mitochondrial content due to their relatively high energy demand (like cardiomyocytes). In line with this consideration, intraperitoneally delivered spermidine (and spermine) reversed age-associated alterations in myocardial morphology and inhibited apoptosis in cardiomyocytes (179). This finding was further corroborated by a study showing that spermidine could counteract induced myocardial infarction in a rat model by enhancing autophagic flux (174). Further, administration of spermidine during pregnancy could prevent detrimental effects of hypoxia, such as structural defects in mitochondria, reduced mitochondrial biogenesis, and respiratory dysfunction, on neonatal rats (23), highlighting a potentially protective basis similar to that previously demonstrated for cardiomyocytes (32).
Besides its capacity to induce autophagy within cardiomyocytes, spermidine may improve cardiac function by systemic actions, including dampening chronic inflammation [by diminishing circulating levels of tumor necrosis factor α (TNF-α)] and reducing blood pressure. The latter effect may be explained by enhanced bioavailability of arginine, which increases the levels of the vasodilator nitric oxide (32). Moreover, spermidine may reduce blood pressure through autophagy-mediated improvement of renal function. Indeed, animals supplemented with spermidine exhibited increased renal spermidine content and elevated autophagy levels (179). In Dahl rats, which have impaired renal salt metabolism, treatment with spermidine delayed the appearance of several signs of hypertensive injury to the kidney (32).
예를 들어, 스페르미딘의 식이 섭취량 증가가 전향적 인구 기반 코호트에서 심혈관 건강 개선과 직접적인 관련이 있는 것으로 나타났습니다 (71). 전임상 데이터에 따르면, 설치류에서 스페르미딘에 의한 심혈관 개선은 거대자가포식을 촉진하는 능력에 기인할 수 있습니다. ]
마우스 심근세포에서 스페르미딘은
기능 장애 미토콘드리아를 제거하는 특정 형태의 자가포식인 미토파지를 유도합니다 (32).
손상된 미토콘드리아는 유해한 활성산소종을 과도하게 생성하고 세포 사멸 경로를 활성화할 수 있으며, 이 경우 그 제거는 세포 기능을 개선합니다(33). 이는 상대적으로 높은 에너지 요구량으로 인해 미토콘드리아 함량이 높은 세포(예: 심근 세포)에서 특히 중요합니다. 이 점을 고려할 때, 복강 내 투여된 스페르미딘(및 스페르민)은 심근 세포의 연령 관련 형태학적 변화를 역전시키고 세포 사멸을 억제했습니다(179). 이 결과는 쥐 모델에서 심근경색을 유발한 후 스페르미딘이 자식작용 흐름을 강화하여 이를 역전시킨다는 연구로 추가로 확인되었습니다(174). 또한 임신 중 스페르미딘 투여는 신생아 쥐에서 저산소증의 유해한 영향(미토콘드리아 구조 결함, 미토콘드리아 생합성 감소, 호흡 기능 장애)을 예방했으며, 이는 심근세포에서 이전에 입증된 보호 메커니즘과 유사한 잠재적 보호 기전을 강조합니다(32).
심장근 세포 내에서 자가포식을 유도하는 능력 외에도, 스퍼미딘은 만성 염증을 완화하고 (순환하는 종양 괴사 인자 α (TNF-α)의 수치를 감소시킴으로써) 혈압을 낮추는 등 전신 작용을 통해 심장 기능을 개선할 수 있습니다. 후자의 효과는 혈관 확장제인 산화질소의 수치를 증가시키는 아르기닌의 생체 이용률을 높임으로써 설명될 수 있습니다 (32). 또한, 스퍼미딘은 자가포식을 통한 신장 기능 개선을 통해 혈압을 낮출 수 있습니다. 실제로, 스퍼미딘을 보충한 동물은 신장 스퍼미딘 함량이 증가하고 자가포식 수준이 높아진 것으로 나타났습니다 (179). 신장 염분 대사가 손상된 달 쥐에서 스퍼미딘으로 치료한 결과, 고혈압으로 인한 신장 손상의 여러 징후가 늦게 나타났습니다 (32).
The proautophagic capacity of spermidine suggests it can affect normal brain function and protect against neurodegeneration, which are tightly connected to autophagy (42). Indeed, the first pilot trial of a cohort of individuals with subjective cognitive decline (SCD), which is characterized by self-experienced deterioration in cognitive performance that cannot (yet) be detected objectively by formal neuropsychological examination, suggests that administration of spermidine-rich wheat extract can enhance memory performance (172). This potential for neuroprotection is supported by several preclinical studies (83). For example, in a mouse model of multiple sclerosis, orally administered spermidine abated disease progression (50, 176). Spermidine also reduces frontotemporal lobar dementia in mice expressing transgenic transactive response DNA–binding protein 43 kDa (TDP-43) (169). A recent report shows neuroprotective effects of spermidine against rotenone-induced Parkinson disease (PD) in rats by avoiding the PD-associated loss of dopaminergic neurons in substantia nigra pars compacta and nerve terminals (140). In line with these observations, spermidine feeding protects worms and flies against neurotoxicity exerted by α-synuclein, which is believed to be a crucial toxic trigger of PD (18). Further studies of fly models have shown that administration of spermidine protects against age-induced loss of memory (52) and locomotor activity (95). In these models, induction of autophagy may play a fundamental role, possibly by promoting synaptic flexibility and plasticity (51).
스퍼미딘의 자가포식 촉진 능력은
자가포식과 밀접한 관련이 있는 정상적인 뇌 기능에 영향을 미치고
신경 퇴화를 방지할 수 있음을 시사합니다 (42).
실제로
주관적 인지 저하(SCD)를 가진 개인을 대상으로 한 첫 번째 시범 연구에서,
공식적인 신경심리학적 검사로 아직 객관적으로 검출되지 않는 인지 기능 저하를 경험한 참가자들에게
스퍼미딘이 풍부한 밀 추출물을 투여한 결과 기억력 성능이 향상되었습니다(172).
이 신경 보호 잠재력은 여러 전임상 연구(83)에 의해 뒷받침됩니다.
예를 들어, 다발성 경화증 마우스 모델에서 경구 투여된 스페르미딘은 질병 진행을 억제했습니다(50, 176). 스페르미딘은 또한 트랜스액티브 반응 DNA 결합 단백질 43 kDa(TDP-43)를 발현하는 마우스에서 전두측두엽 치매를 감소시켰습니다(169). 최근 보고서에 따르면, 스페르미딘은 쥐에서 로테논으로 유발된 파킨슨병(PD)에 대한 신경 보호 효과를 보여주며, 흑질 밀집부(substantia nigra pars compacta)와 신경 말단에서의 PD와 관련된 도파민 신경세포 손실을 방지했습니다(140). 이러한 관찰과 일치하게, 스페르미딘 투여는 파킨슨병의 중요한 독성 유발 요인으로 여겨지는 알파-시누클레인에 의한 신경 독성으로부터 벌레와 파리를 보호합니다(18). 파리 모델에 대한 추가 연구에 따르면 스퍼미딘을 투여하면 노화로 인한 기억력 상실 (52) 및 운동 활동 (95)을 예방하는 효과가 있는 것으로 나타났습니다. 이러한 모델에서 자가포식 유도는 시냅스 유연성과 가소성을 촉진함으로써 근본적인 역할을 할 수 있습니다 (51).
Given the neuroprotective effects of spermidine, the extent to which nutritional spermidine is able to cross the blood-brain barrier requires further investigation. In rats, 5 s after an acute intraarterial injection of labeled spermidine, brain uptake index (BUI) values of approximately 5–6% could be determined (note that nonpassable substances could give BUI values of less than 2%, which suggests a low capability of spermidine to pass the blood-brain barrier) (49, 141). Another study using arterial and intravenous injection of tracer spermidine suggests that a specific transport mechanism may enable spermidine to access the brain (30). Still, more work is required to clarify the neuroavailability of dietary spermidine.
Importantly, several preclinical studies of mice support the anticancer activity of spermidine as suggested by the Bruneck and the Salzburg Atherosclerosis Prevention Program in Subjects at High Individual Risk (SAPHIR) studies (71, 72). Besides its role in increased immunosurveillance (118), spermidine production by spermidine synthase is crucial for the antineoplastic activity of tumor-associated macrophages in colorectal cancer (90). Moreover, dietary administration of spermidine to mice attenuates chemically induced liver fibrosis and reduces the incidence of hepatocellular carcinomas (178) and colon tumorigenesis in young animals (147). In the latter study, however, the maximum size of established tumors increased (147). Thus, spermidine might be able to block tumorigenesis but stimulate the growth of existing tumors, which rely on autophagy for further growth and stress resistance. Future studies will need to explore in detail the possible impact of dietary spermidine on the growth of existing tumors.
스퍼미딘의 신경 보호 효과를 고려할 때,
영양 스퍼미딘이 혈액-뇌 장벽을 통과할 수 있는 정도는
추가 연구가 필요합니다.
쥐에서 급성 동맥 내 주사 후 5초 후, 뇌 흡수 지수(BUI) 값이
약 5–6%로 측정되었습니다
(참고:
혈액-뇌 장벽을 통과하지 못하는 물질은 BUI 값이 2% 미만일 수 있으며,
이는 스페르미딘의 혈액-뇌 장벽 통과 능력이 낮음을 시사합니다) (49, 141).
추적자 스페르미딘을 동맥 및 정맥 주사로 사용한 다른 연구는 특정 운반 메커니즘이 스페르미딘이 뇌에 접근할 수 있게 할 수 있음을 시사합니다(30). 그러나 식이 스페르미딘의 신경 가용성을 명확히 하기 위해서는 추가 연구가 필요합니다.
중요하게도, 브루네크 연구와 고위험군 대상 심혈관 질환 예방 프로그램(SAPHIR) 연구(71, 72)에서 제시된 바와 같이, 여러 전임상 연구에서 스페르미딘의 항암 활성이 마우스에서 확인되었습니다. 스페르미딘 합성효소에 의해 생성되는 스페르미딘은 면역 감시 강화(118) 외에도 대장암에서 종양 연관 대식세포의 항종양 활성에 필수적입니다(90). 또한, 쥐에게 식이 스페르미딘을 투여하면 화학적으로 유발된 간 섬유화를 완화하고 간세포 암종 발생률을 감소시키며(178), 젊은 동물에서 대장 종양 발생을 억제합니다(147). 그러나 후자의 연구에서는, 확립된 종양의 최대 크기가 증가했습니다 (147). 따라서, 스퍼미딘은 종양 형성을 차단할 수 있지만, 추가적인 성장과 스트레스 저항을 위해 자가포식에 의존하는 기존 종양의 성장을 촉진할 수도 있습니다. 향후 연구에서는 식이 스퍼미딘이 기존 종양의 성장에 미치는 가능한 영향을 자세히 조사할 필요가 있습니다.
Systemic administration of spermidine has also been linked to improved immune recognition of neoplastic cells in mice (118). Spermidine-induced autophagy in cancer cells promotes the release of ATP, which acts as a chemotactic factor for myeloid cells, thus initiating an anticancer immune response (80, 91). Accordingly, mice treated with spermidine presented an autophagy-dependent and T lymphocyte–dependent inhibition of tumor growth in the context of chemotherapy (118). Other preclinical studies have further evinced the multifaceted effects of spermidine on the immune system. For instance, memory lymphocyte function, which has been shown to decline in humans with ongoing age (117), can be enhanced in mice by spermidine treatment (122). Moreover, spermidine shows strong anti-inflammatory properties in rodents (25, 111), a finding that may be relevant to several pathophysiological scenarios. This is connected to the suppression of several proinflammatory modulators and cytokines, including TNF-α (32, 70), which is slightly but chronically increased in plasma during aging.
Other diseases, such as metabolic syndrome–related pathologies like obesity and type 2 diabetes, may be influenced by PAs. Although this needs further investigation, several preclinical studies suggest application of exogenous spermidine and/or spermine has protective effects. For instance, mice fed a high-fat diet supplemented with spermine showed reduced adiposity and improved glucose tolerance (131). Moreover, weight gain and obesity-related pathologies were reduced in mice fed a hypercaloric diet administered with spermidine (41). Of note, this reduction was correlated with induced autophagy in white adipose tissue (41).
Collectively, these preclinical studies reflect the multipronged activity of spermidine, which in turn explains its protective potential against multiple diseases. In fact, the preclinical evidence has initiated several clinical trials and a prospective epidemiological cohort study (72, 116, 173) that address the possible impact of dietary intake of spermidine on longevity, cardiovascular disease, and age-dependent cognitive decline.
스퍼미딘의 전신 투여는 또한 쥐에서 신생 세포의 면역 인식 개선과 관련이 있는 것으로 밝혀졌습니다 (118).
스퍼미딘에 의해 유도된 암세포의 자가포식은
골수 세포의 화학주성 인자로 작용하는
ATP의 방출을 촉진하여 항암 면역 반응을 시작합니다 (80, 91).
이에 따라,
스퍼미딘으로 치료한 마우스는 화학요법에서
자가포식 및 T 림프구 의존적인 종양 성장 억제를 보였습니다 (118).
다른 전임상 연구에서는
스퍼미딘이 면역 체계에 미치는 다양한 효과가 더욱 명확하게 입증되었습니다.
예를 들어, 인간에서는 나이가 들면서 저하되는 것으로 알려진 기억 림프구 기능 (117)이 스퍼미딘 치료를 통해 마우스에서 향상될 수 있습니다 (122). 또한 스페르미딘은 설치류에서 강력한 항염증 효과를 나타냅니다(25, 111), 이는 여러 병리생리학적 시나리오에 관련될 수 있습니다. 이는 TNF-α(32, 70)를 포함한 여러 염증 조절 인자와 사이토카인의 억제와 연결됩니다. TNF-α는 노화 과정에서 혈장에서 약간이지만 만성적으로 증가합니다.
대사증후군 관련 질환인 비만과 제2형 당뇨병과 같은 다른 질환도 PAs에 의해 영향을 받을 수 있습니다. 이는 추가 연구가 필요하지만, 여러 전임상 연구는 외인성 스퍼미딘 및/또는 스퍼민 투여가 보호 효과를 보일 수 있음을 시사합니다. 예를 들어, 스퍼민을 보충한 고지방 식단을 섭취한 쥐는 지방이 감소하고 포도당 내성이 개선되었습니다 (131). 또한, 스퍼민을 투여한 고칼로리 식단을 섭취한 쥐에서는 체중 증가와 비만 관련 병리가 감소했습니다 (41). 주목할 만한 점은 이러한 감소가 백색 지방 조직에서 유도된 자가포식과 상관관계가 있다는 것입니다 (41).
이러한 전임상 연구들은
스페르미딘의 다각적인 활성을 반영하며,
이는 다시 여러 질환에 대한 보호 잠재력을 설명합니다.
실제로 전임상 증거는
스페르미딘의 식이 섭취가 수명, 심혈관 질환,
연령 관련 인지 기능 저하에 미치는 가능성을 탐구하는
여러 임상 시험과 전향적 역학 코호트 연구(72, 116, 173)를 촉발했습니다.
7. CROSS TALK BETWEEN POLYAMINES AND THE GUT MICROBIOTA
Nutrition and the gut microbiota, which may consist of myriad species (123), are closely intertwined and affect each other in multiple ways. In fact, a series of microorganisms in the intestine are equipped with pathways to fully or partially produce PAs (156). Accordingly, the administration of probiotics (live bacteria) may be another way to increase luminal PA levels (156). In a small-scale study, consumption of yogurt containing the probiotic bifidobacteria strain LKM512 and free arginine (Arg) led to increased levels of putrescine and spermidine in serum (87), suggesting the feasibility of this approach. In rodents, the same procedure extended life span and improved several markers of physiological and cellular senescence, and Arg alone led to increased putrescine levels in the gut and increased spermidine and spermine levels in blood (70).
Overall, although data are still scarce, it appears plausible that a PA-rich diet might influence the gut microbiota. Likewise, intestinal microorganisms may produce PAs from different dietary substrates, modulate nutritional PA content, or both. Thus, future dietary studies of PA intake in humans should closely explore the interplay between these factors, as they may influence each other in ways that are not yet fully understood.
7. 폴리아민과 장 미생물군집 간의 상호작용
영양과 장 미생물군집은 수많은 종으로 구성될 수 있으며(123),
서로 밀접하게 연결되어 다양한 방식으로 상호작용합니다.
실제로 장 내의 일부 미생물은
폴리아민(PA)을 완전히 또는 부분적으로 생성하는 경로를 갖추고 있습니다(156).
따라서
프로바이오틱스(생균)의 투여는
장 내 PA 수준을 증가시키는 또 다른 방법이 될 수 있습니다(156).
소규모 연구에서
프로바이오틱스 bifidobacteria 균주 LKM512와 자유 아르기닌(Arg)을 함유한 요거트를 섭취한 결과,
혈청 내 푸트레신과 스페르미딘 수준이 증가했으며(87),
이 접근법의 가능성을 시사했습니다.
쥐 실험에서 동일한 절차는 수명을 연장하고 생리적 및 세포 노화 지표를 개선했으며,
아르기닌 단독 투여는 장 내 푸트레신 수치를 증가시키고
혈중 스퍼미딘과 스퍼민 수치를 증가시켰습니다(70).
전체적으로,
데이터는 아직 부족하지만,
PA가 풍부한 식단이 장 미생물에 영향을 미칠 수 있다는 것이 가능해 보입니다.
마찬가지로,
장 내 미생물은 다양한 식이 기질로부터 PA를 생성하거나,
영양소 내 PA 함량을 조절하거나,
둘 다를 통해 작용할 수 있습니다.
따라서
인간에서의 PA 섭취를 대상으로 한 향후 식이 연구는
이러한 요인 간의 상호작용을 자세히 탐구해야 하며,
이는 서로에게 영향을 미치는 방식이 아직 완전히 이해되지 않았기 때문입니다.
8. EXCRETORY SYSTEMS
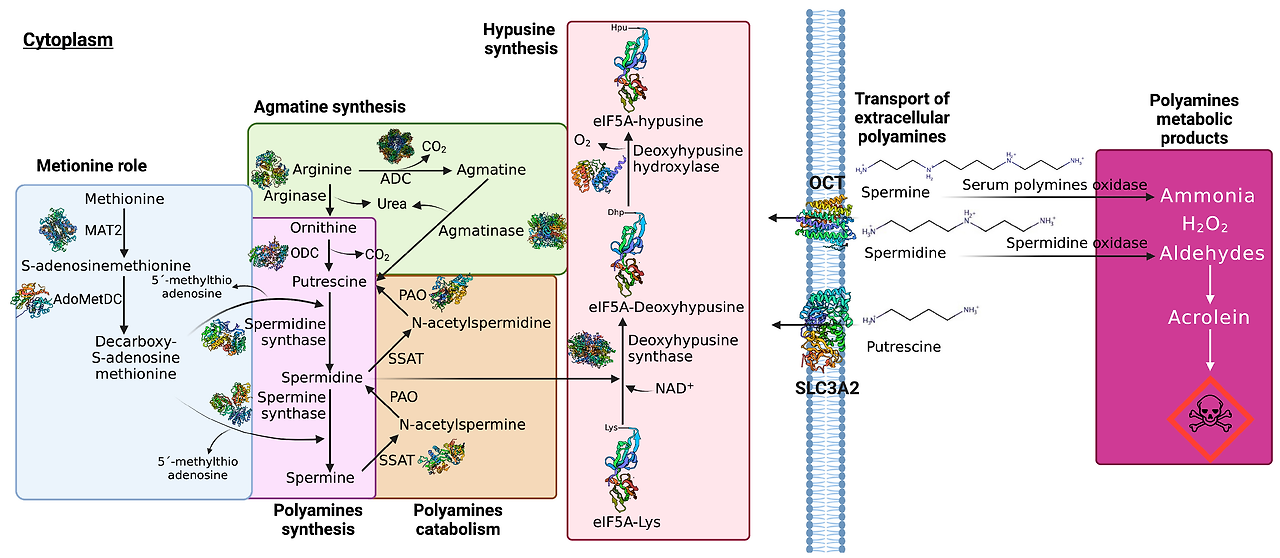
The effective intracellular concentrations of spermidine are dictated both by its (partly reversible) conversion to other PAs and by its secretion from cells. In either case, spermidine acetylation, a process controlled mainly by cytoplasmic spermidine/spermine N 1-acetyltransferase (SSAT), plays a major role ( Figure 4 ).
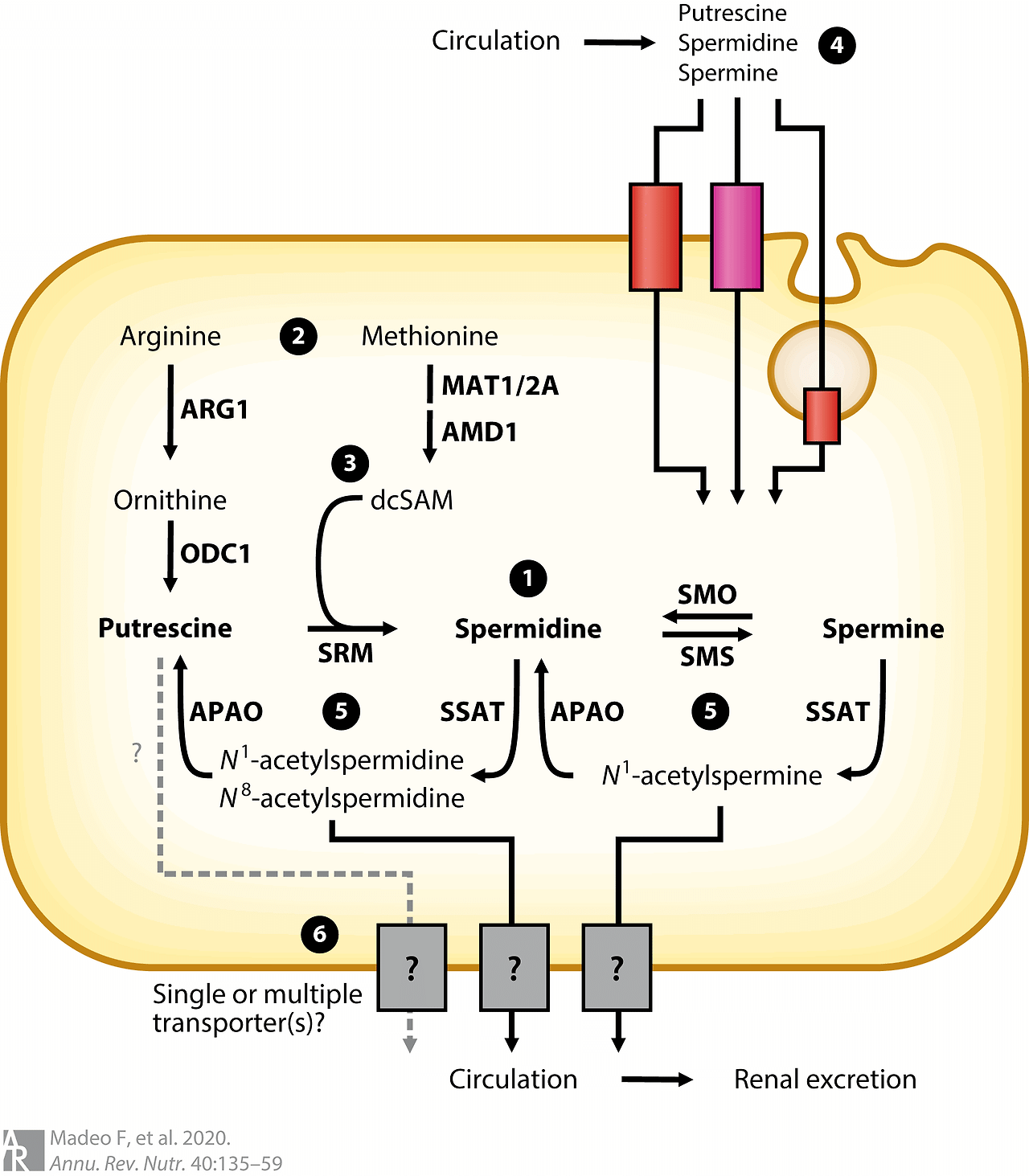
Figure 4 Cellular diamine and polyamine metabolism. (❶) Intracellular de novo synthesis of putrescine, spermidine, and spermine involves the amino acids arginine, ornithine, and methionine. (❷) Arginine is hydrolyzed to ornithine, which is then decarboxylated to putrescine; methionine is metabolized to SAM and subsequently to dcSAM and serves as an aminopropyl group donor to produce spermidine from putrescine. (❸) dcSAM also functions as an aminopropyl group donor to generate spermine from spermidine. (❹) In addition, extracellular putrescine, spermidine, and spermine may enter the cell via specific transporters or by endocytosis. (❺) Interconversion reactions between putrescine, spermidine, and spermine further modulate their intracellular levels. (❻) Cellular secretion is accomplished via acetylated forms of spermidine and spermine. Putrescine has also been suggested to undergo active secretion, although the process of putrescine secretion is not yet understood.
8. 배설 시스템
스퍼미딘의 효과적인 세포 내 농도는 그 자체의 (부분적으로 가역적인) 다른 PA로의 전환과 세포로부터의 분비에 의해 결정됩니다. 어느 경우든 스퍼미딘 아세틸화 과정은 주로 세포질 내 스퍼미딘/스퍼민 N-1-아세틸트랜스퍼레이즈(SSAT)에 의해 조절되며, 이 과정이 주요 역할을 합니다( Figure 4 ).
그림 4 세포 내 다이아민 및 폴리아민 대사.
(❶) 세포 내 신생합성으로 푸트레신, 스페르미딘, 스페르민이 아르기닌, 오르니틴, 메티오닌이라는 아미노산으로부터 생성됩니다.
(❷) 아르기닌은 오르니틴으로 가수분해된 후 오르니틴은 푸트레신으로 탈카복실화됩니다. 메티오닌은 SAM으로 대사된 후 dcSAM으로 전환되어 푸트레신으로부터 스퍼미딘을 생성하는 아미노프로필 그룹 기증체로 작용합니다.
(❸) dcSAM은 또한 스퍼미딘으로부터 스퍼민을 생성하는 아미노프로필 그룹 기증체로 기능합니다.
(❹) 또한, 세포 외부의 푸트레신, 스퍼미딘, 스퍼민은 특정 운반체나 엔도사이토시스(endocytosis)를 통해 세포 내로 들어갈 수 있습니다.
(❺) 푸트레신, 스퍼미딘, 스퍼민 간의 상호 전환 반응은 그들의 세포 내 농도를 추가로 조절합니다.
(❻) 세포 분비는 스퍼미딘과 스퍼민의 아세틸화 형태를 통해 이루어집니다. 푸트레신은 활성 분비 과정을 거친다는 제안이 있지만, 푸트레신의 분비 메커니즘은 아직 명확히 이해되지 않았습니다.
Abbreviations: AMD1, S-adenosyl-l-methionine decarboxylase 1; APAO, acetyl polyamine oxidase; ARG1, arginase 1; dcSAM, decarboxylated S-adenosylmethionine; MAT1/2A, methionine adenosyltransferase 1/2A; ODC1, ornithine decarboxylase 1; SAM, S-adenosylmethionine; SMO, spermine oxidase; SMS, spermine synthase; SRM, spermidine synthase; SSAT, spermidine/spermine N 1-acetyltransferase.
Click to view
SSAT is instrumental in the conversion of spermidine to its upstream precursor, the diamine putrescine, and in the regeneration of spermidine from its downstream product, spermine. On the one hand, SSAT produces N 1-acetylspermidine, which can be converted back to putrescine by acetyl polyamine oxidase (APAO). On the other hand, SSAT acetylates spermine to generate N 1-acetylspermine, which can be a substrate of APAO, thereby regenerating spermidine (reviewed in 100). SSAT can further acetylate N 1-acetylspermine to N 1,N 12-diacetylspermine, which in turn can be processed by APAO to form N 1-acetylspermidine (64, 114). Of note, spermine can be directly reconverted to spermidine by spermine oxidase (170). Besides N 1-acetylspermidine, N 8-acetylspermidine, another acetylated spermidine variant, can be formed via nuclear spermidine N 8-acetyltransferase (37). N 8-acetylspermidine can be hydrolyzed back to spermidine. Although specific cytosolic N 8-acetylspermidine deacetylase activity has been characterized in vivo (84), the actual enzyme remains to be identified. Finally, a diacetylated form of spermidine (N 1 ,N 8-diacetylspermidine) has been identified (57).
These acetylation reactions not only serve intracellular PA interconversions but can also directly and indirectly regulate the actual degradation and secretion of spermidine ( Figure 4 ). For instance, the acetylated products of the SSAT reactions can be directly exported to the extracellular space (92). The characterization of this process (and of mammalian PA transporters in general) remains inconclusive, but there is some evidence that the amino acid transporter SLC3A2 is involved. In particular, SSAT seems to be associated with SLC3A2 in the plasma membrane, which may catalyze the export of acetylated PAs and putrescine through an Arg antiporter mechanism (160).
Thus, increased generation of putrescine via sequential SSAT and APAO reactions on spermidine may indirectly contribute to the export of cellular spermidine. In the same line, conversion of spermidine to putrescine enhances the substrate preference (lowered Michaelis constant) for diamine oxidase, thus allowing effective degradation by this enzyme (36, 96). Importantly, the oxidase reactions catalyzed by APAO and spermine oxidase also generate reactive aldehydes (3-acetoaminopropanal and 3-aminopropanal, respectively) and hydrogen peroxide, which can cause cellular damage. This may be especially relevant for spermine oxidase, which in contrast to APAO does not reside in peroxisomes (112).
The main excretory pathway for spermidine (and PAs in general) is urinary secretion. Acetylputrescine and N 1- and N 8-acetylspermidine together account for more than 90% of the PAs excreted in human urine (69). The levels of diacetylated PA species (N 1,N 12-diacetylspermine and N 1,N 8-diacetylspermidine) are low (0.5% and 1.4%, respectively), but variations between individuals seem to be small and their excretory share is strictly regulated (57). Whereas the intracellular generation of acetylated spermidine and spermine species has been largely characterized (see above), it remains unclear how acetylputrescine is produced before or during renal excretion. Importantly, circulating spermidine and spermine can be oxidized by serum amine oxidase to putrescine and acrolein, a toxic by-product of PA metabolism, respectively. Both putrescine and acrolein levels increase in the plasma of patients with chronic renal failure (60). Therefore, dietary supplementation with spermidine in individuals with renal failure should be scrutinized for potential adverse side effects.
PAs can also be eliminated through fecal excretion. This route is tightly connected to the gut microbiota, which produces a diverse array of metabolites, including spermidine. The levels of PAs in the intestinal tract can originate from dietary intake, but it is thought that the largest contribution comes from synthesis by intestinal microbiota (125). Accordingly, the administration of prebiotics and probiotics may affect PA levels in the intestine, as previously shown in rodents (70, 88, 103). The level of PAs in the intestine is strongly influenced by portal circulation and biliary excretion (109), but elimination by the feces may play a role as well (86).
SSAT는 스퍼미딘을 그 상류 전구체인 다이아민 푸트레신으로 전환하는 데 필수적이며, 스퍼미딘을 그 하류 생성물인 스퍼민으로부터 재생하는 데도 관여합니다. 한 편으로, SSAT는 N 1-아세틸스페르미딘을 생성하며, 이는 아세틸 폴리아민 산화효소(APAO)에 의해 푸트레신으로 다시 전환될 수 있습니다. 다른 한편으로, SSAT는 스퍼민을 아세틸화하여 N 1-아세틸스퍼민을 생성하며, 이는 APAO의 기질로 작용하여 스퍼미딘을 재생성합니다(리뷰 참조: 100). SSAT는 N 1-아세틸스페르민을 N 1,N 12-디아세틸스페르민으로 아세틸화할 수 있으며, 이는 다시 APAO에 의해 N 1-아세틸스페르민으로 처리될 수 있습니다(64, 114). 참고로, 스퍼민은 스퍼민 산화효소(170)에 의해 직접 스퍼민으로 재변환될 수 있습니다. N 1-아세틸스퍼미딘 외에도, 핵 내 스퍼민 N 8-아세틸전달효소(37)를 통해 형성되는 다른 아세틸화 스퍼민 변이체인 N 8-아세틸스퍼미딘이 존재합니다. N 8-아세틸스퍼미딘은 수분해되어 스퍼민으로 돌아갈 수 있습니다. 특정 세포질 N 8-아세틸스페르미딘 탈아세틸화 효소 활성이 체내에서 특성화되었지만(84), 실제 효소는 아직 확인되지 않았습니다. 마지막으로, 스페르미딘의 디아세틸화 형태(N 1 ,N 8-디아세틸스페르미딘)가 확인되었습니다(57).
이 아세틸화 반응은 세포 내 PA 상호 변환을 촉진할 뿐만 아니라 스페르미딘의 실제 분해 및 분비에 직접적 또는 간접적으로 조절할 수 있습니다( 그림 4 ). 예를 들어, SSAT 반응의 아세틸화 제품은 직접 세포 외 공간으로 수출될 수 있습니다(92). 이 과정의 특성화(및 포유류 PA 운반체 전반)는 아직 명확하지 않지만, 아미노산 운반체 SLC3A2가 관여한다는 일부 증거가 있습니다. 특히 SSAT는 세포막에서 SLC3A2와 연관되어 있으며, 아르기닌 안티포터 메커니즘을 통해 아세틸화 PA와 푸트레신(putrescine)의 수출을 촉매할 수 있습니다(160).
따라서, 스페르미딘에 대한 SSAT와 APAO 반응의 연속적인 진행을 통해 푸트레신 생성이 증가하면 세포 내 스페르미딘의 수출에 간접적으로 기여할 수 있습니다. 동일한 맥락에서, 스페르미딘에서 푸트레신으로의 전환은 다이아민 산화효소의 기질 선호도(마이클리스 상수 감소)를 높여 이 효소에 의한 효과적인 분해를 가능하게 합니다(36, 96). 중요하게도, APAO와 스퍼민 산화효소에 의해 촉매되는 산화효소 반응은 반응성 알데히드(각각 3-아세토아미노프로판알과 3-아미노프로판알)와 과산화수소를 생성하며, 이는 세포 손상을 유발할 수 있습니다. 이는 APAO와 달리 과산화체에 존재하지 않는 스퍼민 산화효소에 특히 관련될 수 있습니다(112).
스퍼미딘(및 PA 전반)의 주요 배설 경로는 요로 배설입니다. 아세틸푸트레스신과 N 1- 및 N 8-아세틸스퍼미딘은 인간 소변에 배설되는 PA의 90% 이상을 차지합니다(69). 디아세틸화 PA 종(N 1,N 12-디아세틸스페르민과 N 1,N 8-디아세틸스페르민)의 농도는 낮습니다(각각 0.5%와 1.4%), 하지만 개인 간 변동은 작으며 배설 비율은 엄격히 조절됩니다(57). 세포 내 아세틸화 스페르미딘과 스페르민 종의 생성 메커니즘은 대부분 규명되었지만(위 참조), 아세틸푸트레신(acetylputrescine)이 신장 배설 전 또는 배설 과정에서 어떻게 생성되는지는 아직 명확하지 않습니다. 중요하게도, 순환하는 스페르미딘과 스페르민은 혈청 아민 산화효소에 의해 각각 푸트레신과 아크롤레인으로 산화될 수 있으며, 이는 PA 대사 과정의 독성 부산물입니다. 만성 신부전 환자의 혈장에서는 푸트레신과 아크롤레인 수치가 증가합니다(60). 따라서 신부전 환자에게 스퍼미딘을 식이 보충제로 투여할 경우 잠재적인 부작용을 주의 깊게 모니터링해야 합니다.
PA는 대변 배설을 통해 배출될 수도 있습니다. 이 경로는 장 미생물군과 밀접하게 연결되어 있으며, 장 미생물군은 스페르미딘을 포함한 다양한 대사물을 생성합니다. 장 내 PA 수준은 식이 섭취에서 유래할 수 있지만, 가장 큰 기여는 장 미생물군에 의한 합성에서 비롯된다고 추정됩니다(125). 따라서, 이전에 설치류에서 보여진 바와 같이(70, 88, 103), 프리바이오틱스와 프로바이오틱스의 투여는 장 내 PA 수준에 영향을 미칠 수 있습니다. 장 내 PA 수준은 문맥 순환과 담즙 배설에 의해 강하게 영향을 받지만(109), 대변을 통한 배설도 역할을 할 수 있습니다(86).
9. CLINICAL TRIALS
The prospective Bruneck Study (enrollment of a study population in 1990 as an age- and sex-stratified random sample of all inhabitants of Bruneck, Bolzano Province, Italy) involved a detailed dietary assessment using dietitian-administered, scientifically validated (171) FFQs (2,540 assessments) repeated over 20 years. The analysis involved 829 participants aged 45–84, in which 341 deaths occurred during the follow-up between 1995 and 2015 (71). The analysis of this study revealed a correlation between high dietary intake of spermidine and low mortality from one of three categories of death (vascular deaths, cancer deaths, or deaths from other causes) (71) and from fatal heart failure specifically (32) ( Figure 5 ). This correlation withstood correction for possible confounding factors, including alcohol and aspirin consumption, quality of diet, level of physical activity, and socioeconomic status, among others. Instead, health-related effects of the dietary intake of the spermidine precursors putrescine, Arg, and methionine were not observed, while the spermidine-related and interconvertible PA spermine showed similar, but weaker, associations (71). These epidemiological associations based on the FFQs, in view of the accumulating, broad, and supporting preclinical data, principally substantiate the concept that the PAs spermidine and spermine may promote survival in an evolutionarily conserved manner. The main sources of spermidine intake in the Bruneck Study were whole grains (13.4%), apples and pears (13.3%), green salad (9.8%), vegetable sprouts (7.3%), and potatoes (6.4%) ( Figure 2 ). Importantly, the authors did not find any association between the effect on mortality and the dietary origin of spermidine (71). The analysis revealed a sex- and age-dependent correlation with spermidine intake: Women showed higher intake, and increased age was connected to reduced consumption (71). Taken together, the findings from the Bruneck Study give important insights into the possible impact of dietary PAs on humans, albeit in a locally restricted population. The study showed positive correlations of spermidine/spermine intake levels with diverse health aspects (e.g., reduced risk of cardiovascular disease) and an inverse association with general (including cancer-related) mortality. Although the favorable associations withstood extensive corrections for possible confounding factors, the data from the Bruneck Study have their limitations given their basis in FFQs, and future clinical trials with targeted dietary supplementation with spermidine are required to confirm the causality of spermidine in humans.
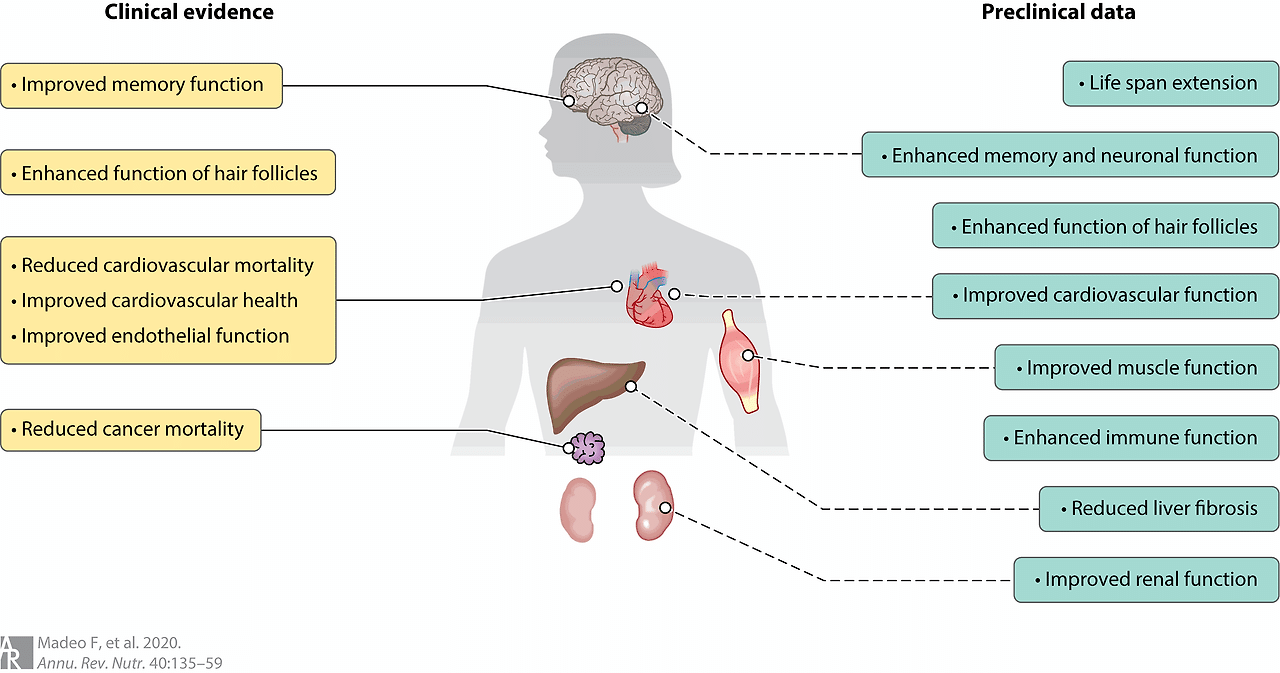
Figure 5 Proposed health benefits of dietary spermidine in humans according to epidemiological and clinical data, highlighting possible future avenues based on preclinical studies. (Left) Health benefits proposed in clinical and epidemiological studies: improved memory function (173), enhanced function of hair follicles (129), reduced cardiovascular mortality (71), improved cardiovascular health (32) and endothelial function (87), and reduced cancer mortality (71). (Right) Diverse beneficial effects of spermidine administration proposed in preclinical, nonhuman studies: extended life span (32, 145, 178), enhanced memory and neuronal function (50–52, 140, 169, 180), enhanced function of hair follicles (126, 128), improved cardiovascular function (23, 32, 76, 174, 179) and muscle function (26, 39, 47), enhanced immune function (122, 176), reduced liver fibrosis (178), and improved renal function (32, 73, 145).
9. 임상 시험
전향적 Bruneck 연구(1990년에 이탈리아 볼차노 주 브루네크의 모든 주민을 연령 및 성별에 따라 무작위로 선정한 연구 대상군 등록)는 영양사 의해 실시된 과학적으로 검증된(171) FFQ(2,540건)를 20년간 반복하여 상세한 식이 평가를 수행했습니다. 분석에는 1995년부터 2015년까지의 추적 기간 동안 341명의 사망이 발생한 45세에서 84세 사이의 829명의 참가자가 포함되었습니다(71). 이 연구의 분석 결과, 스페르미딘의 높은 식이 섭취량과 세 가지 사망 카테고리(혈관성 사망, 암 사망, 기타 원인 사망) 중 하나에서의 낮은 사망률(71) 및 심부전으로 인한 사망률(32) 사이에 상관관계가 발견되었습니다( Figure 5 ). 이 상관관계는 알코올 및 아스피린 섭취, 식이 품질, 신체 활동 수준, 사회경제적 지위 등 잠재적 혼란 요인을 조정해도 유지되었습니다. 반면, 스페르미딘 전구체인 푸트레신, 아르기닌, 메티오닌의 식이 섭취와 관련된 건강 효과는 관찰되지 않았으며, 스페르미딘 관련 및 상호 변환 가능한 폴리페놀 아민(PA)인 스퍼민은 유사하지만 약한 연관성을 보였습니다(71). FFQ를 기반으로 한 이 역학 연관성은 축적된 광범위하고 지원적인 전임상 데이터를 고려할 때, PA인 스페르미딘과 스페르민이 진화적으로 보존된 방식으로 생존을 촉진할 수 있다는 개념을 주로 뒷받침합니다. 브루넥 연구에서 스페르미딘 섭취의 주요 원천은 전체 곡물(13.4%), 사과와 배(13.3%), 녹색 샐러드(9.8%), 채소 싹(7.3%), 감자(6.4%)였습니다( Figure 2 ). 중요하게도, 저자들은 스페르미딘의 식이 기원과의 연관성과 사망률 효과 사이에 어떠한 연관성도 발견하지 못했습니다(71). 분석 결과, 스페르미딘 섭취량은 성별과 연령에 따라 상관관계를 보였습니다: 여성은 섭취량이 높았고, 연령이 증가할수록 섭취량이 감소했습니다(71). 종합적으로, 브루네크 연구의 결과는 식이 PA가 인간에게 미치는 잠재적 영향에 대한 중요한 통찰을 제공하지만, 지역적으로 제한된 인구 집단에서 진행된 연구라는 점을 고려해야 합니다. 이 연구는 스페르미딘/스페르민 섭취 수준과 다양한 건강 측면(예: 심혈관 질환 위험 감소) 간의 긍정적 상관관계 및 일반 사망률(암 관련 사망 포함)과의 역상관 관계를 보여주었습니다. 그러나 이러한 유리한 연관성은 가능한 혼란 요인에 대한 광범위한 조정에도 불구하고 유지되었지만, 브루네크 연구의 데이터는 FFQ에 기반을 두고 있다는 한계가 있으며, 인간에서의 스페르미딘의 인과 관계를 확인하기 위해 표적 식이 보충을 포함한 임상 시험이 필요합니다.
그림 5 역학 및 임상 데이터에 따른 인간에서의 식이 스페르미딘의 건강 혜택 제안, 전임상 연구를 기반으로 한 미래 연구 방향 제시. (왼쪽) 임상 및 역학 연구에서 제안된 건강 혜택: 기억 기능 개선 (173), 모낭 기능 향상 (129), 심혈관 사망률 감소 (71), 심혈관 건강 개선 (32) 및 내피 기능 (87), 암 사망률 감소 (71). (오른쪽) 전임상 및 비인간 연구에서 제안된 스페르미딘 투여의 다양한 유익한 효과: 수명 연장 (32, 145, 178), 기억력과 신경 기능 향상 (50–52, 140, 169, 180), 모낭 기능 향상 (126, 128), 심혈관 기능 개선(23, 32, 76, 174, 179) 및 근육 기능 개선(26, 39, 47), 면역 기능 강화(122, 176), 간 섬유화 감소(178), 신장 기능 개선(32, 73, 145).
Click to view
The Bruneck Study was replicated in the SAPHIR Study, in which a second, independent cohort of 1,770 healthy unrelated participants (663 women and 1,107 men aged 39–67) was examined from 1999 to 2002, with follow-up for deaths until 2013 (71). Compared with that in the Bruneck Study, the contribution of individual foods to spermidine intake in the SAPHIR Study was nearly identical for green salad (10.8%) and potatoes (6.6%) but lower for whole grains (6.5%). The contribution from fruit (24.1%) and vegetables other than green salad (30.5%) was comparably high. Again, women showed a higher intake of spermidine. Most importantly, the SAPHIR Study corroborated the finding from the Bruneck Study that spermidine-rich nutrition is associated with increased survival: Spermidine showed the most prominent inverse correlation with mortality for the 146 macronutrients and micronutrients that were identified in the nutrition of the subjects (71).
This observation aligns with the fact that spermidine (and spermine) levels decrease during aging (102, 116, 134, 168). Long-lived people (nonagenarians and centenarians) maintain whole-blood levels of PAs similar to those of middle-aged individuals (121), corroborating the potential importance of spermidine and spermine for longevity. Accordingly, a PA-rich diet has been connected to a low incidence of cardiovascular disease and a long life span (14, 146). Thus, one may argue that as a person ages, spermidine levels decrease to a detrimental extent and thus need to be replenished through dietary or pharmacological supplementation. In this respect, spermidine might reach vitamin status for aged individuals (81).
Despite the potential of spermidine to protect against cancer as suggested by the Bruneck and the SAPHIR studies, PAs have been connected to procarcinogenic activities. Specifically, an upregulation in biosynthesis and thus in PA levels has been reported for skin, breast, colon, lung, and prostate cancers (107). Increased levels of acetylated PAs in urine or blood have been described as biomarkers for different tumor types (reviewed in 21). One study suggested that increased dietary intake of PAs might exacerbate the risk of developing colorectal adenoma (167), but in a follow-up work, the same authors could not confirm this proposed connection (166).
Nutritional modulation of spermidine levels may be achieved not only by directly ingesting PA-rich foods but also by boosting PA production through dietary regulation of intestinal microbiota. A clinical trial has recently explored this potential (87). A yogurt preparation with Bifidobacterium animalis subsp. lactis (Bifal) and free Arg was administered to 18 subjects (100 g of yogurt once a day, after lunch, for 12 weeks). All subjects were nonsmokers (10 men, 8 women), aged 30–65 years, and had a body mass index less than 30. A corresponding placebo group (n = 16) was used as a control. Arg is a precursor of putrescine, and the microbial hybrid putrescine biosynthesis system, which involves different types of bacteria (among them B. animalis subsp. lactis), can promote intestinal production of putrescine from free Arg (but not from dietary protein-bound Arg) (74). The ingestion of the Bifal-Arg yogurt resulted in positive effects (87). The reactive hyperemia index, a measure of endothelial responsiveness, was increased, suggesting reduced risk of cardiovascular conditions. The Bifal-Arg group exhibited diminished systolic and diastolic blood pressure and enhanced high-density lipoprotein–cholesterol levels in serum, which are correlated with a reduced risk for cardiovascular disease (124) ( Figure 5 ). Moreover, the Bifal-Arg group exhibited reduced platelet and serum triglyceride concentrations, two factors connected to atherosclerosis (104, 154). Finally, the Bifal-Arg group showed increased putrescine levels in feces (in accord with the fact that Arg is a precursor of putrescine) and elevated concentrations of spermidine in serum (with no changes in the fecal concentration). No alterations in fecal or serum spermine levels were detected. The authors suggest that treatment with Bifal-Arg induces microbial production of putrescine, which after intestinal absorption is used to biosynthesize spermidine to exert protective effects on endothelial function (87).
An alternative strategy for increasing spermidine intake consists of direct supplementation with enriched foods or food extracts. A recent report (172) used spermidine-rich wheat germ extract, which had been previously validated for safety and tolerability in older adults (135). The study was designed as a pilot trial (3 months) and tested the memory performance of a cohort of individuals (n = 30, aged 60–80) with SCD. Therefore, these subjects represent a high-risk group that may benefit from early spermidine-based intervention. Specifically, the authors evaluated mnemonic discrimination, the ability to differentiate among highly similar remembrances, as well as memory and executive functions. Application of spermidine-rich extract enhanced both memory performance and mnemonic discrimination (172) ( Figure 5 ). Currently, a second trial (12 months, n = 100) is ongoing: The recruitment finished in March 2019 and the last follow-up check is planned for September 2020 (173). This study will extend the previous pilot trial and assess memory performance, as well as changes in neurocognitive, behavioral, and physiological parameters, in subjects with SCD. A recent study demonstrated that higher levels of spermidine in serum weakly, but significantly, correlate with improved cognitive performance of elderly people taking the Mini-Mental State Exam (116).
Another interesting benefit for dietary supplementation with spermidine is its impact on hair growth and hair follicles (127). Supported by several preclinical in vivo and in vitro studies (40, 126–128), a recent clinical study examined the effects of a spermidine-based nutritional supplement (which was not further defined) on hair follicles in healthy humans. After three months, the supplement-treated group showed a prolonged anagen phase (active growth phase of hair follicles) compared with the placebo group (129).
Future clinical trials will further elucidate how dietary modulation of spermidine influences human health. Therefore, it will be important to include laboratory assessments that analyze the causal relationship between protective effects and pathways ignited by spermidine, including autophagy.
브루네크 연구는 SAPHIR 연구에서 재현되었으며, 이 연구에서는 1999년부터 2002년까지 39세에서 67세 사이의 건강한 관련 없는 참가자 1,770명(여성 663명, 남성 1,107명)을 대상으로 조사했으며, 사망 추적 조사는 2013년까지 진행되었습니다(71). 브루네크 연구와 비교했을 때, SAPHIR 연구에서 개별 식품의 스페르미딘 섭취 기여도는 녹색 샐러드(10.8%)와 감자(6.6%)는 거의 동일했지만, 전체 곡물(6.5%)은 더 낮았습니다. 과일(24.1%)과 녹색 샐러드 외의 채소(30.5%)의 기여도는 유사하게 높았습니다. 다시 한 번 여성은 스페르미딘 섭취량이 더 높았습니다. 가장 중요한 점은 SAPHIR 연구가 Bruneck 연구의 결과를 확인했다는 점입니다. 즉, 스페르미딘이 풍부한 영양 섭취는 생존율 증가와 연관되어 있습니다: 스페르미딘은 대상자의 영양 성분에서 식별된 146개의 매크로영양소와 미세영양소 중 사망률과 가장 강한 역상관 관계를 보였습니다 (71).
이 관찰 결과는 스페르미딘(및 스페르민) 수치가 노화 과정에서 감소한다는 사실과 일치합니다(102, 116, 134, 168). 장수자(90세 이상 및 100세 이상)는 중년층과 유사한 전혈 PA 수치를 유지합니다(121), 이는 스페르미딘과 스페르민의 장수 잠재적 중요성을 뒷받침합니다. 따라서 PA가 풍부한 식단은 심혈관 질환 발생률 감소와 장수와의 연관성이 보고되었습니다(14, 146). 따라서 노화 과정에서 스페르미딘 수치가 유해한 수준으로 감소하므로 식이 또는 약물 보충을 통해 보충이 필요할 수 있습니다. 이 점에서 스페르미딘은 노년층에서 비타민 지위를 얻을 수 있을 것입니다(81).
브루네크와 SAPHIR 연구에서 암 예방 잠재성이 제시되었음에도 불구하고, PAs는 발암 촉진 활동과 연관되어 있습니다. 구체적으로, 피부, 유방, 대장, 폐, 전립선 암에서 생합성 증가 및 PA 수준 상승이 보고되었습니다(107). 소변이나 혈액에서의 아세틸화 PA 수준 증가가 다양한 종양 유형의 바이오마커로 묘사되었습니다(21에서 검토됨). 한 연구에서는 PA 섭취 증가가 대장 선종 발병 위험을 증가시킬 수 있다고 제안했지만(167), 후속 연구에서 동일한 저자들은 이 연관성을 확인하지 못했습니다(166).
스페르미딘 수치를 조절하는 영양학적 방법은 PA가 풍부한 식품을 직접 섭취하는 것뿐 아니라 장내 미생물군집을 조절하여 PA 생성을 촉진하는 식이 조절을 통해 달성될 수 있습니다. 최근 임상 시험에서 이 가능성을 탐구했습니다(87). Bifidobacterium animalis subsp. lactis (Bifal)와 자유 아르기닌을 함유한 요거트 제제를 18명(100g의 요거트를 하루에 한 번 점심 후, 12주간)에게 투여했습니다. 모든 참가자는 비흡연자(남성 10명, 여성 8명)로, 연령은 30–65세이며 체질량 지수(BMI)가 30 미만이었습니다. 대조군으로 동일한 조건의 위약군(n = 16)이 사용되었습니다. 아르기닌은 푸트레신(putrescine)의 전구체이며, 다양한 세균(그 중 B. animalis subsp. lactis 포함)이 관여하는 미생물 하이브리드 푸트레신 생합성 시스템은 자유 아르기닌으로부터 장 내 푸트레신 생성을 촉진하지만(식이 단백질 결합 아르기닌からは 아니며)(74). Bifal-Arg 요거트의 섭취는 긍정적인 효과를 나타냈습니다(87). 내피 반응성을 측정하는 반응성 혈관 확장 지수가 증가했으며, 이는 심혈관 질환 위험 감소와 연관되었습니다. Bifal-Arg 그룹은 수축기 및 이완기 혈압이 감소하고 혈청 고밀도 지단백 콜레스테롤 수치가 증가했으며, 이는 심혈관 질환 위험 감소와 관련이 있습니다(124) ( Figure 5 ). 또한 Bifal-Arg 그룹은 동맥경화증과 관련된 두 가지 요인인 혈소판 및 혈청 트리글리세라이드 농도가 감소했습니다 (104, 154). 마지막으로 Bifal-Arg 그룹은 분변 내 푸트레신 수치가 증가했으며 (아르기닌이 푸트레신의 전구체이기 때문) 혈청 내 스퍼미딘 농도가 증가했으나 (분변 농도는 변화 없음) 분변 또는 혈청 내 스퍼민 수치는 변화가 없었습니다. 저자들은 Bifal-Arg 치료가 미생물による 푸트레신 생성을 유도하며, 이 푸트레신이 장 흡수 후 스퍼미딘 생합성에 사용되어 내피 기능 보호 효과를 발휘한다고 제안합니다(87).
스페르미딘 섭취를 증가시키는 대안 전략은 강화 식품이나 식품 추출물을 직접 보충하는 것입니다. 최근 보고서(172)에서는 안전성과 내약성이 노인에서 검증된 스페르미딘 풍부한 밀 배아 추출물을 사용했습니다(135). 이 연구는 3개월간의 시범 연구로 설계되었으며, SCD를 가진 개인(n = 30, 60–80세)의 기억 성능을 평가했습니다. 따라서 이 대상군은 조기 스페르미딘 기반 개입으로부터 혜택을 받을 수 있는 고위험군을 대표합니다. 구체적으로 저자들은 기억력 차별화(고도로 유사한 기억을 구분하는 능력) 및 기억력과 실행 기능을 평가했습니다. 스페르미딘 풍부 추출물의 적용은 기억력 성능과 기억력 차별화를 모두 향상시켰습니다(172) ( Figure 5 ). 현재 두 번째 임상 시험(12개월, n = 100)이 진행 중입니다: 모집은 2019년 3월에 완료되었으며, 마지막 추적 검사는 2020년 9월에 예정되어 있습니다(173). 이 연구는 이전 시범 연구를 확장하여 SCD를 가진 대상자의 기억력 성능 및 신경인지, 행동, 생리학적 매개변수의 변화를 평가할 것입니다. 최근 연구에서 혈청 내 스페르미딘 수치가 높을수록 노인 대상 미니 정신 상태 검사(Mini-Mental State Exam)의 인지 기능이 약하지만 유의미하게 개선되는 것으로 나타났습니다(116).
스페르미딘을 포함한 식이 보충제의 또 다른 흥미로운 효과는 모발 성장과 모낭에 미치는 영향입니다(127). 여러 전임상 in vivo 및 in vitro 연구(40, 126–128)를 바탕으로 최근 임상 연구는 건강한 인간에서 스페르미딘 기반 영양 보충제(구체적으로 정의되지 않음)가 모낭에 미치는 영향을 조사했습니다. 3개월 후, 보충제 투여 그룹은 위약 그룹에 비해 모낭의 활성 성장 단계인 안상기(anagen phase)가 연장되었습니다(129).
향후 임상 시험을 통해 스페르미딘의 식이 조절이 인체 건강에 미치는 영향이 더욱 명확해질 것입니다. 따라서, 자가포식 등 스페르미딘에 의해 촉발되는 보호 효과와 그 경로의 인과 관계를 분석하는 실험실 평가도 포함하는 것이 중요할 것입니다.
10. FUTURE DIRECTIONS AND CONCLUSION
In this review, we summarize the field of dietary PAs, especially spermidine, in human nutrition and health. Accumulating data from numerous preclinical studies, as well as a growing number of clinical studies, substantiate the hypothesis that PAs are important determinants of healthy human nutrition. Overall, spermidine, among other diamines and polyamines, plays crucial roles in diverse physiological and disease-related scenarios. However, we do not yet fully understand the mechanistic relationship between spermidine, health, and disease. This is also outlined by the observation that increased levels of spermidine occur in disease-specific contexts (24, 110, 133), whereas preclinical data suggest potent protective effects of spermidine in such pathologies. Whether altered levels of spermidine in disease contexts indicate a homeostatic cellular stress response or reflect metabolic alterations causally linked to disease progression remains to be solved.
While the cornerstones of the complex interplay between dietary PAs and health are gradually outlined by ongoing preclinical and clinical studies, it will be crucial to explore in more detail PA stability during food cultivation, processing, and storage. Ultimately, refining nutritional databases to estimate PAs and examining the exact PA contents in standardized meals prepared for trial purposes will help define the role of food-derived PAs in human health. In fact, a deeper understanding of dietary PAs will help shape future standards of a healthy diet and guide the development of dietary plans that favor life span and health span.
10. 향후 방향 및 결론
이 리뷰에서는 인체 영양 및 건강에 대한 식이 PA, 특히 스페르미딘에 대해 요약했습니다. 수많은 전임상 연구와 점차 증가하는 임상 연구의 데이터는 PA가 건강한 인간 영양의 중요한 결정 요인이라는 가설을 뒷받침합니다. 전반적으로 스페르미딘은 다른 다이아민과 폴리아민과 함께 다양한 생리적 및 질병 관련 상황에서 중요한 역할을 합니다. 그러나 스페르미딘, 건강, 질병 간의 메커니즘적 관계는 아직 완전히 이해되지 않았습니다. 이것은 질병 특이적 맥락에서 스페르미딘 수치가 증가한다는 관찰(24, 110, 133)과 전임상 데이터가 이러한 병리학적 상태에서 스페르미딘의 강력한 보호 효과를 시사한다는 점에서 명확히 드러납니다. 질병 맥락에서 스페르미딘 수치의 변화가 세포 내 항상성 스트레스 반응을 나타내는지, 아니면 질병 진행과 인과적으로 연관된 대사 변화의 반영인지 여부는 여전히 해결되어야 할 과제입니다.
식이 PA와 건강 사이의 복잡한 상호작용의 기반은 진행 중인 전임상 및 임상 연구를 통해 점차 명확해지고 있지만, 식품 재배, 가공, 보관 과정에서 PA의 안정성을 더 자세히 탐구하는 것이 중요할 것입니다. 최종적으로, PA를 추정하기 위한 영양 데이터베이스를 정교화하고 시험 목적으로 준비된 표준화된 식사에서 정확한 PA 함량을 분석하는 것은 식품 유래 PA의 인간 건강에 대한 역할을 정의하는 데 도움이 될 것입니다. 실제로, 식이 PA에 대한 깊은 이해는 건강한 식단의 미래 기준을 형성하고 수명과 건강 수명을 촉진하는 식이 계획 개발을 안내하는 데 기여할 것입니다.
disclosure statement
D.C.-G., G.K., and F.M. are the scientific cofounders of Samsara Therapeutics, a company that develops novel pharmacological autophagy inducers. T.P. has equity interests in Samsara Therapeutics. F.M. and D.C.-G. have equity interests in The Longevity Labs (TLL), a company founded in 2016 that develops natural food extracts. T.E. has equity interests in and conducts paid consultancies for TLL. G.K. holds research contracts with Bayer Healthcare, Genentech, GlaxoSmithKline, Institut Mérieux, Kaleido Biosciences, Lytix Biopharma, NuCana, Oncolinx, PharmaMar, Samsara Therapeutics, SOTIO, and Tioma Therapeutics. G.K. is on the Board of Directors of the Bristol Myers Squibb Foundation France. G.K. is a scientific cofounder of everImmune, a biotech company that develops immunostimulatory bacteria, and Therafast Bio.
acknowledgments
We thank Thomas Kuenzer for technical assistance with compiling Figure 2 and Stefan Kiechl, as well as Raimund Pechlaner, for critical discussions about and assistance with developing Figure 2 . F.M. is grateful to the Austrian Science Fund FWF (SFB-LIPOTOX F3007 & F3012, W1226, P29203, P29262, P27893, and P31727); the Austrian Federal Ministry of Education, Science and Research; and the University of Graz for grants Unkonventionelle Forschung-InterFast and flysleep (BMWFW-80.109/0001-WF/V/3b/2015) and the field of excellence program BioHealth. We acknowledge support from NAWI Graz, the BioTechMed-Graz flagship project EPIAge, and the field of excellence program BioHealth. G.K. is supported by the Ligue Contre le Cancer Comité de Charente-Maritime (Equipe Labellisée); the Agence National de la Recherche (ANR)–Projets blancs; the ANR under the frame of E-Rare-2, the ERA-Net for Research on Rare Diseases; the Association pour la Recherche sur le Cancer (ARC); the Cancéropôle Île-de-France; the Institut National du Cancer (INCa); the Institut Universitaire de France; the Fondation pour la Recherche Médicale (FRM); the European Commission (ArtForce); the European Research Council (ERC); the Leducq Foundation; the LabEx Immuno-Oncology; the Recherche Hospitalo-Universitaire Torino Lumière; the Site de Recherche Intégrée e sur le Cancer (SIRIC) Stratified Oncology Cell DNA Repair and Tumor Immune Elimination (SOCRATE); the SIRIC Cancer Research and Personalized Medicine (CARPEM); and the Paris Alliance of Cancer Research Institutes (PACRI).
literature cited