
Front Immunol
. 2023 Jul 14;14:950465. doi: 10.3389/fimmu.2023.950465
Immunomodulatory actions of vitamin D in various immune-related disorders: a comprehensive review
Amirhossein Ghaseminejad-Raeini 1, Ali Ghaderi 1, Amirmohammad Sharafi 1, Behrad Nematollahi-Sani 1, Maryam Moossavi 2, Afshin Derakhshani 3, Gholamreza Anani Sarab 4,*
- Author information
- Article notes
- Copyright and License information
PMCID: PMC10379649 PMID: 37520529
Abstract
For many years, vitamin D has been acknowledged for its role in maintaining calcium and phosphate balance. However, in recent years, research has assessed its immunomodulatory role and come up with conflicting conclusions. Because the vitamin D receptor is expressed in a variety of immune cell types, study into the precise role of this molecule in diseases, notably autoimmune disorders, has been made possible. The physiologically activated version of vitamin D also promotes a tolerogenic immunological condition in addition to modulating innate and acquired immune cell responses. According to a number of recent studies, this important micronutrient plays a complex role in numerous biochemical pathways in the immune system and disorders that are associated with them. Research in this field is still relatively new, and some studies claim that patients with severe autoimmune illnesses frequently have vitamin D deficiencies or insufficiencies. This review seeks to clarify the most recent research on vitamin D’s immune system-related roles, including the pathophysiology of major disorders.
초록
오랜 세월 동안 비타민 D는
칼슘과 인의 균형을 유지하는 역할로 알려져 왔습니다.
그러나 최근 몇 년간 연구에서는
비타민 D의 면역 조절 역할을 평가하여 상반된 결론을 도출해냈다.
비타민 D 수용체가 다양한 면역 세포 유형에서 발현되기 때문에,
특히 자가면역 질환을 비롯한 질병에서
이 분자의 정확한 역할을 연구할 수 있게 되었다.
생리적으로 활성화된 형태의 비타민 D는
선천적 및 후천적 면역 세포 반응을 조절할 뿐만 아니라
관용성 면역 상태를 촉진한다.
최근 여러 연구에 따르면,
이 중요한 미량영양소는
면역 체계 및 관련 질환의 수많은 생화학적 경로에서 복합적인 역할을 수행한다.
이 분야의 연구는
아직 비교적 초기 단계이며,
일부 연구는 중증 자가면역 질환 환자들이 비타민 D 결핍 또는 부족 상태를
자주 보인다고 주장한다.
본 리뷰는 주요 질환의 병리생리학을 포함하여
비타민 D의 면역 체계 관련 역할에 대한
최신 연구를 명확히 하는 것을 목표로 한다.
Keywords: Vitamin D, autoimmunity, innate immunity, acquired immunity, autoimmune disorders
Introduction
Vitamin D is an attractive molecule that has received particular attention recently. It is a major calcium homeostasis and bone metabolism modulator, increasing phosphorus and calcium absorption from the intestine, decreasing their excretion from the kidney, and promoting osteogenesis (1). It is also one of the crucial immune system regulator hormones that affect immune responses. Vitamin D acts as a pro-survival molecule. This vitamin defends cells against damaging signals by inhibiting inflammatory responses, such as changing the pathways through which T-helper-2 (Th2), M2 macrophages, and regulatory T cells (Treg) differentiate in order to maintain energy and redox homeodynamics by supplying a tolerogenic state (2). Vitamin D insufficiency continues to be one of the most common causes of osteoporosis, muscle weakness, falling fractures (particularly in the elderly), numerous malignancies, metabolic syndrome, cardiovascular illnesses, immune-mediated diseases (including autoimmune diseases), and infections (3–8). Ultraviolet (UV) rays that reach the epidermal layer of the skin and regular diet are the two main sources of vitamin D. That suggests that it should not be viewed solely as a vitamin: pro-hormone is the proper category (9). The normal range for vitamin D is still disputed among different nations. However, it is generally acknowledged that an adult can deal with a lower limit of 50–75 nmol/L. Numerous problems, including impaired bone metabolism, falling risk, various myopathies, and immune system dysregulation, are linked to low vitamin D levels (9–12).
서론
비타민 D는
최근 특별한 관심을 받고 있는 매력적인 분자입니다.
이는 주요 칼슘 항상성 및 골 대사 조절제로서,
장에서의 인과 칼슘 흡수를 증가시키고
신장에서의 배설을 감소시키며 골형성을 촉진합니다(1).
또한 면역 반응에 영향을 미치는
중요한 면역 체계 조절 호르몬 중 하나입니다.
비타민 D는
세포 생존 촉진 분자로 작용한다.
이 비타민은
T-헬퍼-2(Th2), M2 대식세포, 조절 T 세포(Treg)의 분화 경로를 변화시켜
에너지 및 산화환원 평형 상태를 유지하고
내성 상태를 제공함으로써 염증 반응을 억제하여
세포를 손상 신호로부터 보호한다(2).
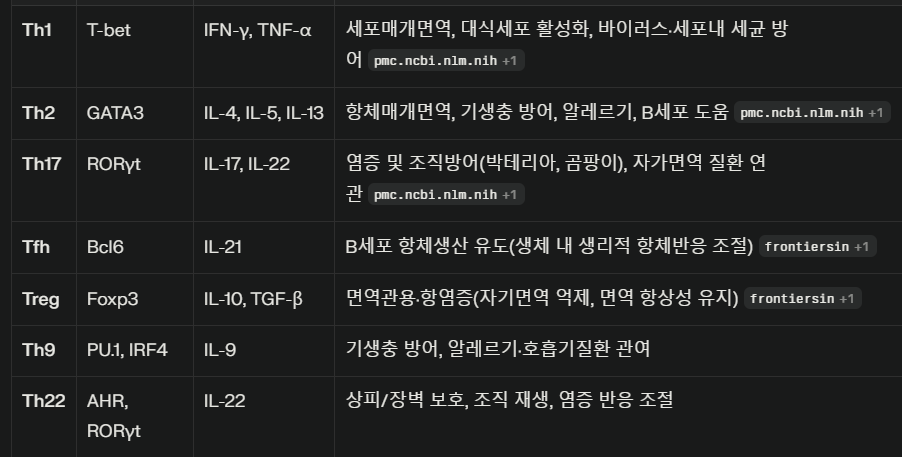
Th1: 세포내 미생물 방어, IFN-γ 생산, 대식세포 활성
Th2: 기생충·알레르기, IL-4/5/13, B세포 도움
Th17: 외부세균·곰팡이, IL-17/22, 자가면역 질환
Tfh: B세포 항체발생 조력, IL-21
Treg: 면역 억제·조절, IL-10, TGF-β
Th9/Th22: 특정 조직·염증, 최근 중요성 부각

비타민 D 결핍은
골다공증, 근력 약화, 낙상 골절(특히 노인층),
다양한 악성 종양,
대사 증후군,
심혈관 질환,
면역 매개 질환(자가면역 질환 포함),
감염증의 가장 흔한 원인 중 하나로 남아 있습니다(3–8).
피부 표피층에 도달하는 자외선(UV)과 규칙적인 식단이 비타민 D의 두 가지 주요 공급원이다. 이는 비타민 D를 단순한 비타민으로만 간주해서는 안 된다는 점을 시사한다: 프로호르몬이 적절한 분류이다(9). 비타민 D의 정상 범위는 여전히 국가별로 논란이 있다. 그러나 일반적으로 성인의 경우 50–75 nmol/L의 하한선을 유지할 수 있다는 점은 널리 인정됩니다. 낮은 비타민 D 수치는 골대사 장애, 낙상 위험 증가, 다양한 근육병증, 면역 체계 조절 장애 등 다양한 문제와 연관됩니다(9–12).
The amount of vitamin D the body receives from food sources is typically insufficient, and these abundant sources are also scarce. These are the main factors that contribute to vitamin D deficiency (13). Vitamin D is present in small amounts in butter, peanuts, and eggs, but is present in large quantities in some foods like fish liver oil. Additionally, both cow milk and breast milk are deficient in vitamin D (1, 14). Despite the fact that vitamin D can be gained through diet, the skin is still the primary source of this pro-hormone. Seven-dehydrogenated cholesterol undergoes spontaneous transformation into vitamin D3 under the influence of UV radiation (13). The primary molecule that carries vitamin D and its subsequent metabolites in the blood is vitamin D binding protein (DBP). This vitamin needs to be hydroxylated twice in order to be physiologically active (14). The expression of the enzyme 1-hydroxylase, which converts 25-hydroxyvitamin D3 (25-OH D3) (precursor) to 1,25-(OH)2 D3 enabling immune microenvironments to respond to this substance in antigen-presenting cells, is one of the factors contributing to the recent interest in the immune-related function of vitamin D (13). It is initially hydroxylated by hydroxylase and several cytochrome P450 isoforms on the 25th carbon. Vitamin D status is mostly tracked by measuring 25-OH D3, which has a 2-week half-life and is the primary form of the vitamin in circulation.
As a result of the CYP27B1 gene expression, 1-alpha-hydroxylase carries out the second stage of hydroxylation in the kidney, skin, and immune cells, resulting in the production of 1,25-(OH)2 D3 or calcitriol (15, 16). The binding of vitamin D to its nuclear receptors, known as vitamin D receptors or VDRs, inside target cells controls gene expression. VDR is also found in non-classical tissues like the brain, eye, heart, pancreatic islet beta cells, and immune cells. The principal mechanism of action of vitamin D in those tissues is metabolism (17). The identification of VDR in immune cells is related to the putative function of vitamin D in controlling immunological responses, cell proliferation, differentiation, and apoptosis induction. B cells, TCD4, TCD8-activated cells, neutrophils, monocytes, macrophages, NK cells, and dendritic cells all contain this receptor (18, 19). It modifies the genes of chromatin-modifying enzymes through direct and indirect interactions (20).
The VDR gene, which has 10 introns and 11 exons, is located on chromosome 12. It contains more than 900 SNPs, according to the literature. The DNA binding domain is encoded by exons 2 and 3, where the majority of these polymorphisms accumulate. Exon changes result in alterations to this domain and impact the structure of the receptor, which precludes vitamin D binding (21). Vitamin D receptors molecular signaling is somehow complex. The VDR binds to retinoid X receptors to form a complex, which is what makes up the traditional route. By attaching to the VDR-RXR, vitamin D controls the expression of many genes. VDR could, however, manifest as an intra-membranous receptor. These are the main substances that initiate the alternate routes that activate the cytochromes. Secosteroids are among the chemicals that are produced by the downstream enzymes. The metabolites modulate the function of some transcription factors and alter gene expression (22, 23).
식품을 통해 체내로 흡수되는 비타민 D 양은
일반적으로 부족하며, 풍부한 공급원 역시 드뭅니다.
이러한 요인들이
비타민 D 결핍의 주요 원인이다(13).
버터, 땅콩, 달걀에는 소량의 비타민 D가 포함되어 있으나,
생선 간유 같은 일부 식품에는 다량 함유되어 있다.
또한 우유와 모유
식이 섭취를 통해 비타민 D를 얻을 수 있음에도 불구하고,
피부는 여전히 이 프로호르몬의 주요 공급원이다.
7-탈수소콜레스테롤은 자외선(UV)의 영향으로
비타민 D3로 자연적으로 변환됩니다(13).
혈액 내에서 비타민 D와 그 후속 대사물을 운반하는 주요 분자는
비타민 D 결합 단백질(DBP)입니다.
이 비타민은 생리적으로 활성 상태가 되기 위해
두 번의 하이드록실화 과정을 거쳐야 합니다(14).
25-하이드록시비타민 D3(25-OH D3)(전구체)를
1,25-(OH)2 D3로 전환시켜 항원제시세포 내 면역 미세환경이 이 물질에 반응할 수 있게 하는
효소 1-하이드록실라제의 발현은
최근 비타민 D의 면역 관련 기능에 대한 관심 증가를 이끈 요인 중 하나이다(13).
비타민 D는
25번 탄소에 위치한 하이드록실라제와 여러 시토크롬 P450 이소형에 의해
초기 하이드록실화됩니다.
비타민 D 상태는
주로 2주 반감기를 가지며
순환계에서 주요 형태인 25-OH D3 측정을 통해 추적됩니다.
CYP27B1 유전자 발현의 결과로,
1-알파-하이드록실라아제는
신장, 피부 및 면역 세포에서
두 번째 단계의 하이드록실화를 수행하여
1,25-(OH)2 D3 또는 칼시트리올(15, 16)을 생성합니다.
비타민 D가
표적 세포 내부의 비타민 D 수용체(VDR)로 알려진
핵 수용체에 결합함으로써 유전자 발현을 조절합니다.
VDR은
뇌, 눈, 심장, 췌도 베타 세포, 면역 세포와 같은
비전형적 조직에서도 발견됩니다.
해당 조직에서
비타민 D의 주요 작용 기전은 대사입니다(17).
면역 세포에서 VDR의 확인은
비타민 D가
면역 반응 조절, 세포 증식, 분화, 세포 사멸 유도에서 가지는
추정 기능과 관련이 있습니다.
B 세포, CD4 양성 T 세포, CD8 양성 T 세포 활성화 세포,
호중구, 단핵구, 대식세포, 자연살해세포(NK 세포),
수지상 세포 모두 이 수용체를 포함합니다(18, 19).
이는
직접적 및 간접적 상호작용을 통해
염색질 변형 효소의 유전자를 조절합니다(20).
10개의 인트론과 11개의 엑손을 가진 VDR 유전자는 12번 염색체에 위치한다. 문헌에 따르면 900개 이상의 단일염기다형성(SNP)을 포함한다. DNA 결합 도메인은 엑손 2와 3에 의해 암호화되며, 이러한 다형성의 대부분이 이 영역에 집중된다. 엑손 변이는 이 도메인의 구조적 변화를 초래하여 수용체 구조에 영향을 미치며, 이는 비타민 D 결합을 방해한다(21).
비타민 D 수용체의 분자 신호 전달은
다소 복잡하다.
VDR은
레티노이드 X 수용체(RXR)와 결합하여 복합체를 형성하는데,
이것이 전통적인 경로를 구성한다.
VDR-RXR 복합체에 결합함으로써
비타민 D는 다수 유전자의 발현을 조절한다.
그러나
VDR은 막 내 수용체로도 작용할 수 있다.
이들은 시토크롬을 활성화하는
대체 경로를 시작하는 주요 물질들이다.
하류 효소에 의해 생성되는 화학 물질 중에는
세코스테로이드가 포함됩니다.
이 대사산물들은
일부 전사 인자의 기능을 조절하고 유전자 발현을 변화시킵니다(22, 23).
Vitamin D and the innate immune system
The innate immune system, which is the body’s first line of defense against pathogens, is in charge of quick reactions, pathogen detection, and elimination to stop an illness from getting worse. Vitamin D has a crucial role in innate immunity by stimulating the production of pattern recognition receptors (PRRs), antimicrobial peptides, and cytokines in the cells. Additionally, it can prevent the maturation and activation of dendritic cells as well as the differentiation of monocytes into macrophages. Cathelicidins, alpha- and beta-defensins, and other cationic antimicrobial peptides make up the majority of the immune system. The primary function of vitamin D signaling is to control innate immunological responses, according to numerous studies, especially those conducted in recent decades (24). The production of antimicrobial peptides by intestinal epithelial cells, Paneth cells, monocyte/macrophages, and neutrophils is one of the key factors in this control (24). Since the middle of the nineteenth century, vitamin D has been known to induce the antibacterial activity of human monocytes and macrophages (25). The phagocytic and chemo-like activity of macrophages is enhanced by 1,25-(OH)2 D3 (26). The generation of antimicrobial cathelicidin peptides is stimulated by the activation of the toll-like receptor in monocytes and macrophages, which also results in the positive expression of the VDR and alpha 1-hydroxylase genes, killing intrathecal Mycobacterium tuberculosis (27). However, 1,25-(OH)2 D3 suppresses the expression of TLR2 and TLR4 genes in macrophages. After 72 hours, this situation frequently takes control and negatively affects TLR activation and inflammation during the late infection stage. The conversion of 25-OH D3 into 1,25-(OH)2 D3 occurs during infection as a result of increased CYP27B1 expression in activated macrophages and monocytes brought on by cytokines like interferon- γ (IFN- γ) along with toll-like receptor signaling. The 1,25-(OH)2 D3 is then used to enhance the antibacterial activity of macrophages and monocytes via the VDR-RXR pathway. The outcome is an increase in cathelicidin production. The microbial membranes of invasive bacteria and fungus are destabilized by this peptide (28). As a result, 1,25-(OH)2 D3 is immunomodulatory in Mycobacterium TB infection (29). Antimicrobial peptides including 2-defensin and cathelicidin are activated by the calcitriol complex, retinoid X receptor, and VDR (30). Human cathelicidins, such as hCAP18 (either its 17-kDa (140 amino acids) or 5-kDa (37 amino acids) forms) and Leucine-leucine-37 (LL-37), isolated from a large prepropeptide in immune cells (neutrophils) or non-immune tissues (like testis), act against bacteria, fungi, and viruses as a response to infections and destroy microbial membranes (31). Vitamin D signaling has been shown to influence the physiological intestinal tract, aid intestinal hemostasis, and regulate microbiota in healthy individuals (24). Innate lymphoid cells (ILCs) and NK cells are also affected by 1,25-(OH)2 D3. T cell and dendritic cell (DC) responses are modulated by NK cells, which are crucial components of the innate immune system (32). ILCs are a crucial component of immunity. All mucosal tissues, particularly the colon, contain these cells. They are also among the first immune cells to promote cell growth, the healing of wounds, the release of anti-inflammatory mediators in response to infections, and the secretion of antimicrobial peptides (33–35). Through their VDR receptors, 1,25-(OH)2 D3 enhances the cytotoxic activity of NK cells and ILCs. The expression of their inflammatory cytokines is similarly decreased ( Figure 1 ) (24, 36–40) ( Table 1 ).
비타민 D와 선천성 면역 체계
병원체에 대한 신체의 첫 번째 방어선인 선천성 면역 체계는
질병이 악화되는 것을 막기 위해
신속한 반응, 병원체 탐지 및 제거를 담당합니다.
비타민 D는
세포 내에서 패턴 인식 수용체(PRRs),
항균 펩타이드 및 사이토카인의 생성을 자극함으로써
선천성 면역에 중요한 역할을 합니다.
또한,
수지상 세포의 성숙 및 활성화와
단핵구의 대식세포 분화를
억제할 수 있습니다.
카텔리시딘, 알파- 및 베타-디펜신, 기타 양이온성 항균 펩타이드가
면역 체계의 대부분을 구성합니다.
수많은 연구,
특히 최근 수십 년간 수행된 연구에 따르면(24),
비타민 D 신호전달의 주요 기능은 선천성 면역 반응을 조절하는 것이다.
장 상피세포,
파네스 세포,
단핵구/대식세포 및 호중구에 의한 항균 펩타이드 생산은
이러한 조절의 핵심 요소 중 하나이다 (24).
19세기 중반부터 비타민 D가
인간 단핵구 및 대식세포의 항균 활성을 유도한다는 사실이 알려져 왔다(25).
대식세포의 식균 및 화학유도성 활동은
1,25-(OH)2 D3에 의해 증강된다 (26).
항균성 카텔리시딘 펩타이드 생성은
단핵구 및 대식세포 내 톨 유사 수용체(TLR) 활성화에 의해 자극되며,
이는 또한 비타민 D 수용체(VDR) 및 알파 1-하이드록실라제 유전자의 양의 발현을 초래하여
척수강 내 결핵균(Mycobacterium tuberculosis)을 사멸시킵니다(27).
그러나
1,25-(OH)₂D₃는
대식세포에서 TLR2 및 TLR4 유전자 발현을 억제한다.
72시간 후,
이러한 상황은 종종 지배적 상태가 되어 후기 감염 단계에서
TLR 활성화와 염증에 부정적 영향을 미친다.
25-OH D₃가 1,25- (OH)2 D3로의 전환은
감염 중 인터페론-γ(IFN-γ)와 같은 사이토카인 및 톨 유사 수용체 신호전달에 의해 활성화된
대식세포와 단핵구에서 CYP27B1 발현 증가로 인해 발생합니다.
이후 1,25-(OH)2 D3는 VDR-RXR 경로를 통해
대식세포와 단핵구의 항균 활성을 강화하는 데 활용됩니다.
그 결과 카텔리시딘 생산이 증가합니다.
이 펩타이드(28)는
침습성 세균 및 곰팡이의 미생물 막을 불안정화시킵니다.
결과적으로 1,25-(OH)2 D3는
결핵균(Mycobacterium TB) 감염에서 면역조절 작용을 합니다(29).
2-디펜신 및 카텔리시딘을 포함한 항균 펩타이드들은
칼시트리올 복합체, 레티노이드 X 수용체(RXR), 및 VDR에 의해 활성화됩니다(30).
인간 카텔리시딘(hCAP18의 17-kDa(140 아미노산) 또는 5-kDa(37 아미노산) 형태,
류신-류신-37(LL-37) 등)은 면역 세포(호중구) 또는 비면역 조직(고환 등)에서
큰 프리프로펩타이드로부터 분리된 이들은 감염에 대한 반응으로
박테리아, 곰팡이, 바이러스에 대항하여 작용하며 미생물 막을 파괴한다(31).
비타민 D 신호 전달은
건강한 개인의 생리적 장관 기능에 영향을 미치고,
장 내 혈액 응고를 돕고,
미생물 군집을 조절하는 것으로 밝혀졌다 (24).
선천성 림프구 세포(ILCs)와 자연살해세포(NK 세포) 역시
1,25-(OH)₂D₃의 영향을 받습니다.
T 세포 및 수지상 세포(DC) 반응은
선천성 면역 체계의 핵심 구성 요소인
NK 세포에 의해 조절됩니다(32).
ILCs는
면역 체계의 핵심 구성 요소입니다.
모든 점막 조직,
특히 대장에는 이러한 세포가 존재합니다.
또한 감염에 대한 반응으로
세포 성장 촉진, 상처 치유, 항염증 매개체 방출, 항균 펩타이드 분비를 최초로 수행하는
1,25-(OH)₂D₃는 VDR 수용체를 통해
NK 세포와 ILC의 세포독성 활성을 강화합니다.
염증성 사이토카인의 발현 역시
유사하게 감소합니다( 그림 1 )(24, 36–40)( 표 1 ).
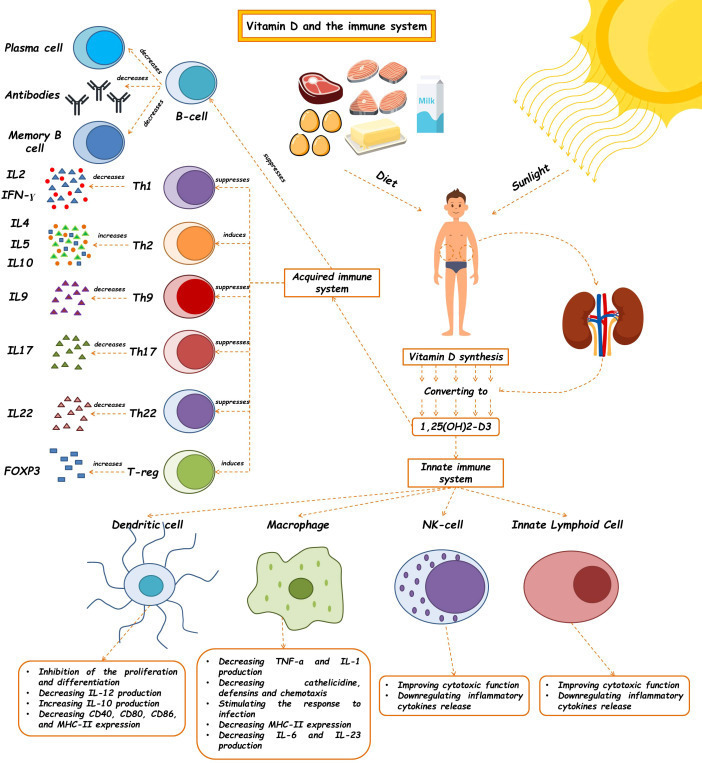
Figure 1.
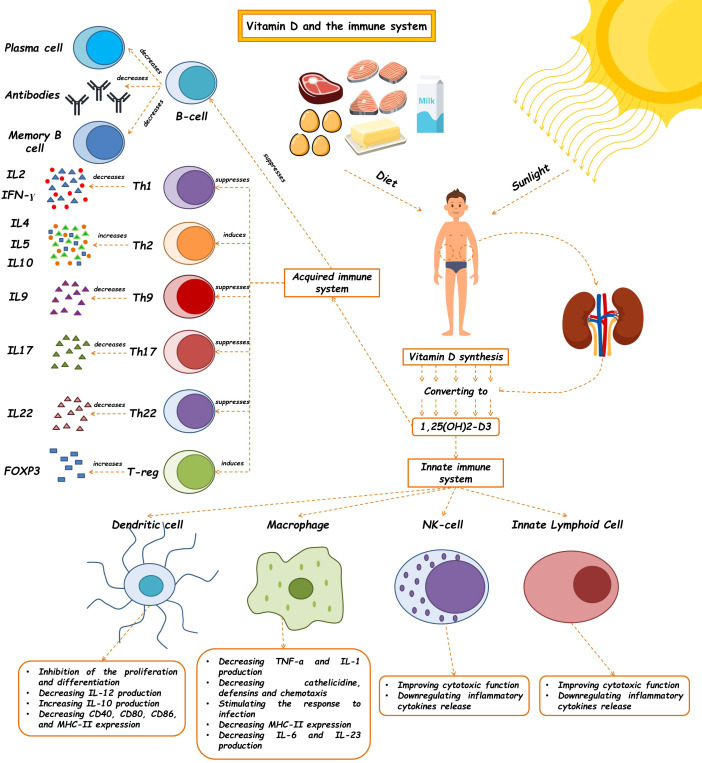
The effects of vitamin D on the immune system. Vitamin D and 1,25(OH)2D3 modulate the innate immune response. The regulatory role of this molecule has been shown to affect the innate immune system, such as macrophages, dendritic cells, Nk cells, and ILCs, so, as a critical molecule plays a role in many diseases' pathophysiology. This vitamin also contributes to making an acquired immune response. (See text for additional details). Th, T helper cell; IL, Interleukin; IFN-γ, Interferon-γ.
면역 체계에 대한 비타민 D의 영향.
비타민 D와 1,25(OH)2D3는 선천성 면역 반응을 조절합니다.
이 분자의 조절 역할은 대식세포, 수지상 세포, NK 세포, ILC와 같은
선천성 면역 체계에 영향을 미치는 것으로 밝혀졌으며,
따라서 중요한 분자로서 많은 질병의 병리생리학에서 역할을 합니다.
이 비타민은 또한 후천성 면역 반응 형성에 기여합니다(추가 세부 사항은 본문 참조).
Th, T 보조 세포; IL, 인터루킨; IFN-γ, 인터페론-γ.
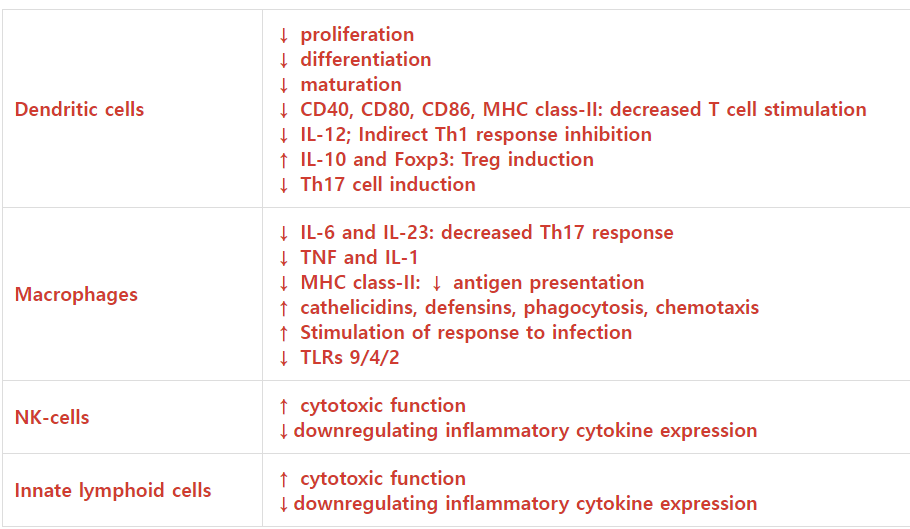
Table 1.
Effects of 1, 25(OH) 2D3 on innate immunity.
CellEffects of 1,25(OH)2D3References
| Dendritic cells | ↓ proliferation ↓ differentiation ↓ maturation ↓ CD40, CD80, CD86, MHC class-II: decreased T cell stimulation ↓ IL-12; Indirect Th1 response inhibition ↑ IL-10 and Foxp3: Treg induction ↓ Th17 cell induction | (41, 42) |
| Macrophages | ↓ IL-6 and IL-23: decreased Th17 response ↓ TNF and IL-1 ↓ MHC class-II: ↓ antigen presentation ↑ cathelicidins, defensins, phagocytosis, chemotaxis ↑ Stimulation of response to infection ↓ TLRs 9/4/2 | (41, 42) |
| NK-cells | ↑ cytotoxic function ↓downregulating inflammatory cytokine expression | (24, 43) |
| Innate lymphoid cells | ↑ cytotoxic function ↓downregulating inflammatory cytokine expression | (24, 44) |
Upward arrow means increasing.
Downward arrow means decreasing.
Vitamin D and the acquired immune system
Although the active form of vitamin D leads to the stimulation of innate immune responses, this vitamin causes the suppression of acquired immune responses ( Table 2 ). The most significant secretors of IL-2 and interferon-γ (IFN-γ) are T-helper 1 (Th1) cells, induced by the activation of the T cell receptor (TCR) and CD4+ membranous protein. In fact, Th1 is a key player in stimulating other inflammatory leukocytes and serves as a marker of cellular immunity activation. 1,25-(OH)2 D3 inhibits the synthesis of the pro-inflammatory cytokines IL-2 and IFN γ as well as Th1-mediated responses. By inhibiting the nuclear factor of activated T cells (NFAT) and activator protein-1 (AP-1) factors, 1,25-(OH)2 D3 encounters this inhibitory action (49). Additionally, 1,25-(OH)2 D3 increases the production of Th2 anti-inflammatory cytokines (including IL-3, -4, -5, and -10), while decreasing the production of Th9 (IL-9) and Th22 (IL-22) pro-inflammatory cytokines (48, 50). IL-9 is essential for attracting immune cells to the sites of inflammation, particularly mast cells. It is mostly produced by Treg cells. Th9 cell release of IL-9 may be the cause of allergic reactions and inflammatory reactions. The majority of IL-22-producing body cells are still Th22 cells. This crucial interleukin promotes the proliferation and development of keratinocytes. IL-22 enhances the secretion of anti-microbial peptides in the gut epithelium, which may result in a more effective defense against encroaching microorganisms. The anti-inflammatory function of T-regulatory cells, which is crucial for autoimmune control and homeostasis, is induced by 1,25-(OH)2 D3. The primary transcription factor in this class is Forkhead Box P3 (Foxp3). It is essential for 1,25-(OH)2 D3’s transcriptional upregulation as well as for the maturation, maintenance, and function of Tregs (51). It has been suggested that 1,25-(OH)2 D3 in both in vivo and in vitro conditions increases the amount of Tregs to reduce autoimmunity (52). In general, 1,25-(OH)2 D3 suppresses the induction of T-helper 1 (Th1)-cell cytokines, particularly IFN-γ; however, it also enhances Th2-cell immunological responses, which are mediated both directly by raising IL-4 production and indirectly by suppressing IFN-γ production (53). Many autoimmune and inflammatory disorders, including systemic lupus erythematosus, multiple sclerosis, and rheumatoid arthritis, are caused by Th17 cells, a type of inflammatory lymphocytes that promote inflammation and phagocytosis, notably neutrophils. Through mechanisms such as inhibition of the NFAT and RORt transcription factors, recruitment of histone deacetylase (HDAC), Runt-related transcription factor 1 (Runx1), and a direct impact on induction of Foxp3, the complex of vitamin D/VDR would result in the suppression of IL-17 production (54). Additionally, it may result in T cell homing at inflammatory areas and in the skin via CCR5 and CCR10, respectively. The homeostasis of B cells is directly impacted by VDR expression in their membrane. The active form of vitamin D causes apoptosis in antibody-producing cells, neutralizing the production and differentiation of B cells into plasma cells and memory cells, reducing the production of antibodies, and increasing the homing of these cells through CCR10 to the skin (53). The clinical significance of this influence on B cells can be shown in autoimmune illnesses including those linked to autoreactive antibodies. B cells produced a variety of autoantibodies. These have the power to harm the organs and start an inflammatory reaction that leads to autoimmune diseases. Additionally, a large number of regulatory B cells have been found to suppress the production of autoantibodies (55). In reality, the biologically active form of vitamin D suppresses B cell proliferation and controls their responses. Through lowering stimulant molecules like CD40, CD80, CD86, and MHC class-II in cells presenting antigens like dendritic cells, this vitamin also leads to T cell suppression and immune response modification ( Figure 1 ) (41). Let us explore the specific roles that vitamin D plays in some key immune-related disorders in the present review ( Table 3 ).
비타민 D와 후천적 면역 체계
비타민 D의 활성 형태는
선천적 면역 반응을 자극하지만,
이 비타민은 후천적 면역 반응을 억제합니다 ( 표 2 ).
IL-2 및 인터페론-γ(IFN-γ)의 가장 주요한 분비 세포는
T 세포 수용체(TCR)와 CD4+ 막 단백질의 활성화에 의해 유도되는
T-헬퍼 1(Th1) 세포입니다.
실제로 Th1은
다른 염증성 백혈구를 자극하는 핵심 역할을 하며
세포성 면역 활성화의 지표로 작용합니다.
1,25- (OH)₂D₃는
전염증성 사이토카인인 IL-2와 IFN-γ의 합성 및 Th1 매개 반응을 억제합니다.
활성화된 T 세포의 핵 인자(NFAT)와 활성화 단백질-1(AP-1) 인자를 억제함으로써,
1,25-(OH)₂D₃는 이러한 억제 작용을 수행합니다 (49).
또한 1,25-(OH)2 D3는
Th2 항염증성 사이토카인(IL-3, -4, -5, -10 포함)의 생산을 증가시키는 동시에
Th9(IL-9) 및 Th22(IL-22) 염증 촉진성 사이토카인의 생산을 감소시킵니다(48, 50).
IL-9는 특히
비만세포를 포함한 면역세포를 염증 부위로 유인하는 데 필수적이다.
주로 Treg 세포에서 생성된다.
Th9 세포의 IL-9 분비는
알레르기 반응 및 염증 반응의 원인이 될 수 있다.
IL-22를 생성하는 체세포의 대부분은
여전히 Th22 세포이다.
이 중요한 인터루킨은
각질세포의 증식과 발달을 촉진한다.
IL-22는
장 상피에서 항균 펩타이드 분비를 증진시켜
침입 미생물에 대한 방어 효과를 높일 수 있다.
자가면역 조절과 항상성 유지에 핵심적인 T조절세포의 항염증 기능은
1,25-(OH)2 D3에 의해 유도된다.
이 계열의 주요 전사인자는
포크헤드박스 단백질 P3 (Foxp3)입니다.
이는 1,25-(OH)2 D3의 전사적 상향 조절과
Treg의 성숙, 유지 및 기능에 필수적입니다(51).
in vivo 및 in vitro 조건 모두에서
1,25-(OH)2 D3가 자가면역 반응을 감소시키기 위해
Treg의 양을 증가시킨다는 것이 제안되었습니다(52).
일반적으로 1,25-(OH)2 D3는
T-헬퍼 1(Th1) 세포 사이토카인,
특히 IFN-γ의 유도를 억제합니다.
그러나 동시에
Th2 세포 면역 반응을 증강시키는데,
이는 IL-4 생산을 직접 증가시키고
IFN-γ 생산을 간접적으로 억제함으로써 매개됩니다 (53).
전신성 홍반성 루푸스, 다발성 경화증, 류마티스 관절염을 포함한
많은 자가면역 및 염증성 질환은
염증과 식세포작용(특히 호중구)을 촉진하는
염증성 림프구 유형인 Th17 세포에 의해 유발됩니다.
NFAT 및 RORt 전사 인자의 억제,
히스톤 탈아세틸화효소(HDAC)의 동원,
런트 관련 전사 인자 1(Runx1)의 동원,
그리고 Foxp3 유도에 대한 직접적 영향과 같은 메커니즘을 통해
비타민 D/VDR 복합체는 IL-17 생산을 억제할 수 있다(54).
또한, 각각 CCR5와 CCR10을 통해
염증 부위와 피부로의 T 세포 귀소(homing)를 유도할 수 있다.
B 세포의 항상성은
세포막 내 VDR 발현에 직접적으로 영향을 받는다.
활성형 비타민 D는
항체 생성 세포에서 세포 사멸을 유발하여
B 세포의 생산 및 형질 세포와 기억 세포로의 분화를 중화시키고,
항체 생산을 감소시키며,
CCR10을 통한 피부로의 이 세포들의 귀소(homing)를 증가시킵니다(53).
B 세포에 대한 이러한 영향의 임상적 중요성은
자가반응성 항체와 관련된 자가면역 질환을 포함한
자가면역 질환에서 확인할 수 있습니다.
B 세포는
다양한 자가항체를 생성합니다.
이러한 항체는 장기를 손상시키고
자가면역 질환으로 이어지는 염증 반응을 유발할 수 있습니다.
또한, 다수의 조절 B 세포가 자가항체 생성을 억제하는 것으로 밝혀졌습니다(55). 실제로, 생물학적 활성 형태의 비타민 D는 B 세포 증식을 억제하고 그 반응을 조절합니다. 또한 이 비타민은 수지상 세포와 같은 항원 제시 세포에서 CD40, CD80, CD86, MHC II급과 같은 자극 분자를 감소시켜 T 세포 억제와 면역 반응 조절을 유도합니다( 그림 1 )(41). 본 리뷰에서는 비타민 D가 주요 면역 관련 질환에서 수행하는 구체적인 역할을 살펴보겠습니다( 표 3 ).
Table 2.
Effects of 1, 25(OH)2D3 on adaptive immunity.
CellEffects of 1,25(OH)2D3References
| B cells | ↓ proliferation ↓ Plasma cell development ↓ Antibody secretion ↓Memory B cell differentiation ↑CCR10: Homing to skin | (45) | |
| T cells | Th1 | ↓ IL‐2 transcription ↓ IFN-γ transcription | (46) |
| Th2 | ↑Th2 Cytokines(IL4,IL5,IL10) | (47) | |
| Treg | ↑Treg cell differentiation ↑ Foxp3 transcription ↑IL10,CTLA4 | (46) | |
| Th17 | ↓ IL ‐17,IL21 transcription | (46) | |
| Th22 | ↓IL22 | (48) | |
| Th9 | ↓IL -9 | (48) | |
Upward arrow means increasing.
Downward arrow means decreasing.
Table 3.
Summarization of vitamin D function in different immune related disorders.
DiseaseCells affected by vitamin DMechanism of actionTarget genesRef
| Allergic rhinitis | T-helper type 2, Eosinophil | Decreased expression of CD86 | MIR17HG miR-17-92a-1 cluster host gene | (56, 57) |
| Asthma | CD4 + T cells | Respiratory infection prevention via enhancing the immunity of the lungs, inhibiting steroid resistance by increasing the production of IL-10 | VDR gene | (58, 59) |
| Atopic Dermatitis (AD) | Keratinocytes | Regulation of epidermal function and local immune response | CYP24A1 | (60, 61) |
| Rheumatoid Arthritis | T cells | Decreasing the production of IL-12 via NF-kB downregulation, inhibition of IFN-γ | TaqI | (62, 63) |
| Multiple sclerosis (MS) | Whole body | HLA-DRB*15 upregulation | HLA-DRB1 | (64) |
| Parkinson disease (PD) | Alterations in VDR expression levels | BsmI, FokI | (65) | |
| Infection-related disorders | Macrophages, monocytes, Paneth cells | Enhancement of cell autophagy, release of antimicrobial proteins | mTOR, cathelicidine | (66, 67) |
| Cancer | Tumor cells | MAPK and Nf-kB inhibition, immune regulation | MKP5, Nf-kB | (9, 68) |
| Diabetes mellitus (DM) | DCs and macrophages, cytotoxic T cells | Self-tolerance and immune regulation | MHC-II and co-stimulatory molecules | (69, 70) |
| Inflammatory bowel disease (IBD | B cells, T cells, dendritic cells, and macrophages | Enhancing the expression of IL-10, suppressing the proliferation of B and T cells | VDR, IL-10, Cathelicidine | (50, 71) |
Allergic rhinitis
Allergic rhinitis (AR) is a nasal mucosal disease characterized by an allergen reaction due to IgE production (72). The role of vitamin D is explained in multiple investigations related to this disorder. Examining the relationship between vitamin D serum levels and allergic diseases in adults using the third National Health and Nutrition Survey (NHANES III), Wjst et al. noted that AR worsened in vitamin D-deficient patients (73). Another Finnish study tried to investigate maternal intake of vitamin D in the course of pregnancy and its association with asthma and allergic rhinitis incidence in newborns. They recruited 1,669 children affected by allergic rhinitis, atopic eczema, and asthma. It was discovered that high levels of vitamin D intake in pregnant women were related to an allergic risk reduction in 5-year-old children (74). Additionally, Chen et al. suggested that prenatal vitamin D sufficiency has a protective effect on developing allergic rhinitis and aeroallergen sensitization at childhood (75).
Furthermore, pieces of evidence from clinical investigations demonstrated that AR risk can be inversely related to the serum vitamin D level (76, 77). On the contrary, Feng et al. indicated no causal association between them. This study goes against the previous claims of vitamin D supplementation’s protective effects on allergic rhinitis (78). In addition, Searing et al., in an in vitro study, explained that this important vitamin may affect dexamethasone’s stimulation on circulatory mononuclear cells’ IL-10 and mitogen-activated protein kinase phosphatase-1 (MAPKP-1). Vitamin D levels reflect a negative correlation with the dose of the inhaler, oral of steroids. The induced mRNA amount of mitogen-activated protein kinase phosphatase-1 (MKP-1) and IL-10-induced vitamin D with dexamethasone was significantly higher than those induced by dexamethasone by itself. MKP-1 and IL-10 are critical for glucocorticoid-dependent anti-inflammatory and repressive effects (79). Also, according to other in vitro studies, there is growing evidence that serum vitamin D level is correlated with inflammatory factors. Eosinophil infiltration, allergic symptom scores, and mRNA levels of IL-4 and IL-13 were all lower in the mice group under vitamin D supplementation. Moreover, CD86 expression in the cervical lymph nodes was decreased among T-helper type 2-mediated inflammation and CD11c+major histocompatibility complex II-high (MHCII high) cells. IL-4 was also conversely correlated with vitamin D levels (56, 80).
The MiR-17-92 cluster is a human miRNA located on chromosome 13. Increasing the expression of this miRNA has been reported in many immune disorders such as cancers and some allergic diseases, but the regulatory mechanism is not well defined. One way to treat allergic diseases is specific immunotherapy. It has been noted that vitamin D raises specific immunotherapy effects on MiR-17-92 cluster suppression in peripheral B cells in allergic rhinitis patients (81). This study confirmed that vitamin D improves the anti-inflammatory function of corticosteroids in patients with allergic rhinitis. Regarding the effects of vitamin D supplementation in the treatment regimen of allergic rhinitis, Bakhshaee et al. concluded that it could relatively improve symptoms of clinical AR, further emphasizing vitamin D supplementation as a therapeutic agent (82).
알레르기성 비염
알레르기성 비염(AR)은 IgE 생성으로 인한 알레르겐 반응이 특징인 비점막 질환입니다(72). 비타민 D의 역할은 이 질환과 관련된 여러 연구에서 설명됩니다. 제3차 국민건강영양조사(NHANES III)를 활용하여 성인의 비타민 D 혈청 농도와 알레르기 질환 간의 관계를 조사한 Wjst 등은 비타민 D 결핍 환자에서 AR이 악화되는 것을 확인했습니다(73). 또 다른 핀란드 연구는 임신 중 모체의 비타민 D 섭취량과 신생아의 천식 및 알레르기성 비염 발병률 간의 연관성을 조사했습니다. 연구진은 알레르기성 비염, 아토피성 습진, 천식에 걸린 1,669명의 아동을 모집했다. 그 결과, 임신 중 비타민 D 섭취량이 높을수록 5세 아동의 알레르기 위험이 감소하는 것으로 나타났다(74). 또한 Chen 등은 태아기 비타민 D 충분 공급이 아동기 알레르기성 비염 발병 및 공기 중 알레르겐 감작에 대한 보호 효과가 있다고 제안했다 (75).
또한 임상 연구 증거들은 알레르기성 비염 위험이 혈청 비타민 D 수치와 역상관 관계에 있을 수 있음을 보여주었다(76, 77). 반면, Feng 등은 이 둘 사이에 인과관계가 없다고 지적했다. 이 연구는 비타민 D 보충이 알레르기성 비염에 대한 보호 효과를 가졌다는 기존 주장과 상반된다 (78). 또한 Searing 등은 in vitro 연구에서 이 중요한 비타민이 순환 단핵구 세포의 IL-10 및 미토겐 활성화 단백질 키나아제 인산화효소-1(MAPKP-1)에 대한 덱사메타손의 자극에 영향을 미칠 수 있다고 설명했다. 비타민 D 수치는 흡입형 및 경구형 스테로이드 용량과 음의 상관관계를 보인다. 미토겐 활성화 단백질 키나아제 인산화효소-1(MKP-1) 및 IL-10 유도 비타민 D와 덱사메타손의 유도 mRNA 양은 덱사메타손 단독 유도량보다 유의하게 높았다. MKP-1과 IL-10은 글루코코르티코이드 의존성 항염증 및 억제 효과에 핵심적이다 (79). 또한 다른 in vitro 연구에 따르면, 혈청 비타민 D 수치가 염증 인자와 상관관계가 있다는 증거가 점점 더 많아지고 있다. 비타민 D 보충군 마우스에서 호산구 침윤, 알레르기 증상 점수, IL-4 및 IL-13 mRNA 수준이 모두 낮았다. 또한 경부 림프절에서 T-헬퍼 2형 매개 염증 및 CD11c+ 주요 조직적합성 복합체 II 고발현(MHCII high) 세포의 CD86 발현이 감소하였다. IL-4는 비타민 D 수치와 역상관 관계에 있었습니다(56, 80).
MiR-17-92 클러스터는 13번 염색체에 위치한 인간 miRNA입니다. 이 miRNA의 발현 증가는 암 및 일부 알레르기 질환과 같은 많은 면역 장애에서 보고되었지만, 그 조절 메커니즘은 아직 명확하게 밝혀지지 않았습니다. 알레르기 질환 치료법 중 하나는 특이 면역요법이다. 알레르기 비염 환자에서 비타민 D가 말초 B 세포 내 MiR-17-92 클러스터 억제를 통해 특이 면역요법 효과를 증진시킨다는 점이 확인되었다(81). 본 연구는 비타민 D가 알레르기성 비염 환자의 코르티코스테로이드 항염증 기능을 개선함을 확인하였다. 알레르기성 비염 치료 요법에서의 비타민 D 보충 효과와 관련하여, Bakhshaee 등은 임상적 알레르기성 비염 증상을 상대적으로 개선할 수 있다고 결론지었으며, 이는 치료제로서의 비타민 D 보충의 중요성을 더욱 강조한다(82).
Asthma
The role of vitamin D in asthma is still uncertain. The CDX2 polymorphism is in the 9,913th position in the promoter region of the VDR gene emerging from the substitution of A with G. It has been mentioned that this polymorphism changes the levels of VDR transcription and its overall activity. It also subsequently modulates the genes effective in inflammation, regulation of immunity, and airways remodeling. This polymorphism in its homozygous form has been associated with the diagnosis of asthma and decreased FEV1 (21).
Some cross-sectional studies have indicated a possible relationship between asthma and vitamin D clinically (83). Studies have concluded that a drop in serum level of 1,25-(OH)2 D3 was associated with an advance in prevalence, hospitalization, the number of emergency visits, respiratory rate, and a reduction in lung function in children with asthma (84). Recent clinical trials have proved the protective effect of vitamin D supplements in asthmatic patients (85–87). One study demonstrated that weekly oral calcifediol supplementation in vitamin D-deficient adults could help control the disease course and improve patients’ quality of life (88). One study by Gapta et al. reported that the low serum levels of vitamin D in children with steroid-resistant asthma (STRAs) are characterized by decreased lung function, increased corticosteroid use, and asthma exacerbation. The possible reason was that low vitamin D levels help smooth muscles of the respiratory tract to grow and diminish lung function in severe asthma (89). Examples of vitamin D activity in asthma include improving the immune function of the lung tissue and preventing the development of respiratory infections (85, 90, 91) or overcoming resistance to steroids by increasing the production of IL -10 via CD4 + T cells (92). In contrast with the asthma prevention duty of vitamin D, it can cause the exacerbation of it. Low levels of vitamin D (<30 ng/mL) increase the risk of asthma (83, 93).
Furthermore, several studies could not show a significant correlation between vitamin D levels and the incidence of asthma in children and adults (94–96). In addition, several clinical trials failed to find a significant association between vitamin D supplementation in deficient individuals and improvement in clinical outcomes such as controlling the disease course, lessening symptoms and side effects, improving respiratory volumes and ratios, reducing exacerbation episodes, and decreasing required medications (97–99). In addition, vitamin D intake during pregnancy enhances the risk of asthma in children and adults (100, 101).
천식
비타민 D의 천식에서의 역할은 여전히 불확실하다. CDX2 다형성은 VDR 유전자 프로모터 영역의 9,913번째 위치에서 A가 G로 치환되어 나타난다. 이 다형성은 VDR 전사 수준과 전반적 활성을 변화시킨다고 알려져 있다. 또한 염증, 면역 조절, 기도 재형성에 관여하는 유전자들을 후속적으로 조절한다. 이 다형성의 동형접합 형태는 천식 진단 및 FEV1 감소와 연관성이 확인되었다 (21).
일부 단면 연구에서는 임상적으로 천식과 비타민 D 간의 가능한 연관성을 시사하였다(83). 연구 결과, 혈청 1,25-(OH)2 D3 수치 저하는 천식 아동의 유병률 증가, 입원, 응급실 방문 횟수, 호흡수 증가 및 폐 기능 저하와 연관되었다(84) . 최근 임상시험들은 천식 환자에서 비타민 D 보충제의 보호 효과를 입증하였다(85–87). 한 연구는 비타민 D 결핍 성인에게 주간 경구 칼시페디올 보충이 질환 경과 조절과 환자 삶의 질 개선에 도움이 될 수 있음을 보여주었다(88). Gapta 등의 연구에 따르면, 스테로이드 저항성 천식(STRAs) 소아에서 낮은 혈청 비타민 D 수치는 폐 기능 저하, 코르티코스테로이드 사용 증가, 천식 악화로 특징지어진다. 가능한 원인은 낮은 비타민 D 수치가 중증 천식에서 호흡기 평활근의 증식을 촉진하고 폐 기능을 감소시키기 때문일 수 있다(89). 비타민 D의 천식 관련 작용 예로는 폐 조직의 면역 기능 개선 및 호흡기 감염 예방(85, 90, 91) 또는 CD4+ T 세포를 통한 IL-10 생산 증가로 스테로이드 저항성 극복(92) 등이 있다. 비타민 D의 천식 예방 효과와 대조적으로, 오히려 천식 악화를 유발할 수도 있다. 비타민 D 수치가 낮을수록(<30 ng/mL) 천식 발병 위험이 증가한다(83, 93).
또한 여러 연구에서 비타민 D 수치와 소아 및 성인의 천식 발병률 사이에 유의미한 상관관계를 보여주지 못했다(94–96). 또한 여러 임상 시험에서 비타민 D 결핍자에게 보충제를 투여했을 때, 질병 경과 조절, 증상 및 부작용 완화, 호흡량 및 비율 개선, 악화 횟수 감소, 필요 약물 감소와 같은 임상적 결과 개선 사이의 유의미한 연관성을 찾지 못했습니다(97–99). 또한 임신 중 비타민 D 섭취는 아동 및 성인의 천식 위험을 증가시킵니다(100, 101).
Atopic dermatitis
Among the factors involved in atopic dermatitis (AD), the growing importance of vitamin D deficiency was noted in atopic patients. Furthermore, vitamin D is correlated with the antimicrobial peptide (AMP) production by keratinocytes. Vitamin D and its analog play a vital role in treating AD, psoriasis, vitiligo, and acne (17, 102–104). Few investigations have surveyed the prevalence and severity of AD in people with vitamin D deficiency. Atopic dermatitis is associated with vitamin D levels, and vitamin D deficiency increases the risk of atopic dermatitis (105).
On the other hand, it has been noticed that vitamin D levels were higher in mild AD patients than in those with moderate to severe dermatitis (95). It seems that children born to mothers who have a low intake of fish or vitamin D during pregnancy have a higher risk of developing atopic dermatitis symptoms (106, 107). Also, as Wang et al. suggested, low breast milk vitamin D levels may influence the infant’s immune system, inversely correlated with persistent AD symptoms (108).
However, despite the positive relationship between hypovitaminosis D in the above studies and the prevalence or severity of AD, several texts have shown the reverse association (76, 109). Another investigation discovered that children of mothers with elevated serum 25-OH D3 levels had a higher risk of emerging advanced eczema at 9 months and 9 years old (100). Moreover, research carried out by Tian et al. claimed that the risk of atopic dermatitis (AD) in children at the first year of age is generally increased with higher maternal serum vitamin D levels throughout pregnancy (110). From the above considerations, it can be implied that this is a very controversial topic. Vitamin D is sometimes a protective agent and sometimes a risk factor for AD. However, it seems that at least in the majority of studies, it has been suggested that there is a reverse relationship between vitamin D serum levels (food intake or sunlight) and AD prevalence and severity. Further fueling the conflicting evidence in this matter, Lucas et al. believed that 1-hydroxylase CYP27B1 (responsible for 1,25-Vitamin D3 synthesis), the vitamin D receptor, and the vitamin D-mediated signaling target gene CYP24A1 are all upregulated as a result of allergic sensitization, which subsequently auto-downregulates vitamin D receptor-mediated signaling through reducing available ligand accumulations. This study suggested that an increase in local vitamin D-mediated signaling is a pro-allergic condition at the inflammation site, which results in low serum levels of vitamin D (111).
Vitamin D plays an essential role in regulating innate and acquired immune mechanisms. Vitamin D receptors (VDRs) have been found in various cells, including keratinocytes and multiple immune cells (112). 1,25-(OH)2 D3 prevents T cell proliferation, especially Th1s producing IL-2 and interferon-γ leading to macrophages and Th17s activation. It induces production of IL-17 and IL-22 (113–115). Moreover, 1,25-(OH)2 D3 reproduce CD4 +/CD25 + cells through stimulating IL-10 production, which ultimately impairs the Th1s and Th17s development (116, 117).
The polymorphisms of the VDR gene may cause differences in response to vitamin D in inflammatory conditions. Some of them might be discovered in severe AD patients, such as rs2228570, rs1544410, rs7975232, and rs731236. This indicates that the VDR controls AD by regulating epidermal function or affecting the local immune response (60). Langerhans and inflammatory dendritic epidermal cells (IDEC), both located in the epidermis of patients suffering from AD, expressing FcϵRI (high-affinity IgE receptor) and sensing allergens. Herrmann et al. explained that active vitamin D3 could downregulate the receptor at the protein and mRNA levels of its α-chain, impairing IgE-mediated inflammatory processes afterward (118). Cristi et al. also concluded that vitamin D sufficiency lowers the allergic phenotype of circulating DCs in AD children (119). As Mansour et al. suggested, vitamin D supplementation can be regarded as an effective treatment, decreasing the risk of severe atopic dermatitis symptoms, adding it to the existing studies already confirming vitamin D adjuvant therapy to be beneficial in mild to moderate cases (120).
아토피 피부염
아토피 피부염(AD) 관련 요인 중 아토피 환자에서 비타민 D 결핍의 중요성이 점차 부각되고 있다. 또한 비타민 D는 각질세포의 항균 펩타이드 (AMP) 생산과 상관관계가 있습니다. 비타민 D와 그 유사체는 아토피 피부염, 건선, 백반증, 여드름 치료에 중요한 역할을 합니다(17, 102–104). 비타민 D 결핍 환자의 아토피 피부염 유병률과 중증도를 조사한 연구는 거의 없습니다. 아토피 피부염은 비타민 D 수치와 연관되어 있으며, 비타민 D 결핍은 아토피 피부염 발병 위험을 증가시킵니다(105) .
반면, 경증 아토피 피부염 환자의 비타민 D 수치가 중등도에서 중증 피부염 환자보다 높은 것으로 관찰되었습니다(95). 임신 중 생선 또는 비타민 D 섭취량이 낮은 어머니에게서 태어난 아이들은 아토피 피부염 증상 발병 위험이 더 높은 것으로 보입니다(106, 107). 또한 왕(Wang) 등이 제안한 바와 같이, 모유 내 낮은 비타민 D 수치는 영아의 면역 체계에 영향을 미쳐 지속성 아토피 피부염 증상과 역상관 관계를 보일 수 있다 (108).
그러나 위 연구들에서 비타민 D 결핍과 아토피 피부염의 유병률 또는 중증도 사이의 양의 상관관계에도 불구하고, 여러 문헌에서는 반대의 연관성을 보여주었습니다(76, 109). 또 다른 연구에서는 혈청 25-OH D3 수치가 높은 어머니의 자녀가 9개월 및 9세에 중증 습진이 발생할 위험이 더 높다는 사실을 발견했습니다(100). 또한 Tian 등의 연구는 임신 기간 동안 모체의 혈청 비타민 D 수치가 높을수록 생후 첫해 아동의 아토피 피부염(AD) 발병 위험이 전반적으로 증가한다고 주장하였다(110). 위와 같은 고려 사항들을 종합해 볼 때, 이는 매우 논란의 여지가 있는 주제임을 시사한다. 비타민 D는 때로는 보호 인자로, 때로는 AD의 위험 요인으로 작용한다. 그러나 대다수의 연구에서는 비타민 D 혈청 농도(식이 섭취 또는 일광 노출)와 아토피 피부염 유병률 및 중증도 사이에 역상관 관계가 존재한다는 점이 제시된 것으로 보인다. 이러한 상반된 증거를 더욱 부채질하는 연구로, 루카스(Lucas) 등은 1-하이드록실라제 CYP27B1(1,25-비타민 D3 합성 담당), 비타민 D 수용체, 그리고 비타민 D 매개 신호 전달 표적 유전자 CYP24A1이 모두 알레르기 감작의 결과로 상향 조절되며, 이는 이후 이용 가능한 리간드 축적을 감소시켜 비타민 D 수용체 매개 신호 전달을 자가 하향 조절한다고 주장했습니다. 이 연구는 국소 비타민 D 매개 신호 전달의 증가가 염증 부위에서 알레르기 유발 조건을 조성하여 혈청 비타민 D 수치를 낮춘다고 제안했습니다(111).
비타민 D는 선천적 및 후천적 면역 기전 조절에 필수적인 역할을 한다. 비타민 D 수용체(VDR)는 각질세포 및 다양한 면역세포를 포함한 여러 세포에서 발견된다 (112). 1,25-(OH)2 D3는 특히 IL-2와 인터페론-γ를 생성하는 Th1 세포의 증식을 억제하여 대식세포와 Th17 세포의 활성화를 유도합니다. 이는 IL-17과 IL-22의 생산을 촉진합니다(113–115). 또한, 1,25-(OH)2 D3는 IL-10 생산을 자극하여 CD4+/CD25+ 세포를 재생산하며, 이는 궁극적으로 Th1 및 Th17 세포의 발달을 저해합니다(116, 117).
VDR 유전자의 다형성은 염증 상태에서 비타민 D에 대한 반응 차이를 유발할 수 있습니다. 그중 일부는 중증 아토피 피부염 환자에서 발견될 수 있으며, rs2228570, rs1544410, rs7975232, rs731236 등이 해당됩니다. 이는 VDR이 표피 기능을 조절하거나 국소 면역 반응에 영향을 미쳐 아토피 피부염을 제어함을 시사합니다(60). . 아토피 피부염 환자의 표피에 위치한 랑게르한스 세포와 염증성 수지상 표피 세포(IDEC)는 FcϵRI(고친화성 IgE 수용체)를 발현하며 알레르겐을 감지한다. Herrmann 등은 활성 비타민 D3가 이 수용체의 α-사슬 단백질 및 mRNA 수준에서 발현을 억제하여 이후 IgE 매개 염증 과정을 저해할 수 있다고 설명했다(118). 크리스티(Cristi) 등은 비타민 D 충분량이 아토피 피부염 아동의 순환성 DC(수지상 세포) 알레르기 표현형을 감소시킨다는 결론도 내렸다(119). 만수르(Mansour) 등이 제안한 바와 같이, 비타민 D 보충은 경증에서 중등도 사례에 비타민 D 보조 요법이 유익함을 이미 확인한 기존 연구에 더해, 중증 아토피 피부염 증상 위험을 감소시키는 효과적인 치료법으로 간주될 수 있다(120).
Rheumatoid arthritis
Rheumatoid arthritis (RA) is an autoimmune disease of connective tissue that mainly affects synovial joints, causing grueling pain and reducing life expectancy (121). Although the exact cause is not entirely understood, researchers have suggested that genetic and environmental factors contribute to the RA pathogenesis (122). Considering the suppressant effects of vitamin D and the possible association between vitamin D deficiency and autoimmune disorders (123), it has been studied as a potential aid to the pathogenesis of autoimmune diseases, including RA (124). Studies have shown that many autoimmune disorders are correlated with lacking vitamin D (125, 126). This is confirmed that 1,25-(OH)2 D3 reduces the production of IL-12 production through NF-kB downregulation, inhibits the secretion of IFN-γ, and limits the expression of IL-6 receptor; in vivo administration of 1,25-(OH)2 D3 appears to have preventive effects on autoimmune diseases (77, 127, 128). Also, by inhibiting the expression of macrophage aromatases, vitamin D can reduce the conversion of androgens to estrogens which play a significant part in the activation of B lymphocytes and consequently the autoimmune response in RA (62).
The activity of vitamin D depends on VDR, and the activation of VDR can inhibit pro-inflammatory T cells and DC differentiation. In addition, VDR agonists induce T-regulator and NK cells and thus suppress self-immunity (63). It has been proved that VDR polymorphism accelerates RA sensitivity (129). One of these polymorphisms is TaqI or rs731236, located within Exon 9 at the 3′ end of the VDR gene. Probably the TT genotype of this polymorphism is a risk factor for RA (130). Studies have indicated that high levels of vitamin D absorption can reduce the risk of rheumatoid arthritis by 24% (131). In addition, vitamin D deficiency in these patients can lead to a more severe and active course of the disease; thus, vitamin D serum level may be a predictive factor for one-year disability and disease progression (132, 133). But not all evidence is in favor of the preventative effects of vitamin D. A recent study on RA patients concluded no significant differences between vitamin D-deficient and -non-deficient patients considering criteria such as swollen joints count (SJC), VAS-pain, tender joints count (TJC), and DAS28 scores (134). Further investigations can shed light on various features of the relationship between RA and vitamin D.
류마티스 관절염
류마티스 관절염(RA)은 주로 활막 관절을 침범하여 극심한 통증을 유발하고 기대 수명을 단축시키는 결합 조직의 자가면역 질환이다(121). 정확한 원인은 완전히 밝혀지지 않았으나, 연구자들은 유전적 및 환경적 요인이 RA 발병 기전에 기여한다고 제안했다(122). 비타민 D의 억제 효과와 비타민 D 결핍 및 자가면역 질환 간의 연관성 가능성(123)을 고려하여, 비타민 D는 RA를 포함한 자가면역 질환의 병인에 대한 잠재적 보조제로 연구되어 왔다(124). 연구에 따르면 많은 자가면역 질환이 비타민 D 결핍과 상관관계가 있는 것으로 나타났다(125, 126). 1,25-(OH)2 D3가 NF-kB 하향 조절을 통해 IL-12 생산을 감소시키고, IFN-γ 분비를 억제하며, IL-6 수용체 발현을 제한한다는 사실이 확인되었습니다. 생체 내(in vivo) 1,25-(OH)2 D3 투여는 자가면역 질환에 예방 효과가 있는 것으로 보입니다(77, 127, 128). 또한, 비타민 D는 대식세포 아로마타아제 발현을 억제함으로써 안드로겐이 에스트로겐으로 전환되는 것을 감소시킬 수 있으며, 이는 B 림프구 활성화와 결과적으로 RA의 자가면역 반응에 중요한 역할을 합니다 (62).
비타민 D의 활성은 VDR에 의존하며, VDR의 활성화는 전염증성 T 세포와 DC 분화를 억제할 수 있습니다. 또한 VDR 작용제는 T-조절 세포와 NK 세포를 유도하여 자가면역을 억제합니다(63). VDR 다형성이 RA 감수성을 가속화한다는 것이 입증되었습니다(129). 이러한 다형성 중 하나는 VDR 유전자 3′ 말단 엑손 9 내에 위치한 TaqI 또는 rs731236입니다. 이 다형성의 TT 유전자형은 RA의 위험 인자일 가능성이 있습니다(130). 연구에 따르면 높은 수준의 비타민 D 흡수는 류마티스 관절염 위험을 24% 감소시킬 수 있다(131). 또한, 이들 환자에서 비타민 D 결핍은 더 심각하고 활동적인 질병 경과로 이어질 수 있으므로, 비타민 D 혈청 수치는 1년 장애 및 질병 진행의 예측 인자가 될 수 있다(132, 133). 그러나 모든 증거가 비타민 D의 예방 효과를 지지하는 것은 아니다. 최근 류마티스 관절염 환자를 대상으로 한 연구에서는 부종 관절 수(SJC), VAS 통증, 압통 관절 수(TJC), DAS28 점수 등의 기준을 고려할 때 비타민 D 결핍군과 비결핍군 간 유의미한 차이가 없다고 결론지었다(134). 추가 연구를 통해 류마티스 관절염과 비타민 D의 관계에 대한 다양한 특징을 밝힐 수 있을 것이다. 다 관절 수(TJC), DAS28 점수 등 기준을 고려했을 때 유의미한 차이가 없다고 결론지었습니다(134). 추가 연구를 통해 류마티스 관절염과 비타민 D의 관계에 대한 다양한 특징을 밝힐 수 있을 것입니다.
Multiple sclerosis
The pattern of MS occurrence varies throughout the world: its prevalence shows a steep slope over the equator, and the disease is more prevalent in areas near the poles (135). This can be associated with the level of UVB exposure (136) and can support the theory that environmental factors frequently influence the MS risk in early life. Studies have determined a relationship between the serum level of 25-OH D3 and MS risk development, namely, and there is a negative association between vitamin D levels and MS (137, 138). Obesity and smoking remain the two other MS risk factors correlated with vitamin D deficiency (139, 140). Although smoking and obesity may affect the MS risk by changing the vitamin D level, they may also affect the risk of MS in a vitamin D-independent way (141, 142). The association between MS and five loss-of-function mutations on the CYP27B1 gene encoding the 25-OH vit-D-1a-hydroxylase enzyme strongly indicates vitamin D’s critical role in MS etiology has been confirmed that these mutations decrease the level of vitamin D (143). However, three subsequent attempts to repeat this finding were unsuccessful. Now it seems that although these variants are associated with the risk of developing MS, their contribution to MS inheritance is small (144–146). Furthermore, the expression of HLA-DRB1*1501, the most potent genetic marker for MS, is regulated through the VDRE (vitamin D response element) in the promoter region (147, 148). Further investigations have revealed that vitamin D receptor gene polymorphisms could affect vitamin D absorption and increase MS susceptibility in various populations (148, 149). According to the meta-analysis conducted by Imani et al., Taql and Bsml polymorphisms, despite Apal polymorphism, lead to MS risk enhancement (150). Another risk reduction theory was explained in the study by Spanier et al. It stated that CTLA-4 functions as a mediator for MS prevention and, in the presence of vitamin D, its expression is significantly increased inside intracerebral myeloid cells (151).
More than 200 SNPs were detected out of the HLA region during the GWAS studies which are significantly related to MS disease. Among them, some SNPs are associated with genes responsible for vitamin D metabolisms such as rs2248359, CYP24A1, rs2248137, rs12368653, rs703842, rs10876994, CYP27B1, rs201202118, rs703842, and rs701006 (152, 153). These observations indicate that vitamin D relates to the transcription of the genes associated with MS and alters their mechanism of action (154). This important nutrient is assumed to have a key role in repairing genes expression, especially MYH, OGG1, MTH1, and NRF2 in MS patients (155).
다발성 경화증
다발성 경화증(MS)의 발생 패턴은 전 세계적으로 다양합니다: 유병률은 적도를 중심으로 급격히 증가하며, 극지방 근처 지역에서 더 흔하게 나타납니다(135). 이는 자외선 B(UVB) 노출 수준과 연관될 수 있으며(136), 환경적 요인이 생애 초기 다발성 경화증 위험에 영향을 미친다는 이론을 뒷받침할 수 있습니다. 연구에 따르면 혈청 25-OH D3 수치와 다발성 경화증 발병 위험 간에 관계가 확인되었으며, 특히 비타민 D 수치와 다발성 경화증 간에는 음의 상관관계가 존재합니다(137, 138). 비만과 흡연은 비타민 D 결핍과 연관된 다른 두 가지 다발성 경화증 위험 요인으로 남아 있습니다(139, 140). 흡연과 비만이 비타민 D 수치 변화를 통해 다발성 경화증 위험에 영향을 미칠 수 있지만, 비타민 D와 무관한 방식으로 위험에 영향을 줄 수도 있습니다(141, 142). 다발성 경화증과 25-OH 비타민 D-1α-하이드록실라아제 효소를 암호화하는 CYP27B1 유전자의 5가지 기능 상실 돌연변이 사이의 연관성은 비타민 D가 다발성 경화증 발병 기전에서 중요한 역할을 한다는 점을 강력히 시사하며, 이러한 돌연변이가 비타민 D 수치를 감소시킨다는 사실이 확인되었습니다(143). 그러나 이후 세 차례에 걸친 이 발견을 재현하려는 시도는 모두 실패로 돌아갔습니다. 현재 이러한 변이체들은 MS 발병 위험과 연관되지만, MS 유전에 기여하는 정도는 미미한 것으로 보인다(144–146). 또한, MS의 가장 강력한 유전적 표지자인 HLA-DRB1*1501의 발현은 프로모터 영역의 VDRE(비타민 D 반응 요소)를 통해 조절된다(147, 148). 추가 연구를 통해 비타민 D 수용체 유전자 다형성이 비타민 D 흡수에 영향을 미치고 다양한 인구 집단에서 MS 감수성을 증가시킬 수 있음이 밝혀졌다(148, 149). Imani 등의 메타분석에 따르면, Apal 다형성과는 달리 Taql 및 Bsml 다형성이 MS 위험 증가로 이어진다(150). Spanier 등의 연구에서는 또 다른 위험 감소 이론이 제시되었습니다. CTLA-4가 다발성 경화증 예방의 매개체 역할을 하며, 비타민 D 존재 시 뇌내 골수계 세포 내에서 그 발현이 현저히 증가한다는 것입니다(151).
GWAS 연구 과정에서 HLA 영역 외부에 다발성 경화증 질환과 유의미하게 관련된 200개 이상의 단일핵산다형성(SNP)이 검출되었다. 이 중 일부 SNP는 rs2248359, CYP24A1, rs2248137, rs12368653, rs703842, rs10876994, CYP27B1, rs201202118, rs703842 및 rs701006 (152, 153) 등이 있습니다. 이러한 관찰 결과는 비타민 D가 다발성 경화증 관련 유전자 전사와 연관되어 그 작용 기전을 변화시킨다는 점을 시사합니다 (154). 이 중요한 영양소는 특히 다발성 경화증 환자에서 MYH, OGG1, MTH1 및 NRF2와 같은 유전자 발현을 복구하는 데 핵심적인 역할을 하는 것으로 추정됩니다 (155).
Parkinson disease
Parkinson’s disease (PD) is a motor disorder characterized by tremor, stiffness, acne, and loss of local reflexes, leading to immobility and frequent corrosion. There were pieces of evidence that manifested vitamin D deficiency can increase the prevalence of PD (156–158). Interestingly, people with high concentrations of vitamin D in their serum show a reduction in Parkinson’s risk (159). This is also related to exposure to ultraviolet radiation (160). Many studies have proved that vitamin D is critical for the growth and function of the brain. VDRs and 1-alpha-hydroxylase, the enzyme responsible for vitamin D activation, are observed in the substantia nigra and the hypothalamus’s principal neurons and glial cells (161). Mice whose VDRs have been knocked out have developed muscular and motorized dysfunctions (162). In addition, higher levels of 1,25-(OH)2 D3 and VDR FokI CC genotypes are associated with mild forms of Parkinson’s disease (163). Different VDR polymorphisms such as the DHCR7/NADSYN1 locus and the CYP2R1 gene can affect clinical symptoms of PD through an impaired mechanism of turning vitamin D into valuable chemicals (164).
Recent studies have demonstrated the association between BsmI and FokI polymorphisms in VDR and PD sensitivity (165, 166). The BsmI bb genotype is more common in PD and causes the alteration in the VDR expression levels of mRNA. In patients with PD, FokI CC and TC genotypes are more prevalent than TT. In those regions with higher UV radiation, an association between UV and TaqI and ApaI has been found. The PD risk is reduced in the homozygous form of the TT TaqI genotype and the homozygous form of the GG ApaI genotype (167).
파킨슨병
파킨슨병(PD)은 떨림, 경직, 근육 경직 및 국소 반사 신경 상실을 특징으로 하는 운동 장애로, 이로 인해 움직임이 제한되고 빈번한 퇴행이 발생합니다. 비타민 D 결핍이 PD의 유병률을 증가시킬 수 있다는 증거가 여러 건 제시되었습니다(156–158). 흥미롭게도 혈청 내 비타민 D 농도가 높은 사람들은 파킨슨병 발병 위험이 감소하는 것으로 나타났습니다(159). 이는 자외선 노출과도 관련이 있습니다 (160). 다수의 연구에서 비타민 D가 뇌의 성장과 기능에 필수적임을 입증하였습니다. 흑질과 시상하부의 주요 뉴런 및 신경교세포에서 비타민 D 활성화 효소인 VDR과 1-알파-하이드록실라제가 관찰됩니다(161). VDR이 결손된 마우스는 근육 및 운동 기능 장애를 보였습니다(162). 또한, 높은 수준의 1,25-(OH)2 D3와 VDR FokI CC 유전자형은 경증 파킨슨병과 연관되어 있다(163). DHCR7/NADSYN1 유전자좌와 CYP2R1 유전자와 같은 다양한 VDR 다형성은 비타민 D를 유용한 화학물질로 전환하는 메커니즘 장애를 통해 파킨슨병의 임상 증상에 영향을 미칠 수 있다 (164).
최근 연구에서는 VDR의 BsmI 및 FokI 다형성과 파킨슨병 감수성 간의 연관성이 입증되었다(165, 166). BsmI bb 유전자형은 파킨슨병에서 더 흔하며, mRNA의 VDR 발현 수준 변화를 유발한다. 파킨슨병 환자에서 FokI CC 및 TC 유전자형은 TT보다 더 흔하다. 자외선(UV) 방사량이 높은 지역에서는 UV와 TaqI, ApaI 다형성 간의 연관성이 발견되었다. TT TaqI 유전자형의 동형접합체와 GG ApaI 유전자형의 동형접합체에서는 파킨슨병 위험이 감소한다(167).
Infection-related disorders
Vitamin D plays an important role in regulatory actions of the immune system. This is essential for controlling infection-related disorders. Prior investigations indicated that respiratory infections, human immunodeficiency virus (HIV), and Mycobacterium tuberculosis (TB) were strongly associated with low levels of vitamin D in the circulation (168). The major antimicrobial protein, cathelicidin, is known to be necessary in the defensive actions of monocytes against the invading pathogens (66). Vitamin D receptor signaling crosstalks with the production of cathelicidin in these cells (169). Also, vitamin D-cathelicidin axis is vital in intestinal inflammation preventing gastrointestinal infections (170). The enhancement of the Paneth cells in response to the vitamin D receptor signaling was also studied very much (171). Toll-like receptors 1/2 (TLR 1/2) have been identified to be activated by 1,25-dihydroxy-vitamin D (vitamin D3) inducing the antimicrobial effects of tissue macrophages (27). By means of mammalian target of rapamycin (mToR) signaling, this micronutrient is also capable of inflammation attenuation in airway systems through enhancing cell autophagy (67).
Vitamin D supplementation and prevention of the infections such as coronavirus disease (COVID-19) has recently been investigated by many scientists (172–174). The results are still conflicting. Regarding TB infection, a large randomized clinical trial was conducted with a sample size of 8,851 children. The conclusion stated that vitamin D had no superior effect on TB infection risk than placebo (173). On the other hand, some studies demonstrated that vitamin D supplementation had a promising lowering impact on the risk of upper respiratory infections (172, 174). There remains a huge demand for larger and more accurate studies in order to assess the net effect of vitamin D on the incidence of various infection types.
감염 관련 질환
비타민 D는 면역 체계의 조절 작용에서 중요한 역할을 합니다. 이는 감염 관련 질환을 통제하는 데 필수적입니다. 선행 연구에 따르면 호흡기 감염, 인간 면역결핍 바이러스(HIV), 결핵균(TB)은 혈중 비타민 D 농도 저하와 강한 연관성을 보였습니다(168). 주요 항균 단백질인 카텔리시딘은 침입한 병원체에 대한 단핵구의 방어 작용에 필수적인 것으로 알려져 있다(66). 비타민 D 수용체 신호전달은 이러한 세포에서 카텔리시딘 생산과 교차작용한다(169). 또한, 비타민 D-카텔리시딘 축은 위장관 감염을 예방하는 장 염증에 매우 중요하다(170). 비타민 D 수용체 신호전달에 대한 파네스 세포의 활성화도 광범위하게 연구되었다(171). 톨 유사 수용체 1/2(TLR 1/2)은 1,25-디하이드록시-비타민 D(비타민 D3)에 의해 활성화되어 조직 대식세포의 항균 효과를 유도하는 것으로 확인되었다(27). 이 미량영양소는 포유류 라파마이신 표적(mTOR) 신호전달을 통해 세포 자가포식을 강화함으로써 기도 시스템의 염증 완화에도 기여할 수 있다(67).
비타민 D 보충과 코로나바이러스 감염증(COVID-19) 같은 감염 예방에 관한 연구가 최근 다수 진행되었다(172–174). 그러나 결과는 여전히 상충된다. 결핵 감염과 관련하여, 8,851명의 어린이를 대상으로 한 대규모 무작위 임상시험이 수행되었다. 결론은 비타민 D가 위약보다 결핵 감염 위험에 대해 우월한 효과가 없다고 밝혔다(173). 반면, 일부 연구에서는 비타민 D 보충이 상기도 감염 위험을 유망하게 낮추는 영향을 보인다고 입증하였다(172, 174). 다양한 감염 유형의 발생률에 대한 비타민 D의 순 효과를 평가하기 위해서는 더 대규모의 정확한 연구가 여전히 절실히 요구된다.
Cancer
Cancers are among the most common and important immune system-related disorders in the world. They emerge from the dysfunction occurring in cell proliferation, differentiation, and apoptosis (9, 175). The association between the serum level of vitamin D and the risk of various cancers has been investigated several times in the past. Colorectal cancer (176), breast cancer (177), skin cancer (178), prostate cancer (179), liver cancer (180), and head and neck cancers (181) are some of the examples. According to Ma et al.’s study, high blood levels of vitamin D was correlated with a 33% reduction in the risk of colorectal cancer (182). Regarding head and neck neoplasms, high vitamin D serum levels decreased the incidence by 32% and also lowered the mortality risk in these patients (183).
VDR is upregulated in many tumor cells of different types of cancers. For instance, epigenetic studies indicated that in colorectal cancers, the adipose tissue overexpressed VDR. As we probably know, adipose tissue dysfunction is a vital mechanism underlying the emergence of colorectal cancer (184). This overexpression has been observed in prostate and ovarian cancers, too (179, 185). However, prior investigations have suggested that in some cases more VDR expression in tumor cells might lead to a better prognosis and treatment response (186, 187). Inflammation and immune response remained a matter of discussion in cancer progression and spreading (188). As mentioned, vitamin D has been identified to have a major impact on the regulation of inflammation, especially in microenvironments. The signaling might be activated or inhibited through two main pathways: MAP Kinase Phosphatase 5 (MKP5) and Nf-kB (9). The existing evidence revealed that vitamin D might upregulate the MKP5 in tumor cells causing MAPK inhibition and, following that, decreased production of IL-6 (189, 190). This resulted in the regulation of inflammatory response of the immune cells. Additionally, previous articles have stated that this important micronutrient could inhibit the activity of Nf-kB as the upstream compounds of another pro-inflammatory cytokine, IL-8, production (191). Also, the binding of Nf-kB to the DNA might be disturbed in the presence of vitamin D (68).
Concerning the use of vitamin D supplementation in preventing or treating distinct types of cancers, many randomized or non-randomized clinical trials have been conducted (9). A large randomized clinical trial with 25,871 patients revealed that vitamin D supplementation did not influence the incidence of invasive cancers (192). Also, another study on healthy postmenopausal women confirmed the inability of vitamin D in cancer prevention (193). On the other hand, some studies have suggested that vitamin D might improve the survival rate in patients suffering from cancer. Akiba et al. achieved favorable results regarding non-small cell lung cancers (194). Further large multicenter trials are absolutely required in order to finally build a consensus about this major issue.
암
암은 전 세계적으로 가장 흔하고 중요한 면역 체계 관련 질환 중 하나이다. 암은 세포 증식, 분화, 세포 사멸(아포토시스) 과정에서 발생하는 기능 장애에서 비롯된다(9, 175). 과거 여러 차례 혈청 비타민 D 수치와 다양한 암 발병 위험 간의 연관성이 연구되었습니다. 대장암(176), 유방암(177), 피부암(178), 전립선암(179), 간암(180), 두경부암(181) 등이 그 예입니다. Ma 등의 연구에 따르면, 혈중 비타민 D 수치가 높을수록 대장암 발병 위험이 33% 감소하는 것으로 나타났다(182). 두경부 신생물의 경우, 높은 혈청 비타민 D 수치는 발병률을 32% 감소시켰으며, 해당 환자군의 사망 위험도 낮췄다 (183).
VDR은 다양한 유형의 암에서 많은 종양 세포에서 상향 조절됩니다. 예를 들어, 후성유전학적 연구에 따르면 대장암에서 지방 조직이 VDR을 과발현하는 것으로 나타났습니다. 우리가 알고 있듯이, 지방 조직 기능 장애는 대장암 발생의 핵심 기전 중 하나입니다(184). 이러한 과발현은 전립선암과 난소암에서도 관찰되었습니다(179, 185). 그러나 선행 연구들은 일부 경우 종양 세포에서 더 높은 VDR 발현이 오히려 더 나은 예후와 치료 반응으로 이어질 수 있음을 시사했습니다(186, 187). 염증과 면역 반응은 암 진행 및 전이 과정에서 여전히 논쟁의 대상이었습니다(188). 앞서 언급한 바와 같이, 비타민 D는 특히 미세환경에서 염증 조절에 주요한 영향을 미치는 것으로 확인되었습니다. 이 신호 전달은 주로 두 가지 경로, 즉 MAP 키나제 인산화효소 5(MAP Kinase Phosphatase 5, MKP5)와 NF-κB(9)를 통해 활성화되거나 억제될 수 있습니다. 기존 증거에 따르면 비타민 D는 종양 세포에서 MKP5를 상향 조절하여 MAPK 억제를 유발하고, 그 결과 IL-6 생산이 감소할 수 있습니다(189, 190). 이는 면역 세포의 염증 반응 조절로 이어집니다. 또한, 이전 논문들은 이 중요한 미량영양소가 또 다른 친염증성 사이토카인인 IL-8 생성의 상류 화합물로서 NF-κB의 활성을 억제할 수 있다고 보고했습니다(191). 또한, 비타민 D가 존재할 경우 NF-κB의 DNA 결합이 방해받을 수 있습니다(68).
다양한 유형의 암 예방 또는 치료를 위한 비타민 D 보충제 사용과 관련하여, 다수의 무작위 또는 비무작위 임상 시험이 수행되었습니다(9). 25,871명의 환자를 대상으로 한 대규모 무작위 임상 시험에서는 비타민 D 보충이 침습성 암 발생률에 영향을 미치지 않는 것으로 나타났습니다 (192). 또한 건강한 폐경 후 여성을 대상으로 한 다른 연구에서도 비타민 D의 암 예방 효과가 확인되지 않았다(193). 반면 일부 연구에서는 비타민 D가 암 환자의 생존율을 향상시킬 수 있다고 제안했다. Akiba 등은 비소세포폐암에 대해 긍정적인 결과를 얻었다(194). 이 중대한 문제에 대한 최종적인 합의 도출을 위해서는 추가적인 대규모 다기관 임상시험이 반드시 필요하다.
Diabetes mellitus
Type 1 diabetes (T1D) is a prevalent disease across the globe with a combination of factors (genetic and environmental) as its causes. It is considered an autoimmune disease induced by a T cell-mediated mechanism in which dendritic cells (DC) and different pro-inflammatory cytokines play vital roles (195–197). On the other hand, studies are getting increasingly confident in the role of vitamin D deficiency in different autoimmune diseases (198–200). Therefore, vitamin D is discussed in many studies as a protective factor in developing T1D (201, 202).
The seasonal pattern of T1D and its various prevalence depending on latitude degree and ultraviolet B (UVB) irradiance support this association theory (203–209). Epidemiological studies show a trend of higher T1D incidents in adults and children suffering from vitamin D deficiency (196, 210–212). In addition, it is stated that there is an association between several polymorphisms of VD-related genes and T1D (196). Polymorphic expression of genes encoding vitamin D metabolizing enzymes, CYP27B1 as well as CYP2R1 and 7-dehydrocholesterol reductase (DHCR7), unlike CYP24A1 gene expression, has been suggested to be associated with T1D susceptibility (213–215). Although there is conflicting evidence regarding the association of VDR polymorphism with T1D (216, 217), Zhang et al. indicated that at least one of four VDR gene polymorphisms is linked with a higher possibility for T1D (218).
Multiple factors are involved in the vitamin D level impacting the immunopathogenesis of T1D and affecting both innate and acquired immunity (17, 195). During T1D development, islet autoantigens appear at the antigen-presenting cells (APCs) surface, including DCs and macrophages, which induce a cytotoxic T cell response (196). Vitamin D is produced by dendritic cells (DC) and also applies immunomodulatory effects toward self-tolerance in these cells (69, 219). As a matter of fact, almost all of the immune system cells express the VDR (220). The active form of vitamin D prevents the maturation of DCs. As a result, surface expression of major histocompatibility complex (MHC)-II and co-stimulatory molecules is hampered, and antigen presentation and T cell activation are stopped (70). Furthermore, this active form induces mature DCs apoptosis. Also, it differentiates them into a tolerogenic state. Therefore, regulatory T cells (Treg) are induced to a greater extent (221–223). Moreover, Mauf et al. suggested that 25-OH D3 shows its immunomodulatory effects by differentiating monocytes less into DCs and more into intermediate cells with similar phenotypes to those of tolerogenic DCs (69). Besides this indirect effect of vitamin D on T cells, they can be targeted directly, too (196). It is worth mentioning that vitamin D can also directly affect pancreatic beta cells and their insulin secretion, therefore making them more resistant (196).
As mentioned, vitamin D deficiency is considered an environmental risk factor for developing autoimmune diseases like T1D (212, 224). Therefore, many studies have evaluated its potential preventive or therapeutic effect (199, 210). It is demonstrated in animal models that the active form of vitamin D can perform immune modulation in diabetes-prone mice in several ways. Increasing Tregs, triggering a Th1/Th2 shift in the islets and the pancreatic draining lymph nodes, preserving defective T cell selection in the thymus, and eliminating apoptosis-resistant T cells are all parts of that immunomodulatory action (225–229). Apart from this non-antigen-specific immunomodulation, antigen-based immunotherapies for T1D are also reported (224). Several studies have discussed the protective immunological effect of vitamin D3 in T1D patients, especially T cell modulation (212, 230). Gabbay et al. reported a significant increase in Tregs upon 12 months of vitamin D3 supplementation in patients with recent-onset T1D (231). Also, Treiber et al. observed a significant increase in the suppressive function of Tregs after vitamin D3 supplementation for 12 months (232). Contradictory to these results, some studies show no meaningful protective effect of vitamin D (202, 233–236). That makes it crucial for future studies to better evaluate the disease intervention by assessing the administering of vitamin D, its exact compound choice, the dosage needed, and the ideal treatment regimen (224).
당뇨병
제1형 당뇨병(T1D)은 유전적 및 환경적 요인이 복합적으로 작용하는 전 세계적 유병 질환이다. 이는 수지상 세포(DC)와 다양한 전염증성 사이토카인이 핵심 역할을 하는 T 세포 매개 기전에 의해 유발되는 자가면역 질환으로 간주된다(195–197). 한편, 비타민 D 결핍이 다양한 자가면역 질환에 미치는 역할에 대한 연구 결과는 점차 확신을 얻고 있다(198–200). 따라서 비타민 D는 T1D 발병을 예방하는 보호 인자로서 많은 연구에서 논의되고 있다(201, 202).
제1형 당뇨병의 계절적 패턴과 위도 및 자외선 B(UVB) 조사량에 따른 다양한 유병률은 이러한 연관성 이론을 뒷받침합니다(203–209). 역학 연구에 따르면 비타민 D 결핍을 겪는 성인 및 소아에서 제1형 당뇨병 발생률이 더 높은 경향이 나타납니다(196, 210–212). 또한, 비타민 D 관련 유전자의 여러 다형성과 제1형 당뇨병 사이에 연관성이 있다고 보고되었습니다(196). 비타민 D 대사 효소인 CYP27B1, CYP2R1 및 7-데하이드로콜레스테롤 환원효소(DHCR7)를 암호화하는 유전자의 다형성 발현은 CYP24A1 유전자 발현과 달리 제1형 당뇨병(T1D) 감수성과 연관될 수 있다고 제안되었습니다(213–215). 비타민 D 수용체(VDR) 다형성과 제1형 당뇨병(T1D)의 연관성에 대해서는 상반된 증거가 존재하지만(216, 217), 장(Zhang) 등은 네 가지 VDR 유전자 다형성 중 적어도 하나가 T1D 발병 가능성 증가와 연관되어 있음을 시사하였다(218).
비타민 D 수치는 T1D의 면역병리 발생에 영향을 미치며 선천적 및 후천적 면역 모두에 관여하는 다중 요인에 의해 조절된다(17, 195). T1D 발병 과정에서, DC 및 대식세포를 포함한 항원제시세포(APC) 표면에 섬자동항원이 나타나 세포독성 T 세포 반응을 유도한다(196). 비타민 D는 수지상세포(DC)에서 생성되며, 이들 세포에서 자가내성(self-tolerance)을 향한 면역조절 효과도 발휘한다(69, 219). 사실상 거의 모든 면역계 세포는 VDR(비타민 D 수용체)을 발현한다(220). 활성형 비타민 D는 DC의 성숙을 억제한다. 그 결과, 주요 조직적합성 복합체(MHC)-II 및 공동자극 분자의 표면 발현이 저해되어 항원 제시와 T 세포 활성화가 중단된다(70). 또한 이 활성형은 성숙한 DC의 세포사멸을 유도한다. 또한 DC를 내성 유도 상태로 분화시킵니다. 따라서 조절 T 세포(Treg)가 더 많이 유도됩니다(221–223). 더욱이 Mauf 등은 25-OH D3가 단핵구를 DC로 분화시키는 것을 억제하고 내성 유도 DC와 유사한 표현형을 가진 중간 세포로 더 많이 분화시킴으로써 면역 조절 효과를 나타낸다고 제안했습니다(69). 비타민 D가 T 세포에 미치는 이러한 간접적 효과 외에도, T 세포를 직접 표적으로 삼을 수도 있습니다(196). 비타민 D가 췌장 베타 세포와 그 인슐린 분비에도 직접 영향을 미쳐 내성을 높일 수 있다는 점은 주목할 만합니다(196).
앞서 언급한 바와 같이, 비타민 D 결핍은 제1형 당뇨병(T1D)과 같은 자가면역 질환 발병의 환경적 위험 요인으로 간주됩니다(212, 224). 따라서 많은 연구에서 비타민 D의 잠재적 예방 또는 치료 효과를 평가해 왔습니다(199, 210). 동물 모델 연구에서 활성형 비타민 D가 당뇨병 발병 경향 마우스에서 여러 방식으로 면역 조절을 수행할 수 있음이 입증되었습니다. 조절 T세포(Tregs) 증가, 섬 및 췌장 배액 림프절에서의 Th1/Th2 전환 유도, 흉선에서의 결함 있는 T세포 선택 보존, 그리고 세포사멸 저항성 T세포 제거 등이 모두 이러한 면역조절 작용의 일부이다(225–229). 이러한 비항원특이적 면역조절 외에도, 제1형 당뇨병을 위한 항원 기반 면역요법도 보고되었다(224). 여러 연구에서 비타민 D3의 T1D 환자 보호적 면역학적 효과, 특히 T 세포 조절에 대해 논의하였다(212, 230). Gabbay 등은 최근 발병한 T1D 환자에서 12개월간 비타민 D3 보충 후 Tregs가 유의미하게 증가했다고 보고하였다(231). 또한 Treiber 등은 12개월간 비타민 D3 보충 후 Treg의 억제 기능이 유의미하게 증가하는 것을 관찰했다(232). 이러한 결과와 상반되게, 일부 연구에서는 비타민 D의 의미 있는 보호 효과가 나타나지 않았습니다(202, 233–236). 따라서 향후 연구에서는 비타민 D 투여 방식, 정확한 화합물 선택, 필요한 용량, 이상적인 치료 요법을 평가하여 질병 개입 효과를 더 잘 평가하는 것이 중요합니다(224).
Inflammatory bowel disease
Inflammatory bowel diseases (IBD) are a group of chronic immune-mediated diseases, with ulcerative colitis and Crohn’s disease being the most renowned ones. Several studies have shown that the prevalence of vitamin D deficiency in patients with IBD is higher than in a healthy population (237–242). Although it has not been precisely determined that this difference is a cause or consequence of the disease, it has drawn attention to the possible impacts of vitamin D on the etiology and course of the disease. In addition to human studies, in vitro and in vivo model analysis put forward three possible mechanisms that vitamin D may affect the onset and progression of IBD.
Gut microbiota may be another target for vitamin D to ameliorate the IBD course or even prevent its onset (243, 244). These bacteria exert their effects through different metabolites. Butyrate is one of these metabolites, which, in addition to being an energy substrate for mucosal cells, accelerates epithelium healing (245, 246). Lithocholic acid, another bacterial metabolite, suppresses IL-2 production and subsequently decreases inflammation (247). It is worth noting that vitamin D and microbiota have a bidirectional interaction which means microbiota can also utilize vitamin D downstream pathways (248–250).
Vitamin D can target B cells, T cells, dendritic cells, and macrophages throughout innate and acquired immune systems, considering they all express VDR (251). In vivo and in vitro studies suggest that vitamin D is able to enhance the expression of IL-10 in dendritic cells and the production of cathelicidin by macrophages (71, 252). In contrast, toll-like receptors and IL-12 expression in macrophages and dendritic cells are inhibited by the activated form of vitamin D (29, 253). This inhibition leads to less dendritic cell-induced activation of T cells. Besides, vitamin D can directly suppress B and T cell proliferation (50). Vitamin D was able to interfere in inflammatory/anti-inflammatory production balance, resulting in reduced production of T cell-inflammatory cytokines, including IL-2, interferon (IFN)-γ, IL-17, and TNF-α, and enhanced anti-inflammatory cytokines production such as IL-10 by regulatory T cells and IL-4 by Th2 cells (50, 254–256). Overall, the induction of regulatory cells like Tregs and CD8αα was increased (255, 257).
Various human studies have suggested a positive effect on different outcomes from vitamin D supplementation in IBD patients. Reduced disease activity, decreased risk of postoperative endoscopic recurrence, lower clinical activity score, lower relapse rate, and improved odds of remission were reported by different studies (258–263). One study even reported vitamin D effects on all-cause mortality (264). However, not all evidence is in favor of the preventative effects of vitamin D (265). One RCT concluded no difference in CRP, fecal calprotectin, Crohn’s disease activity index (CDAI), and quality of life between supplemented and control groups (266). At the same time, another RCT showed only a non-significant lower relapse rate in the experimental group (267). Three meta-analyses of different RCTs were conducted. Two established that vitamin D supplementation improves clinical and biochemical disease activity scores, while the third did not report such improvements (261, 268, 269). Further investigations can reveal more aspects of the complex relationship between IBD and vitamin D.
염증성 장 질환
염증성 장 질환(IBD)은 만성 면역 매개 질환군으로, 궤양성 대장염과 크론병이 가장 잘 알려져 있다. 여러 연구에서 IBD 환자의 비타민 D 결핍 유병률이 건강한 인구보다 높다는 사실이 확인되었다(237–242). 이러한 차이가 질병의 원인인지 결과인지는 정확히 규명되지 않았으나, 비타민 D가 질병의 발병 기전과 경과에 미칠 수 있는 영향에 대한 관심을 불러일으켰습니다. 인간 연구 외에도 in vitro 및 in vivo 모델 분석을 통해 비타민 D가 IBD의 발병 및 진행에 영향을 미칠 수 있는 세 가지 가능한 메커니즘이 제시되었습니다.
장내 미생물 군집은 비타민 D가 IBD 경과를 완화하거나 발병 자체를 예방할 수 있는 또 다른 표적이 될 수 있다(243, 244). 이러한 박테리아는 다양한 대사 산물을 통해 효과를 발휘한다. 부티레이트는 이러한 대사 산물 중 하나로, 점막 세포의 에너지 기질 역할을 할 뿐만 아니라 상피 세포의 치유를 촉진한다(245, 246). 또 다른 세균 대사산물인 리토콜산은 IL-2 생성을 억제하여 염증을 감소시킵니다(247). 주목할 점은 비타민 D와 미생물군집이 양방향 상호작용을 한다는 것으로, 이는 미생물군집 또한 비타민 D의 하류 경로를 활용할 수 있음을 의미합니다(248–250).
비타민 D는 선천적 및 후천적 면역 체계 전반에 걸쳐 B 세포, T 세포, 수지상 세포, 대식세포를 표적으로 삼을 수 있는데, 이는 이들 모두 VDR(비타민 D 수용체)을 발현하기 때문이다(251). 생체 내(in vivo) 및 시험관 내(in vitro) 연구에 따르면 비타민 D는 수지상 세포에서 IL-10 발현을 증가시키고 대식세포의 카텔리시딘 생성을 촉진할 수 있다(71, 252). 반면, 활성화된 형태의 비타민 D는 대식세포와 수지상 세포에서 톨 유사 수용체(TLR) 및 IL-12 발현을 억제합니다(29, 253). 이 억제는 수지상 세포에 의한 T 세포 활성화 감소로 이어집니다. 또한 비타민 D는 B 세포와 T 세포 증식을 직접 억제할 수 있습니다(50). 비타민 D는 염증성/항염증성 사이토카인 생산 균형에 개입하여, T 세포 염증성 사이토카인(IL-2, 인터페론(IFN)-γ, IL-17, TNF-α 등) 생산을 감소시키고, 조절 T 세포의 IL-10 및 Th2 세포의 IL-4와 같은 항염증성 사이토카인 생산을 증가시킬 수 있다(50, 254–256). 전반적으로 Tregs 및 CD8αα와 같은 조절 세포의 유도가 증가했습니다 (255, 257).
다양한 인간 연구에서 비타민 D 보충이 IBD 환자의 여러 결과에 긍정적 영향을 미친다는 것이 제안되었습니다. 여러 연구에서 질병 활동성 감소, 수술 후 내시경적 재발 위험 감소, 임상 활동 점수 저하, 재발률 감소, 관해 확률 개선이 보고되었습니다(258–263). 한 연구에서는 비타민 D가 모든 원인에 의한 사망률에 미치는 영향까지 보고했습니다(264). 그러나 모든 증거가 비타민 D의 예방 효과를 지지하는 것은 아니다(265). 한 무작위 대조 시험(RCT)은 보충군과 대조군 간에 C반응성 단백질(CRP), 분변 칼프로텍틴, 크론병 활동 지수(CDAI), 삶의 질에 차이가 없다고 결론지었다(266). 동시에 다른 RCT는 실험군에서 재발률이 유의미하지 않게 낮았을 뿐이라고 보고했다(267). 서로 다른 RCT를 대상으로 한 세 건의 메타분석이 수행되었습니다. 두 연구는 비타민 D 보충이 임상적 및 생화학적 질환 활동 점수를 개선한다고 입증한 반면, 세 번째 연구는 그러한 개선을 보고하지 않았습니다(261, 268, 269). 추가 연구를 통해 IBD와 비타민 D 사이의 복잡한 관계에 대한 더 많은 측면을 밝혀낼 수 있을 것입니다.
Conclusion
Studies have shown a strong correlation between vitamin D and the innate and adaptive immune systems, suggesting that low vitamin D levels may contribute to immune response dysregulation. However, in recent years, the precise function of the alternate pathways of vitamin D and its receptor has not yet been sufficiently elucidated. We all need to be aware of what these signaling pathways do in various immune system components. Reviews of the literature revealed that, during the past 40 years, a number of studies have been conducted to suggest the protective effect of vitamin D in autoimmune illnesses. Randomized controlled clinical trials are still lacking, though, in this area. Larger clinical investigations will now be necessary to determine the precise impact of vitamin D supplementation on the pathophysiology of different diseases. Of the immunomodulatory treatments now on the market, they might be as effective as the others. Additionally, the right supplement dosage and manner of administration must be determined. But for present approaches to preventing diseases brought on by compromised immune-homeostasis, vitamin D has emerged as a potential and relatively safe supplement.
결론
연구들은 비타민 D와 선천적 및 후천적 면역 체계 간의 강한 상관관계를 보여주며, 낮은 비타민 D 수치가 면역 반응 조절 장애에 기여할 수 있음을 시사한다. 그러나 최근까지도 비타민 D와 그 수용체의 대체 경로의 정확한 기능은 아직 충분히 규명되지 않았다. 우리는 이러한 신호 전달 경로가 다양한 면역 체계 구성 요소에서 어떤 역할을 하는지 모두 인지해야 합니다. 문헌 검토 결과, 지난 40년간 자가면역 질환에서 비타민 D의 보호 효과를 시사하는 다수의 연구가 수행된 것으로 나타났습니다. 그러나 이 분야에서는 여전히 무작위 대조 임상시험이 부족합니다. 이제 비타민 D 보충이 다양한 질환의 병리생리학에 미치는 정확한 영향을 규명하기 위해 대규모 임상 연구가 필요할 것이다. 현재 시판 중인 면역조절 치료제들 중 비타민 D 보충제가 다른 치료제들만큼 효과적일 수 있다. 또한 적절한 보충제 용량과 투여 방식도 결정되어야 한다. 그러나 면역 항상성 손상으로 유발되는 질환을 예방하기 위한 현재의 접근법에서, 비타민 D는 잠재적이고 상대적으로 안전한 보충제로 부상하고 있다.
Author contributions
AR: Study design, searching databases, writing manuscript, final revise. AG: searching databases, writing manuscript, final revise. AS: writing manuscript, final revise. BS: writing manuscript, final revise. MM: writing manuscript, final revise. AD: writing manuscript, final revise. GS: study design, supervising all steps, resolving conflicts, final revise. All authors contributed to the article and approved the submitted version.
Conflict of interest
The authors declare that the research was conducted in the absence of any commercial or financial relationships that could be construed as a potential conflict of interest.
Publisher’s note
All claims expressed in this article are solely those of the authors and do not necessarily represent those of their affiliated organizations, or those of the publisher, the editors and the reviewers. Any product that may be evaluated in this article, or claim that may be made by its manufacturer, is not guaranteed or endorsed by the publisher.
References
- 1. Taene A, Niazi S, Bijari B, Esmaeili S, Anani sarab G. Prevalence of vitamin d deficiency and its related factors in AqQala city in 2016. J Birjand Univ Med Sci (2017) 24(2):108–16. [Google Scholar]
- 2. Chirumbolo S, Bjørklund G, Sboarina A, Vella A. The role of vitamin d in the immune system as a pro-survival molecule. Clin Ther (2017). doi: 10.1016/j.clinthera.2017.03.021 [DOI] [PubMed] [Google Scholar]
- 3. Janssen HC, Samson MM, Verhaar HJ. Vitamin d deficiency, muscle function, and falls in elderly people. Am J Clin Nutr (2002) 75(4):611–5. doi: 10.1093/ajcn/75.4.611 [DOI] [PubMed] [Google Scholar]
- 4. Pilz S, Tomaschitz A, Obermayer-Pietsch B, Dobnig H, Pieber TR. Epidemiology of vitamin d insufficiency and cancer mortality. Anticancer Res (2009) 29(9):3699–704. [PubMed] [Google Scholar]
- 5. Judd SE, Tangpricha V. Vitamin d deficiency and risk for cardiovascular disease. Am J Med Sci (2009) 338(1):40–4. doi: 10.1097/MAJ.0b013e3181aaee91 [DOI] [PMC free article] [PubMed] [Google Scholar]
- 6. Shoenfeld N, Amital H, Shoenfeld Y. The effect of melanism and vitamin d synthesis on the incidence of autoimmune disease. Nat Clin Pract Rheumatol (2009) 5(2):99–105. doi: 10.1038/ncprheum0989 [DOI] [PubMed] [Google Scholar]
- 7. Adams JS, Liu PT, Chun R, Modlin RL, Hewison M. Vitamin d in defense of the human immune response. Ann N Y Acad Sci (2007) 1117:94–105. doi: 10.1196/annals.1402.036 [DOI] [PubMed] [Google Scholar]
- 8. Nnoaham KE, Clarke A. Low serum vitamin d levels and tuberculosis: a systematic review and meta-analysis. Int J Epidemiol (2008) 37(1):113–9. doi: 10.1093/ije/dym247 [DOI] [PubMed] [Google Scholar]
- 9. El-Sharkawy A, Malki A. Vitamin d signaling in inflammation and cancer: molecular mechanisms and therapeutic implications. Molecules (Basel Switzerland) (2020) 25(14). doi: 10.3390/molecules25143219 [DOI] [PMC free article] [PubMed] [Google Scholar]
- 10. Valcour A, Blocki F, Hawkins DM, Rao SD. Effects of age and serum 25-OH-vitamin d on serum parathyroid hormone levels. J Clin Endocrinol Metab (2012) 97(11):3989–95. doi: 10.1210/jc.2012-2276 [DOI] [PubMed] [Google Scholar]
- 11. LeBlanc ES, Zakher B, Daeges M, Pappas M, Chou R. Screening for vitamin d deficiency: a systematic review for the U. S. Prev Serv Task Force. Ann Internal Med (2015) 162(2):109–22. doi: 10.7326/M14-1659 [DOI] [PubMed] [Google Scholar]
- 12. Gillespie LD, Robertson MC, Gillespie WJ, Sherrington C, Gates S, Clemson LM, et al. Interventions for preventing falls in older people living in the community. Cochrane Database systematic Rev (2012) 2012(9):Cd007146. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 13. Harrison SR, Li D, Jeffery LE, Raza K, Hewison M. Vitamin d, autoimmune disease and rheumatoid arthritis. Calcified Tissue Int (2020) 106(1):58–75. doi: 10.1007/s00223-019-00577-2 [DOI] [PMC free article] [PubMed] [Google Scholar]
- 14. Lamberg-Allardt C. Vitamin d in foods and as supplements. Prog biophysics Mol Biol (2006) 92(1):33–8. doi: 10.1016/j.pbiomolbio.2006.02.017 [DOI] [PubMed] [Google Scholar]