
Front Genet
. 2022 Jan 3;12:781597. doi: 10.3389/fgene.2021.781597
A Comprehensive Review of the Therapeutic Value of Urine-Derived Stem Cells
Qian Zhou 1,†, Yiyu Cheng 1,†, Fang Sun 1,†, Jie Shen 1, M I Nasser 2, Ping Zhu 2, Xueyan Zhang 1, Yuxiang Li 3, Guangming Yin 3,*, Yuequn Wang 4,*, Xiushan Wu 2,4,*, Mingyi Zhao 1,2,*
- Author information
- Article notes
- Copyright and License information
PMCID: PMC8762167 PMID: 35047009
Abstract
Stem cells possess regenerative powers and multidirectional differentiation potential and play an important role in disease treatment and basic medical research. Urine-derived stem cells (USCs) represent a newly discovered type of stem cell with biological characteristics similar to those of mesenchymal stromal cells (MSCs), including their doubling time and immunophenotype. USCs are noninvasive and can be readily obtained from voided urine and steadily cultured. Based on advances in this field, USCs and their secretions have increasingly emerged as ideal sources. USCs may play regulatory roles in the cellular immune system, oxidative stress, revascularization, apoptosis and autophagy. This review summarizes the applications of USCs in tissue regeneration and various disease treatments. Furthermore, by analysing their limitations, we anticipate the development of more feasible therapeutic strategies to promote USC-based individualized treatment.
초록
줄기세포는
재생 능력과 다방향 분화 잠재력을 갖추고 있으며,
질병 치료와 기초 의학 연구에서 중요한 역할을 합니다.
소변 유래 줄기세포(USCs)는
중간엽 줄기세포(MSCs)와 유사한 생물학적 특성을 가진
새로운 유형의 줄기세포로, 증식 시간과 면역형질 등이 유사합니다.
USCs는
비침습적이며 배뇨된 소변에서 쉽게 얻을 수 있으며 안정적으로 배양 가능합니다.
이 분야의 진전에 따라 USCs와 그 분비물은
이상적인 소스로서 주목받고 있습니다.
USC는
세포 면역 체계, 산화 스트레스, 혈관 재형성, 세포 사멸 및 자가포식에서 조절 역할을 할 수 있습니다.
이 리뷰는
조직 재생 및 다양한 질병 치료에 USC의 응용을 요약합니다.
또한, USC의 한계를 분석하여 USC 기반의 개별화된 치료를 촉진하기 위한 보다
실용적인 치료 전략의 개발을 기대합니다.
Keywords: urine-derived stem cells, multiple differentiation, molecular mechanisms, disease treatment, drug discovery, tissue engineering
Introduction
Stem cells, including embryonic stem cells (ESCs), adult stem cells (ASCs) and induced pluripotent stem cells (iPSCs), have increasingly emerged as research hot spots due to their roles in sustaining tissue homeostasis and regeneration and promoting tissue repair and responses (Daley, 2015; Dayem et al., 2020). Although significant progress has been made in stem cell research, ESC applications are still limited by ethical and tumour formation issues. Nevertheless, ASCs have gradually attracted increasing attention because they have expanded our understanding of disease pathogeneses. Multiple types of ASCs have been identified, such as mesenchymal stem cells (MSCs) and haematopoietic stem cells (HSCs). Among them, MSCs are an important type of ASC that can be separated from human bone marrow (Baker et al., 2015), adipose tissue (Mazini et al., 2020) and urine (Liu et al., 2021). Bone marrow-derived mesenchymal stem cells (BMSCs), adipose tissue-derived stem cells (ADSCs) and urine-derived stem cells (USCs), all of which have been demonstrated to be capable of self-renewal and multidirectional differentiation, regenerate corresponding tissues, such as functional bone, muscle, nerve, and endothelial tissue (Zhang et al., 2014). Among ADSCs, BMSCs and USCs, USCs have been noted to exhibit a higher proliferative rate and vascularization potential and to have better adipogenic, myogenic, neurogenic and endothelial differentiation potential with high efficiency; moreover, the collection of USCs is advantageously noninvasive and inexpensive (Kang et al., 2015; Wu et al., 2018). Therefore, the study of USCs could be of great value.
USCs were first identified by Zhang et al. (2008), and their autologous application represents a novel breakthrough in stem cell research. USCs exhibit a strong proliferation ability and are capable of multidirectional differentiation from MSCs isolated from urine. USCs can be isolated directly from urine by centrifugation and inoculated into culture medium, which is a simple, inexpensive and noninvasive procedure, while the overwhelming majority of ASCs (such as BMSCs and ADSCs) require invasive and painful collection procedures, which could be problematic for donors (Brown et al., 2019). In addition, a study found that a single cell can form 5–7 cell clones/100 ml urine at 2–3 days and then individually expanded to a large number of USCs due to their higher telomerase activity and long telomeres (Bharadwaj et al., 2013; Lang et al., 2013). USCs can be broadly applied to facilitate cutaneous regeneration and wound healing, attenuate osteoporosis, etc., (Chen et al., 2018a; Chen et al., 2019). Additionally, USCs have mesodermal differentiation potential and can differentiate into osteoblasts (OBs) or lipid-forming cells (Kim et al., 2020a). USCs have great potential and can produce donor-specific autologous cells for the repair of various tissues and the maintenance of organ functional integrity, thereby compensating for the shortcomings and deficiencies of existing treatment methods. For example, the current treatment options for patients with organ failure, such as drug therapies (Feng et al., 2020) and temporary replacement therapies (Dalal, 2015), are limited by objective factors. Especially in organ transplantation, in addition to the limited sources of organs, the subsequent need for long-term treatment with immunosuppressive agents to prevent immune rejection can have potentially fatal complications. Furthermore, autologous tissue transplantation is commonly utilized without immune rejection. In general, USCs have a wide range of potential applications in clinical cell therapy.
Similarly, most studies have shown that USCs exert therapeutic effects via paracrine mechanisms, which can be activated by extracellular vesicles (EVs), including exosomes and microvesicles. Jiang et al. first extracted exosomes from USCs after finding spherical vesicles that were approximately 50–100 nm in size (Jiang et al., 2016). Subsequently, Liu et al. found that these exosomes had the potential to facilitate angiogenesis and promote cell survival by producing growth factor (GF) and transforming growth factor-β1 (TGF-β1) (Liu and Wu, 2020). Studies have shown that, compared with USC implantation, USC-EV implantation has similar or even better therapeutic effects and that these cells possess the immune-privileged characteristics of their original cells. Moreover, USC-EVs are easier to store and manage and have a lower risk of tumour formation. USC-EV treatment is a superior strategy due to their efficacy, convenience and safety (Basu and Ludlow, 2016). Additionally, USC-derived induced pluripotent stem cells (USC-iPSCs) have recently become a hot research topic. These cells have been reprogrammed by retroviruses, mRNA transfection, and Sendai viruses, as exhibited by their high expression of the pluripotent genes SOX2, OCT4, NANOG, and CRIPTO/TDGF1 (Wang et al., 2017a; Cao et al., 2018; Kim et al., 2020b). Thus far, USC-iPSCs have been reported to rapidly proliferate and efficiently differentiate into many cell types with higher yields and less immunological rejection, mainly in endocrine systems (Guo et al., 2017a; Guo et al., 2017b) and digestive systems (Niemietz et al., 2016). In addition, USC-iPSCs can potentially be used to establish disease models based on their ability to provide an unlimited source of cells with the same genes as diseased cells (Fus-Kujawa et al., 2021). However, iPSCs are characterized by genetic instability and self-renewal ability, especially in regards to undifferentiated pluripotent stem cells forming tumours in the body, which is particularly worrying. In response to this problem, Ben-David et al. proposed the use of a small molecule targeting stearoyl-CoA desaturase 1. The molecule can selectively induce the death of undifferentiated iPSCs/ESCs and may be an effective therapeutic strategy with an improved safety profile. However, current research on the risk of using USC-iPSCs is limited, and these cells may become the focus of future research (Ben-David et al., 2013; Barreca et al., 2020). In the future, USC-iPSC-based treatment could potentially benefit humans.
Since the identification of their biological characteristics, USCs have been shown to be extracted easily and are regarded as an economical, convenient, and safe cell source with strong proliferation characteristics and in vitro multilineage differentiation potential. Here, we provide an overview of up-to-date studies investigating USCs and their therapeutic value in various diseases.
Isolation and Culture of USCsExtraction of USCs
USCs were isolated by conventional centrifugation, and the impure cells were removed gradually. Tayhan et al. noted that air-isolated, cryopreserved urine from healthy young adults was the best sample for the extraction of fresh USCs. While some initial studies reported that USCs could not be extracted from diabetic patients (Tayhan et al., 2017), the latest research confirms that they can indeed be successfully extracted from these patients but that their regenerative ability is significantly reduced and they thus cannot be used for treatment (Xiong et al., 2019a). Therefore, appropriate sample selection is the premise for USC extraction. After the proper samples are collected, penicillin or streptomycin is added to reduce contamination. At room temperature, USCs can be isolated by centrifugation at 400 ×g for 10 min. Then, the supernatant is discarded, and the sample is washed twice with PBS and resuspended. Since urine contains different types of cells, it is necessary to identify the separated components after separation. The International Society for Cellular Therapy (ISCT) proposed that MSCs be identified by the following markers: 1) the cells can adhere to plastic culture bottles; 2) at least 95% of the cell population expresses specific surface antigens, including CD105, CD73 and CD90, and do not express CD45, CD34, CD14, CD11b, CD79α, CD19 or HLA-II antigens; and 3) the cells can be differentiated into OBs, chondroblasts and adipocytes under appropriate conditions (Dominici et al., 2006). Because USCs meet the criteria for MSCs, isolated USCs may express similar typical surface markers, such as CD29, CD44, CD54, CD73, CD90, CD166 and STRO-1 (Bharadwaj et al., 2013; Li et al., 2020; Xiang et al., 2020). In addition, pericyte (CD146) (Bharadwaj et al., 2013), epithelial (E-cadherin, claudin 1 and occludin), fibroblast (vimentin and fibronectin) and renal epithelial (L1CAM and NR3C2) (Kim et al., 2020b) markers are expressed in USCs.
소개
줄기세포는
배아 줄기세포(ESCs), 성인 줄기세포(ASCs), 유도 만능 줄기세포(iPSCs) 등을 포함하며,
조직 항상성 유지 및 재생, 조직 수리 및 반응 촉진 역할로 인해 연구의 주요 주제로 부상해 왔습니다
(Daley, 2015; Dayem et al., 2020).
줄기세포 연구에서 상당한 진전이 이루어졌지만,
ESC의 응용은 윤리적 문제와 종양 형성 문제로 인해 여전히 제한적입니다.
그럼에도 불구하고
ASC는 질병 병리 메커니즘에 대한 이해를 확장시켰기 때문에 점차 주목받고 있습니다.
다양한 유형의 ASC가 식별되었으며,
그 중 골수 유래 간엽 줄기세포(MSCs)와
혈액 생성 줄기세포(HSCs)가 대표적입니다.
이 중 MSC는
인간 골수(Baker et al., 2015),
지방 조직(Mazini et al., 2020) 및
소변(Liu et al., 2021)에서 분리될 수 있는 중요한 유형의 ASC입니다.
골수 유래 중간엽 줄기세포(BMSCs),
지방 조직 유래 줄기세포(ADSCs) 및
소변 유래 줄기세포(USCs)는
모두 자기 재생 능력과 다방향 분화 능력을 갖추고 있으며,
기능적 뼈, 근육, 신경 및 내피 조직과 같은 대응 조직을 재생하는 것으로 입증되었습니다(Zhang et al., 2014).
ADSCs, BMSCs 및 USCs 중 USCs는
더 높은 증식 속도와 혈관 형성 잠재력을 보이며,
지방 분화, 근육 분화, 신경 분화 및 내피 분화 잠재력이 높고 효율성이 우수합니다.
또한 USCs의 수집은
비침습적이고 비용이 저렴하다는 장점이 있습니다(Kang et al., 2015; Wu et al., 2018).
따라서
USCs의 연구는 큰 가치를 가질 수 있습니다.
USCs는 Zhang et al. (2008)에 의해 처음 식별되었으며,
그 자가 이식 적용은 줄기세포 연구에서 새로운 돌파구를 마련했습니다.
USCs는
강한 증식 능력을 보여주며,
소변에서 분리된 MSCs로부터 다방향 분화 능력을 갖추고 있습니다.
USCs는
소변에서 원심분리만으로 직접 분리되어 배양 매체에 접종될 수 있으며,
이는 단순하고 비용이 적으며 비침습적인 절차입니다.
반면
대부분의 ASCs(예: BMSCs 및 ADSCs)는
침습적이고 통증 동반되는 수집 절차가 필요하며,
이는 기증자에게 문제가 될 수 있습니다(Brown et al., 2019).
또한 연구 결과,
단일 세포가 2~3일 내에 소변 100ml당 5~7개의 세포 클론을 형성하며,
높은 텔로머라제 활성과 긴 텔로머르로 인해
개별적으로 대규모 USC로 확장될 수 있음을 확인했습니다(Bharadwaj et al., 2013; Lang et al., 2013).
USCs는
피부 재생 및 상처 치유 촉진, 골다공증 완화 등에
광범위하게 적용될 수 있습니다(Chen et al., 2018a; Chen et al., 2019).
또한
USCs는
중간엽 분화 잠재력을 갖추고 있어
골세포(OBs) 또는 지질 형성 세포로 분화될 수 있습니다(Kim et al., 2020a).
USCs는
다양한 조직의 복구와 장기 기능적 완전성 유지에 필요한
기증자 특이적 자가 세포를 생산할 수 있어
기존 치료법의 한계와 결점을 보완할 수 있는 큰 잠재력을 가지고 있습니다.
예를 들어,
장기 기능 장애 환자의 현재 치료 옵션인
약물 치료(Feng et al., 2020)와 일시적 대체 치료(Dalal, 2015)는
객관적 요인에 의해 제한됩니다.
특히 장기 이식 분야에서 장기 공급원의 한계 외에도
면역 거부 반응을 방지하기 위해 장기 투여가 필요한 면역 억제제 사용은
잠재적으로 치명적인 합병증을 유발할 수 있습니다.
또한
자가 조직 이식은
면역 거부 반응 없이 일반적으로 활용됩니다.
일반적으로
USCs는
임상 세포 치료 분야에서 광범위한 잠재적 응용 가능성을 가지고 있습니다.
同様に, 대부분의 연구는
USCs가 파라크라인 메커니즘을 통해 치료 효과를 발휘하며,
이는 엑소좀과 미세소포체 등 세포외 소포체(EVs)에 의해 활성화될 수 있음을 보여주었습니다.
Jiang 등(Jiang et al., 2016)은
USCs에서 약 50–100 nm 크기의 구형 소포체를 발견한 후
엑소좀을 추출했습니다(Jiang et al., 2016).
이후 Liu 등(Liu and Wu, 2020)은 이러한 엑소좀이
성장 인자(GF)와 변형 성장 인자-β1(TGF-β1)을 생성하여
혈관新生을 촉진하고 세포 생존을 증진시키는 잠재력을 가지고 있음을 발견했습니다.
연구 결과,
USC 이식 대비 USC-EV 이식은
유사하거나 더 우수한 치료 효과를 보이며,
이러한 세포는 원천 세포의 면역 특권 특성을 유지한다는 것이 밝혀졌습니다.
또한 USC-EV는
보관 및 관리가 용이하며
종양 형성 위험이 낮습니다.
USC-EV 치료는
효능, 편의성 및 안전성 측면에서 우수한 전략입니다(Basu and Ludlow, 2016).
또한
USC 유래 유도 만능 줄기세포(USC-iPSCs)는
최근 뜨거운 연구 주제로 부상했습니다.
이 세포들은
레트로바이러스, mRNA 전사, 센다이 바이러스 등을 통해 재프로그래밍되었으며,
다능성 유전자 SOX2, OCT4, NANOG, CRIPTO/TDGF1의 높은 발현을 보여줍니다
(Wang et al., 2017a; Cao et al., 2018; Kim et al., 2020b).
현재까지 USC-iPSCs는
내분비계(Guo et al., 2017a; Guo et al., 2017b)와 소화계(Niemietz et al., 2016)에서
높은 수율과 낮은 면역 거부 반응으로
다양한 세포 유형으로 효율적으로 분화되며 빠르게 증식하는 것으로 보고되었습니다.
또한 USC-iPSCs는
질병 세포와 동일한 유전자를 가진 무한한 세포 공급원을 제공할 수 있는 능력으로 인해
질병 모델을 구축하는 데 잠재적으로 활용될 수 있습니다 (Fus-Kujawa et al., 2021).
그러나
iPSCs는 유전적 불안정성과 자기 재생 능력으로 특징지어지며,
특히 체내에서 종양을 형성하는 미분화 다능성 줄기세포와 관련하여
이는 특히 우려스러운 문제입니다.
이 문제에 대응하여 Ben-David 등(2013)은 스테아로일-코엔자임 A 탈수소효소 1을 표적하는 소분자의 사용을 제안했습니다. 이 분자는 미분화 iPSCs/ESCs의 선택적 사멸을 유도할 수 있으며, 개선된 안전성 프로파일을 갖춘 효과적인 치료 전략이 될 수 있습니다. 그러나 USC-iPSC 사용의 위험성에 대한 현재 연구는 제한적이며, 이러한 세포는 미래 연구의 초점이 될 수 있습니다 (Ben-David et al., 2013; Barreca et al., 2020). 미래에는 USC-iPSC 기반 치료법이 인간에게 잠재적인 혜택을 제공할 수 있습니다.
생물학적 특성이 확인된 이후로 USCs는 쉽게 추출 가능하며, 강력한 증식 특성 및 in vitro 다계열 분화 잠재력을 갖춘 경제적, 편리하고 안전한 세포원으로 인정받고 있습니다. 본 연구에서는 다양한 질환에서 USCs의 치료적 가치를 탐구한 최신 연구 결과를 개괄적으로 소개합니다.
Culture of USCs
The most frequently used medium for USC culture is a 1:1 mixture of keratinocyte serum-free medium (KSFM, 50 μg/L basic fibroblast growth factor, 1% L-glutamine, 5 μg/L proepidermal growth factor, and 1% penicillin) and progenitor cell culture medium (75% DMEM, 25% F-12, 10% foetal bovine serum, 0.4 mg/L cortisol, 10 μg/L insulin, 5 μg/L transferrin, 2 × 10−9 mol/L triiodothyronine, 10 μg/L proepidermal growth factor, 1.8 × 10−4 mol/L adenine, 1% penicillin, and 1% L-glutamine). USCs are adherent and usually begin to form clones on the 5–7th day, reaching confluence on the 10th day (Lang et al., 2013; Burdeyron et al., 2020). A study reported the overall success rate of fresh urine cell cloning to be approximately 83% and the mean population doubling time of USCs to be 46–49 h (Lang et al., 2013). USCs are in high demand and in limited supply, and strategies such as better culture conditions and shorter culture periods in vitro can improve the challenges. For example, Chun et al. proposed the use of a reconstituted condition with an extracellular matrix (ECM) protein (collagen type I) and 5% O2 hypoxia as an optimized approach allowing for the expansion of harvested USCs while maintaining their chromosomal stability and multilineage differentiation potential (Chun et al., 2016). Gelatine, which is an ECM protein, was used as a coating material on a cell culture dish (Bharadwaj et al., 2013). A recent study reported that Matrigel, flavonoids and Y-27632 (a rho-associated protein kinase (ROCK) inhibitor) could be utilized to promote the efficiency of the isolation, yield, colony formation ability and differentiation capacity of USCs. The Matrigel culture group had two to three times more colonies after 5 days than the gelatine-coated Petri dish group. In addition, the number of cells cultured for 14 days after treatment with Y-27632 was increased by approximately 40-fold compared with that of cells cultured on gelatine-coated Petri dishes. Overall, Y-27632 and Matrigel provided the highest yield of isolated USCs (Kim et al., 2020a). When the cell fusion rate reached 80–90%, the cells were passaged at a ratio of 1:2 or 1:3 every 2–3 days. Fourth and tenth generation cells were reported to exhibit a pebble morphology (Wu et al., 2018), while other studies described them as stone-like (Kang et al., 2015) or grain-like (Lang et al., 2013; Zhang et al., 2021). However, to produce a large number of differentiated cells before transplantation, maximum expansion of USCs is often required in vitro, which results in cell ageing after repeated passages (Halley et al., 1988). Kang et al. seeded USCs at a density of 500 cells/cm2 in 24-well plates and found that their growth ability decreased gradually as the number of passages increased (Kang et al., 2015). Liu et al. mixed nondifferentiated USCs used at an early in vitro passage (≤p3) with an hp-HA gel containing growth factors, and the cells exhibited an improved viability, engraftment ability and vascular, neural and myogenic differentiation potential after subcutaneous implantation in vivo (Liu et al., 2020a).
USCs의 분리 및 배양USCs의 추출
USCs는
전통적인 원심분리법을 통해 분리되었으며,
불순물 세포는 점차 제거되었습니다.
Tayhan 등(2017)은
건강한 젊은 성인의 공기 분리 및 동결 보존된 소변이
신선한 USCs 추출에 가장 적합한 샘플임을 보고했습니다.
일부 초기 연구에서는
당뇨병 환자로부터 USCs를 추출할 수 없다고 보고되었습니다 (Tayhan et al., 2017),
그러나 최신 연구는
이러한 환자들로부터 USCs를 성공적으로 추출할 수 있음을 확인했으나,
그들의 재생 능력이 크게 감소되어 치료에 사용할 수 없음을 밝혔습니다 (Xiong et al., 2019a).
따라서 적절한 샘플 선택은 USC 추출의 전제 조건입니다.
적절한 샘플을 수집한 후,
오염을 줄이기 위해 페니실린 또는 스트렙토마이신을 추가합니다.
실온에서
400 ×g로 10분간 원심분리하여
USCs를 분리합니다.
그 후 상층액을 버리고
샘플을 PBS로 두 번 세척한 후 재현탁합니다.
소변에는 다양한 유형의 세포가 포함되어 있으므로 분리 후 분리된 성분을 식별해야 합니다. 세포 치료 국제 학회(ISCT)는 MSC를 다음과 같은 표지자로 식별하도록 제안했습니다:
1) 세포가 플라스틱 배양 용기에 부착될 수 있으며;
2) 세포 집단의 95% 이상이 특정 표면 항원을 발현하며, CD105, CD73 및 CD90을 포함하며, CD45, CD34, CD14, CD11b, CD79α, CD19 또는 HLA-II 항원을 발현하지 않으며;
3) 적절한 조건 하에서 OB, 연골세포 및 지방세포로 분화될 수 있습니다 (Dominici et al., 2006).
USCs가 MSC의 기준을 충족하기 때문에, 분리된 USCs는 CD29, CD44, CD54, CD73, CD90, CD166 및 STRO-1과 같은 유사한 전형적인 표면 마커를 발현할 수 있습니다 (Bharadwaj et al., 2013; Li et al., 2020; Xiang et al., 2020). 또한, USC에서는 페리사이트(CD146) (Bharadwaj et al., 2013), 상피세포(E-cadherin, claudin 1 및 occludin), 섬유아세포(vimentin 및 fibronectin) 및 신장 상피세포(L1CAM 및 NR3C2) (Kim et al., 2020b) 표지자가 발현됩니다.
USC 배양
USC 배양에 가장 자주 사용되는 배지 혼합물은 케라티노사이트 무혈청 배지(KSFM, 기본 섬유아세포 성장인자 50 μg/L, L-글루타민 1%, 프로에피데르말 성장인자 5 μg/L, 페니실린 1%)와 전구세포 배지(DMEM 75%, F-12 25%, 태아 소 혈청 10%)의 1:1 혼합물입니다. 0.4 mg/L 코르티솔, 10 μg/L 인슐린, 5 μg/L 트랜스페린, 2 × 10−9 mol/L 트리요오드티로닌, 10 μg/L 프로에피데르말 성장 인자, 1.8 × 10−4 mol/L 아데닌, 1% 페니실린, 및 1% L-글루타민)입니다. USCs는 부착성이 있으며 일반적으로 5~7일째에 클론 형성을 시작하여 10일째에 완전 부착에 도달합니다 (Lang et al., 2013; Burdeyron et al., 2020). 한 연구에서는 신선한 소변 세포 클론화 전체 성공률이 약 83%이며 USCs의 평균 인구 배양 시간이 46–49시간으로 보고되었습니다(Lang et al., 2013). USCs는 수요가 높고 공급이 제한적이며, in vitro에서 더 나은 배양 조건과 짧은 배양 기간과 같은 전략이 도전 과제를 개선할 수 있습니다. 예를 들어, Chun 등(2016)은 콜라겐 유형 I과 5% O2 저산소 조건을 포함한 재구성된 배양 조건을 최적화된 접근법으로 제안했습니다. 이 조건은 수확된 USCs의 증식을 유지하면서 염색체 안정성과 다계열 분화 잠재력을 유지할 수 있습니다(Chun et al., 2016). ECM 단백질인 젤라틴은 세포 배양 접시의 코팅 재료로 사용되었습니다(Bharadwaj et al., 2013). 최근 연구에서는 Matrigel, 플라보노이드 및 Y-27632(rho 관련 단백질 키나제(ROCK) 억제제)가 USC의 분리 효율, 수율, 콜로니 형성 능력 및 분화 능력을 향상시키는 데 활용될 수 있음을 보고했습니다. Matrigel 배양 그룹은 5일 후 젤라틴 코팅 페트리 접시 그룹보다 2~3배 많은 콜로니를 형성했습니다. 또한 Y-27632 처리 후 14일 동안 배양된 세포 수는 젤라틴 코팅 페트리 접시에서 배양된 세포 수보다 약 40배 증가했습니다. 전체적으로 Y-27632와 Matrigel은 분리된 USCs의 가장 높은 수율을 제공했습니다 (Kim et al., 2020a). 세포 융합률이 80–90%에 도달하면 세포는 2–3일마다 1:2 또는 1:3의 비율로 분배되었습니다. 4세대와 10세대 세포는 돌멩이 모양(Wu et al., 2018)으로 보고되었으며, 다른 연구에서는 돌 모양(Kang et al., 2015) 또는 곡물 모양(Lang et al., 2013; Zhang et al., 2021)으로 묘사되었습니다. 그러나 이식 전에 분화된 세포를 대량으로 생산하기 위해 USCs의 최대 확장이 in vitro에서 자주 요구되는데, 이는 반복적인 배양으로 인해 세포 노화가 발생합니다 (Halley et al., 1988). Kang et al.은 24-well 플레이트에 500 세포/cm2의 밀도로 USCs를 배양했으며, 배양 횟수가 증가함에 따라 성장 능력이 점차 감소함을 발견했습니다 (Kang et al., 2015). Liu 등(2020a)은 초기 체외 배양 단계(≤p3)의 미분화 USCs를 성장 인자를 함유한 hp-HA 겔과 혼합한 후, 체내 피하 이식 후 세포의 생존율, 이식 능력 및 혈관, 신경, 근육 분화 잠재력이 개선되었음을 확인했습니다(Liu et al., 2020a).
Underlying Mechanisms of USCs
Regulating Immune Systems
To date, some studies have found that USCs can affect immune system regulation. Wu et al. found that the lack of costimulatory molecules and MHC-II markers on cultured USCs indicates that they can escape recognition by the recipient’s immune system due to their low immunogenicity. In addition, the coculture of USCs with human peripheral blood mononuclear cells (PBMCs) significantly increases the USC expression levels of immunomodulatory cytokines (such as IL-6 and IL-8) and immunomodulatory chemokines (such as MCP-1). The secretion of cytokines (such as RANTES, GRO-α and GM-CSF) indicates that USCs have good immunomodulatory properties (Wu et al., 2021). Zhou et al. cocultured USCs with human CD4+ T cells stimulated with phytohemagglutinin (PHA) and observed that CD4+ T cell proliferation was inhibited in a dose-dependent manner and that the mRNA levels of IFN-γ, T-bet, IL-17A and RORC were significantly reduced. USCs can regulate CD4+ T cell activation and the Th1/Th17 immune response (Zhou et al., 2020). In addition, USCs reduce myeloperoxidase (MPO) activity and the number of MPO+ cells in the tissue, indicating reduced neutrophil infiltration. Therefore, in a mouse model of inflammatory bowel disease induced by dextran sulfate sodium or 2,4,6-trinitrobenzene sulfonic acid, the expression of proinflammatory factors was significantly reduced after treatment with USCs, thereby reducing the inflammatory response and improving the survival rate of the mice (Zhou et al., 2020). Similarly, Kang et al. cocultured USCs with PBMCs and observed a dose-dependent inhibitory effect on PBMC proliferation induced by USCs. Lymphocyte proliferation was further inhibited as the number of USCs increased (Kang et al., 2015). Additionally, Choi et al. found a low expression level of HLA (human leukocyte antigen)-DR in USCs, indicating their suppressed immunogenicity (Choi et al., 2017). HLA-DR is a surface receptor on MHC class II cells that plays an important role in antigen recognition, presentation, immune response and regulation. The absence of class II HLA expression enables the allograft to escape the recognition of antigen-presenting immune system cells; thus, there is basically no risk of immune rejection, and severe complications such as transplantation failure, late rejection and graft-versus-host-disease (GVHD) are reduced (Choi et al., 2017; Kot et al., 2019). All of the results of the studies mentioned above suggest that USCs negatively regulate immunoreactions and that this immunomodulatory effect is an efficient way to reduce inflammation. The various underlying mechanisms are summarized in Figure 1.
USCs의 기저 메커니즘면역 체계 조절
현재까지 일부 연구에서 USCs가
면역 체계 조절에 영향을 미친다는 결과가 보고되었습니다.
Wu 등(2019)은 배양된 USCs에 공극 자극 분자와 MHC-II 표지자가 결여되어 있어 낮은 면역원성으로 인해 수혜자의 면역 체계로부터 인식되지 않을 수 있음을 발견했습니다. 또한, USCs와 인간 말초 혈액 단핵구(PBMCs)의 공배양은 USCs의 면역 조절 사이토킨(예: IL-6 및 IL-8) 및 면역 조절 케모카인(예: MCP-1) 발현 수준을 유의미하게 증가시켰습니다. 사이토킨(RANTES, GRO-α 및 GM-CSF 등)의 분비는 USCs가 우수한 면역조절 특성을 갖는다는 것을 나타냅니다(Wu et al., 2021). Zhou 등(2020)은 PHA로 자극된 인간 CD4+ T 세포와 USCs를 공배양한 결과, CD4+ T 세포 증식이 용량 의존적으로 억제되었으며, IFN-γ, T-bet, IL-17A 및 RORC의 mRNA 수준이 유의미하게 감소함을 관찰했습니다. USCs는 CD4+ T 세포 활성화 및 Th1/Th17 면역 반응을 조절합니다(Zhou et al., 2020). 또한 USCs는 조직 내 마이엘로퍼옥시다제(MPO) 활성과 MPO+ 세포 수를 감소시켜 중성구 침윤이 감소함을 나타냅니다. 따라서, 데크스트란 황산나트륨 또는 2,4,6-트리니트로벤젠 설폰산으로 유발된 염증성 장 질환 마우스 모델에서 USCs 투여 후 염증성 인자 발현이 유의미하게 감소하여 염증 반응이 감소하고 마우스의 생존율이 개선되었습니다 (Zhou et al., 2020). 또한 Kang 등(2015)은 USCs와 PBMCs를 공배양하여 USCs에 의해 유발된 PBMC 증식에 대한 용량 의존적 억제 효과를 관찰했습니다. USCs의 수가 증가함에 따라 림프구 증식이 더욱 억제되었습니다(Kang et al., 2015). 또한 Choi 등(Choi et al., 2017)은 USCs에서 HLA(인간 백혈구 항원)-DR의 발현 수준이 낮음을 발견했으며, 이는 USCs의 면역원성 억제를 나타냅니다. HLA-DR은 MHC 클래스 II 세포의 표면 수용체로, 항원 인식, 제시, 면역 반응 및 조절에 중요한 역할을 합니다. MHC 클래스 II HLA 발현의 부재는 이종 이식편이 항원 제시 면역 세포의 인식을 회피하게 하여, 기본적으로 면역 거부 위험이 없으며 이식 실패, 지연 거부, 이식편 대 숙주 질환(GVHD)과 같은 심각한 합병증이 감소합니다(Choi et al., 2017; Kot et al., 2019).
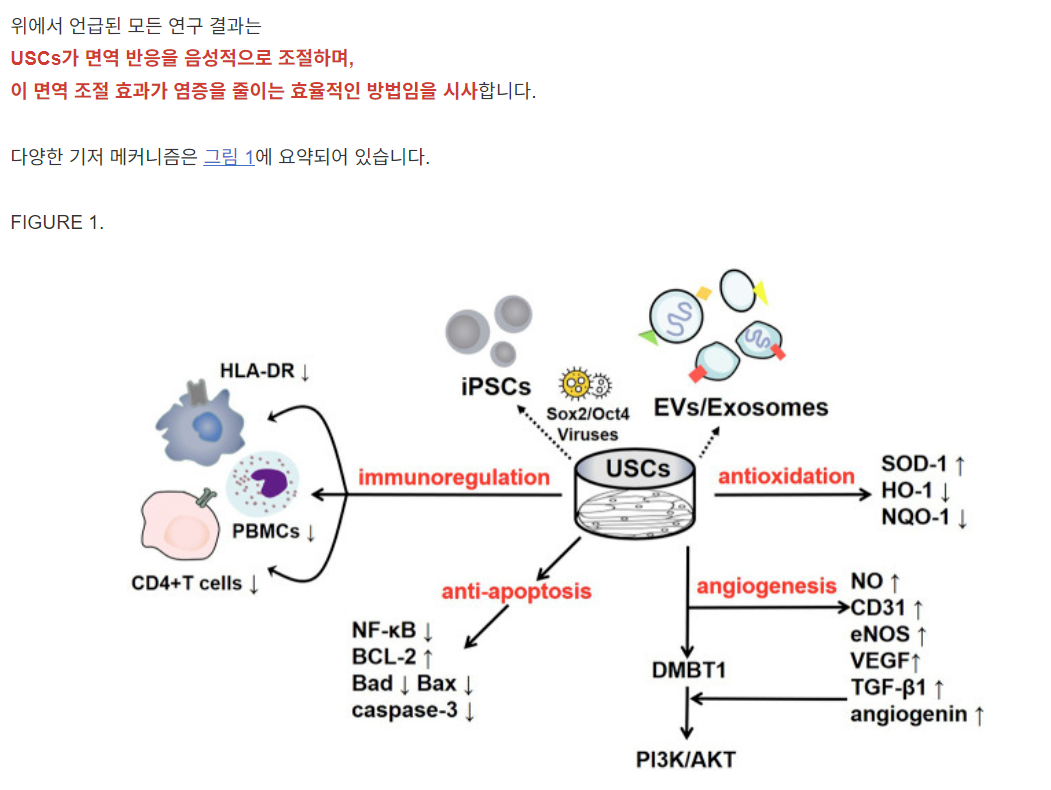
위에서 언급된 모든 연구 결과는
USCs가 면역 반응을 음성적으로 조절하며,
이 면역 조절 효과가 염증을 줄이는 효율적인 방법임을 시사합니다.
다양한 기저 메커니즘은 그림 1에 요약되어 있습니다.
FIGURE 1.
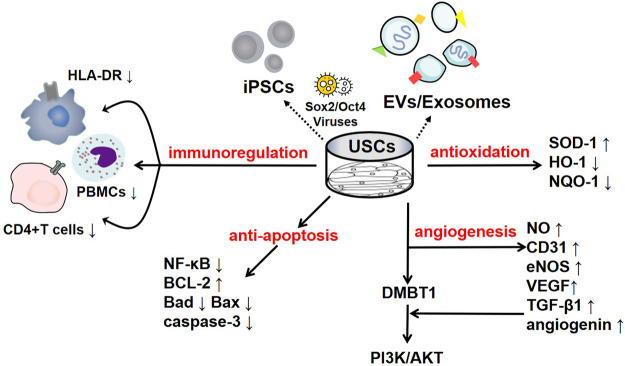
The regulatory mechanisms of USCs and their secreted products. USCs and their secreted products, such as exosomes, extracellular vesicles, and USC-iPSCs, play an important role in disease the pathogeneses. USCs exert negative immunoregulatory functions and serve as antioxidants, as manifested by their increased SOD-1 levels and reduced HO-1 levels. USCs exert an antiautophagic effect, characterized by increased p62 levels and decreased levels of LC3-II and Beclin1. Furthermore, USCs promote angiogenesis mediated by VEGF, angiogenin, and PI3K/AKT pathway activation. Interestingly, their effect on apoptosis remains controversial, as they exhibit increased levels of the apoptotic protein Bax and decreased levels of the antiapoptotic protein Bcl-2.
USCs 및 그 분비물의 조절 메커니즘.
USCs 및 그 분비물(예: 엑소좀, 세포외 소포, USC-iPSCs)은
질병의 병리학적 과정에 중요한 역할을 합니다.
USCs는
SOD-1 수준 증가와 HO-1 수준 감소로 나타나는 음성 면역 조절 기능을 발휘하며
항산화 작용을 합니다.
USCs는
p62 수준 증가와 LC3-II 및 Beclin1 수준 감소로 특징지어지는
항자식작용 효과를 나타냅니다.
또한 USCs는
VEGF, angiogenin, 및 PI3K/AKT 경로 활성화에 의해 매개되는
혈관新生을 촉진합니다.
흥미롭게도, 그들의 세포 사멸에 대한 영향은 논란의 여지가 있습니다. 이는 세포 사멸 단백질 Bax의 증가와 항세포 사멸 단백질 Bcl-2의 감소로 나타납니다.
Modulating Oxidative Stress
Oxidative stress is a harmful process that can lead to a variety of diseases, including cancer, cardiovascular diseases, neurological disorders, respiratory diseases, kidney diseases, chronic inflammation and accelerated ageing (Pizzino et al., 2017). Upon stimulation, the body produces many free radicals, such as reactive oxygen species (ROS) and reactive nitrogen species (RNS), which disrupt oxidation homeostasis and antioxidant mechanisms, leading to oxidative stress (Pizzino et al., 2017). The effect of USCs on the regulation of oxidative stress in the body is highly significant. Superoxide dismutase (SOD-1), which can inhibit tissue damage caused by free radicals, is considered a key antioxidant in the assessment of mitochondrial oxidative activities, and malondialdehyde (MDA) is considered to be an important marker of oxidative stress (Marrocco et al., 2017). Li et al. found that USC-derived exosomes (USC-Exos) reduced oxidative stress by increasing the activity of SOD and reducing the MDA content, thereby protecting human kidney cortex/proximal tubule cells (HK2) from hypoxia-reoxygenation (H/R)-induced damage (Li et al., 2020). Xiong et al. reported that treatment with USCs in a diabetic nephropathy (DN) model slowed the progression of renal fibrosis due to the obvious downregulation of nicotinamide adenine dinucleotide phosphate (NADPH) oxidase levels, whose increase promotes the progression of DN (Xiong et al., 2020). Similarly, Zhang et al. found elevated levels of SOD-1 in USC-treated rats with chronic kidney disease (CKD) (Zhang et al., 2020a). Moreover, the antioxidant effect of USCs has been observed in interstitial cystitis, which manifests as notably decreased levels of oxidative stress-associated indicators, including haem oxygenase (HO)-1 and NADPH quinine oxidoreductase (NQO)-1 (Li et al., 2017). Previous studies have demonstrated that USCs can alleviate oxidative stress damage in cells and have a certain therapeutic effect on kidney diseases.
산화 스트레스 조절
산화 스트레스는
암, 심혈관 질환, 신경계 장애, 호흡기 질환, 신장 질환, 만성 염증 및 가속화된 노화 등
다양한 질병을 유발할 수 있는 유해한 과정입니다 (Pizzino et al., 2017).
자극을 받으면 신체는
활성산소종(ROS)과 활성질소종(RNS)과 같은 많은 자유 라디칼을 생성하며,
이는 산화 균형과 항산화 메커니즘을 방해하여 산화 스트레스를 유발합니다(Pizzino et al., 2017).
USC가
신체 내 산화 스트레스 조절에 미치는 영향은 매우 중요합니다.
자유 라디칼로 인한 조직 손상을 억제하는 슈퍼옥사이드 디스뮤타제(SOD-1)는
미토콘드리아 산화 활성 평가에서 핵심 항산화제로 간주되며,
말론디알데히드(MDA)는 산화 스트레스의 중요한 지표로 여겨집니다(Marrocco et al., 2017).
Li et al.은
USC 유래 엑소좀(USC-Exos)이 SOD 활성을 증가시키고
MDA 함량을 감소시켜 인간 신장 피질/근위 세뇨관 세포(HK2)를
저산소-재산소화(H/R)로 인한 손상으로부터 보호한다는 것을 발견했습니다(Li et al., 2020).
Xiong 등(2020)은 당뇨병성 신증(DN) 모델에서
USC 치료가 니코틴아미드 아데닌 디뉴클레오티드 포스페이트(NADPH) 산화효소 수치의 현저한 감소로 인해
신장 섬유화 진행을 늦췄다고 보고했습니다.
이 효소의 증가가
DN 진행을 촉진합니다(Xiong et al., 2020).
유사하게,
Zhang 등(Zhang et al., 2020a)은
만성 신장 질환(CKD)을 가진 USC 처리 쥐에서 SOD-1 수치가 증가했음을 발견했습니다(Zhang et al., 2020a).
또한
USC의 항산화 효과는 간질성 방광염에서 관찰되었으며,
이는 헤모글로빈 산화효소(HO)-1 및 NADPH 퀴닌 산화환원효소(NQO)-1과 같은
산화 스트레스 관련 지표의 현저한 감소로 나타났습니다(Li et al., 2017).
이전 연구들은
USC가 세포 내 산화 스트레스 손상을 완화하고
신장 질환에 대한 일정한 치료 효과를 갖는다는 것을 보여주었습니다.
Enhancing Angiogenic Activities
Angiogenesis is a critical process involving the repair and regeneration of tissues exposed to severe ischaemia/hypoxia (such as wound healing, myocardial ischaemia, cerebral ischaemia, and cancer) and is mediated by endothelial cell (EC) proliferation and migration (Kargozar et al., 2020). As the time prior to the reception of revascularization therapy increases, the risk of endothelial dysfunction is markedly elevated. Hence, clinical investigations of rapid revascularization represent an excellent approach to improve patient prognosis.
As an endothelial marker, CD31 has been widely used to evaluate the density of blood vessels. Zhao et al. discovered dramatically elevated CD31 levels in the islets of mice treated with low-dose streptozotocin (MLD-STZ) after USC transplantation, indicating that USCs can help rebuild the islet architecture (Zhao et al., 2018). Additionally, proangiogenic microRNAs provided by USCs, such as miR-10, miR-21, and miR-30, have been found to participate in angiogenic growth in rats with diabetic erectile dysfunction (DED), as shown by the enhanced expression of CD31 and endothelial nitric oxide synthase (eNOS) (Ouyang et al., 2019). In USC-polycaprolactone/gelatine-treated wounds, the microvessel density was increased compared with that in the controls, and this stimulatory effect was prompted by vascular endothelial growth factor (VEGF) and TGF-β1, providing compelling evidence that the paracrine factors released by USCs play a key role in angiogenesis (Fu et al., 2014). Jiang et al. concluded that USC-Exos could promote angiogenesis by increasing the expression levels of VEGF, TGF-β1, and angiogenin (Jiang et al., 2016). Similarly, the deleted in malignant brain tumour 1 (DMBT1) protein is enriched in USC-Exos, and DMBT1 has been proven to function as a promoter of angiogenesis that activates the PI3K/AKT pathway by increasing the secretion of VEGF, nitric oxide (NO) and angiogenin (Karar and Maity, 2011; Chen et al., 2018a). Chen et al. showed that when human microvascular endothelial cells were exposed to USC-Exos, the proliferation of wound healing-related cells, such as fibroblasts and masses of capillary-like structures, was activated; when DMBT1 expression was suppressed, the functions of the USC-Exos were remarkably inhibited, as manifested by low levels of VEGF-A and Akt phosphorylation (Chen et al., 2018a). Thus, USCs clearly play a role in angiogenesis.
혈관新生 활동 강화
혈관신생은
심한 허혈/저산소 환경에 노출된 조직의 수리 및 재생 과정으로,
상처 치유, 심근 허혈, 뇌 허혈, 암 등에서 발생하며
내피 세포(EC)의 증식 및 이동에 의해 매개됩니다(Kargozar et al., 2020).
재혈관화 치료를 받기 전 시간이 길어질수록
내피 기능 장애의 위험이 현저히 증가합니다.
따라서
빠른 재혈관화 치료의 임상적 연구는
환자 예후 개선을 위한 우수한 접근 방식입니다.
내피 세포 표지자로서 CD31은 혈관 밀도를 평가하는 데 널리 사용됩니다. Zhao 등(2018)은 저용량 스트레프토조토신(MLD-STZ)으로 처리된 쥐의 췌장 섬에서 USC 이식 후 CD31 수치가 현저히 증가함을 발견했으며, 이는 USC가 췌장 섬 구조 재건에 도움을 줄 수 있음을 시사합니다(Zhao et al., 2018). 또한 USC가 제공하는 혈관新生 촉진 마이크로RNA(miRNA)인 miR-10, miR-21, miR-30은 당뇨병성 발기 장애(DED)를 가진 쥐에서 혈관新生 성장에 참여하는 것으로 나타났으며, 이는 CD31과 내피형 산화질소 합성효소(eNOS)의 발현 증가로 확인되었습니다(Ouyang et al., 2019). USC-폴리카프로락톤/젤라틴으로 처리된 상처에서 미세혈관 밀도가 대조군에 비해 증가했으며, 이 자극 효과는 혈관 내피 성장 인자(VEGF)와 TGF-β1에 의해 유발되어 USC에서 분비되는 파라크린 인자가 혈관新生에 핵심 역할을 한다는 강력한 증거를 제공했습니다(Fu et al., 2014). Jiang 등(Jiang et al., 2016)은 USC-Exos가 VEGF, TGF-β1, 및 angiogenin의 발현 수준을 증가시켜 혈관新生을 촉진한다고 결론지었습니다. 同様に, 악성 뇌종양에서 삭제된 1번 유전자(DMBT1) 단백질은 USC-Exos에 풍부하게 존재하며, DMBT1은 VEGF, 질산산화물(NO) 및 혈관신생인 분비를 증가시켜 PI3K/AKT 경로를 활성화함으로써 혈관신생 촉진제로 기능함이 입증되었습니다(Karar and Maity, 2011; Chen et al., 2018a). Chen 등(2018a)은 인간 미세혈관 내피 세포가 USC-Exos에 노출될 때 상처 치유 관련 세포(섬유아세포 및 모세혈관 유사 구조물 군집)의 증식이 활성화되었으며, DMBT1 발현이 억제될 경우 USC-Exos의 기능이 현저히 억제되었음을 보여주었습니다. 이는 VEGF-A 및 Akt 인산화 수준이 낮게 나타남으로 확인되었습니다(Chen et al., 2018a). 따라서 USCs는 혈관新生에 명확한 역할을 합니다.
Regulating Apoptosis
Apoptosis is a programmed cell death process that involves the formation of distinct apoptotic bodies to maintain homeostasis and regulate the regular cell cycle. However, excessive apoptosis can further impair tissue function, which, in turn, leads to more severe pathological conditions (Xu et al., 2019). Therefore, inhibiting apoptosis is regarded as rescuing impaired tissue. Several signalling pathways, such as the NF-κB and Bax/Bcl-2 pathways, and apoptosis-associated proteins, such as cleaved caspase-3 and metalloproteinase 1 (TIMP1), are involved.
The Bcl-2/Bax pathway is an important component of the endogenous apoptosis pathway. After the apoptosis pathway is activated, cells express the proapoptotic protein Bax to promote the release of cytochrome C (Cyt C) into the cytoplasm, which initiates the caspase cascade and leads to apoptosis. Sun et al. emphasized that USCs downregulated the expression of the proapoptotic proteins Bax and Caspase 3 and upregulated the expression of the antiapoptotic protein Bcl-2 in acute kidney injury (AKI) models. Compared with those in the control group, the renal function and histological damage of NRK-52E cells induced by cisplatin were significantly improved, and the proliferation of renal tubular epithelial cells was significantly increased (Sun et al., 2019). Similarly, in an interstitial cystitis model, treatment with USCs downregulated apoptotic levels by markedly reducing the levels of caspase-3 and Bax and notably increasing the level of Bcl-2, and fewer apoptotic nuclei were observed (Li et al., 2017). Moreover, USCs combined with chondroitinase ABC (chABC) can suppress neuronal apoptotic levels with high Bax and low Bcl-2 levels when administered to rats with spinal cord injuries (Li and Wu, 2017). ChABC functions by degrading the glycosaminoglycan side chains of chondroitin sulfate proteoglycans, ameliorating the inhibition of glial scar regeneration.
USCs and their secreted products are involved in the regulation of apoptosis. Jiang et al. found that after exposure to high glucose, podocytes and tubular epithelial cells of diabetic rats become damaged and overexpress caspase-3; nevertheless, USC-Exos protect podocytes and renal tubular epithelial cells by downregulating Caspase-3 overexpression and inhibiting apoptosis (Jiang et al., 2016). More importantly, these authors confirmed the role of USC-Exos in ameliorating human podocyte apoptosis in their follow-up experiment (Xiong et al., 2020). TIMP1 is a natural inhibitor of matrix metalloproteinases (MMPs). The recombinant human TIMP1 protein inhibited apoptosis by activating the PI3K and JNK signalling pathways. Chen et al. found that TIMP1 was highly enriched in USC-EVs and could enhance the antiapoptotic effects of OBs and endothelial cells and thus play a protective role (Guo et al., 2006; Chen et al., 2020). In addition, miR-146a-5p delivered by USC-Exos was reported to inhibit the expression of interleukin-1 receptor-associated kinase 1 (IRAK1) via posttranslational expression and significantly reduce NF-κB P65 nuclear localization, thus inhibiting the IRAK1-NF-κB signalling pathway (Li et al., 2020). Similarly, abundant miR-216a-5p carried in USC-Exos was shown to be transferred to human proximal tubular epithelial cells (HK-2) and further promote phosphatase and tensin homolog (PTEN) silencing and the activation of Akt phosphorylation, thereby protecting HK-2 cells from apoptosis (Zhang et al., 2020b). The various underlying mechanisms are summarized in Figure 1.
세포 사멸 조절
세포 사멸은
세포의 정상적인 세포 주기를 유지하고 항상성을 조절하기 위해
특이적인 세포 사멸 체를 형성하는 프로그램된 세포 사멸 과정입니다.
그러나 과도한 세포 사멸은 조직 기능을 더욱 손상시켜 더 심각한 병리적 상태로 이어질 수 있습니다(Xu et al., 2019). 따라서 아포토시스를 억제하는 것은 손상된 조직을 회복시키는 것으로 간주됩니다. NF-κB 및 Bax/Bcl-2 경로와 같은 여러 신호전달 경로와 cleaved caspase-3 및 metalloproteinase 1 (TIMP1)과 같은 아포토시스 관련 단백질이 관여합니다.
Bcl-2/Bax 경로는 내인성 아포토시스 경로의 중요한 구성 요소입니다. 세포 사멸 경로가 활성화되면 세포는 프로아포토틱 단백질 Bax를 발현하여 세포질로 사이토크롬 C(Cyt C)를 방출시켜 카스파제 캐스케이드를 유발하고 세포 사멸을 유도합니다. Sun 등(2020)은 급성 신장 손상(AKI) 모델에서 USCs가 프로아포토틱 단백질 Bax와 카스파제 3의 발현을 억제하고 항아포토틱 단백질 Bcl-2의 발현을 증가시켰다고 강조했습니다. 대조군과 비교했을 때, 시스플라틴으로 유도된 NRK-52E 세포의 신장 기능과 조직학적 손상이 유의미하게 개선되었으며, 신장 관상 상피 세포의 증식이 유의미하게 증가했습니다(Sun et al., 2019). 同様に, 간질성 방광염 모델에서 USCs는 caspase-3 및 Bax의 수준을 현저히 감소시키고 Bcl-2의 수준을 크게 증가시켜 세포 사멸 수준을 억제했으며, 세포 사멸 핵의 수가 감소했습니다 (Li et al., 2017). 또한, USCs와 콘드로이틴아제 ABC (chABC)를 결합한 치료는 척수 손상 쥐에 투여 시 Bax 수준이 높고 Bcl-2 수준이 낮은 신경세포의 세포사멸 수준을 억제했습니다 (Li and Wu, 2017). ChABC는 콘드로이틴 설페이트 프로테오글리칸의 글리코사미노글리칸 측쇄를 분해하여 글리아 흉터 재생 억제를 완화합니다.
USCs와 그 분비물은
세포 사멸 조절에 관여합니다.
Jiang 등(2016)은 고혈당 노출 후 당뇨병 쥐의 포도체와 관상 상피 세포가 손상되고 caspase-3 과발현을 보였지만, USC-Exos가 caspase-3 과발현을 억제하고 세포 사멸을 억제함으로써 포도체와 신장 관상 상피 세포를 보호한다는 것을 발견했습니다(Jiang et al., 2016). 더 중요한 것은 이 연구자들이 후속 실험에서 USC-Exos가 인간 포도세포의 아포토시스를 완화하는 역할을 확인했다는 점입니다(Xiong et al., 2020). TIMP1은 매트릭스 메탈로프로테아제(MMPs)의 자연적 억제제입니다. 재조합 인간 TIMP1 단백질은 PI3K 및 JNK 신호전달 경로를 활성화하여 세포 사멸을 억제했습니다. Chen 등(2006)은 TIMP1이 USC-EVs에 풍부하게 존재하며 OBs 및 내피 세포의 항세포 사멸 효과를 강화하여 보호 역할을 한다고 보고했습니다(Guo et al., 2006; Chen et al., 2020). 또한 USC-Exos에 의해 전달된 miR-146a-5p는 포스트트랜스레이셔널 발현을 통해 인터루킨-1 수용체 연관 키나제 1(IRAK1)의 발현을 억제하고 NF-κB P65의 핵 내 국소화를 유의미하게 감소시켜 IRAK1-NF-κB 신호전달 경로를 억제했습니다(Li et al., 2020). 유사하게, USC-Exos에 풍부하게 포함된 miR-216a-5p는 인간 근위 세뇨관 상피 세포(HK-2)로 전달되어 인산화 효소 및 텐신 동형체(PTEN)의 침묵화를 촉진하고 Akt 인산화를 활성화시켜 HK-2 세포의 아포토시스를 보호하는 것으로 나타났습니다(Zhang et al., 2020b). 다양한 기전들은 그림 1에 요약되어 있습니다.
Applications of USCs
Renal Diseases
Chronic Kidney Disease
Renal diseases and complications are regarded as important factors leading to high hospitalization rates and a poor quality of life and pose substantial burdens on patients. The global prevalence of CKD ranges from 11 to 13%, and the global mortality rate represents 4.6% of the total mortality rate; CKD was the 12th leading cause of death in 2017 (Hill et al., 2016; GBD Chronic Kidney Disease Collaboration, 2020). As kidney tissue-specific stem cells, USCs may be the best choice for kidney tissue repair and have promise as a treatment for CKD. Zhang et al. found that the implantation of USCs protected the number of nephrons and significantly improved renal function in a rat CKD model due to their strong proliferation ability and ability to reduce fibrin matrix formation and inhibit renal inflammation. Therefore, USCs may improve renal function and prevent tissue structure damage caused by CKD in the clinic (Zhang et al., 2020a).
Renal Regeneration
Due to the high cost of haemodialysis and the shortage of kidney sources, renal regeneration is considered a possible and effective means to treat renal failure. However, the kidney is one of the most difficult organs to regenerate, and previous stem cells strategies have failed. Therefore, because they are derived from the kidney, readily available and safe, researchers have attempted to determine whether USCs can promote kidney tissue regeneration.
Therefore, we have confirmed that USCs play an active role in the repair of kidney tissue, but doubts remain about their ability to regenerate kidney tissue. After using human kidney differentiation medium for 2 weeks, Choi and others observed decreased expression of stem cell markers (SSEA4) and increased expression of renal lineage-specific markers (PAX2, WT1 and Cadherin-6), suggesting that USCs have a significant renal cell-lineage differentiation ability. In addition, USCs can secrete growth factors such as VEGF and PDGF-BB and do not induce histological abnormalities, suggesting their safety in vivo. Therefore, USCs may be a promising treatment for renal regeneration due to their good renal spectrum differentiation ability, accessibility and enhanced safety. However, due to the limitations of in vitro experiments, no kidney tissue-like morphologies have been observed and need to be confirmed by subsequent in vivo experiments, which will be the focus of future research. Thus, to date, the utility of USCs in renal tissue regeneration has not been demonstrated (Choi et al., 2017).
Acute Kidney Injury
AKI is an important clinical disease characterized by tubular injury and a rapid decline in renal function. At present, there is no method for complete recovery (Guo et al., 2019). AKI occurs in approximately 20% of hospitalized patients, and the mortality rate can reach 50% without renal transplantation (Levey and James, 2017). Therefore, alternative therapies are the key to improving the treatment and prognosis of patients with AKI. Studies have shown that USCs can inhibit inflammation in the kidney and significantly improve renal function and histological damage, suggesting their potential in the treatment of AKI and representing a new clinical treatment strategy. Tian et al. created rat models of ischaemic AKI and found upregulated expression levels of anti-inflammatory factors (IL-10 and TGF-β1) and downregulated levels of proinflammatory factors (INF-γ and IL-1β) in the USC-treated group, indicating that USCs exerted a good anti-inflammatory effect (Tian et al., 2017). Sun and others concluded that USCs alleviated renal function damage in a cisplatin-induced AKI model, which was manifested by reduction in blood urea nitrogen (BUN) and serum creatinine (SCr) levels and improvements in histology and ultrastructure. In vitro, the authors cocultured cisplatin-induced NRK-52E cells with USCs, and the cells exhibited a higher viability and lower apoptosis rate than the control group cells (Sun et al., 2019).
신장 질환만성 신장 질환
신장 질환 및 합병증은 높은 입원율과 낮은 삶의 질을 초래하는 중요한 요인으로 간주되며, 환자에게 심각한 부담을 초래합니다. 전 세계 CKD 유병률은 11~13%이며, 전 세계 사망률의 4.6%를 차지하며, 2017년 사망 원인 12위였습니다(Hill et al., 2016; GBD Chronic Kidney Disease Collaboration, 2020). 신장 조직 특이적 줄기세포인 USCs는 신장 조직 재생에 가장 적합한 선택지로 여겨지며, CKD 치료법으로의 잠재력을 가지고 있습니다. Zhang et al.은 쥐 CKD 모델에서 USCs의 이식이 강한 증식 능력과 섬유소 매트릭스 형성 감소 및 신장 염증 억제 능력으로 인해 신장 기능이 유의미하게 개선되고 신장 단위체 수를 보호한다는 사실을 발견했습니다. 따라서 USCs는 임상에서 CKD로 인한 신장 기능 개선 및 조직 구조 손상 예방에 기여할 수 있습니다(Zhang et al., 2020a).
신장 재생
혈액 투석의 높은 비용과 신장 공급원 부족으로 인해 신장 재생은 신부전 치료를 위한 가능하고 효과적인 방법으로 고려되고 있습니다. 그러나 신장은 재생이 가장 어려운 장기 중 하나이며, 이전 줄기세포 전략은 실패했습니다. 따라서 신장에서 유래되었고 쉽게 구할 수 있으며 안전한 특성 때문에 연구자들은 USCs가 신장 조직 재생을 촉진할 수 있는지 확인하기 위해 노력해 왔습니다.
따라서 우리는 USCs가 신장 조직 복구에 활성 역할을 한다는 것을 확인했지만, 신장 조직 재생 능력에 대한 의문이 남아 있습니다. 인간 신장 분화 배지에서 2주간 배양한 후 Choi 등(2020)은 줄기세포 표지자(SSEA4)의 발현이 감소하고 신장 계통 특이적 표지자(PAX2, WT1 및 Cadherin-6)의 발현이 증가함을 관찰했습니다. 이는 USCs가 신장 세포 계통 분화 능력에 유의미한 영향을 미친다는 것을 시사합니다. 또한 USCs는 VEGF 및 PDGF-BB와 같은 성장 인자를 분비하며 조직학적 이상을 유발하지 않아 in vivo에서의 안전성을 시사합니다. 따라서 USCs는 우수한 신장 분화 능력, 접근성 및 향상된 안전성으로 인해 신장 재생 치료제로 유망할 수 있습니다. 그러나 in vitro 실험의 한계로 인해 신장 조직 유사 형태가 관찰되지 않았으며, 이는 후속 in vivo 실험을 통해 확인되어야 하며, 이는 향후 연구의 초점이 될 것입니다. 따라서 현재까지 USCs의 신장 조직 재생에 대한 유용성은 입증되지 않았습니다 (Choi et al., 2017).
급성 신장 손상
AKI는 관상 손상과 신장 기능의 급격한 저하를 특징으로 하는 중요한 임상 질환입니다. 현재 완전한 회복을 위한 방법은 없습니다 (Guo et al., 2019). AKI는 입원 환자의 약 20%에서 발생하며, 신장 이식 없이 사망률이 50%에 달할 수 있습니다(Levey and James, 2017). 따라서 AKI 환자의 치료 및 예후 개선을 위해 대체 치료법이 필수적입니다. 연구 결과, USCs는 신장 내 염증을 억제하고 신장 기능 및 조직학적 손상을 유의미하게 개선하여 AKI 치료에 잠재력을 보여주며 새로운 임상 치료 전략을 제시합니다. Tian 등(2017)은 허혈성 AKI 쥐 모델을 생성하고 USC 처리 그룹에서 항염증 인자(IL-10 및 TGF-β1)의 발현 수준이 증가하고 염증 촉진 인자(INF-γ 및 IL-1β)의 발현 수준이 감소함을 발견했습니다. 이는 USC가 우수한 항염증 효과를 발휘함을 나타냅니다(Tian et al., 2017). Sun 등(2019)은 시스플라틴으로 유도된 AKI 모델에서 USCs가 신장 기능 손상을 완화시켰으며, 이는 혈청 요소 질소(BUN) 및 혈청 크레아티닌(SCr) 수치 감소와 조직학 및 초미세 구조 개선으로 나타났습니다. In vitro에서 저자들은 시스플라틴으로 유도된 NRK-52E 세포와 USCs를 공배양했으며, 이 세포들은 대조군 세포에 비해 더 높은 생존율과 낮은 세포 사멸률을 나타냈습니다(Sun et al., 2019).
Diabetic Nephropathy
DN has emerged as the main cause of end-stage renal disease, especially since the number of DN patients is expected to reach 3 billion by 2025 (Xiong et al., 2020). Studies have shown that USCs can protect podocytes in patients with DN and inhibit apoptosis while improving renal tissue fibrosis. Jiang et al. investigated STZ-induced rat models and found marked increases in their urine volume and urinary albumin concentration, alleviated mesangial expansion and downregulated expression of podocyte survival factors, such as bone morphogenetic protein 7 (BMP-7). On the other hand, these effects were markedly attenuated after treatment with USC-Exos, indicating that USC-Exos are highly important for the survival of podocytes and endothelial cells (Jiang et al., 2016). Subsequently, Duan et al. proposed that USC-Exos can secrete microRNA-16-5p to inhibit podocyte apoptosis by suppressing high glucose-induced VEGF-A expression, as demonstrated by the upregulation of the podocyte surface marker protein nephrin and downregulation of glomerular smooth muscle-specific proteins (α-SMA) and apoptotic proteins (Bax and Caspase-3). Furthermore, microRNA-16-5p was overexpressed following an intravenous injection of USC-Exos and may have protected podocytes in a diabetes rat model (Duan et al., 2019). Moreover, Xiong et al. observed that USCs had renoprotective effects, as they protected against renal interstitial fibrosis, as demonstrated by remarkable reductions in BUN and SCr levels, improved fibrous hyperplasia in renal tissues and reduced expression of α-SMA (Xiong et al., 2020).
당뇨병성 신증
DN은 말기 신부전의 주요 원인으로 부상했으며, 특히 2025년까지 DN 환자가 30억 명에 달할 것으로 예상됩니다(Xiong et al., 2020). 연구 결과, USCs는 DN 환자의 포도세포를 보호하고 세포 사멸을 억제하며 신장 조직 섬유화를 개선하는 것으로 나타났습니다. Jiang 등(2016)은 STZ 유도 쥐 모델을 조사하여 소변량과 소변 알부민 농도가 현저히 증가했으며, 메사글리얼 확장 완화 및 포도세포 생존 인자(예: 골형성 단백질 7, BMP-7)의 발현이 감소함을 발견했습니다. 반면, USC-Exos 투여 후 이러한 효과는 현저히 완화되었으며, 이는 USC-Exos가 포도세포와 내피 세포의 생존에 매우 중요함을 시사합니다(Jiang et al., 2016). 이후 Duan 등(2019)은 USC-Exos가 고혈당에 의해 유도된 VEGF-A 발현을 억제함으로써 포도세포 사멸을 억제하기 위해 microRNA-16-5p를 분비한다고 제안했습니다. 이는 포도세포 표면 마커 단백질 네프린의 발현 증가와 사구체 평활근 특이적 단백질(α-SMA) 및 사멸 단백질(Bax와 Caspase-3)의 발현 감소로 입증되었습니다. 또한, USC-Exos의 정맥 내 주입 후 microRNA-16-5p가 과발현되었으며, 이는 당뇨병 쥐 모델에서 포도세포를 보호했을 가능성이 있습니다(Duan et al., 2019). 또한 Xiong 등(2020)은 USC가 신장 보호 효과를 나타내며, 신장 간질 섬유화를 억제하여 혈청 요소 질소(BUN) 및 크레아티닌(SCr) 수치 감소, 신장 조직의 섬유화 과다 증식 개선, α-SMA 발현 감소 등을 통해 이를 입증했습니다(Xiong et al., 2020).
Bladder Diseases
Bladder Reconstruction
Infection, cancer, trauma, inflammation, and iatrogenic injury can all cause bladder dysfunction, resulting in a reduced ability to effectively store and empty urine. The best method of urethral reconstruction after radical cystectomy is ileal cystoplasty or neobladder (Serrano-Aroca et al., 2018). However, bladder reconstruction using gastrointestinal tissue and other materials produce a series of sequelae and complications, such as metabolic abnormalities and chronic urinary tract infection, which substantially affect patient quality of life; thus, bladder reconstruction remains difficult. Therefore, tissue engineering has potential as an alternative method for bladder reconstruction, but it is not currently available in clinical practice and requires further study.
Utilizing the properties of basic fibroblast growth factor (bFGF) (providing a favourable microenvironment for the proliferation of mesenchymal cells and the production of ECM), Lee et al. studied a partial cystectomy rat model and found a synergistic effect between USCs and heparin-immobilized bFGF-loaded scaffolds, as demonstrated by an elevated bladder capacity, compliance or decreased inflammation and tissue regeneration. These authors proposed that this novel composite biomaterial represents a promising therapeutic strategy for bladder reconstruction and provides the possibility for the structural and functional repair of damaged tissues; however, problems, such as vascularization and neurotization, remain and must be solved before clinical application (Lee et al., 2015). Li et al. conducted an experiment on female rats with protamine/lipopolysaccharide-induced interstitial cystitis and found that USCs had a restorative effect on bladder function reconstruction by inhibiting oxidative stress, inflammatory reactions, and apoptosis (Li et al., 2017). Inflammation-related factors, such as lower IL-6 and TNFα levels and reduced mast cell infiltration, were observed in the urinary bladders of the IC control group but were markedly improved in the IC + USC groups. Although induced rat models cannot completely replicate diseases in humans, such as interstitial cystitis, these findings provide a solid basis for a prospective clinical trial.
Overactive and Underactive Bladder
Overactive bladder (OAB), manifesting as urinary urgency and frequent nocturia, is often treated with invasive botulinum toxin or neuromodulation and reconstructive surgery (Robinson and Cardozo, 2019). Large conductance voltage and Ca2+-activated K+ (BK) channels have been noted as excellent therapeutic candidates for OAB based on their effectiveness at reducing sexual excitability and the contractility of bladder smooth muscle by hyperpolarizing the membrane (Li et al., 2019). Interestingly, stem cells have multifarious ion channels that are thought to be involved in cell proliferation. Wang et al. proposed that the overexpression of BK channels in USCs can modulate cell growth (G1/S phase) and apoptosis. When these authors applied the BK channel antagonist iberiotoxin, they found elevated apoptosis rates in USCs, whereas decreased rates were observed after treatment with the BK agonist NS1619 (Wang et al., 2017b). Although these results are certainly exciting, the in vitro experiment did not necessarily reveal the same effect as the simulated experiment in the OAB models. Therefore, their study verifies only the effect of BK channels on USCs, and experimental data on the interactions of USCs are lacking. Whether USCs can serve as “vectors” to increase the effect of BK channels and therefore be useful as a treatment for OAB remains unknown.
Interestingly, the effect of USCs on underactive bladder (UAB) has been investigated. UAB is a complex urologic condition with severe complications, such as bladder outlet obstruction and stress urinary incontinence (SUI). Interstitial Cajal-like cells (ICC-LCs), pacemaker cells in the urinary system, have shown a downward trend in UAB (Feng et al., 2017) and have thus emerged as an ideal therapy to satisfactorily adjust spontaneous vesical contractions (Liu et al., 2017a; Ko et al., 2017). By transfecting lentiviral vectors with exogenous gene hyperpolarization-activated cyclic nucleotide-gated (HCN4) modification, Sun et al. inefficiently induced the directional differentiation of USCs into ICC-LCs, resulting in a morphological alteration from “rice grain”-like cells to spindle-shaped cells with multiple branches, higher expression of the ICC surface marker c-Kit, and a visible automatic depolarization current. Thus, the overexpression of HCN4 produced a preliminary ICC-LC-like phenotype in USCs. Additional studies could reveal the function of successful USC differentiation in the treatment of UAB (Sun et al., 2020).
Urethral Diseases
Stress Urinary Incontinence
Urinary incontinence (UI) is the involuntary leakage of urine through the urethra. SUI, the most common type of UI, is caused by the involuntary loss of urine caused by dysfunction of the urethral sphincter or the pelvic floor muscles. The prevalence of SUI ranges from 10 to 40% in females aged greater than 50 years (Capobianco et al., 2018).
After the injection of a mixture of USCs, microbeads, and collagen gel-type 1 into mice, an improved myogenic differentiation capacity and enhanced revascularization, innervation, and tissue regeneration were observed, highlighting the possible utilization of this strategy in SUI (Liu et al., 2013). By establishing an SUI rat model via vaginal balloon inflation, Wu et al. found that USC-Exos play a role in treating SUI, as demonstrated by improved urodynamic parameters, recovery of pubococcygeal muscle tissue, and the activation of the proliferation and differentiation of muscle satellite cells by the phosphorylation of extracellular-regulated protein kinases (Wu et al., 2019). Therefore, USCs may be a new and feasible treatment for SUI, which is worthy of further exploration.
Urinary Tract Reconstruction
The toxic effects of urine can be isolated in urothelial cells, usually obtained through bladder biopsy, which can be invasive and damaging to the donor. However, contemporary studies have illustrated the potential role of the noninvasive and unlimited nature of USCs in noninvasive urinary tract reconstruction. Thus, USC-derived endothelial cells, urothelium and functional smooth muscle cells can be used to establish urinary tract mucosa, the urinary wall and blood vessels, respectively (Abbas et al., 2020).
Zhao et al. initially used a modified technique to prepare the vessel extracellular matrix (VECM), which comprises both the vascular basement membrane and the interstitial ECM and serves as a microporous seeding-cell structure, and found that VECM is likely involved in angiogenesis based on its traits, which are similar to those of VEGF. Then, these authors differentiated USCs into urothelial and functional contractile smooth muscle phenotypes using induction media containing factors such as TGF-β1 and miR-199a-5p. Finally, these authors combined these cells with VECM to successfully construct an intact and multilayered urothelium and lamellar dense connective smooth muscle after 2 months of ureter reconstruction in a rat urethral defect model, while the control group exhibited only one layer of discontinuous epithelial cells and a few smooth muscle bundles. If the tensile and rupture strengths of such regenerated ureters are satisfactory, tissue-engineered grafts might be applied for the treatment of long-segment ureteral defects in the future (Zhao et al., 2019). Liu et al. seeded USCs on the small intestinal submucosa (SIS) of a rabbit urethral defect model; compared with the control group rabbits (received only SIS and no USCs), these rabbits exhibited an ameliorated urethral calibre, an increased urothelial regeneration speed, a greater smooth muscle content, and a higher vessel density (Liu et al., 2017b). Wan et al. successfully induced the differentiation of USCs from six healthy adult individuals into urothelial cells, and the resulting cells were phenotypically comparable to the native urothelium and functionally comparable to their tight junctions based on their barrier function and ultrastructure (Wan et al., 2018). Analogously, Yang et al. differentiated rabbit USCs that were preexposed to PDGF-BB and TGF-β1 into not only smooth muscle cells expressing α-SMA but also urothelial cells expressing urothelial-specific proteins, including AE1/AE3 and E-cadherin, by exposing the cells to epidermal growth factor (EGF) (Yang et al., 2018). Although the authors of this paper did not conduct further experiments, there are reasons to believe that these two cell types that are efficiently differentiated by USCs may be used for lower urinary tract tissue regeneration.
방광 질환방광 재건
감염, 암, 외상, 염증, 의료적 손상 등은 모두 방광 기능 장애를 유발하여 소변을 효과적으로 저장하고 배출하는 능력을 감소시킵니다. 근치적 방광 절제술 후 요도 재건의 최상의 방법은 회장 방광 성형술 또는 신방광(Serrano-Aroca et al., 2018)입니다. 그러나 위장관 조직이나 다른 재료로 방광 재건술을 시행할 경우 대사 이상, 만성 요로 감염 등 일련의 합병증이 발생하여 환자의 삶의 질에 심각한 영향을 미치며, 따라서 방광 재건술은 여전히 어려운 과제입니다. 따라서 조직 공학은 방광 재건술의 대체 방법으로 잠재력을 가지고 있지만, 현재 임상에서 사용 가능하지 않으며 추가 연구가 필요합니다.
기본 섬유아세포 성장 인자(bFGF)의 특성(중간엽 세포 증식 및 ECM 생성 촉진)을 활용해 Lee 등(2023)은 부분적 방광 절제술 쥐 모델을 연구했으며, USCs와 헤파린 고정 bFGF 함유 스캐폴드 간의 시너지 효과를 확인했습니다. 이는 방광 용량 증가, 순응도 향상, 염증 감소 및 조직 재생으로 입증되었습니다. 이 연구자들은 이 새로운 복합 생체재료가 방광 재건의 유망한 치료 전략을 제시하며 손상된 조직의 구조적 및 기능적 복원 가능성을 제공한다고 제안했습니다. 그러나 혈관화 및 신경화 문제 등이 남아 있으며 임상 적용 전 해결되어야 합니다 (Lee et al., 2015). Li 등(Li et al., 2017)은 프로타민/리포폴리사카라이드(proline/lipopolysaccharide)로 유발된 간질성 방광염을 가진 암컷 쥐를 대상으로 실험을 진행했으며, USC가 산화 스트레스, 염증 반응, 세포 사멸을 억제함으로써 방광 기능 재건에 회복 효과를 나타냈습니다(Li et al., 2017). 염증 관련 요인인 IL-6 및 TNFα 수준 감소와 비만 세포 침윤 감소가 IC 대조군 방광에서 관찰되었으나, IC + USC 그룹에서는 현저히 개선되었습니다. 유도된 쥐 모델은 간질성 방광염과 같은 인간 질환을 완전히 재현할 수는 없지만, 이러한 결과는 향후 임상 시험의 탄탄한 기반을 제공합니다.
과활동성 및 저활동성 방광
과활동성 방광(OAB)은 배뇨 급박감과 빈번한 야간 배뇨로 나타납니다. 이는 침습적 보툴리눔 독소나 신경 조절, 재건 수술로 치료됩니다(Robinson and Cardozo, 2019). 대용량 전압 및 Ca2+-활성화 K+ (BK) 채널은 성적인 흥분성과 방광 평활근 수축성을 감소시키는 데 효과적이라는 점에서 OAB의 우수한 치료 후보로 주목받고 있습니다(Li et al., 2019). 흥미롭게도 줄기세포는 세포 증식에 관여하는 것으로 추정되는 다양한 이온 채널을 보유하고 있습니다. Wang 등(Wang et al., 2017b)은 USC에서 BK 채널의 과발현이 세포 성장(G1/S 단계)과 아포토시스 조절에 영향을 미친다고 제안했습니다. 이 연구자들은 BK 채널 억제제인 iberiotoxin을 적용했을 때 USC에서 아포토시스율이 증가했으며, BK 작용제 NS1619 처리 후에는 감소했다고 보고했습니다(Wang et al., 2017b). 이러한 결과는 분명히 흥미롭지만, in vitro 실험은 OAB 모델에서 시뮬레이션된 실험과 동일한 효과를 반드시 보여주지 않았습니다. 따라서 이 연구는 BK 채널이 USCs에 미치는 효과를 검증했을 뿐이며, USCs 간의 상호작용에 대한 실험적 데이터는 부족합니다. USCs가 BK 채널의 효과를 증강시키는 '벡터'로 작용하여 OAB 치료에 유용할 수 있는지 여부는 아직 알려지지 않았습니다.
흥미롭게도 USCs가 과민성 방광(UAB)에 미치는 영향이 조사되었습니다. UAB는 방광 배출 장애와 스트레스성 요실금(SUI)과 같은 심각한 합병증을 동반하는 복잡한 비뇨기과적 질환입니다. 방광 내 Cajal 유사 세포(ICC-LCs)는 요로계의 박동 세포로, UAB에서 감소 추세를 보였으며(Feng et al., 2017), 따라서 자발적 방광 수축을 적절히 조절하는 이상적인 치료법으로 부상했습니다(Liu et al., 2017a; Ko et al., 2017). Sun 등(2020)은 외인성 유전자 과분극 활성화 사이클릭 뉴클레오티드 게이트(HCN4) 변형을 포함한 렌티바이러스 벡터를 전사하여 USC의 ICC-LC로의 방향성 분화를 비효율적으로 유도했습니다. 이 결과, “쌀알” 모양 세포에서 다중 분지 구조를 가진紡錘형 세포로의 형태학적 변화, ICC 표면 마커 c-Kit의 발현 증가, 가시적인 자동 탈분극 전류가 관찰되었습니다. 따라서 HCN4의 과발현은 USC에서 ICC-LC 유사 형질을 초래했습니다. 추가 연구는 USC 분화의 성공이 UAB 치료에 미치는 기능을 밝힐 수 있을 것입니다 (Sun et al., 2020).
요도 질환스트레스성 요실금
요실금(UI)은 요도를 통해 소변이 의도하지 않게 유출되는 현상입니다. SUI는 요도 괄약근 또는 골반저 근육의 기능 장애로 인한 소변의 의도하지 않은 유출로 인해 발생하는 가장 흔한 유형의 UI입니다. 50세 이상 여성의 SUI 유병률은 10~40%입니다(Capobianco et al., 2018).
마우스에 USC, 미세구체, 콜라겐 젤-1 혼합물을 주입한 후, 근육 분화 능력 향상, 혈관 재형성, 신경 분포, 조직 재생이 관찰되어 이 전략의 SUI 치료 가능성을 시사했습니다(Liu et al., 2013). Wu 등(2019)은 질 풍선 팽창을 통해 SUI 쥐 모델을 구축하여 USC-Exos가 SUI 치료에 역할을 한다는 것을 보여주었습니다. 이는 요역동학 파라미터 개선, 골반저근 조직 회복, 세포외 조절 단백질 키나제(ERK)의 인산화를 통해 근육 위성 세포의 증식 및 분화 활성화로 입증되었습니다(Wu et al., 2019). 따라서 USC는 SUI의 새로운 치료법으로 유망하며 추가 연구가 필요합니다.
요로 재건
요로의 독성 효과는 방광 생검을 통해 얻은 요로 상피 세포에서 분리될 수 있지만, 이는 기증자에게 침습적이고 손상을 입힐 수 있습니다. 그러나 최근 연구는 USC의 비침습적이고 무제한적인 특성이 비침습적 요로 재건에 잠재적 역할을 할 수 있음을 보여주었습니다. 따라서 USC에서 유래한 내피 세포, 요상피 및 기능적 평활근 세포는 각각 요로 점막, 요로 벽 및 혈관을 형성하는 데 사용될 수 있습니다(Abbas et al., 2020).
Zhao et al.은 혈관 외세포 기질(VECM)을 준비하기 위해 수정된 기술을 처음 사용했습니다. VECM은 혈관 기저막과 간질 ECM을 모두 포함하며 미세다공성 세포 배양 기질로 기능합니다. 이 연구진은 VECM의 특성이 VEGF와 유사하다는 점을 바탕으로 VECM이 혈관新生에 관여할 가능성이 있음을 발견했습니다. 이후 이 연구진은 TGF-β1 및 miR-199a-5p와 같은 인자를 포함한 유도 매체를 사용하여 USCs를 요상피 세포와 기능적 수축성 평활근 세포로 분화시켰습니다. 마지막으로, 이 연구진은 VECM과 결합한 세포를 쥐 요도 결손 모델에서 요관 재건 후 2개월 만에 완전하고 다층 구조의 요상피와 층상 밀집형 평활근 조직을 성공적으로 구축했으며, 대조군에서는 단일층의 불연속 상피 세포와 소수의 평활근 뭉치만 관찰되었습니다. 이러한 재생 요관의 인장 강도와 파열 강도가 만족스럽다면, 조직 공학 이식편은 미래에 장구간 요관 결손의 치료에 적용될 수 있을 것입니다 (Zhao et al., 2019). Liu 등(2017b)은 토끼 요도 결손 모델의 소장 점막하층(SIS)에 USCs를 이식했습니다. 대조군 토끼(SIS만 이식받고 USCs는 받지 않은 그룹)와 비교했을 때, 이식군 토끼는 요도 직경이 개선되었으며, 요상피 재생 속도가 증가했고, 평활근 함량이 더 높았으며, 혈관 밀도가 더 높았습니다(Liu et al., 2017b). Wan 등(Wan et al., 2018)은 6명의 건강한 성인에서 추출한 USCs를 요상피 세포로 분화시키는 데 성공했으며, 분화된 세포는 원시 요상피와 형질적으로 유사했으며, 장벽 기능과 초미세 구조를 기반으로 한 밀접 연결 기능에서도 유사했습니다. 유사하게, 양 등(Yang et al.)은 PDGF-BB와 TGF-β1에 사전 노출된 토끼 USCs를 상피 성장 인자(EGF)에 노출시켜 α-SMA를 발현하는 평활근 세포뿐만 아니라 AE1/AE3 및 E-cadherin과 같은 요로 상피 특이적 단백질을 발현하는 요로 상피 세포로 분화시켰습니다(Yang et al., 2018). 이 논문의 저자들은 추가 실험을 수행하지 않았지만, USCs에 의해 효율적으로 분화되는 이 두 세포 유형이 하부 요로 조직 재생에 활용될 수 있다는 근거가 있습니다.
Diabetes
Diabetes is characterized by pancreatic β-cell destruction and insulin resistance and is well known as the ninth leading cause of death. Approximately 451 million people have been diagnosed with diabetes, and 5 million people died from its multiple comorbidities in 2018 or “and 5 million people have died from its multiple comorbidities since 2018 (Amanat et al., 2020; Lu and Zhao, 2020).” Although islet transplantation and replacement of pancreatic β-cells may serve as practical curative strategies, existing data support the applicability of USCs and as a new strategy for the treatment of diabetes.
Studies have confirmed that isolated USCs can differentiate into insulin-producing β cells (Hwang et al., 2019) and promote their survival and pancreatic islet angiogenesis (Zhao et al., 2018), which is suitable for the treatment of diabetes. USCs can be converted into insulin-producing cells, expressing insulin and glucagon mRNA and protein and secreting insulin in response to glucose stimulation. Due to their relatively more abundant source, rebuilding functional insulin-producing cells differentiated from USCs is better than performing organ grafting (Hwang et al., 2019). Accordingly, after USC transplantation resulted in islet vascular regeneration, improved glucose tolerance and islet morphology and enhanced insulin content were observed in MLD-STZ-treated mice, and it can be inferred that USCs may contribute to the survival of β cells by promoting the revascularization of islets. Moreover, improved blood glucose levels were observed in mice injected with USCs with high-dose STZ (Zhao et al., 2018). Unexpectedly, Dong et al. showed that the tail vein injections of USCs six times per week did not markedly reduce the fasting glucose levels in type II diabetic rats (Dong et al., 2016). Similarly, Ouyang et al. found that USCs had no significant effect on blood glucose after injecting USCs once into a sponge to investigate their effects on diabetic ED (Ouyang et al., 2014). Given that other studies investigating USCs showed improved glucose tolerance in diabetic animals, these results seem contradictory. Among the various approaches, intrapancreatic injections of USCs may be the most efficient approach, while intravenous injections have a limited effect on improving blood glucose because of the risk of trapping in the lung capillary (Dong et al., 2016). After some speculation, the conflicting data indicate that the dose and route of injection play a key role in treatment.
Complications of diabetes, including diabetic cardiomyopathy, kidney disease, neuropathy, retinopathy and bladder disease, are serious problems and can even be life-threatening (Cole and Florez, 2020). Because of their multidirectional differentiation and paracrine function, USCs are believed to be effective at reducing the loss of other tissues caused by diabetes. Dong et al. injected USCs into rats and found only small amounts of USCs in the pancreas and kidneys, while no USCs were observed in the heart and bladder. Additionally, these authors concluded that USCs could inhibit cell apoptosis and decrease the fibrosis index via a paracrine signalling mechanism, thereby improving left ventricular function and myocardial remodelling, rescuing glomerular function and increasing detrusor contractility (Dong et al., 2016). In summary, USCs may be a promising new and feasible strategy for the treatment of diabetes and its complications.
당뇨병
당뇨병은 췌장 β-세포 파괴와 인슐린 저항성을 특징으로 하며, 제9의 주요 사망 원인으로서 잘 알려져 있습니다. 2018년 기준 약 4억 5,100만 명이 당뇨병으로 진단받았으며, 500만 명이 당뇨병의 다양한 합병증으로 사망했습니다(Amanat et al., 2020; Lu and Zhao, 2020). 췌도 이식 및 췌장 β-세포 대체는 실용적인 치료 전략으로 작용할 수 있지만, 기존 데이터는 USCs의 적용 가능성과 당뇨병 치료를 위한 새로운 전략으로서의 역할을 지원합니다.
연구 결과, 분리된 USCs는 인슐린을 생성하는 β-세포로 분화할 수 있으며 (Hwang et al., 2019), 그 생존과 췌장 췌도 혈관新生을 촉진합니다 (Zhao et al., 2018), 이는 당뇨병 치료에 적합합니다. USCs는 인슐린과 글루카곤 mRNA 및 단백질을 발현하고 포도당 자극에 반응하여 인슐린을 분비하는 인슐린 분비 세포로 전환될 수 있습니다. 상대적으로 풍부한 공급원 때문에 USCs에서 분화한 기능적 인슐린 분비 세포를 재건하는 것이 장기 이식보다 우수합니다(Hwang et al., 2019). 이에 따라 USC 이식 후 췌도 혈관 재생, 포도당 내성 개선, 췌도 형태 개선 및 인슐린 함량 증가가 MLD-STZ 처리 마우스에서 관찰되었으며, USC가 췌도 재혈관화를 촉진함으로써 β 세포 생존에 기여할 수 있음을 추론할 수 있습니다. 또한 고농도 STZ를 투여받은 마우스에 USC를 주사한 경우 혈당 수치가 개선되었습니다(Zhao et al., 2018). 예상치 않게 Dong et al.은 주 6회 꼬리 정맥 주사로 USCs를 투여한 경우 제2형 당뇨병 쥐의 공복 혈당 수치가 유의미하게 감소하지 않았다고 보고했습니다 (Dong et al., 2016). 유사하게 Ouyang et al.은 당뇨병성 ED에 대한 USCs의 효과를 조사하기 위해 스폰지에 USCs를 한 번 주입한 후 혈당에 유의미한 영향을 미치지 않았다고 발견했습니다 (Ouyang et al., 2014). 다른 연구에서 USCs가 당뇨병 동물에서 혈당 내성을 개선했다는 결과와 비교할 때, 이러한 결과는 모순되는 것처럼 보입니다. 다양한 접근법 중 USCs의 췌장 내 주사가 가장 효율적인 방법일 수 있으며, 정맥 내 주사는 폐 모세혈관에서의 포획 위험으로 인해 혈당 개선에 제한적인 효과를 보입니다(Dong et al., 2016). 일부 추측에 따르면, 상반된 데이터는 투여량과 주사 경로가 치료에 핵심적인 역할을 한다는 것을 시사합니다.
당뇨병의 합병증인 당뇨병성 심근병증, 신장 질환, 신경병증, 망막병증 및 방광 질환은 심각한 문제이며 생명에 위협을 줄 수 있습니다(Cole and Florez, 2020). 다방향 분화 능력과 파라크린 기능을 갖춘 USC는 당뇨병으로 인한 다른 조직 손실을 줄이는 데 효과적일 것으로 추정됩니다. 동 등(Dong et al.)은 쥐에 USCs를 주입한 결과 췌장과 신장에서만 소량의 USCs가 관찰되었으며, 심장과 방광에서는 USCs가 관찰되지 않았습니다. 또한 이 연구진은 USCs가 파라크린 신호 전달 메커니즘을 통해 세포 사멸을 억제하고 섬유화 지수를 감소시켜 좌심실 기능과 심근 재형성을 개선하며, 사구체 기능을 회복시키고 방광 수축력을 증가시킨다고 결론지었습니다(Dong et al., 2016). 요약하면, USCs는 당뇨병 및 그 합병증 치료를 위한 유망한 새로운 치료 전략으로 활용될 수 있습니다.
Digestive System Diseases
Hepatocyte transplantation (HCT), a cell-based therapy, can be used to treat congenital metabolic disease and acute and chronic liver failure in patients lacking suitable donors (Anderson and Zarrinpar, 2018). Hu et al. found that a small number of USCs differentiated into hepatocytes after coincubation with hepatic progenitor cells, which indicated that USCs can be an alternative autologous stem cell source for HCT (Hu et al., 2020). Moreover, the transplantation of USCs into an acute liver injury model improved the levels of serum markers such as alanine aminotransferase (ALT) and aspartate aminotransferase (AST) and partially ameliorated pathological changes, indicating that USCs can partially restore liver function after acute liver injury (Hu et al., 2020). A hypoxic preconditioning strategy may influence the adaptation of transplanted cells in vivo. It has been reported that after hypoxic pretreatment, the liver recovery efficiency of USCs is slightly enhanced by the induction of autophagy in a chronic liver fibrosis mouse model (Hu et al., 2020). In addition, C-X-C motif chemokine (CXC) receptor 4 (CXCR4) was significantly upregulated in USCs after hypoxic preconditioning and then interacted with the (CXC) ligand 12 (CXCL12) (an important chemokine for cell transport and homing) expressed at high levels in damaged liver tissues, thus promoting the proliferation, colony formation and migration of USCs (Hu et al., 2021). Moreover, the cell fusion rate between USCs and hepatocytes was increased after hypoxic preconditioning, and these polyploid stem cells may be involved in liver regeneration (Hu et al., 2021). All of these findings confirm the value of hypoxic preconditioning in improving the therapeutic efficacy of USCs in patients with end-stage liver disease.
Although studies investigating USCs in the digestive system are limited, we can reasonably infer the mechanism based on existing research. As mentioned above, USCs can participate in negative immune regulation. It is well known that the gastrointestinal tract is the largest immune organ in the human body and contains numerous immune cells, gut microbes and their metabolites, which can alter immune homeostasis. In contrast, alteration of the intestinal flora can upset this balance and lead to a series of inflammatory reactions (Pickard et al., 2017). Thus, it is reasonable to assume that USCs may play a nonnegligible role the treatment of inflammatory bowel diseases, such as Crohn’s disease and ulcerative colitis. Moreover, USCs are highly significant in angiogenesis; thus, ischaemic bowel disease may be fundamentally curable by vascular remodelling based on intestinal wall ischaemia caused by mesenteric artery stenosis or occlusion mostly in elderly patients with atherosclerosis. More experiments are needed to test these hypotheses (Table 1).
소화기 질환
간세포 이식(HCT)은 적합한 기증자가 없는 환자의 선천성 대사 질환 및 급성 및 만성 간부전을 치료하기 위한 세포 기반 치료법입니다(Anderson and Zarrinpar, 2018). Hu 등(2020)은 간 전구세포와 동시 배양 후 소수의 USCs가 간세포로 분화되었음을 발견했으며, 이는 USCs가 HCT를 위한 대체 자가 줄기세포 소스로 활용될 수 있음을 시사합니다(Hu et al., 2020). 또한 급성 간 손상 모델에 USCs를 이식한 결과, 알라닌 아미노전달효소(ALT) 및 아스파르테이트 아미노전달효소(AST)와 같은 혈청 마커 수치가 개선되었으며 병리학적 변화가 부분적으로 완화되어 USCs가 급성 간 손후 간 기능을 부분적으로 회복시킬 수 있음을 보여주었습니다(Hu et al., 2020). 저산소 전처리 전략은 생체 내 이식된 세포의 적응에 영향을 미칠 수 있습니다. 저산소 전처리 후, 만성 간 섬유증 마우스 모델에서 자가포식이 유도되어 USC의 간 회복 효율이 약간 향상된 것으로 보고되었습니다 (Hu et al., 2020). 또한, C-X-C 모티프 케모카인(CXC) 수용체 4(CXCR4)는 저산소 전처치 후 USCs에서 유의미하게 상향 조절되었으며, 손상된 간 조직에서 고농도로 발현되는 (CXC) 리간드 12(CXCL12)(세포 이동 및 귀환에 중요한 케모카인)와 상호작용하여 USCs의 증식, 콜로니 형성 및 이동을 촉진했습니다(Hu et al., 2021). 또한 저산소 전처치 후 USCs와 간세포 간의 세포 융합률이 증가했으며, 이 다배체 줄기세포는 간 재생에 관여할 수 있습니다(Hu et al., 2021). 이러한 모든 결과는 말기 간 질환 환자의 USCs 치료 효과를 개선하는 데 저산소 전처치의 가치를 확인합니다.
소화계에서 USCs를 연구한 연구는 제한적이지만, 기존 연구를 바탕으로 메커니즘을 합리적으로 추론할 수 있습니다. 위에서 언급된 바와 같이 USCs는 음성 면역 조절에 참여합니다. 소화관은 인체에서 가장 큰 면역 기관으로, 수많은 면역 세포, 장 미생물 및 그 대사산물을 포함하며, 이는 면역 균형을 변화시킬 수 있습니다. 반면, 장내 미생물군의 변화는 이 균형을 깨뜨리고 염증 반응의 연쇄 반응을 유발할 수 있습니다 (Pickard et al., 2017). 따라서 USC가 크론병과 궤양성 대장염과 같은 염증성 장 질환의 치료에 무시할 수 없는 역할을 할 수 있다는 가설을 제기할 수 있습니다. 또한 USC는 혈관新生에 매우 중요하며, 따라서 장벽 허혈로 인한 장 허혈 질환은 주로 동맥경화증을 가진 노인 환자에서 장간막 동맥 협착 또는 폐쇄로 인해 발생하는 장벽 허혈을 기반으로 한 혈관 재형성으로 근본적으로 치료 가능할 수 있습니다. 이러한 가설을 검증하기 위해 추가 실험이 필요합니다 (표 1).
TABLE 1.
USC-based therapies for various diseases of bodily systems.
DiseaseModelMechanismObservations
| Renal diseases | Chronic kidney disease | Chronic kidney disease (CKD) rat models | Antioxidative stress and antifibrotic activity | Reduced degrees of glomerular sclerosis and atrophic renal tubules, improved SCr and GFR Zhang et al. (2020a) |
| Renal transplantation | USC | Decreased SSEA4 levels and gradual upregulation of kidney differentiation-related markers | Assessment of renal cell-lineage differentiation ability Choi et al. (2017) | |
| Acute kidney injury | Rat models of ischaemic AKI | USC-based treatment | Upregulated levels of interleukin-10 and TGF-β1, downregulated levels of interferon-γ and IL-1β Tian et al. (2017) | |
| Models of cisplatin-induced AKI | USC treatment in vivo; coculture of cisplatin-induced NRK-52E cells with USCs in vitro | Reduced BUN and SCr levels; higher cell viability and a lower apoptosis in vitro Sun et al. (2019) | ||
| Diabetic nephropathy | STZ-induced rat models | USC-Exo treatment | Increased urine volume and albumin, downregulation of the podocyte survival factor BMP-7 Jiang et al. (2016) | |
| Podocytes treated with USC-Exos | Synergistic effect of USC-Exos and microRNA-16-5p | Protects podocytes via VEGFA Duan et al. (2019) | ||
| Renal tissues | USC-targeted treatment | Reduced levels of BUN and SCr, improved fibrous hyperplasia, reduced expression of α-SMA Xiong et al. (2020) | ||
| Bladder diseases | Bladder reconstruction | Partial cystectomy rat model | Heparin-immobilized basic fibroblast growth factor-loaded scaffolds | Elevated bladder capacity, compliance or decreased inflammation and tissue regeneration Lee et al. (2015) |
| Overactive bladder | Large conductance voltage and Ca2+-activated K+ (BK) channels in USCs | Overexpression of BK channels in USCs | The BK channel antagonist iberiotoxin increased the apoptosis of USCs; USC apoptosis was decreased by treatment with the BK agonist NS1619 Wang et al. (2017b) | |
| Underactive bladder | Preliminary ICC-LC-like phenotype of USCs | Differentiation of USCs into ICC-LCs by the transfection of lentiviral vectors with exogenous gene modifications | Higher c-Kit expression, an automatic depolarization current Sun et al. (2020) | |
| Urethral diseases | Stress urinary incontinence | Mice | Injection of USCs, microbeads and the collagen gel-type 1 | Improved myogenic differentiation, enhanced revascularization and innervation, tissue regeneration Liu et al. (2013) |
| SUI rat models | Treatment of USC-Exos with phosphorylated extracellular-regulated protein kinases | Improved urodynamic parameters, recovered pubococcygeus muscle tissue Wu et al. (2019) | ||
| Urinary tract reconstruction | USCs; tissue-engineered grafts | Induction of media with components such as TGF-β1 and miR-199a-5p | Differentiation of USCs into urothelial and functional contractile smooth muscles Zhao et al. (2019) | |
| Urethral defect rabbit models | Seeding of USCs onto the small intestinal submucosa | Ameliorated urethral calibres, sped up urothelial regeneration, increased smooth muscle content Liu et al. (2017b) | ||
| USCs from healthy adults | Induction of USC differentiation into urothelial cells | Structures phenotypically and functionally comparable to those of the native urothelium Wan et al. (2018) | ||
| USCs from rabbits | Exposure to PDGF-BB and TGF-β1 | High expression of α-SMA and urothelial-specific proteins (AE1/AE3 and E-cadherin) Yang et al. (2018) | ||
| Diabetes | USCs | Conversion to insulin-producing cells | High mRNA levels of the pancreatic transcription factors Pdx1, insulin and glucagon Hwang et al. (2019) | |
| Transplanted USCs from mice that were injected with high-dose STZ | USC transplantation to promote islet vascular regeneration | Improved glucose tolerance and islet morphology, enhanced insulin content, improved blood glucose Zhao et al. (2018) | ||
| Type II diabetic rats | Tail vein injection of USCs six times every week | Did not markedly reduce fasting glucose levels Dong et al. (2016) | ||
| Mice | Single injection of USCs into a sponge | Had no significant effect on blood glucose Ouyang et al. (2014) | ||
| Digestive system diseases | Hepatocyte transplantation | Chronic liver fibrosis mouse model | Promotion of autophagy, proliferation, colony formation, migration and cell fusion | Enhanced liver recovery efficiency Hu et al. (2020), Hu et al. (2021) |
| Nervous system diseases | Neurogenesis | Mouse brain | Seeding of USCs onto a hydrogel scaffold and transplantation into the rat brain | Survived at the lesion site with a great growth rate, differentiated into neuron-like cells Guan et al. (2014) |
| USCs | Combination of laminin and platelet-derived growth factor-BB | Increased levels of neuronal markers (MAP2, NFM and NeuN) Kim et al. (2018) | ||
| USCs in chemical-only induction protocol | Induction of ISX9, I-BET and RA; improved conversion of USCs into neuronal cells | Increased levels of neuron-specific markers (Tuj1, Map2 and Tau), improvement of electrophysiological properties Liu et al. (2020b) | ||
| Spinal cord injury | Spinal cord injury rat models | Elevated expression levels of nerve growth factors and brain-derived neurotrophic factors | Improved motor function in rats Li and Wu (2017), Chen et al. (2018b) | |
| Ischaemic stroke | Rat models of ischaemic stroke | USC‐Exo injection; increased number of EdU+/Nestin+ cells in the subventricular zone | Attenuated neurological deficits, reduced infarct volume Ling et al. (2020) | |
| Oxygen‐glucose deprivation/reoxygenation-processed NSCs | USC‐Exos; exosomal microRNA‐26a | Exerted neurogenic effects on the suppression of histone deacetylase 6 (HDAC6) Ling et al. (2020) | ||
| Locomotor system diseases | Osteoporosis | Ovariectomized rat models | USC-EVs; mediated by the collagen triple-helix repeat containing 1 (CTHRC1) and osteoprotegerin (OPG) proteins | Increased bone mass, effective for the treatment of osteoporosis Chen et al. (2019) |
| Treatment of USC-EVs to promote osteoblastic bone formation | High levels of osteoblast formation-related mRNAs (osteocalcin, Alp, and Runx2) Chen et al. (2019) | |||
| Muscle regeneration | Mice | USCs promote skeletal muscle regeneration | Specific skeletal muscle lineage cell transcripts and protein markers such as myf5, myoD and myosin Chen et al. (2017) | |
| USCs | Combination of USCs and growth factors; hyaluronic-heparin hydrogel scaffold | Increased muscular cell survival rate Liu et al. (2020a) | ||
| Mice with hindlimb suffering due to ischaemia | Transplantation of USC-EVs; angiogenesis | HMEC-1 and C2C12 cell proliferation, muscle regeneration Zhu et al. (2018) | ||
| Cutaneous regeneration and wound healing | Rabbit full-thickness skin defect models | Uses of biocompatible polycaprolactone/gelatine nanofibrous membrane scaffolds | Improved wound contraction, skin appendage regeneration, reepithelialization and neovascularization Fu et al. (2014) | |
| Human umbilical vein endothelial cells (HUVECs) | Significantly enhanced the proliferation, motility and tube formation ability of HUVECs Fu et al. (2014) | |||
| Endothelial cells, full-thickness excisional wounds | Paracrine effects | Improved the proliferation of endothelial cells, promoted fibroblast differentiation, increased the levels of vWF, collagen and fibronectin Zhang et al. (2018) | ||
| Rat full-thickness skin wound models | Proliferation and survival of EAhy926 cells | Accelerated collagen deposition and angiogenesis Cao et al. (2019) | ||
| Seeding of USCs onto a small SIS scaffold in preconditioned hypoxia | Increased the secretion of VEGF, collagen and elastic fibre s Zhang et al. (2020c) | |||
| Streptozotocin-induced diabetic mice | High expression of DMBT1 | Sped up revascularization and collagen deposition Chen et al. (2018a) | ||
| Periodontal tissue engineering | Human periodontal ligament stem cells (PDLSCs) | Noncontact coculture of USCs; improved proliferation and osteoblastic/cementoblastic differentiation of PDLSCs | Increased the density of collagen layers, the levels of the cementogenic protein and ALP activity Yang et al. (2020) | |
| ECM derived from USCs | Enhanced proliferation, osteogenic differentiation potential, and angiogenesis Xiong et al. (2019b) | |||
| Erectile dysfunction | Bilateral cavernous nerve injury (CNI) rat models | Injection of USCs; lower rate of cell apoptosis | Markedly increased the ICP level and the ICP/MAP ratio, increased the ratio of smooth muscle to collagen in the corpus cavernosum Chen et al. (2018c) | |
| USCs modified with pigment epithelium-derived factor (PEDF); antiapoptosis | Exerted protective effects on nerves and ECs in subjects with erectile function Yang et al. (2016) | |||
| Male rat models of streptozotocin injection | Treatment with USC-EVs | Increased endothelial expression and the smooth muscle content, increased the ICP level and the ICP/MAP ratio Ouyang et al. (2019) | ||
| DED rats | USC-EVs; treatment | Increased endothelial expression and the smooth muscle content, increased the ICP level and the ICP/MAP ratio Zhou et al. (2019) |
Nervous System Diseases
Due to the absence of transplantable human neurons and insufficient technological means of neuron proliferation, challenges remain in the clinical treatment of neuronal apoptosis caused by spinal cord injury, acute brain ischaemia and neurodegenerative diseases (Fricker et al., 2018). The capacity of USCs to differentiate into neurons brings great hope for the revitalization of neurons, but increasing their proliferation and differentiation is urgently required. USCs have been proven to be important elements in the field of neuronal regenerative medicine. In addition, as a useful noninvasive cell source for disease modelling, USCs have high proliferation and differentiation capabilities and have great potential in neurological disease modelling (Shi and Cheung, 2021).
After seeding USCs onto hydrogel scaffolds and transplanting them into rat brains, Guan et al. found that USCs could not only survive at the lesion site with an excellent growth rate but also differentiate into neuron-like cells expressing neural phenotype-related proteins (Guan et al., 2014). In a study by Kim et al., the combination of laminin and platelet-derived growth factor-BB had a synergistic effect on the differentiation potential of USCs, as indicated by increased levels of neuronal markers, such as MAP2, NFM and NeuN (Kim et al., 2018). Additionally, Liu et al. used a chemical-only induction protocol involving the neuronal differentiation inducer ISX9, the disrupter of nonneuronal genes I-BET, and a metabolite of vitamin A1 (namely, RA) and observed that this treatment led to the improved conversion of USCs into neuronal cells based on the detection of the neuron-specific markers Tuj1, Map2 and Tau and their electrophysiological properties (Liu et al., 2020b). Clearly, USCs help with neurogenesis.
Regarding the therapeutic effects of USCs on diseases, Chen et al. transplanted USCs and chABC in combination into the impaired spinal cords of rats to evaluate functional injuries in their lower extremities, and both groups showed significantly improved motor function, which was attributed to the elevated expression of nerve GF and brain-derived neurotrophic factor (Li and Wu, 2017; Chen et al., 2018b). Notably, in rat models of ischaemic stroke, Ling et al. demonstrated that the injection of USC-Exos could attenuate neurological deficits and promote neuronal recovery, as indicated by a reduced infarct volume and enhanced neurogenesis. An increased number of EdU+/Nestin+ cells was observed in the subventricular zone, where adult neural stem cells (NSCs) mainly reside (Ling et al., 2020). In addition, using oxygen-glucose deprivation/reoxygenation-processed NSCs as in vitro models, these authors found that USC-Exos could transfer microRNA-26a to induce the degradation of histone deacetylase 6 (HDAC6) mRNA and inhibit the translation of HDAC6 mRNA, thereby increasing the self-renewal and differentiation of NSCs (Ling et al., 2020). The proneurogenic effects of USC-Exos in vivo may be related to the role of the miR-26a/HDAC6 axis, but further studies are needed for verification. In conclusion, USCs can enhance the proliferation and differentiation of neurons, providing a new idea for the treatment of diseases related to neuronal apoptosis.
신경계 질환
이식 가능한 인간 신경세포의 부재와 신경세포 증식 기술의 부족으로 인해 척수 손상, 급성 뇌 허혈 및 신경퇴행성 질환으로 인한 신경세포 사멸의 임상적 치료에 도전 과제가 남아 있습니다 (Fricker et al., 2018). USCs의 신경세포 분화 능력은 신경세포 재생에 큰 희망을 제시하지만, 그 증식 및 분화 능력을 향상시키는 것이 시급합니다. USCs는 신경 재생 의학 분야에서 중요한 요소로 입증되었습니다. 또한 질병 모델링을 위한 유용한 비침습적 세포원으로, 높은 증식 및 분화 능력을 갖추고 있어 신경 질환 모델링에 큰 잠재력을 가지고 있습니다(Shi and Cheung, 2021).
USCs를 하이드로겔 스캐폴드에 접종하고 쥐 뇌에 이식한 후, Guan 등(2014)은 USCs가 손상 부위에서 우수한 성장 속도로 생존할 뿐만 아니라 신경 세포와 유사한 세포로 분화하여 신경 세포 관련 단백질을 발현한다는 것을 발견했습니다(Guan et al., 2014). Kim 등(2018)의 연구에서 라미닌과 혈소판 유래 성장 인자-BB의 조합은 신경 마커인 MAP2, NFM 및 NeuN의 수준 증가를 통해 USCs의 분화 잠재력에 시너지 효과를 나타냈습니다(Kim et al., 2018). 또한 Liu 등(2020)은 신경 분화 유도제 ISX9, 비신경 세포 유전자 억제제 I-BET, 비타민 A1의 대사산물(즉, RA)을 포함한 화학물질 단독 유도 프로토콜을 사용했습니다. 이 치료는 신경 특이적 마커인 Tuj1, Map2 및 Tau의 검출과 전기생리학적 특성 개선을 통해 USCs의 신경 세포로의 전환이 향상되었음을 관찰했습니다(Liu et al., 2020b). 분명히 USCs는 신경 발생에 도움을 줍니다.
USCs의 질병 치료 효과에 대해 Chen et al.은 쥐의 손상된 척수에 USCs와 chABC를 결합하여 이식하고 하체 기능 손상을 평가했으며, 두 그룹 모두 운동 기능이 유의미하게 개선되었으며 이는 신경 성장 인자(GF)와 뇌유래 신경 영양 인자(BDNF)의 발현 증가에 기인한 것으로 나타났습니다(Li and Wu, 2017; Chen et al., 2018b). 특히, 허혈성 뇌졸중 쥐 모델에서 Ling 등(2020)은 USC-Exos 주사가 신경학적 결손을 완화하고 신경 회복을 촉진함을 보여주었습니다. 이는 뇌경색 부피 감소와 신경생성 증가로 나타났으며, 성인 신경 줄기세포(NSCs)가 주로 존재하는 뇌실하 영역에서 EdU+/Nestin+ 세포 수가 증가했습니다(Ling et al., 2020). 또한 산소-포도당 박탈/재산소화 처리된 NSC를 in vitro 모델로 사용한 연구에서, 이 연구진은 USC-Exos가 microRNA-26a를 전달하여 히스톤 탈아세틸화 효소 6(HDAC6) mRNA의 분해를 유도하고 HDAC6 mRNA의 번역을 억제함으로써 NSC의 자기 재생 및 분화를 증가시킨다는 것을 발견했습니다(Ling et al., 2020). USC-Exos의 신경유도 효과는 miR-26a/HDAC6 축의 역할과 관련될 수 있지만, 추가 연구가 필요합니다. 결론적으로, USCs는 신경 세포의 증식과 분화를 촉진하여 신경 세포 사멸과 관련된 질환의 치료에 새로운 아이디어를 제공합니다.
Locomotor System Diseases
Osteoporosis
Osteoporosis, characterized by a reduced bone mineral density and decreased bone strength, is a systemic bone disorder that predisposes patients to an increased risk of fracture; its pathogenesis is ascribed to the apoptosis of OBs and the proliferation of osteoclasts (OCs) (Miller, 2016). Because EVs secreted by USCs are capable of promoting healing in various damaged parenchymal tissues, researchers are attempting to use them to treat osteoporosis (Riazifar et al., 2017).
Chen et al. speculate that USC-EVs may promote bone formation and prevent the development of osteoporosis. To investigate this hypothesis, they used heterogeneous rat models of different ages, sexes and health conditions to confirm that USC-EVs express and mediate the collagen triple helium repeat containing 1 (CTHRC1) and bone protein (OPG) proteins and thereby promote bone formation and inhibit bone formation. How these proteins are sorted into USC-EVs and then reused by recipient cells remains unclear, and their effectiveness in preventing osteoporosis requires further investigation (Chen et al., 2019). The ability of USCs to proliferate and differentiate into OBs can be used for not only the treatment of osteoporosis but also the repair of large segmental bone defects (Liu et al., 2021). In addition to their remarkable osteogenic ability, USCs have a cartilage repair effect similar to that of BMSCs in vivo and can be used as a stem cell replacement for cartilage regeneration, providing a powerful platform for clinical transformation (Sun et al., 2021). Some researchers have pointed out that USCs may serve as a new treatment option for osteoporosis.
Muscle Regeneration
Skeletal muscle is one of the largest organs in the human body. Healthy and complete skeletal muscle has decisive effects on human health and quality of life. Muscle injury and regeneration imbalance lead to the occurrence and development of diseases, and while muscle satellite stem cells (MuSCs) are the main source of muscle regeneration, their function gradually decreases over time. Therefore, alternative therapies are urgently needed (Yamakawa et al., 2020). USCs have the potential for myoblast differentiation and may be significant candidates for skeletal muscle regeneration, as indicated by their expression of specific skeletal muscle lineage transcripts and protein markers, such as myf5, myoD, and myosin (Chen et al., 2017).
After the implantation of USCs cultured in myogenic differentiation medium into the anterior tibialis muscles of mice, skeletal muscle lineage cell markers were found to be stably expressed, suggesting that USCs play a role in skeletal muscle regeneration (Chen et al., 2017). Since long-term muscular conversion from USCs in vitro always leads to high cell death and low differentiation, researchers have explored novel methods to improve their survival rate in vivo by applying primary USCs to a hyaluronic-heparin hydrogel containing various GFs, such as myogenic-related IGF1, HGF, and PDGF-BB. The increased cell survival rate and the expression of myogenic and endothelial cell markers revealed the combinatory effect of USCs and GFs on muscle tissue engineering (Liu et al., 2020a). After transplanting USC-EVs into mouse hindlimbs suffering from ischaemia, remarkably higher levels of angiogenesis, HMEC-1 and C2C12 cell proliferation, and muscle regeneration were observed by Zhu et al. (2018). Thus, their achievement suggests a novel therapy for attenuating hindlimb ischaemic injury in the future.
운동계 질환
골다공증
골다공증은 골밀도 감소와 골 강도 저하를 특징으로 하는 전신성 골 질환으로, 골절 위험을 증가시키며, 그 병인은 OB의 사멸과 골세포(OC)의 증식에 기인합니다(Miller, 2016). USCs에서 분비되는 엑소좀(EVs)이 다양한 손상된 실질 조직의 치유를 촉진할 수 있다는 점에서 연구자들은 이를 골다공증 치료에 활용하려는 시도를 진행 중입니다(Riazifar et al., 2017).
Chen 등(2019)은 USC-EVs가 골 형성을 촉진하고 골다공증의 발병을 예방할 수 있다고 추측했습니다. 이 가설을 검증하기 위해 그들은 다양한 연령, 성별 및 건강 상태의 이질적인 쥐 모델을 사용해 USC-EVs가 콜라겐 삼중 헬릭스 반복 구조를 포함하는 1(CTHRC1)과 골 단백질(OPG) 단백질을 발현하고 전달하며, 이를 통해 골 형성을 촉진하고 골 형성을 억제한다는 사실을 확인했습니다. 이 단백질이 USC-EV에 분류되는 메커니즘과 수신 세포에 의해 재사용되는 과정은 아직 명확하지 않으며, 골다공증 예방 효과는 추가 연구가 필요합니다 (Chen et al., 2019). USC의 증식 및 OB로 분화 능력은 골다공증 치료뿐 아니라 대규모 골절 부위 재생에도 활용될 수 있습니다 (Liu et al., 2021). USCs는 뛰어난 골형성 능력 외에도 BMSCs와 유사한 연골 재생 효과를 in vivo에서 보여주며, 연골 재생 위한 줄기세포 대체제로 활용될 수 있어 임상 적용을 위한 강력한 플랫폼을 제공합니다(Sun et al., 2021). 일부 연구자들은 USCs가 골다공증의 새로운 치료 옵션으로 활용될 수 있다고 지적했습니다.
근육 재생
골격근은 인체에서 가장 큰 기관 중 하나입니다. 건강하고 완전한 골격근은 인간의 건강과 삶의 질에 결정적인 영향을 미칩니다. 근육 손상과 재생 불균형은 질병의 발생과 진행을 초래하며, 근육 위성 줄기세포(MuSCs)가 근육 재생의 주요 원천이지만 그 기능은 시간이 지남에 따라 점차 감소합니다. 따라서 대체 치료법이 시급히 필요합니다(Yamakawa et al., 2020). USCs는 골격근 분화 잠재력을 갖추고 있으며, myf5, myoD, 마이오신(myosin)과 같은 특정 골격근 계통 전사체 및 단백질 마커의 발현을 통해 골격근 재생의 중요한 후보로 제시되고 있습니다(Chen et al., 2017).
마우스의 전경골근에 근육 분화 배지에서 배양된 USCs를 이식한 후, 골격근 계통 세포 표지자가 안정적으로 발현되었으며, 이는 USCs가 골격근 재생에 역할을 한다는 것을 시사합니다(Chen et al., 2017). USCs의 장기적인 근육 전환은 in vitro에서 항상 높은 세포 사멸과 낮은 분화율을 초래하기 때문에, 연구자들은 다양한 성장 인자(GFs)를 함유한 히알루론산-헤파린 하이드로겔에 원시 USCs를 적용하여 in vivo에서의 생존율을 개선하기 위한 새로운 방법을 탐구해 왔습니다. 세포 생존율 증가와 근육 및 내피 세포 표지자의 발현은 USC와 성장 인자의 근육 조직 공학에 대한 복합적 효과를 보여주었습니다(Liu et al., 2020a). 허혈을 겪은 쥐의 후지부에 USC-EV를 이식한 후, Zhu et al. (2018)은 혈관新生, HMEC-1 및 C2C12 세포 증식, 근육 재생이 현저히 증가한 것을 관찰했습니다. 따라서 이 성과는 미래에 후지 허혈성 손상을 완화하는 새로운 치료법으로 제안됩니다.
Other Diseases
Cutaneous Regeneration and Wound Healing
Appropriate skin tissue scaffolds can promote wound healing, but the lack of appropriate scaffold materials is an obstacle in skin tissue engineering. The available data have shown that USCs combined with some novel biomaterials can promote neovascularization, which is a crucial part of the wound healing process. As a result, USCs, which have multidirectional differentiation potential, have become an important strategy for the construction of engineered skin tissue to promote the healing of extensive skin injuries caused by wounds, ulcers, burns and inflammation.
Fu and coworkers fabricated biocompatible polycaprolactone/gelatine nanofibrous membranes as scaffolds for wound repair and showed that they had a mechanical strength similar to that of human skin tissue; they then seeded USCs onto these composite meshes. Compared to that in rabbit full-thickness skin defect models that were treated with the PCL/GT membrane alone, markedly accelerated wound healing was observed following USC-PCL/GT treatment, which manifested as remarkably improved wound contraction, thicker granulation tissue, regeneration of skin appendages (such as hair follicles), faster reepithelialization and neovascularization, higher levels of collagen and higher capillary density (Fu et al., 2014). In an in vitro experiment, after culturing human umbilical vein endothelial cells (HUVECs) in USC-conditioned medium, the authors observed significantly enhanced proliferation, motility and tube formation abilities of the HUVECs (Fu et al., 2014). Bioglass, which is a type of bioactive silicate, is a special glass that is directly connected to living bone or soft tissue to repair damage. Bioglass can upregulate the secretion of VEGF and bFGF from USCs; this product is called bioglass-activated USCs and can enhance the wound healing ability of endothelial cells and fibroblasts. Using this property, Zhang et al. confirmed that USCs combined with bioglass could promote wound healing by activating the paracrine effects between USCs and recipient cells by applying bioglass-activated USCs to full-thickness wounds. This effect was manifested as improvements in endothelial cell proliferation and myofibroblast differentiation into fibroblasts, upregulated VEGF and bFGF levels, capillary-like network formation and elevated levels of vWF, collagen and fibronectin (Zhang et al., 2018). By combining USCs with biomaterials, namely, surface-structured bacterial cellulose (S-BC), Cao et al. found that USCs promoted the proliferation and survival of EAhy926 cells (a type of HUVEC) and that their synergistic effect accelerated collagen deposition and angiogenesis upon their evaluation of rat wound closure (Cao et al., 2019). Scholars have provided a novel idea, designated as hypoxic preconditioning, for the prevention and treatment of damage resulting from a hypoxic environment involving the repeated short-term exposure of tissues or cells to hypoxia; hypoxic preconditioning can improve tolerance to hypoxia. It is well known that this method improves the survival and proliferation of transplanted stem cells. Furthermore, in preconditioned hypoxia, USCs seeded on a SIS scaffold, which is a tool widely used in soft tissue repair, can increase the secretion of VEGF, bFGF, collagen, and elastic fibres to facilitate full-thickness skin wound healing in mouse models (Zhang et al., 2020c). Moreover, Chen et al. reported that USC-Exos have beneficial effects, such as accelerated revascularization and collagen deposition, on soft tissue wound repair in STZ-induced diabetic rats and that these effects may be attributed to the high expression of the proangiogenic protein DMBT1 (Chen et al., 2018a). USC-based skin stents may be a new method to promote skin wound healing, but they have not yet been used in clinical treatment.
기타 질환피부 재생 및 상처 치유
적절한 피부 조직 스캐폴드는 상처 치유를 촉진하지만, 적절한 스캐폴드 재료의 부족은 피부 조직 공학의 장애물입니다. 기존 연구 결과는 USC와 일부 새로운 생체재료의 결합이 상처 치유 과정의 중요한 부분인 신혈관 형성을 촉진함을 보여주었습니다. 따라서 다방향 분화 잠재력을 갖춘 USCs는 상처, 궤양, 화상, 염증으로 인한 광범위한 피부 손상의 치유를 촉진하기 위한 공학화된 피부 조직 구축의 중요한 전략으로 부상했습니다.
Fu와 동료들은 상처 복구를 위한 생체적합성 폴리카프로락톤/젤라틴 나노섬유 막을 스캐폴드로 제작했으며, 이 막이 인간 피부 조직과 유사한 기계적 강도를 갖는 것을 보여주었습니다. 이후 이들은 이 복합 메쉬에 USCs를 접종했습니다. 토끼의 전체 두께 피부 결손 모델에서 PCL/GT 막 단독 처리 대비 USC-PCL/GT 처리 후 상처 치유가 현저히 가속화되었으며, 이는 상처 수축 개선, 더 두꺼운 육아 조직, 피부 부속기(모낭 등) 재생, 상피화 및 신혈관 형성 속도 증가, 콜라겐 수준 및 모세혈관 밀도 증가로 나타났습니다(Fu et al., 2014). in vitro 실험에서 인간 제대 정맥 내피 세포(HUVECs)를 USC 조건화 매체에서 배양한 후, 저자들은 HUVECs의 증식, 이동성 및 관 형성 능력이 유의미하게 향상되었음을 관찰했습니다(Fu et al., 2014). 바이오글라스는 생체 활성 실리케이트의 일종으로, 손상된 뼈나 연조직과 직접 연결되어 손상을 복구하는 특수 유리입니다. 바이오글라스는 USC로부터 VEGF와 bFGF의 분비를 증가시키며, 이 제품은 바이오글라스 활성화 USC로 불리며 내피 세포와 섬유아세포의 상처 치유 능력을 향상시킵니다. 이 특성을 활용해 Zhang 등(2019)은 바이오글라스 활성화 USC를 전층 상처에 적용함으로써 USC와 수신 세포 간의 파라크린 효과를 활성화하여 상처 치유를 촉진함을 확인했습니다. 이 효과는 내피 세포 증식 및 근육 섬유모세포의 섬유모세포 분화 개선, VEGF 및 bFGF 수준 증가, 모세혈관 유사 네트워크 형성 및 vWF, 콜라겐 및 피브로네ктиן 수준 상승으로 나타났습니다 (Zhang et al., 2018). USCs와 생체재료인 표면 구조화 세균 셀룰로오스(S-BC)를 결합한 Cao 등(2019)은 USCs가 EAhy926 세포(HUVEC의 한 유형)의 증식과 생존을 촉진하며, 쥐 상처 치유 평가 시 콜라겐 침착과 혈관新生을 가속화하는 시너지 효과를 확인했습니다(Cao et al., 2019). 학자들은 저산소 환경에 의해 유발되는 조직 또는 세포의 반복적인 단기 저산소 노출로 인한 손상의 예방 및 치료를 위한 새로운 개념인 '저산소 사전 조건화'를 제안했습니다. 이 방법은 저산소 내성을 향상시키며, 이 방법이 이식된 줄기세포의 생존 및 증식을 개선한다는 것은 잘 알려져 있습니다. 또한, 저산소 전처치 상태에서 SIS 스캐폴드(연조직 복구에 널리 사용되는 도구)에 배양된 USC는 VEGF, bFGF, 콜라겐, 탄성 섬유의 분비를 증가시켜 쥐 모델에서 완전 두께 피부 상처 치유를 촉진했습니다(Zhang et al., 2020c). 또한 Chen 등(Chen et al., 2018a)은 STZ로 유도된 당뇨병 쥐의 연부 조직 상처 치유에 USC-Exos가 혈관 재형성 가속화와 콜라겐 침착과 같은 유익한 효과를 보였으며, 이러한 효과는 혈관新生 단백질 DMBT1의 높은 발현에 기인할 수 있다고 보고했습니다. USC 기반 피부 스텐트는 피부 상처 치유를 촉진하는 새로운 방법일 수 있지만, 아직 임상 치료에 사용되지 않았습니다.
Periodontal Tissue Engineering
Human periodontal ligament stem cells (PDLSCs) are considered to be an important material for periodontal tissue regeneration and can be used in the treatment of diseases such as periodontitis and gingivitis. PDLSCs are largely not afflicted by the disadvantage of not allowing complete periodontal tissue regeneration affecting current clinical treatment strategies. However, due to the limited number of PDLSCs, developing strategies to promote cell proliferation and differentiation is currently the top priority.
There is evidence of improved proliferation and osteoblastic/cementoblastic differentiation in PDLSCs, as demonstrated by denser collagen layers and elevated levels of the cementogenic protein cementum protein 1 (CEMP1), alkaline phosphatase (ALP) activity, runt-related transcription factor 2 (RUNX2) and osteocalcin (OCN) in a noncontact coculture of USCs (Yang et al., 2020). Additionally, Xiong et al. found that ECM derived from USCs enhanced the proliferation, osteogenic differentiation potential, and angiogenesis of PDLSCs compared to native PDLSCs (Xiong et al., 2019b). These results indicate that USCs may be the most suitable substrate for the coacceleration of osteogenic reactions with PDLSCs, but they have not yet been applied in clinical practice.
치주 조직 공학
인간 치주 인대 줄기세포(PDLSCs)는 치주 조직 재생의 중요한 재료로 간주되며, 치주염 및 치은염과 같은 질환의 치료에 활용될 수 있습니다. PDLSCs는 현재 임상 치료 전략에 영향을 미치는 완전한 치주 조직 재생이 불가능하다는 단점을 크게 받지 않습니다. 그러나 PDLSCs의 수가 제한적이기 때문에 세포 증식 및 분화를 촉진하는 전략 개발이 현재 최우선 과제입니다.
USC(인체 연골 세포)와의 비접촉 공배양에서 PDLSCs의 증식 및 골모세포/시멘토블라스틱 분화가 개선되었다는 증거가 있습니다. 이는 더 밀집된 콜라겐 층과 시멘토겐 단백질 1(CEMP1), 알칼리 포스파타제(ALP) 활성, 런트 관련 전사 인자 2(RUNX2) 및 골칼시틴(OCN)의 증가로 확인되었습니다(Yang et al., 2020). 또한 Xiong 등(2019b)은 USCs에서 유래한 ECM이 원시 PDLSCs에 비해 PDLSCs의 증식, 골형성 분화 잠재력 및 혈관新生을 향상시킨다는 것을 발견했습니다(Xiong et al., 2019b). 이러한 결과는 USCs가 PDLSCs와의 골형성 반응 동시 촉진에 가장 적합한 기질일 수 있음을 시사하지만, 아직 임상实践에 적용되지 않았습니다.
Erectile Dysfunction
The average prevalence of ED, which is associated with many risk factors, such as diabetes, is 30% in patients of different ages. Due to their reduced quality of life, these patients often undergo high-cost penile prosthesis implantation, causing distressing complications, such as corporal fibrosis (Yafi et al., 2016). Many studies have shown that USCs play a key role in the treatment of ED.
USCs can improve erectile function and repair the endothelial structure of the cavernous body by protecting nerves, reducing fibrosis, and inhibiting cell apoptosis in cavernous tissue (Chen et al., 2018c). In the experiments performed by Yang et al., USCs modified with pigment epithelium-derived factor (PEDF) improved erectile function in rats with cavernous nerve injury (CNI) by exerting protective effects on nerves and ECs in combination with their antiapoptotic effects (Yang et al., 2016). According to the observations reported by Ouyang et al., USC-EVs ameliorate diabetic erectile dysfunction (DED) by increasing the endothelial expression and smooth muscle content in male rat models established by STZ injection (Ouyang et al., 2019). Similarly, Zhang et al. revealed that increased autophagy activity is related to the improved function of cavernous endothelial cells in the DED model, suggesting that the reversal of autophagy may serve as a new therapeutic target for DED (Zhou et al., 2019). However, the improvement of ED by USCs is based on animal experiments such as rats, and further clinical studies are needed to verify the results.
발기 장애
당뇨병 등 다양한 위험 요인과 관련된 발기부전의 평균 유병률은 다양한 연령대의 환자에서 30%입니다. 삶의 질 저하로 인해 이러한 환자들은 고비용의 음경 보형물 삽입술을 받게 되며, 이는 음경 조직의 섬유화(Yafi et al., 2016)와 같은 고통스러운 합병증을 유발합니다. 많은 연구에서 USCs가 발기부전 치료에 핵심적인 역할을 한다는 것이 입증되었습니다.
USCs는 음경 해면체 조직에서 신경 보호, 섬유화 감소, 세포 사멸 억제를 통해 음경 해면체의 내피 구조를 복원하고 발기 기능을 개선합니다 (Chen et al., 2018c). Yang 등(2016)의 실험에서 색소 상피 유래 인자(PEDF)로 수정된 USC는 동맥 신경 손상(CNI)을 가진 쥐에서 신경과 내피 세포(ECs)에 대한 보호 효과와 항세포 사멸 효과를 결합하여 발기 기능을 개선했습니다(Yang et al., 2016). Ouyang 등(2019)의 관찰 결과에 따르면, USC-EVs는 STZ 주사로 유도된 수컷 쥐 모델에서 내피 세포 발현과 평활근 함량을 증가시켜 당뇨병성 발기 장애(DED)를 개선했습니다(Ouyang et al., 2019). 마찬가지로 Zhang 등(Zhang et al.)은 DED 모델에서 자가포식 활동의 증가가 동굴 내피 세포의 기능 개선과 관련이 있음을 밝혔으며, 이는 자가포식의 역전이 DED의 새로운 치료 표적이 될 수 있음을 시사합니다(Zhou et al., 2019). 그러나 USC에 의한 ED의 개선은 쥐와 같은 동물 실험을 기반으로 한 것이기 때문에, 그 결과를 확인하기 위해서는 추가적인 임상 연구가 필요합니다.
Current Challenges
Despite the substantial potential of USCs, there are still challenges that need to be overcome. When the cells used in experiments are derived from individuals with different genetic backgrounds, their diversity can affect the experimental reproducibility (Ji et al., 2017a). The age, sex, and health status of the urine donor may affect the proliferation and pluripotency of stem cells; for example, USCs from the urine of young and healthy people have a higher ability to proliferate and differentiate into various lineages (Tayhan et al., 2017), while USCs from patients with diabetes have a significantly reduced ability to regenerate (Xiong et al., 2019a).
As mentioned above, USCs have multidirectional differentiation potential; however, given their decreased potential for osteogenic and chondrogenic differentiation compared with that of BMSCs, strategies to improve their directed differentiation efficiency are urgently needed (Ji et al., 2017a; Wu et al., 2018). Moreover, the differentiation of USCs has mostly been demonstrated in vitro, and their differentiation ability in vivo should be further explored. Preconditioning, including gene modification, drug pretreatment and coculture, can be used to enhance the differentiation ability of USCs in vivo (Hu et al., 2020). Additionally, Dong et al. suggested that USCs can differentiate into PDX1-positive cells in the rat pancreas (Dong et al., 2016). However, in 2018, Zhao et al. revealed that USCs could protect beta cells from apoptosis induced by minor-to-moderate injuries in STZ-induced diabetic mice; however, these cells could not replace the already dead beta cells (Zhao et al., 2018). These two contradictory results remain controversial and require further experimental evidence.
Before USCs can be formally applied in clinical practice, standardized products must be acquired and storage and transport, in vitro amplification, administration and dosing, and cell homing must be optimized. In addition, the curative effect of basic cell therapy must be improved, and the cell therapy protocol must be optimized.
Safety and effectiveness should also be considered. Recent research suggests that the proliferation and differentiation of implanted cells, such as USCs, and their corresponding scaffolds are in danger of reconstruction in the urinary tract due to the highly cytotoxic nature of urine (Abbas et al., 2020).
Reprogrammed iPSCs from USCs are affected by genomic instability and epigenetic memory associated with the reprogramming process, resulting in aberrant differentiation in vitro and even influencing disease modelling and clinical applications (Ji et al., 2017b). Teratoma formation is a major side effect of iPSC transplantation (Parrotta et al., 2019).
Exosomes derived from USCs represent a novel cell-free therapeutic strategy that have the advantages of long-term maintenance of biological activity, low immunogenicity and no promotion of tumour formation. Nevertheless, specifically labelling and tracking exosomes in vivo remains challenging (Li et al., 2020).
Conclusion
Overall, USCs and their secreted factors play roles in immune regulation, oxidative stress modulation, revascularization, cell apoptosis and autophagy. Through the mechanisms above, USCs have substantial potential in tissue engineering and personalized therapeutic strategies and exert therapeutic effects on a variety of diseases, such as those of the urinary, nervous, locomotor, reproductive endocrine and digestive systems. Although several challenges currently exist, we anticipate that future research will identify solutions to the existing problems and expand the application range.
현재의 과제
USCs의 상당한 잠재력에도 불구하고 극복해야 할 과제들이 여전히 존재합니다. 실험에 사용된 세포가 서로 다른 유전적 배경을 가진 개인으로부터 유래된 경우, 그 다양성이 실험 재현성에 영향을 미칠 수 있습니다 (Ji et al., 2017a). 소변 기증자의 연령, 성별, 건강 상태는 줄기세포의 증식 및 다능성에 영향을 미칠 수 있습니다. 예를 들어, 젊은 건강한 사람의 소변에서 유래된 USCs는 다양한 계통으로 분화하는 능력이 더 높습니다(Tayhan et al., 2017), 반면 당뇨병 환자의 소변에서 유래된 USCs는 재생 능력이 현저히 감소합니다(Xiong et al., 2019a).
위에서 언급된 바와 같이 USCs는 다방향 분화 잠재력을 가지고 있지만, BMSCs에 비해 골분화 및 연골분화 잠재력이 낮기 때문에, 그들의 방향성 분화 효율을 향상시키는 전략이 시급히 필요합니다 (Ji et al., 2017a; Wu et al., 2018). 또한 USCs의 분화는 주로 in vitro에서 입증되었으며, in vivo에서의 분화 능력은 추가로 탐구되어야 합니다. 전처리(유전자 수정, 약물 사전 처리 및 공배양)는 USCs의 체내 분화 능력을 향상시키는 데 활용될 수 있습니다(Hu et al., 2020). 또한 Dong et al.은 쥐의 췌장에서 USCs가 PDX1 양성 세포로 분화할 수 있음을 제안했습니다(Dong et al., 2016). 그러나 2018년 Zhao 등(Zhao et al., 2018)은 STZ로 유도된 당뇨병 쥐에서 경도에서 중등도의 손상으로 인한 베타 세포의 아포토시스를 USCs가 보호할 수 있음을 보여주었으나, 이 세포들은 이미 죽은 베타 세포를 대체할 수 없었다. 이 두 상반된 결과는 여전히 논란의 여지가 있으며 추가 실험적 증거가 필요합니다.
USCs가 임상实践에 공식적으로 적용되기 전에 표준화된 제품이 확보되어야 하며, 보관 및 운송, in vitro 증식, 투여 및 용량 조절, 세포 귀환이 최적화되어야 합니다. 또한 기본 세포 치료의 치료 효과를 개선하고 세포 치료 프로토콜을 최적화해야 합니다.
안전성과 효과도 고려되어야 합니다. 최근 연구는 소변의 고도로 독성 있는 특성으로 인해 이식된 세포(예: USCs)와 그 대응 스캐폴드가 요로에서 재구성될 위험이 있음을 제시했습니다(Abbas et al., 2020).
USC에서 재프로그래밍된 iPSC는 재프로그래밍 과정과 관련된 유전체 불안정성과 에피게놈 기억으로 인해 체외에서 이상 분화(in vitro)를 보이며, 이는 질병 모델링과 임상 적용에도 영향을 미칩니다(Ji et al., 2017b). iPSC 이식의 주요 부작용은 테라토마 형성입니다(Parrotta et al., 2019).
USC에서 유래된 엑소좀은 장기적인 생물학적 활성 유지, 낮은 면역원성, 종양 형성을 촉진하지 않는 장점을 가진 새로운 세포 무함유 치료 전략을 대표합니다. 그러나 in vivo에서 엑소좀을 특정적으로 표지하고 추적하는 것은 여전히 도전 과제입니다(Li et al., 2020).
결론
전반적으로, USC와 그 분비 인자는 면역 조절, 산화 스트레스 조절, 혈관 재형성, 세포 사멸 및 자가포식에서 역할을 합니다. 위의 메커니즘을 통해 USC는 조직 공학 및 개인 맞춤형 치료 전략에 상당한 잠재력을 가지고 있으며, 비뇨기, 신경, 운동, 생식 내분비 및 소화기 계통과 같은 다양한 질병에 치료 효과를 발휘합니다. 현재 몇 가지 과제가 남아 있지만, 향후 연구를 통해 기존 문제의 해결책이 발견되고 적용 범위가 확대될 것으로 기대됩니다.
Acknowledgments
AJE edited the manuscript for grammar, punctuation and spelling.
Author Contributions
YC, FS, QZ, XW, and MZ conceived of and designed the study, revised the manuscript for important intellectual content. QZ, XZ, and JS performed the literature search and performed the comparison. YC, GY, and YL generated the figures and tables and performed the background research. QZ, MZ, YW, PZ, and MN edited the manuscript. QZ and FS drafted the manuscript. All authors have read and approved the content of the manuscript.
Funding
This work was supported by the National Natural Science Foundation of China (81970248), Natural Science Foundation of Hunan Province, China (2020JJ4864), National Key Research and Development Program of China (2018YFA0108700, 2017YFA0105602) and National Undergraduate Training Program for Innovation and Entrepreneurship (No.S2021105330363).
Conflict of Interest
The authors declare that the research was conducted in the absence of any commercial or financial relationships that could be construed as a potential conflict of interest.
Publisher’s Note
All claims expressed in this article are solely those of the authors and do not necessarily represent those of their affiliated organizations, or those of the publisher, the editors and the reviewers. Any product that may be evaluated in this article, or claim that may be made by its manufacturer, is not guaranteed or endorsed by the publisher.
References
- Abbas T. O., Ali T. A., Uddin S. (2020). Urine as a Main Effector in Urological Tissue Engineering-A Double-Edged Sword. Cells 9 (3), 538. 10.3390/cells9030538 [DOI] [PMC free article] [PubMed] [Google Scholar]