Annual Review of Immunology Volume 37, 2019
Review Article Free
Neuro–Immune Cell Units: A New Paradigm in Physiology
- Cristina Godinho-Silva1, Filipa Cardoso1 and Henrique Veiga-Fernandes1
- Vol. 37:19-46 (Volume publication date April 2019) https://doi.org/10.1146/annurev-immunol-042718-041812
- First published as a Review in Advance on October 31, 2018
ABSTRACT
The interplay between the immune and nervous systems has been acknowledged in the past, but only more recent studies have started to unravel the cellular and molecular players of such interactions. Mounting evidence indicates that environmental signals are sensed by discrete neuro–immune cell units (NICUs), which represent defined anatomical locations in which immune and neuronal cells colocalize and functionally interact to steer tissue physiology and protection. These units have now been described in multiple tissues throughout the body, including lymphoid organs, adipose tissue, and mucosal barriers. As such, NICUs are emerging as important orchestrators of multiple physiological processes, including hematopoiesis, organogenesis, inflammation, tissue repair, and thermogenesis. In this review we focus on the impact of NICUs in tissue physiology and how this fast-evolving field is driving a paradigm shift in our understanding of immunoregulation and organismal physiology.
초록
면역계와 신경계 간의 상호작용은 과거에도 인정되어 왔으나,
이러한 상호작용의 세포적·분자적 요인들을 규명하기 시작한 것은
최근 연구들이다.
환경 신호가
신경-면역 세포 단위(NICU)에 의해 감지된다는 증거가 축적되고 있으며,
이러한 NICU는 면역 세포와 신경 세포가 공존하며 기능적으로 상호작용하여
조직 생리학과 보호 기능을 조율하는 명확한 해부학적 위치를 나타낸다.
이러한 단위는
현재 림프기관, 지방조직, 점막 장벽을 포함한
전신 다중 조직에서 확인되었다.
따라서 NICU는
조혈, 장기 발생, 염증, 조직 복구, 열생성 등
다중 생리학적 과정의 중요한 조정자로 부상하고 있다.
본 리뷰에서는
조직 생리학에서 NICU의 영향력과 이 급속히 진화하는 분야가
면역 조절 및 유기체 생리학에 대한
우리의 이해에 어떻게 패러다임 전환을 주도하고 있는지에 초점을 맞춘다.
Keywords
- neuroimmunology,
- neuro–immune cell units,
- neuroimmune interactions,
- mucosal immunology,
- immunophysiology
1. INTRODUCTION
Organismal physiology and health depend on the coordinated action of multiple cellular networks. A perfect example is provided by the immune system and the nervous system, which harbor myriads of immune and neuronal cell subsets that can sense and respond to multiple environmental conditions and aggressions. Cross talk between the immune and nervous systems has been reported in healthy and disease states, and recent studies indicate that neuro-immune interactions can operate as important immunoregulatory hubs. Notably, immune cells and neuronal cells can colocalize and interact at discrete anatomical sites to drive tissue protection and physiology. These multicellular platforms, known as neuro–immune cell units (NICUs) (1), are challenging our views on how tissue physiology is orchestrated and are likely among the most exciting challenges in immunology over the coming decades.
Neuro-immune interactions are mostly mediated by soluble factors such as neurotransmitters, neuropeptides, and cytokines (2). Immune cells are equipped to respond to neuronal signals by expressing receptors for neuronal cell–derived molecules and, reciprocally, neurons express receptors for immune-derived cytokines and neurotransmitters, which can affect neuronal function (3–5). As such, neuro-immune interactions have been involved in multiple aspects of tissue physiology and have also been described in several conditions, including autism, cancer, multiple sclerosis, and chronic inflammatory disorders (2). Nevertheless, the cellular and molecular fingerprints of NICUs remain poorly understood, but progress in this direction may identify yet unappreciated therapeutic targets.
1. 서론
유기체 생리학과 건강은
다중 세포 네트워크의 조화된 작용에 달려 있다.
Organismal physiology and health depend on
the coordinated action of multiple cellular networks
면역계와 신경계가 대표적인 예로,
수많은 면역 세포 및 신경 세포 하위 집합을 보유하여
다양한 환경 조건과 공격을 감지하고 반응할 수 있다.
A perfect example is provided by the immune system and the nervous system,
which harbor myriads of immune and neuronal cell subsets that can sense and respond to
multiple environmental conditions and aggressions
면역계와 신경계 간의 교신은
건강 상태와 질병 상태 모두에서 보고되었으며,
최근 연구들은 신경-면역 상호작용이 중요한 면역 조절 허브로 기능할 수 있음을 시사한다.
Cross talk between the immune and nervous systems
has been reported in healthy and disease states,
and recent studies indicate that neuro-immune interactions
can operate as important immunoregulatory hubs.
특히, 면역 세포와 신경 세포는
조직 보호와 생리 기능을 촉진하기 위해 특정 해부학적 부위에서 공존하며 상호작용할 수 있다.
신경-면역 세포 단위(NICU)(1)로 알려진 이러한 다세포 플랫폼은
조직 생리학이 어떻게 조율되는지에 대한 우리의 관점에 도전장을 내밀고 있으며,
향후 수십 년간 면역학 분야에서 가장 흥미로운 과제 중 하나가 될 것이다.
신경-면역 상호작용은
주로 신경전달물질, 신경펩타이드, 사이토카인(2)과 같은 용해성 인자에 의해 매개됩니다.
면역 세포는
신경세포 유래 분자에 대한 수용체를 발현함으로써
신경 신호에 반응할 수 있으며,
반대로 신경세포는 면역 유래 사이토카인과 신경전달물질에 대한 수용체를 발현하여
따라서
신경-면역 상호작용은 조직 생리학의 다양한 측면에 관여해 왔으며,
자폐증, 암, 다발성 경화증, 만성 염증성 질환 등
여러 질환에서도 보고된 바 있다(2).
그럼에도 NICU의 세포적·분자적 지문은 아직 제대로 이해되지 않고 있으나,
이 방향의 진전은 아직 주목받지 못한 치료 표적을 규명할 수 있을 것이다.
2. NERVOUS SYSTEM CONSIDERATIONS
Neuro-immune interactions can operate in the central nervous system (CNS) and in the peripheral nervous system. The latter comprises neurons and glial cells organized in nerve bundles, coming from the CNS. Immune responses have been shown to be modulated by the peripheral nervous system, notably by the autonomic nervous system, but also by sensory and motor nervous system inputs (6).
The autonomic nervous system can be classified into (a) the sympathetic nervous system (SNS), (b) the parasympathetic nervous system (PaNS), and (c) the enteric nervous system (ENS). Sympathetic nerves emerge from the thoracolumbar spinal cord and produce catecholamines ( Figure 1 ). SNS stimulation was shown to impact a wide range of immune parameters, including function, survival, proliferation, circulation, and trafficking of immune cells (5). Adrenergic receptors targeted by catecholamines are expressed by immune cells, and their stimulation regulates expression of receptors and cytokines essential for coordinated immune responses (7). PaNS neurons emerge from the cranial nerves and the sacral spinal cord and regulate involuntary responses at resting states ( Figure 1 ). However, the extent to which PaNS cholinergic neurons regulate immunity remains unresolved, since it is still unclear which lymphoid organs are innervated by the PaNS. The cell bodies of the ENS are localized within the walls of the gastrointestinal tract, in contrast to the SNS and PaNS cell bodies that are found in the spinal cord ganglia (2) ( Figure 1 ).
2. 신경계 고려사항
신경-면역 상호작용은
중추신경계(CNS)와 말초신경계에서 작동할 수 있다.
후자는
중추신경계에서 나온 신경 다발로 조직된 뉴런과 신경교세포로 구성된다.
면역 반응은
말초신경계, 특히 자율신경계에 의해 조절되는 것으로 밝혀졌으며,
감각 및 운동 신경계 입력에 의해서도 조절된다(6).
자율신경계는
(a) 교감신경계(SNS), (b) 부교감신경계(PaNS), (c) 장신경계(ENS)로 분류될 수 있다.
교감신경은
흉요추 척수에서 발생하며 카테콜아민을 생성한다(그림 1). .
SNS 자극은
면역 세포의 기능, 생존, 증식, 순환 및 이동을 포함한
광범위한 면역 매개변수에 영향을 미치는 것으로 밝혀졌다(5).

| 신경계와 면역계가 유전자 조절, 신호전달, 세포 간 통신, 초세포적 조직화 메커니즘을 공유한다는 강력한 증거가 나타나고 있다. 이는 두 시스템 간 공통점의 발생학적·진화적 기원을 비롯한 수많은 의문을 제기한다. 이러한 질문에 답함으로써 면역학자와 신경생물학자는 각자의 분야에서 메커니즘적·개념적 유사성을 점차 드러내고, 복잡한 세포 시스템의 조직화를 지배하는 근본 원리 이해를 촉진하고 있다. 본 논문과 Immunity 및 Neuron에 실린 리뷰 논문들은 면역계와 신경계 간의 공통점에 관한 일련의 사례들을 과학계 전반에 알리고, 두 분야 간의 대화와 아이디어 교류를 증진시키려는 시도를 담고 있다. |
카테콜아민이 표적으로 하는 아드레날린성 수용체는 면역 세포에 발현되며,
이들의 자극은 조화된 면역 반응에 필수적인 수용체 및 사이토카인 발현을 조절한다(7).
PaNS 뉴런은
뇌신경(미주신경)과 천골 척수에서 발생하며
휴식 상태에서의 비자발적 반응을 조절한다(그림 1).
그러나
PaNS 콜린성 뉴런이 면역에 미치는 조절 정도는 아직 명확하지 않다.
PaNS가
어떤 림프기관을 신경 분포하는지 아직 밝혀지지 않았기 때문이다.



ENS의 세포체는 위장관 벽 내에 국한되어 있는 반면,
SNS와 PaNS의 세포체는 척수 신경절에서 발견된다(2)( 그림 1).
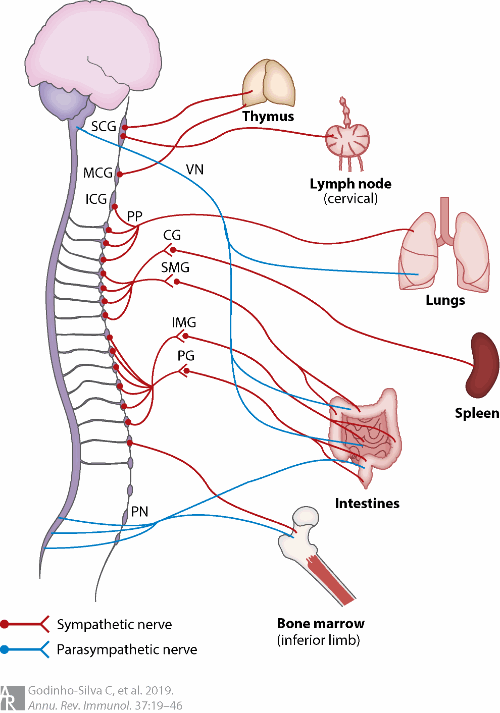
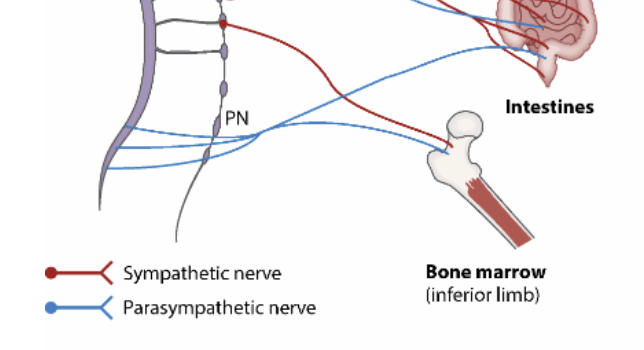
Figure 1 Lymphoid tissue and mucosal innervation.
The major autonomic pathways that innervate lymphoid organs and mucosae are illustrated. These include two branches of the autonomic nervous system: the SNS (red) and the PaSNS (blue). The SNS circuit is a two-neuron chain with preganglionic sympathetic neurons innervating postganglionic neurons whose nerve endings reach target organs. The PaSNS is also a two-neuron chain of efferent nerves with preganglionic neurons in the CNS that end upon postganglionic neurons in the organs they supply. Abbreviations: CG, celiac ganglia; ICG, inferior cervical ganglia; IMG, inferior mesenteric ganglia; MCG, medial cervical ganglia; PaSNS, parasympathetic nervous system; PG, pelvic ganglia; PN, pelvic nerve; PP, pulmonary plexus; SCG, superior cervical ganglia; SMG, superior mesenteric ganglia; SNS, sympathetic nervous system; VN, vagus nerve. This figure was modified from Servier Medical Art, licensed under a Creative Commons Attribution 3.0 Generic License. https://smart.servier.com/ .
그림 1 림프 조직과 점막 신경 분포.
림프 기관과 점막을 신경 분포하는
주요 자율 신경 경로를 나타냅니다.
여기에는 자율 신경계의 두 가지 분지인 SNS(적색)와 PaSNS(청색)가 포함됩니다. SNS 회로는 전신교 신경절 교감 신경 세포가 후신교 신경 세포를 신경 분포하고, 이 후신교 신경 세포의 신경 말단이 표적 기관에 도달하는 2개의 신경 세포로 이루어진 사슬입니다. PaSNS 역시 두 개의 신경 세포로 이루어진 원심성 신경 사슬로, 중추신경계(CNS)의 전신경절 신경세포가 공급 기관의 후신경절 신경세포에 종결된다.
약어: CG, 위장 신경절; ICG, 하경부 신경절; IMG, 하장간막 신경절; MCG, 내경부 신경절; PaSNS, 부교감신경계; PG, 골반신경절; PN, 골반신경; PP, 폐신경총; SCG, 상경신경절; SMG, 상장간막신경절; SNS, 교감신경계; VN, 미주신경. 본 그림은 Servier Medical Art에서 수정하였으며, 크리에이티브 커먼즈 저작자표시 3.0 일반 라이선스 하에 배포됩니다. https://smart.servier.com/ .
Click to view
Finally, neuro-immune interactions can also be established at a systemic level, whereby neurotransmitters and hormones can be released into circulation from the CNS in response to environmental stimuli. Reciprocally, systemic and peripheral release of immune-derived cytokines can regulate neuronal functions as discussed further below (6, 7).
마지막으로,
신경-면역 상호작용은 전신 수준에서도 확립될 수 있으며,
이 경우 환경 자극에 반응하여
중추신경계(CNS)로부터 신경전달물질과 호르몬이 순환계로 방출될 수 있습니다.
반대로,
전신 및 말초에서 면역 유래 사이토카인의 방출은
아래에서 더 자세히 논의될 신경 기능을 조절할 수 있습니다(6, 7).
3. TISSUE INNERVATION AND IMMUNE REGULATION
3.1. Neuronal Control of Hematopoiesis
Immune cells originate from hematopoietic stem cells (HSCs) through a developmentally regulated process that gives rise to all blood cell lineages: hematopoiesis (8). In adult mammals, hematopoiesis mostly takes place in the bone marrow, whereas T lymphocyte development occurs in the thymus. Innervation of the bone marrow by the autonomic nervous system regulates the development of new lymphoid and myeloid cells (9). Early evidence for innervation of the bone marrow was provided by the histological studies of Calvo (10) in 1968, when he postulated the control of bone marrow function by autonomic and sensory neurons. Sympathetic nerve fibers are the most important neuronal inputs in the bone marrow ( Figure 1 ). While the periosteal bone region is the most densely innervated, when total volume is considered it is the bone marrow that receives most SNS innervation (11–13). Sympathetic nerves and stromal cells form neuroreticular complexes present in hematopoietic niches, where HSCs are maintained and differentiate (14–16). One example of neuronal-hematopoietic regulation is the circadian mobilization of HSCs to the bloodstream. In this process, catecholamines suppress stromal cell niche functions, increasing the egress of hematopoietic cells from the bone marrow. Notably, circadian oscillations of bone marrow noradrenaline induce rhythmic expression of CXCL12 by mesenchymal stem and progenitor cells leading to the rhythmic release of HSCs (17, 18). More recently, it was found that bone marrow innervation by the SNS declines with age and this reduction leads to the aging of HSCs (19). Interestingly, the decline in regenerative capacity and differentiation potential of aged HSCs critically relies on the loss of SNS nerves or adrenoreceptor β3 signaling in the hematopoietic niche (19). Sympathetic signals are also critical regulators of hematopoietic regeneration following exposure to cytotoxic drugs or irradiation. Sympathetic neuropathy leads to hematopoietic exhaustion, which can be rescued by administration of neuroprotective agents (20). Furthermore, sympathetic neuropathy is present in acute and chronic myeloid leukemia, and these neuronal defects can enhance leukemia malignancy by altering mesenchymal niche activities and expansion of malignant HSCs (20, 21). Finally, SNS-derived neuropeptide Y also promotes the release of HSCs from their niche through the activation of matrix metalloproteinase 9 (22–24), while substance P and neurokinin A stimulate stromal cells to produce hematopoietic cytokines (25).
3. 조직 신경 분포와 면역 조절
3.1. 신경에 의한 조혈 조절
면역 세포는
모든 혈액 세포 계통을 생성하는 발달적으로 조절되는 과정인 조혈(hematopoiesis)을 통해
조혈 줄기세포(HSCs)에서 기원한다(8).
성인 포유류에서 조혈은
주로 골수에서 이루어지며,
T 림프구 발달은 흉선에서 발생한다.
자율 신경계에 의한 골수의 신경 분포는
새로운 림프구 및 골수구 세포의 발달을 조절한다(9).
골수 신경 분포에 대한 초기 증거는
1968년 칼보(Calvo)의 조직학적 연구(10)에서 제시되었으며,
그는 자율신경 및 감각 신경에 의한 골수 기능 조절을 제안했다.
교감신경 섬유는
골수 내 가장 중요한 신경 입력이다(그림 1).
골막 골 영역이 가장 밀집된 신경 분포를 보이지만,
총 부피를 고려할 때
교감신경계(SNS) 신경 분포를 가장 많이 받는 것은 골수이다(11–13).
교감신경과 기질 세포는
조혈모세포(HSCs)가 유지되고 분화하는
조혈 틈새(hematopoietic niches)에 존재하는
신경망상 복합체(neuroreticular complexes)를 형성한다(14–16).
신경-조혈 조절의 한 예는
HSCs가 혈류로 이동하는 일주기적 과정이다.
이 과정에서 카테콜아민은
기질 세포 틈새 기능을 억제하여 조
혈세포의 골수 이탈을 증가시킨다.
특히, 골수의 노르아드레날린 일주기 진동은
중간엽 줄기세포 및 전구세포에 의해 CXCL12의 리드미컬한 발현을 유도하여
최근 연구에서는
교감신경계에 의한 골수 신경 분포가 노화와 함께 감소하며,
이러한 감소가 HSCs의 노화를 초래한다는 사실이 밝혀졌다(19)
https://pmc.ncbi.nlm.nih.gov/articles/PMC6095812/

| 조혈모세포(HSCs)의 노화는 재생 능력과 다계열 분화 잠재력의 저하와 연관되어 혈액 질환 발생에 기여한다. 최근 골수 미세환경이 HSC 노화에 영향을 미친다는 가설이 제기되었으나, 그 기전은 대부분 알려지지 않았다. 본 연구에서는 HSC 노화가 교감신경계(SNS)의 골수 신경 분포에 크게 의존함을 보여주었다. 젊은 생쥐의 골수 미세환경에서 SNS 신경이나 아드레날린 수용체 β3(ADRβ3) 신호전달을 상실시키면, 생리적 노화를 연상시키는 HSC 표현형의 출현으로 입증되듯 조기 HSC 노화가 발생했다. 놀랍게도, 노화 마우스에 ADRβ3에 선택적으로 작용하는 교감신경 작용제를 보충하면 노화된 조혈모세포의 생체 내 기능이 현저히 회복되었으며, 이는 노화 과정에서 골수 SNS 신경 분포를 보존하거나 회복시키는 것이 새로운 조혈모세포 재생 전략의 잠재력을 지닐 수 있음을 시사한다. |
흥미롭게도 노화된 HSC의 재생 능력 및 분화 잠재력 저하는
골수 미세환경에서 교감신경계 신경 손실
또는 β3 아드레노수용체 신호전달 상실에 크게 의존한다(19).
교감신호는
또한 세포독성 약물 또는 방사선 노출 후 골수 재생의 핵심 조절자이다.
교감신경병증은
골수 고갈을 초래하며,
이는 신경보호제 투여로 회복될 수 있다(20).
https://www.cell.com/cell-stem-cell/comments/S1934-5909(14)00296-3

| 혈관 주위 중간엽 줄기 및 전구 세포(MSPCs)는 건강한 조혈모세포(HSC) 니치 형성에 필수적이다. 그러나 급성 골수성 백혈병(AML) 줄기 세포와 미세환경 간의 상호작용 및 영향은 여전히 대부분 연구되지 않았다. 우리는 MLL-AF9 AML 모델에서 교감신경계(SNS)의 신경병증이 백혈병성 골수 침윤을 촉진한다는 의외의 사실을 발견했다. AML 발병은 SNS 신경과 네스틴+ 니치 세포의 휴면 상태를 교란시켜, HSC를 유지하는 NG2+ 동맥주위 니치 세포를 희생시키면서 골아세포 분화 준비가 된 표현형 MSPCs의 확장을 초래한다. 백혈병 발생을 촉진하는 아드레날린성 신호전달은 백혈병성 골수 기질세포에 발현된 β2 아드레날린 수용체를 통해 전달되나, β3 수용체는 관여하지 않는다. 이러한 결과는 교감신경병증이 악성 세포가 미세환경을 동원하는 메커니즘일 수 있음을 시사하며, 골수 내 악성 및 정상 조혈모세포에 대해 서로 다른 중간엽 니치 활동이 존재함을 암시한다. |
또한 교감신경병증은
급성 및 만성 골수성 백혈병에서 관찰되며,
이러한 신경학적 결함은 중간엽 니치 활동 변화와 악성 조혈모세포(HSCs)의 증식을 통해
마지막으로,
SNS 유래 신경펩타이드 Y는
매트릭스 메탈로프로테이나제 9(MMP-9) 활성화를
통해 조혈모세포가 니치에서 방출되도록 촉진하며(22–24),
서브스턴스 P와 뉴로키닌 A는 조혈 사이토카인 생산을 위해
기질 세포를 자극한다(25).
As for the PaNS, despite some evidence for the presence of cholinergic nerve fibers at hematopoietic sites ( Figure 1 ), little is known of its role in hematopoiesis (26). In a recent study, Pierce et al. (27) showed that expression of muscarinic receptor type 1 (CHRM1) in the CNS controls HSC release from the bone marrow via release of glucocorticoids from the hypothalamic-pituitary-adrenal axis and not from local parasympathetic nerves. Sensory peptidergic innervation is also found in the bone marrow. Sensory nerves reach the bone marrow through perivascular plexuses and feed back to autonomic control centers in the spinal cord regulating sympathetic tone through intraspinal reflex arches (28). Sensory neurons produce neuropeptide Y, substance P, vasoactive intestinal peptide (VIP), and calcitonin gene–related peptide (CGRP) (6, 12, 28, 29). Importantly, ablation of these nerves reduces blood cell counts and bone marrow cellular density, and in vitro stimulation of HSCs with sensory nerve–derived neuropeptides stimulates progenitor activity (28). Overall, release of neuropeptides from sensory nerve terminals in the bone marrow appears to have a positive stimulatory effect on HSC activity and hematopoiesis (11, 30–32).
Schwann cells, a special type of glial cells that ensheathe nerves within the bone marrow, can also control HSC quiescence through activation of latent TGF-β (33). Glial cell–derived neurotrophic factor (GDNF) family ligands also regulate hematopoiesis since ablation of their receptor in hematopoietic cells impairs survival of HSCs. Notably, activation of the GDNF family ligand receptor RET provides HSCs with critical Bcl2 and Bcl2l1 surviving cues, which are essential for cell-autonomous stress response and reconstitution potential (34).
PaNS의 경우,
조혈 부위에 콜린성 신경 섬유가 존재한다는 일부 증거가 있음에도 불구하고( 그림 1),
조혈에서 그 역할에 대해서는 거의 알려져 있지 않다(26).
최근 연구에서 Pierce 등(27)은
중추신경계(CNS)의 무스카린 수용체 1형(CHRM1) 발현이
시상하부-뇌하수체-부신 축을 통한 글루코코르티코이드 분비로
골수에서 조혈모세포(HSC) 방출을 조절하며,
이는 국소 부교감 신경이 아닌 경로를 통해 이루어짐을 보여주었다.
감각성 펩타이드성 신경 분포도 골수에서 발견된다.
감각 신경은 혈관 주위 신경총을 통해 골수에 도달하며,
척수 내 반사 고리를 통해 교감신경 긴장을 조절하는
척수 내 자율신경 조절 센터로 피드백된다(28).
감각 신경세포는
신경펩타이드 Y, 서브스턴스 P, 혈관활성 장펩타이드(VIP),
칼시토닌 유전자 관련 펩타이드(CGRP)를 생성한다(6, 12, 28, 29).
중요한 점은, 이러한 신경의 절제가 혈구 수와 골수 세포 밀도를 감소시키며, 감각 신경 유래 신경펩타이드로 HSC를 체외에서 자극하면 전구세포 활성이 촉진된다는 것이다(28). 전반적으로, 골수 내 감각 신경 말단에서 방출되는 신경펩타이드들은 HSC 활동과 조혈에 긍정적인 자극 효과를 미치는 것으로 보인다(11, 30–32).
골수 내에서 신경을 감싸는 특수한 유형의 신경교 세포인 슈반 세포도 잠재적 TGF-β의 활성화를 통해 HSC의 휴지 상태를 제어할 수 있습니다(33). 아교세포 유래 신경 영양 인자(GDNF) 계열 리간드 역시 조혈을 조절하는데, 이는 조혈 세포에서 해당 수용체를 제거하면 조혈모세포의 생존이 저해되기 때문이다. 특히 GDNF 계열 리간드 수용체인 RET의 활성화는 조혈모세포에 중요한 생존 신호인 Bcl2 및 Bcl2l1을 제공하며, 이는 세포 자율적 스트레스 반응과 재구성 능력에 필수적이다(34).
The presence of catecholamines in the mammalian thymus was first demonstrated in 1974 (35). It is now well established that sympathetic nerve fibers innervate the thymus. Notably, thymic sympathetic nerves originate in the superior cervical and stellate ganglia, both belonging to the upper paravertebral ganglia of the sympathetic chain (36) ( Figure 1 ). SNS fibers enter the thymic cortical regions through the thymic capsule alongside blood vessels, and these fibers are predominantly found in the cortex, especially in the corticomedullary junction (37). Sympathetic neurons are found in close proximity to thymocytes, thymic epithelial cells, mast cells, and macrophages (6). These neuronal cells express catecholamine receptors and tyrosine hydroxylase; thus, they produce norepinephrine (38). Catecholamines were shown to have an inhibitory action on thymopoiesis (6, 39). Similar to the bone marrow, sympathetic innervation changes with age-related thymic involution (40). During thymic involution, the density of nerve fibers and the norepinephrine concentration increase, suggesting a role for sympathetic innervation in age-associated immune deregulation (41).
Thymic PaNS innervation was initially identified by histochemical and immunocytochemical studies of choline acetyl transferase, revealing positive nerve fibers around blood vessels in the thymic parenchyma (38) ( Figure 1 ). Nevertheless, the functional relevance of these PaNS fibers remains mostly unexplored. More recently, nonmyelinating Schwann cells were found to form a network in all thymic compartments, and these glial cells closely associate with blood vessels, dendritic cells (DCs), and lymphocytes (42).
포유류 흉선 내 카테콜아민 존재는 1974년 최초로 입증되었다(35). 현재 교감신경 섬유가 흉선을 신경 분포한다는 사실은 확립되었다. 특히, 흉선 교감 신경은 상부 교감 신경 사슬의 상부 척추측 신경절에 속하는 상부 경추 신경절과 성상 신경절에서 기원한다(36) (그림 1). SNS 섬유는 혈관과 함께 흉선 캡슐을 통해 흉선 피질 영역으로 진입하며, 이러한 섬유는 주로 피질, 특히 피질-수질 접합부에서 발견된다 (37). 교감 신경 세포는 흉선 세포, 흉선 상피 세포, 비만 세포 및 대식세포와 매우 근접한 위치에 존재한다(6). 이러한 신경 세포들은 카테콜아민 수용체와 티로신 하이드록실라아제를 발현하므로 노르에피네프린을 생성한다(38). 카테콜아민은 흉선생성에 억제 작용을 하는 것으로 밝혀졌다(6, 39). 골수와 유사하게, 교감신경 분포는 연령 관련 흉선 퇴행과 함께 변화한다(40). 흉선 퇴행 과정에서 신경 섬유 밀도와 노르에피네프린 농도가 증가하여, 교감신경 분포가 연령 관련 면역 조절 장애에 역할을 함을 시사한다(41).
흉선 부신경계(PaNS) 신경 분포는 콜린 아세틸전달효소에 대한 조직화학적 및 면역세포화학적 연구를 통해 처음 확인되었으며, 흉선 실질 내 혈관 주위에 양성 신경 섬유가 존재함이 밝혀졌다(38)(그림 1). 그럼에도 불구하고 이러한 PaNS 섬유의 기능적 관련성은 대부분 미개척 상태이다. 최근에는 비수초성 슈반 세포가 모든 흉선 구획에서 네트워크를 형성하는 것으로 밝혀졌으며, 이러한 신경교세포는 혈관, 수지상 세포(DC), 림프구와 밀접하게 연관되어 있다(42).
3.2. Neuronal Inputs in Secondary Lymphoid Organs
Autonomic innervation of the spleen is exclusively provided by the splenic nerve, which comprises SNS fibers from the superior mesenteric-celiac ganglion ( Figure 1 ). The sympathetic circuit to the spleen also includes preganglionic cholinergic sympathetic neurons that innervate postganglionic neurons (43). Postganglionic nerve terminals reach the spleen alongside blood vessels, forming a substantial network in the white pulp, becoming less dense in the red pulp and in B cell follicles (44). Nerve terminals in the splenic parafollicular zones are found in the vicinity of T cells, macrophages, and B cells (45).
The impact of splenic sympathetic innervation has been extensively explored. It is mainly regulated by norepinephrine, and it has been named the inflammatory reflex (46). The splenic inflammatory reflex is controlled by noradrenergic and cholinergic neuronal inputs, which result in attenuated activation of splenic macrophages (47). While there is no direct parasympathetic innervation in the spleen (43, 47), the splenic sympathetic tone can be controlled by the vagus nerve (48). This was termed the cholinergic anti-inflammatory pathway, since stimulation of the vagus nerve was shown to inhibit tumor necrosis factor (TNF) in inflammatory settings (49). In contrast, vagotomy significantly increases systemic TNF levels in response to intravenous endotoxin (50). Vagal regulation of splenic immunity was shown to be indirect, as it relies on the migration of vagus-primed immune cells from the gut to the spleen (50–52). A more controversial hypothesis is that vagal nerve inputs activate sympathetic neurons in the celiac ganglion (52, 53). Nevertheless, it is generally accepted that the cholinergic anti-inflammatory pathway leads to increased splenic norepinephrine (7, 54, 55).
Neuropeptides produced by sympathetic and sensory neurons are also relevant in the context of splenic immune regulation. Neuropeptide Y controls effector T and B cell expansion and IgG2a production (56, 57). Sympathetic cell– and T cell–derived VIP downregulates proinflammatory cytokine production by macrophages and T cells and activates tolerogenic DCs, leading to generation of regulatory T cells (Tregs) (58, 59). Sensory neuron–derived substance P stimulates lymphocyte proliferation through induction of IL-2, IL-4, and IFN-γ (60). Substance P also acts as a proinflammatory signal by inducing granulocyte- and macrophage-derived proinflammatory cytokines (60, 61). Sensory neuron–derived CGRP downregulates inflammation by acting on DCs, T cells, macrophages, and neutrophils (62–64). Finally, neuronal regulation of the spleen is also mediated by systemic neural and endocrine mediators found in the bloodstream (7).
3.2. 이차 림프 기관의 신경 입력
비장의 자율신경 분포는 상복대동맥-복강신경절에서 기원하는 교감신경계(SNS) 섬유로 구성된 비장신경에 의해 독점적으로 이루어진다(그림 1). 비장으로 향하는 교감신경 회로에는 또한 포신경절 신경세포를 분포시키는 전신경절성 콜린성 교감신경 세포도 포함된다(43). 후교감 신경 말단은 혈관과 함께 비장에 도달하여 백색 펄프에서 상당한 네트워크를 형성하며, 적색 펄프와 B 세포 소엽에서는 밀도가 낮아진다(44). 비장 소엽 주변 영역의 신경 말단은 T 세포, 대식세포 및 B 세포 근처에서 발견된다(45).
비장 교감 신경 분포의 영향은 광범위하게 연구되었다. 이는 주로 노르에피네프린에 의해 조절되며, 염증 반사(46)로 명명되었다. 비장 염증 반사는 노르아드레날린성 및 콜린성 신경 세포 입력에 의해 제어되며, 이는 비장 대식세포의 활성화 감소를 초래한다 (47). 비장에는 직접적인 부교감 신경 분포가 없지만(43, 47), 비장 교감 신경 긴장도는 미주 신경에 의해 조절될 수 있다(48). 이는 미주 신경 자극이 염증 환경에서 종양괴사인자(TNF)를 억제하는 것으로 밝혀져 콜린성 항염증 경로로 명명되었다(49). 반대로, 미주신경절제술은 정맥 내 내독소 투여에 대한 전신적 TNF 수치를 현저히 증가시킨다(50). 미주신경에 의한 비장 면역 조절은 장에서 비장으로 이동하는 미주신경에 의해 활성화된 면역 세포에 의존하므로 간접적인 것으로 밝혀졌다(50–52). 더 논란의 여지가 있는 가설은 미주신경 입력이 복강신경절의 교감신경 세포를 활성화한다는 것이다(52, 53) . 그럼에도 콜린성 항염증 경로가 비장 내 노르에피네프린 증가로 이어진다는 점은 일반적으로 인정된다(7, 54, 55).
교감 및 감각 신경세포가 생성하는 신경펩타이드 역시 비장 면역 조절 맥락에서 중요하다. 신경펩타이드 Y는 효과기 T세포 및 B세포 증식과 IgG2a 생성을 조절한다(56, 57). 교감 신경 세포 및 T 세포 유래 VIP는 대식세포와 T 세포의 전염증성 사이토카인 생산을 억제하고 내성 유도성 DC를 활성화하여 조절 T 세포(Tregs) 생성을 유도한다(58, 59). 감각 신경 세포 유래 서브스턴스 P는 IL-2, IL-4 및 IFN-γ 유도를 통해 림프구 증식을 촉진한다(60) . 서브스턴스 P는 또한 과립구 및 대식세포 유래 염증성 사이토카인을 유도함으로써 염증성 신호로 작용한다(60, 61). 감각 신경 유래 CGRP는 DC, T 세포, 대식세포 및 호중구에 작용하여 염증을 억제한다(62–64). 마지막으로, 비장에 대한 신경 조절은 혈류에서 발견되는 전신 신경 및 내분비 매개체에 의해 매개되기도 한다(7).
The anatomical origin of lymph node innervation has been less explored when compared with the spleen counterpart, but it is likely to be region specific. For example, SNS fibers in cervical lymph nodes originate from the superior cervical ganglia (65) ( Figure 1 ). Sympathetic nerve fibers enter lymph nodes alongside blood vessels into the subcapsular plexus (65). From the medulla to the paracortical regions, SNS fibers continue along blood vessels into T cell zones. In contrast, SNS fibers are not found in the nodular regions and germinal centers (13, 66). Norepinephrine release in lymph nodes is essential for antigen processing and efflux of activated lymphocytes into circulation, and the effect of catecholamines is dependent on the timing of their release in relation to other neuron-derived molecules (67). Without norepinephrine, cytotoxic T lymphocyte activation is reduced, while type 2 T helper (Th2) cell responses are unperturbed (13, 67–69). Substance P– and CGRP-producing nerve fibers have been detected in the vicinity of lymph node lymphocytes despite lack of evidence for lymph node cholinergic fibers (6). Finally, neuronal innervation contributes to lymph node development during embryogenesis. Notably, motor neuron–derived retinoic acid seemingly activates stromal cells that sequentially attract lymphoid tissue–inducer cells (70, 71).
Peyer patches are located in the antimesenteric side of the small intestine, and similar to lymph nodes they have organized T and B cell zones. Peyer patch development requires recruitment of hematopoietic cells to the gut and depends on neuroregulatory signals (71). Notably, expression of the neuroregulator RET in CD11c+ lymphoid tissue initiator cells is required for Peyer patch organogenesis (72). RET signaling in trans occurs in these cells through the GFRα3 (GDNF family receptor alpha) RET coreceptor and the glial cell–derived neurotrophic factor Artemin (72, 73). Interestingly, RET signals in cis are essential for ENS formation, via GFRα1 and the GDNF (72, 73). Thus, differential RET signaling pathways drive development of the enteric lymphoid and nervous systems. This solidifies the hypothesis that the immune and nervous systems may have evolved to integrate common signals that are essential for their development and function (1, 74, 75).
림프절 신경 분포의 해부학적 기원은 비장에 비해 덜 연구되었으나, 지역 특이적일 가능성이 높다. 예를 들어, 경부 림프절의 교감신경계(SNS) 섬유는 상경부 신경절(65)에서 기원한다( 그림 1). 교감신경 섬유는 혈관과 함께 림프절로 들어가 피막하 신경총으로 진입한다(65). 수질에서 피질주위 영역에 이르기까지 SNS 섬유는 혈관을 따라 T 세포 영역으로 계속 이어진다. 반면, SNS 섬유는 결절 영역과 생식 중심부에서는 발견되지 않는다(13, 66). 림프절에서의 노르에피네프린 방출은 항원 처리와 활성화된 림프구의 순환계 유출에 필수적이며, 카테콜아민의 효과는 다른 신경 유래 분자들과의 방출 시점에 따라 달라진다(67). 노르에피네프린이 없으면 세포독성 T 림프구 활성화는 감소하는 반면, 제2형 T 헬퍼(Th2) 세포 반응은 영향을 받지 않는다(13, 67–69). 림프절 콜린성 섬유에 대한 증거는 부족하지만, 서브스턴스 P 및 CGRP 생성 신경 섬유는 림프절 림프구 주변에서 검출되었다(6). 마지막으로, 신경 분포는 배아 발생 중 림프절 발달에 기여한다. 특히 운동 신경 세포 유래 레티노산은 간질 세포를 활성화하여 순차적으로 림프 조직 유도 세포를 유인하는 것으로 보인다(70, 71).
페이어 패치는 소장의 장간막 반대측에 위치하며, 림프절과 유사하게 조직화된 T 및 B 세포 영역을 가진다. 페이어 패치 발달은 장으로의 조혈 세포 모집을 필요로 하며 신경조절 신호에 의존한다(71). 특히, CD11c+ 림프조직 개시 세포에서의 신경조절인자 RET 발현은 페이어 패치 장기형성에 필수적이다(72). 이 세포들에서 RET 신호 전달은 GFRα3(GDNF 가족 수용체 알파) RET 코수용체와 신경교세포 유래 신경 영양 인자 아르테민(Artemin)을 통해 전이적으로 발생한다(72, 73). 흥미롭게도, RET 신호는 GFRα1과 GDNF를 통해 위장관 신경계(ENS) 형성에 필수적인 근접 신호 전달을 한다(72, 73). 따라서 차등적인 RET 신호 전달 경로는 장 림프계와 신경계의 발달을 주도한다. 이는 면역계와 신경계가 그들의 발달과 기능에 필수적인 공통 신호를 통합하도록 진화했을 수 있다는 가설을 확고히 한다(1, 74, 75).
3.3. Neuronal Inputs in the Intestine
Intestinal neurons can be classified as intrinsic (cell bodies are found within the gut: ENS) and extrinsic (cell bodies located outside the intestine: sympathetic and parasympathetic autonomic nervous system).
3.3. 장 내 신경 입력
장 신경세포는 내재성(세포체가 장 내부에 위치: ENS)과 외재성(세포체가 장 외부에 위치: 교감 및 부교감 자율신경계)으로 분류된다.
3.3.1. The enteric nervous system.
The adult intestine contains the largest immune cell compartment in the body and a neural network with as many neurons as the spinal cord. There are millions of enteric neurons, and thus the term second brain was coined (76). ENS neurons are intrinsic, since their cell bodies are within the walls of the gastrointestinal tract. Enteric neuronal networks are organized into the myenteric (or Auerbach) plexus and the inner submucosal (or Meissner) plexus, forming two layers of interconnected ganglia (77). Submucosal neurons control gut secretions, nutrient absorption, and local blood flow, while neurons in the myenteric plexus coordinate smooth muscle contractions (77, 78). A network of millions of enteric sensory neurons, interneurons, and motor neurons is able to produce panoplies of neurotransmitters and neuropeptides (2, 77, 79). The ENS is derived from multipotent neural crest cells that during embryonic development give rise to neurons and glial cells (77). However, neurogenesis and gliogenesis also occur postnatally (80).
3.3.1. 장 신경계.
성인 장은 신체 내 가장 큰 면역 세포 구획과 척수와 동등한 수의 뉴런을 가진 신경망을 포함한다. 수백만 개의 장 신경이 존재하기 때문에 '제2의 뇌'라는 용어가 만들어졌다(76). ENS 뉴런은 세포체가 위장관 벽 내에 위치하므로 내재성이다. 장 신경망은 근육층 신경총(또는 아우어바흐 신경총)과 점막하 신경총(또는 마이슬러 신경총)으로 구성되어 상호 연결된 두 개의 신경절 층을 형성한다(77). 점막하 신경세포는 장 분비, 영양소 흡수, 국소 혈류를 조절하는 반면, 근육층 신경총의 신경세포는 평활근 수축을 조정한다(77, 78). 수백만 개의 장 감각 신경세포, 중간신경세포, 운동신경세포로 구성된 네트워크는 다양한 신경전달물질과 신경펩타이드를 생성할 수 있다(2, 77, 79). ENS는 배아 발달 과정에서 신경세포와 신경교세포를 생성하는 다능성 신경능선세포에서 유래한다(77). 그러나 신경생성과 신경교세포생성은 출생 후에도 발생한다(80).
Enteric glial cells are found in enteric ganglia, within interganglionic tracts, in the smooth muscle, and in the lamina propria. In the lamina propria, glial cells and neuronal projections form a continuous network that extends from the base of the crypts to the mucosa. This neuronal network localizes in close proximity to subepithelial myofibroblasts, the epithelial membrane, and lymphatic vessels (81). Intestinal glial cells outnumber enteric neurons and can be identified by the expression of p75, Sox-10, GFAP, and S100β (82). Early studies indicated that glial cell ablation leads to complete disruption of intestinal barrier integrity, resulting in fatal jejunoileitis (83, 84). However, recent studies where partial conditional ablation of enteric glial cells was performed failed to induce intestinal inflammation and disrupted intestinal barrier (85). Interestingly, enteric glial cells were shown to express MHC-II molecules in the inflamed ileum of Crohn disease patients, suggesting that glial cells have critical roles in this condition (86, 87). In line with this idea, enteric glial cells were shown to sense pathogens and to produce neurotrophic factors that stimulate protective immune responses and help maintain the epithelial barrier integrity (88–92). Finally, enteric glial cells can transdifferentiate into enteric neurons upon damage-induced neuronal loss (74, 93).
The maintenance of gut homeostasis depends on the coordinated development and response of the ENS and the intestinal immune systems (74, 77, 80). As previously discussed, the most notable example is the coordinated development of Peyer patches and ENS via RET signals (72, 73, 94). Similarly, the development of fetal lymphoid tissue–inducer cells depends on retinoic acid that may be supplied by local enteric neurons (70, 95).
장 신경교세포는 장 신경절, 신경절간 경로, 평활근, 점막하층에서 발견된다. 점막하층에서는 신경교세포와 신경 돌기가 연속적인 네트워크를 형성하여 소장 기저부에서 점막까지 확장된다. 이 신경망은 상피하 근섬유모세포, 상피막, 림프관과 매우 근접한 위치에 존재한다 (81). 장 신경교세포는 장 신경세포보다 수가 많으며 p75, Sox-10, GFAP, S100β 발현으로 식별 가능하다(82). 초기 연구에 따르면 신경교세포 제거는 장 장벽 무결성의 완전한 파괴를 초래하여 치명적인 공장염을 유발한다(83, 84). 그러나 장 신경교세포의 부분적 조건부 제거를 수행한 최근 연구에서는 장 염증이 유발되지 않았으며 장 장벽이 파괴되었다 (85). 흥미롭게도 크론병 환자의 염증성 회장에서는 장 신경교세포가 MHC-II 분자를 발현하는 것으로 확인되어, 이 질환에서 신경교세포가 중요한 역할을 함을 시사한다(86, 87). 이와 일치하게, 장 신경교세포는 병원체를 감지하고 보호적 면역 반응을 자극하며 상피 장벽 무결성 유지에 기여하는 신경영양인자를 생성하는 것으로 밝혀졌다(88–92). 마지막으로, 장 신경교세포는 손상으로 인한 신경세포 손실 시 장 신경세포로 전분화될 수 있다(74, 93).
장 내 환경의 균형 유지에는 ENS와 장 면역계의 조화된 발달 및 반응이 필수적이다(74, 77, 80). 앞서 논의한 바와 같이, 가장 주목할 만한 사례는 RET 신호를 통한 페이어 패치와 ENS의 조화된 발달이다(72, 73, 94). 마찬가지로, 태아 림프구 조직 유도 세포의 발달은 국소 장 신경세포가 공급할 수 있는 레티노산에 의존한다(70, 95).
3.3.2. Sympathetic inputs in the intestine.
Intestinal peripheral nervous system neurons provide an axis between the CNS and the intestine, and this communication route has been termed the gut-brain axis. Sympathetic innervation of the gut is achieved by norepinephrine-producing efferent neurons extrinsic to the ENS (96, 97) ( Figure 1 ). SNS nerve terminals densely innervate the intestine in contact with the serosa, mucosa, muscularis, and myenteric plexus neurons (98–100). Sympathetic signals were shown to regulate intestinal immune responses through norepinephrine release, and adrenergic receptors are expressed by most innate and adaptive immune cell populations (101). Sympathetic neurons are present in Peyer patches, where they are found in close proximity to DCs, plasma cells, and T cell zones. Norepinephrine stimulates cytokine production by T cells, B cell proliferation, and immunoglobulin secretion (102, 103). In the muscularis, interactions between intestinal macrophages and sympathetic varicosities suppress TNF-α secretion and phagocytosis (104). The SNS is also involved in intestinal pathologies. Activation of the sympathetic reflex by inflammatory molecules leads to impaired gastrointestinal motility and modulates the intestinal immune system in conditions such as postoperative ileus, intestinal parasitic infection, and experimental colitis models (96). Crohn disease patients also have altered sympathetic innervation (105). Reciprocally, inflammation also impacts sympathetic nerves by inducing sprouting of fibers surrounding sensory neurons of the dorsal root ganglia, contributing to visceral hypersensitivity in inflammatory bowel diseases (106, 107).
3.3.2. 장의 교감신경 입력.
장 말초 신경계 뉴런은 중추신경계(CNS)와 장 사이의 축을 제공하며, 이 소통 경로는 장-뇌 축(gut-brain axis)으로 명명되었다. 장의 교감 신경 분포는 ENS 외부에서 노르에피네프린을 생성하는 원심성 뉴런에 의해 이루어진다(96, 97) (그림 1). 교감신경계(SNS) 신경 말단은 장의 장막, 점막, 근육층 및 장신경총 신경세포와 접촉하며 장을 밀집하게 분포한다(98–100). 교감신호는 노르에피네프린 방출을 통해 장 면역 반응을 조절하는 것으로 밝혀졌으며, 아드레날린 수용체는 대부분의 선천적 및 후천적 면역 세포 집단에 발현된다(101). 교감 신경 세포는 페이어 패치에 존재하며, 여기서 그들은 DC, 형질 세포 및 T 세포 영역과 근접해 있다. 노르에피네프린은 T 세포의 사이토카인 생산, B 세포 증식 및 면역글로불린 분비를 자극한다(102, 103). 근육층에서는 장 대식세포와 교감 신경 다발 사이의 상호작용이 TNF-α 분비와 식작용을 억제한다(104). 교감신경계는 장 병리에도 관여한다. 염증 분자에 의한 교감 반사 활성화는 위장 운동 장애를 초래하며, 수술 후 장폐색, 장 기생충 감염, 실험적 대장염 모델과 같은 상태에서 장 면역계를 조절한다(96). 크론병 환자에서도 교감 신경 분포가 변화한다(105). 반대로 염증은 후근 신경절의 감각 신경 세포를 둘러싼 섬유들의 분지를 유도함으로써 교감 신경에도 영향을 미치며, 이는 염증성 장 질환에서 내장 과민성에 기여한다(106, 107).
3.3.3. Parasympathetic inputs in the intestine.
Parasympathetic innervation in the gut is a two-neuron chain, with pre- and postganglionic neurons. Efferent neurons reach the midgut coming from the vagal dorsal nucleus, while efferent neurons reach the distal colon via the sacral spinal nerves (108) ( Figure 1 ). The vagus nerve also plays a role in gut immunomodulation establishing connections with the ENS in the intestinal myenteric plexus (109). Vagal nerve activation of enteric glia enhances barrier function through nicotinic acetylcholine receptor (nAChR) signaling (109). By controlling the inflammatory reflex, vagal innervation can also inhibit enteric innate immune responses (109). Parasympathetic inputs also modulate intestinal immunity through secretion of neuropeptides and stimulation of the hypothalamic-pituitary-adrenal axis (2).
3.3.3. 장 내 부교감 신경 입력.
장 내 부교감 신경 분포는 전신경절 및 후신경절 뉴런으로 구성된 이중 뉴런 사슬이다. 구심성 신경은 미주신경의 등측핵에서 중장까지 도달하며, 원심성 신경은 천골 척수신경을 통해 원위 결장까지 도달한다(108)( 그림 1). 미주신경은 또한 장내 신경계(ENS)와 장의 장신경총에서 연결을 형성함으로써 장 면역조절에 역할을 한다(109). 미주 신경에 의한 장 신경교세포 활성화는 니코틴성 아세틸콜린 수용체(nAChR) 신호전달을 통해 장벽 기능을 강화한다(109). 미주 신경 분포는 염증 반사를 조절함으로써 장 선천성 면역 반응을 억제할 수도 있다(109). 부교감 신경 입력은 또한 신경펩타이드 분비와 시상하부-뇌하수체-부신 축(HPA 축) 자극을 통해 장 면역 반응을 조절한다(2).
3.4. Neuronal Inputs in the Lung
The respiratory and gastrointestinal tracts have many structural similarities: an extensive luminal surface, an epithelial barrier, and an overlying mucous layer, which provide a barrier for commensals, pathogens, and foreign antigens. A dense network of pulmonary nerve fibers is found throughout the parenchyma of the respiratory system. Innervation of the airways is associated with glands, epithelial barrier, smooth muscle, and vasculature. There are even a small number of intrinsic neuronal ganglia in the lung that, akin to those of the ENS, derive from neural crest cells (110, 111). Efferent innervation of the airways comes from sympathetic and parasympathetic postganglionic nerve fibers ( Figure 1 ). These nerve fibers are involved in the regulation of mucous gland secretion, airway tone, and vascular smooth muscle tone (112). Sympathetic innervation comes from the superior cervical and stellate sympathetic ganglia, while parasympathetic innervation originates in the nucleus ambiguus in the brainstem, with a small number of neurons coming from the vagus nerve ( Figure 1 ) (113, 114). Sympathetic nerve fibers are characterized by the expression of tyrosine hydroxylase, neuropeptide Y, nitric oxide synthase, VIP, and ATP (112, 115), and adrenergic receptor stimulation through norepinephrine modulates pulmonary immune function (101). Curiously, and in contrast to other mammals, sympathetic innervation of smooth muscle in humans is almost absent, and regulation of bronchial tone mostly relies on circulating catecholamines (116).
3.4. 폐의 신경 입력
호흡기와 위장관은 광범위한 내강 표면, 상피 장벽, 그리고 공생균, 병원체 및 외부 항원에 대한 장벽 역할을 하는 점막층이라는 구조적 유사점을 많이 공유한다. 폐 신경 섬유의 조밀한 네트워크는 호흡기 계통의 실질 전체에 걸쳐 발견된다. 기도의 신경 분포는 선, 상피 장벽, 평활근 및 혈관과 연관되어 있다. 폐에는 소수의 내재성 신경절도 존재하는데, 이는 ENS의 신경절과 유사하게 신경능 세포에서 유래한다(110, 111). 기도의 원심성 신경 분포는 교감 및 부교감 신경절 후 신경 섬유에서 비롯됩니다( 그림 1). 이 신경 섬유들은 점액선 분비, 기도 긴장도, 혈관 평활근 긴장도 조절에 관여합니다(112). 교감 신경 분포는 상부 경추 교감 신경절과 성상 교감 신경절에서 비롯되며, 부교감 신경 분포는 뇌간의 모호핵에서 기인하며, 소수의 신경세포는 미주신경에서 유래한다(그림 1)(113, 114). 교감 신경 섬유는 티로신 하이드록실라제, 뉴로펩타이드 Y, 질소산화물 합성효소, VIP, ATP 발현으로 특징지어지며(112, 115), 노르에피네프린을 통한 아드레날린성 수용체 자극은 폐 면역 기능을 조절한다(101). 흥미롭게도, 다른 포유류와 달리 인간의 평활근에 대한 교감 신경 분포는 거의 존재하지 않으며, 기관지 긴장도 조절은 주로 순환하는 카테콜아민에 의존한다(116).
Pulmonary parasympathetic neurons can be classified into two main populations, classic cholinergic neurons in the airway walls and noncholinergic postganglionic neurons (112, 117). The main function of pulmonary cholinergic neurons is the induction of smooth muscle contraction and consequent bronchoconstriction (117). Noncholinergic postganglionic neurons originate in the myenteric plexus of the esophagus and in the outer striated longitudinal muscle layers (118). Acetylcholine signals through muscarinic receptors and nAChRs in immune cells. Similar to the case of other organ systems, in the airways, muscarinic receptor activation has proinflammatory effects while nAChR signaling has anti-inflammatory effects (112, 117). Parasympathetic neurons also release nitric oxide and VIP, which induce airway smooth muscle relaxation (115). Acute and chronic inflammatory respiratory diseases were shown to be modulated by immune and nervous system inputs. PaNS activation is a major source of lung inflammation in viral and bacterial infections, allergic asthma, and chronic obstructive pulmonary disease. Notably, vagal efferent and afferent neurons control symptoms such as bronchospasm, cough, dyspnea, and airway hyperreactivity (119).
Lung sensory neurons originate in the vagus nerve and lower cervical and upper thoracic spinal dorsal root ganglia (112, 113). Sensory innervation is essential for the pulmonary cycle, bronchomotor and vasomotor tones, and mucus secretion (112, 120). Sensory nerves also initiate respiratory sensations and reflexes (coughing and sneezing) in pathologic conditions (112). Additionally, there is evidence for the control of inflammation by peptidergic sensory neurons. For example, during viral infection, increased activity in sensory and autonomic innervation leads to the urge to cough (120). Nociceptor activation was also shown to induce the release of neuropeptides involved in recruitment and activation of immune cells (64, 121). In line with these findings, asthma patients have increased length and number of sensory nerves, which are also more sensitive to inflammatory stimuli (115, 122, 123). Thus, airway inflammation induces release of neuropeptides by sensory neurons, and this promotes sustained proinflammatory responses. Nevertheless, in humans the effect of neuropeptides on airway inflammation remains elusive since human sensory nerves have low expression of neuropeptides (124, 125).
폐 부교감 신경 세포는 두 가지 주요 집단으로 분류될 수 있는데, 기도 벽의 고전적 콜린성 신경 세포와 비콜린성 후신경절 신경 세포이다(112, 117). 폐 콜린성 신경 세포의 주요 기능은 평활근 수축을 유도하여 결과적으로 기관지 수축을 일으키는 것이다(117). 비콜린성 후신경절 신경세포는 식도의 장신경총과 외측 줄무늬 종근층에서 기원한다(118). 아세틸콜린은 면역 세포의 무스카린성 수용체와 nAChR을 통해 신호를 전달한다. 다른 장기 시스템과 마찬가지로, 기도에서 무스카린성 수용체 활성화는 염증 촉진 효과를 나타내는 반면, nAChR 신호전달은 항염증 효과를 보인다(112, 117). 부교감 신경 세포는 또한 일산화질소와 VIP를 분비하여 기도 평활근 이완을 유도한다(115). 급성 및 만성 염증성 호흡기 질환은 면역계와 신경계의 입력에 의해 조절되는 것으로 밝혀졌다. PaNS 활성화는 바이러스 및 세균 감염, 알레르기성 천식, 만성 폐쇄성 폐질환에서 폐 염증의 주요 원인이다. 특히 미주신경 원심성 및 구심성 뉴런은 기관지경련, 기침, 호흡곤란, 기도 과민성 등의 증상을 조절한다(119).
폐 감각 신경은 미주신경과 하부 경추 및 상부 흉추 척수 후근 신경절에서 기원한다(112, 113). 감각 신경 분포는 폐순환, 기관지운동 및 혈관운동 긴장도, 점액 분비에 필수적이다(112, 120). 감각 신경은 또한 병리적 상태에서 호흡 감각과 반사(기침 및 재채기)를 유발한다(112). 더불어 펩타이드성 감각 신경세포에 의한 염증 조절 증거도 존재한다. 예를 들어 바이러스 감염 시 감각 및 자율 신경 분포의 활동 증가가 기침 충동을 유발한다(120). 통각 수용체 활성화는 또한 면역 세포의 모집 및 활성화에 관여하는 신경펩타이드의 분비를 유도하는 것으로 나타났습니다(64, 121). 이러한 결과와 일치하게, 천식 환자는 감각 신경의 길이와 수가 증가하며, 염증 자극에 대한 민감도도 더 높습니다(115, 122, 123). 따라서 기도 염증은 감각 신경세포에 의한 신경펩타이드 분비를 유도하며, 이는 지속적인 염증성 반응을 촉진한다. 그러나 인간에서는 감각 신경의 신경펩타이드 발현이 낮기 때문에(124, 125), 신경펩타이드가 기도 염증에 미치는 영향은 여전히 불분명하다.
4. IMMUNE-DERIVED SIGNALS AND NERVOUS SYSTEM FUNCTION
Neuroimmune interactions are bidirectional, and immune-derived cues can signal to neurons. Immune cells produce cytokines; neuropeptides, such as enkephalins and endorphins; neurotransmitters, such as norepinephrine and acetylcholine; and hormones, such as luteinizing hormone and prolactin (126). Release of these molecules by immune cells has a significant impact in the nervous system. A notable example is the production of bone morphogenetic protein 2 (BMP2) by enteric macrophages, which stimulates expression of colony stimulatory factor 1 (CSF1) by neurons. This cross talk leads to an increase in peristaltic contractions and macrophage proliferation (127). The role of T cell–derived cytokines in neurons is also nicely illustrated by the finding that type 2 cytokines can induce chronic itch via sensory neuron activation in the skin (157).
One of the most relevant pathways of neuroimmune cross talk is the gut-brain axis. The enteric immune system can communicate directly and indirectly with the CNS to fine-tune responses to pathogens and tissue damage. The indirect route is mediated by the release of cytokines into circulation. Cytokines can reach the brain and activate neurons at circumventricular organs or can be actively transported to other brain regions (44). One example is the role of TNF and TNF-family cytokines in nervous system development and function (128–130). The direct route of gut-brain communication involves vagus nerve afferents and visceral afferents, which convey local immune signals to the brain (78, 109). Gut-brain communication modulates sympathetic input to immune organs. SNS cues can fine-tune immune responses, notably by modulating blood flow and cell distribution, but the SNS itself is also a target of immune-derived molecules. For example, the inflammatory molecule IL-1 increases circulating corticosteroids, which in turn promote the turnover of norepinephrine by hypothalamic noradrenergic neurons, thus resulting in a decrease of norepinephrine in the spleen (131, 132). However, the exact mechanisms behind the gut-brain axis have not yet been fully unraveled, in particular the CNS pathways that influence sympathetic outflow (132). Sympathetic deregulation can also lead to immune pathologies and vice versa. For example, human inflammatory conditions and mouse models of lupus present sympathetic neuropathy (133). In humans, high SNS activation or sympathetic neuropathy can be found in patients with diabetes, lupus, rheumatoid arthritis, heart failure, and chronic obstructive pulmonary disease (134–137). However, SNS regulation is only one dimension of the complex gut-brain axis. Enteric glial cells also seem to be involved in CNS disorders. Indeed, in transmissible spongiform encephalopathy, enteric glial cells act as a reservoir of infective prions serving as a template for misfolding proteins that then travel to the brain through autonomic pathways (138–140). Glial cells are also involved in the gut-brain axis in Parkinson disease, where enteric neurons and glial cells exhibit pathological features of Parkinson disease (141, 142).
4. 면역 유래 신호와 신경계 기능
신경-면역 상호작용은 양방향적이며, 면역 유래 신호는 뉴런에 신호를 전달할 수 있다. 면역 세포는 사이토카인, 엔케팔린 및 엔도르핀과 같은 신경펩타이드, 노르에피네프린 및 아세틸콜린과 같은 신경전달물질, 황체형성호르몬 및 프로락틴과 같은 호르몬을 생성한다(126). 면역 세포에 의한 이러한 분자들의 방출은 신경계에 상당한 영향을 미친다. 주목할 만한 예로 장내 대식세포가 생성하는 골형성인자 2(BMP2)가 신경세포의 군집자극인자 1(CSF1) 발현을 자극하는 현상이 있다. 이러한 교차작용은 연동수축 증가와 대식세포 증식을 유발한다(127). T 세포 유래 사이토카인의 신경세포 내 역할은 2형 사이토카인이 피부 감각 신경 활성화를 통해 만성 가려움을 유발할 수 있다는 연구 결과에서도 잘 드러난다(157).
신경-면역 교차 소통의 가장 핵심 경로 중 하나는 장-뇌 축이다. 장내 면역계는 중추신경계(CNS)와 직접적·간접적으로 소통하여 병원체 및 조직 손상에 대한 반응을 정밀 조절한다. 간접 경로는 순환계로의 사이토카인 방출을 통해 매개된다. 사이토카인은 뇌에 도달하여 뇌실 주위 기관의 뉴런을 활성화하거나 다른 뇌 영역으로 능동 수송될 수 있다(44). 한 예로 TNF 및 TNF 계열 사이토카인이 신경계 발달과 기능에서 수행하는 역할이 있다(128–130). 장-뇌 소통의 직접 경로는 미주신경 구심성 신경과 내장 구심성 신경을 통해 국소 면역 신호를 뇌로 전달한다(78, 109). 장-뇌 소통은 면역 기관에 대한 교감신경계 입력을 조절한다. 교감신경계 신호는 특히 혈류와 세포 분포 조절을 통해 면역 반응을 미세 조정할 수 있으나, 교감신경계 자체도 면역 유래 분자의 표적이 된다. 예를 들어, 염증성 분자인 IL-1은 순환하는 코르티코스테로이드를 증가시키며, 이는 차례로 시상하부 노르아드레날린성 뉴런에 의한 노르에피네프린의 전환을 촉진하여 비장의 노르에피네프린 농도를 감소시킵니다(131, 132). 그러나 장-뇌 축의 정확한 메커니즘, 특히 교감신경 유출에 영향을 미치는 중추신경계 경로는 아직 완전히 밝혀지지 않았습니다(132). 교감신경 조절 장애는 면역 병리를 유발할 수 있으며 그 반대의 경우도 마찬가지다. 예를 들어, 인간 염증성 질환 및 루푸스 마우스 모델에서는 교감신경병증이 관찰된다 (133). 인간에서는 당뇨병, 루푸스, 류마티스 관절염, 심부전, 만성 폐쇄성 폐질환 환자에서 높은 교감신경계(SNS) 활성화 또는 교감신경병증이 관찰된다(134–137). 그러나 SNS 조절은 복잡한 장-뇌 축의 한 측면에 불과하다. 장 신경교세포 역시 중추신경계 장애에 관여하는 것으로 보인다. 실제로 전염성 스폰지형 뇌병증(TSE)에서는 장 신경교세포가 감염성 프리온의 저장소 역할을 하며, 이는 단백질 변형을 유도하는 템플릿으로 작용하여 자율신경 경로를 통해 뇌로 이동한다(138–140). 파킨슨병에서도 장 신경교세포가 장-뇌 축에 관여하며, 장 신경세포와 신경교세포는 파킨슨병의 병리학적 특징을 보인다(141, 142).
신경-면역 교감의 또 다른 경로는 폐 염증에 의해 유발되는 중추 반사 활동이다. 감각 신경세포는 자극을 감지하여 구심성 미주신경을 통해
Another pathway of neuroimmune cross talk is the central reflex activity caused by lung inflammation. Sensory neurons can sense stimuli that are conveyed to the nucleus tractus solitarius in the brain through the afferent vagus nerve (117). Activation of sensory lung neurons leads to neuropeptide production that activates central reflexes such as cough. Central reflexes are immune dependent, since inflammation can modulate the activation of sensory neurons (118). Nociceptors can also be activated by proinflammatory cytokines and communicate these signals to the brain (143). For example, IL-5 stimulates sensory neurons expressing IL-5Ra to produce VIP (144). Thus, lung vagal afferent neurons play an important role during lung infection and inflammation, through the pulmonary vagal inflammatory reflex.
Aberrant immune responses can also affect neuronal function and behavior. A canonical example is the impact of infection on behavior. During infection, systemic proinflammatory cytokines reach a threshold where mammals develop symptoms such as fever, lethargy, anorexia, and social isolation. These sickness-induced behavioral changes allow the body to recover without spreading infection and limit inflammatory tissue damage (145). While behavioral changes during disease are mediated mostly by circulating proinflammatory cytokines, we cannot ignore the role of CNS immune cells. Microglia, brain-resident macrophages, are involved in neuronal regulation and consequently in pathological processes of many neurological diseases (146). The CNS immune repertoire is limited, but meningeal immune cells can cross the blood-brain barrier, and the release of cytokines in the brain can have profound impacts on behavior. For example, IFN-γ controls neural connectivity and can induce changes in social behavior through signaling in prefrontal cortex neurons (147). Another cytokine that impacts behavior is IL-17, which during fetal development regulates neuronal function and is involved in autism spectrum disorders, schizophrenia, and multiple sclerosis (148, 149). Meningeal IL-4-producing T cells have also been implicated in learning and memory (150). More recently, a new study has placed B lymphocytes as important regulators of oligodendrocyte proliferation and neuron myelination during early development, suggesting that B cell dysfunction may also contribute to mental disorders (151).
뇌의 고립핵(nucleus tractus solitarius)으로 전달한다(117). 폐 감각 신경세포의 활성화는 기침과 같은 중추 반사를 활성화하는 신경펩타이드 생성을 유발한다. 중추 반사는 염증이 감각 신경세포의 활성화를 조절할 수 있기 때문에 면역 의존적이다(118). 통각 수용체 또한 전염증성 사이토카인에 의해 활성화될 수 있으며 이러한 신호를 뇌로 전달한다(143). 예를 들어, IL-5는 IL-5Ra를 발현하는 감각 신경세포를 자극하여 VIP를 생성하게 한다(144). 따라서 폐 미주 신경 구심성 뉴런은 폐 미주 염증 반사를 통해 폐 감염 및 염증 과정에서 중요한 역할을 수행한다.
비정상적인 면역 반응은 신경 기능과 행동에도 영향을 미칠 수 있다. 전형적인 예는 감염이 행동에 미치는 영향이다. 감염 시 전신성 전염증성 사이토카인이 특정 역치에 도달하면 포유류는 발열, 무기력, 식욕 부진, 사회적 고립 등의 증상을 보인다. 이러한 질병 유발 행동 변화는 감염 확산 없이 신체가 회복되도록 하며 염증성 조직 손상을 제한한다(145). 질병 중 행동 변화는 주로 순환하는 전염증성 사이토카인에 의해 매개되지만, 중추신경계(CNS) 면역 세포의 역할을 간과할 수 없다. 뇌 상주 대식세포인 미세아교세포는 신경 조절에 관여하며 결과적으로 많은 신경학적 질환의 병리적 과정에 관여한다 (146). 중추신경계 면역 레퍼토리는 제한적이지만, 뇌막 면역 세포는 혈뇌 장벽을 통과할 수 있으며, 뇌 내 사이토카인 방출은 행동에 중대한 영향을 미칠 수 있다. 예를 들어, IFN-γ는 신경 연결성을 조절하며 전전두엽 피질 뉴런의 신호 전달을 통해 사회적 행동 변화를 유도할 수 있다(147). 행동에 영향을 미치는 또 다른 사이토카인은 IL-17으로, 태아 발달 기간 동안 신경 기능을 조절하며 자폐 스펙트럼 장애, 정신분열증, 다발성 경화증과 연관된다(148, 149). 뇌막 내 IL-4 생성 T 세포 역시 학습과 기억에 관여하는 것으로 밝혀졌다(150). 최근 연구에서는 B 림프구가 초기 발달 과정에서 올리고도교세포 증식과 신경 세포의 수초 형성에 중요한 조절자 역할을 한다는 사실이 밝혀져, B 세포 기능 장애 역시 정신 장애에 기여할 수 있음을 시사한다(151).
5. NEURO–IMMUNE CELL UNITS
5.1. Neuron-Neutrophil Interactions
Neutrophils provide a first line of host defense against tissue injury and invading pathogens via rapid mobilization, engulfment, intracellular killing, and release of antimicrobial factors and neutrophil extracellular traps. However, a limited number of studies have addressed the physiological relevance of neuron-neutrophil interactions in host defense. Nevertheless, current knowledge points to an inhibitory role of the SNS on neutrophil activation. Noradrenaline was shown to suppress neutrophil chemotaxis, activation, and phagocytosis in stroke (152). Furthermore, it was recently reported that the sensory nervous system suppresses peripheral neutrophil–mediated immunity in the lung and skin (153, 154). Nociceptor TRPV1+ sensory neurons release CGRP, suppressing pulmonary neutrophil recruitment and activation during Staphylococcus aureus lung infection (154) ( Figure 2a ). Nevertheless, distinct sensory neuron subsets (TRPV1+ and/or Nav1.8+) may have different functional contributions in pulmonary immunity and barrier function. Nociceptor-derived CGRP was also shown to inhibit neutrophil recruitment and opsonophagocytic activity in the skin during Streptococcus pyogenes necrotizing infection (153). Bacteria directly activate TRPV1+ nociceptor neurons through secretion of the pore-forming toxin streptolysin S, and nociceptor activation triggers local neuronal release of CGRP, mediating immune suppression (153). In both studies, a CGRP antagonist improved infection outcome (153, 154), suggesting that targeting this neuroimmune pathway could be a strategy to enhance host defense against invasive bacterial infections.
5. 신경-면역 세포 단위
5.1. 신경-호중구 상호작용
호중구는 신속한 동원, 포식, 세포 내 살상, 항균 인자 및 호중구 세포외 트랩(NET) 방출을 통해 조직 손상 및 침입 병원체에 대한 숙주 방어의 첫 번째 방어선을 제공한다. 그러나 신경-호중구 상호작용이 숙주 방어에서 가지는 생리학적 관련성을 다룬 연구는 제한적이다. 그럼에도 현재 지식은 교감신경계(SNS)가 호중구 활성화에 억제적 역할을 한다는 점을 시사한다. 노르아드레날린은 뇌졸중에서 호중구의 화학유인, 활성화 및 식작용을 억제하는 것으로 나타났다(152). 또한 최근 보고에 따르면 감각 신경계가 폐와 피부에서 말초 호중구 매개 면역을 억제한다(153, 154). 통각 수용체 TRPV1+ 감각 신경세포는 CGRP를 분비하여 황색포도상구균 폐 감염 시 폐 내 호중구 모집 및 활성화를 억제한다(154) ( 그림 2a). 그럼에도 불구하고, 서로 다른 감각 신경 세포 하위 집합(TRPV1+ 및/또는 Nav1.8+)은 폐 면역과 장벽 기능에서 서로 다른 기능적 기여를 할 수 있다. 통각 수용체 유래 CGRP는 또한 연쇄상구균 괴사성 감염 동안 피부에서 호중구 모집 및 식균작용 활성을 억제하는 것으로 나타났다(153). 박테리아는 기공 형성 독소인 스트렙톨리신 S를 분비하여 TRPV1+ 통각 수용체 뉴런을 직접 활성화하며, 통각 수용체 활성화는 CGRP의 국소 신경 세포 방출을 유발하여 면역 억제를 매개한다(153). 두 연구 모두에서 CGRP 길항제가 감염 결과를 개선시켰다(153, 154). 이는 이 신경면역 경로를 표적화하는 것이 침습성 세균 감염에 대한 숙주 방어력을 강화하는 전략이 될 수 있음을 시사한다.
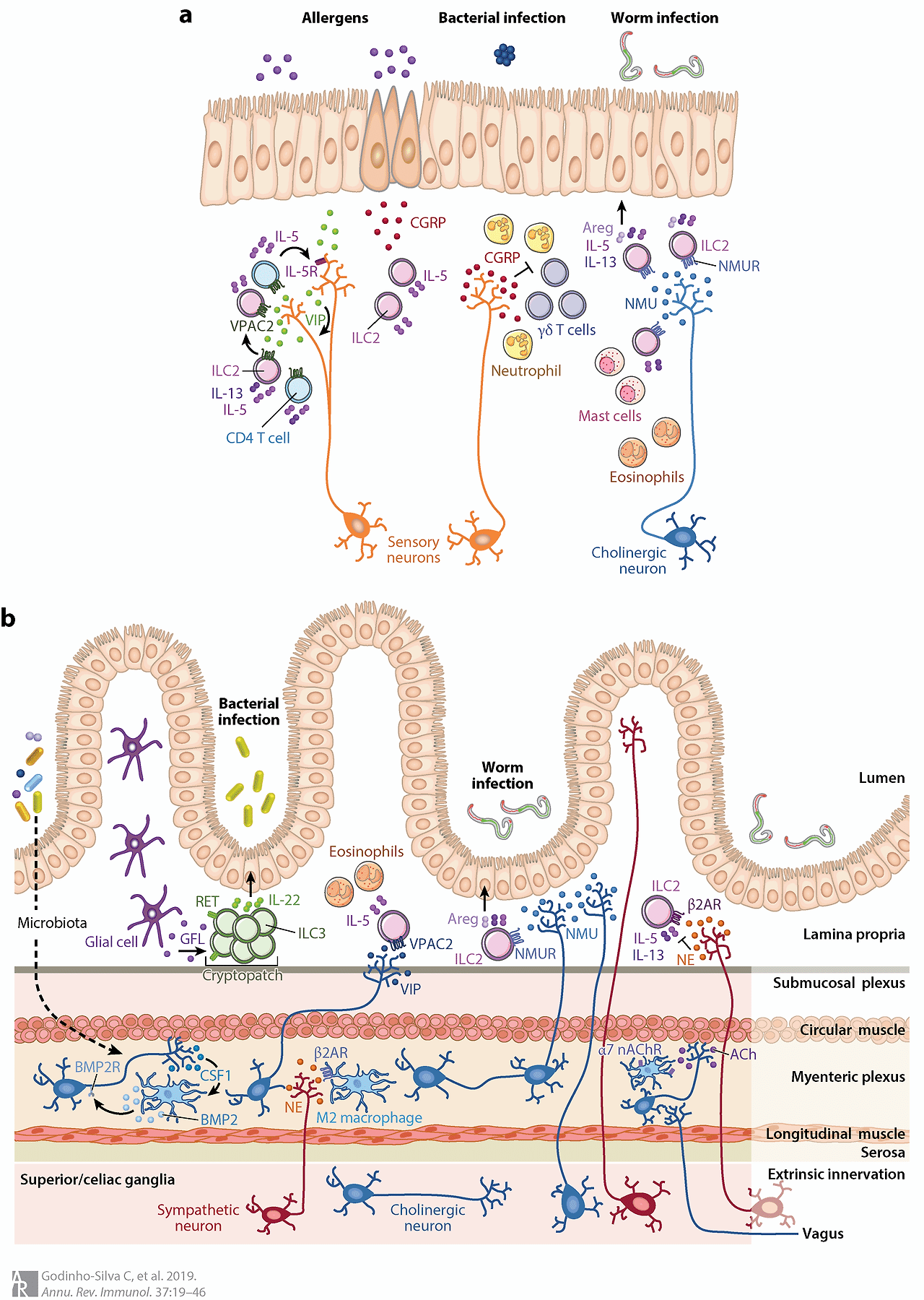
Figure 2 Neuro–immune cell units in the lung and intestine. (a) Pulmonary cholinergic neurons release NMU to stimulate ILC2s, promoting protective responses to parasites. Pulmonary sensory neurons also control ILC2 function through the release of CGRP, which stimulates IL-5 production. On the other hand, CGRP suppresses pulmonary neutrophil recruitment and activation, and resident γδ T cell–mediated host defense during Staphylococcus aureus lung infection. Sensory neuron–derived VIP increases IL-5 production by ILC2s, which stimulates nociceptors to produce increased VIP, generating a type 2 loop that potentiates allergy. (b) Enteric cholinergic neuron–derived NMU activates ILC2 responses and protects against helminth infection. Lamina propria ILC2 function is also regulated by VIP and NE. Glial cell–derived neurotrophic factors stimulate IL-22 production by lamina propria ILC3s, promoting barrier integrity. In the myenteric plexus, muscularis macrophages directly modulate neuronal function by secreting BMP2, which regulates peristaltic activity. SNS-derived NE induces a tissue-protective phenotype in muscularis macrophages. Cholinergic neuron–derived acetylcholine modulates macrophage activity reducing intestinal inflammation. Abbreviations: ACh, acetylcholine; α7 nAChR, alpha 7 nicotinic acetylcholine receptor; Areg, amphiregulin; β2AR, β2-adrenergic receptor; BMP2, bone morphogenetic protein 2; BMP2R, bone morphogenetic protein 2 receptor; CGRP, calcitonin gene–related peptide; CSF1, colony stimulating factor 1; NE, norepinephrine; NMU, neuromedin U; NMUR, neuromedin U receptor; SNS, sympathetic nervous system; VIP, vasoactive intestinal peptide; VPAC2, vasoactive intestinal peptide receptor 2.
그림 2 폐와 장의 신경-면역 세포 단위. (a) 폐 콜린성 뉴런은 NMU를 분비하여 ILC2를 자극함으로써 기생충에 대한 보호 반응을 촉진한다. 폐 감각 뉴런 또한 CGRP 분비를 통해 ILC2 기능을 조절하며, 이는 IL-5 생성을 자극한다. 반면 CGRP는 황색포도상구균 폐 감염 시 폐 호중구 모집 및 활성화와 상주 γδ T 세포 매개 숙주 방어를 억제한다. 감각 신경세포 유래 VIP는 ILC2의 IL-5 생산을 증가시켜 통각 수용체가 더 많은 VIP를 생성하도록 자극하며, 이는 알레르기를 증폭시키는 2형 루프를 생성한다. (b) 장 콜린성 신경세포 유래 NMU는 ILC2 반응을 활성화하고 선충 감염으로부터 보호한다. 점막하층 ILC2 기능 역시 VIP와 NE에 의해 조절된다. 신경교세포 유래 신경성장인자는 점막하층 ILC3의 IL-22 생산을 자극하여 장벽 무결성을 증진시킨다. 장신경총에서 근육층 대식세포는 BMP2 분비를 통해 신경 기능을 직접 조절하며, 이는 연동 운동을 조절한다. 교감신경계 유래 NE는 근육층 대식세포에 조직 보호형 표현형을 유도한다. 콜린성 신경세포 유래 아세틸콜린은 대식세포 활성을 조절하여 장 염증을 감소시킵니다. 약어: ACh, 아세틸콜린; α7 nAChR, 알파 7 니코틴성 아세틸콜린 수용체; Areg, 암피레굴린; β2AR, β2-아드레날린성 수용체; BMP2, 골형성인자 2; BMP2R, 골형성단백질 2 수용체; CGRP, 칼시토닌 유전자 관련 펩타이드; CSF1, 군집자극인자 1; NE, 노르에피네프린; NMU, 뉴로메딘 U; NMUR, 뉴로메딘 U 수용체; SNS, 교감신경계; VIP, 혈관활성 장펩타이드; VPAC2, 혈관활성 장펩타이드 수용체 2.
클릭하여 보기
Click to view
Neuron-mediated immune suppression during bacterial invasion can be detrimental. However, since pain accompanies inflammation, neuromodulation of neutrophils may provide a feedback mechanism to limit tissue damage by excessive inflammation (153). In addition, the impact of nociceptors in host defense may differ according to the type of pathogen. Neutrophil mobilization is protective in S. aureus pneumonia and S. pyogenes necrotizing fasciitis (153, 154). Thus, activation of immunosuppressive activity of nociceptors in these infections may mirror some degree of evolutionary pathogenic mechanisms. In contrast, sensory neurons promote host defense against skin infection with Candida albicans (155). Sensory neuron interactions with immune cells drive immune activation and inflammation in contact dermatitis (156, 157) and psoriasis (158) and mediate allergic airway inflammation in the respiratory tract (144, 159). Nevertheless, whether neuron-mediated immune suppression is context dependent and which signals might trigger a deleterious versus protective effect warrant clarification.
세균 침입 시 신경 매개 면역 억제는 해로울 수 있다. 그러나 염증에는 통증이 동반되므로, 과도한 염증에 의한 조직 손상을 제한하기 위한 피드백 메커니즘으로 호중구의 신경 조절이 작용할 수 있다(153). 또한, 병원체 유형에 따라 통각 수용체의 숙주 방어 영향은 다를 수 있다. 호중구 동원은 황색포도상구균 폐렴 및 연쇄상구균 괴사성 근막염에서 보호적 역할을 한다(153, 154). 따라서 이러한 감염에서 통각수용체의 면역억제 활성화를 유도하는 것은 어느 정도 진화적 병원성 기전을 반영할 수 있다. 반면, 감각신경세포는 칸디다 알비칸스 피부감염에 대한 숙주 방어를 촉진한다(155). 감각 신경세포와 면역세포의 상호작용은 접촉성 피부염(156, 157) 및 건선(158)에서 면역 활성화와 염증을 유발하며, 호흡기에서 알레르기성 기도 염증을 매개한다(144, 159). 그럼에도 불구하고, 신경세포 매개 면역 억제가 상황에 따라 달라지는지, 그리고 어떤 신호가 유해한 효과와 보호 효과를 유발하는지는 명확히 밝혀져야 한다.
5.2. Neuron–Mast Cell Interactions
Close anatomical association between mast cells and sensory and autonomic neurons has been described at barrier sites, such as the skin and the respiratory and the intestinal mucosae. Thus, the existence of a bidirectional and functional neuron–mast cell axis has long been proposed. Several studies support that mast cell mediators, such as histamine, serotonin, and tryptase, induce nociceptor sensitization (160). Activation of nociceptors drives the release of neuropeptides, including CGRP, corticotropin-releasing hormone (CRH), VIP, and substance P (160). Neuropeptides stimulate mast cell activation and degranulation, thus creating a bidirectional positive-signaling loop that may result in neurogenic inflammation (160, 161). Stress can trigger the release of neuropeptides (substance P and CRH) that promote the release of mast cell mediators and increase mast cells’ susceptibility to activation by bacterial antigens (160). Furthermore, neuron–mast cell interactions might have an important contribution to intestinal disorders, such as irritable bowel syndrome and inflammatory bowel disease (160, 162). Interactions between mast cells and sensory neurons have also been implicated in the pathophysiology of food and airway allergy and skin inflammation (163). Nevertheless, direct in vivo evidence of such neuroimmune functional units in the pathogenesis of allergic diseases is essentially lacking.
In addition to sensory neurons, sympathetic and cholinergic neurons might control mast cell function. Mast cells express β2-adrenergic receptors, which upon activation inhibit the release of histamine and other inflammatory mediators (44). Evidence for parasympathetic regulation of mast cells comes from several findings: (a) Intestinal mucosal mast cells contact vagal afferent terminals; (b) nAChRs and muscarinic cholinergic receptors are expressed by mast cells; (c) vagal stimulation or acetylcholine administration increases histamine in intestinal mast cells; and (d) nAChR agonists attenuate mast cell responses (164).
5.2. 신경-비만세포 상호작용
피부, 호흡기 및 장 점막과 같은 장벽 부위에서 비만세포와 감각 및 자율신경 세포 간의 밀접한 해부학적 연관성이 보고되었다. 따라서 양방향적이고 기능적인 신경-비만세포 축의 존재는 오랫동안 제안되어 왔다. 여러 연구에서 히스타민, 세로토닌, 트립타제와 같은 비만세포 매개물질이 통각수용체 감작을 유발한다는 사실을 뒷받침한다(160). 통각수용체의 활성화는 CGRP, 코르티코트로핀 방출 호르몬(CRH), VIP, 서브스턴스 P를 포함한 신경펩타이드의 방출을 촉진한다(160). 신경펩타이드들은 비만세포의 활성화와 탈과립을 자극하여, 신경성 염증을 유발할 수 있는 양방향적 양성 신호 전달 고리를 형성한다(160, 161). 스트레스는 비만세포 매개체 방출을 촉진하고 세균 항원에 의한 비만세포 활성화 감수성을 증가시키는 신경펩타이드(서브스턴스 P 및 CRH)의 방출을 유발할 수 있다(160). 또한, 신경-비만세포 상호작용은 과민성 대장 증후군 및 염증성 장 질환과 같은 장 장애에 중요한 기여를 할 수 있다(160, 162). 비만세포와 감각 신경세포 간의 상호작용은 또한 식품 및 기도 알레르기 및 피부 염증의 병리생리학에도 관여하는 것으로 알려져 있다(163). 그럼에도 불구하고, 알레르기 질환의 발병 기전에서 이러한 신경면역 기능 단위의 직접적인 생체 내 증거는 본질적으로 부족하다.
감각 신경 외에도 교감 신경 및 콜린성 신경이 비만세포 기능을 조절할 수 있다. 비만세포는 β2-아드레날린 수용체를 발현하며, 이 수용체가 활성화되면 히스타민 및 기타 염증 매개체의 방출을 억제한다(44). 비만세포의 부교감신경 조절에 대한 증거는 다음과 같은 여러 발견에서 비롯된다: (a) 장 점막 비만세포가 미주신경 구심성 말단과 접촉함; (b) 비만세포가 nAChR 및 무스카린성 콜린성 수용체를 발현함; (c) 미주신경 자극 또는 아세틸콜린 투여가 장 비만세포의 히스타민을 증가시킴; (d) nAChR 작용제가 비만세포 반응을 약화시킴 (164).
5.3. Neuron-Macrophage Interactions
Tissue-resident macrophages are highly heterogeneous and specialized phagocytes found in most body tissues. Macrophages recognize, engulf, and destroy target cells, present antigens to T cells, and initiate inflammatory processes. Macrophage-induced inflammatory effects are well known to be counteracted by the autonomic nervous system (53). Accordingly, the involvement of macrophages in the cholinergic anti-inflammatory pathway has been an area of extensive research (53, 165–167). Herein, we highlight recent studies that have been identifying macrophages as part of functional NICUs that regulate tissue-specific processes in the intestine and adipose tissue.
In the intestine, neuron-macrophage interactions regulate intestinal motility (127) and promote tissue protection during injury and infection (78, 168) ( Figure 2b ). In a mouse model of postoperative ileus, in which inflammation of the muscle layer impairs the contractility of the intestine, stimulation of the vagus nerve reduced intestinal inflammation and improved disease outcome (78). This process requires α7 nAChR expression on muscularis macrophages. Vagus nerve endings synapse with cholinergic myenteric neurons, in close contact with muscularis macrophages expressing α7 nAChR. Therefore, it has been proposed that vagal signals, through the ENS, modulate intestinal macrophage responses, inflammation, and, consequently, gut function (78). The relevance of the neuron-macrophage cross talk is further supported by studies showing that, in steady state, enteric neurons maintain muscularis macrophages through secretion of CSF1, a growth factor required for macrophage development (127). Reciprocally, muscularis macrophages can directly modulate neuronal function by secreting BMP2, which activates BMP receptor (BMPR)-expressing enteric neurons (127). This bidirectional cross talk regulates the peristaltic activity of the colon. Interestingly, commensal microbe-derived signals modulated BMP2 and CSF1 expression by macrophages and enteric neurons, respectively (127). This suggests that an intricate microbe-neuron-macrophage axis controls gastrointestinal motility, contributing to tissue homeostasis in steady-state conditions (127).
Using imaging and transcriptional profiling tools, Gabanyi and colleagues (168) demonstrated that intestinal macrophages exhibit intratissue specialization and compartmentalization. Lamina propria macrophages are similar to M1 (proinflammatory) macrophages, whereas muscularis macrophages display a tissue-protective program, being phenotypically similar to M2 (regulatory) macrophages. Activation of extrinsic sympathetic ganglia by enteric bacterial infection further enhances the tissue-protective profile of muscularis macrophages, via norepinephrine signaling in β2-adrenergic receptor–expressing macrophages (168).
Maintenance of an anti-inflammatory tissue environment is vital to preserve intestinal tissue homeostasis. Moreover, this is of special relevance in tissues where cells with reduced proliferative or regenerative potential are present, such as neurons. Therefore, striking parallels can be made between the gut and the CNS, where neuronal signals maintain the anti-inflammatory state of microglia, the CNS-resident macrophages (169). While these studies clearly demonstrate the relevance of neuron-macrophage cross talk for intestinal physiology, the neuronal sensing mechanisms by which luminal aggressions are detected, the potential involvement of both extrinsic and intrinsic innervation, and the exact circuits (afferent and efferent) involved in this process remain unknown. How dysregulated interactions between neurons and macrophages might contribute to tissue damage in gastrointestinal disorders and which signals might trigger such conditions also deserve attention.
Akin to their intestinal counterparts, specialized macrophages in the adipose tissue were recently shown to respond to neuronal cues (170) ( Figure 3a ). Pirzgalska and colleagues (170) identified a discrete population of macrophages tightly associated with sympathetic axons innervating the white adipose tissue, which the authors named sympathetic neuron–associated macrophages (SAMs). Importantly, SAMs take up and catabolize norepinephrine through expression of the norepinephrine transporter SLC6A2 and the norepinephrine-degrading enzyme monoamine oxidase A, respectively. Activation of the SNS, through optogenetics, resulted in increased norepinephrine uptake by SAMs. Additionally, genetic ablation of Slc6a2 in hematopoietic cells improved browning of white adipose tissue, increased thermogenesis and fat oxidation, and resulted in sustained weight loss in obese mice (170). A similar macrophage-mediated norepinephrine-degrading activity that compromises lipolysis was reported in the adipose tissue during aging (171). Nevertheless, whether the decline of lipolysis with aging is associated with increased SAMs in adipose tissue remains unclear. Tissue-resident macrophages were also found to control sympathetic innervation of brown adipose tissue, thus indirectly controlling local norepinephrine signaling, thermogenesis, and obesity (172). Hence, similarly to microglia in the brain and muscularis macrophages in the small intestine, adipose tissue macrophages seem to function as important hubs that integrate neuron-derived cues. Thus, it is tempting to speculate that brain, small intestine, and adipose tissue (and perhaps other tissues) have parallel mechanisms of macrophage-mediated neuronal protection in steady-state conditions and that disrupting the macrophage-neuron axis might result in tissue-specific pathology.
5.3. 뉴런-대식세포 상호작용
조직 상주 대식세포는 대부분의 신체 조직에서 발견되는 매우 이질적이고 특화된 식세포이다. 대식세포는 표적 세포를 인식, 포식 및 파괴하고, 항원을 T 세포에 제시하며, 염증 과정을 시작한다. 대식세포에 의해 유발되는 염증 효과는 자율신경계에 의해 상쇄된다는 것이 잘 알려져 있다(53). 이에 따라 콜린성 항염증 경로에서 대식세포의 관여는 광범위한 연구 분야가 되어 왔다(53, 165–167). 본고에서는 장 및 지방 조직에서 조직 특이적 과정을 조절하는 기능적 NICU의 일부로 대식세포를 규명해 온 최근 연구들을 중점적으로 소개한다.
장에서 신경-대식세포 상호작용은 장 운동성을 조절하며(127), 손상 및 감염 시 조직 보호를 촉진한다(78, 168)( 그림 2b). 근육층의 염증으로 장 수축력이 저하되는 수술 후 장폐색 마우스 모델에서, 미주신경 자극은 장 염증을 감소시키고 질병 예후를 개선했다(78). 이 과정은 근육층 대식세포에 α7 니코틴성 아세틸콜린 수용체(α7 nAChR) 발현이 필요하다. 미주 신경 말단은 α7 nAChR을 발현하는 근육층 대식세포와 밀접하게 접촉하는 콜린성 장신경절 신경세포와 시냅스를 형성한다. 따라서 미주 신호가 ENS를 통해 장 대식세포 반응, 염증 및 결과적으로 장 기능을 조절한다는 가설이 제기되었다(78). 신경-대식세포 간 교신의 중요성은 안정 상태에서 장 신경세포가 대식세포 발달에 필요한 성장인자인 CSF1 분비를 통해 근육층 대식세포를 유지한다는 연구 결과로 더욱 뒷받침된다(127). 반대로, 근육층 대식세포는 BMP2를 분비하여 BMP 수용체(BMPR) 발현 장신경세포를 활성화함으로써 신경 기능을 직접 조절할 수 있다(127). 이러한 양방향 교신은 결장의 연동 운동을 조절한다. 흥미롭게도 공생 미생물 유래 신호는 각각 대식세포와 장 신경세포에 의해 BMP2 및 CSF1 발현을 조절하였다(127). 이는 복잡한 미생물-신경-대식세포 축이 위장관 운동성을 제어하여 정상 상태에서 조직 항상성에 기여함을 시사한다(127).
이미징 및 전사 프로파일링 도구를 사용한 Gabanyi 등의 연구(168)에 따르면, 장 대식세포는 조직 내 특이성과 구획화를 나타낸다. 점막하층 대식세포는 M1(염증성) 대식세포와 유사한 반면, 근육층 대식세포는 조직 보호 프로그램을 나타내며, 표현형상 M2(조절성) 대식세포와 유사하다. 장내 세균 감염에 의한 외인성 교감 신경절의 활성화는 β2-아드레날린 수용체를 발현하는 대식세포에서의 노르에피네프린 신호전달을 통해 근육층 대식세포의 조직 보호 프로파일을 더욱 강화한다(168).
항염증성 조직 환경의 유지는 장 조직 항상성 보존에 필수적이다. 특히 신경세포처럼 증식 또는 재생 능력이 제한된 세포가 존재하는 조직에서는 더욱 중요하다. 따라서 장과 중추신경계(CNS) 간에 놀라운 유사점을 발견할 수 있는데, CNS 상주 대식세포인 미세아교세포의 항염증 상태는 신경 신호에 의해 유지된다(169). 이러한 연구들은 장 생리학에서 신경-대식세포 간 상호작용의 중요성을 분명히 보여주지만, 관강 내 공격을 감지하는 신경 감지 메커니즘, 외인성 및 내인성 신경 분포의 잠재적 관여, 그리고 이 과정에 관여하는 정확한 회로(구심성 및 원심성)는 여전히 알려지지 않았다. 신경과 대식세포 간의 조절 장애된 상호작용이 위장관 장애에서 조직 손상에 어떻게 기여할 수 있는지, 그리고 어떤 신호가 그러한 상태를 유발할 수 있는지도 주목할 가치가 있다.
장 내 대식세포와 유사하게, 지방 조직 내 특수화된 대식세포 역시 최근 신경 신호에 반응하는 것으로 밝혀졌다(170)(그림 3a). Pirzgalska와 동료들(170)은 백색 지방 조직을 신경 분포하는 교감 신경 축삭과 밀접하게 연관된 별개의 대식세포 집단을 확인했으며, 이를 교감 신경 관련 대식세포(SAMs)라고 명명하였다. 중요한 점은 SAMs가 노르에피네프린 수송체 SLC6A2 발현을 통해 노르에피네프린을 흡수하고, 노르에피네프린 분해 효소인 모노아민 산화효소 A 발현을 통해 이를 분해한다는 것이다. 광유전학을 통한 교감신경계(SNS) 활성화는 SAMs의 노르에피네프린 흡수 증가로 이어졌다. 또한 조혈 세포에서 Slc6a2의 유전적 제거는 백색 지방 조직의 갈색화를 개선하고 열생성 및 지방 산화를 증가시켜 비만 마우스에서 지속적인 체중 감소를 초래했습니다(170). 노화 과정에서 지방 조직에서 유사한 대식세포 매개 노르에피네프린 분해 활성이 보고되었으며, 이는 지방 분해를 저해한다(171). 그럼에도 불구하고 노화에 따른 지방 분해 감소가 지방 조직 내 SAMs 증가와 연관되는지는 여전히 불분명하다. 조직 상주 대식세포는 갈색 지방 조직의 교감 신경 분포를 조절하여 간접적으로 국소 노르에피네프린 신호전달, 열생성 및 비만을 제어하는 것으로 밝혀졌다(172). 따라서 뇌의 미세아교세포나 소장의 근육층 대식세포와 유사하게, 지방 조직 대식세포는 신경세포 유래 신호를 통합하는 중요한 허브 역할을 수행하는 것으로 보인다. 따라서 뇌, 소장, 지방 조직(그리고 아마도 다른 조직들)이 정상 상태에서 대식세포 매개 신경 보호 메커니즘을 병행적으로 가질 수 있으며, 대식세포-신경 축의 교란이 조직 특이적 병리를 초래할 수 있다는 추측이 유혹적이다.
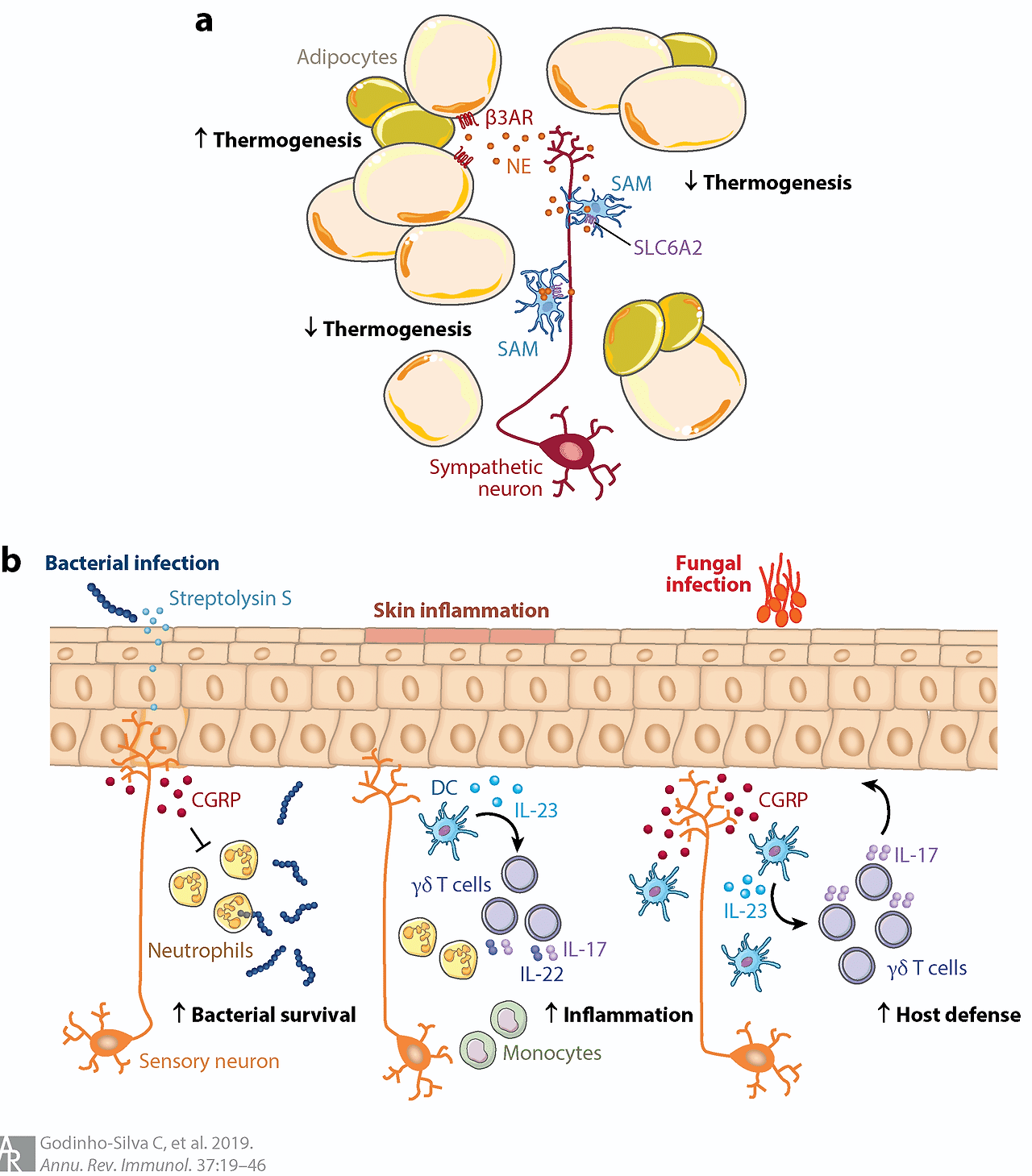
Figure 3 Neuro–immune cell units in adipose tissue and skin. (a) NE released by sympathetic neurons in the adipose tissue can be scavenged by SAMs through the NE transporter SLC6A2, possibly to prevent tissue-damaging NE spillover. Scavenging of NE also prevents the activation of the thermogenesis process via β3AR activation in adipocytes. (b) Sensory neurons in the skin are activated by Streptococcus pyogenes–derived streptolysin S toxin and release CGRP, mediating suppression of peripheral neutrophil–mediated immunity. DCs can also be modulated by sensory-derived CGRP in skin inflammation and Candida albicans infection. Nav1.8+ TRPV1+ nociceptor neurons induce IL-23 production by nearby dermal DCs, which then act on IL-23R+ γδ T cells to produce IL-17 and IL-22. Abbreviations: β3AR, β3-adrenergic receptor; CGRP, calcitonin gene–related peptide; DC, dendritic cell; NE, norepinephrine; SAM, sympathetic neuron–associated macrophage; SLC6A2, solute carrier family 6 member 2; TRPV1, transient receptor potential cation channel subfamily V member 1.
그림 3 지방 조직 및 피부의 신경-면역 세포 단위. (a) 지방 조직 내 교감 신경 세포가 분비한 NE는 SAMs에 의해 NE 수송체 SLC6A2를 통해 회수될 수 있으며, 이는 조직 손상을 유발하는 NE 유출을 방지하기 위함일 수 있다. NE 포획은 또한 지방세포 내 β3AR 활성화를 통한 열생성 과정의 활성화도 방지한다. (b) 피부의 감각 신경세포는 연쇄상구균(Streptococcus pyogenes) 유래 스트렙토리신 S 독소에 의해 활성화되어 CGRP를 분비하며, 이는 말초 호중구 매개 면역 억제를 매개한다. 피부 염증 및 칸디다 알비칸스 감염 시 감각계 유래 CGRP에 의해 DC도 조절될 수 있다. Nav1.8+ TRPV1+ 통각 수용체 신경세포는 인근 진피 DC의 IL-23 생산을 유도하며, 이는 IL-23R+ γδ T 세포에 작용하여 IL-17 및 IL-22를 생성한다. 약어: β3AR, β3-아드레날린 수용체; CGRP, 칼시토닌 유전자 관련 펩타이드; DC, 수지상 세포; NE, 노르에피네프린; SAM, 교감 신경 세포 관련 대식세포; SLC6A2, 용질 운반체 가족 6 구성원 2; TRPV1, 일시적 수용체 잠재력 양이온 채널 아가족 V 구성원 1.
Click to view
5.4. Neuron–Innate Lymphoid Cell Units
In the last decade, innate lymphoid cells (ILCs) have emerged as critical integrators of complex environmental and host-derived cues, playing key roles in lymphoid organogenesis, immunity to infection, inflammation, tissue remodeling, metabolic homeostasis, and cancer (173). At mucosal barriers ILCs reside in close proximity to neurons and glial cells, and multiple studies have explored the physiological relevance of such functional neuron-ILC units (174) ( Figure 2 ).
In the lung and small intestine, group 2 ILCs (ILC2s) respond to VIP through VPAC2 receptor–mediated signaling, which results in increased IL-5 production (144, 175). Innate IL-5 and IL-13 coexpression is enhanced after caloric intake, linking eosinophil levels with metabolic cycling (175). In the lung, VIP released by nodose afferent nociceptor sensory neurons stimulates ILC2s to produce IL-5, which can act directly on nociceptors, further increasing VIP expression and generating a type 2 inflammatory signaling loop that potentiates allergic inflammation (144). Strikingly, pulmonary neuroendocrine cells (PNECs), a rare population of airway epithelial cells that secrete GABA under the control of a neural circuitry (176), were also found to be in close proximity with ILC2s and to potentiate allergic asthma responses (177). Upon allergen challenge, PNECs enhance ILC2 cytokine production through CGRP secretion (177). Three other independent studies provided additional insight into how neuron-ILC2 interactions regulate type 2 immune responses. In response to helminthic infection or allergens, pulmonary and intestinal cholinergic neurons regulate ILC2 function via production of neuromedin U (NMU) (178–180). NMU signals through NMU receptor 1 (NMUR1) expressed in ILC2s and leads to a rapid and potent production of type 2 inflammatory cytokines, IL-5 and IL-13, and of the tissue-protective cytokine amphiregulin (178, 180). In vivo activation of this signaling axis enhances ILC2 responses and confers immediate tissue protection to helminthic infection. Subsequently, neuron-ILC2 units were identified as part of a neuron-based regulatory circuit that dampens ILC2-mediated type 2 inflammation (181). ILC2s express the β2-adrenergic receptor and colocalize with adrenergic neurons in the intestine. Abrogation of β2-adrenergic receptor–mediated signaling resulted in increased ILC2 responses, type 2 inflammation, and lower helminth infection burden, effects that were reversed by β2-adrenergic receptor agonist treatment (181). Together, these studies demonstrate that ILC2s can integrate distinct neuronal pathways—the cholinergic and sympathetic—revealing complex regulatory mechanisms by which ILC2 responses can be turned on and off. Thus, one can speculate that neuron-ILC2 units might regulate the balance between protective and pathological type 2 immune responses in health and disease.
A pioneering study revealed that enteric ILC3s are part of neuroglia-ILC3 units orchestrated by neurotrophic factors (92). Enteric glial cells sense microbial and host alarmin cues, which leads to increased glia-derived production of neurotrophic factors that in turn induce IL-22 production by RET-expressing ILC3s. Consequently, this glia-ILC3 axis is necessary for intestinal tissue repair upon inflammatory and infection insults (92). In addition to local neural cues, vagus nerve–derived signals have also been implicated in the regulation of ILC3 responses to bacterial infections in the peritoneal cavity (182). Importantly, glial cells and mucosal neurons were shown to sense local environmental perturbations, notably microbial cues, worm products, and host alarmins, through MYD88-dependent signaling (92, 178). Enteric neural cells can therefore coordinate ILC-mediated immune responses through the production of ILC-activating neuroregulators (92, 178). These seminal studies uncovering how neuron-ILC units trigger fast tissue protection through coordinated neuroimmune responses hold promise for targeting NICUs to fine-tune immune responses by dampening excessive detrimental inflammation or potentiating protective immunity and tissue repair.
Natural killer (NK) cells were identified in the early 1970s due to their ability to spontaneously kill leukemia cells and are now known as key effectors in cancer immunosurveillance, viral immunity, transplantation rejection, and autoimmunity (183). Nevertheless, whether NK cells establish functional interactions with neurons is mostly unexplored. Early studies indicate that catecholamines can have a dual time-dependent effect on NK cells. Catecholamines were shown to increase circulating NK cell numbers in an acute manner (184), whereas chronic stress or prolonged in vivo treatment with β2-adrenergic receptor agonists suppresses circulating NK cell numbers and activity (185). α1- and α2-adrenergic receptor mRNAs have also been detected in splenic NK cells, and agonist activation of either subtype increases NK cell cytotoxicity (186). More recently, reciprocal interactions between neural stem cells and NK cells in the brain were found to regulate neuroregenerative processes during neurological inflammatory disorders (187). During the chronic phase of multiple sclerosis in humans and experimental autoimmune encephalomyelitis (EAE) in mice, NK cells are retained in the subventricular zone of the brain, where they preferentially localize nearby neural stem cells. Neural stem cell–derived IL-15 sustains NK cell proliferation, survival, and function (187). In turn, NK cells inhibit neural stem cells, impairing their neuronal repair capacity, and NK cell removal promotes EAE recovery. Thus, neural stem cell–NK cell units in the brain regulate tissue repair and recovery from inflammation.
5.4. 신경-선천성 림프구 세포 단위
지난 10년간 선천성 림프구 세포(ILCs)는 복잡한 환경적 및 숙주 유래 신호의 핵심 통합자로 부상하여 림프기관 발생, 감염 면역, 염증, 조직 재구성, 대사 항상성 및 암에서 중요한 역할을 수행해 왔습니다(173). 점막 장벽에서 ILC는 뉴런 및 신경교 세포와 매우 근접한 위치에 존재하며, 여러 연구에서 이러한 기능적 뉴런-ILC 단위의 생리학적 관련성을 탐구했습니다(174) ( 그림 2).
폐와 소장에서 그룹 2 ILC(ILC2)는 VPAC2 수용체 매개 신호 전달을 통해 VIP에 반응하여 IL-5 생산을 증가시킵니다(144, 175). 선천성 IL-5 및 IL-13의 공동 발현은 열량 섭취 후 강화되어 호산구 수준을 대사 주기와 연결합니다 (175). 폐에서는 노도스(nodose) 통각 수용체 감각 뉴런이 분비하는 VIP가 ILC2를 자극하여 IL-5를 생성하게 하며, 이는 통각 수용체에 직접 작용하여 VIP 발현을 더욱 증가시키고 알레르기 염증을 증폭시키는 제2형 염증 신호 루프를 생성한다(144). 놀랍게도, 신경 회로에 의해 조절되는 GABA 분비 기능(176)을 가진 희귀한 기도 상피 세포 집단인 폐 신경내분비 세포(PNECs) 역시 ILC2와 근접해 위치하며 알레르기성 천식 반응을 증폭시키는 것으로 밝혀졌다(177). 알레르겐 자극 시 PNECs는 CGRP 분비를 통해 ILC2 사이토카인 생산을 증진시킨다(177). 다른 세 건의 독립적 연구는 신경-ILC2 상호작용이 제2형 면역 반응을 조절하는 방식에 대한 추가적 통찰을 제공했다. 기생충 감염이나 알레르겐에 반응하여, 폐 및 장의 콜린성 신경세포는 뉴로메딘 U(NMU) 생산을 통해 ILC2 기능을 조절한다(178–180). NMU는 ILC2에 발현되는 NMU 수용체 1(NMUR1)을 통해 신호 전달하며, 제2형 염증성 사이토카인인 IL-5 및 IL-13과 조직 보호 사이토카인인 암피레굴린(178, 180)의 신속하고 강력한 생산을 유도한다. 생체 내 이 신호 축의 활성화는 ILC2 반응을 증강시키고 기생충 감염에 대한 즉각적인 조직 보호를 부여한다. 이후, 뉴런-ILC2 단위는 ILC2 매개 2형 염증을 억제하는 뉴런 기반 조절 회로의 일부로 확인되었다(181). ILC2는 β2-아드레날린 수용체를 발현하며 장 내 아드레날린성 뉴런과 공위치를 이룬다. β2-아드레날린 수용체 매개 신호전달을 차단하면 ILC2 반응과 제2형 염증이 증가하고 기생충 감염 부담이 감소하는 효과가 나타났으며, 이는 β2-아드레날린 수용체 작용제 치료로 역전되었다(181). 종합하면, 이러한 연구들은 ILC2가 콜린성 및 교감신경계와 같은 서로 다른 신경 경로를 통합할 수 있음을 보여주며, ILC2 반응을 켜고 끌 수 있는 복잡한 조절 기전을 밝혀냈다. 따라서 신경-ILC2 단위가 건강과 질병 상태에서 보호적 및 병리적 제2형 면역 반응 간의 균형을 조절할 수 있다고 추측할 수 있다.
선구적 연구에 따르면 장내 ILC3는 신경영양인자에 의해 조율되는 신경교세포-ILC3 단위의 일부이다(92). 장 신경교세포는 미생물 및 숙주 경보 신호를 감지하여 신경 영양 인자의 교세포 유래 생산을 증가시키고, 이는 차례로 RET 발현 ILC3에 의한 IL-22 생산을 유도한다. 결과적으로 이 교세포-ILC3 축은 염증 및 감염 손상 시 장 조직 회복에 필수적이다(92). 국소 신경 신호 외에도, 미주신경 유래 신호는 복막강 내 세균 감염에 대한 ILC3 반응 조절에도 관여하는 것으로 밝혀졌다(182). 중요한 점은, 신경교세포와 점막 신경세포가 MYD88 의존적 신호전달을 통해 국소 환경 교란, 특히 미생물 신호, 기생충 생성물 및 숙주 알라민을 감지한다는 사실이 입증되었다(92, 178). 따라서 장 신경 세포는 ILC 활성화 신경 조절 인자의 생산을 통해 ILC 매개 면역 반응을 조정할 수 있다(92, 178). 신경-ILC 단위가 어떻게 조화된 신경면역 반응을 통해 신속한 조직 보호를 유발하는지 밝힌 이러한 선구적 연구들은 과도한 유해 염증을 억제하거나 보호 면역 및 조직 회복을 강화함으로써 면역 반응을 미세 조정하기 위한 NICU 표적화에 대한 가능성을 제시한다.
자연살해(NK) 세포는 1970년대 초 백혈병 세포를 자발적으로 사멸시키는 능력으로 확인되었으며, 현재 암 면역감시, 바이러스 면역, 이식 거부반응, 자가면역의 핵심 효과기로 알려져 있다(183). 그럼에도 불구하고 NK 세포가 신경세포와 기능적 상호작용을 형성하는지는 대부분 연구되지 않았다. 초기 연구에 따르면 카테콜아민은 NK 세포에 시간 의존적 이중 효과를 나타낼 수 있다. 카테콜아민은 급성적으로 순환 NK 세포 수를 증가시키는 것으로 밝혀졌으나(184), 만성 스트레스 또는 β2-아드레날린 수용체 작용제의 장기간 생체 내 투여는 순환 NK 세포 수와 활성을 억제한다(185). 비장 NK 세포에서도 α1- 및 α2-아드레날린 수용체 mRNA가 검출되었으며, 두 하위 유형의 작용제 활성화 모두 NK 세포 세포독성을 증가시킵니다(186). 최근 연구에서는 신경계 염증성 질환 동안 뇌 내 신경 줄기 세포와 NK 세포 간의 상호작용이 신경 재생 과정을 조절한다는 사실이 밝혀졌다(187). 인간 다발성 경화증 및 실험적 자가면역 뇌척수염(EAE)의 만성 단계에서 NK 세포는 뇌의 뇌실하 영역에 잔류하며, 이곳에서 신경 줄기 세포 근처에 선택적으로 국소화된다. 신경 줄기세포 유래 IL-15는 NK 세포의 증식, 생존 및 기능을 유지한다(187). 반대로 NK 세포는 신경 줄기세포를 억제하여 신경 세포 복구 능력을 저해하며, NK 세포 제거는 EAE 회복을 촉진한다. 따라서 뇌 내 신경 줄기세포-NK 세포 단위는 조직 복구와 염증 회복을 조절한다.
5.5. Neuron-DC Interactions
DCs are professional antigen-presenting cells with key roles in the initiation and regulation of adaptive immune responses. DCs recognize, process, and present antigens to T cells and, depending on the context of antigen presentation, can either promote T cell activation and differentiation or induce tolerance and differentiation of Tregs (188). Expression of adrenergic and neuropeptide receptors by DCs suggests that neuronal cues may modulate DC function. Therefore, several studies have addressed the impact of catecholamines and neuropeptides on DCs, while less attention has been given to cholinergic effects (189, 190). β2-adrenergic receptor signaling in DCs was shown to inhibit antigen cross-presentation to CD8 T cells, to suppress Th1 immune responses, and to promote Th2 and Th17 responses (44, 189). In contrast, stimulation of α-adrenergic receptors enhances antigen uptake and endocytosis and modulates DC migration (44, 189). VIP was also shown to regulate DCs, notably by inducing regulatory and tolerogenic DCs, which promote differentiation of Tregs, with important implications in autoimmune disorders and in transplantation (191–193). However, most of these studies were based on in vitro observations or in vivo administration of catecholamines or neuropeptides. Thus, evidence for cell-intrinsic neuron-DC interactions in vivo is still missing. Nevertheless, two recent studies described neuron-DC cross talk taking place in the skin (155, 158). Skin nociceptor neurons interact with DCs and modulate the IL-23/IL-17 pathway in the context of infection and inflammation (155, 158) ( Figure 3b ). Nav1.8+ TRPV1+ nociceptor neurons induce IL-23 production by nearby dermal DCs, which then act on IL-23R+ γδ T cells to produce IL-17F and IL-22. This results in recruitment of circulating neutrophils and monocytes, driving skin inflammation (158). In a subsequent study, sensory neurons were found to sense Candida albicans and enhance host resistance via secretion of the neuropeptide CGRP. CGRP triggered IL-23 production from DCs that then elicited protective IL-17A production from dermal γδ T cells, consequently controlling infection (155). Thus, these studies indicate that nociceptor fibers can integrate environmental signals to modulate local DC-mediated innate immune responses to infection and inflammation. Nevertheless, whether peripheral neurons can interact and directly modulate the activity of γδ T cells and how neuron-DC interactions modulate adaptive T cell responses in vivo are currently unknown.
5.5. 신경-DC 상호작용
DC는 적응 면역 반응의 개시 및 조절에 핵심적인 역할을 하는 전문 항원제시세포이다. DC는 항원을 인식, 처리하여 T 세포에 제시하며, 항원 제시 맥락에 따라 T 세포 활성화 및 분화를 촉진하거나 Treg의 관용 및 분화를 유도할 수 있다(188). DC의 아드레날린성 및 신경펩타이드 수용체 발현은 신경 신호가 DC 기능을 조절할 수 있음을 시사한다. 따라서 여러 연구에서 카테콜아민과 신경펩타이드가 DC에 미치는 영향을 다루었으나, 콜린성 효과에 대한 관심은 상대적으로 적었다(189, 190). DC 내 β2-아드레날린 수용체 신호전달은 CD8 T 세포에 대한 항원 교차제시를 억제하고, Th1 면역 반응을 억제하며, Th2 및 Th17 반응을 촉진하는 것으로 나타났다(44, 189). 반면, α-아드레날린 수용체 자극은 항원 포획 및 세포내흡수를 증진시키고 DC 이동을 조절한다(44, 189). VIP 또한 DC를 조절하는 것으로 밝혀졌는데, 특히 Treg 분화를 촉진하는 조절성 및 내성 유도성 DC를 유도함으로써 자가면역 질환 및 이식 분야에서 중요한 의미를 지닌다(191–193). 그러나 이러한 연구 대부분은 시험관 내 관찰 또는 생체 내 카테콜아민이나 신경펩타이드 투여를 기반으로 했다. 따라서 생체 내에서 세포 내재적 신경-DC 상호작용에 대한 증거는 여전히 부족하다. 그럼에도 최근 두 연구에서 피부에서 발생하는 신경-DC 교신(cross talk)을 기술하였다(155, 158). 피부 통각 수용체 뉴런은 감염 및 염증 상황에서 DC와 상호작용하며 IL-23/IL-17 경로를 조절한다(155, 158)( 그림 3b). Nav1.8+ TRPV1+ 통각 수용체 뉴런은 인근 진피 DC의 IL-23 생산을 유도하며, 이는 IL-23R+ γδ T 세포에 작용하여 IL-17F 및 IL-22를 생성한다. 이로 인해 순환 중성구와 단핵구가 유입되어 피부 염증을 유발한다(158). 후속 연구에서 감각 신경세포가 칸디다 알비칸스를 감지하고 신경펩타이드 CGRP 분비를 통해 숙주 저항성을 강화하는 것으로 밝혀졌다. CGRP는 DC로부터 IL-23 생산을 유발했으며, 이는 피부 γδ T 세포로부터 보호적 IL-17A 생산을 유도하여 감염을 제어했다(155). 따라서 이러한 연구들은 통각 수용체 섬유가 환경 신호를 통합하여 감염 및 염증에 대한 국소 DC 매개 선천 면역 반응을 조절할 수 있음을 시사한다. 그럼에도 불구하고 말초 신경세포가 γδ T 세포의 활동과 상호작용하고 직접 조절할 수 있는지, 그리고 신경-DC 상호작용이 생체 내에서 어떻게 적응성 T 세포 반응을 조절하는지는 현재 알려지지 않았다.
5.6. Neuron–T Cell Interactions
Autonomic regulation of adaptive immunity has long been appreciated, with most studies focusing on the impact of catecholamines in T and B lymphocyte function. The prevailing perspective is that the SNS modulates T and B lymphocytes, via β2-adrenergic receptor signaling, suppressing Th1 and promoting Th2, Th17, Treg, and antibody responses (44, 194). However, most of these studies were based on in vitro or ex vivo approaches following administration of adrenergic agonists/antagonists, or in vivo strategies to manipulate sympathetic neurotransmission. Thus, evidence for cell-intrinsic neuron-lymphocyte interactions in vivo is still missing.
In addition to the potential modulation of lymphocyte functions, adrenergic signals were also shown to control lymphocyte trafficking (195), and T cell–intrinsic circadian clocks imprint rhythmicity to lymphocyte migration (196). Thus, akin to HSCs, lymphocyte behavior might be modulated by the molecular clock via adrenergic signals. Nevertheless, whether the circadian neuronal axis is operational in T lymphocytes is currently unknown.
Reciprocally, lymphocytes can modulate neuronal signals, as illustrated by the cholinergic anti-inflammatory pathway. Vagus nerve stimulation requires sympathetic β2-adrenergic receptor signaling on CD4 lymphocytes to induce T cell–derived acetylcholine. The resulting CD4 T cell–derived acetylcholine activates nAChR expressed by splenic macrophages, suppressing the production of TNF-α and other proinflammatory cytokines (52, 54). Thus, in addition to local modulation of inflammation, neuron-lymphocyte interactions can also play a role in complex neuroimmunomodulatory circuits (4). Finally, the impact of lymphocytes on CNS neurons, neurophysiology, and behavior is an area of extensive research in the neuroimmunology field (197). Several lymphocyte-CNS interactions have been documented in health and disease (197); some of these aspects are discussed in Section 4.
5.6. 뉴런-T 세포 상호작용
자율신경계에 의한 적응면역 조절은 오래전부터 인식되어 왔으며, 대부분의 연구는 카테콜아민이 T 및 B 림프구 기능에 미치는 영향에 초점을 맞추어 왔다. 지배적인 관점은 교감신경계(SNS)가 β2-아드레날린 수용체 신호전달을 통해 T 및 B 림프구를 조절하여 Th1을 억제하고 Th2, Th17, Treg 및 항체 반응을 촉진한다는 것이다(44, 194). 그러나 이러한 연구 대부분은 아드레날린성 작용제/길항제 투여 후 체외(in vitro) 또는 생체 외(ex vivo) 접근법, 혹은 교감 신경 전달을 조작하는 생체 내(in vivo) 전략에 기반했다. 따라서 생체 내에서 세포 내재적 신경-림프구 상호작용에 대한 증거는 여전히 부족하다.
림프구 기능 조절 가능성 외에도, 아드레날린성 신호는 림프구 이동을 제어하는 것으로 밝혀졌으며(195), T 세포 내재적 생체시계는 림프구 이동에 리듬성을 부여한다(196). 따라서 HSC와 유사하게, 림프구 행동은 아드레날린성 신호를 통한 분자 시계에 의해 조절될 수 있다. 그럼에도 불구하고, 생체시계-신경축이 T 림프구에서 작동하는지는 현재 알려지지 않았다.
반대로, 림프구는 콜린성 항염증 경로에서 보듯이 신경 신호를 조절할 수 있다. 미주신경 자극은 CD4 림프구 상의 교감 β2-아드레날린 수용체 신호전달을 필요로 하여 T 세포 유래 아세틸콜린을 유도한다. 그 결과 생성된 CD4 T 세포 유래 아세틸콜린은 비장 대식세포가 발현하는 nAChR을 활성화하여 TNF-α 및 기타 전염증성 사이토카인의 생성을 억제한다(52, 54). 따라서 염증의 국소적 조절 외에도, 신경-림프구 상호작용은 복잡한 신경면역조절 회로에서도 역할을 할 수 있다(4). 마지막으로, 림프구가 중추신경계(CNS) 신경세포, 신경생리학 및 행동에 미치는 영향은 신경면역학 분야에서 광범위하게 연구되는 영역이다(197). 건강 및 질병 상태에서 여러 림프구-CNS 상호작용이 보고되었다(197); 이러한 측면 중 일부는 제4장에서 논의된다.
6. CONCLUDING REMARKS AND PERSPECTIVES
Known parallels between the immune and nervous systems suggest that intricate interactions between these systems might jointly integrate environmental cues and coordinate physiological processes (2, 5). While the role of inflammation in neuronal function and the impact of neuron-derived molecules in immune cells have been explored in the last decades, the more recent elucidation of NICUs as critical regulators of tissue homeostasis and physiology has revealed a picture that is far more complex than initially predicted (1). The complexity of NICUs is reflected in the myriad of tissues where they are present, the diversity of neurons and immune cell types they combine, the neuronal circuits they integrate, and the range of physiological processes they modulate. NICUs sense and integrate multiple environmental and host-derived signals and coordinate neuroimmune communication pathways to orchestrate tissue homeostasis. Thus, these coordinated neuroimmune regulatory responses might have been evolutionarily preserved to ensure organismal homeostasis throughout evolution.
The remarkable recent progress on the understanding of neuroimmune interactions is raising even more complex and exciting questions that warrant implementation of novel interdisciplinary approaches. Future challenges include the definition of local, regional, and systemic neuronal and immune circuits that communicate with discrete NICUs. State-of-the-art tools developed to target neuronal activity in vivo, such as optogenetics and chemogenetics, might help in deciphering some of these aspects.
Another remarkable challenge concerns the exploration of the potential of NICUs as therapy targets. Insights into the molecular mechanisms involved in neuroimmune interactions have been explored as new therapeutic possibilities in the clinical settings of inflammatory and autoimmune diseases. The main neuroimmune pathways that were therapeutically explored comprise the modulation of the inflammatory reflex through electrical vagus nerve stimulation. Pharmacological approaches, including α7 nAChR agonists, acetylcholinesterase inhibitors, muscarinic acetylcholine receptor agonists, and β2-adrenoreceptor agonists, are also being explored (198–208). Galantamine, an acetylcholinesterase inhibitor acting on the CNS, and in clinical use to treat Alzheimer disease, is currently being tested in a clinical trial, as a pharmacological approach for neuronal modulation of inflammation, in patients with metabolic syndrome (200, 207, 209). In addition to pharmacological therapies, electroacupuncture and implantable bioelectronic devices are being successfully explored as treatment strategies in which neural circuits are modulated to deliver anti-inflammatory signals to target organs. Electroacupuncture is able to trigger brain AChR-mediated signaling, which results in catecholaminergic signaling in the spleen through efferent vagus nerve activity. The result of this vagal stimulation is a reduction in proinflammatory cytokines that improves survival in an endotoxemia model (210). Similarly, electric stimulation of the sciatic nerve increases dopamine secretion in the adrenal medulla, suppressing the systemic inflammatory response, which results in increased survival in murine sepsis (211). Electric modulation of the inflammatory reflex has also been explored in the clinical context, in rheumatoid arthritis and inflammatory bowel disease conditions (212, 213). A recent clinical trial using a bioelectronic device for vagal stimulation demonstrated potential in reducing disease severity in 17 rheumatoid arthritis patients (212). In Crohn disease, vagal stimulation may also be a valuable therapeutic tool, since current pharmacological approaches have side effects and clinical studies have established that vagus nerve tone is attenuated in patients with this condition. This potential was demonstrated in a small clinical trial in which electrical vagus nerve stimulation was performed in 7 Crohn disease patients, resulting in disease remission at six months (213). The positive results of vagal stimulation in the clinical setting show promise for the establishment of bioelectronic devices as an alternative to pharmacological approaches. Therefore, a detailed understanding of the specificity of the molecular fingerprints and cellular players involved in NICUs holds promise for the discovery of novel therapeutic targets and the implementation of innovative therapies in the context of inflammatory, infectious, metabolic, and oncogenic conditions that are important public health concerns.
Still, many other aspects remain unexplored: Are NICUs regulated by the CNS? And conversely, can peripheral information from NICUs reach the brain and affect neuronal processes and behavior? Addressing the molecular, cellular, and circuitry aspects of bidirectional neuroimmune interactions is a major challenge for the decades to come. Nevertheless, it is tempting to speculate that peripheral NICUs might allow for sensing of environmental and endogenous threats, jointly hardwiring the CNS and peripheral organs, to maintain organismal homeostasis in health and disease.
6. 결론 및 전망
면역계와 신경계 사이의 알려진 유사성은 이 두 시스템 간의 복잡한 상호작용이 환경 신호를 통합하고 생리적 과정을 조정할 수 있음을 시사한다(2, 5). 지난 수십 년간 염증이 신경 기능에 미치는 역할과 신경세포 유래 분자가 면역세포에 미치는 영향이 탐구되어 왔지만, 최근 NICU가 조직 항상성과 생리학의 핵심 조절자로 밝혀지면서 초기 예측보다 훨씬 복잡한 양상이 드러났다(1). NICU의 복잡성은 그들이 존재하는 수많은 조직, 결합하는 신경세포와 면역세포 유형의 다양성, 통합하는 신경회로, 그리고 조절하는 생리학적 과정의 범위에 반영된다. NICU는 다중 환경 및 숙주 유래 신호를 감지·통합하고 신경면역 통신 경로를 조정하여 조직 항상성을 조율한다. 따라서 이러한 조화된 신경면역 조절 반응은 진화 과정에서 유기체 항상성을 보장하기 위해 진화적으로 보존되었을 수 있다.
신경면역 상호작용에 대한 최근의 놀라운 진전은 더욱 복잡하고 흥미로운 질문들을 제기하며, 이를 해결하기 위해 새로운 학제간 접근법의 도입이 요구된다. 향후 과제로는 개별 NICU와 소통하는 국소적, 지역적, 전신적 신경 및 면역 회로의 규명이 있다. 광유전학 및 화학적 유전학 등 생체 내 신경 활동을 표적화하기 위해 개발된 최신 기술들이 이러한 측면들을 해독하는 데 도움이 될 수 있다.
또 다른 주목할 만한 과제는 NICU의 치료 표적으로서의 잠재력 탐구와 관련됩니다. 신경면역 상호작용에 관여하는 분자적 메커니즘에 대한 통찰은 염증성 및 자가면역 질환의 임상 환경에서 새로운 치료 가능성으로 탐구되어 왔습니다. 치료적으로 탐구된 주요 신경면역 경로는 전기적 미주신경 자극을 통한 염증 반사 조절을 포함합니다. 약리학적 접근법으로는 α7 니코틴성 아세틸콜린 수용체 작용제, 아세틸콜린에스테라제 억제제, 무스카린성 아세틸콜린 수용체 작용제, β2-아드레날린 수용체 작용제 등이 연구되고 있다(198–208). 중추신경계에 작용하는 아세틸콜린에스테라제 억제제인 갈란타민은 알츠하이머병 치료에 임상적으로 사용되며, 현재 대사증후군 환자에서 염증의 신경 조절을 위한 약리학적 접근법으로 임상 시험 중입니다(200, 207, 209). 약리학적 치료법 외에도, 신경 회로를 조절하여 표적 기관에 항염증 신호를 전달하는 치료 전략으로 전기침술과 이식형 생체전자장치가 성공적으로 연구되고 있다. 전기침술은 뇌의 아세틸콜린 수용체(AChR) 매개 신호전달을 유발하여, 미주신경 원심성 활동을 통해 비장에서 카테콜아민 신호전달을 유도한다. 이러한 미주신경 자극의 결과로 전염증성 사이토카인이 감소하여 내독소혈증 모델에서 생존율이 향상된다(210). 마찬가지로, 좌골신경의 전기 자극은 부신 수질에서 도파민 분비를 증가시켜 전신 염증 반응을 억제하며, 이는 생쥐 패혈증 모델에서 생존율 증가로 이어진다(211). 염증 반사의 전기적 조절은 류마티스 관절염 및 염증성 장질환(IBD)과 같은 임상적 맥락에서도 탐구되었다(212, 213). 미주신경 자극을 위한 생체전자 장치를 사용한 최근 임상시험은 17명의 류마티스 관절염 환자에서 질환 중증도 감소 가능성을 보여주었다(212). 크론병에서도 미주신경 자극은 유용한 치료 도구가 될 수 있다. 현재의 약리학적 접근법은 부작용이 있으며, 임상 연구를 통해 이 질환 환자에게서 미주신경 긴장도가 약화된다는 사실이 확인되었기 때문이다. 이러한 가능성은 소규모 임상 시험에서 입증되었는데, 7명의 크론병 환자에게 전기적 미주신경 자극을 시행한 결과 6개월 만에 질병이 완화되었다(213). 임상 환경에서 미주신경 자극의 긍정적 결과는 약리학적 접근법의 대안으로서 생체전자 장치의 확립 가능성을 시사한다. 따라서 NICU(신생아 중환자실)에 관여하는 분자 지문과 세포적 요소의 특이성에 대한 상세한 이해는 공중보건상 중요한 염증성, 감염성, 대사성 및 발암성 질환 맥락에서 새로운 치료 표적 발견과 혁신적 치료법 구현에 기여할 수 있다.
그럼에도 불구하고, 여전히 탐구되지 않은 많은 측면들이 남아 있습니다: NICU는 중추신경계(CNS)에 의해 조절되는가? 반대로, NICU에서 발생하는 말초 정보가 뇌에 도달하여 신경 과정과 행동에 영향을 미칠 수 있는가? 양방향 신경면역 상호작용의 분자적, 세포적, 회로적 측면을 다루는 것은 향후 수십 년 동안의 주요 과제입니다. 그럼에도 불구하고, 말초 NICU가 환경적 및 내인성 위협을 감지하여 중추신경계와 말초 기관을 공동으로 하드와이어링함으로써 건강과 질병 상태에서 유기체의 항상성을 유지할 수 있을 것이라는 추측은 유혹적이다.
FUTURE ISSUES
- 1. Uncover novel multiple-tissue NICUs and their impact on tissue physiology.
- 2. Address the spatiotemporal dynamics of NICUs.
- 3. Explore the potential of NICUs for therapy targeting and design.
- 4. Map local and regional neuronal and immune circuits connecting to NICUs.
- 5. Explore the role of NICUs in hardwiring the CNS.
- 6. Explore the role of NICUs in organismal homeostasis in health and disease.
disclosure statement
The authors are not aware of any affiliations, memberships, funding, or financial holdings that might be perceived as affecting the objectivity of this review.
ACKNOWLEDGMENTS
acknowledgments
C.G.-S. is supported by Fundação para a Ciência e Tecnologia (FCT), Portugal. F.C. is a LisbonBiomed PhD student and is supported by FCT, Portugal. H.V.-F. is supported by ERC (647274), EU; and FCT, Portugal.
literature cited
- [Google Scholar]
- [Google Scholar]
- [Google Scholar]
- [Google Scholar]
- [Google Scholar]
- [Google Scholar]
- [Google Scholar]
- [Google Scholar]
- [Google Scholar]
- [Google Scholar]