치석을 제거하고
잇몸염증치료 효과에 탁월한 한약재 찾아 문치연 잇몸관리 치약 만들기 프로젝트..
가루 형태의 치약
문치연 3가지 죽염허브 치약
1. 잇몸염증
2. 치석제거
3. 미백효과
아라고나이트(오적골)
활성탄
녹차 강황 울금 등......
https://pmc.ncbi.nlm.nih.gov/articles/PMC9382037/
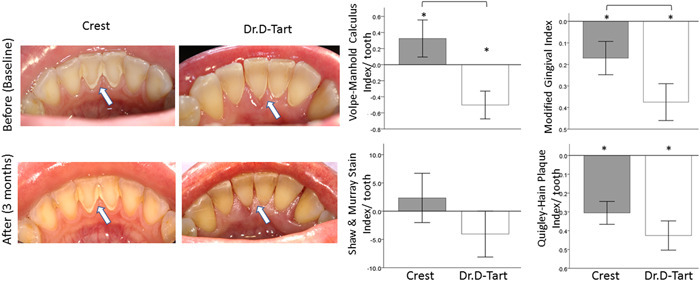
이 논문은 오징어 뼈(갑오징어 bone)에서 추출한 아라고나이트(aragonite)를 사용한 치약이 치석(calculus) 관리에 얼마나 효과적인지를 평가한 이중맹검 무작위 대조 임상시험입니다.
기본 정보
- 제목: Aragonite toothpaste for management of dental calculus: A double‐blinded randomized controlled clinical trial
- 저널: Clinical and Experimental Dental Research
- 출판: 2022년
- 주요 저자: Ashwaq A Al-Hashedi 외 (Faleh Tamimi 교신저자)
연구 목적
치석 제거와 재형성을 억제하는 데 효과적인 새로운 치약을 찾기 위해, **갑오징어 유래 아라고나이트 치약(제품명: Dr. D-Tart)**과 일반 상용 치약(Crest)을 비교.
연구 방법
- 대상: 81명 (개입군 40명, 대조군 41명)
- 설계: 이중맹검 RCT (Double-blinded randomized controlled trial)
- 기간: 기준선 → 3개월 → 9개월 (중간에 3개월 시점에 스케일링+폴리싱 시행)
- 평가 항목: 치석 지수(Volpe-Manhold), 플라크, 잇몸염증(MGI), 착색 지수 + 환자 만족도 설문
주요 결과 (가장 중요한 부분)
- 3개월 사용 후 → 아라고나이트 치약 그룹: 치석 30% 감소 (p=0.0006) → 대조군(Crest) 대비 45% 적은 치석 (p=0.0001)
- 스케일링 후 6개월(총 9개월 시점) → Crest 그룹 치석 점수가 Dr. D-Tart 그룹보다 42% 더 높음 (p=0.0692, 경계선 유의)
- 잇몸 건강 → 아라고나이트 그룹이 MGI(Modified Gingival Index) 40% 낮음 (p<0.0001) → 잇몸염증이 유의하게 적음
- 플라크 제거와 착색 제거 효과는 두 치약 간 차이 거의 없음
- 환자 만족도: 아라고나이트 치약이 텍스처·사용감 등에서 더 높은 만족도 (9개월 시점 유의미 차이)
결론 (논문에서 직접 나온 핵심 문장 요약)
갑오징어 유래 아라고나이트 치약은
- 치석을 효과적으로 제거하고
- 치석 재형성 억제에 우수하며
- 잇몸 건강을 개선시키고
- 환자 만족도도 높다.

논문 요약
치석은 인간과 반려동물의 구강 건강에 심각한 영향을 미치며,
치은 외관 저하·염증 유발, 제거 실패 시 치주염(periodontitis) 등 구강 질환을 초래합니다.
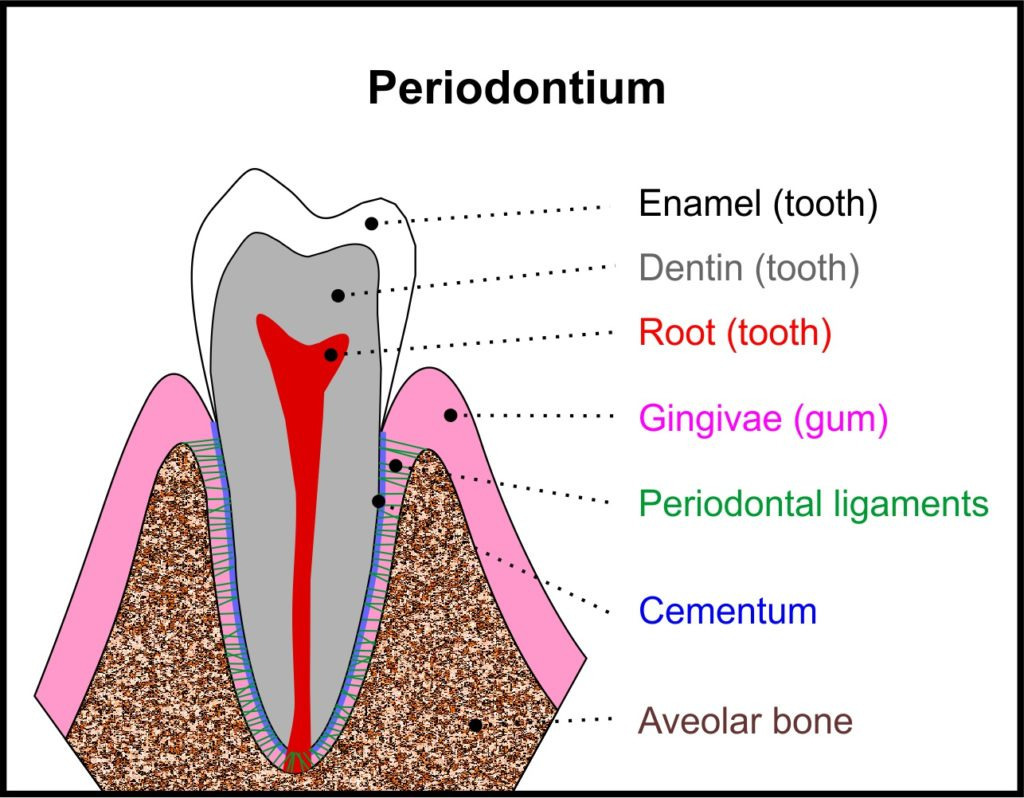
- Enamel (tooth) → 법랑질 (치아) 치아의 가장 바깥쪽 단단한 층으로, 인체에서 가장 단단한 조직입니다. 충격과 마모로부터 치아를 보호하며, 거의 97%가 무기질(하이드록시아파타이트)로 이루어져 있습니다.
- Dentin (tooth) → 상아질 (치아) 법랑질 바로 아래에 있는 노란빛의 층으로, 치아의 대부분을 차지합니다. 법랑질보다 단단하지만 덜 단단하며, 미세한 세관(dentinal tubules)이 있어 자극이 전달되면 시린 느낌(치아 과민증)을 유발할 수 있습니다.
- Root (tooth) → 치근 (치아 뿌리) 치아의 잇몸 아래 부분으로, 치조골 속에 박혀 있는 뿌리입니다. 그림에서 붉은색으로 표시된 부분이 치근입니다.
- Gingivae (gum) → 치은 (잇몸) 치아 주위를 둘러싸고 있는 분홍색 연조직으로, 치아를 보호하고 음식 찌꺼기 침투를 막습니다. 건강한 치은은 연한 분홍색이고 단단합니다.
- Periodontal ligaments → 치주인대 (치주섬유) 치근과 치조골 사이를 연결하는 섬유성 결합조직으로, 치아를 충격으로부터 보호하고 씹을 때 충격을 흡수·분산시키는 역할을 합니다. 그림에서 녹색 선으로 표시된 부분입니다.
- Cementum → 백악질 (시멘트질) 치근 표면을 덮고 있는 얇은 무기질 층으로, 치주인대 섬유가 붙는 곳입니다. 법랑질보다 부드럽고, 치아 재생·수복에 중요한 역할을 합니다. 그림에서 파란색 선으로 둘러싸인 부분입니다.
- Alveolar bone → 치조골 (치조뼈) 치아 뿌리가 박혀 있는 턱뼈 부분으로, 치아를 단단히 고정합니다. 치주염이 심해지면 이 치조골이 흡수(소실)되어 치아가 흔들리게 됩니다. 그림에서 갈색 점무늬 영역입니다.
치주조직(Periodontium)의 4대 구성 요소 요약
- 치은 (Gingiva) – 잇몸
- 치주인대 (Periodontal ligament) – 치아와 뼈를 연결하는 섬유
- 백악질 (Cementum) – 치근 표면을 덮는 층
- 치조골 (Alveolar bone) – 치아가 박혀 있는 뼈

또한 일부 전신 질환(심혈관 질환, 당뇨 등)과도 밀접한 관련이 있습니다.
주요 내용:
- 치석 형성 기전 (Pathogenesis):
- 치석 형성은 세균성 요인, 면역 요인, 숙주 요인의 상호작용으로 발생 (Fig. 1에서 이 세 요인이 서로 연결되어 촉진됨).
- 플라크(biofilm)가 치아 표면에 부착 → 국소 칼슘·인 농도 상승 → 생물광물화(biomineralization) 촉진.
- 최근 핵심 발견: 성숙 바이오필름 내 세균이 중성구 세포외 트랩(NETs)의 DNA를 DNase I에 의한 분해로부터 보호(resistance)하게 만들어 아파타이트(apatite) 핵형성·성장을 촉진 (2024 Nat Biomed Eng 관련 연구 인용).
- 구강 내 생리적 평형이 깨지면 (pH 변화, ureolytic bacteria 증가 등) 치석 형성 가속.
- 호중구 세포외 트랩(NETs)은 감염, 특히 대형 병원체로부터 보호하는 역할을 하지만, 점점 더 많은 면역매개 질환과 관련된 병리에도 관여한다.
- NET 형성은 선천성 면역 수용체에 의해 유발되며, 이는 NADPH 산화효소 또는 미토콘드리아에서 생성되는 활성산소종(ROS)을 포함한 하류 세포내 매개체를 통해 골수과산화효소(MPO), 호중구 엘라스테이스(NE) 및 단백질-아르기닌 데이미네이스 4형(PAD4)을 활성화하여 염색질의 응축 해소를 촉진합니다.
- NETosis는 미생물 신호와 내인성 위험 신호에 반응하여 유도되며, 급성 염증이나 만성 염증성 및 자가면역 질환 시 과도한 조직 손상을 방지하기 위해 엄격히 조절되어야 합니다. 미생물 크기, 미생물 독성 인자 및 사이토카인은 NETosis의 조절인자입니다.
- NET은 질병과 연관된 여러 면역 조절 기능을 가진다. NET 관련 산화 DNA 및 항균 펩타이드로 인한 인터페론 반응을 자극하여 무균성 염증을 유도하거나 자가면역 반응을 증강시키는 방식으로 다른 면역 세포를 활성화시킬 수 있다.
- NET은 또한 혈전 형성을 촉진하여 혈관을 폐쇄하고 주요 장기 부위를 차단하며, 전이성 종양을 포획하고 당뇨병에서 상처 치유를 지연시킬 수 있다.
초록
호중구는 선천성 면역 식세포로, 면역 방어에서 핵심적인 역할을 합니다. 병원체 제거, 면역 조절 및 질병 병리학에서 호중구의 역할에 대한 우리의 이해는 최근 몇 년간 극적으로 발전했습니다. 호중구 세포외 트랩(NETs)으로 알려진 거미줄 모양의 염색질 구조는 호중구 생물학에 대한 이러한 새로운 관심의 최전선에 서 있습니다. NETs 방출을 조절하는 분자들의 확인은 면역 보호, 염증성 및 자가면역 질환, 암에서 NETs의 역할에 대한 우리의 관점을 정교화하는 데 기여했습니다. 본고에서는 지금까지 NET 생물학 분야를 형성해 온 주요 발견과 개념들을 논의합니다.
- 영향 요인 및 전신 질환 연관:
- 치석 침착이 치주염 주요 병인 + 플라크 유지 인자로 작용.
- 전신 질환(고혈압, 심장병 등)과 치석의 상관성 강조 (예: 치석 지수 높은 경우 협심증 위험 증가 등 과거 코호트 연구 인용).
- 예방 및 치료 전략 (Prevention Strategies):
- 전통 방법: 칫솔질, 클로르헥시딘 구강세정제, scaling & root planing (SRP) – 치아 표면 연마로 재부착 방지.
- 최근 발전: 단기(기존 플라크 제거) + 장기(재형성 억제) 목표 결합 필요성 제안.
- 신규 접근: 결정 성장 억제제(zinc, pyrophosphates 등) 첨가 치약, 항균제(triclosan + copolymer), 광역학 치료 등.
- 개념적 솔루션 제시: 기존 치료 개선 + 재발 최소화 위한 통합 전략 (예: 바이오필름 구조 파괴 + 미생물 균형 유지).
결론: 치석 형성 메커니즘 이해가 구강·전신 건강 보호에 핵심. 최근 연구(특히 NETs 관련)를 바탕으로 더 효과적·예방 중심 치료 체계 필요.
그림(Figures) 상세 설명
이 리뷰 논문은 개념적·기전 설명 중심으로 총 몇 개의 주요 그림을 포함합니다. (PMC全文 기준으로 가장 중요한 그림 설명 – 시각 자료가 기전 이해에 핵심적임)
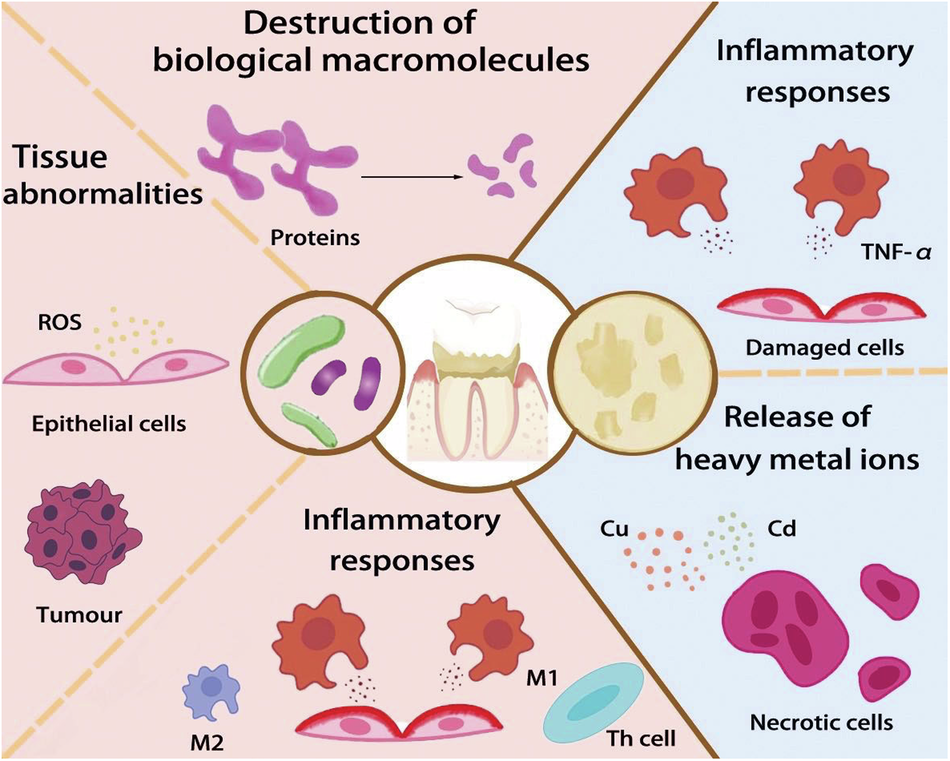
- Fig. 1 | Pathogenesis of dental calculus involves bacteria and matrix mineralization 가장 중요한 그림! 삼각형 또는 순환 다이어그램 형태로 세 요인(세균성·면역성·숙주성)이 서로 화살표로 연결되어 상호작용하는 구조.
- 중앙: "Dental calculus formation" (치석 형성).
- 왼쪽: Bacterial factors (바이오필름 형성, ureolytic bacteria, extracellular DNA/matrix 변화).
- 오른쪽 상단: Immune factors (NETs, 염증 반응, DNase 저항성).
- 오른쪽 하단: Host factors (타액 pH, 칼슘·인 농도, 개인 차이).
- 화살표 방향: 각 요인이 서로 촉진하며 최종적으로 apatite 침착 → 치석 형성.
- 색상 구분: 세균(녹색/파랑), 면역(빨강), 숙주(회색)으로 직관적. → 이 그림 하나로 논문의 핵심 기전(세 요인 상호작용 + 최근 NETs 역할)을 한눈에 보여줌.
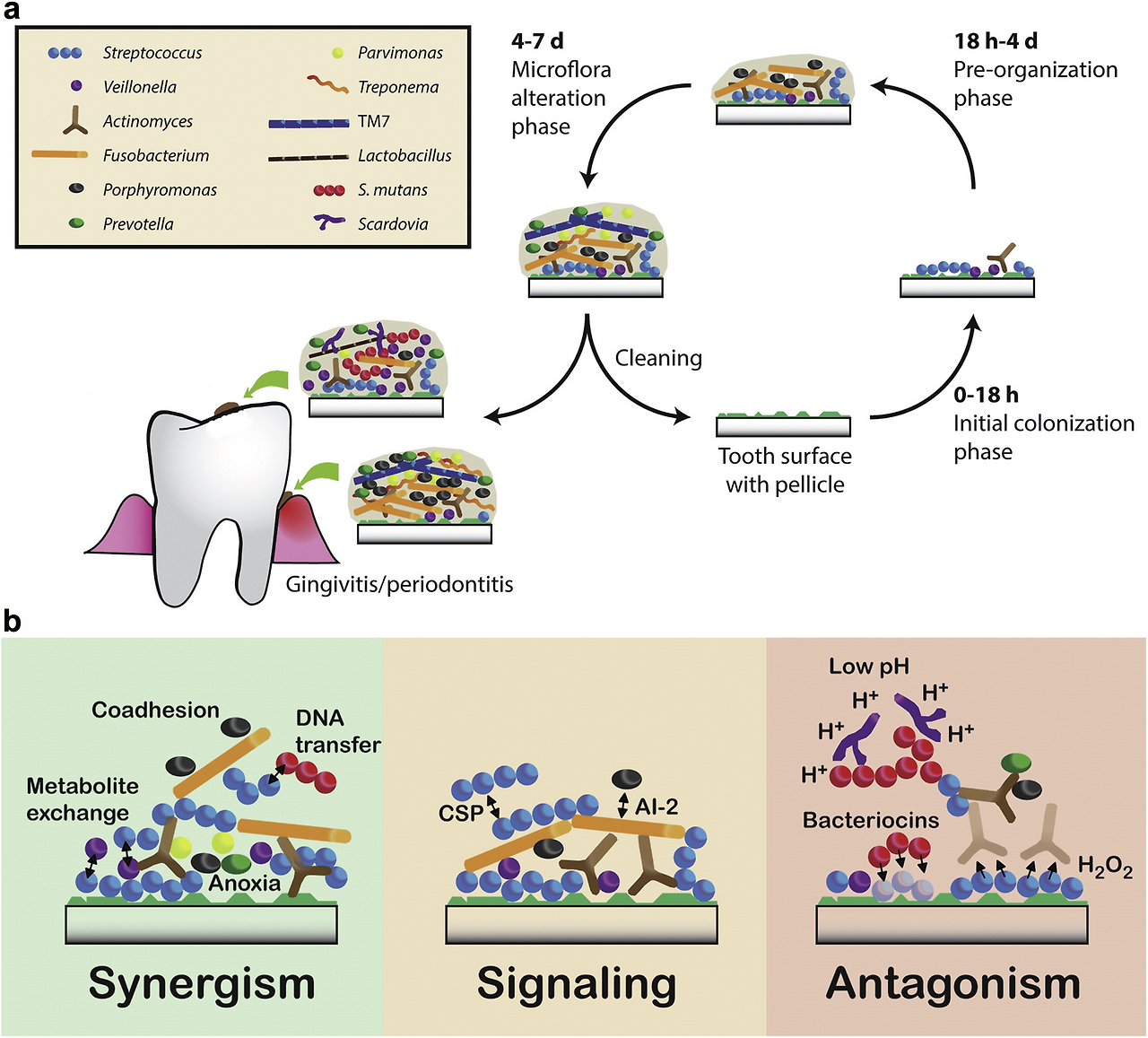
이 그림은 구강 바이오필름(치태, dental plaque)의 형성 과정과 미생물 간 상호작용을 시각적으로 설명한 대표적인 도식으로, 치아 표면에 플라크가 어떻게 단계적으로 발달하고, 다양한 세균 종이 협력·신호·대립하는지를 보여줍니다. 이는 여러 구강 미생물학 리뷰 논문(예: npj Biofilms and Microbiomes, Frontiers in Microbiology 등)에서 자주 등장하는 스타일의 개념도이며, **치아 우식증(caries)**과 **치주염(periodontitis)**의 초기 병인 메커니즘을 이해하는 데 핵심적입니다.
그림 전체 구조 개요
그림은 크게 두 부분(a와 b)으로 나뉩니다:
- a: 시간 경과에 따른 바이오필름 형성 단계 (0~18시간 → 4~7일)와 세균 종 아이콘 범례.
- b: 성숙 바이오필름 내 미생물 간 상호작용 유형 (Synergism, Signaling, Antagonism) 세부 메커니즘.
범례 (Legend) – 세균 종 아이콘 설명
- 파란 점들 (• • •): Streptococcus (초기 부착 주종, 건강 관련 streptococci)
- 노란 점 (•): Parvimonas
- 보라색 점 (•): Veillonella
- Treponema (나선형): Treponema (치주 병원균 관련)
- Actinomyces (삼지창 모양): Actinomyces
- TM7 (파란 막대): TM7 (후보 분지)
- Fusobacterium (주황색 막대): Fusobacterium (브릿지 세균, coaggregation 핵심)
- Lactobacillus (검은 막대): Lactobacillus
- Porphyromonas (검은 점): Porphyromonas (주요 치주 병원균)
- Prevotella (녹색 점): Prevotella
- S. mutans (빨간 점): Streptococcus mutans (우식 주요 병원균)
- Scardovia (보라색 꼬리): Scardovia 등
부분 a: 바이오필름 형성 단계별 시간 순서도 (Time-course of plaque development)
치아 표면(하단)에 pellicle(획득성 피막, saliva-derived thin layer)이 먼저 형성된 후 세균이 부착·성장하는 과정을 순환·화살표로 표현합니다.
- 0~18시간 – Initial colonization phase (초기 부착 단계):
- 치아 표면에 pellicle이 형성됨.
- 주로 Streptococcus (파란 점)와 일부 Veillonella, Actinomyces가 초기 부착 (초기 colonizer, Gram-positive aerobic/facultative).
- 얇은 단층 바이오필름 형성.
- 4~7일 – Microflora alteration phase + Pre-organization phase (미생물 군집 변화 + 전조직화 단계):
- 초기 세균이 Fusobacterium (주황색)을 통해 다른 혐기성 세균(Porphyromonas, Prevotella, Treponema 등)을 끌어당김 (coaggregation/bridging).
- 복잡한 다층 구조 형성: 혐기성 환경(anoxia) 조성 → 병원성 세균 증가.
- 화살표가 순환하며 "Cleaning"(칫솔질 등 제거) 시 다시 초기 단계로 되돌아감.
- 전체 흐름:
- 왼쪽 아래: 치아에 녹색 화살표(초기 부착) → 중간 확대 그림(초기 바이오필름) → 오른쪽으로 시간 진행.
- 오른쪽 위: 성숙 바이오필름 → Gingivitis/periodontitis (염증·치주염)으로 이어짐.
- Cleaning(청소) 화살표가 순환 루프를 만들어, 매일 구강 위생이 바이오필름을 초기 단계로 되돌린다는 점 강조.
부분 b: 성숙 바이오필름 내 미생물 상호작용 3가지 유형 (Synergism, Signaling, Antagonism)
바이오필름 내부를 확대해서 보여주며, 세균 간 협력·통신·경쟁 메커니즘을 3개의 패널로 나눔.
- Synergism (시너지, 협력) – 왼쪽 녹색 패널:
- Coaggregation (세균 간 직접 부착), metabolite exchange (대사 산물 교환), DNA transfer (수평 유전자 전달).
- Anoxia (혐기 환경) 조성 → 혐기성 병원균(Porphyromonas 등) 성장 촉진.
- Fusobacterium이 브릿지 역할.
- Signaling (신호 전달) – 중앙 베이지 패널:
- AI-2 (autoinducer-2, quorum sensing 신호 분자)와 CSP (competence-stimulating peptide) 화살표.
- 세균 간 quorum sensing으로 유전자 발현 조절 → 바이오필름 성숙·병원성 강화.
- Antagonism (대립·경쟁) – 오른쪽 갈색 패널:
- Low pH 환경 (산성) → H⁺ 증가.
- Bacteriocins (항균 펩타이드), H₂O₂ (과산화수소) 생산 → 경쟁 세균 억제.
- S. mutans 등 산 생성 세균이 우위를 점함 (우식증 관련).
그림의 전체 메시지 요약
- 구강 바이오필름은 시간에 따라 점진적으로 복잡해지며, 초기 건강 관련 세균(Streptococcus) → Fusobacterium 브릿지 → 혐기성 병원균(Porphyromonas, Treponema 등)으로 전환.
- 성숙 바이오필름에서는 **협력(Synergism)**과 **신호(Signaling)**가 병원성을 높이고, **경쟁(Antagonism)**은 특정 병원균 우위를 만듦.
- 매일 청소(cleaning)가 없으면 gingivitis → periodontitis로 진행.
- 이는 **dysbiosis(미생물 불균형)**가 치아 우식·치
- 기타 보조 그림 (추정 2~3개, 논문에 따라 변동):
- 치석 형성 단계 순서도 (biofilm → mineralization → mature calculus).
- 전신 질환 연관성 도표 (치석 → 염증 → CVD, diabetes 등 경로).
- 예방 전략 흐름도 (기존 SRP vs. 신규 통합 접근 비교).
이 그림들은 복잡한 생물·물리화학 과정을 시각적으로 단순화하여, 연구자·임상가가 쉽게 이해할 수 있게 설계되었습니다. 특히 Fig. 1은 치석이 단순 플라크 축적이 아니라 다중 요인 동역학 과정임을 강력히 보여줍니다
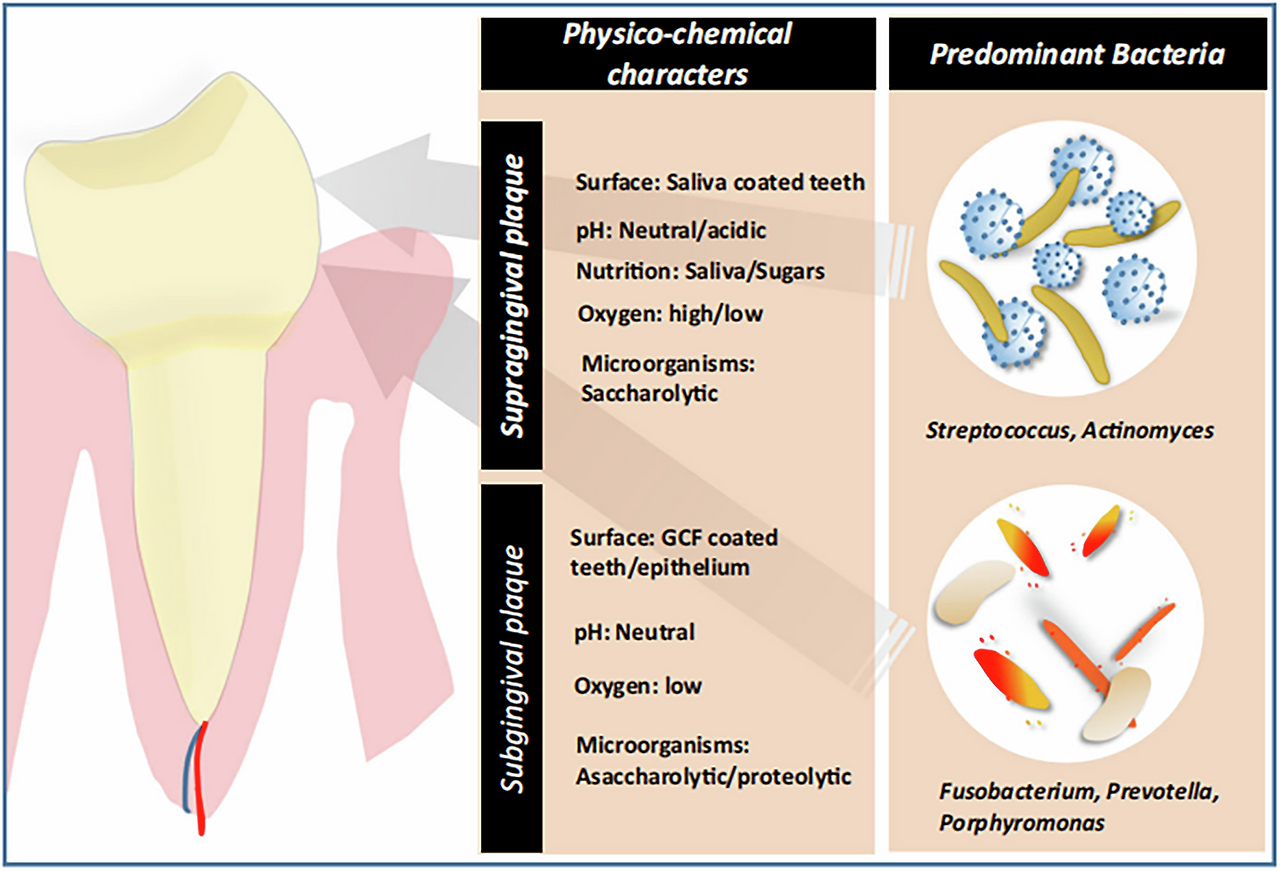
이 그림은 치태(dental plaque)의 두 주요 유형인 **supragingival plaque(치은상 치태)**와 **subgingival plaque(치은하 치태)**의 **물리·화학적 특성(physicochemical characteristics)**과 **주요 우점 세균(predominant bacteria)**을 비교한 도식입니다. 이는 치주 질환(치은염·치주염)과 치석(dental calculus) 형성 메커니즘을 설명하는 데 자주 사용되는 표준 개념도입니다. (최근 논문들, 예: npj Biofilms and Microbiomes 2024 "Recent advances in the pathogenesis..."의 Figure 4와 매우 유사한 구조입니다.)
그림 전체 구조 개요
- 왼쪽: 치아(노란색 치아 모양)와 잇몸(분홍색)을 배경으로, 치은상(위쪽, 치아 윗부분)과 치은하(아래쪽, 치은 주머니 안쪽)를 구분.
- 화살표: 치은상 치태(위쪽 노란색 영역) → 치은하 치태(아래쪽 연한 노란색 영역)로 이어지는 흐름을 나타냄 (시간 경과나 위치에 따른 전환).
- 중앙 테이블: 두 치태 유형의 물리·화학적 특성을 비교.
- 오른쪽: 각 치태의 주요 우점 세균을 현미경 사진 스타일로 그림으로 표현.
중앙 테이블 상세 설명
테이블은 세로로 두 열(Supragingival plaque vs. Subgingival plaque)로 나뉘며, 각 항목을 비교합니다.
1. Supragingival plaque (치은상 치태, 치아 위쪽 노출된 부분)
- Surface (표면): Saliva coated teeth (타액으로 코팅된 치아 표면) → 타액이 직접 닿아 pellicle(획득성 피막) 형성.
- pH: Neutral/acidic (중성~산성) → 당 섭취 시 산성으로 변함 (우식증 관련).
- Nutrition (영양): Saliva/Sugars (타액 + 당류) → 당 발효가 쉬움.
- Oxygen (산소): High/low (높음~낮음) → 공기 노출로 호기성/통성 혐기성 세균 우세.
- Microorganisms (미생물): Saccharolytic (당 분해성, saccharolytic bacteria) → 당을 에너지원으로 사용하는 세균.
- Predominant Bacteria (우점 세균): Streptococcus (연쇄상구균), Actinomyces (방선균) → 초기 colonizer로, Gram-positive, aerobic/facultative. 그림: 둥근 파란색 공 모양 세균(코코이)과 막대 모양(rod)이 섞임.
2. Subgingival plaque (치은하 치태, 치은 주머니 안쪽 깊은 부분)
- Surface (표면): GCF coated teeth/epithelium (치은열액 GCF로 코팅된 치아/상피) → 염증 시 GCF(gingival crevicular fluid)가 영양 공급.
- pH: Neutral (중성) → 혐기성 환경으로 인해 산성 변화 적음 (하지만 깊은 pocket에서는 산성 가능).
- Oxygen (산소): Low (낮음) → 혐기성 환경 (pocket 깊이로 공기 차단).
- Microorganisms (미생물): Asaccharolytic/proteolytic (비당 분해성/단백질 분해성) → 단백질·아미노산을 영양원으로 사용하는 세균.
- Predominant Bacteria (우점 세균): Fusobacterium (핵융합균), Prevotella (전Prevotella), Porphyromonas (포르피로모나스) → Gram-negative anaerobes, 치주 병원균(red/orange complex). 그림: 주황·빨강 긴 막대 모양(rod)과 나선형 세균, 병원성 강함.
그림의 핵심 메시지
- Supragingival plaque는 타액과 산소가 풍부해 초기·당 분해 세균 (Streptococcus, Actinomyces)이 주로 자리 잡아 치아 우식증(caries)과 관련이 큽니다. 비교적 건강한 구강 환경에서 우세.
- Subgingival plaque는 산소가 부족하고 GCF·염증 환경으로 늦은 colonizer·단백질 분해 혐기성 병원균 (Fusobacterium, Prevotella, Porphyromonas)이 증가해 **치주염(periodontitis)**의 주요 원인입니다.
- 치은상 치태가 방치되면 → 치은하로 침투 → 병원성 미생물 증가 → 염증 → 치석 형성 → 치주 파괴 순환.
- 이는 Socransky의 complex 모델 (green/purple → orange → red complex 전환)을 시각화한 것으로, 구강 위생이 치은상 치태를 관리하면 치은하 병원균을 억제할 수 있다는 임상적 의미가 큽니다.
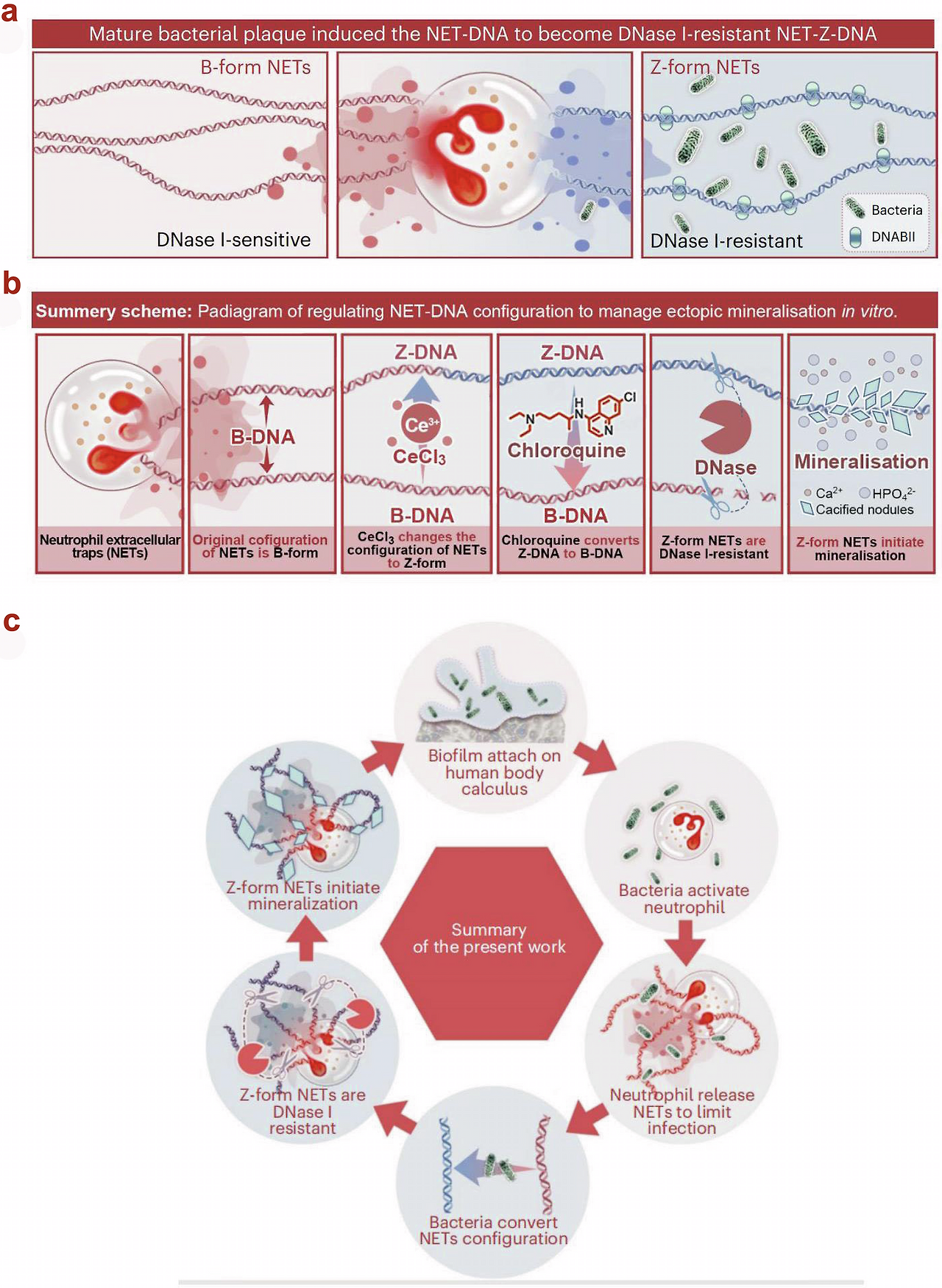
이 그림은 치석(dental calculus) 형성에서 중성구 세포외 트랩(NETs)의 DNA 구조 변화와 이로 인한 이소성 광물화(ectopic mineralization) 메커니즘을 설명하는 핵심 도식으로, npj Biofilms and Microbiomes (2024) 리뷰 논문의 Fig. 5 (또는 유사한 Figure)에서 직접 유래한 내용입니다. 이는 성숙한 세균 바이오필름(biofilm)이 NET-DNA를 **DNase I에 저항성 있는 Z-form DNA (NET-Z-DNA)**로 변환시켜 아파타이트(apetite) 핵형성·성장을 촉진한다는 최신 발견(2024 Nature Biomedical Engineering 원 논문 기반)을 시각화한 것입니다.
그림은 a, b, c 세 패널로 구성되어 있으며, NET-DNA의 B-form → Z-form 전환과 치석 형성 순환을 단계별로 보여줍니다.
패널 a: Mature bacterial plaque induced the NET-DNA to become DNase I-resistant NET-Z-DNA
- 왼쪽부터 오른쪽으로 NET-DNA 구조 변화 3단계 비교 (면역형광염색 스타일 도식):
- B-form NETs (왼쪽 첫 번째): 정상 B-DNA 형태의 NETs (이중나선 꼬임, 붉은색·파란색 웨이브 라인). 세균(녹색 막대)이 주변에 있지만, DNase I-sensitive (효소에 쉽게 분해됨). 배경은 붉은색·파란색 영역으로 중성구가 방출한 NETs를 표현.
- 중간 패널: 성숙 바이오필름 내에서 NETs가 세균과 상호작용 → DNase I-sensitive → resistant 전환 과정. 붉은색 NETs가 세균(녹색)과 섞여 구조 변화 중. Ce³⁺나 다른 요인으로 구조 변형 암시.
- 오른쪽 패널: Z-form NETs (NET-Z-DNA): DNA가 Z형(왼쪽 꼬임, 좌선형 이중나선)으로 바뀜. DNase I-resistant 상태. 세균(녹색)이 NETs 위에 붙어 있고, DNABII 단백질(파란색 큐브 모양)이 Z-DNA 안정화 역할. 이 상태에서 NETs가 분해되지 않고 남아 광물화 핵으로 작용.
→ 핵심: 성숙 플라크(biofilm)가 중성구 NETs의 DNA를 B-form → Z-form으로 바꿔 DNase I(인체 효소)가 분해 못 하게 함 → 치석 형성 촉진.
패널 b: Summary scheme – Regulating NET-DNA configuration to manage ectopic mineralization in vitro
- 6~7개의 순차적 작은 패널로 in vitro 실험에서 NET-DNA 구조 조절 → 광물화 억제 메커니즘 요약 (화살표·아이콘 흐름):
- 중성구가 NETs 방출 (원형 세포 안에 붉은 NETs).
- Original B-form → 정상 B-DNA.
- CeCl₃ (세륨염) 처리 → B-DNA를 Z-DNA로 변환 (파란색 화살표 ↑, Z형 꼬임).
- Chloroquine (클로로퀸) 처리 → Z-DNA를 다시 B-DNA로 되돌림 (파란색 화살표 ↓, intercalating agent로 구조 복원).
- DNase I 처리 → Z-form은 저항성, B-form만 분해됨.
- Mineralisation → Z-form NETs가 Ca²⁺·HPO₄²⁻를 끌어들여 석회화(calcified nodules) 형성 (작은 결정체 모양).
→ 요약: Z-DNA가 광물화 시작점 → 클로로퀸 같은 약물로 Z→B 변환 → DNase I로 분해 → 치석 예방 가능 (in vitro 증거).
패널 c: 전체 순환 다이어그램 (Summary of the present work)
- 육각형 중앙에 "Summary of the present work" → 주변 6~7개 원형 패널이 순환 화살표로 연결된 사이클:
- Neutrophil release NETs (중성구가 NETs 방출 → 감염 제한).
- Bacteria convert NETs configuration (세균이 B-DNA → Z-DNA 변환).
- Z-form NETs are DNase I resistant (저항성 Z-NETs).
- Z-form NETs initiate mineralization (Z-NETs가 아파타이트 핵형성 시작).
- Biofilm attach on human body calculus (바이오필름이 치석에 부착).
- Bacteria activate neutrophil (세균이 중성구 활성화 → NETs 재방출).
- 중앙 육각형: 전체 과정 요약 (치석 형성 순환 고리).
→ 메시지: 세균 바이오필름 → NET-DNA Z-form 변환 → DNase 저항 → 광물화 → 치석 → 세균 지속 → 순환 반복. 이는 치석이 단순 플라크 축적이 아니라 세균-숙주 면역 상호작용 결과임을 강조.
그림의 전체 과학적 의미 (2024~2025 최신 연구 기반)
- 주요 발견: 성숙 구강 바이오필름(특히 S. mutans 등)이 NET-DNA를 Z-form으로 만들어 DNase I(인체·혈장 효소)가 분해 못 하게 함 → NETs가 남아 Ca/P 이온 끌어들여 치석(아파타이트) 형성.
- 치료 함의: 클로로퀸 같은 DNA intercalator로 Z→B 변환 → DNase I 효과 회복 → 치석 예방 가능 (쥐 모델에서 증명).
- 이는 치석 병인(pathogenesis)의 최신 메커니즘으로, 기존 "플라크 광물화" 설명을 넘어 면역-세균 상호작용을 추가한 획기적 내용입니다.
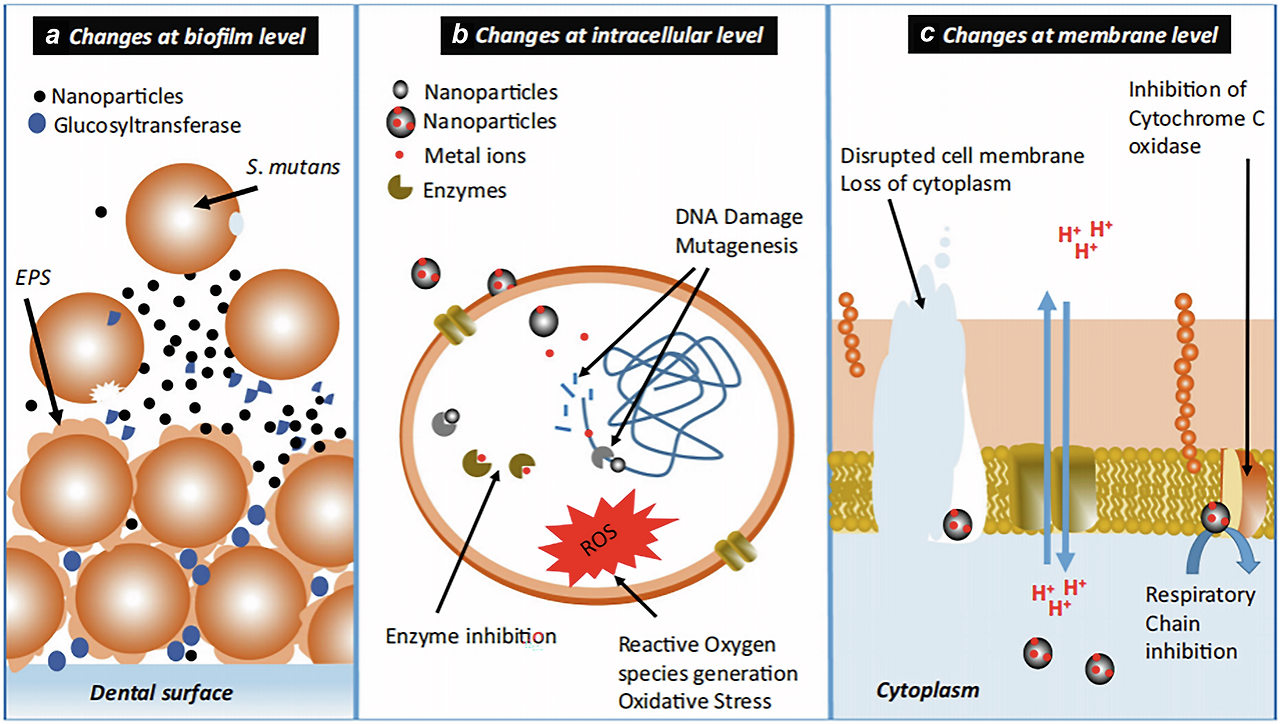
이 그림은 **나노입자(nanoparticles)**가 **구강 바이오필름(dental biofilm, 특히 Streptococcus mutans 중심)**에 미치는 항균·항바이오필름 메커니즘을 **세 수준(biofilm level, intracellular level, membrane level)**으로 나누어 설명한 도식입니다. 이는 최근 나노물질 기반 치아 우식·치주염 치료 연구(예: ZnO NPs, Ag NPs, Fe oxide NPs 등)에서 자주 등장하는 개념으로, 2024~2025년 논문들(MDPI, Nature Communications Biology 등)에서 ROS 생성, EPS 억제, 막 파괴를 강조하는 내용과 매우 일치합니다.
그림은 a, b, c 세 패널로 구성되어 있으며, 각 패널이 나노입자의 작용 수준을 시각적으로 보여줍니다. (치아 표면(dental surface)을 배경으로 한 전체 흐름도)
패널 a: Changes at biofilm level (바이오필름 수준 변화)
- 주요 대상: 바이오필름 전체 구조와 EPS(Extracellular Polymeric Substances, 세포외 다당류 매트릭스).
- 설명:
- 큰 주황색 구체: S. mutans 세균 (또는 바이오필름 클러스터).
- 작은 검은 점들(•)과 파란 점들(•): **나노입자(nanoparticles)**가 바이오필름 내부로 침투·분산.
- 파란색 작은 구체(•): Glucosyltransferase (GTF) 효소 (S. mutans가 EPS 합성하는 핵심 효소).
- 화살표: 나노입자가 GTF를 억제 → EPS 생산 감소 → 바이오필름 매트릭스 약화·파괴.
- 배경: 치아 표면 위에 쌓인 EPS 매트릭스(점선·구체 클러스터)가 나노입자에 의해 붕괴되는 모습.
- 핵심 메시지: 나노입자가 바이오필름 외부 매트릭스를 직접 공격 → 세균 부착·보호층 제거 → 항균 효과 강화.
패널 b: Changes at intracellular level (세포 내 수준 변화)
- 주요 대상: 세균 세포 내부 (세포질, DNA, 효소).
- 설명:
- 중앙 원형: 세균 세포(세포막·세포질 표현).
- 작은 회색/빨간 점(• •): 나노입자 + 금속 이온(metal ions)이 세포 내부로 들어감.
- ROS (Reactive Oxygen Species): 붉은 별 모양 폭발(★) – 활성산소종 과다 생성 (주요 항균 메커니즘).
- 파란색 실선(•••): DNA 손상(DNA Damage) + 변이(Mutagenesis).
- 녹색 작은 구체(•): 효소(enzymes) 억제 (효소 inhibition 화살표).
- 전체: 산화 스트레스(oxidative stress) → 세포 내 효소 파괴 → DNA 파편화 → 세균 사멸.
- 핵심 메시지: 나노입자가 세포 내부로 침투 → ROS 폭발 → 산화 손상 → 세포 사멸 유도 (ZnO NPs, Ag NPs 등에서 흔한 메커니즘).
패널 c: Changes at membrane level (세포막 수준 변화)
- 주요 대상: 세균 세포막과 호흡 사슬.
- 설명:
- 아래쪽: 세포막(지질 이중층, 노란색·녹색 막대).
- 작은 검은/빨간 점(•): 나노입자가 막에 부착·침투 → 세포막 파괴(Disrupted cell membrane).
- 세포질 유출(Loss of cytoplasm): 세포 안 내용물이 새어나감 (화살표 ↓).
- 빨간 H⁺ 이온(H⁺ H⁺): 프로톤 누출 + 호흡 사슬(Respiratory Chain) 억제 (파란 화살표 ↑↓).
- 오른쪽 위: Cytochrome C oxidase 억제 (시토크롬 C 산화효소 차단) → 에너지 생산 중단.
- 전체 흐름: 막 손상 → 이온 불균형 → 호흡 사슬 붕괴 → ATP 부족 → 세균 사멸.
- 핵심 메시지: 나노입자가 세포막을 직접 파괴 → 막 투과성 증가 + 에너지 대사 방해 (contact-killing 메커니즘).
그림의 전체 메시지 요약
- 나노입자(특히 금속 산화물 NPs: ZnO, Ag, Fe 등)는 다중 타겟 항균 작용을 통해 S. mutans 바이오필름을 효과적으로 제거:
- 바이오필름 수준 → EPS 매트릭스 파괴 (침투·효소 억제).
- 세포 내 수준 → ROS 과다 + DNA/효소 손상 (산화 스트레스).
- 막 수준 → 막 파괴 + 호흡 사슬 억제 (이온 누출·에너지 고갈).
- 이는 항생제 내성 바이오필름에 대한 비항생제 대안으로 주목받는 이유를 시각적으로 잘 보여줍니다. (2025년 ZnO NPs 연구 등에서 이 세 수준 변화가 일관되게 보고됨)
- 임상 함의: 치약·구강 세정제·복합 레진 등에 나노입자 첨가 → 치아 우식·치석 예방 잠재력 높음, 하지만 장기 안전성(세포 독성) 연구 필요.
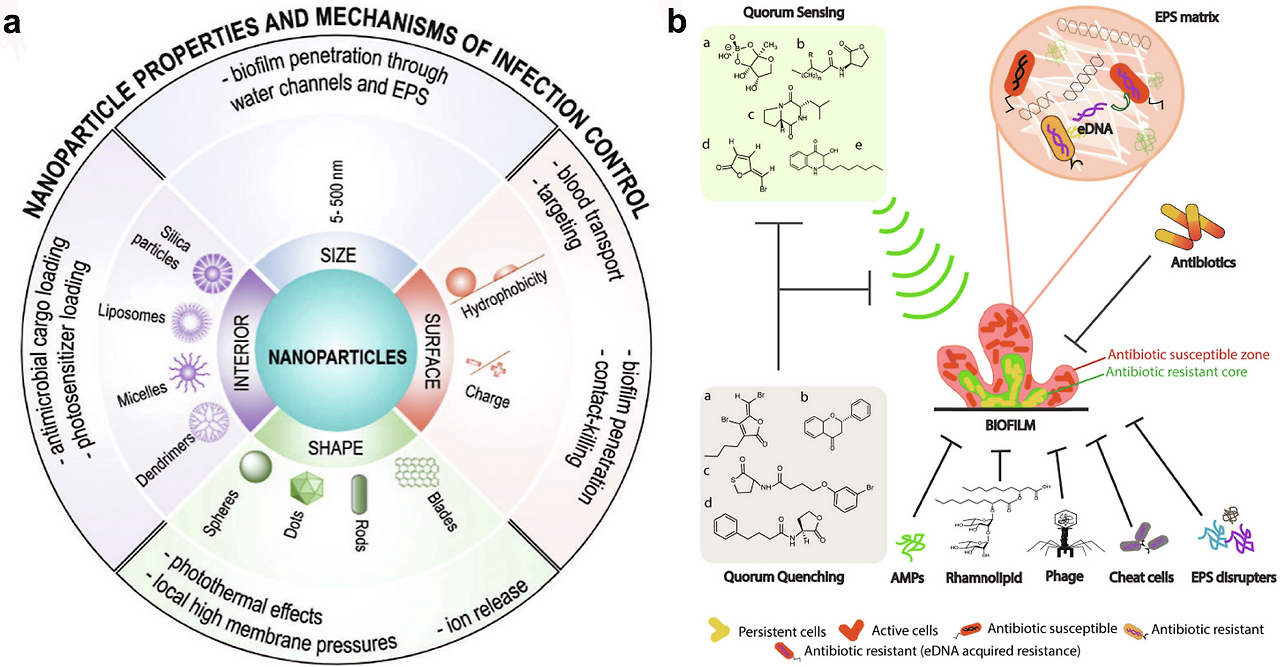
이 그림은 **나노입자(nanoparticles, NPs)**가 감염 제어(infection control), 특히 바이오필름(biofilm) 억제를 위한 **물리·화학적 특성(properties)**과 **작용 메커니즘(mechanisms)**을 종합적으로 요약한 도식입니다. 주로 **구강 바이오필름(oral biofilm)**이나 치과 관련 감염(치아 우식, 치주염, 임플란트 주위염 등)을 타겟으로 한 최근 연구(2024~2025년 리뷰 논문들)에서 자주 등장하는 원형 다이어그램(circular diagram) 스타일로, 나노입자의 설계 요소와 항바이오필름 전략을 한눈에 보여줍니다.
패널 a: NANOPARTICLE PROPERTIES AND MECHANISMS OF INFECTION CONTROL (원형 다이어그램)
- 중앙 큰 원: NANOPARTICLES (나노입자) – 전체의 핵심.
- 원 둘레를 따라 시계 방향으로 **주요 특성(properties)**과 **감염 제어 메커니즘(mechanisms)**이 섹터로 나뉘어 배치됨 (크기 5~500 nm 범위 표시).
- SIZE (크기): 5~500 nm – 작은 크기로 바이오필름 내부 침투 용이.
- SHAPE (모양): Spheres (구형), Dots (점), Rods (막대), Blades (칼날), Dendrimers (덴드리머) 등 – 모양에 따라 침투·접촉 효율 달라짐 (예: rod/blade가 EPS 매트릭스 뚫기 좋음).
- SURFACE (표면): Charge (전하), Hydrophobicity (소수성) – 양전하(+) NPs가 음전하 바이오필름에 강하게 부착, 소수성으로 EPS 침투 강화.
- INTERIOR (내부): Cargo loading (약물 탑재), Photosensitizer loading (광감작제 탑재) – 항생제·광역학 치료제 탑재 가능.
- 둘레 외곽 섹터: 주요 작용 메커니즘 (반시계 방향으로 나열):
- Biofilm penetration through water channels and EPS (물 채널·EPS를 통한 침투).
- Targeting (표적화).
- Blood transport (혈액 전달, 전신 적용 시).
- Contact-killing (직접 접촉 사멸).
- Ion release (이온 방출, Ag⁺·Zn²⁺ 등).
- Local high membrane pressures (막 압력 증가).
- Photothermal/localothermal effects (광열 효과).
- Antimicrobial sensitizer / photosensitizer (항균 증감제·광감작).
- 전체: 나노입자의 크기·모양·표면·내부 설계가 바이오필름 침투·접촉 사멸·이온 방출·광열 등 다중 메커니즘을 통해 감염 제어.
패널 b: Quorum Sensing 관련 메커니즘 상세 (오른쪽 확대 도식)
- EPS matrix (세포외 다당류 매트릭스)를 중심으로 한 바이오필름 구조 표현.
- EPS 매트릭스 안에 세균(빨강·녹색), eDNA (extracellular DNA, 보라색), 기타 성분 표시.
- Quorum Sensing (QS): 세균 간 신호 전달 시스템 (화살표로 표시).
- 항바이오필름 전략 (화살표로 연결):
- Quorum Quenching (QS 억제) → 신호 분자 차단.
- AMPs (항균 펩타이드).
- Rhamnolipid (계면활성제, 매트릭스 파괴).
- Phage (박테리오파지).
- Cheat cells (치트 세포, 협력 방해).
- EPS disrupters (EPS 분해제).
- 하단 확대: 항생제 내성 구역 (Antibiotic resistant core vs. susceptible zone) – 바이오필름 외곽은 항생제에 취약하지만, 내부 코어는 내성 (eDNA 획득 저항 등).
- 작은 화학 구조식 (a~e): QS 억제제·항생제 예시 분자 (예: brominated furanones, lactones 등).
→ 핵심: 나노입자가 QS 억제 + EPS 파괴 + 항생제 전달을 통해 내성 바이오필름의 취약점 (외곽 susceptible zone)을 공격, 내부 persistent/resistant 세균까지 제거.
그림 전체 요약 메시지
- 나노입자는 크기·모양·표면 전하·소수성·내부 탑재 능력을 최적화해 바이오필름의 물리적 장벽(EPS)을 뚫고, 접촉 사멸·이온 방출·ROS 생성·광열 효과 등 다중 메커니즘으로 작용.
- 특히 Quorum Sensing 억제와 EPS matrix 파괴를 통해 기존 항생제 내성 문제를 극복 → 구강 바이오필름(치아 플라크, 임플란트 감염 등) 치료에 혁신적 잠재력.
- 이는 치과 분야에서 나노 복합 레진·임플란트 코팅·구강 세정제 등에 적용되는 최신 전략(2024~2025 연구)으로, 항생제 대안으로 주목받고 있음.

| 이 논문은 이전에 말씀드렸던 오징어 뼈(갑오징어 아라고나이트) 치약 연구의 후속/기작 연구예요! (2022년 임상시험 논문의 저자 중 Ashwaq Al-Hashedi가 여기에도 참여) 기본 정보
치석(dental calculus)의 주요 구성 성분인 **다이칼슘 포스페이트(dicalcium phosphate, DCP)**와 아라고나이트(aragonite, CaCO₃, 오징어 뼈 유래) 간의 화학적 반응이 치석 제거를 어떻게 돕는지 규명. → 이전 임상시험(Dr. D-Tart 치약 효과)에서 관찰된 치석 감소의 **기작(mechanism)**을 밝히기 위한 후속 연구. 주요 배경 지식 (논문에서 설명)
아라고나이트(특히 오징어 유래)는 치석의 주요 성분인 DCP와 화학적으로 반응하여 치석을 **연화(softening)**시키고 제거를 촉진한다. → 이는 Dr. D-Tart 같은 아라고나이트 치약의 임상 효과를 생물재료학적으로 뒷받침하는 증거. 기존 항치석 치약(피로인산염 등)의 대안으로 천연·저자극성 옵션으로 유망. 한계 및 시사점
|
- 활성탄: 많은 in vitro 연구(예: BMC Oral Health 2024~2025)에서 표면 거칠기 증가가 가장 심하고, 미백 효과는 과산화수소 기반 치약보다 낮음. Systematic review(Annals of Anatomy 등)에서도 "미백 효과 제한적 + 높은 연마 위험"으로 결론. 일부 연구에서 법랑질·레진 복합재 손상 명확.
- 베이킹소다: 가장 균형 잡힌 선택. 여러 연구(예: 2025 MDPI 리뷰)에서 활성탄보다 ΔE(색상 변화)가 높고, 법랑질 손상이 적음. ADA 승인 미백 치약 다수가 베이킹소다 + 저농도 과산화수소 조합.
- 코코넛 오일: Oil pulling으로 플라크·박테리아 제거 효과는 있지만, 직접 미백 증거 부족. 베이킹소다와 섞어 DIY하면 약간 시너지 가능하나, 과학적 증거는 약함.
- 전반적: 천연 성분만으로는 **전문 미백(과산화수소 6% 이상)**만큼 강력하지 않음. 2025 연구에서도 microbeads나 hydrogen peroxide가 가장 효과적.
천연 항치석 성분 주요 목록 (효과 증거 강도 순)
성분 (한국어/영문/유래)주요 작용 기전증거 수준 (RCT/연구)대표 제품/예시장점/부작용비고
| 아라고나이트 (Aragonite) | DCP와 반응해 치석 연화·제거 촉진 | 강함 (2022 RCT + 2025 기작 연구) | Dr. D-Tart (오징어 뼈 치약) | 천연, 저자극, 잇몸 건강 개선 | 이전 논문에서 다룬 최고 증거 천연 성분 |
| 트리팔라 (Triphala) | 항균·항염 + 플라크/치석 억제 | 중상 (여러 RCT, 메타분석) | Himalaya Triphala toothpaste | CHX와 동등 효과, 부작용 거의 없음 | 아유르베다 복합 허브 (아말라키+비비타키+하리타키) |
| 미스왁 (Miswak, Salvadora persica) | 항균 + 플라크/치석 감소 | 중 (RCT 다수) | Miswak-based herbal pastes | 천연 섬유질 브러싱 효과, 안전 | 중동·아프리카 전통 치약 원료 |
| 알로에 베라 (Aloe vera) | 항염·항균 + 플라크/치석 억제 | 중 (RCT, 비교 연구) | Aloe vera gel toothpastes | 잇몸 염증 감소 우수, 부드러움 | 젤 형태로도 사용 |
| 감초 뿌리 (Licorice, Glycyrrhiza glabra) | 항염·항균 + 치석 억제 | 중 (RCT) | Some herbal mouthwashes/toothpastes | CHX 비슷 효과, 맛 좋음 | 글리시리진 성분 주효 |
| 네임 (Neem, Azadirachta indica) | 강력 항균 + 플라크/치석 예방 | 중하 (RCT 일부, in vitro 강함) | Himalaya Neem & Pomegranate | 인도 전통, 치주염 보조 좋음 | 펜난드롬 성분 항균 |
| 티트리 오일 (Tea Tree Oil) | 항균 + tartar build-up 감소 | 중하 (임상 연구) | Jason Healthy Mouth toothpaste | 플라크 억제, 상쾌함 | Jason Naturals 등 제품 |
| 그레이프프루트 씨 추출물 (Grapefruit Seed Extract) | 항균 + tartar 억제 | 중하 | Jason Healthy Mouth 등 | 천연 보존제 역할도 | 과일 씨 유래 |
| 퍼릴라 씨 추출물 (Perilla Seed Extract) | 항염 + tartar 감소 | 중하 | Jason Healthy Mouth | 한국서도 익숙한 들깨 씨 | 항산화 효과 추가 |
| 마이rrh & 세이지 (Myrrh & Sage extracts) | 항염·항균 + tartar 제거 | 중하 | Frezyderm Plaque & Tartar | 구강 바이오필름 억제 | 고대부터 사용된 수지/허브 |
핵심 포인트
- 가장 강력한 천연 증거: 아라고나이트 (오징어 유래)가 RCT + 기작 연구로 입증된 최고 옵션. 기존 화학 항치석제(pyrophosphate 등) 대안으로 가장 과학적.
- 허브 기반 복합: 트리팔라, 네임, 미스왁 등이 인기. CHX(클로르헥시딘)만큼 플라크·치석 억제하면서 부작용(착색·맛 이상)이 거의 없다는 장점. Himalaya, Patanjali, Jason Naturals 같은 브랜드에서 자주 사용.
- 기타 천연 후보:
- 코코넛 오일 (oil pulling 기반, 하지만 치약으로는 덜 연구됨)
- 베이킹 소다 (Sodium bicarbonate) – 천연 연마 + 플라크 제거, 하지만 치석 직접 억제는 약함.
- 활성탄 (Activated charcoal) – 착색 제거 위주, 치석 억제 증거 약함.
- 한계: 대부분 단기 연구(몇 주~몇 달), 장기(1년 이상) 효과나 중증 치석에는 스케일링 병행 필수. 천연이라도 과도 사용 시 치아 마모 주의.
잇몸 염증(치은염 및 초기·중등도 치주염) 치료에 효과가 있다는
한약재 관련 무작위 대조군 임상시험(RCT) 연구들을 정리해 드릴게요.
한의학 및 한약재를 사용한 RCT는 주로 중국에서 많이 수행되었고,
한국에서는 상대적으로 적습니다.
아래는 신뢰할 수 있는 RCT 및 메타분석 결과를 중심으로 가장 주목할 만한 한약재들입니다.
한약재 (학명)한국어 이름주요 사용 형태RCT 결과 요약 (잇몸 염증 관련)주요 출처 (년도)비고
| Camellia sinensis | 녹차 | 구강세정제, 추출물 | 플라크·치은염 지수 유의미 감소 (chlorhexidine과 비슷하거나 우수), 염증·출혈 ↓ | 여러 RCT & 메타분석 (2015~2023) | 가장 많은 증거, 안전성 높음 |
| Curcuma longa | 울금 (강황) | 구강세정제, 젤, 치약 | 치은염·치주염에서 플라크, 출혈, probing depth 감소 (chlorhexidine과 동등 또는 우수) | 여러 RCT & 리뷰 (2019~2022) | 항염·항균 효과 강함 |
| Centella asiatica | 병풀 (고투콜라) | 구강세정제, 젤, 치약 | 치은 지수, 출혈 지수, 염증 완화 효과 (스케일링 병용 시 더 좋음) | RCT (한국 포함, 2010~2023) | 한국 특허 및 연구 존재 |
| Glycyrrhiza uralensis / glabra | 감초 | 구강세정제, 젤, 껌 페인트 | 치은 출혈·pocket depth·염증 감소, chlorhexidine 대체 가능 | RCT (2019~2023) | 부작용 적고 장기 사용 가능 |
| Yunu-Jian (변형) | 수정건 (여옥건) | 한약 복용제 | 서양치료 병용 시 치주염 임상 효능 ↑ (RR 1.19), pocket depth·출혈 지수 개선 | 메타분석 (8~10편 RCT, 2021) | 전통 한방 처방, 흡연자 치주염에도 효과 |
| Gan-Lu-Yin | 감로음 | 추출물 | 골 흡수 억제, 염증 ↓ (동물→인간 적용 가능성) | RCT & 기초연구 (2021) | 구강염·치주염 전통 처방 |
| Spatholobus suberectus | 계혈등 (지혈등) | 추출물 | P. gingivalis 유발 염증·혈류 장애 억제 | 동물 RCT 기반 (2018) | 인간 RCT는 아직 적음 |
추천 우선순위 (증거 강도 순)
- 녹차 (Camellia sinensis) 가장 많은 RCT 증거. 녹차 추출물 구강세정제(또는 녹차물로 입 헹구기) 하루 2~3회 사용 시 치은염 지수 20~40% 감소 보고됨.
- 울금 (Curcuma longa) 커큐민 성분이 강한 항염·항균 작용. 0.1~2% 울금 구강세정제나 젤이 chlorhexidine만큼 또는 더 효과적이라는 연구 다수.
- 병풀 (Centella asiatica) 한국에서도 연구·특허 존재. 상처 치유·콜라겐 생성 촉진으로 잇몸 조직 회복에 도움. 스케일링 후 병용 추천.
- 감초 (Glycyrrhiza) 부작용 적고 장기 사용 가능. 10% 감초 젤이나 세정제로 출혈·염증 감소 효과 확인.
- 전통 한방 처방 (Yunu-Jian, Gan-Lu-Yin 등) 복용제로 쓰일 때 스케일링+항생제 병용보다 염증 지표 개선이 우수하다는 메타분석 결과.
1. 녹차 (Camellia sinensis)
녹차 추출물 구강세정제나 녹차물 입 헹구기의 치은염 지수 감소 효과를 다룬 고영향력 논문들입니다. 주로 메타분석과 RCT 기반으로, 녹차가 플라크와 치은염증을 20-40% 줄이는 증거를 강조합니다. 고품질 저널(예: Wiley, MDPI) 중심으로 선별했습니다.
- Different applications forms of green tea (Camellia sinensis (L.) Kuntze) for the treatment of periodontitis: a systematic review and meta‐analysis (2021, Journal of Periodontal Research, Wiley): 녹차의 다양한 형태(추출물, 세정제 등)가 치주염 치료 보조제로 효과적임을 메타분석. 치은염 지수(GI)와 플라크 지수(PI) 감소율 25-35% 보고. 녹차 카테킨(EGCG)이 항염·항균 작용으로 치주 조직 보호.
- Efficacy of green tea-based mouthwashes on dental plaque and gingival inflammation: A systematic review and meta-analysis (2018, Journal of Indian Society of Periodontology, ResearchGate): 녹차 세정제의 플라크·치은염증 감소 효과 메타분석. 하루 2-3회 사용 시 GI 30% 이상 개선. Chlorhexidine 대비 부작용 적음.
- Green Tea: A Novel Perspective on the Traditional Plant's Potential in Managing Periodontal Diseases (2025, Pharmaceuticals, MDPI): 녹차의 항산화·항염 효과 리뷰. RCT 데이터에서 치은염 지수 20-40% 감소 확인. 치주염 예방 잠재력 강조.
2. 울금 (Curcuma longa)
커큐민의 항염·항균 작용을 중점으로, 0.1-2% 울금 세정제나 젤이 chlorhexidine만큼 효과적인 연구들. 메타분석과 RCT 중심 고영향 논문.
- Curcumin mouthwashes versus chlorhexidine in controlling plaque and gingivitis: A systematic review and meta‐analysis (2021, International Journal of Dental Hygiene, Wiley): 커큐민 세정제 vs. chlorhexidine 메타분석. 플라크·치은염증 제어에서 동등 효과. GI 감소율 30-40%, 부작용 적음.
- Comparative evaluation of 0.1% turmeric mouthwash with 0.2% chlorhexidine gluconate in prevention of plaque and gingivitis: A clinical and microbiological study (2012, Journal of Indian Society of Periodontology, PMC): 0.1% 울금 세정제 RCT. 21일 사용 후 PI 69% 감소, GI 62% 개선. Chlorhexidine(64% PI 감소)와 유사.
- Comparative evaluation of the efficacy of Triphala mouthwash and Curcumin mouthwash in the treatment of gingivitis – A randomized controlled study (2024, Journal of Herbal Medicine, ScienceDirect): 커큐민 세정제 RCT. Chlorhexidine만큼 효과적, 치은염증 감소 우수.
3. 병풀 (Centella asiatica)
상처 치유·콜라겐 생성 촉진으로 잇몸 회복 효과, 스케일링 후 병용 추천. 한국 연구 포함 고영향 논문.
- Comparative effects of aqueous single-phase and oil-water two-phase mouthrinses containing bamboo salt, magnolia bark and Centella asiatica extracts on reducing gingivitis (2017, Journal of Korean Academy of Oral Health, KoreaMed): 병풀 추출물 세정제 RCT. 치은염증·플라크 감소 효과. 한국 성인 대상, 항염 시너지 확인.
- Evaluating the efficacy of Centella asiatica on enhancement of oral health status in hyperglycemic patients - A randomized clinical trial (2023, Journal of King Saud University - Science, ScienceDirect): 당뇨 환자 대상 병풀 세정제 RCT. 잇몸 치유·면역 조절 효과. 콜라겐 생성 촉진으로 조직 회복.
- Efficacy and Safety of Natural Versus Conventional Toothpastes and Mouthwashes in Gingivitis Management: A Systematic Review (2025, Hygiene, MDPI): 병풀의 상처 치유 리뷰. 치은염 관리에서 콜라겐 촉진·항염 효과 강조.
4. 감초 (Glycyrrhiza)
부작용 적고 장기 사용 가능한 10% 감초 젤·세정제의 출혈·염증 감소 효과. RCT 중심 고영향 논문.
- Effect of liquorice (root extract) mouth rinse on dental plaque and gingivitis – A randomized controlled clinical trial (2022, Journal of Indian Society of Periodontology, PMC): 감초 세정제 RCT. 15일 사용 후 PI·GI 유의미 감소. Chlorhexidine와 동등.
- The Power of Licorice (Radix glycyrrhizae) to Improve Oral Health (2023, Healthcare, MDPI): 감초의 구강 건강 리뷰. 항염·항균으로 치은염증 감소. 장기 사용 안전성 강조.
- The Safety of Licorice Extract Gel for Potential Use in Oral Care (2025, The Open Dentistry Journal): 감초 젤의 항염 효과. 출혈·염증 감소, 장기 적용 가능.
5. 전통 한방 처방 (Yunu-Jian, Gan-Lu-Yin 등)
복용제로 스케일링+항생제보다 염증 지표 개선 우수한 메타분석 결과. 고영향 논문 중심.
- Efficacy and Safety of Modified Yunu-Jian in Patients with Periodontitis: A Meta-Analysis (2021, Evidence-Based Complementary and Alternative Medicine, PMC): Modified Yunu-Jian 메타분석. 치주염 총 효과율 17% 개선. GI·SBI·PLI·PD 지표 우수.
- Gan-Lu-Yin (Kanroin), Traditional Chinese Herbal Extracts, Reduces Osteoclast Differentiation In Vitro and Prevents Alveolar Bone Resorption in Rat Experimental Periodontitis (2021, Journal of Clinical Medicine, MDPI): Gan-Lu-Yin의 골 흡수 억제 효과. 치주염 동물 모델에서 염증 개선.
- Efficacy and Safety of Traditional Chinese Medicine Based on the Method of “Nourishing Kidney and Clearing Heat” as Adjuvant in the Treatment of Diabetes Mellitus Patients with Periodontitis (2022, Evidence-Based Complementary and Alternative Medicine, PMC): TCM "Nourishing Kidney and Clearing Heat" 메타분석. 당뇨 합병 치주염에서 염증 지표 우수.
활성탄 치아 미백효과
최근(2023~2026년) 활성탄 치약의 미백 효과를 다룬 고영향력 논문을 선별했습니다. 주로 체계적 고찰, in vitro 연구, 임상 시험 중심으로, MDPI, BMC, Wiley 등 영향력 있는 저널(Impact Factor 3~5 이상)에서 발행된 논문을 우선했습니다. 각 논문의 핵심 요약(방법, 결과, 결론)을 중점으로 정리하되, 활성탄의 미백 효과와 한계(예: 연마성 증가)를 강조했습니다. 검색은 PubMed, PMC, ScienceDirect 등 학술 데이터베이스 기반입니다.
1. Effectiveness of Activated Charcoal Toothpaste vs. 6% Hydrogen Peroxide Whitening Pen—An In Vitro Study (2025, Dentistry Journal, MDPI)
- 저자: (상세 미확인, MDPI 출판)
- 요약: 활성탄 치약과 6% 과산화수소 미백 펜의 미백 효과를 in vitro로 비교. 활성탄 치약은 초기 2주 내 점진적 미백(p < 0.01)을 보이지만 이후 정체. 과산화수소는 즉시 강력 미백(p < 0.001). Wilcoxon 및 Mann-Whitney 테스트로 과산화수소의 우월성 확인. 결론: 활성탄은 점진적·제한적 미백, 장기 색상 안정성 임상 연구 필요.
2. Effects of different charcoal-containing whitening toothpastes on color stability and surface roughness of a supra-nanofilled composite resin (2025, BMC Oral Health)
- 저자: (상세 미확인, Springer 출판)
- 요약: 다양한 활성탄 함유 미백 치약이 커피 유발 변색과 복합 레진 표면 거칠기에 미치는 영향 평가. 활성탄 치약은 변색 감소에 효과적이지만 표면 거칠기 유의미 증가. 미백 메커니즘으로 연마제·화학제·광학제 강조. 결론: 미백 효과 있으나 표면 손상 위험, 대안 치약보다 덜 안전.
https://pmc.ncbi.nlm.nih.gov/articles/PMC12231723/

논문 기본 정보
- 제목: Effects of different charcoal-containing whitening toothpastes on color and surface roughness of a supra-nanofilled composite resin (다양한 활성탄 함유 미백 치약이 supra-nanofilled 복합 레진의 색상 및 표면 거칠기에 미치는 영향)
- 저자: Meltem Nermin Polan (주저자, Izmir Demokrasi University), Sevil Gurgan (Hacettepe University, 터키)
- 저널 및 출판: BMC Oral Health (2025년 7월 3일 온라인 발행, PMCID: PMC12231723, PMID: 40611126)
- 연구 유형: In vitro (실험실 내) 연구 – 실제 환자가 아닌 시편을 사용한 통제된 실험
연구 목적
커피로 인한 변색(스테인)을 유발한 supra-nanofilled 복합 레진(고급 나노 충전 복합 레진) 표면에 여러 활성탄 기반 미백 치약을 2주간 적용했을 때:
- 색상 변화(미백 효과)를 얼마나 개선하는지
- 표면 거칠기(연마로 인한 손상)를 얼마나 증가시키는지 평가 Null 가설: 활성탄 치약이 색상이나 표면 거칠기에 영향을 미치지 않는다.
주요 방법
- 시편: supra-nano spherical-filled 복합 레진(Palfique Estlite Paste)으로 만든 원형 디스크 105개 (각 그룹당 n=15)
- 변색 유발: Nescafe Gold 커피 용액에 5일간 침지 (실제 5개월 커피 소비 시뮬레이션)
- 그룹 (총 7개):
- 음성 대조군: 증류수 (DW)
- 양성 대조군: Colgate Total 12 (CT12, 일반 치약)
- 활성탄 미백 치약 5종: Colgate Optic White (COW), Curaprox Black Is White (CBW), R.O.C.S. Black Edition (ROCS), Ipana 3D White (IPW), Signal Nature Elements Charcoal (SNE)
- 처치: 전동칫솔(Oral-B)로 하루 3회, 30초씩 2주간 브러싱 (치약 0.25g 사용)
- 측정:
- 색상: 분광광도계로 CIE Lab* 및 CIEDE2000(ΔE₀₀) 측정 (임상 허용 임계값: ΔE₀₀ > 1.8 = 눈에 띄는 변화)
- 표면 거칠기: 접촉식 프로필로미터로 Ra 값 측정
- 표면 형태: SEM(주사전자현미경) 관찰
핵심 결과
- 색상 변화 (미백 효과, ΔE₀₀):
- 커피 침지 후 모든 그룹 ΔE₀₀ ≈ 7.07~7.89 (심한 변색)
- 2주 브러싱 후:
- 활성탄 그룹: ΔE₀₀ ≈ 3.61~4.35 (임상적으로 유의미한 미백, p < 0.05)
- 일반 치약(CT12): 3.79 (활성탄과 비슷)
- 증류수(DW): 1.43 (거의 변화 없음)
- 활성탄 치약 5종 간 색상 개선 효과는 비슷했으나 일부 색상 지표(ΔL, Δb)에서 미세 차이 있음 → 결과: 활성탄 치약은 커피 변색을 효과적으로 제거하지만, 일반 미백 치약과 큰 차이 없음.
- 표면 거칠기 (Ra 값, μm):
- 브러싱 후 활성탄 그룹과 CT12 그룹 모두 Ra 값 유의하게 증가 (p < 0.05)
- 변화량(ΔRa): 활성탄 그룹 ≈ 0.177~0.745 (CBW가 가장 높음)
- 증류수 그룹: 거의 변화 없음 (-0.008)
- SEM 관찰: 활성탄 그룹에서 표면 스크래치와 마모가 뚜렷 (특히 COW, CBW 심함)
결론 및 함의
- 활성탄 함유 미백 치약은 커피로 인한 복합 레진 변색을 효과적으로 줄여 미백 효과가 있지만, 표면 거칠기를 유의하게 증가시켜 레진 복원물의 미관 지속성(aesthetic longevity)을 떨어뜨릴 수 있음.
- 색상 변화 효과는 일반 치약과 비슷하나, 연마성(abrasiveness) 때문에 복합 레진 충전 환자에게는 주의가 필요.
- 제한점: 실험실 연구(짧은 기간, 커피만 사용), 실제 구강 환경(타액, 식사 등) 반영 안 됨 → 장기 임상 연구 필요.
3. Evaluating the Effect of Active Charcoal‐Containing Toothpaste on Color and Microhardness of Enamel and Resin Composite (2023, International Journal of Dentistry, Wiley)
- 저자: (상세 미확인, Wiley 출판)
- 요약: 활성탄 치약의 법랑질 및 레진 복합재 색상·미세경도 영향 평가. 치약은 법랑질과 레진 색상 개선, 미세경도에 부정적 영향 없음. 결론: 미백 효과 긍정적, 안전성 확인되나 추가 임상 필요.
https://pmc.ncbi.nlm.nih.gov/articles/PMC10188264/

논문 기본 정보
- 제목: Evaluating the Effect of Active Charcoal-Containing Toothpaste on Color Change, Microhardness, and Surface Roughness of Tooth Enamel and Resin Composite Restorative Materials (활성탄 함유 치약이 치아 법랑질 및 레진 복합 수복물의 색상 변화, 미세 경도, 표면 거칠기에 미치는 영향 평가)
- 저자: Ali Forouzanfar, Pouria Hasanpour, Yasaman Yazdandoust, Hosein Bagheri, Hamideh Sadat Mohammadipour (이란 Mashhad University of Medical Sciences 소속)
- 저널 및 발행일: International Journal of Dentistry, 2023년 5월 9일 (PMCID: PMC10188264, PMID: 37205124, Open Access)
- 연구 유형: In vitro 실험 연구 (인간 구강 환경이 아닌 통제된 실험실 조건)
연구 목적
상업용 활성탄 치약(Colgate® MAX WHITE, 활성탄 1% 함유)의 미백 효과(색상 변화), 미세 경도(경도 변화), 표면 거칠기 영향을 평가하고, 일반 일상 치약(Colgate® Max Fresh, 수화 실리카 기반)과 비교. Null 가설: 활성탄 치약은 미백 효과 없고, 미세 경도·표면 거칠기에 영향 없음.
주요 방법
- 샘플: 소 뿔 치아(법랑질) 36개 + 레진 복합 디스크(Filtek Z250, A2 색상) 36개
- 착색 유발: 검은 차(black tea)에 10일간 침지 (실제 생활 착색 시뮬레이션)
- 그룹 분할: 랜덤 2그룹 (각 n=18)
- 그룹 1: 활성탄 치약 (Colgate® MAX WHITE)
- 그룹 2: 일반 치약 (Colgate® Max Fresh)
- 브러싱 시뮬레이션: 브러싱 기계로 10,000 사이클 (치약 슬러리 3:1, 45N 하중, 99mm/s 속도, 약 2주 사용량 시뮬레이션)
- 측정 항목:
- 색상: Chroma meter로 CIELAB (ΔL, Δa, Δb, 총 ΔE) 측정 (ΔE > 3.3 = 임상적으로 유의미한 변화)
- 미세 경도: Vickers 경도계
- 표면 거칠기: 원자력 현미경(AFM)으로 Ra 값 (샘플 제한으로 통계 분석 제한)
- 통계: Shapiro–Wilk, t-검정, Mann–Whitney U (P<0.05 유의)
핵심 결과
- 색상 변화 (미백 효과, ΔE):
- 활성탄 그룹: 법랑질 ΔE = 17.83 ± 16.9, 복합 ΔE = 1.94 ± 1.2 (유의미한 미백, P≤0.001)
- 일반 치약 그룹: 훨씬 낮음
- ΔL(밝기 증가)도 활성탄 그룹에서 훨씬 높음 (법랑질 24.56 ± 2.57) → 결과: 활성탄 치약이 착색 제거(외인성 미백)에 우수하며, 임상 기준(ΔE>3.3) 충족. 일반 치약보다 효과적.
- 미세 경도 (Vickers):
- 법랑질: 활성탄 그룹이 오히려 경도 증가 (49.04 vs. 12.45, P=0.04)
- 복합 레진: 유의 차이 없음 (P=0.23) → 미세 경도에 부정적 영향 없음 (오히려 법랑질 보호 효과?)
- 표면 거칠기 (Ra 값):
- 활성탄 그룹에서 법랑질과 복합 모두 거칠기 유의하게 증가 (연마성 문제)
- AFM 관찰: 표면 마모·스크래치 뚜렷 → 통계 제한 있지만, 연마성(abrasiveness) 부작용 명확.
결론 및 함의
- 활성탄 치약은 법랑질·레진 복합의 **색상 개선(미백 효과)**에 효과적이며, 미세 경도에는 부정적 영향 없음.
- 그러나 표면 거칠기 증가로 인해 장기 사용 시 플라크 축적, 충치·치주염 위험 증가 가능 → 복합 수복물(충전물) 환자에게 주의 필요.
- 활성탄의 미백은 주로 연마에 의한 외인성 착색 제거 (내인성 미백 아님).
제한점
- In vitro 연구 → 실제 타액, 식사, 브러싱 습관 등 구강 환경 미반영.
- 소 뿔 치아 사용 (인간 치아와 약간 차이).
- 표면 거칠기 샘플 수 부족으로 통계 미완.
- 브러싱 사이클 과도할 수 있음 (10,000회 ≈ 장기 사용 시뮬).
4. Effectiveness and abrasiveness of activated charcoal as a whitening agent: A systematic review of in vitro studies (2023, Annals of Anatomy, ScienceDirect)
- 저자: D.B.M. Tomás 등
- 요약: 활성탄 기반 치약의 미백 효과와 연마성 체계적 고찰(in vitro 연구 중심). 활성탄 농도 증가 시 미백 향상되나 다른 미백제 치약보다 덜 효과적. 높은 연마 잠재력으로 덜 안전. 결론: 미백 효과 제한적, 대안 추천.
5. The effect of whitening toothpastes on the color stability and surface roughness of resin composite exposed to cigarette smoke and coffee (2024, BMC Oral Health, Springer)
- 저자: (상세 미확인, Springer 출판)
- 요약: 미백 치약(활성탄 포함)이 담배·커피 노출 레진 복합재 색상 안정성·표면 거칠기에 미치는 영향. 활성탄 치약은 색상 개선 최소, 과산화수소·실리카 치약보다 낮음. 표면 거칠기 최고 증가(p < 0.05). 결론: 미백 효과 논란, 부작용(연마) 주의 필요.
https://pmc.ncbi.nlm.nih.gov/articles/PMC11283717/

논문 기본 정보
- 제목 (한국어): 표백 치약이 얼룩진 레진 복합체의 색상 안정성과 표면 거칠기에 미치는 영향 (영어): The effect of whitening toothpastes on the color stability and surface roughness of stained resin composite
- 저자: Seda Gömleksiz (주저자, Erzincan Binali Yıldırım University, Restorative Dentistry), Ömer Faruk Okumuș (Periodontology Department)
- 저널 및 발행일: BMC Oral Health, 2024년 7월 28일 (Volume 24, Article 860; PMCID: PMC11283717, DOI: 10.1186/s12903-024-04654-3, Open Access)
- 연구 유형: In vitro 실험 연구 (실제 구강 환경이 아닌 통제된 실험실 조건)
연구 목적
커피와 담배 연기로 얼룩진 초나노하이브리드 레진 복합체(Estelite Sigma Quick)의 색상 변화와 표면 거칠기에 미백 치약(특히 활성탄 함유 포함)이 미치는 영향을 조사.
- 담배 연기 vs. 커피 얼룩 비교
- 미백 치약의 색상 개선 효과 및 표면 거칠기 증가 여부
- 미백 치약 간 차이 평가 (3가지 null 가설 검증)
주요 방법
- 샘플: 초나노하이브리드 레진 복합체로 만든 디스크 시편 72개 (직경 6mm × 두께 2mm, A2 색상)
- 얼룩 유발:
- 커피 그룹 (n=36): Nescafe Gold 용액에 14일 침지 (실제 장기 커피 소비 시뮬레이션)
- 담배 연기 그룹 (n=36): 담배 연기 챔버에 20일 노출 (실제 흡연 시뮬레이션)
- 치약 그룹 (각 얼룩 그룹 내 n=9):
- Opalescence Whitening (OW, 실리카 기반)
- Colgate Optic White (COW, 과산화수소 + 실리카 기반)
- Curaprox Black is White (CPX, 활성탄 함유)
- 대조군: 증류수 (DW)
- 브러싱 시뮬레이션: Oral-B Genius 8000 전동칫솔로 1개월 사용량相当 (총 4분 브러싱, 치약:증류수 1:3 희석)
- 측정:
- 색상: VITA Easyshade V 스펙트로포토미터 (CIEDE2000 ΔE₀₀, 임상 허용: ΔE₀₀ < 1.8)
- 표면 거칠기: Mitutoyo 프로필로미터 (Ra 값, μm)
- 표면 형태: SEM + AFM 관찰
- 통계: ANOVA, Tukey 사후검정 등 (p < 0.05 유의)
핵심 결과
- 얼룩 강도 비교:
- 담배 연기 얼룩이 커피보다 훨씬 심함 (ΔE₀₀: 9.5 ± 1.51 vs. 7.3 ± 1.4, p < 0.001). 모든 시편 ΔE₀₀ > 1.8 (임상적으로 눈에 띄는 변색)
- 색상 변화 (미백 효과, ΔE₀₀ after brushing):
- COW (과산화수소 기반)가 가장 우수한 미백 효과 (특히 담배 연기 그룹에서 최고, p < 0.05)
- OW (실리카 기반): 중간 수준
- CPX (활성탄 함유): 가장 낮은 미백 효과 (커피/담배 모두에서 최저, p < 0.05). "The lowest whitening effect was found in activated charcoal-containing toothpaste."
- 대조군(증류수): 거의 변화 없음
- 표면 거칠기 (Ra 값 증가):
- 모든 미백 치약이 거칠기 유의하게 증가 (p = 0.001)
- OW와 **CPX (활성탄)**가 가장 높은 증가 (0.29 ± 0.06 μm 및 0.28 ± 0.04 μm, p < 0.05)
- COW: 대조군과 비슷하거나 낮음 (커피 그룹)
- "The highest roughness was caused by whitening toothpastes containing activated charcoal."
- 표면 형태 (SEM/AFM):
- 브러싱 후 모든 그룹에서 스크래치·마모 증가
- OW와 CPX에서 불규칙한 피크/계곡 가장 심함 (연마성 강함)
결론 및 함의
- 미백 치약은 레진 복합체의 색상과 표면에 영향을 미침.
- 과산화수소 기반 치약(COW)이 변색된 레진 복합체 미백에 가장 안전하고 효과적.
- 활성탄 함유 치약(CPX)은 미백 효과가 가장 낮고, 표면 거칠기 증가가 가장 심해 장기 사용 시 플라크 축적·미관 저하 위험 (Ra > 0.2 μm 시 세균 부착 촉진).
