포틀랜드 시멘트의 주요 화합물은, ① 알라이트(3CaO·SiO2), ② 벨라이트 (2CaO·SiO2)로 불리우는 규산 칼슘 화합물, ③ 알루네이트 상 (3CaO·A12O3) ④ 페라이트 상 (4CaO·A12O3·Fe2O3)으로 불리우는 간극질, ⑤ 또 석고 (CaSO4·2H2O) 이다. 또 시멘트의 수화물 생성물을 대별하면, 알라이트, 벨라이트로 부터 생성하는 ① 규산 칼슘 수화물(C-S-H), ② 수산화 칼슘, 간극상 물질과 석고에서 생성하는 ③ 에트린자이트, ④ 모노 설페이트 수화물로 나뉜다. 그것들의 반응식을 나타내면,
(규산칼슘 화합물의 수화)
3CaO·SiO2 + (3 -m+n) H2O → mCaO·SiO2·nH2O+(3-m)Ca(OH)2
2CaO·SiO2 + (2- m+n)H2O → mCaO·SiO2·nH2O+(2- m)Ca(OH)2
(2CaO·SiO2로부터 생성한 규산 칼슘 수화물의 화학 조성은, 3CaO·SiO2로부터 생성한 것과 매우 같다고 생각해도 좋다.)
m, n의 값은 약간 변동이 있지만, m은 대체로 1.6∼1.7이다. 그것에 대해, n은 대체로 2.0∼2.6으로 CaO의 m에 비교해 변동이 크다. 이것은 다음에 말하는 결합수를 측정하는 건조 조건의 차이나 측정 방법의 차이에 의한 것이라고 생각된다. 또 재령에 의해서도 조성이 변화한다고 한다.
<간극상 물질의 수화>
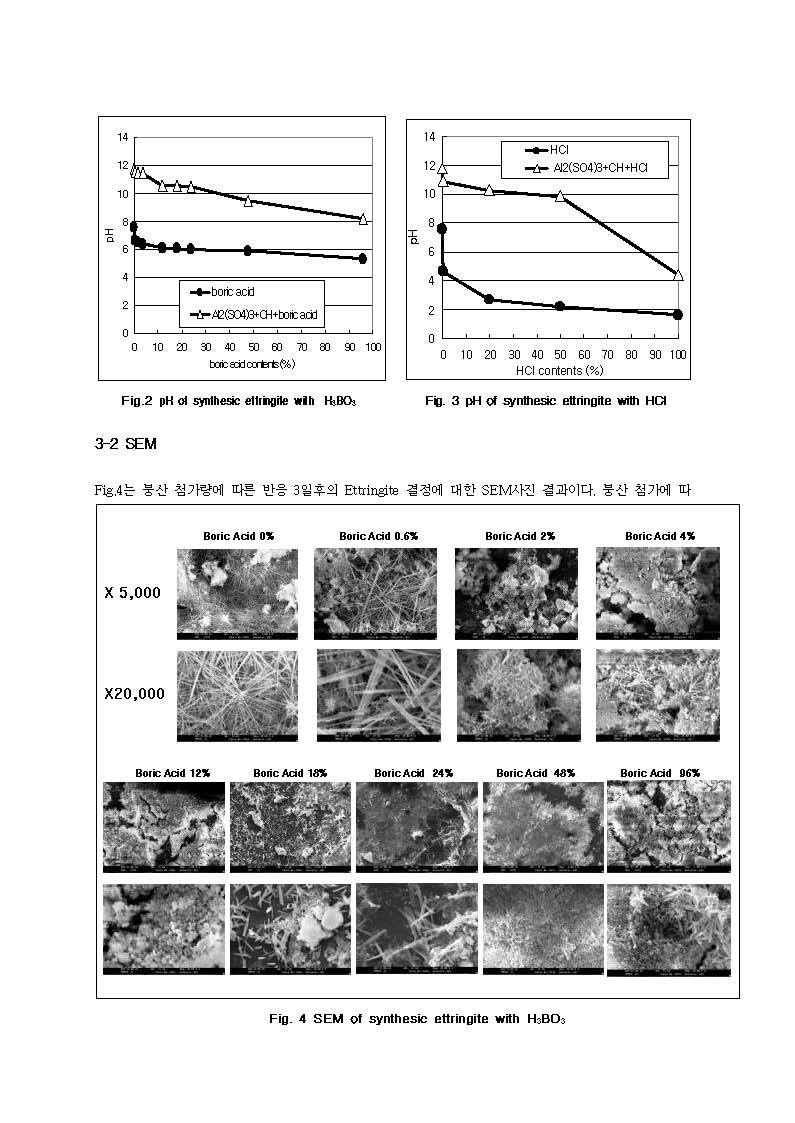
3CaO·A12O3 + 3(CaSO4·2H2O) + 26∼28H2O → 3CaO·Al2O3·3CaSO4·30∼32H2O(에트린자이트)
2(3CaO·A12O3) + 3CaO·A12O3·3CaSO4·30∼32H2O + ℓ H2O → 3(3CaO·A12O3·CaSO4·11∼12H2O)(모노 설페이트 수화물)
ferrite상의 수화는 3CaO·A12O3과 같은 반응을 하여 수화물은 Fe2O3가 일부 고용하여, A12O3을 (A12O3)x(Fe2O3)1- x으로 치환된 형태로 표현할 수 있다.
==============
위 내용이 어렵게 설명해 놓은것 같지만,
시멘트의 주요성분인 "규산화 칼슘"이 물과 반응... 즉 수화반응(경화작용)으로
고형물인 "규산화칼슘-수화물"과 알카리성을 띠는 "수산화칼슘"으로 변하는 겁니다.
물의 성분인 H, O와의 반응으로 생성되는 것으로 다른 물질인 기름은 물보다 반응성이 떨어지던가, 반응자체가 안일어 나겠죠..
또, 화학식을 보더라도 물이 무한정 필요한게 아니라 적당량이 필요해야 한다는 것을 아실수 있으실 겁니다..
최고의 강도발현을 위해서는 자유수가 없는 반응수만을 넣어야 하지만, 너무 된 반죽이 되어서 작업성이 떨어지죠.. 이걸 워커빌리티가 떨어진다고 합니다.
보통은 약간의 작업성을 위해서 반응수보다 자유수를 좀더 첨가하거나 AE제(연행공기)같은 혼화제(배합설계시 고려안함)을 넣어서 작업성을 확보합니다.
|
| ||
|
![]() Ettringite의 생성에 미치는 pH의 영향.pdf
Ettringite의 생성에 미치는 pH의 영향.pdf