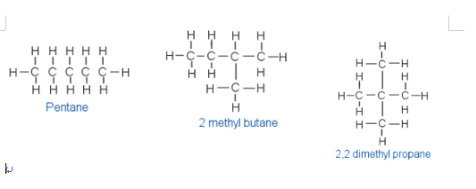
화학식 C5H12. 알칸에 속하는 탄소 5개인 탄화수소의 총칭. 3종의 이성질체가 알려져 있는데, 보통 노르말 사슬모양의 펜탄, 즉 n-펜탄을 가리킨다. n-펜탄은 석유 에테르의 주성분이며, 분자량 72.1, 녹는점 -129.1℃, 끓는점 36.07℃, 비중 0.62624(측정온도 20℃), 용해도 0.36g/dm![]() (물 16℃), 인화점 -40℃ 이하이다. 가연성의 액체로 폭발한계는 1.4~8.0%(공기 속)이며, 자동발화점은 309℃이다. 알코올·에테르에도 녹으며, 추출용제·마취제 등으로 쓰인다.
(물 16℃), 인화점 -40℃ 이하이다. 가연성의 액체로 폭발한계는 1.4~8.0%(공기 속)이며, 자동발화점은 309℃이다. 알코올·에테르에도 녹으며, 추출용제·마취제 등으로 쓰인다.
이소펜탄은 녹는점-159.900℃ , 끓는점 27.852℃ 이며 , 네오펜탄은 녹는점 -16.55℃ , 끓는점 9.503℃ 이다.
구조이성질체의 끓는점의 차이는 분산력의 차이에 있다.
분산력은 유발 쌍극자-유발 쌍극자 사이의 인력이다. 영구 쌍극자가 있는 분자를 포함한 모든 분자에서 순간적인 전자의 분포는 항상 변화하므로 모든 분자와 분자사이에는 분산력이 존재한다.분자의 부피가 클수록 전자 분포의 비대칭성이 커질 수 있으므로 분산력도 크게 된다. 따라서 전자의 수가 많은 분자일수록 편극이 잘 일어나므로 분산력이 증가하며, 분자량이 클수록 전자수가 많기 때문에 분산력이 크다.분자량이 같은 경우에는 분자의 모양에 따라 다르며, 분자의 부피가 클수록 분산력이 크다.
다음검색