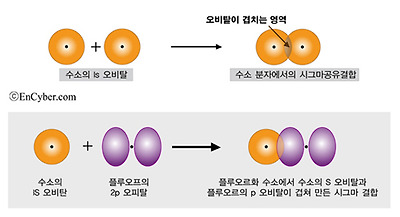
화학 결합은 결합에 참여하는 원자의 오비탈이 겹쳐져 형성된다. 예를 들면, 수소 분자는 두 수소 원자의 1s 오비탈이 겹쳐져 형성되고,
플루오린화수소에서는 수소 원자의 1s 오비탈과
플루오린의 2p 오비탈이 겹쳐져 형성된다.
이 두 물질에서 결합을 이루고 있는 전자는, 결합을 이루고 있는 두 원자의 핵을 잇는 축(결합축)을 중심으로 그 둘레에 위치하고 있어 전자의 분포가 원통형 대칭이 된다. 이와 같은 결합을
시그마 결합이라고 한다.
시그마 결합과 다른 특성을 보이는 결합으로
파이 결합이 있다. p
y 오비탈과 p
y 오비탈이 겹쳐 결합을 이루는 경우
전자 구름은 결합축의 위와 아래로 분포하게 되는데 이 결합을 파이 결합이라고 한다.