
|
물질은 온도에 따라 상이 다르고, 상변화가 일어나는 동안에는 온도 변화가 없다. 물질의 상변화가 일어나는 온도로 녹는점과 끓는점이 있다. 녹는점과 끓는점은 물질에 따라 다르고, 외부 압력에 따라서도 달라진다. 어는점은 녹는점과 같은 경우가 많지만 다른 경우도 있다. 이들은 어떻게 다를까? | |
아이스크림이 녹고 있다.
|
녹는점(용융점, melting point)

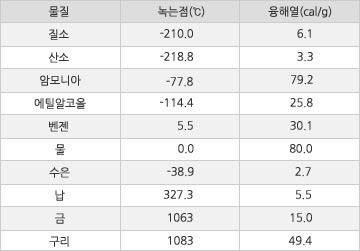
녹는점은 물질의 상이 고체에서 액체로 바뀌는 온도이다. 예를 들어 저온에서 고체인 얼음을 가열하면 어떤 온도(녹는점)에서 더 이상 온도가 올라가지 않고 액체인 물로 바뀌기 시작한다. 또 상온에서 고체인 납이나 철도 가열하면 어떤 온도(용융점)에서 녹아서 액체로 바뀌기 시작한다. 이와 같이 물질의 상이 고체에서 액체로 바뀌는 것을 융해라고 하고, 이때의 온도를 녹는점(용융점, melting point)이라고 한다. 얼음이 녹는점은 0℃이고, 납이 녹는점은 327℃, 철이 녹는점은 1535℃이다. 다음은 1기압 하에서 여러 물질들의 녹는점과 융해열을 나타낸 것이다.
| |
|
고체를 가열하면 왜 액체로 변할까?

단단한 고체를 이루는 분자들은 서로 간의 인력에 붙들린 채 제자리에서 진동한다. 분자들이 충분한 열에너지를 흡수하면 분자들 사이의 응집력을 이겨내고 어느 정도 자유롭게 움직일 수 있다. 이 에너지가 융해열이다. 융해열이 물질마다 다른 것은 분자들의 응집력이 다르기 때문이다. 고체를 가열하면 분자들이 열에너지를 흡수하여 진동은 더욱 격렬해진다. 고체를 계속 가열하여 녹는점에 도달하면 진동뿐 아니라 회전 운동까지 가능해진다. 회전이 가능해지면 입자들은 이웃입자들의 구속으로부터 벗어나 어느 정도 자유롭게 움직일 수 있게 된다. 이러한 상태가 바로 액체 상태이다.
과냉각 : 순수한 물질은 어는점 아래에서 얼기도 한다

순수한 물질은 온도가 어는점 아래로 내려가도 얼지 않기도 한다. 이러한 현상을 과냉각(supercooling)이라고 한다. 과냉각은 액체가 평형상태에서의 상변화 온도 이하로 냉각되어도 상변화를 일으키지 않는 현상이다. 예를 들어 보통의 물은 1기압에서 0℃에서 얼지만 얼음의 핵을 형성할 물질이 없는 순수한 물은 ?42℃까지 냉각되어도 얼지 않기도 한다. 과냉각 상태에 있는 물을 얼리려면 다른 이온이나 먼지입자를 넣어주거나 흔들어주면 된다. 이러한 원리는 인공강우에 이용되고 있다.
| |

녹는점, 어는점 및 과냉각 현상을 설명하는 동영상. <출처: EBS클립뱅크>

|
어는점(빙점, 응고점, freezing point)

어는점은 물질의 상이 액체에서 고체로 바뀌는 온도이다. 예를 들어 물을 냉각시키면 더 이상 온도가 내려가지 않고 고체인 얼음으로 바뀌기 시작하는 온도(어는점)가 있다. 용융된 금속도 마찬가지로 냉각시키면 어떤 온도(응고점)에서 굳어져서 고체로 바뀐다. 이와 같이 물질의 상이 액체에서 고체로 바뀌는 것을 응고라고 하고, 이때의 온도를 어는점(빙점, 응고점, freezing point)이라고 한다.
| |
액체를 냉각시키면 왜 고체가 되는가?

|
액체를 냉각시키면 분자들의 운동이 느려지고 분자들 사이의 거리가 점점 가까워진다. 어는점에서는 분자 사이의 인력에 의해서 분자들은 융합되게 되어 더 이상 자유로이 돌아다닐 수 없게 된다. 이 때 분자들 사이의 응집력이 분자들을 한데 뭉치도록 일을 하여 열이 방출되는데 이 열이 응고열이다.
녹는점과 어는점은 항상 같은 것은 아니다

대부분의 물질에 있어서 녹는점과 어는점은 거의 같다. 예를 들어 상온에서 액체인 수은의 녹는점과 어는점은 똑같이 ?38.83℃이다. 하지만 어떤 물질들은 녹는점과 어는점이 서로 다르다. 대표적인 물질이 한천이다. 한천을 가열하면 85℃에서 액체가 된다. 하지만 액체 상태의 한천을 식히면 31~40℃에서 굳어진다. 또 비정질(amorphous) 고체는 녹는점이나 어는점이 일정하지 않다. 비정질 고체는 유리나 플라스틱과 같이 원자 배열이 불규칙하여 특징적인 외형을 만들지 못하는 고체를 말한다. | |
|
|

한천으로 만든 디저트. 한천은 녹는점과 어는점이 다르다. | |
어는점 내림(빙점강하, 응고점강하)

|

바닷물이 잘 얼지 않는 이유는 어는점 내림 때문이다. | |
|
|
바닷물은 잘 얼지 않는다. 예를 들어 한 겨울철에 강물은 꽁꽁 얼어도 바닷물은 얼지 않은 것을 볼 수 있다. 그 이유는 바닷물 속에 녹아 있는 소금 이온이 물 분자들이 모여 얼음 결정을 이루는 것을 방해하기 때문이다.
소금뿐 아니라 설탕을 비롯한 다른 물질이 녹아 있는 경우에도 어는점이 내려간다. 이와 같이 액체 속에 다른 물질이 녹아 있을 때 어는점이 내려가는 현상을 어는점 내림(빙점강하)이라고 한다. 녹아있는 물질의 농도가 높을수록 어는점은 더 많이 내려간다. 예를 들어 1리터의 물에 소금 1몰(58g)이 녹아 있으면 어는점은 -5.6℃로 내려간다. | |
|
어는점 내림 현상은 일상에서 유용하게 이용된다

대표적인 예는 자동차의 부동액이다. 부동액(antifreezing solution)은 물에 염화칼슘이나 염화마그네슘과 같은 염류를 넣어서 응고점을 낮게 한 수용액이다. 자동차에는 엔진을 냉각시키기 위한 냉각수가 사용되는데 겨울철에 기온이 영하로 내려가면 얼어서 파열 위험이 있다. 이를 방지하기 위하여 냉각수에 부동액을 넣어준다. 어는점 내림 현상을 이용하는 또 다른 예는 제설제이다. 겨울철, 눈이 쌓인 빙판길에 염화칼슘이나 염화나트륨을 뿌리면 눈이 녹아내려 물이 된다. 이들은 수분을 흡수하여 열을 방출하는 발열반응을 일으키기 때문이다. 이렇게 녹은 물이 다시 얼면 소용이 없을 것이다. 하지만 이 물은 수용액으로 다시 얼지 않는다. 어는점이 낮아졌기 때문이다.
| |
|
염화칼슘은 실온에서 고체 상태이지만 수용액은 최대 ?52 °C까지 어는점이 내려간다. 염화칼슘은 제설제로 염화나트륨 보다 더 효과가 뛰어나다. 하지만 철근이나 시멘트를 부식하는 성질이 매우 강하기 때문에 문제가 되고 있다.
어는점 내림 현상을 이용하면 강물이 오염된 정도를 쉽게 알 수 있다. 강물에 녹아 있는 오염물질이 강물이 어는 온도를 낮추기 때문이다. 오염도가 높은 강물일수록 추운 겨울에도 더 잘 얼지 않는다.
어는점 내림 현상은 순수한 얼음이나 반도체 제조에도 이용된다. 0°C에서 얼음이 처음 얼기 시작할 때 맨 먼저 순수한 물 분자가 얼음이 된다. 그 다음에 다른 순수한 물 분자들이 얼어붙으면서 얼음의 결정이 커져간다. 한편 불순물은 어는점에 도달하지 못하고 액체 상태로 밀려난다. 순수한 얼음이 커질수록 불순물의 농도는 더 진해져서 얼음이 되기는 더 어려워진다. 이와 같은 순수한 얼음을 만드는 원리는 순수한 실리콘 원판을 만들 때도 이용한다. 반도체를 만드는 실리콘 원판은 순도가 99.99999999% 이상이어야 한다.
| |
|
|

제설작업 할 때 뿌리는 염화칼슘은 어는점을 내려 준다. <출처: (cc) Petri_Krohn> | |
|
녹는점은 압력에 따라 달라진다

대부분의 물질은 압력이 높아지면 녹는점도 높아진다. 그 이유는 물질은 대부분 고체에서 액체로 상변화 할 때 부피가 늘어나기 때문이다. 부피가 늘어난다는 것은 분자간의 거리가 늘어나는 것을 의미한다. 따라서 압력이 높아지면 분자들의 거리가 늘어나는 것을 억누르게 되므로 녹는점이 높아지는 것이다.
하지만 예외인 물질도 있는데, 그것은 바로 물이다. 물은 압력이 높아질수록 녹는점이 오히려 낮아진다. 그 이유는 물은 대부분의 물질과 달리 고체(얼음)가 되면 부피가 증가하기 때문이다. 물이 얼 때 부피가 증가하는 이유는 물 분자들이 속이 빈 육각형 구조를 이루기 때문이다. 물은 압력이 높아지면 오히려 녹는점이 내려가는 거의 유일한 물질이다. 또 다른 물질로는 금속인 비스무트가 있다.
| |

얼음 위에서 스케이트를 탈 수 있는 이유는 얼음 위의 얇은 수막 때문이지, 복빙 현상 때문이 아니다.
|
복빙(regelation)은 얼음에 압력을 가하게 되면 녹는점이 내려가서 물이 되고 압력을 제거하면 녹는점이 올라가 다시 얼음이 되는 현상을 말한다. 복빙은 물에서 나타나는 특징이다. 얼음 위에서 스케이트를 탈 수 있는 것은 복빙 때문인 것으로 흔히 알려져 있다. 그러나 스키나 스케이트 날이 누르는 압력은 그리 크지 않을 뿐 아니라 압력에 의한 빙점강하도 크지 않다. 압력이 1기압 증가했을 때 녹는점은 불과 0.007℃ 밖에 내려가지 않는다.
눈이나 얼음 표면이 미끄러운 것은 복빙 때문이 아니라 얼음이나 눈의 표면에 존재하는 얇은 수막 때문이다. 이 수막은 0℃이하에서도 존재한다. 아주 추운 날 눈길이나 빙판길이 미끄럽지 않은 것은 낮은 온도에서는 이 수막도 얼어붙기 때문이다. | |
- 글 김충섭 / 수원대학교 물리학과 교수
- 서울대학교 물리학과를 졸업하고 동 대학에서 박사학위를 받았다. 현재 수원대학교 물리학과 교수이다. 저서로 [동영상으로 보는 우주의 발견] [메톤이 들려주는 달력 이야기] [캘빈이 들려주는 온도 이야기] 등이 있다.















