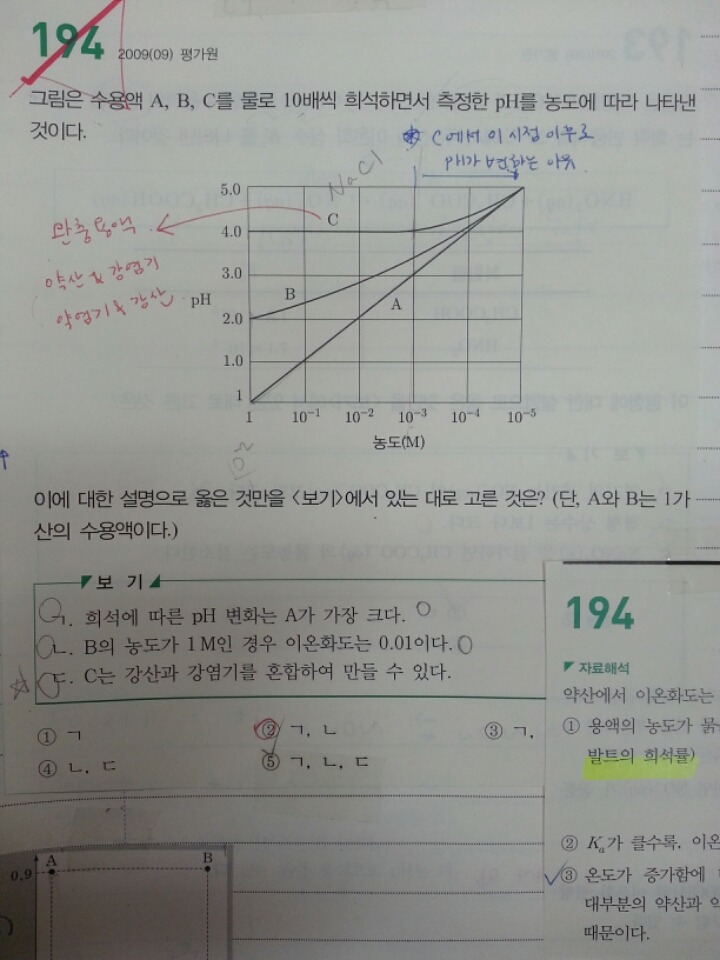
주어진 그래프에서 C가 완충용액인것까지는 알겠는데요. 희석 중 10^(-3)M 보다 낮아지면 pH가 완충범위를 넘어서 증가하거든요. 근데 헨더식식에 따르면 산과 그 짝염기의 비율로 pH를 계산하기때문에 아무리 희석되어도 pH는 4.0으로 일정해야하지않을까라는 의문이 순간 들었는데 10^(-3)M 보다 농도가 낮아지면 pH가 물의 자동이온화에 의한 영향을 점점 더 많이 받게되기 때문인건가요? 결국 pH가 7로 수렴하는 형태가 나올까요?
다음검색
댓글
댓글 리스트-
작성자둘둘말아 작성시간 15.12.24 네 생각하신게 맞아요~ 그래서 저 구간에선 단순히. H-H식을 쓰면 안되구요 물의 자동이온화를 고려한 평형의 체계적 처리로 접근해야 돼요~ 결국 농도가 더 묽어질수록 pH 7에 수렴합니다. 강산 강염기도 마찬가지에요. 특히 강산/강염기의 경우엔 C와는 다르게 10^-5 에서 -7까지 범위서부터 평형의 체계적 처리로 접근 해요. 왜냐면 보통 우리가 어떤 값을 근사하기 위한 무시한다~의 기준이 최소 100배이상 보통은 1000배이상 차이날때를 기준으로 하니까요. 결국 A나 B의 경우도 모두 pH 7로 수렴함을 볼 수있어요
-
답댓글 작성자물화생 작성자 본인 여부 작성자 작성시간 15.12.24 답변 감사합니다. 평형의 체계적처리라함은 근사없는 평형계산을 의미하시는건가요?
-
답댓글 작성자둘둘말아 작성시간 15.12.24 물화생 네 산의 농도와(산의 이온화 평형과) 물의 자동이온화를 모두 고려해서 질량균형 전하균형식 세워서 pH 구하는 거요
-
답댓글 작성자물화생 작성자 본인 여부 작성자 작성시간 15.12.24 둘둘말아 감사합니다 시원하게 해결되었습니다