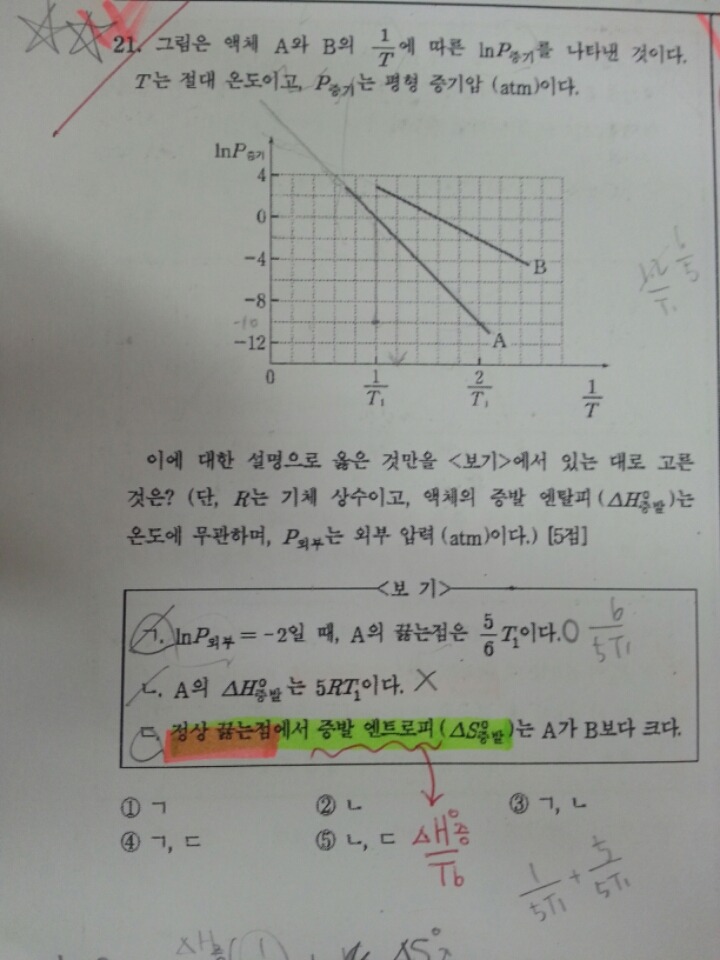
선택지 ㄷ에서 '정상 끓는점'이라는 조건이 들어가있는 이유가 궁금합니다. 정상 끓는점이라는 말이 없으면 증발 엔트로피의 비교가 불가능한건가요??
다음검색
댓글
댓글 리스트-
작성자polar star 작성시간 15.06.20 마지막 보낸 사진 속에 제일 위의 식은 lnP식이 아니라 lnK(평형상수)식으로 그 식을 사용하면 안 될것 같아요
-
작성자polar star 작성시간 15.06.20 dlnP/d(1/T)=-△H/R 이렇게 식이되는데 이걸로부터 그래프의 기울기가 -△H/R이되므로 기울기를 통해 엔탈피변화를 구한 후 lnP=0인 지점의 1/T를통해 끓는점을 구해서 엔탈피변화와 끓는점을 나누어 엔트로피변화를 구하는것이 맞는 것 같습니다
-
답댓글 작성자물화생 작성자 본인 여부 작성자 작성시간 15.06.20 아.. 제가 여태 공식을 잘못 알고있었네요 해설지를 보니 증기압의 온도의존성 공식은 Clausius이고 그것을 평형상수와 관련한 식으로 바꾸면 아래처럼 되는데 혹시 C가 어떻게 델타S/R이 되는건가요? 해설지의 아래쪽에 있는식 lnK=-델타H/R(1/T)+델타S/R 를 이용한다면 바로 y절편을 통해 비교가 가능한가요?
이미지 확대
-
답댓글 작성자polar star 작성시간 15.06.20 물화생 아... dlnP=-△H/Rd(1/T) 을 부정적분하면 적분상수C가 나오는데, 이 문제상황에선 평형상수K가 기체 A의 증기압력이 되기때문에 lnP=lnK가 되어서, lnK식과 비교하여 자연스럽게 적분상수C가 되네요.. 그래서 바로 y절편을 통해 비교가능하고 이 방법이 더 빠른방법이 되겠네요 이 방법을 통하면 압력의 명시가 필요없겠지만, 그래도 논란을 막기위해 정상끓는점이라는 말을 넣어준 것 같습니다