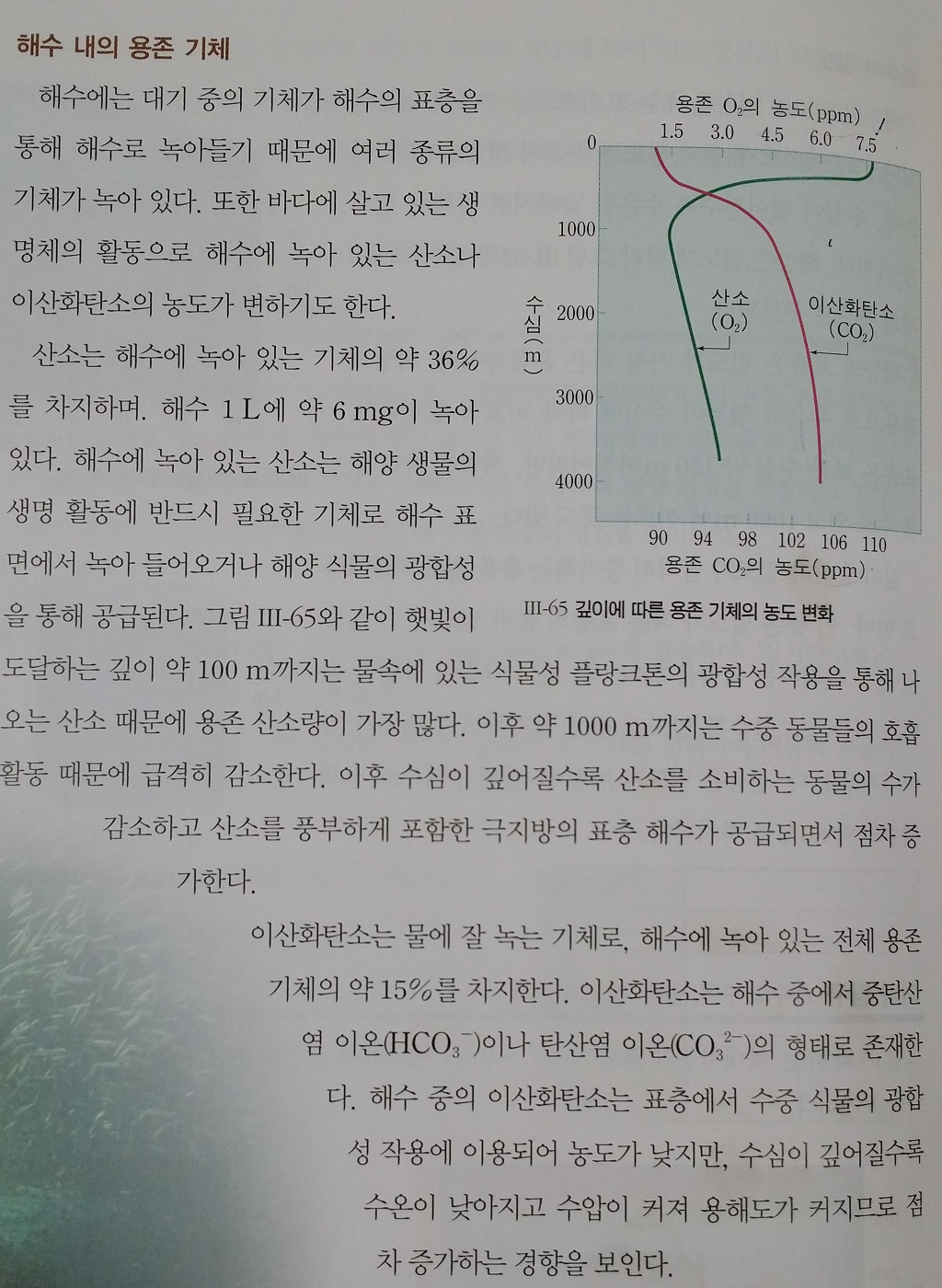
해수내의 용존기체에 대한 내용인데요.
본문에 산소는 해수에 녹아있는 기체의 약 36%를 차지하며, 라고 되어있구 이산화탄소는 물에 잘 녹는 기체로 해수에 녹아있는 전체 용존 기체의 약 15%를 차지한다고 되어있습니다.
% 비율로보면 산소가 더 많이 차지하고 있다고 써있는거죠?
근데 그림에는 이산화탄소의 용존 농도가 90~110ppm으로 더 크고 산소는 1.5~7.5ppm으로 더 작게 나타나있어요.
혹시나 해서 다른 책도 찾아봤는데 같더라구요
... 이거 설명해주실수 있는 분 있나여ㅜㅜ
고수님들 부탁드립니다.ㅜㅜ
다음검색
댓글
댓글 리스트-
답댓글 작성자Twin star 작성시간 17.06.01 제 생각이 바로 그겁니다. 보통 산소보다 용해율이 월등하게 높은 이산화탄소는 해수에서 대부분 탄산(HCO3-)형태로 존재하는데 수용액 속에 탄산이온까지 포함해서 이산화탄소의 ppm수치가 증가되었을 것이라고 생각합니다. 그 외에 해수에 순수 CO2로 존재하는 비율은 굉장히 적으니까 용존산소보다 적게 나타날 것이구요.
-
답댓글 작성자포기안하면합격 작성자 본인 여부 작성자 작성시간 17.06.01 Twin star 혹시 순수하게 존재하는 이산화탄소15퍼는 어떤식으로 측정이 가능할지 아시나요??ㅜㅜ
해수중의 이산화탄소비만 딱 측정하기란 어려울것같아서ㅜㅜ 먼가 학생들+같은 전공쌤과 이야기 해보았는데 이부분에서 풀리지않아서요ㅜㅜㅜ -
답댓글 작성자Twin star 작성시간 17.06.01 포기안하면합격 기체분압에 대한 측정은 화학교육쪽에서 다루는것 같은데. .. 저는 잘 모르겠네요 ㅠㅠ
-
작성자포기안하면합격 작성자 본인 여부 작성자 작성시간 17.06.01 순수한 이산화탄소의 부피비를 어떻게 측정하여 15%가 나오는지. 왜 ppm을 구할때는 순수한 이산화탄소양이 아닌 탄산이온과 탄산염값을 포함하여 계산했는지에 대한 것입니다.
-
작성자체리쌤 작성시간 23.07.08 시간이 지났지만 저도 이부분이 궁금해서 검색했는데 나와서 의견을 덧붙이고자 답글을 답니다 :) 저도 비상교과서 지도서를 보다가 이상하게 생각했는데요, 위에 twin star님이 말씀하신 것이 맞는거 같습니다. 용존산소의 용어정의가 여러 용존기체 중 물속에서 다른 원소와 결합하지않은 상태로 존재하는 산소분자 더라구요! 그러니 용존이산화탄소도 다른 원소와 결합하지않은 순수 CO2 상태의 분자일거같습니다. 따라서 작성자님이 올려주신 교과서 사진 마지막문단쯤 주로 이온의 형태로 존재한다고 했으니 용존이산화탄소기체는 양이 15%로 적지만 녹아있는 농도로만 한다면 산소보다 훨씬 높을거 같습니다 :)